Биохимия ферментов-2.ppt
- Количество слайдов: 19
 2 Механизм действия ферментов Гомельский государственный медицинский университет Кафедра биохимии Доцент кафедры, к. б. н. А. Н. Коваль А. Н. , 2006 (C)
2 Механизм действия ферментов Гомельский государственный медицинский университет Кафедра биохимии Доцент кафедры, к. б. н. А. Н. Коваль А. Н. , 2006 (C)
 Содержание n n n n 2/17/2018 Свойства ферментов (термолабильность, специфичность и др. ). Механизм действия ферментов. Этапы взаимодействия фермента и субстрата. Гипотезы Э. Фишера, Д. Кошланда и современные взгляды. Теория промежуточных соединений. Основы термодинамики катализа. Энергия активации. Энергетический барьер. Кинетика ферментативных реакций (факторы, влияющие на скорость ферментативных реакций: природа фермента и субстрата, их концентрация, p. H, температура, лекарственные препараты и др. ). Km – определение, физиологическое значение. Регуляция активности ферментов. Роль гормонов, ц. АМФ, активаторов, ингибиторов. Регуляция активности путем химической модификации ферментов (ограниченный протеолиз, фосфорилирование, метилирование и др. ). Аллостерическая регуляция и свойства аллостерических ферментов. Виды ингибирования. Коваль А. Н. , 2006 (C) 2
Содержание n n n n 2/17/2018 Свойства ферментов (термолабильность, специфичность и др. ). Механизм действия ферментов. Этапы взаимодействия фермента и субстрата. Гипотезы Э. Фишера, Д. Кошланда и современные взгляды. Теория промежуточных соединений. Основы термодинамики катализа. Энергия активации. Энергетический барьер. Кинетика ферментативных реакций (факторы, влияющие на скорость ферментативных реакций: природа фермента и субстрата, их концентрация, p. H, температура, лекарственные препараты и др. ). Km – определение, физиологическое значение. Регуляция активности ферментов. Роль гормонов, ц. АМФ, активаторов, ингибиторов. Регуляция активности путем химической модификации ферментов (ограниченный протеолиз, фосфорилирование, метилирование и др. ). Аллостерическая регуляция и свойства аллостерических ферментов. Виды ингибирования. Коваль А. Н. , 2006 (C) 2
 Свойства ферментов n n Термолабильность – скорость ферментативных реакций зависит от температуры. Каждый фермент имеет свой p. H-оптимум. n Активность фермента зависит от концентрации субстратов. n Специфичность: абсолютная и относительная (групповая). 2/17/2018 Коваль А. Н. , 2006 (C) 3
Свойства ферментов n n Термолабильность – скорость ферментативных реакций зависит от температуры. Каждый фермент имеет свой p. H-оптимум. n Активность фермента зависит от концентрации субстратов. n Специфичность: абсолютная и относительная (групповая). 2/17/2018 Коваль А. Н. , 2006 (C) 3
 Действие большинства ферментов высокоспецифично n Специфичность n n n 2/17/2018 к типам каталитических реакций (реакционная специфичность), к природе соединений - субстратов (субстратная специфичность). Высокоспецифичные ферменты (тип А) катализируют расщепление только одного типа связи в субстратах определенной структуры. Ферменты типа Б обладают ограниченной реакционной специфичностью, но широкой субстратной специфичностью. Ферменты типа В (с низкой реакционной и низкой субстратной специфичностями) встречаются редко. Коваль А. Н. , 2006 (C) 4
Действие большинства ферментов высокоспецифично n Специфичность n n n 2/17/2018 к типам каталитических реакций (реакционная специфичность), к природе соединений - субстратов (субстратная специфичность). Высокоспецифичные ферменты (тип А) катализируют расщепление только одного типа связи в субстратах определенной структуры. Ферменты типа Б обладают ограниченной реакционной специфичностью, но широкой субстратной специфичностью. Ферменты типа В (с низкой реакционной и низкой субстратной специфичностями) встречаются редко. Коваль А. Н. , 2006 (C) 4
 Механизм действия ферментов. Теории «ключ-замок» , «рукаперчатка» Э. Фишер предложил для объяснения специфичности взаимодействия фермента и субстрата модель «ключа и замка» . n n Эта модель предполагала существование такого центра как особой структуры и без связи с субстратом. Д. Кошленд в 1959 г. предложил теорию индуцированного соответствия ( «рука-перчатка» ): т. е. что субстрат навязывает активному центру свою форму, а активный центр в свою очередь подгоняет форму субстрата под свою собственную. n n 2/17/2018 была подтверждена при помощи метода рентгеноструктурного анализа, позволившего построить пространственную модель фермента. Коваль А. Н. , 2006 (C) 5
Механизм действия ферментов. Теории «ключ-замок» , «рукаперчатка» Э. Фишер предложил для объяснения специфичности взаимодействия фермента и субстрата модель «ключа и замка» . n n Эта модель предполагала существование такого центра как особой структуры и без связи с субстратом. Д. Кошленд в 1959 г. предложил теорию индуцированного соответствия ( «рука-перчатка» ): т. е. что субстрат навязывает активному центру свою форму, а активный центр в свою очередь подгоняет форму субстрата под свою собственную. n n 2/17/2018 была подтверждена при помощи метода рентгеноструктурного анализа, позволившего построить пространственную модель фермента. Коваль А. Н. , 2006 (C) 5
 Механизм действия ферментов. Концепции «дыбы» и «лилипутов» n n В 1954 году была предложена гипотеза связывающая механизм ферментативного каталитического акта с деформацией и напряжением молекулы субстрата при ее сорбции в активном центра фермента. Эта гипотеза вошла в науку под названием концепции «дыбы» или «лилипутов» . n n 2/17/2018 Первое подчеркивало принудительный характер механической деформации гибкого субстрата жестким ферментом. Второе название указывает на то, что слабые нековалентные взаимодействия субстрата и активного центра обеспечивают дестабилизацию субстрата и перевод его в высокоэнергетическое переходное состояние. Коваль А. Н. , 2006 (C) 6
Механизм действия ферментов. Концепции «дыбы» и «лилипутов» n n В 1954 году была предложена гипотеза связывающая механизм ферментативного каталитического акта с деформацией и напряжением молекулы субстрата при ее сорбции в активном центра фермента. Эта гипотеза вошла в науку под названием концепции «дыбы» или «лилипутов» . n n 2/17/2018 Первое подчеркивало принудительный характер механической деформации гибкого субстрата жестким ферментом. Второе название указывает на то, что слабые нековалентные взаимодействия субстрата и активного центра обеспечивают дестабилизацию субстрата и перевод его в высокоэнергетическое переходное состояние. Коваль А. Н. , 2006 (C) 6
 Механизм действия ферментов. Современные взгляды n Современные концепции на механизм ферментативного катализа объединяются в теорию топохимического соответствия и объединяют все вышеперечисленные взгляды. 2/17/2018 Коваль А. Н. , 2006 (C) 7
Механизм действия ферментов. Современные взгляды n Современные концепции на механизм ферментативного катализа объединяются в теорию топохимического соответствия и объединяют все вышеперечисленные взгляды. 2/17/2018 Коваль А. Н. , 2006 (C) 7
 Теория промежуточных соединений n n Выдвинутая в 1913 году Л. Михаэлисом и М. Ментен общая теория ферментативного катализа постулировала, что фермент Е сначала обратимо и относительно быстро связывается с со своим субстратом S в реакции: E + S = ES Образовавшийся при этом фермент-субстратный комплекс ES, не имеющий аналогий в органической химии и химическом катализе, затем распадается в второй более медленной (лимитирующей) стадии реакции: ES = Е + Р 2/17/2018 Коваль А. Н. , 2006 (C) 8
Теория промежуточных соединений n n Выдвинутая в 1913 году Л. Михаэлисом и М. Ментен общая теория ферментативного катализа постулировала, что фермент Е сначала обратимо и относительно быстро связывается с со своим субстратом S в реакции: E + S = ES Образовавшийся при этом фермент-субстратный комплекс ES, не имеющий аналогий в органической химии и химическом катализе, затем распадается в второй более медленной (лимитирующей) стадии реакции: ES = Е + Р 2/17/2018 Коваль А. Н. , 2006 (C) 8
 Теория промежуточных соединений. Этапы взаимодействия фермента и субстрата n n n 1 этап: происходит сближение и ориентация субстрата относительно субстратного центра фермента и его постепенное «причаливание» к «якорной» площадке. 2 этап: напряжение и деформация: индуцированное соответствие - происходит присоединение субстрата, которое вызывает конформационные изменения в молекуле фермента приводящие к напряжению структуры активного центра и деформации связанного субстрата. 3 этап: непосредственный катализ. 2/17/2018 Коваль А. Н. , 2006 (C) 9
Теория промежуточных соединений. Этапы взаимодействия фермента и субстрата n n n 1 этап: происходит сближение и ориентация субстрата относительно субстратного центра фермента и его постепенное «причаливание» к «якорной» площадке. 2 этап: напряжение и деформация: индуцированное соответствие - происходит присоединение субстрата, которое вызывает конформационные изменения в молекуле фермента приводящие к напряжению структуры активного центра и деформации связанного субстрата. 3 этап: непосредственный катализ. 2/17/2018 Коваль А. Н. , 2006 (C) 9
 Теория промежуточных соединений. n Имеется реакция: S→P+Q n Представим эту реакцию в виде отдельных новых стадий: S + E = ES = E + P подстадии: 1. 2. 3. 4. 5. 6. E + S = ES ES = ES** = ES*** = EP EP = E + P 2/17/2018 S*, S*** - новые модификации субстрата, обусловленные изменением энергетической плотности, заряда и т. д. Коваль А. Н. , 2006 (C) 10
Теория промежуточных соединений. n Имеется реакция: S→P+Q n Представим эту реакцию в виде отдельных новых стадий: S + E = ES = E + P подстадии: 1. 2. 3. 4. 5. 6. E + S = ES ES = ES** = ES*** = EP EP = E + P 2/17/2018 S*, S*** - новые модификации субстрата, обусловленные изменением энергетической плотности, заряда и т. д. Коваль А. Н. , 2006 (C) 10
 Основы термодинамики катализа n Из недостаточности чисто статических взаимоотношений в духе «замка и ключа» для объяснения многостадийного каталитического процесса, Д. Кошланд предположил, что с термодинамической точки зрения ферменты ускоряют химические реакции за счет снижения энергии активации. 2/17/2018 Коваль А. Н. , 2006 (C) 11
Основы термодинамики катализа n Из недостаточности чисто статических взаимоотношений в духе «замка и ключа» для объяснения многостадийного каталитического процесса, Д. Кошланд предположил, что с термодинамической точки зрения ферменты ускоряют химические реакции за счет снижения энергии активации. 2/17/2018 Коваль А. Н. , 2006 (C) 11
 Энергия активации. n Энергия активации - энергия, необходимая для перевода всех молекул моля вещества в активное состояние при данной температуре, т. е. это та энергия, которая необходима молекуле, чтобы преодолеть энергетический барьер. n 2/17/2018 Фермент снижает энергию активации путем увеличения числа активированных молекул, которые становятся реакционно-способными на более низком энергетическом уровне, т. е. снижается и энергетический барьер. Коваль А. Н. , 2006 (C) 12
Энергия активации. n Энергия активации - энергия, необходимая для перевода всех молекул моля вещества в активное состояние при данной температуре, т. е. это та энергия, которая необходима молекуле, чтобы преодолеть энергетический барьер. n 2/17/2018 Фермент снижает энергию активации путем увеличения числа активированных молекул, которые становятся реакционно-способными на более низком энергетическом уровне, т. е. снижается и энергетический барьер. Коваль А. Н. , 2006 (C) 12
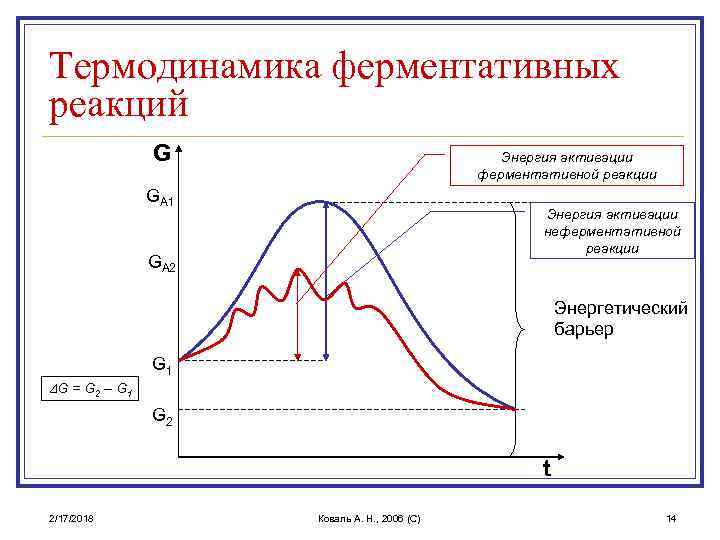 Термодинамика ферментативных реакций G Энергия активации ферментативной реакции GA 1 Энергия активации неферментативной реакции GA 2 Энергетический барьер G 1 DG = G 2 – G 1 G 2 t 2/17/2018 Коваль А. Н. , 2006 (C) 14
Термодинамика ферментативных реакций G Энергия активации ферментативной реакции GA 1 Энергия активации неферментативной реакции GA 2 Энергетический барьер G 1 DG = G 2 – G 1 G 2 t 2/17/2018 Коваль А. Н. , 2006 (C) 14
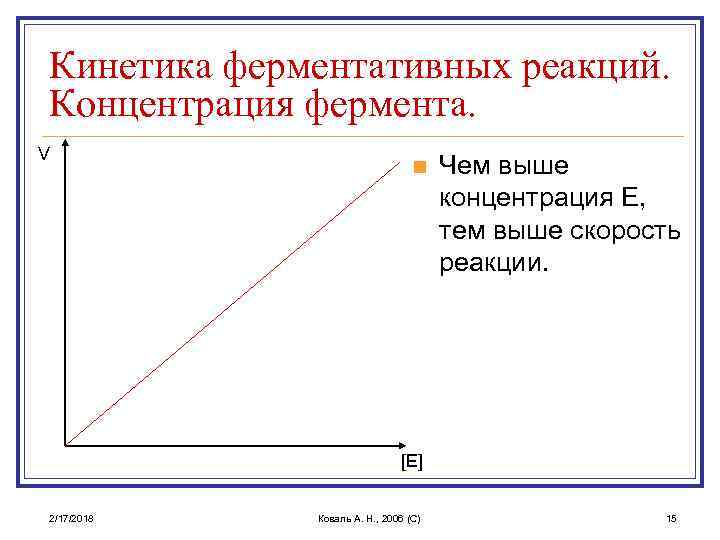 Кинетика ферментативных реакций. Концентрация фермента. V n Чем выше концентрация E, тем выше скорость реакции. [E] 2/17/2018 Коваль А. Н. , 2006 (C) 15
Кинетика ферментативных реакций. Концентрация фермента. V n Чем выше концентрация E, тем выше скорость реакции. [E] 2/17/2018 Коваль А. Н. , 2006 (C) 15
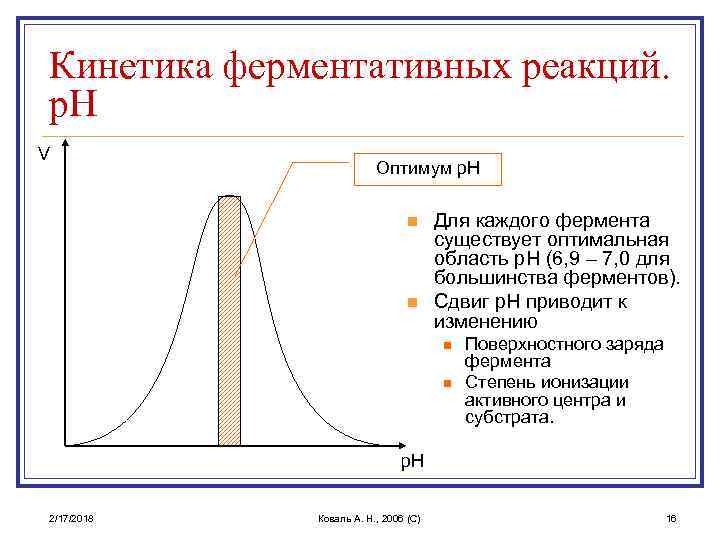 Кинетика ферментативных реакций. p. H V Оптимум p. H n n Для каждого фермента существует оптимальная область p. H (6, 9 – 7, 0 для большинства ферментов). Сдвиг p. H приводит к изменению n n Поверхностного заряда фермента Степень ионизации активного центра и субстрата. p. H 2/17/2018 Коваль А. Н. , 2006 (C) 16
Кинетика ферментативных реакций. p. H V Оптимум p. H n n Для каждого фермента существует оптимальная область p. H (6, 9 – 7, 0 для большинства ферментов). Сдвиг p. H приводит к изменению n n Поверхностного заряда фермента Степень ионизации активного центра и субстрата. p. H 2/17/2018 Коваль А. Н. , 2006 (C) 16
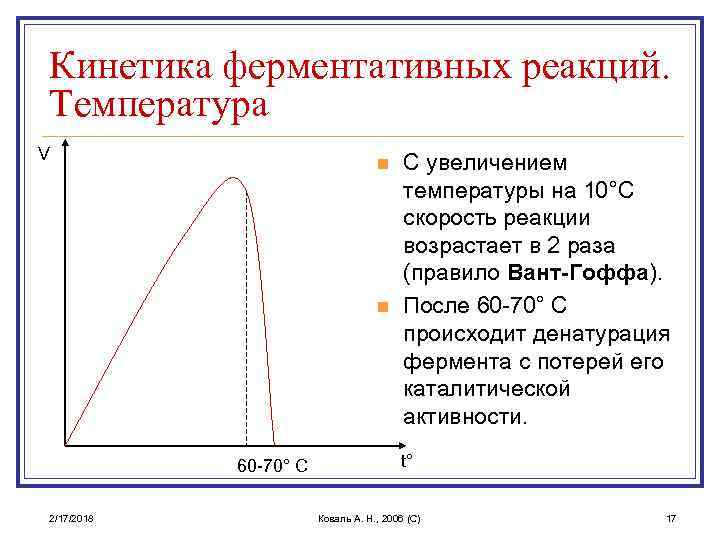 Кинетика ферментативных реакций. Температура V n n 60 -70° C 2/17/2018 С увеличением температуры на 10°C скорость реакции возрастает в 2 раза (правило Вант-Гоффа). После 60 -70° C происходит денатурация фермента с потерей его каталитической активности. t° Коваль А. Н. , 2006 (C) 17
Кинетика ферментативных реакций. Температура V n n 60 -70° C 2/17/2018 С увеличением температуры на 10°C скорость реакции возрастает в 2 раза (правило Вант-Гоффа). После 60 -70° C происходит денатурация фермента с потерей его каталитической активности. t° Коваль А. Н. , 2006 (C) 17
![Кинетика ферментативных реакций. Концентрация субстрата V n n [S] 2/17/2018 Коваль А. Н. , Кинетика ферментативных реакций. Концентрация субстрата V n n [S] 2/17/2018 Коваль А. Н. ,](https://present5.com/presentation/20089621_131533465/image-17.jpg) Кинетика ферментативных реакций. Концентрация субстрата V n n [S] 2/17/2018 Коваль А. Н. , 2006 (C) Для простых ферментов график имеет вид гиперболы и описывается уравнением Михаэлиса. Ментен. При очень высоких концентрациях субстрата наступает субстратное ингибирование 18
Кинетика ферментативных реакций. Концентрация субстрата V n n [S] 2/17/2018 Коваль А. Н. , 2006 (C) Для простых ферментов график имеет вид гиперболы и описывается уравнением Михаэлиса. Ментен. При очень высоких концентрациях субстрата наступает субстратное ингибирование 18
 Кинетика ферментативных реакций n n Исследование зависимости скорости ферментативных реакций от концентрации реагирующих веществ стало одним из главных путей изучения механизма действия ферментов. В 1905 году французский исследователь Генри впервые высказал ряд предположений, которые были экспериментально подтверждены в 1913 году Леонором Михаэлисом и Мод Ментен (США, Канада). 2/17/2018 Коваль А. Н. , 2006 (C) 19
Кинетика ферментативных реакций n n Исследование зависимости скорости ферментативных реакций от концентрации реагирующих веществ стало одним из главных путей изучения механизма действия ферментов. В 1905 году французский исследователь Генри впервые высказал ряд предположений, которые были экспериментально подтверждены в 1913 году Леонором Михаэлисом и Мод Ментен (США, Канада). 2/17/2018 Коваль А. Н. , 2006 (C) 19
 2/17/2018 Коваль А. Н. , 2006 (C) 20
2/17/2018 Коваль А. Н. , 2006 (C) 20


