лекция 14.ppt
- Количество слайдов: 49

14. Механизмы агрегации и массообмена между частицами Рассмотрены механизмы взаимодействия дисперсных частиц, их агрегации-дезагрегации, механизмы переконденсации и срастания, коалесценции и спекания 1

Стабилизация и дестабилизация (коагуляция) золей Притяжение Отталкивание (электростатика) Свойства золя (коллоидного раствора) определяются балансом сил притяжения и отталкивания между частицами. Притяжение – в основном - результат дисперсионного взаимодействия, которое из-за аддитивности убывает гораздо медленнее, чем при взаимодействии пары молекул 2

Межмолекулярные взаимодействия Из-за аддитивности дисперсионных сил при переходе от молекул к частицам близкодействующее дисперсионное межмолекулярное взаимодействие трансформируется в дальнодействующее взаимодействие 3 J. N. Israelashvili, Intermolecular and Surface Forces, Acad Press, N Y 1993

Дисперсионные межмолекулярные взаимодействия Дальнодействие Близкодействие Взаимодействие атомов Взаимодействие групп атомов или частиц~0. 5 -10 нм или молекул А ~10 -19 -10 -21 дж- конст два атома Две сферы Гамакера, зависящая R 2 от среды и материала E=-C 1/D 6 R 1 D D E =-(A/6 D)R 1 R 2/(R 1+R 2) Атом-поверхность Сфера-поверхность R 1 D D Е=-с2/D 3 E =-AR 1/D D l Две параллельных цепных молекулы L E=C 3 l/b 2 r 5 b R 1 1 R 2 Два цилиндра D E =-AL 1/D 3/2[R 1 R 2/(R 1+R 2)]1/2 4 J. N. Israelashvili, Intermolecular and Surface Forces, Acad Press, N Y 1993

В водных растворах дополнительно обнаружены дальнодействующие силы гидрофобного притяжения (самопроизвольное сближение гидрофобных частиц) и гидрофильного отталкивания (самопроизвольное отталкивание гидрофильных частиц) 5

Физические их механизмы пока дискуссионны, в первом приближении гидрофобное отталкивание обусловлено повышенным хим потенциалом молекул воды между гидрофобными поверхностями из-за обрыва решетки водородных связей на границах их раздела 6

В классической теории силы отталкивания в водных растворах – обусловлены преимущественно одноименными электрическими зарядами, возникающими на поверхности частиц и в приповерхностной области раствора (ионными атмосферами). Основные причины появления заряда: а) ионизация или диссоциация групп на поверхности части б) сорбция (связывание) ионов из раствора на исходной незаряженной поверхности 7 с) комбинации этих механизмов

Классические примеры Дисперсные частицы Ag. J в водных растворах заряжены отрицательно из-за большей растворимости Ag, а добавление Ag. NO 3 изменяет заряд (сорбция Ag+). На поверхности углеродных адсорбентов образуются окисленные функциональные группы, диссоциирующие по механизмам, например, С+ + ОН- или –СОО- + Н+ Заряд на поверхности глин и др алюмосиликатов возникает из-за изоморфного замещения Si 4+ на Al 3+ с сорбцией катионов, которые диссоциируют по реакции Al. XSi. YOZ - + Na+ Заряд на каплях воды в облаке возникает из-за поглощения ионов при движении капель и т. д. 8

Заряды на поверхности оксидов и гидроксидов В водных растворах - гидратация поверхности оксидов и гидроксидов и ионизация по схеме р. Н тнз Si. O 2 Ti. O 2 ~6 Fe. OOH ~7 Al(OH)3 ~7 -8 Zn. O ~9 Co(OH)2 ~11. 5 Mg(OH)2 ~12 Ag 2 O -МОН +Н 2 О -МО- +Н 3 О+ при р. Н >p. HТНЗ -МОН +Н 2 О -МОН 2+ +НО- при р. Н<p. HТНЗ Определяется кислотно – основным равновесием При некотором р. Н - ТНЗ – точка нулевого заряда поверхности ~2 -3 ~11 -13 р. Н >ТНЗ –отрицательный заряд поверхности р. Н <ТНЗ –положительный заряд поверхности 9

ТНЗ • Выразим сродство к протону модельными реакциями -МOH 2+ -МOH + Н+ (а) и -МOH - МO- + H+ (b) (II) с константами равновесия Ка = [-МOH][Н+]/[-МOH 2+] Кb = [-МO-][Н+]/[-МOH], р. НТНЗ, соответствует [-МOH 2+]= [-МO-] и Ка. Кb = [Н+]2. В результате р. Нтнз = (1/2)(р. Ка + р. Кb) ТНЗ определяют потенциометрическим титрованием. На практике часто используется ИЭТ – изоэлектрическая точка, соответствующая нулевой подвижности дисперсных частиц в электрическом поле 10

ТНЗ и ИЭТ • ИЭТ – результат взаимной компенсации зарядов (одинаковое число (+) и (-) у поверхности • ТНЗ- отсутствие заряда поверхности). Обычно р. НИЭТ р. НТНЗ Но специфическая адсорбция инородных ионов «раздвигает» эти значения (анионы снижают р. НИЭТ и повышают р. НТНЗ , катионы – противоположное влияние) 11

Силы отталкивания Ионы, образующиеся на поверхности частиц – потенциалопределяющие; На заряженной поверхности сорбируются противоионы, а также полярные и другие молекулы и группы. Вокруг частиц формируется ионно-сольватная атмосфера, находящаяся в динамическом равновесии с раствором У поверхности образуется двойной электрический слой (ДВС), обладающий свойствами электрического конденсатора (слой Штерна-Гельмгольца) Внутренняя обкладка этого конденсатора – потенциалопределяющие ионы на поверхности, внешняя размыта из-за теплового движения противоионов, образуя диффузионное облако зарядов (ионную атмосферу или ионно-сольватную оболочку, которая включает ориентированные диполи воды, коионы с зарядом потенциалопределяющих, противоионы и т. д. ). 12

Идеализированная схема ионносольватной оболочки В А Ионная атмосфера в растворе электролита 0 частица Ионы с зарядом потенциалопределяющих А В Противоионы в растворе (диффузионная атмосфера) Потенциалопреде ляющие ионы 13

Идеализированная схема ионносольватной оболочки Ионная атмосфера в растворе электролита А 0 В Потенциал двойного слоя приближенно описывается = 0 exp(-kdx) частица kd – константа Дебая, А Потенциал скольжения(заряд части ДВС, перемещающейся вместе с частицей) В На расстоянии х = kd потенциал снижается в е раз kd-1 – условная средняя толщина двойного слоя kd-1 = [ k. T/e 2 cizi 2]1/2 , Z –заряд противоиона 14
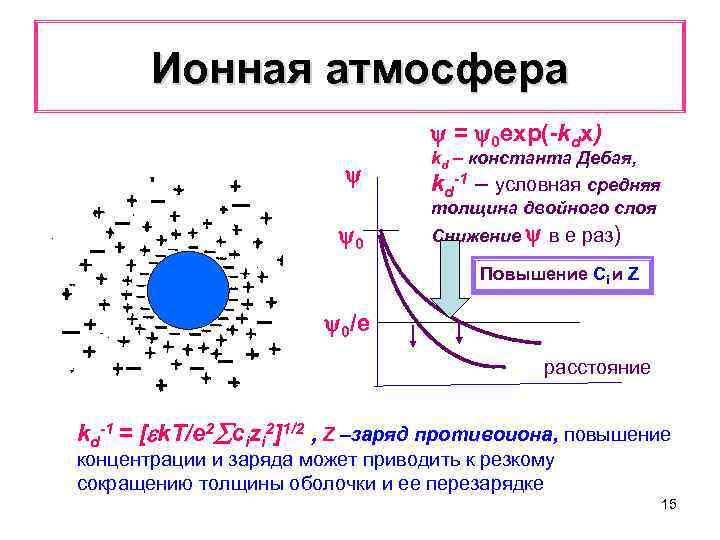
Ионная атмосфера = 0 exp(-kdx) kd – константа Дебая, kd-1 – условная средняя толщина двойного слоя 0 Снижение в е раз) Повышение Сi и Z 0/e расстояние kd-1 = [ k. T/e 2 cizi 2]1/2 , Z –заряд противоиона, повышение концентрации и заряда может приводить к резкому сокращению толщины оболочки и ее перезарядке 15

Электрокинетический потенциал При движении дисперсной частицы с ней увлекается прочно связанная часть двойного электрического слоя частица увлекаемая часть ДВС Внешняя граница ДВС В результате дисперсионная среда и дисперсная фаза Граница скольжения, по которой происходит противоположно заряжены разрыв ДВС, потенциал (зависит от скорости движения, Сi, Zi, Т и др. параметров среды и т. д. ) 16
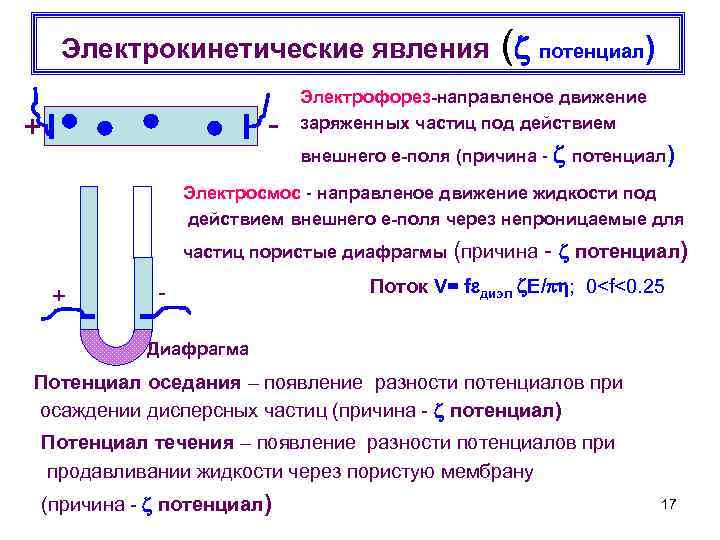
Электрокинетические явления ( - + потенциал ) Электрофорез-направленое движение заряженных частиц под действием внешнего е-поля (причина - потенциал) Электросмос - направленое движение жидкости под действием внешнего е-поля через непроницаемые для частиц пористые диафрагмы (причина + - - потенциал) Поток V= f диэл Е/ ; 0<f<0. 25 Диафрагма Потенциал оседания – появление разности потенциалов при осаждении дисперсных частиц (причина - потенциал) Потенциал течения – появление разности потенциалов при продавливании жидкости через пористую мембрану (причина - потенциал) 17

Теория ДЛФО (Дерягин-Ландау-Фервей-Овербек) Теория взаимодействия в коллоидах на основе дисперсионных сил притяжения и электростатических – отталкивания. Позже введены дополнительные составляющие взаимодействия: осмотическое давление из-за повышенной концентрацией ионов в промежутках между частицами (приводит к дополнительным силам отталкивания). Стерический фактор устойчивости оболочки из прочно адсорбированных молекул (например, ПАВ), препятствующие контактам и т. д 18
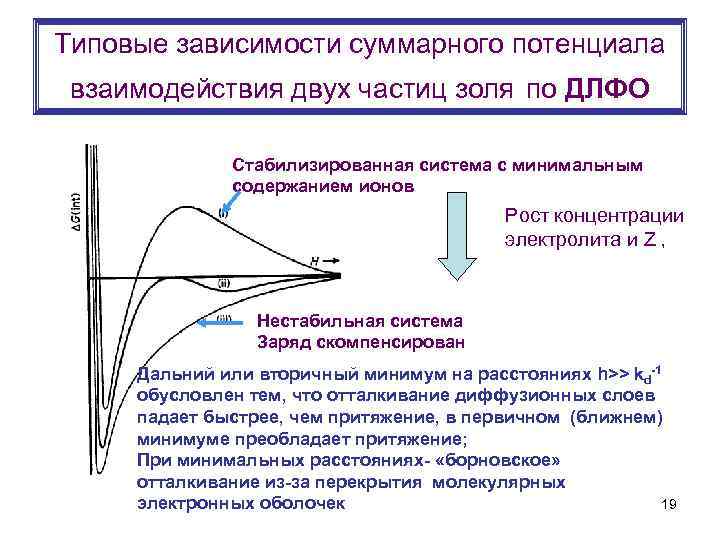
Типовые зависимости суммарного потенциала взаимодействия двух частиц золя по ДЛФО Стабилизированная система с минимальным содержанием ионов Рост концентрации электролита и Z , Нестабильная система Заряд скомпенсирован Дальний или вторичный минимум на расстояниях h>> kd-1 обусловлен тем, что отталкивание диффузионных слоев падает быстрее, чем притяжение, в первичном (ближнем) минимуме преобладает притяжение; При минимальных расстояниях- «борновское» отталкивание из-за перекрытия молекулярных 19 электронных оболочек

Схема взаимодействия частиц по ДЛФО Глубина второго минимума несколько k. Т Образуются рыхлые флокулы 20

Скорость коагуляции При малой величине энергетического барьера каждое соударение частиц приводит к их «слипанию» : быстрая коагуляция по Смолуховскому d. C/d = -8 Rc. Dэф. C 2 Rc- сечение захвата (удвоенный радиус частицы) 0. 5 = (8 Rc. Dэф. C 0)-1 В водных растворах это соответствует времени в десятки сек результат- растут рыхлые агрегаты частиц геля 21

Медленная коагуляция При значительной величине энергетического барьера U кинетика коагуляции подобна бимолекулярным химическим реакциям с энергией активации. Медленная коагуляция d. C/d -8 Rc. Dэф. C 2 exp (- U/k. T) т. е. скорость коагуляции ниже в W раз. Фактор W = exp(U/k. T) - называют отношение стабильности. Медленная коагуляция обычно приводит к относительно плотно упакованным гелям 22

Механизмы массообмена между частицами золей, гидрогелей и ксерогелей (на примере Si. O 2) Определяются законами поверхностных явлений на границах т/ж, т/п и т/ж/п: уравнение Гиббса-Оствальда-Фрейндлиха C = C 0 exp( 2 тжvm/rm. RT) Уравнение Кельвина Р = Р 0 ехр( 2 пжvm/rm. RT) Уравнение Лапласа-Юнга Р = 2 /rm Уравнение Юнга-Дюпре Cos = 2 Wa/Wк – 1 Уравнение Гиббса-Томсона Тпл/Т 0 2 vm/ rm = 0 2 v/r = 0 RTln (P/P 0) = 0 RTln(C/C 0). Кривизнa поверхности 23
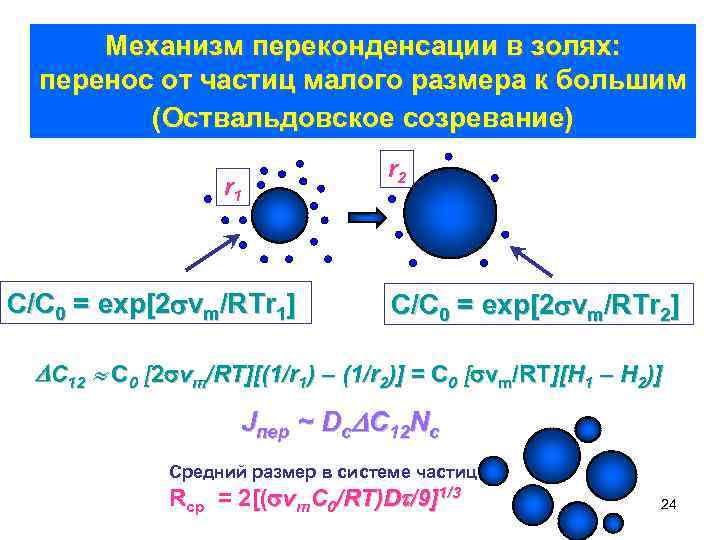
Механизм переконденсации в золях: перенос от частиц малого размера к большим (Оствальдовское созревание) r 1 С/С 0 = exp[2 vm/RTr 1] r 2 С/С 0 = exp[2 vm/RTr 2] С 12 С 0 [2 vm/RT][(1/r 1) – (1/r 2)] = С 0 [ vm/RT][H 1 – H 2)] Jпер ~ Dс С 12 Nc Средний размер в системе частиц Rср = 2[( vm. C 0/RT)D /9]1/3 24
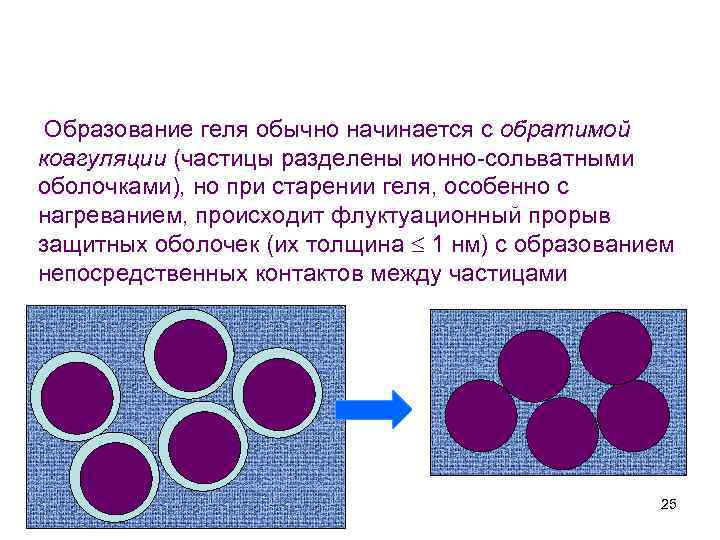
Образование геля обычно начинается с обратимой коагуляции (частицы разделены ионно-сольватными оболочками), но при старении геля, особенно с нагреванием, происходит флуктуационный прорыв защитных оболочек (их толщина 1 нм) с образованием непосредственных контактов между частицами 25

Образование непосредственных контактов между частицами резко изменяет ситуацию: переход от механизма переконденсации к механизму срастания В месте контакта пары частиц возникает зона с отрицательной кривизной R 1 12 = 0 - 2 vm/R 12 R 2 (2 1. 2) = - 2 Vm (1/R 1, 2 -1/R 2); (1 1. 2) = - 2 Vm (1/R 1. 2 - 1/R 1) и (1 2) = - 2 Vm (1/R 1 - 1/R 2), (2 1. 2) (1 1. 2) >> (1 2) Интенсивный перенос может завершаться полным срастанием в одну 26 непористую частицу

Перенос в системе контактирующих частиц Рыхло упакованные гидрогели Si. O 2 образуют жесткие агрегаты из сросшихся глобул, которые препятствуют уплотнению геля при сушке и способствуют формированию крупнопористых силикагелей 27

Плотноупакованные гидрогели В этом случае после срастания мест контактов возможен перенос в объеме раствора из участков с рыхлой упаковкой в плотноупакованные с отрицательной интегральной кривизной вплоть до их полного зарастания Такие частицы допускают плотную упаковку при сушке 28

Гидротермальная обработка гидрогеля Si. O 2 при 100 -3000 C Pore volume, V Коалесценция контактирующих тв частиц по Оствальду p. H=1 I Starting Gel R 2 R 1 II p. H=6 Пептизация p. H = 11 * Surface area, А, m 2/g + После пептизации – Оствальдовское “созревание” – перенос между агрегатами 29
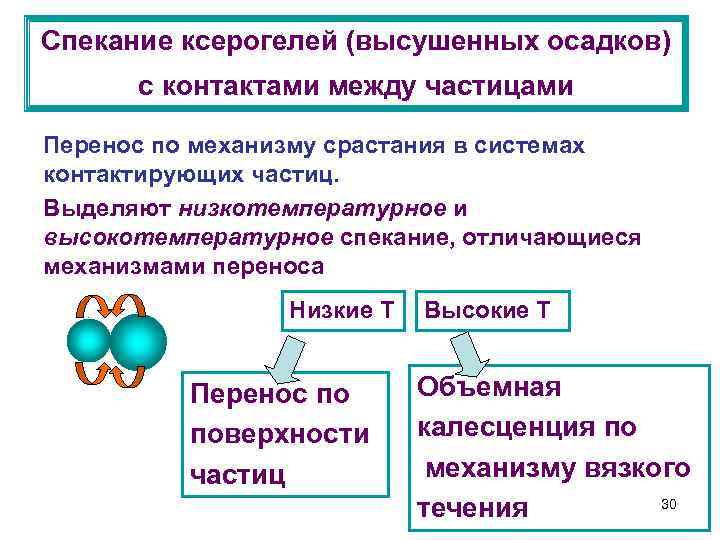
Спекание ксерогелей (высушенных осадков) с контактами между частицами Перенос по механизму срастания в системах контактирующих частиц. Выделяют низкотемпературное и высокотемпературное спекание, отличающиеся механизмами переноса Низкие Т Перенос по поверхности частиц Высокие Т Объемная калесценция по механизму вязкого 30 течения
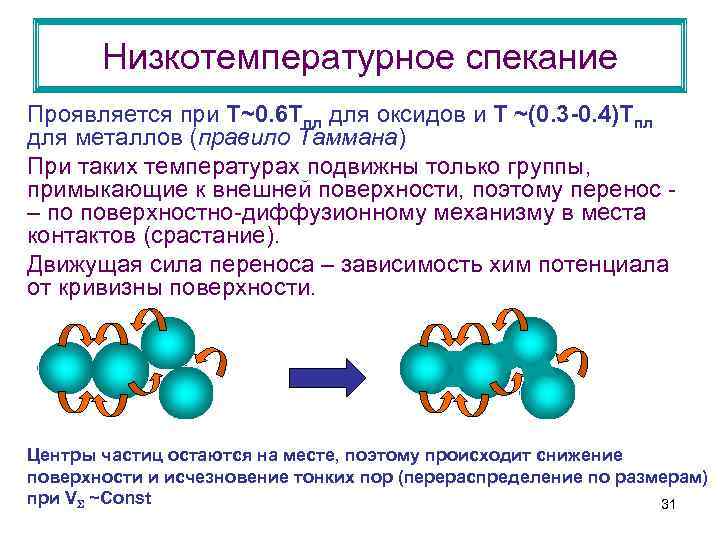
Низкотемпературное спекание Проявляется при Т~0. 6 Тпл для оксидов и Т ~(0. 3 -0. 4)Тпл для металлов (правило Таммана) При таких температурах подвижны только группы, примыкающие к внешней поверхности, поэтому перенос – по поверхностно-диффузионному механизму в места контактов (срастание). Движущая сила переноса – зависимость хим потенциала от кривизны поверхности. Центры частиц остаются на месте, поэтому происходит снижение поверхности и исчезновение тонких пор (перераспределение по размерам) при V ~Сonst 31

Гидротермальная обработка (ГТО) ксерогелей – аналог низкотемпературного спекания с переносом через объем раствора ГТО проводится в автоклавах при температурах до 300 -4000 С и давлении паров воды до 100 -300 атм для интенсификации процессов в осадках. Пористое пространство заполнено раствором, т. к. Р/Р 0=1. Перенос определяется растворимостью частиц твердой фазы в дисперсионной среде и происходит по механизму зарастания (перенос через объем жидкой фазы) без смещения центров частиц. ГТО приводит к снижению поверхности и перераспределению пористости при V ~Сonst 32
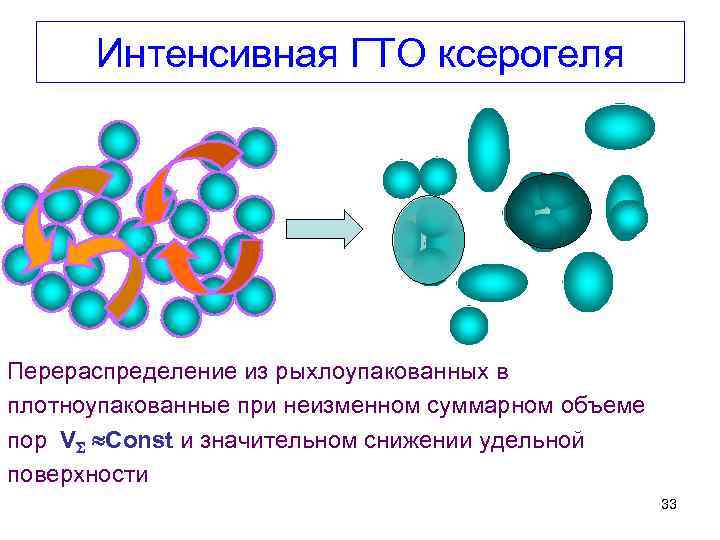
Интенсивная ГТО ксерогеля Перераспределение из рыхлоупакованных в плотноупакованные при неизменном суммарном объеме пор V Сonst и значительном снижении удельной поверхности 33
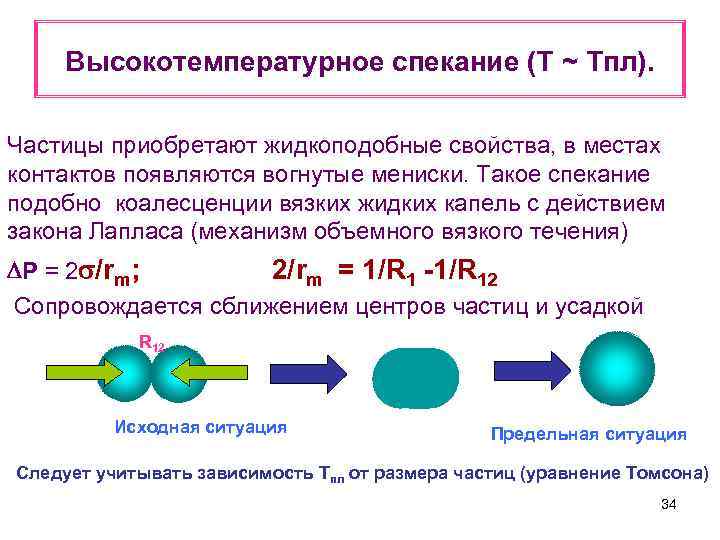
Высокотемпературное спекание (Т ~ Tпл). Частицы приобретают жидкоподобные свойства, в местах контактов появляются вогнутые мениски. Такое спекание подобно коалесценции вязких жидких капель с действием закона Лапласа (механизм объемного вязкого течения) Р = 2 /rm; 2/rm = 1/R 1 -1/R 12 Сопровождается сближением центров частиц и усадкой R 12 Исходная ситуация Предельная ситуация Следует учитывать зависимость Тпл от размера частиц (уравнение Томсона) 34

Высокотемпературное спекание в системе контактирующих частиц + Коалесценция вязких жидкоподобных капель (ур. Лапласа-Юнга) Равнодействующая возникающих капиллярных сил в плотных участках больше, чем в рыхлых, в результате возможна полная коалесценция плотных участков и рост крупных пор (пустот) в исходных рыхлых зонах. Возможно снижение объема частицы и суммарного объема пор 35

ГТО в ксерогелях Результаты могут существенно зависеть от неравномерной локализации примесей, способствующих образованию подвижных форм. Поэтому возможно локальное спекание отдельных зон при малых изменениях в более «чистых» зонах. Неотмытые щелочи приводят к спеканию Si. O 2 уже при 100 -1500 С, соли щелочных металлов – при температурах выше 200 -4000 С 36
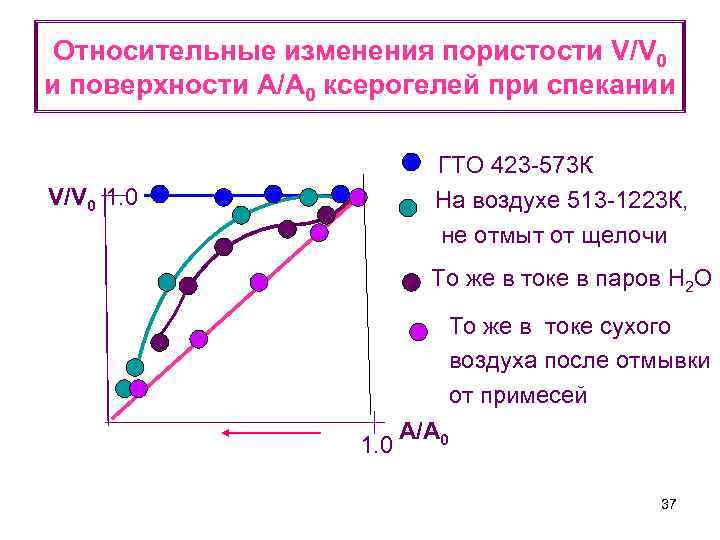
Относительные изменения пористости V/V 0 и поверхности A/A 0 ксерогелей при спекании ГТО 423 -573 К На воздухе 513 -1223 К, не отмыт от щелочи V/V 0 1. 0 То же в токе в паров Н 2 О То же в токе сухого воздуха после отмывки от примесей 1. 0 A/A 0 37

Характерные изменения текстуры при термообработке рост А V снижение dпор Сonst Механизм переноса Спекание при низких Т - зарастание контактов и плотно упакованных участков по механизму поверхностной диффузии (ксерогель) Спекание при высоких Т- коалесценция по механизму объемного течения (ксерогель) Сonst Локальная объемная коалесценция ксерогелей Зарастание контактов на стадии гидрогеля Комбинированный м-зм зарастанияпереконденсации в гидрогеле 38
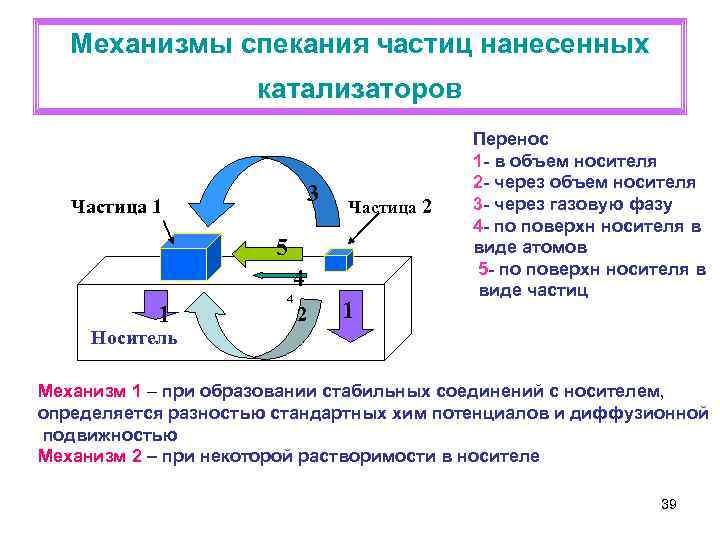
Механизмы спекания частиц нанесенных катализаторов 3 Частица 1 Частица 2 5 4 1 4 2 1 Перенос 1 - в объем носителя 2 - через объем носителя 3 - через газовую фазу 4 - по поверхн носителя в виде атомов 5 - по поверхн носителя в виде частиц Носитель Механизм 1 – при образовании стабильных соединений с носителем, определяется разностью стандартных хим потенциалов и диффузионной подвижностью Механизм 2 – при некоторой растворимости в носителе 39

Механизмы спекания частиц нанесенных катализаторов Механизм переноса через газовую фазу реализуется в химических газотранспортных реакциях при образовании летучих галогенидов, оксогалогенидов, карбонилов, ацетатов и др. при Т 500 -7000 заметна летучесть Pt. Cl 2 и Pt. Cl 4, многих соединений Cr, Ni, Ti, например, Pt(СО)Cl 2 кипит при 3000 С , а Ni(CO)4 –уже при 45 -500 С Ряд таких реакций используется для приготовления нанесенных катализаторов методом CVD (chemical Vapor Deposition) Такие соединения могут переноситься через газовую фазу или по поверхности носителя. 40

«вечная лампочка» Если в лампе накаливания с нитью из W повысить рабочую температуру до 1400 -28000 С, то W будет интенсивно испаряться и осаждаться на стенках. Введем в лампу немного Cl 2 или Br 2 или J 2. На стенке будет образовываться WГ 6, летучий при 300 -4000 С, который будет разлагаться до W и Г 2 в наиболее горячей части нити W +3 Cl 2 WCl 6(газ, 4000 С) Cl 2 + W (14000 С) WCl 6 W галоген играет роль транспортного агента или своеобразного катализатора, возвращающего W в наиболее горячие зоны на поверхность нити 41

Механизмы переноса по поверхности носителя Механизмы переноса частиц по поверхности носителя реализуются при размере частиц 5 нм и зависят от взаимодействия с носителем. Одна из распространенных интерпретаций – механизм “движения гусеницы трактора”: Атомы металла мигируют по поверхности частицы в направлении наибольшей адгезии с носителем, что и приводит к движению частицы При отсутствии преимущественной адгезии – случайная миграция до 42 момента контакта с последующей коалесценцией или срастанием

Механизмы переноса по поверхности носителя Миграция атомов по поверхности обусловлена их сорбцией (адгезией) и зависимостью плотности атомных атмосфер вокруг частиц от их размера C = C 0 ехр(+ 2 vm/rm. RT) 43

Соотношения когезии Wa и адгезии Wk В ряде работ используется критерий h/Rk = 2(1 – Wa/Wk) h –толщина пленки нанесенного компонента, Rk – минимальный размер его стабильного кластера на поверхности. Это условие применимо только для относительно толстых пленок, которые образуются при Wa/Wk 1 при Wa/Wk<1 стабильны кластеры. 44

Соотношения когезии Wa и адгезии Wk При малых заполнениях (и очень тонких пленках) вводят параметр , пропорциональный разнице прочности связей Г/Х и Г/Г. Используется условие 3 h/Rk = 2(1 – Wa/Wk) + /h 3 (металл-пар) <1 при Г/Г >Г/Х и правая часть ур-ния может быть <1 Эти условия благоприятны для кластеров, противоположная ситуация – для пленок. 45

Соотношения когезии Wa и адгезии Wk Соотношение Wa/Wk позволяет оценивать общие ситуации. Окисление металла на оксидном носителе усиливает адгезию и в пределе может сопровождаться растеканием нанесенного компонента. Восстановление в этом случае снижает адгезию, способствует трансформации пленки в кластеры металла. Чередование окислительной и восстановительной обработок может сопровождаться редиспергированием нанесенного металла (Pt, Ir, Rh и др). 46

Факторы, влияющие на процесс спекания нанесённых металлических частиц Специфические механизмы: • Среда термообработки – образование летучих соединений ведёт к наиболее интенсивному спеканию • Температура термообработки – скорость спекания увеличивается с увеличением температуры Общие механизмы: • Взаимодействие металл-металл и металл-носитель • Состав поверхности (функциональные группы, загрязнения) • Морфология поверхности (кривизна, дефектность) • Исходное распределение частиц по размерам (5 нм – пороговый размер для перемещения частиц как целого) • В случае пористых носителей – размер пор 47

48

49
лекция 14.ppt