Оксиды серы.pptx
- Количество слайдов: 43

12 сентября 2011 года

Способы выражения результатов химического анализа

Для обеспечения сравнения результатов измерений содержания газов, паров, твердых частиц, химических загрязнений в воздухе, полученных специалистами разных стран, международный стандарт ИСО 4226 устанавливает единицы измерений и их обозначения, которые унифицированы нв базе международной системы единиц СИ.

Объемную долю составных частей воздуха выражают в объемных процентах. Массовую концентрацию газообразных загрязнителей 3 3 выражают в мг/м или мкг/м. Допускается концентрацию газообразных загрязнителей выражать в мг/л.

Массовую концентрацию твердых взвешенных частиц выражают в мг/м 3, мкг/м 3 или г/м 3. При оценке отложения пыли за определенный период наблюдения (как правило 30 суток) ее слой оценивают в мг/(м 2 30 сут) или г/(м 2 30 сут)

Биологические, микробиологические загрязнения, а также споры, цветочную пыльцу и т. д. выражают в величинах м-3 или дм-3

Формула для расчета содержания загрязняющих веществ в атмосферном воздухе

Приведение объема газа к нормальным условиям

Нормальные условия для газов Температура 273 К (Т) или 0 С (t) Давление (P) 1 атмосфера, 760 мм ртутного столба или 101, 3 к. Па

T 0=273 K; P 0=1 атм. =760 мм РТ ст=101, 3 к. Па
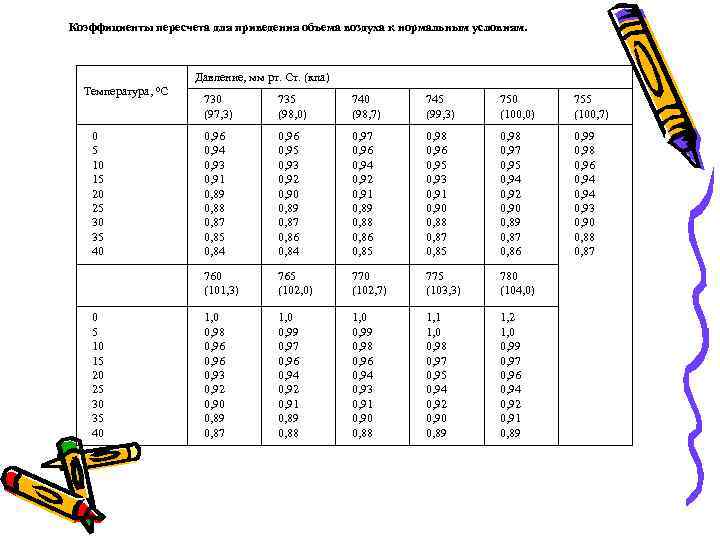
Коэффициенты пересчета для приведения объема воздуха к нормальным условиям. Давление, мм рт. Ст. (кпа) Температура, 0 С 0 5 10 15 20 25 30 35 40 735 (98, 0) 740 (98, 7) 745 (99, 3) 750 (100, 0) 755 (100, 7) 0, 96 0, 94 0, 93 0, 91 0, 89 0, 88 0, 87 0, 85 0, 84 0, 96 0, 95 0, 93 0, 92 0, 90 0, 89 0, 87 0, 86 0, 84 0, 97 0, 96 0, 94 0, 92 0, 91 0, 89 0, 88 0, 86 0, 85 0, 98 0, 96 0, 95 0, 93 0, 91 0, 90 0, 88 0, 87 0, 85 0, 98 0, 97 0, 95 0, 94 0, 92 0, 90 0, 89 0, 87 0, 86 0, 99 0, 98 0, 96 0, 94 0, 93 0, 90 0, 88 0, 87 760 (101, 3) 0 5 10 15 20 25 30 35 40 730 (97, 3) 765 (102, 0) 770 (102, 7) 775 (103, 3) 780 (104, 0) 1, 0 0, 98 0, 96 0, 93 0, 92 0, 90 0, 89 0, 87 1, 0 0, 99 0, 97 0, 96 0, 94 0, 92 0, 91 0, 89 0, 88 1, 0 0, 99 0, 98 0, 96 0, 94 0, 93 0, 91 0, 90 0, 88 1, 1 1, 0 0, 98 0, 97 0, 95 0, 94 0, 92 0, 90 0, 89 1, 2 1, 0 0, 99 0, 97 0, 96 0, 94 0, 92 0, 91 0, 89

Загрязнение атмосферного воздуха оксидами серы и методы их определения

Соединения серы поступают в воздух в основном при сжигании богатых серой видов горючего: угля и мазута. Образующиеся окислы серы загрязняют воздух во многих районах Земного шара. Будучи рассеянными в атмосфере посредством высоких дымовых труб, эти окислы становятся основной причиной кислотных дождей. Тем не менее, топливо необходимо для получения тепла, электричества и энергии для приведения в действие различных машин.

Не все виды топлива содержат значительные количества серы. В углях некоторых сортов содержится всего 0, 5% серы, тогда как в других до 6%. Уголь широко используется в производстве стали, но в первую очередь он применяется как топливо для получения пара и последующего генерирования электроэнергии. Среднее содержание серы в углях, идущих на получение электроэнергии, составляет 2, 5%. При сгорании в топках электростанций каждого миллиона тонн угля выделяется 25 тысяч тонн серы, главным образом в виде сернистого газа – SO 2. В 2005 году для получения электроэнергии в топках электростанций было сожжено 645 млн. т угля, при этом выделилось около 35 млн. т сернистого газа.

Сера также содержится в сырой нефти, однако ее содержание не превышает 1%. При перегонке нефти большая часть серы из продуктов перегонки, таких как бензин и керосин, удаляется. Вот почему керосин и бензин делают лишь небольшой вклад в выбросы окислов серы, попадающих в атмосферу ( 5).

Окислы серы вызывают затруднение дыхания. Уже одного этого достаточно чтобы бороться с выбросами окислов серы в атмосферу. Имеется подозрение на тот счет, что оксиды серы во взаимодействии с другими веществами могут являться причиной онкологических заболеваний.

Высокая концентрация SO 2 и ее производных вызывает серьезное повреждение растительности. При концентрации 3000 мкг/м 3 листья хвоя и другие растительные ткани выглядят побелевшими. Постепенно приобретают вид обожженных, становятся красновато-коричневыми и опадают. Даже когда содержание SO 2 составляет всего 100 мкг/м 3, что нередко имеет место в городах, растения могут приобретать желтоватый оттенок. Фруктовые деревья (яблони, груши) и лесные (сосна, лиственница) чувствительны к повреждениям от окислов серы. Весьма чувствительны к окислам серы хлопчатник, люцерна и ячмень.

И, наконец, SO 2 являются главным фактором, обуславливающим образование кислотных дождей, которые закисляют озера, и которые как полагают, ответственны за широкомасштабную гибель лесов.
Образование кислотных дождей
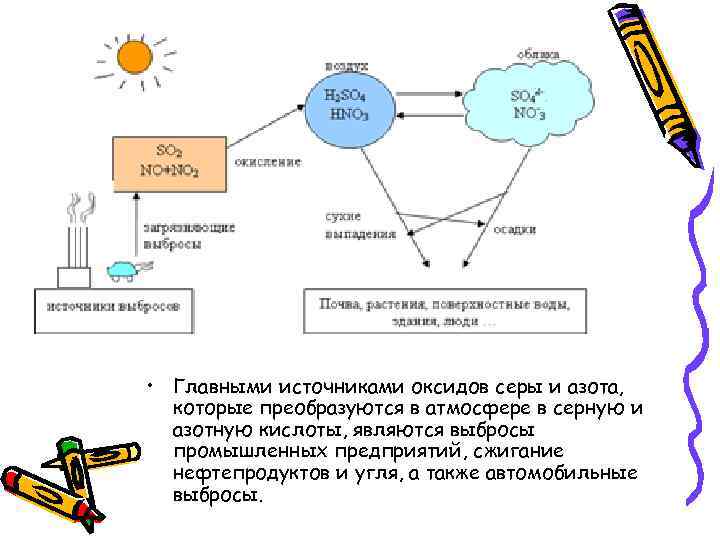
• Главными источниками оксидов серы и азота, которые преобразуются в атмосфере в серную и азотную кислоты, являются выбросы промышленных предприятий, сжигание нефтепродуктов и угля, а также автомобильные выбросы.
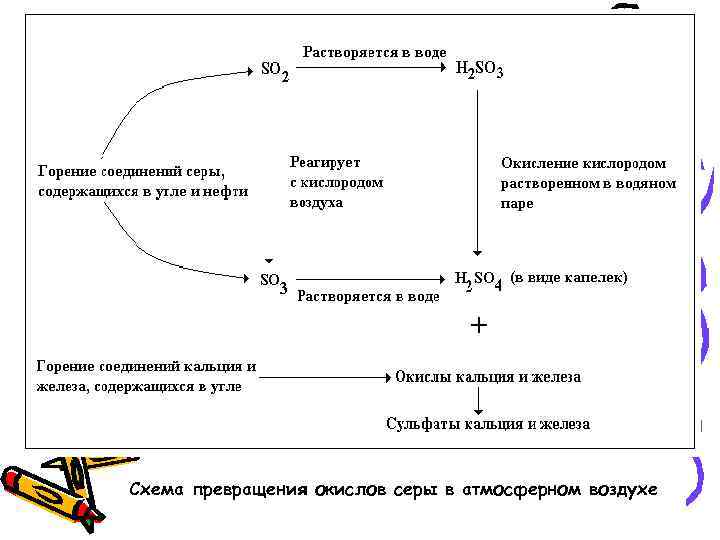
Схема превращения окислов серы в атмосферном воздухе

• При сжигании угля и нефти, содержащаяся в них сера окисляется. При этом образуется в основном SO 2 и SO 3. В процессе первоначального горения до SO 3 окисляется менее 3% серы. Оставшаяся часть превращается в двуокись серы и в таком виде поступает в атмосферу (первичный загрязнитель). Здесь SO 2 постепенно окисляется кислородом воздуха до SO 3. Которая сразу же реагирует с водяным паром, образуя серную кислоту. H 2 SO 4 присутствует в воздухе в виде легкого тумана, состоящего из крошечных капель. Этот туман обладает высокой коррозирующей способностью и разъедает многие материалы, в том числе строительные материалы: мрамор и известь.

• SO 2 образующаяся при сжигании топлива, тоже вступает в реакцию с парами воды, образуя сернистую кислоту (H 2 SO 4). Эта слабая кислота в свою очередь постепенно реагирует с кислородом воздуха, образуя H 2 SO 4. Итак, серная кислота в воздухе образуется двумя путями. В сухом воздухе образуется главным образом SO 3 и затем серная кислота, а при высокой влажности образуется сернистая кислота, которая затем окисляется до серной.

При сжигании топлива образуются также окислы железа и кальция. Эти окислы попадают в атмосферу в больших количествах при сжигании угля, но при сжигании нефти их образуется гораздо меньше. Попавшие в атмосферу окислы железа и кальция обычно вступают в реакцию с серной кислотой с образованием частиц сульфатов: Ca. O + H 2 SO 4 Ca. SO 4 + H 2 O Fe 2 O 3 + 3 H 2 SO 4 Fe 2(SO 4)3 + 3 H 2 O Количество содержащихся в городском воздухе частиц сульфатов и капелек серной кислоты может достигать от 5 до 20%.

Диоксид серы (SO 2) и серный ангидрид (SO 3) в комбинации со взвешенными частицами и влагой оказывают наиболее вредной воздействие на человека, живые организмы и материальные ценности SO 2 бесцветный и негорючий газ, запах которого начинает ощущаться при его концентрации в воздухе 0, 3 -1, 0 млн -1, а при концентрации свыше 3 млн-1 SO 2 имеет острый раздражающий запах. Диоксид серы в смеси с твердыми частицами и серной кислотой (раздражитель более сильный, чем SO 2) уже при среднегодовом содержании 9, 04 -0, 09 млн-1. и концентрации дыма 150 -200 мкг/м 3 приводит к увеличению симптомов затрудненного дыхания и болезней легких, а при среднесуточном содержании SO 2 0, 2 -0, 5 млн-1 и концентрации дыма 500750 мкг/м 3 наблюдается резкое увеличение числа больных и смертельных исходов. При концентрации SO 2 0, 3 -0, 5 млн-1 в течение нескольких дней наступает хроническое поражение листьев растений (особенно шпината, салата, хлопка и люцерны), а также иголок сосны.

Суточный стандарт для окислов серы, принятый в 1971 году и опирающийся на показатели здоровья человека, составляет 365 мкг/м 3, причем этот уровень не должен превышаться более одного раза в течение года. Считают, что о загрязнении необходимо предупреждать, когда 24 -часовое среднее значение превышает 800 мкг/м 3. Годичный стандарт, т. е. усредненное значение за год, составляет 80 мкг/м 3. В сельской местности фоновая концентрация близка к 0, 5 мкг/м 3, однако в городах она в 50 -100 раз выше.

Предельно допустимые концентрации соединений серы. ПДК населенных мест Соединение Максимальная разовая SO 2 Туман H 2 SO 4 0, 5 мг/м 3 0, 3 мг/м 3 Класс опасности Среднесуточная 0, 05 мг/м 3 0, 1 мг/м 3 3 2

Определение сернистого ангидрида проводят нефелометрическим методом. Пробу воздуха (объемом не менее 90 л) со скоростью 6 л/мин пропускают через поглотительный прибор, содержащий раствор хлората калия: 3 SO 2 + KCl. O 3 + 3 H 2 O = 3 H 2 SO 4 + KCl. После чего к полученному раствору добавляют раствор, содержащий хлорид бария и этиленгликоль в качестве стабилизатора. H 2 SO 4 + Ba. Cl 2 = Ba. SO 4 + 2 HCl Через некоторое время определяют светорассеивание на фотоэлектроколриметре или нефелометре, и содержание определяют по калибровочному графику. Для определения содержания сернистого ангидрида можно использовать газоанализатор.

Определение аэрозоля серной кислоты основано на выделении иода при взаимодействии H 2 SO 4 с иодид-иодатной смесью и фотометрическом определении кислоты по желтой окраске раствора. 3 H 2 SO 4 + 5 KI + KIO 3 = 3 I 2 + 3 K 2 SO 4 +3 H 2 O Пробу воздуха (объемом не менее 50 л) со скоростью 10 -15 л/мин протягивают через патрон с фильтром АФА-10 или АФА-ХА-18. Сульфаты и другие газообразные кислые вещества не мешают определению. Затем поглощенную серную кислоту вымывают с фильтра, добавляют иодид-иодатную смесь и через некоторое время определяют оптическую плотность полученного раствора.

Совместное определение аэрозоля серной кислоты и растворимых сульфатов проводят турбидиметрическим методом. Для этого пробу воздуха объемом 90 л протягивают со скоростью 6 л/мин через поглотительный прибор, содержащий раствор хлорида бария и желатин в качестве стабилизатора. H 2 SO 4 + Ba. Cl 2 = Ba. SO 4 + 2 HCl Na 2 SO 4 + Ba. Cl 2 = Ba. SO 4 + 2 Na. Cl После фотометрирования полученной смеси содержание определяют по калибровочному графику.

Титриметрическое определение двуокиси серы Двуокись серы поглощают из воздуха раствором пероксида водорода. При этом образуется серная кислота. Отбор пробы проводят в течение 24 или 48 часов.

Полученный раствор переливают в коническую колбу или химический стакан и перемешивают с помощью магнитной мешалки. Добавляют 1 мл смешанного индикатора (тимоловый синий и бромфеноловый синий) и отмечают р. Н (желтый цвет индикатора – 4, бледно-сиреневый – 4, 5 и сине-фиолетовый – 5). Можно использовать вместо индикатора р. Н-метр. Если р. Н меньше 4, 5 то титруют тетраборатом натрия, а если больше – то серной кислотой до достижения р. Н=4, 5. Отмечают объем раствора, израсходованного на титрование. По результатам титрования вычисляют содержание двуокиси серы.

Спектрофотометрическое определение двуокиси серы • Он применяется для определения массовой концентрации двуокиси серы в окружающем воздухе в пределах от 3, 5 до 150 мкг/м 3 при условии, что объем пробы воздуха составляет 2 м 3, а объем поглотительного раствора – 50 мл.

Сущность метода заключается в поглощении и окислении двуокиси серы, присутствующей в отобранных пробах воздуха, пропускаемых в течение заданного времени через подкисленный раствор пероксида водорода. Образующиеся сульфат-ионы осаждают барием, а избыток бария определяется спектрометрическим измерением его окрашенного комплекса с с торином. Используется метод градуировочного графика.

Метод с применением тетрахлормеркурата и парарозанилина Данный метод применим для определения массовой концентрации двуокиси серы в воздухе в пределах от 20 до 500 мкг/м 3.

Сущность метода заключается в абсорбции двуокиси серы, находящейся в пробе воздуха, при пропускании через раствор тетрахлормеркурата натрия с образованием дихлорсульфитомеркуратного комплекса. Комплекс образует окрашенное соединение после добавления формальдегида и подкисленного раствора солянокислого парарозанилина, которое определяют спектрофотометрическим методом. Предварительно устанавливают градуировочную характеристику.

• Газоанализатор представляет собой автоматический показывающий прибор непрерывного действия, предназначенный для измерения массовой концентрации диоксида серы в атмосферном воздухе. Метрологические параметры прибора обеспечиваются встроенным калибратором. С-310 А ГАЗОАНАЛИЗАТОР
СВ-320 A-1/CB-320 A-2 ГАЗОАНАЛИЗАТОР ДИОКСИДА СЕРЫ, СЕРОВОДОРОДА И СЕРОСОДЕРЖАЩИХ СОЕДИНЕНИЙ В АТМОСФЕРНОМ ВОЗДУХЕ • Хемилюминесцентный газоанализатор представляет собой автоматический показывающий прибор непрерывного действия, предназначенный для измерения массовой концентрации в атмосферном воздухе сероводорода (H 2 S) и диоксида серы (SO 2) в присутствии сероорганических соединений. Прибор имеет два варианта исполнения: в одном корпусе (СВ 320 А-1) и в двух корпусах (СВ-320 А 2). Переключение циклов измерения H 2 S/SO 2 осуществляется автоматически в непрерывном режиме.



• Газовый хроматограф мод. Agilent 6890 N, ф. Agilent Technologies

• Электрохимические многокомпонентные газоанализаторы КАСКАД-Н 511

Хоббит-Т-SO 2 газоанализатор • Предназначены для измерения содержания и диоксида серы в воздухе рабочей зоны и для сигнализации об его увеличении выше допустимого предела
Оксиды серы.pptx