12_okisl_-vosst_r-tsii_2014.pptx
- Количество слайдов: 78
 № 12. Реакции окисления и восстановления органических соединений
№ 12. Реакции окисления и восстановления органических соединений
 Реакции окисления - восстановления реакции, в ходе которых происходит изменение степени окисления атома углерода, являющегося реакционным центром.
Реакции окисления - восстановления реакции, в ходе которых происходит изменение степени окисления атома углерода, являющегося реакционным центром.
 Степень окисления атома углерода в органическом веществе равна алгебраической сумме всех его связей с более ЭО элементом (Cl, O, S, N), учитываемых со знаком «+» , и связей с атомами Н, учитываемых со знаком «-» . При этом связи с соседними атомами углерода не учитываются.
Степень окисления атома углерода в органическом веществе равна алгебраической сумме всех его связей с более ЭО элементом (Cl, O, S, N), учитываемых со знаком «+» , и связей с атомами Н, учитываемых со знаком «-» . При этом связи с соседними атомами углерода не учитываются.
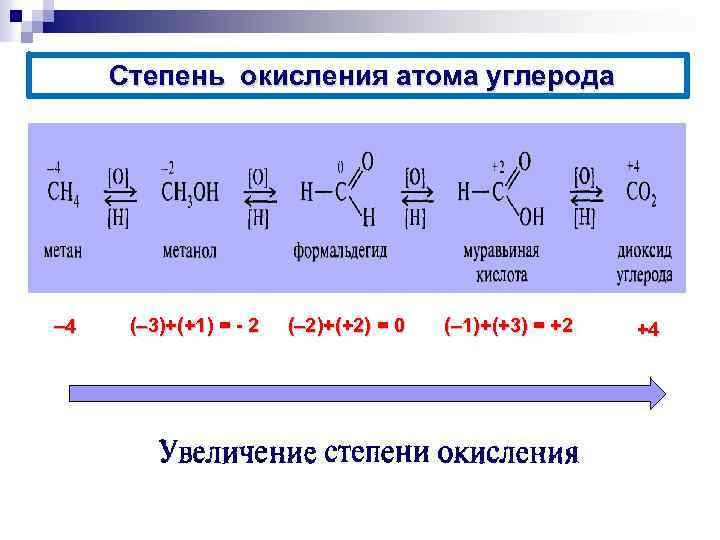 Степень окисления атома углерода 4 ( 3)+(+1) = - 2 ( 2)+(+2) = 0 ( 1)+(+3) = +2 +4
Степень окисления атома углерода 4 ( 3)+(+1) = - 2 ( 2)+(+2) = 0 ( 1)+(+3) = +2 +4
 Окисление Процесс удаления атомов Н с образованием кратной связи ; - замена связей С Н на связи с другими более ЭО элементами. Окисление – процесс перехода электронов n от субстрата к реагенту - окислителю, - «потеря электронов» атомом углерода. (степень окисления С увеличивается)
Окисление Процесс удаления атомов Н с образованием кратной связи ; - замена связей С Н на связи с другими более ЭО элементами. Окисление – процесс перехода электронов n от субстрата к реагенту - окислителю, - «потеря электронов» атомом углерода. (степень окисления С увеличивается)
 Восстановление n замена связей с ЭО элементами на новые связи С Н. Восстановление – процесс перехода электронов от восстановителя к органическому субстрату. - «приобретение электронов» атомом углерода. (степень окисления С уменьшается)
Восстановление n замена связей с ЭО элементами на новые связи С Н. Восстановление – процесс перехода электронов от восстановителя к органическому субстрату. - «приобретение электронов» атомом углерода. (степень окисления С уменьшается)
 Окисление органического соединения протекает тем легче, чем больше выражена в нём тенденция к передаче электронов.
Окисление органического соединения протекает тем легче, чем больше выражена в нём тенденция к передаче электронов.
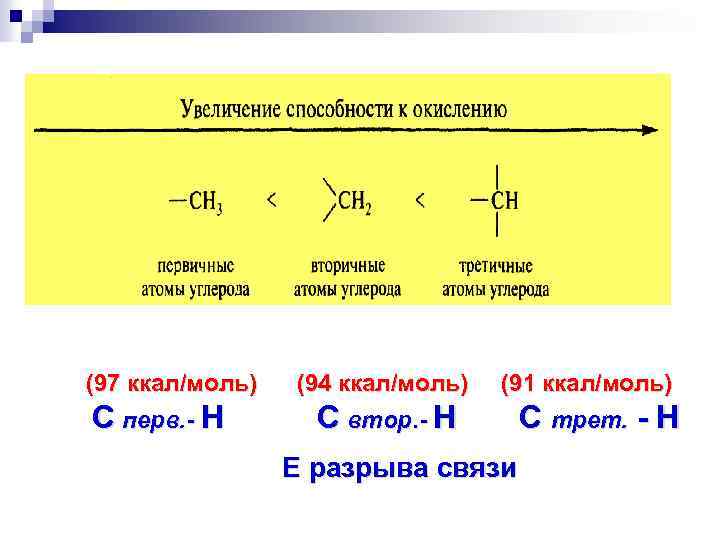 (97 ккал/моль) С перв. - Н (94 ккал/моль) С втор. - Н (91 ккал/моль) С трет. - Н Е разрыва связи
(97 ккал/моль) С перв. - Н (94 ккал/моль) С втор. - Н (91 ккал/моль) С трет. - Н Е разрыва связи
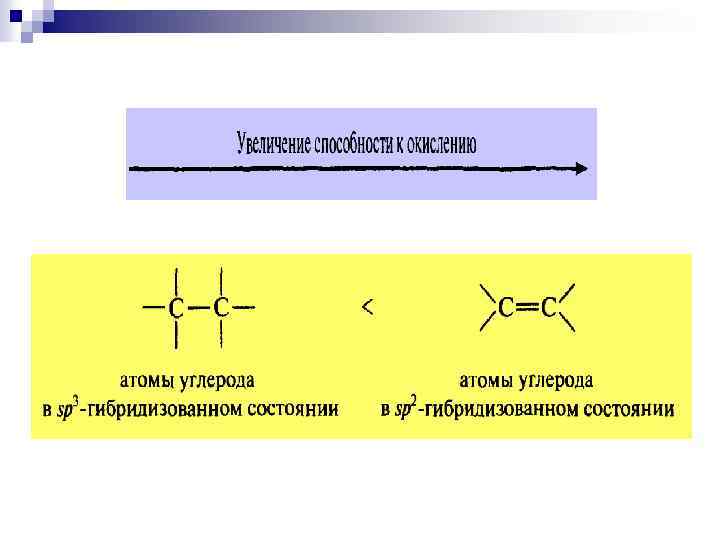
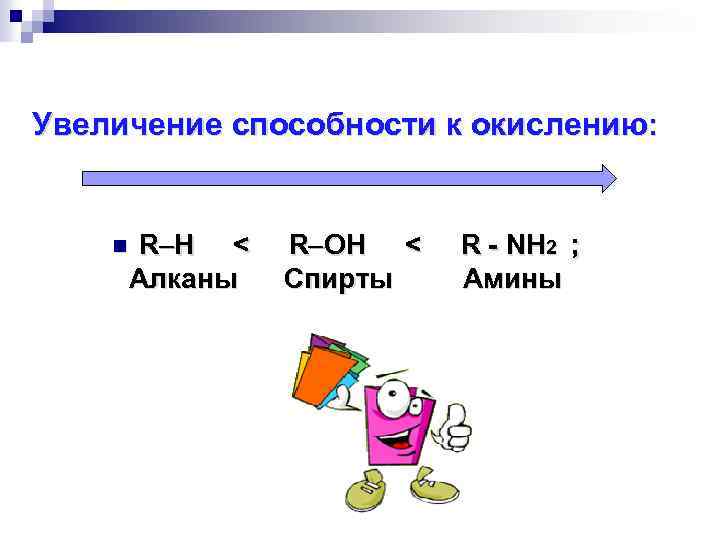 Увеличение способности к окислению: n R H < Алканы R OH < Спирты R - NH 2 ; Амины
Увеличение способности к окислению: n R H < Алканы R OH < Спирты R - NH 2 ; Амины
 Связи С С окисляются с большим трудом и всегда с разрушением соединения Горение алканов ( пламя): СН 4 + О 2 СО 2 + H 2 О + выделение тепла и света (полное окисление). n Окисление алканов сильными окислителями: RH + K 2 Cr 2 O 7 + H 2 SO 4, нагревание Смесь карбоновых кислот (неполное окисление). n
Связи С С окисляются с большим трудом и всегда с разрушением соединения Горение алканов ( пламя): СН 4 + О 2 СО 2 + H 2 О + выделение тепла и света (полное окисление). n Окисление алканов сильными окислителями: RH + K 2 Cr 2 O 7 + H 2 SO 4, нагревание Смесь карбоновых кислот (неполное окисление). n
 Окисление связей С-Н.
Окисление связей С-Н.
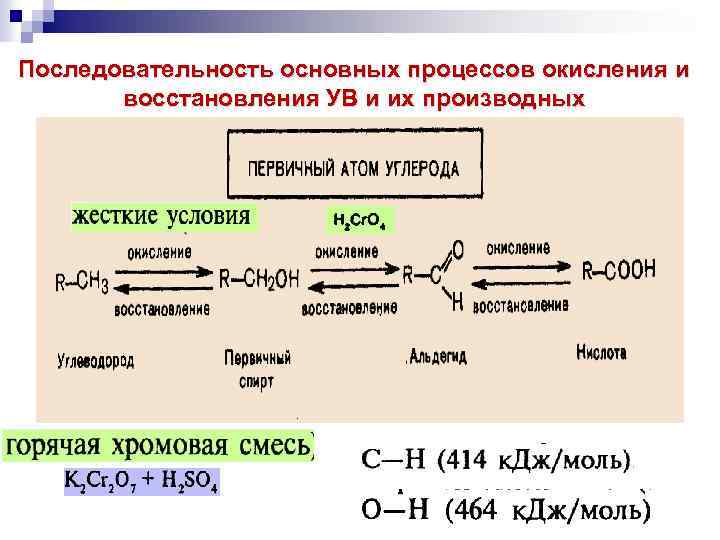 Последовательность основных процессов окисления и восстановления УВ и их производных
Последовательность основных процессов окисления и восстановления УВ и их производных
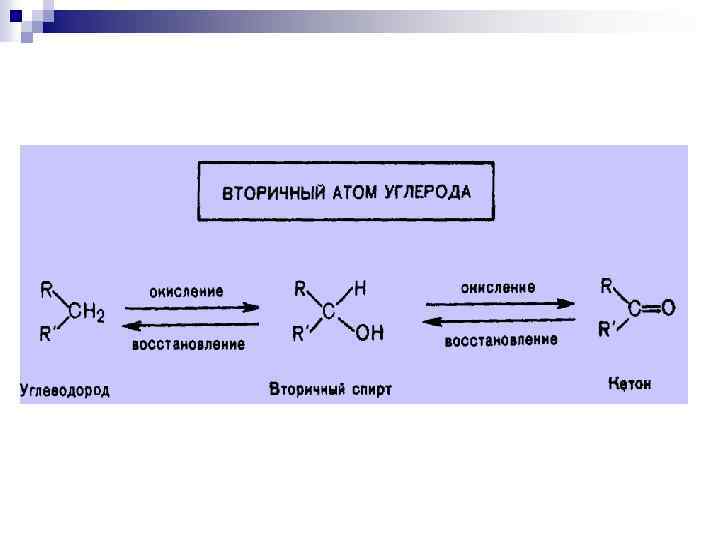
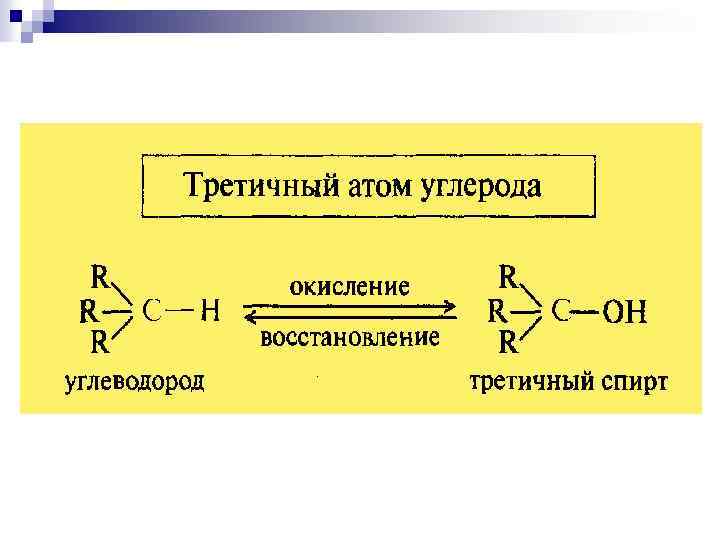
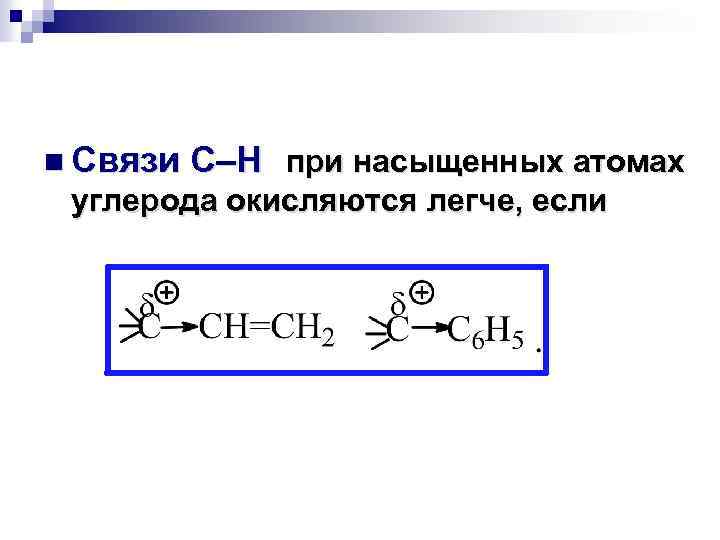 n Связи С–Н при насыщенных атомах углерода окисляются легче, если
n Связи С–Н при насыщенных атомах углерода окисляются легче, если
 Окисление в мягких условиях SR
Окисление в мягких условиях SR
 Пути образования АФК (активных форм кислорода) в организме: гидроксильный радикал
Пути образования АФК (активных форм кислорода) в организме: гидроксильный радикал
 Окислительная способность АФК: супероксидный анион-радикал
Окислительная способность АФК: супероксидный анион-радикал

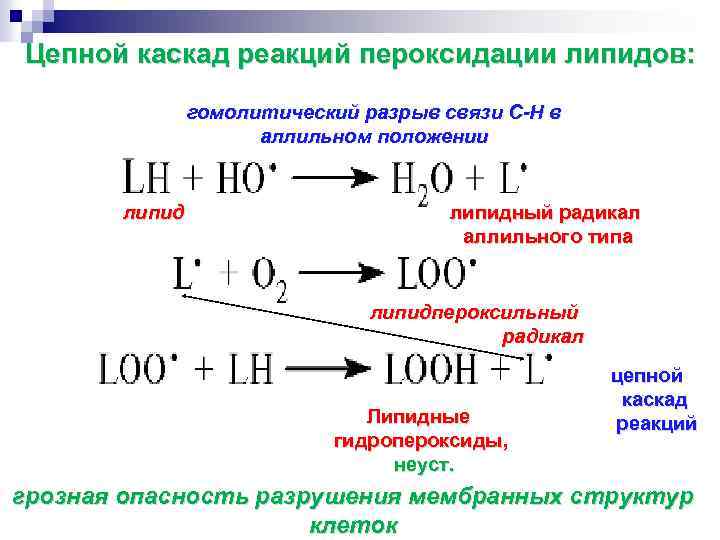 Цепной каскад реакций пероксидации липидов: гомолитический разрыв связи С-Н в аллильном положении липидный радикал аллильного типа липидпероксильный радикал Липидные гидропероксиды, неуст. цепной каскад реакций грозная опасность разрушения мембранных структур клеток
Цепной каскад реакций пероксидации липидов: гомолитический разрыв связи С-Н в аллильном положении липидный радикал аллильного типа липидпероксильный радикал Липидные гидропероксиды, неуст. цепной каскад реакций грозная опасность разрушения мембранных структур клеток
 Механизм эндогеной антиоксидантной защиты от избытка АФК: супероксиддисмутаза
Механизм эндогеной антиоксидантной защиты от избытка АФК: супероксиддисмутаза
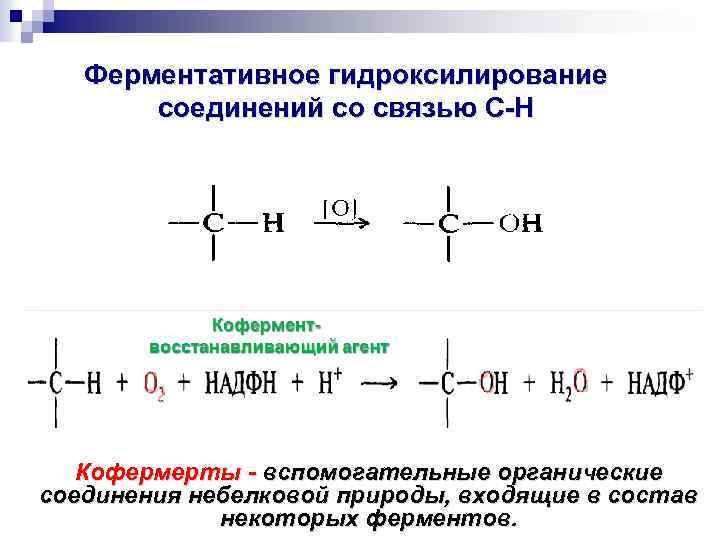 Ферментативное гидроксилирование соединений со связью С-Н Кофермерты - вспомогательные органические соединения небелковой природы, входящие в состав некоторых ферментов.
Ферментативное гидроксилирование соединений со связью С-Н Кофермерты - вспомогательные органические соединения небелковой природы, входящие в состав некоторых ферментов.
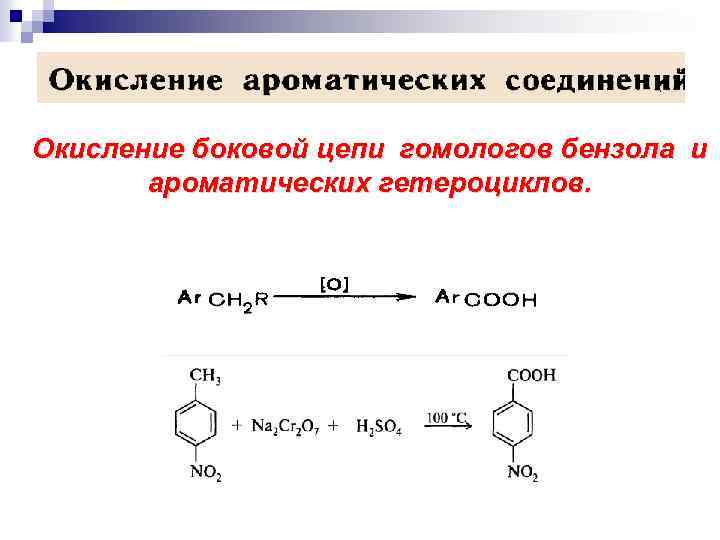 Окисление боковой цепи гомологов бензола и ароматических гетероциклов.
Окисление боковой цепи гомологов бензола и ароматических гетероциклов.
 Окисление спиртов (получение альдегидов и кетонов): n а) дегидрирование спиртов над R CH 2 OH Потеря потере металлическим катализатором + Cu 200 -300 С R CH=O + H 2 субстратом 2 х атомов Н эквивалентна или «восстановительный эквивалент»
Окисление спиртов (получение альдегидов и кетонов): n а) дегидрирование спиртов над R CH 2 OH Потеря потере металлическим катализатором + Cu 200 -300 С R CH=O + H 2 субстратом 2 х атомов Н эквивалентна или «восстановительный эквивалент»
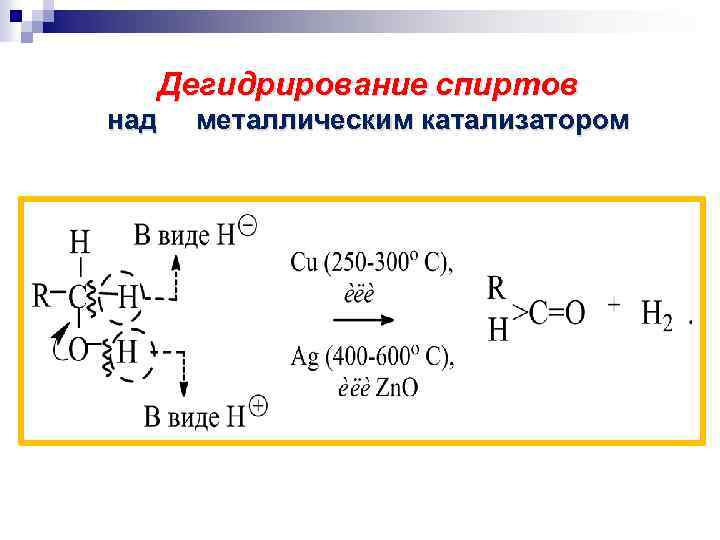 Дегидрирование спиртов над металлическим катализатором
Дегидрирование спиртов над металлическим катализатором
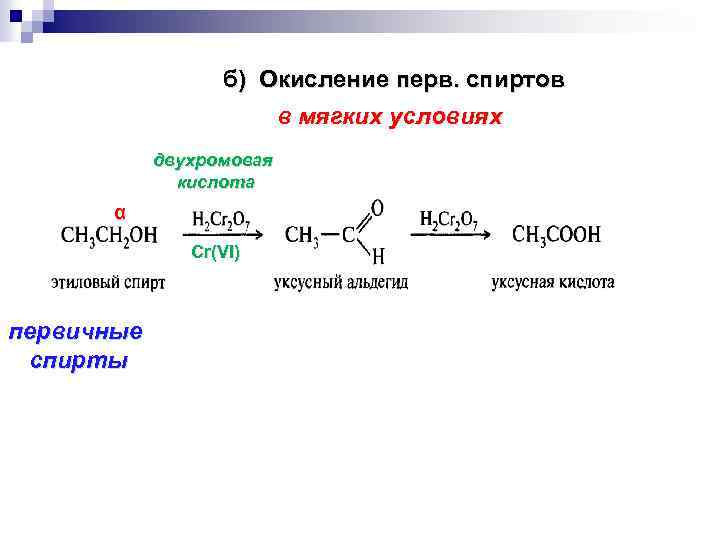 б) Окисление перв. спиртов в мягких условиях двухромовая кислота α Сr(VI) первичные спирты
б) Окисление перв. спиртов в мягких условиях двухромовая кислота α Сr(VI) первичные спирты
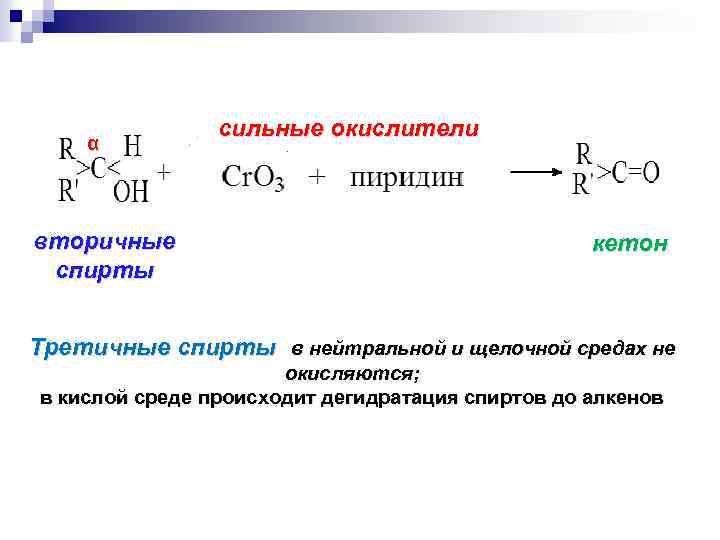 α вторичные спирты сильные окислители кетон Третичные спирты в нейтральной и щелочной средах не окисляются; в кислой среде происходит дегидратация спиртов до алкенов
α вторичные спирты сильные окислители кетон Третичные спирты в нейтральной и щелочной средах не окисляются; в кислой среде происходит дегидратация спиртов до алкенов
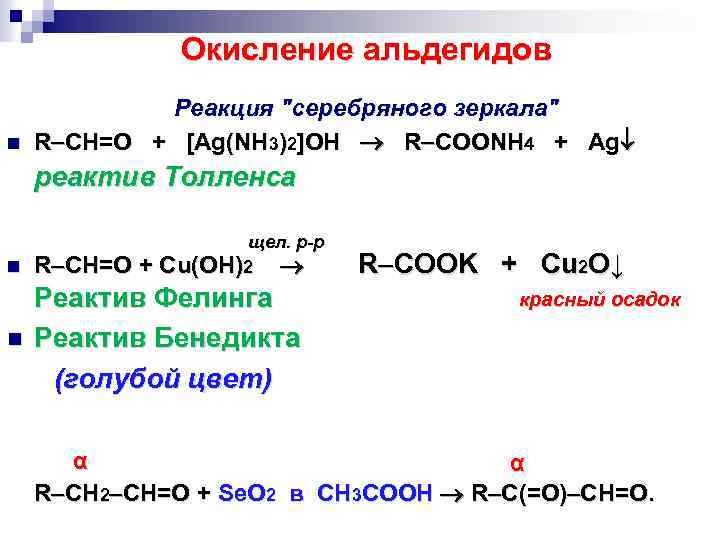 Окисление альдегидов n Реакция "серебряного зеркала" R CH=O + [Ag(NH 3)2]OH R COONH 4 + Ag реактив Толленса щел. р-р Cu(OH)2 n R CH=O + n Реактив Фелинга Реактив Бенедикта (голубой цвет) R COOK + Cu 2 O↓ красный осадок α α R CH 2 CH=O + Se. O 2 в CH 3 COOH R C(=O) CH=O.
Окисление альдегидов n Реакция "серебряного зеркала" R CH=O + [Ag(NH 3)2]OH R COONH 4 + Ag реактив Толленса щел. р-р Cu(OH)2 n R CH=O + n Реактив Фелинга Реактив Бенедикта (голубой цвет) R COOK + Cu 2 O↓ красный осадок α α R CH 2 CH=O + Se. O 2 в CH 3 COOH R C(=O) CH=O.
 1). Кофермент НАД Биологическое окисленная форма дегидрирование: восстановленная форма
1). Кофермент НАД Биологическое окисленная форма дегидрирование: восстановленная форма
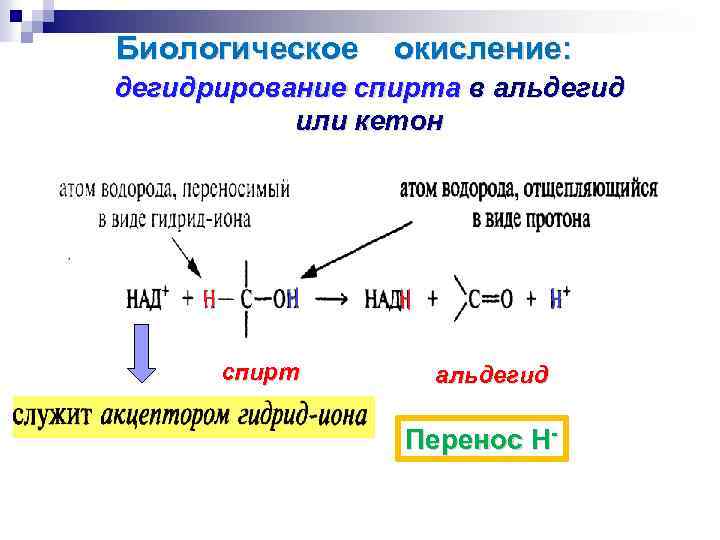 Биологическое окисление: дегидрирование спирта в альдегид или кетон спирт альдегид Перенос Н-
Биологическое окисление: дегидрирование спирта в альдегид или кетон спирт альдегид Перенос Н-
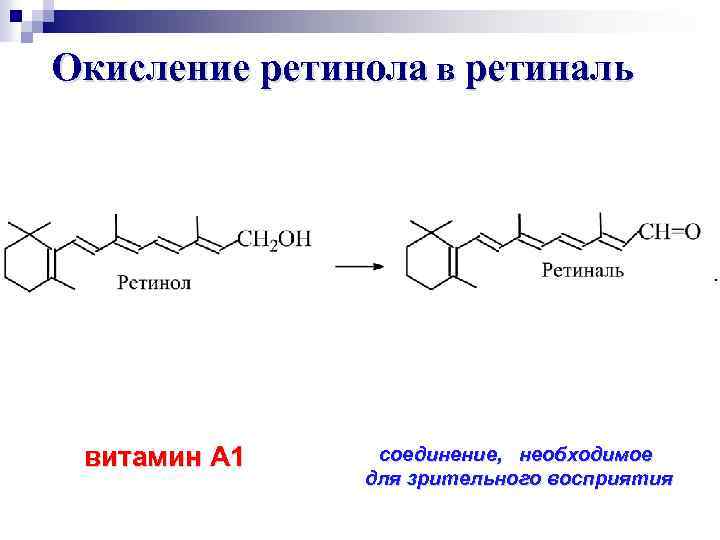 Окисление ретинола в ретиналь витамин А 1 соединение, необходимое для зрительного восприятия
Окисление ретинола в ретиналь витамин А 1 соединение, необходимое для зрительного восприятия
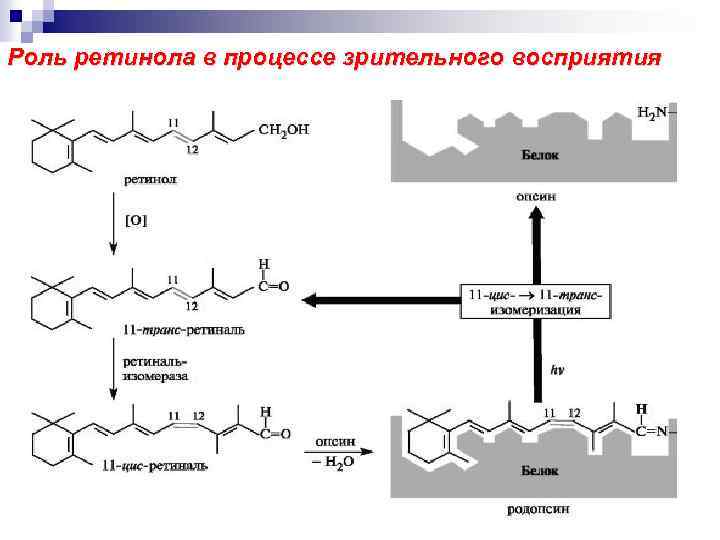 Роль ретинола в процессе зрительного восприятия
Роль ретинола в процессе зрительного восприятия
 Биологическое дегидрирование in vivo 2) Акцептор 2 атомов Н α, β- дегидрирование насыщенных жирных кислот:
Биологическое дегидрирование in vivo 2) Акцептор 2 атомов Н α, β- дегидрирование насыщенных жирных кислот:
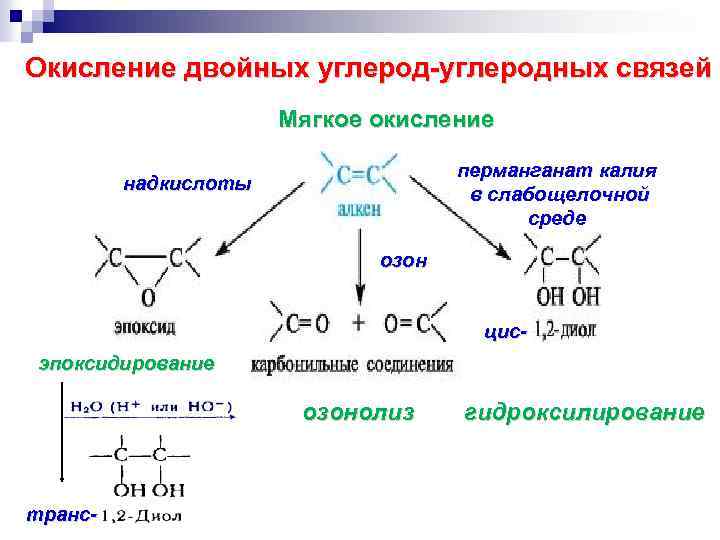 Окисление двойных углерод-углеродных связей Мягкое окисление перманганат калия в слабощелочной среде надкислоты озон цисэпоксидирование озонолиз транс- гидроксилирование
Окисление двойных углерод-углеродных связей Мягкое окисление перманганат калия в слабощелочной среде надкислоты озон цисэпоксидирование озонолиз транс- гидроксилирование
 Окисление двойных углерод-углеродных связей Жёсткие условия
Окисление двойных углерод-углеродных связей Жёсткие условия
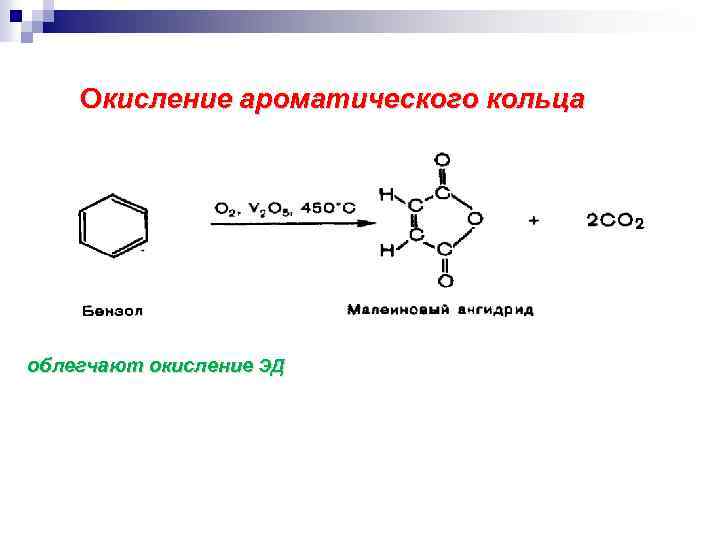 Окисление ароматического кольца облегчают окисление ЭД
Окисление ароматического кольца облегчают окисление ЭД
![Окисление фенолов до двухатомных фенолов: [O] фенол Гидрохинон Окисление фенолов до двухатомных фенолов: [O] фенол Гидрохинон](https://present5.com/presentation/125574593_288643392/image-38.jpg) Окисление фенолов до двухатомных фенолов: [O] фенол Гидрохинон
Окисление фенолов до двухатомных фенолов: [O] фенол Гидрохинон
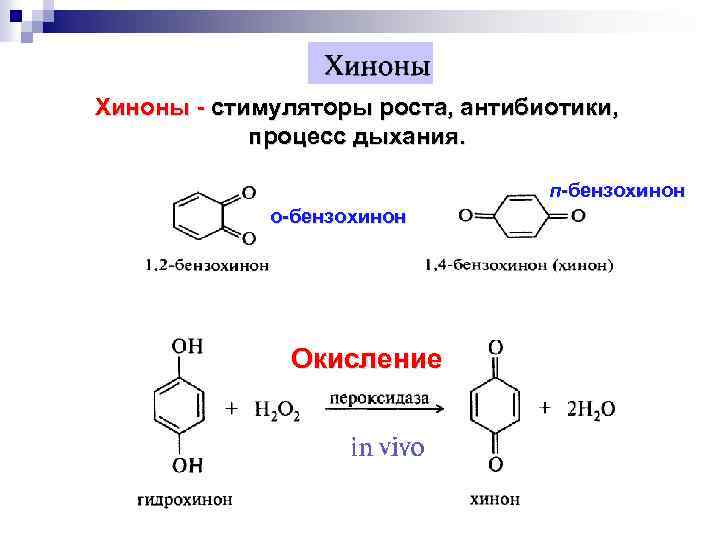 Хиноны - стимуляторы роста, антибиотики, процесс дыхания. п-бензохинон о-бензохинон Окисление
Хиноны - стимуляторы роста, антибиотики, процесс дыхания. п-бензохинон о-бензохинон Окисление
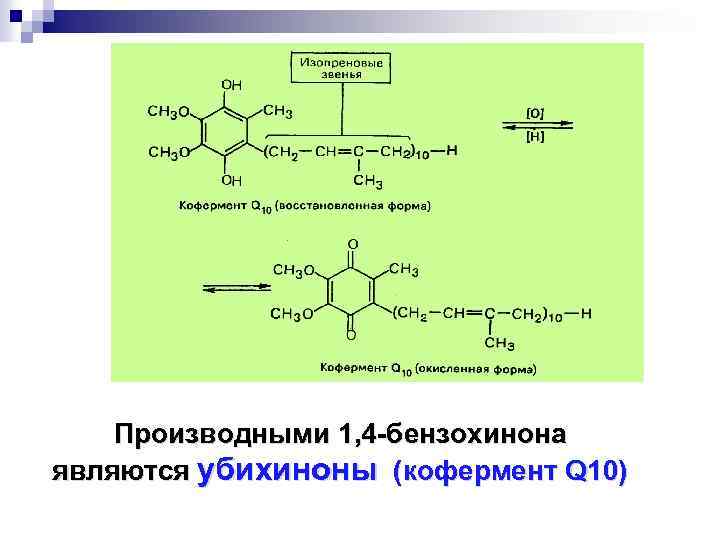 Производными 1, 4 -бензохинона являются убихиноны (кофермент Q 10)
Производными 1, 4 -бензохинона являются убихиноны (кофермент Q 10)
 Co. Q 10 Функции в организме: n *Обеспечивает выработку энергии на клеточном уровне *Положительно влияет на сердечно-сосудистую систему, головной мозг и периферическую нервную систему *Оказывает поддержку иммунной системе *Повышает регенеративные процессы слизистой оболочки десен и других быстрорастущих тканей n *Обладает антиоксидантной активностью
Co. Q 10 Функции в организме: n *Обеспечивает выработку энергии на клеточном уровне *Положительно влияет на сердечно-сосудистую систему, головной мозг и периферическую нервную систему *Оказывает поддержку иммунной системе *Повышает регенеративные процессы слизистой оболочки десен и других быстрорастущих тканей n *Обладает антиоксидантной активностью
 Богатые источники Co. Q 10 n говяжье сердце и другие внутренние органы, яичный желток, печень, треска, молочный жир, различные виды цельного зерна. n В среднем человек должен потреблять приблизительно 5 мг Co. Q 10 в день
Богатые источники Co. Q 10 n говяжье сердце и другие внутренние органы, яичный желток, печень, треска, молочный жир, различные виды цельного зерна. n В среднем человек должен потреблять приблизительно 5 мг Co. Q 10 в день
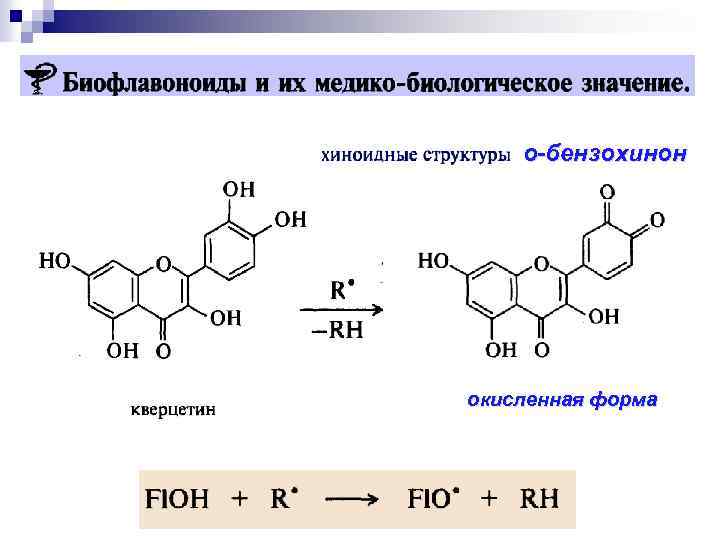 о-бензохинон окисленная форма
о-бензохинон окисленная форма
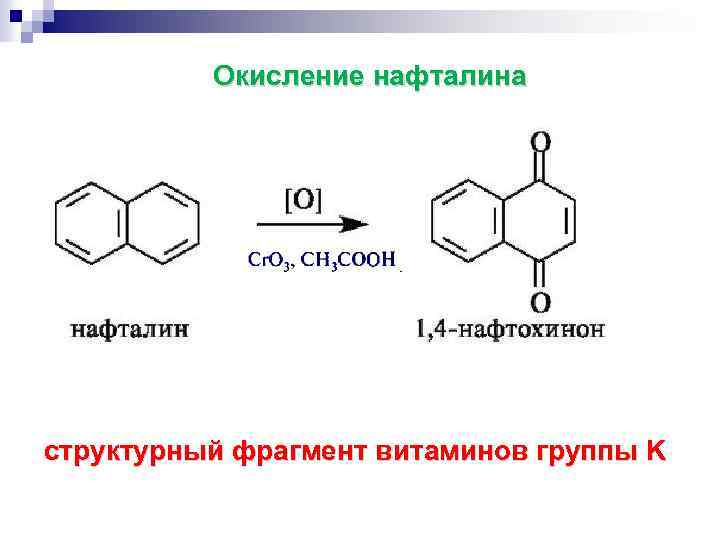 Окисление нафталина структурный фрагмент витаминов группы K
Окисление нафталина структурный фрагмент витаминов группы K
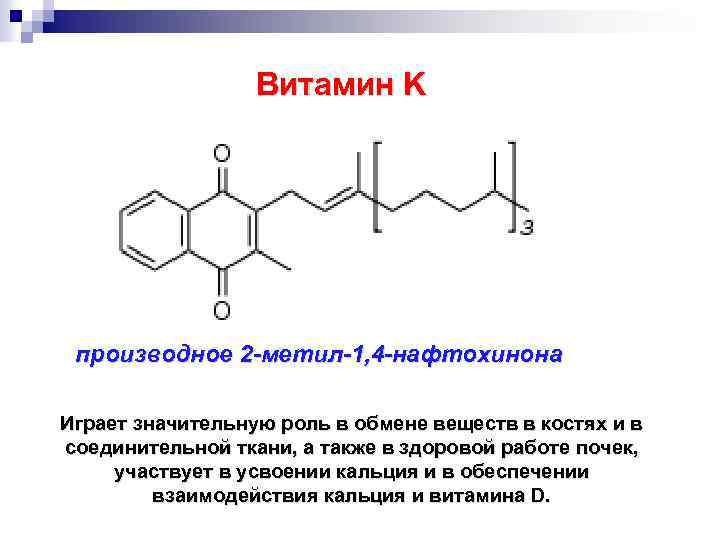 Витамин K производное 2 -метил-1, 4 -нафтохинона Играет значительную роль в обмене веществ в костях и в соединительной ткани, а также в здоровой работе почек, участвует в усвоении кальция и в обеспечении взаимодействия кальция и витамина D.
Витамин K производное 2 -метил-1, 4 -нафтохинона Играет значительную роль в обмене веществ в костях и в соединительной ткани, а также в здоровой работе почек, участвует в усвоении кальция и в обеспечении взаимодействия кальция и витамина D.
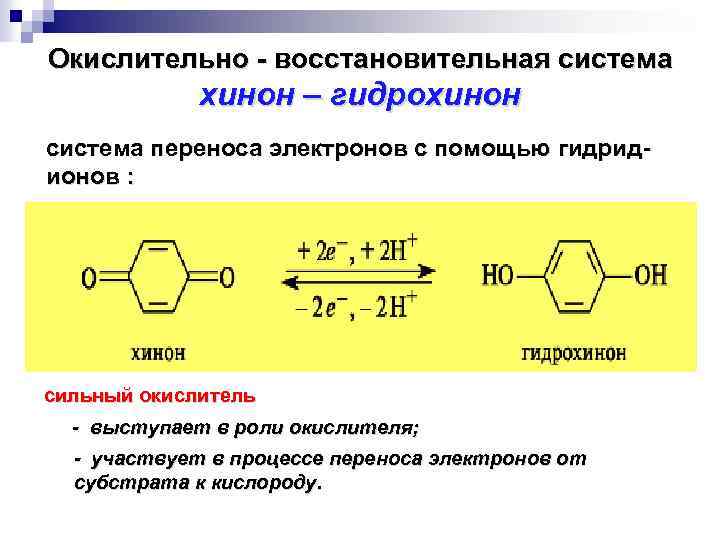 Окислительно - восстановительная система хинон – гидрохинон система переноса электронов с помощью гидридионов : сильный окислитель - выступает в роли окислителя; - участвует в процессе переноса электронов от субстрата к кислороду.
Окислительно - восстановительная система хинон – гидрохинон система переноса электронов с помощью гидридионов : сильный окислитель - выступает в роли окислителя; - участвует в процессе переноса электронов от субстрата к кислороду.
 Окисление серосодержащих соединений Мягкое окисление H 2 O 2, или Cu. Cl 2, или O 2
Окисление серосодержащих соединений Мягкое окисление H 2 O 2, или Cu. Cl 2, или O 2
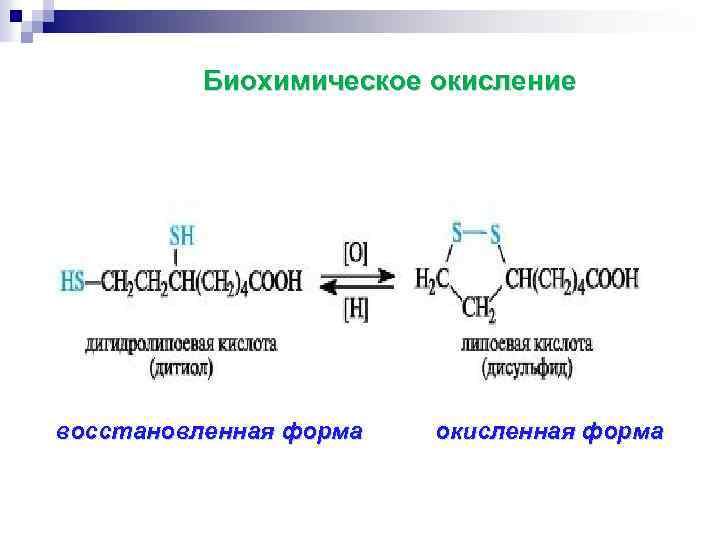 Биохимическое окисление восстановленная форма окисленная форма
Биохимическое окисление восстановленная форма окисленная форма
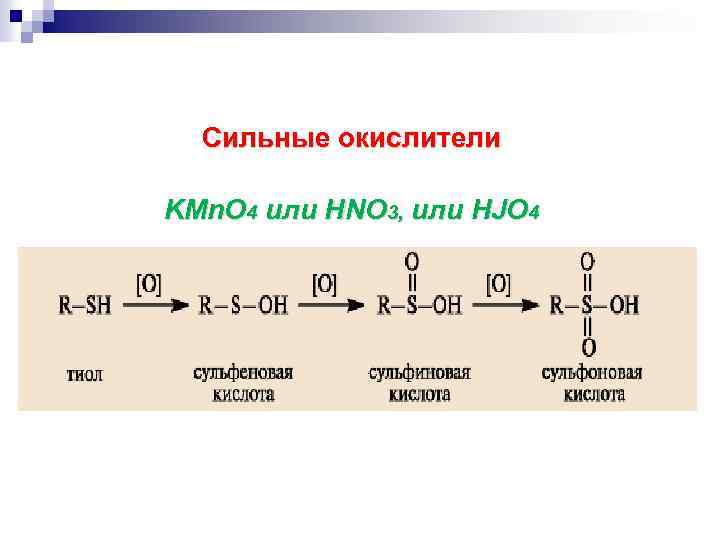 Сильные окислители KMn. O 4 или HNO 3, или HJO 4
Сильные окислители KMn. O 4 или HNO 3, или HJO 4
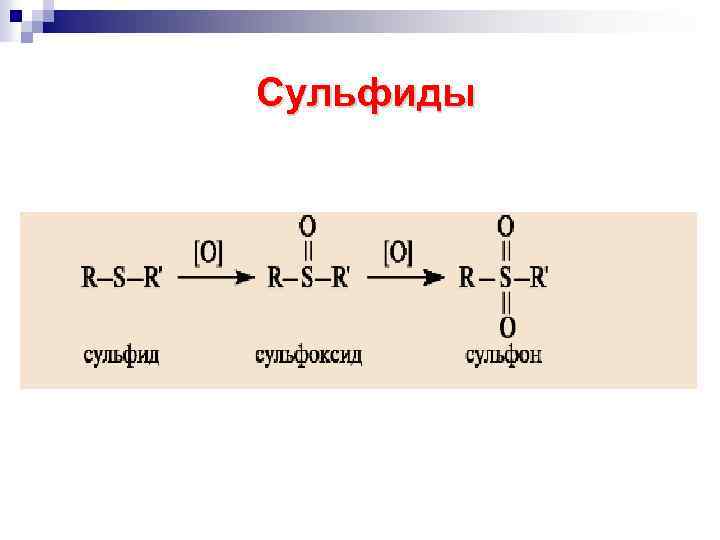 Сульфиды
Сульфиды
 Окисление азотсодержащих соединений Амины легко окисляются.
Окисление азотсодержащих соединений Амины легко окисляются.
 Восстановление органических соединений
Восстановление органических соединений
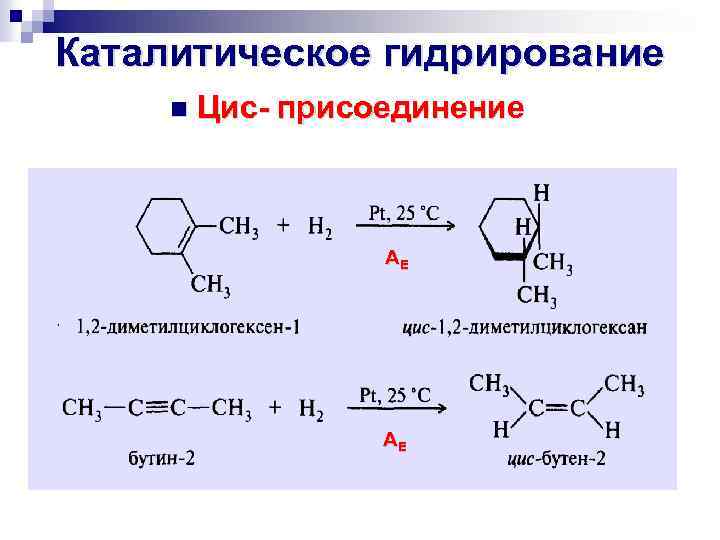 Каталитическое гидрирование n Цис- присоединение АЕ АЕ
Каталитическое гидрирование n Цис- присоединение АЕ АЕ
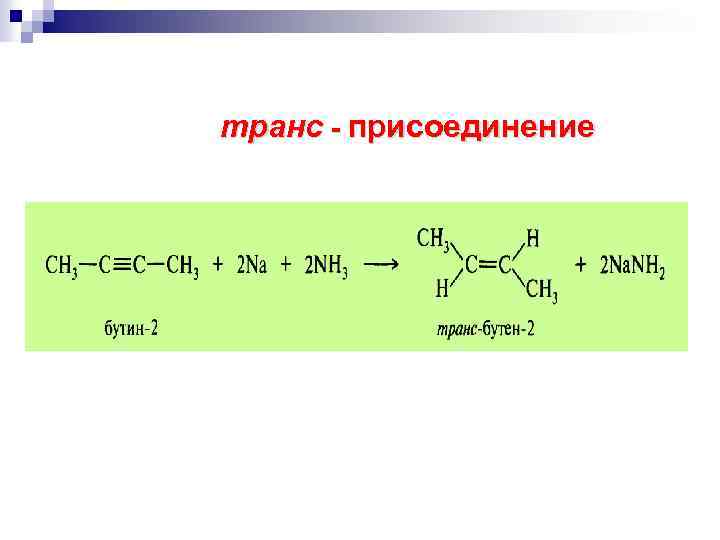 транс - присоединение
транс - присоединение
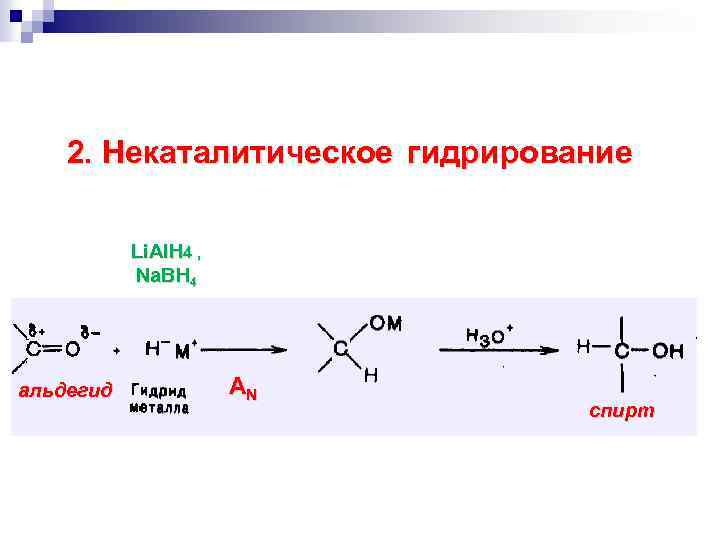 2. Некаталитическое гидрирование Li. Al. H 4 , Na. BH 4 альдегид AN спирт
2. Некаталитическое гидрирование Li. Al. H 4 , Na. BH 4 альдегид AN спирт
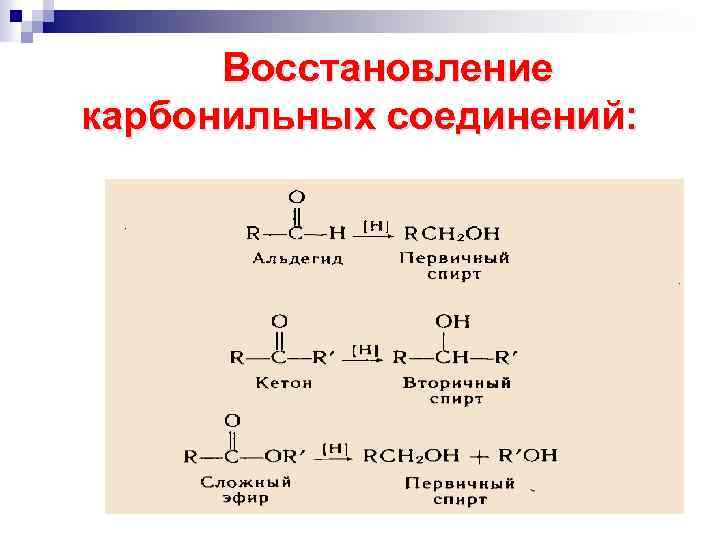 Восстановление карбонильных соединений:
Восстановление карбонильных соединений:
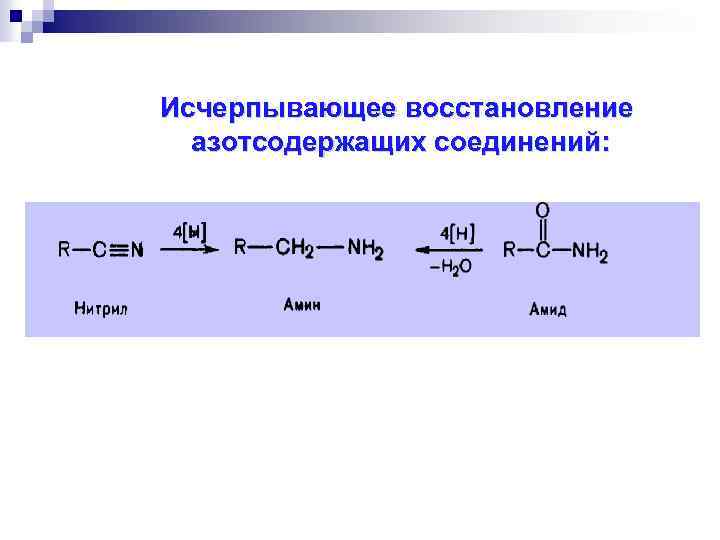 Исчерпывающее восстановление азотсодержащих соединений:
Исчерпывающее восстановление азотсодержащих соединений:
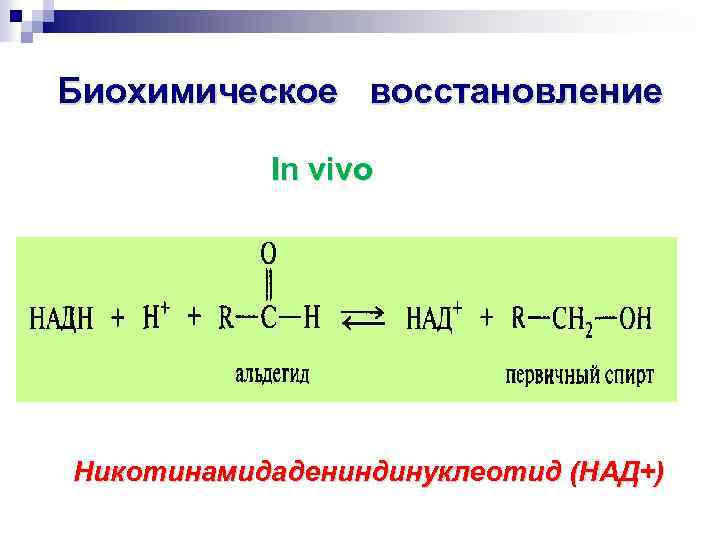 Биохимическое восстановление In vivo Никотинамидадениндинуклеотид (НАД+)
Биохимическое восстановление In vivo Никотинамидадениндинуклеотид (НАД+)
 Никотинамидадениндинуклеотид, НАД n кофермент, присутствующий во всех живых клетках; входит в состав ферментов группы дегидрогеназ n n Открыт в 1904 в дрожжевом соке английскими биохимиками А. Гарденом и У. Йонгом; строение установлено в 1936 г. О. Варбургом и Х. Эйлером.
Никотинамидадениндинуклеотид, НАД n кофермент, присутствующий во всех живых клетках; входит в состав ферментов группы дегидрогеназ n n Открыт в 1904 в дрожжевом соке английскими биохимиками А. Гарденом и У. Йонгом; строение установлено в 1936 г. О. Варбургом и Х. Эйлером.
 ОТТО ГЕНРИХ ВАРБУРГ (1883– 1970), n немецкий биохимик и физиолог, удостоенный в 1931 Нобелевской премии по физиологии и медицине за открытие природы и механизма действия дыхательных ферментов.
ОТТО ГЕНРИХ ВАРБУРГ (1883– 1970), n немецкий биохимик и физиолог, удостоенный в 1931 Нобелевской премии по физиологии и медицине за открытие природы и механизма действия дыхательных ферментов.
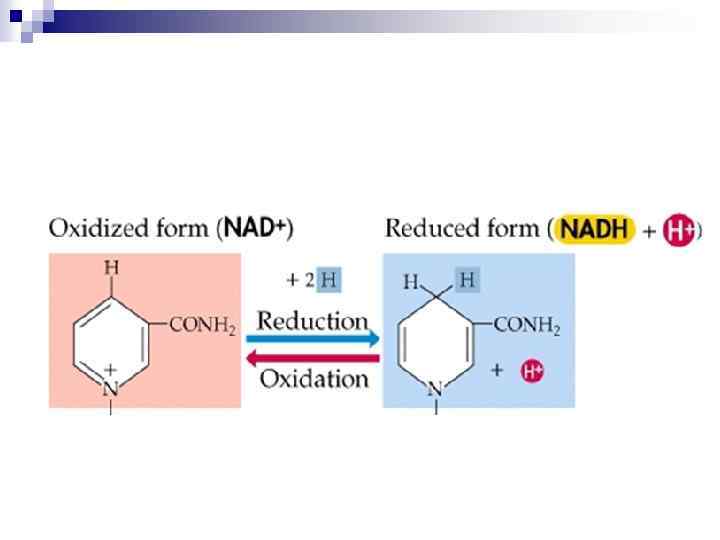
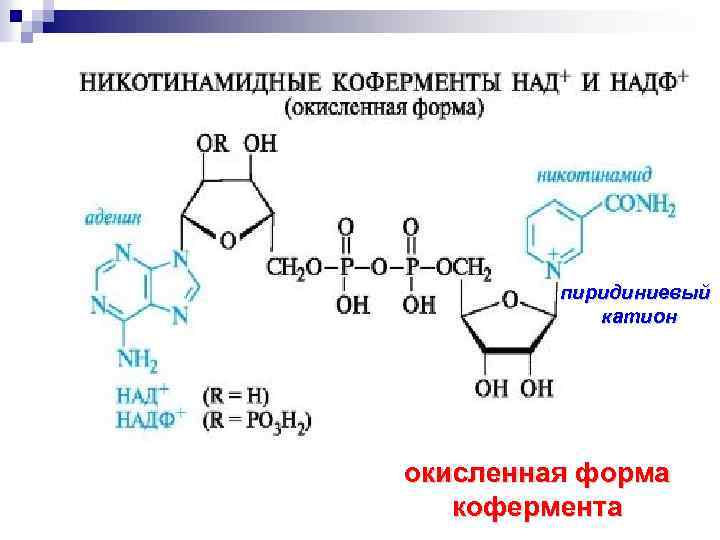 пиридиниевый катион окисленная форма кофермента
пиридиниевый катион окисленная форма кофермента
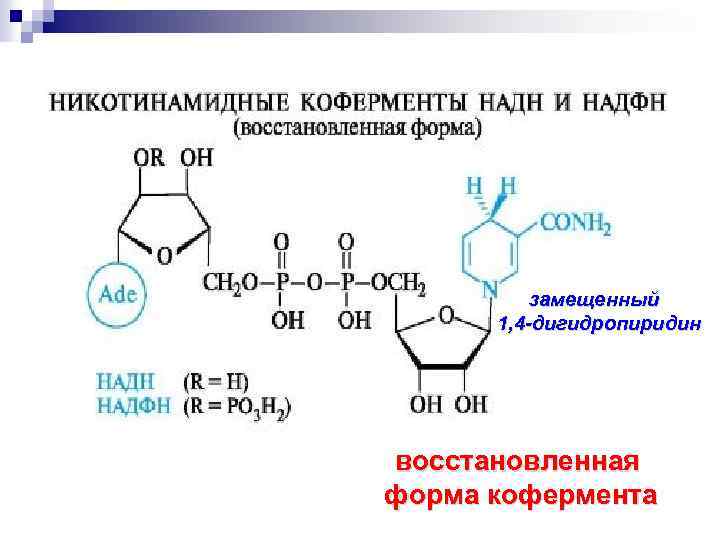 замещенный 1, 4 -дигидропиридин восстановленная форма кофермента
замещенный 1, 4 -дигидропиридин восстановленная форма кофермента
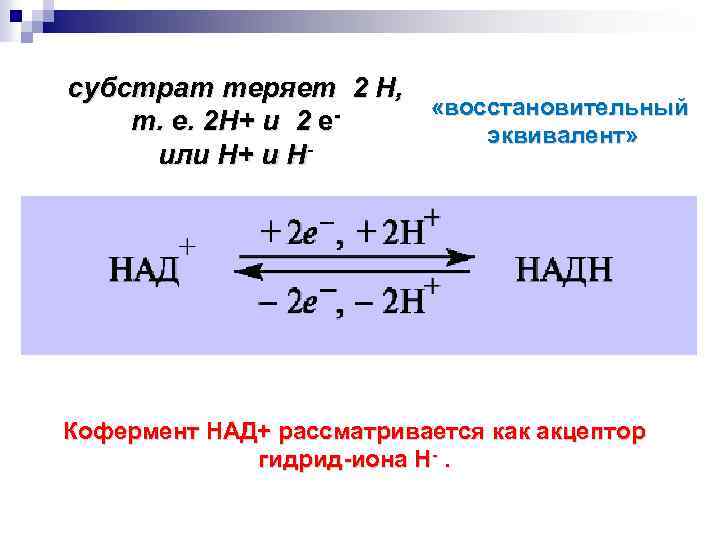 субстрат теряет 2 Н, «восстановительный т. е. 2 Н+ и 2 е эквивалент» или Н+ и Н Кофермент НАД+ рассматривается как акцептор гидрид-иона Н-.
субстрат теряет 2 Н, «восстановительный т. е. 2 Н+ и 2 е эквивалент» или Н+ и Н Кофермент НАД+ рассматривается как акцептор гидрид-иона Н-.
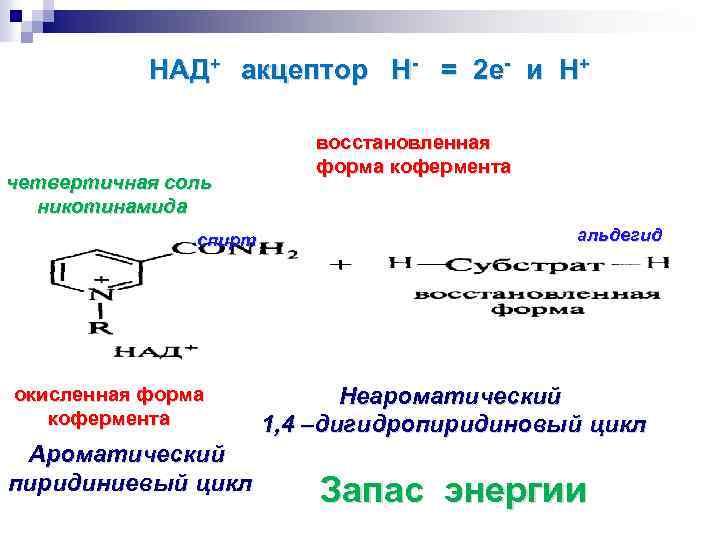 НАД+ акцептор Н- = 2 е- и Н+ четвертичная соль никотинамида спирт окисленная форма кофермента Ароматический пиридиниевый цикл восстановленная форма кофермента альдегид Неароматический 1, 4 –дигидропиридиновый цикл Запас энергии
НАД+ акцептор Н- = 2 е- и Н+ четвертичная соль никотинамида спирт окисленная форма кофермента Ароматический пиридиниевый цикл восстановленная форма кофермента альдегид Неароматический 1, 4 –дигидропиридиновый цикл Запас энергии
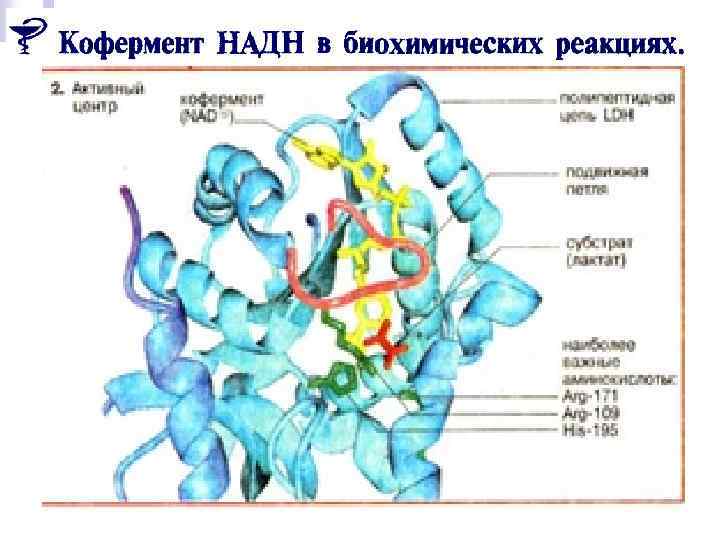
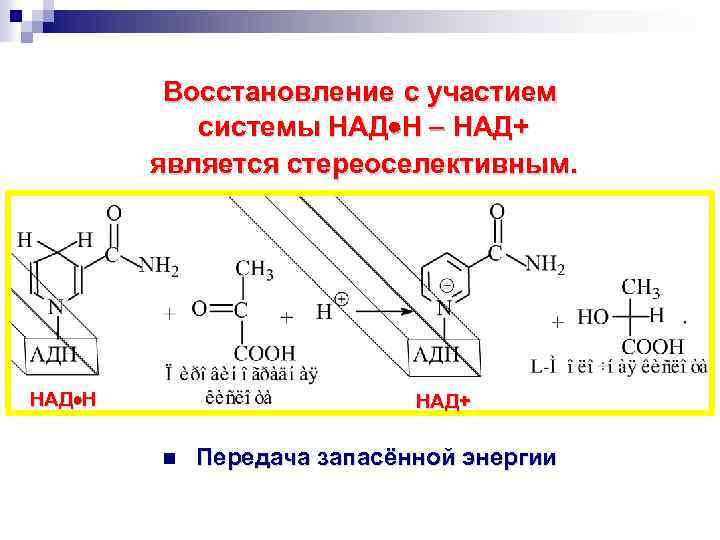 Восстановление с участием системы НАД Н НАД+ является стереоселективным. НАД Н НАД+ n Передача запасённой энергии
Восстановление с участием системы НАД Н НАД+ является стереоселективным. НАД Н НАД+ n Передача запасённой энергии
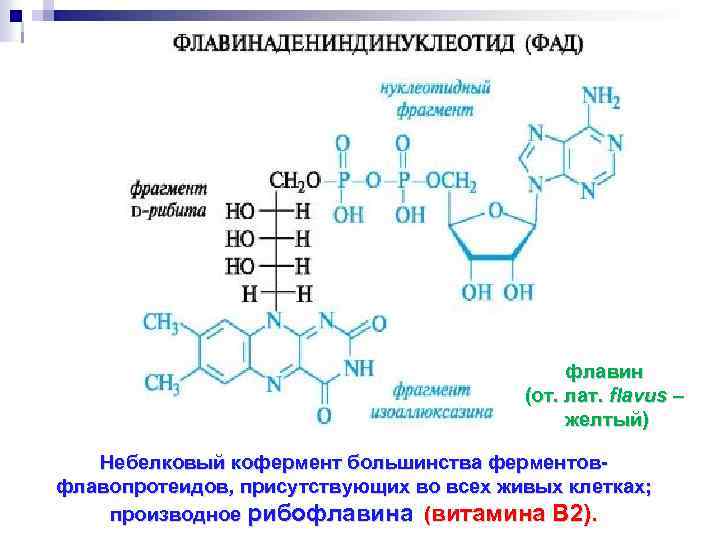 флавин (от. лат. flavus – желтый) Небелковый кофермент большинства ферментовфлавопротеидов, присутствующих во всех живых клетках; производное рибофлавина (витамина В 2).
флавин (от. лат. flavus – желтый) Небелковый кофермент большинства ферментовфлавопротеидов, присутствующих во всех живых клетках; производное рибофлавина (витамина В 2).
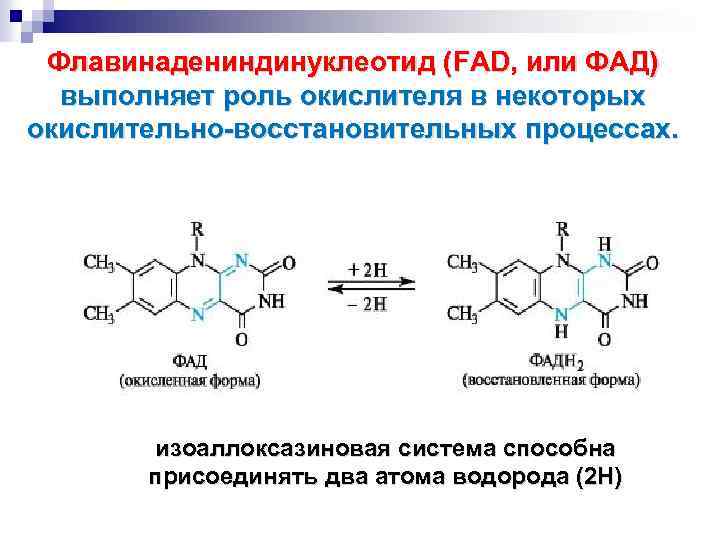 Флавинадениндинуклеотид (FAD, или ФАД) выполняет роль окислителя в некоторых окислительно-восстановительных процессах. изоаллоксазиновая система способна присоединять два атома водорода (2 Н)
Флавинадениндинуклеотид (FAD, или ФАД) выполняет роль окислителя в некоторых окислительно-восстановительных процессах. изоаллоксазиновая система способна присоединять два атома водорода (2 Н)
 Спасибо всем! n Скажи мне – и я забуду, n Покажи мне – и я запомню, n Вовлеки меня – и я научусь! n Китайская мудрость
Спасибо всем! n Скажи мне – и я забуду, n Покажи мне – и я запомню, n Вовлеки меня – и я научусь! n Китайская мудрость

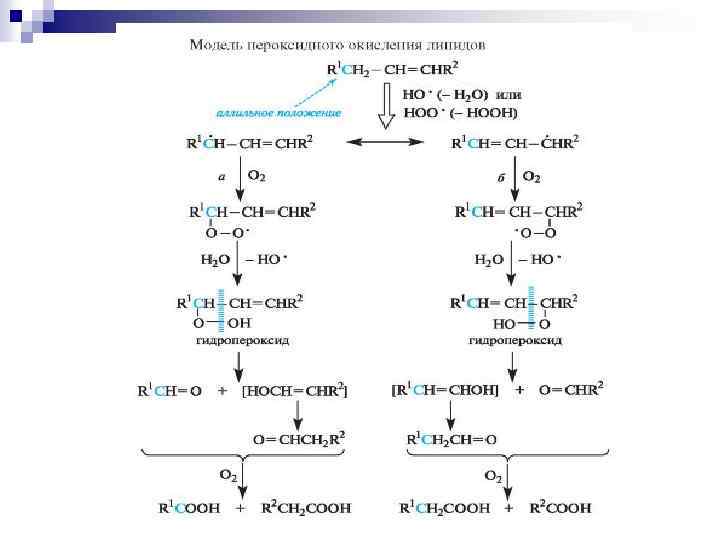
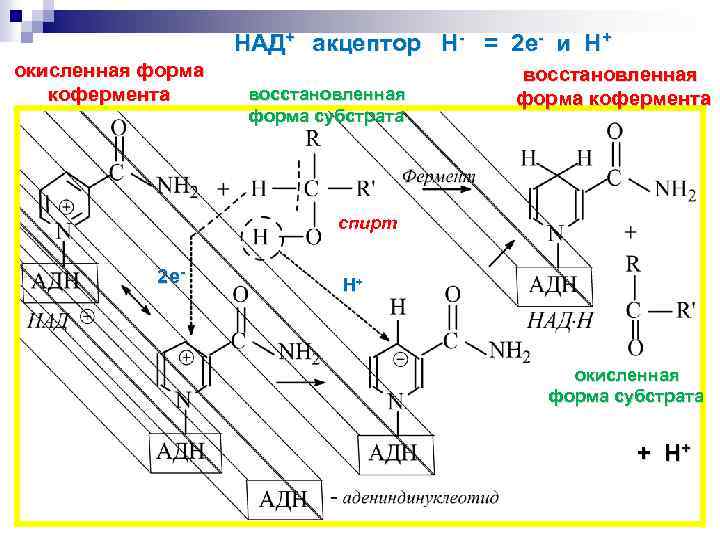 НАД+ акцептор Н- = 2 е- и Н+ окисленная форма кофермента восстановленная форма субстрата восстановленная форма кофермента спирт 2 е- Н+ окисленная форма субстрата + Н+
НАД+ акцептор Н- = 2 е- и Н+ окисленная форма кофермента восстановленная форма субстрата восстановленная форма кофермента спирт 2 е- Н+ окисленная форма субстрата + Н+
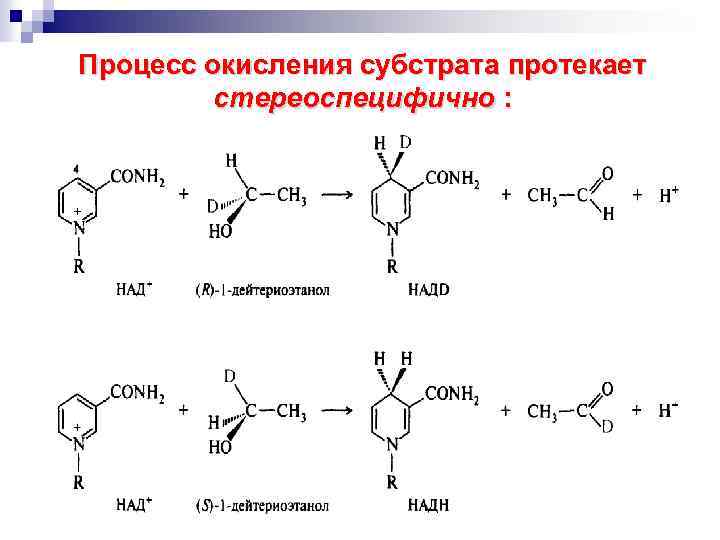 Процесс окисления субстрата протекает стереоспецифично :
Процесс окисления субстрата протекает стереоспецифично :
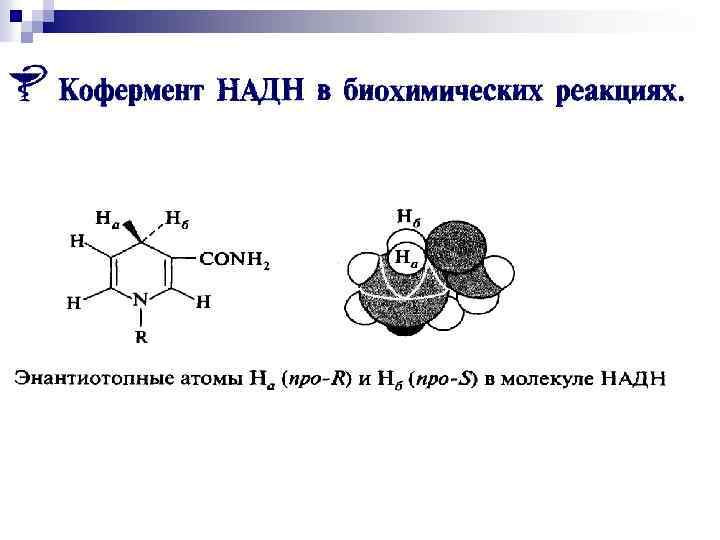
 Флавинадениндинукле д.
Флавинадениндинукле д.
 Ненасыщенные кислоты и липиды с остатками ненасыщенных кислот мягкие условия жесткие условия гликоль
Ненасыщенные кислоты и липиды с остатками ненасыщенных кислот мягкие условия жесткие условия гликоль


