12. Приготовление нанесенных многокомпонентных катализаторов 12.1. Классификация модифицирующих








![Пример: [PtCl6]2 + [ReO4] + Al2O3 → → Pt-Re/-Al2O3 Пример: [PtCl6]2 + [ReO4] + Al2O3 → → Pt-Re/-Al2O3](https://present5.com/presentacii-2/20171208\6538-l_17-spa-sintez_bikomponent_nanesen_kat-rov.ppt\6538-l_17-spa-sintez_bikomponent_nanesen_kat-rov_11.jpg)






6538-l_17-spa-sintez_bikomponent_nanesen_kat-rov.ppt
- Количество слайдов: 23
 12. Приготовление нанесенных многокомпонентных катализаторов 12.1. Классификация модифицирующих добавок 12.2. Способы приготовления нанесенных бикомпонентных катализаторов 12.2.1. Особенности формирования нанесенных катализаторов при совместном нанесении компонентов 12.2.2. Особенности формирования нанесенных катализаторов при раздельном нанесении компонентов Лекция 17
12. Приготовление нанесенных многокомпонентных катализаторов 12.1. Классификация модифицирующих добавок 12.2. Способы приготовления нанесенных бикомпонентных катализаторов 12.2.1. Особенности формирования нанесенных катализаторов при совместном нанесении компонентов 12.2.2. Особенности формирования нанесенных катализаторов при раздельном нанесении компонентов Лекция 17
 Pt (Rh, Ru)/сотовый носитель – очистка выхлопных газов (Pt+M)/Al2O3; M=Re, Ir, Sn – катализатор риформинга и дегидрирования (Co-Mo)S/Al2O3 , (Ni-W)S/SiO2 – катализаторы гидрообессеривания (Co - ThO2 - MgO - SiO2) – синтез Фишера-Тропша { (0.1 - 1% )Pd; (3 - 5%) V2O5 (добавки CuO, Ir, Ru, Pt)}/ Al2O3 – газофазное окисление этилена в ацетальдегид (Cu-Cr-О)/ Al2O3 (+MgO) – катализаторы полного окисления в сжигании топлив (Pt+M)/С; M=W, Cr, Ni – катодный электрокатализатор (активация О2) Pt-Ru/С – анодный электрокатализатор (окисление метанола) Pt-Pd/С – катализаторы гидрирования органических соединений Примеры би- или многокомпонентных нанесенных катализаторов и области их применения
Pt (Rh, Ru)/сотовый носитель – очистка выхлопных газов (Pt+M)/Al2O3; M=Re, Ir, Sn – катализатор риформинга и дегидрирования (Co-Mo)S/Al2O3 , (Ni-W)S/SiO2 – катализаторы гидрообессеривания (Co - ThO2 - MgO - SiO2) – синтез Фишера-Тропша { (0.1 - 1% )Pd; (3 - 5%) V2O5 (добавки CuO, Ir, Ru, Pt)}/ Al2O3 – газофазное окисление этилена в ацетальдегид (Cu-Cr-О)/ Al2O3 (+MgO) – катализаторы полного окисления в сжигании топлив (Pt+M)/С; M=W, Cr, Ni – катодный электрокатализатор (активация О2) Pt-Ru/С – анодный электрокатализатор (окисление метанола) Pt-Pd/С – катализаторы гидрирования органических соединений Примеры би- или многокомпонентных нанесенных катализаторов и области их применения
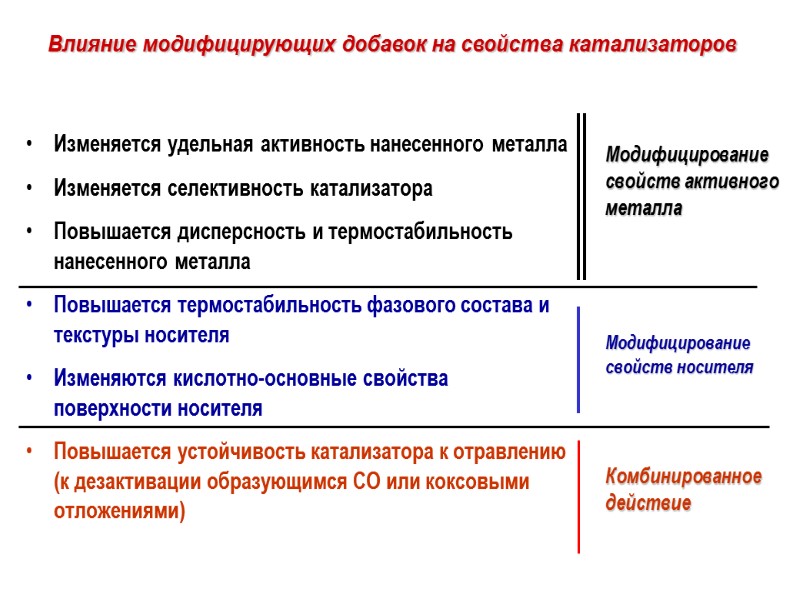
 Изменяется удельная активность нанесенного металла Изменяется селективность катализатора Повышается дисперсность и термостабильность нанесенного металла Повышается термостабильность фазового состава и текстуры носителя Изменяются кислотно-основные свойства поверхности носителя Повышается устойчивость катализатора к отравлению (к дезактивации образующимся СО или коксовыми отложениями) Модифицирование свойств активного металла Модифицирование свойств носителя Комбинированное действие Влияние модифицирующих добавок на свойства катализаторов
Изменяется удельная активность нанесенного металла Изменяется селективность катализатора Повышается дисперсность и термостабильность нанесенного металла Повышается термостабильность фазового состава и текстуры носителя Изменяются кислотно-основные свойства поверхности носителя Повышается устойчивость катализатора к отравлению (к дезактивации образующимся СО или коксовыми отложениями) Модифицирование свойств активного металла Модифицирование свойств носителя Комбинированное действие Влияние модифицирующих добавок на свойства катализаторов
 По каталитической активности: активные в основной реакции или на одной из её стадий, неактивные в основной реакции По способности к восстановлению: легко восстанавливающиеся до металла, не восстанавливающиеся до металлического состояния При этом оксид может оставаться в катализаторе в виде свободной фазы или может взаимодействовать с носителем с образованием различных поверхностных или объемных соединений. По способности к взаимодействию с основным металлом: Не взаимодействующие; Взаимодействующие (химически, с образованием сплавов и т.п.) Различия в способности добавок к восстановлению могут приводить к образованию различных активных компонентов на поверхности восстановленных биэлементных катализаторов 12.1. Классификация модифицирующих добавок
По каталитической активности: активные в основной реакции или на одной из её стадий, неактивные в основной реакции По способности к восстановлению: легко восстанавливающиеся до металла, не восстанавливающиеся до металлического состояния При этом оксид может оставаться в катализаторе в виде свободной фазы или может взаимодействовать с носителем с образованием различных поверхностных или объемных соединений. По способности к взаимодействию с основным металлом: Не взаимодействующие; Взаимодействующие (химически, с образованием сплавов и т.п.) Различия в способности добавок к восстановлению могут приводить к образованию различных активных компонентов на поверхности восстановленных биэлементных катализаторов 12.1. Классификация модифицирующих добавок
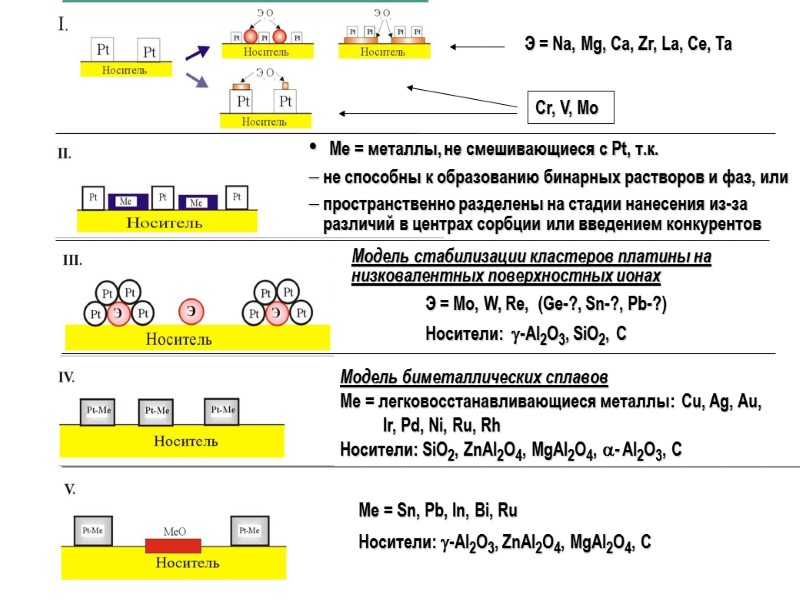
 Э = Na, Mg, Ca, Zr, La, Ce, Ta Cr, V, Mo Me = металлы, не смешивающиеся с Pt, т.к. не способны к образованию бинарных растворов и фаз, или пространственно разделены на стадии нанесения из-за различий в центрах сорбции или введением конкурентов Модель биметаллических сплавов Ме = легковосстанавливающиеся металлы: Cu, Ag, Au, Ir, Pd, Ni, Ru, Rh Носители: SiO2, ZnAl2O4, MgAl2O4, - Al2O3, С Модель стабилизации кластеров платины на низковалентных поверхностных ионах Э = Mo, W, Re, (Ge-?, Sn-?, Pb-?) Носители: -Al2O3, SiO2, C Me = Sn, Pb, In, Bi, Ru Носители: -Al2O3, ZnAl2O4, MgAl2O4, C
Э = Na, Mg, Ca, Zr, La, Ce, Ta Cr, V, Mo Me = металлы, не смешивающиеся с Pt, т.к. не способны к образованию бинарных растворов и фаз, или пространственно разделены на стадии нанесения из-за различий в центрах сорбции или введением конкурентов Модель биметаллических сплавов Ме = легковосстанавливающиеся металлы: Cu, Ag, Au, Ir, Pd, Ni, Ru, Rh Носители: SiO2, ZnAl2O4, MgAl2O4, - Al2O3, С Модель стабилизации кластеров платины на низковалентных поверхностных ионах Э = Mo, W, Re, (Ge-?, Sn-?, Pb-?) Носители: -Al2O3, SiO2, C Me = Sn, Pb, In, Bi, Ru Носители: -Al2O3, ZnAl2O4, MgAl2O4, C
 СПЛАВЫ - макроскопически однородные многокомпонентные системы Среди отдельных фаз сплавов различают: Твердые растворы, в которых атомы или ионы компонентов, смешиваясь в произвольных соотношениях, образуют общую кристаллическую решетку, свойственную для одного из компонентов Интерметаллические соединения, характеризующиеся определенным массовым соотношением между составляющими их элементами и кристаллическими решетками, отличными от решеток образующих их элементов Методы получения: кристаллизация из расплава (основной метод для массивных сплавов); спекание; диффузия легирующего элемента в твердое тело; совместная кристаллизация компонентов из пара; Образование сплавов – наиболее частый случай взаимодействия компонентов при приготовлении многокомпонентных катализаторов
СПЛАВЫ - макроскопически однородные многокомпонентные системы Среди отдельных фаз сплавов различают: Твердые растворы, в которых атомы или ионы компонентов, смешиваясь в произвольных соотношениях, образуют общую кристаллическую решетку, свойственную для одного из компонентов Интерметаллические соединения, характеризующиеся определенным массовым соотношением между составляющими их элементами и кристаллическими решетками, отличными от решеток образующих их элементов Методы получения: кристаллизация из расплава (основной метод для массивных сплавов); спекание; диффузия легирующего элемента в твердое тело; совместная кристаллизация компонентов из пара; Образование сплавов – наиболее частый случай взаимодействия компонентов при приготовлении многокомпонентных катализаторов
 1. Твердые растворы непрерывный ряд (гцк структуры) Pt - Re, Pt - Ir, Pt - Cu, Pt - Pd, Pt - Ni ограниченная растворимость Pt - Sn (8 ат.% Sn) Pt - In (Pt > In) Pt - Au (Pt>Au, Au>Pt) Pt - Zn (Zn < 25 ат.%) 2. Интерметаллические соединения Pt3Sn, Pt3In, Pt3Zn, Pt3Pb - кубическая структура типа Cu3Au PtZn, PtSn, PtPb - гексагональная структура типа CuAu Pt2Sn3 (тип NiAs), PtSn2 (тип CaF2), Pt2In, Pt2In3 Примеры сплавов Pt с модифицирующими добавками
1. Твердые растворы непрерывный ряд (гцк структуры) Pt - Re, Pt - Ir, Pt - Cu, Pt - Pd, Pt - Ni ограниченная растворимость Pt - Sn (8 ат.% Sn) Pt - In (Pt > In) Pt - Au (Pt>Au, Au>Pt) Pt - Zn (Zn < 25 ат.%) 2. Интерметаллические соединения Pt3Sn, Pt3In, Pt3Zn, Pt3Pb - кубическая структура типа Cu3Au PtZn, PtSn, PtPb - гексагональная структура типа CuAu Pt2Sn3 (тип NiAs), PtSn2 (тип CaF2), Pt2In, Pt2In3 Примеры сплавов Pt с модифицирующими добавками
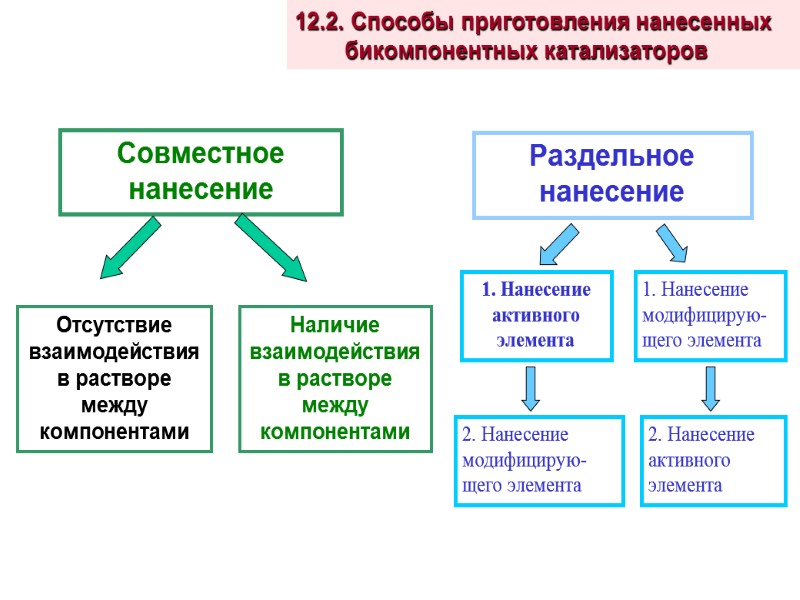
 Совместное нанесение Раздельное нанесение Наличие взаимодействия в растворе между компонентами Отсутствие взаимодействия в растворе между компонентами 1. Нанесение активного элемента 1. Нанесение модифицирую-щего элемента 2. Нанесение модифицирую-щего элемента 2. Нанесение активного элемента 12.2. Способы приготовления нанесенных бикомпонентных катализаторов
Совместное нанесение Раздельное нанесение Наличие взаимодействия в растворе между компонентами Отсутствие взаимодействия в растворе между компонентами 1. Нанесение активного элемента 1. Нанесение модифицирую-щего элемента 2. Нанесение модифицирую-щего элемента 2. Нанесение активного элемента 12.2. Способы приготовления нанесенных бикомпонентных катализаторов
 I) Отсутствие взаимодействия предшественников в растворе 1. Пропитка осаждение в порах носителя при совместной кристаллизации; разделение элементов в пространстве при раздельной кристаллизации; незначительное повышение дисперсности активного компонента по сравнению с монометаллическим катализатором; 2. Сорбция + пропитка а) Ионы одинакового заряда: хемосорбция одного компонента и осаждение в порах второго: система [PdCl4]2 + [BiCl6]3 + C: сильная адсорбция палладия, но отсутствие адсорбции висмута б) Ионы разного заряда: система [PtCl6]2 + RuCl3 + SiO2: отсутствие адсорбции PtCl6]2, но сильная адсорбция [Ru(H2O)6]3+, [RuCl(H2O)5]2+ , [RuCl2(H2O)4]+ система [PtCl6]2 + RuCl3 + Al2O3: сильная адсорбция [PtCl6]2, но отсутствие адсорбции катионов Ru 12.2.1. Особенности формирования нанесенных катализаторов при совместном нанесении компонентов
I) Отсутствие взаимодействия предшественников в растворе 1. Пропитка осаждение в порах носителя при совместной кристаллизации; разделение элементов в пространстве при раздельной кристаллизации; незначительное повышение дисперсности активного компонента по сравнению с монометаллическим катализатором; 2. Сорбция + пропитка а) Ионы одинакового заряда: хемосорбция одного компонента и осаждение в порах второго: система [PdCl4]2 + [BiCl6]3 + C: сильная адсорбция палладия, но отсутствие адсорбции висмута б) Ионы разного заряда: система [PtCl6]2 + RuCl3 + SiO2: отсутствие адсорбции PtCl6]2, но сильная адсорбция [Ru(H2O)6]3+, [RuCl(H2O)5]2+ , [RuCl2(H2O)4]+ система [PtCl6]2 + RuCl3 + Al2O3: сильная адсорбция [PtCl6]2, но отсутствие адсорбции катионов Ru 12.2.1. Особенности формирования нанесенных катализаторов при совместном нанесении компонентов
 3. Совместная сорбция а) Ионы одинакового заряда [PtCl6]2 + [ReO4] + Al2O3 [Pt(NH3)4]2+ + [Ru(NH3)6]3+ + SiO2 Результат конкурентная сорбция: уменьшение величины сорбции каждого из компонентов; сорбция слабосорбирующегося компонента уменьшается в большей степени; закрепление предшественников на различных участках поверхности б) Ионы разного заряда сложное взаимное влияние в случае одновременного закрепления анионов (([PtCl6]2 ) и катионов (Cu2+, Ni2+, In3+, Cr3+) по различным механизмам на MgAl2O4, ZnAl2O4, -Al2O3, C Результат - закрепление предшественников на различных участках поверхности соосаждение в виде сложных комплексных солей
3. Совместная сорбция а) Ионы одинакового заряда [PtCl6]2 + [ReO4] + Al2O3 [Pt(NH3)4]2+ + [Ru(NH3)6]3+ + SiO2 Результат конкурентная сорбция: уменьшение величины сорбции каждого из компонентов; сорбция слабосорбирующегося компонента уменьшается в большей степени; закрепление предшественников на различных участках поверхности б) Ионы разного заряда сложное взаимное влияние в случае одновременного закрепления анионов (([PtCl6]2 ) и катионов (Cu2+, Ni2+, In3+, Cr3+) по различным механизмам на MgAl2O4, ZnAl2O4, -Al2O3, C Результат - закрепление предшественников на различных участках поверхности соосаждение в виде сложных комплексных солей
![>Пример: [PtCl6]2 + [ReO4] + Al2O3 → → Pt-Re/-Al2O3 >Пример: [PtCl6]2 + [ReO4] + Al2O3 → → Pt-Re/-Al2O3](https://present5.com/presentacii-2/20171208\6538-l_17-spa-sintez_bikomponent_nanesen_kat-rov.ppt\6538-l_17-spa-sintez_bikomponent_nanesen_kat-rov_11.jpg) Пример: [PtCl6]2 + [ReO4] + Al2O3 → → Pt-Re/-Al2O3 (совместная сорбция ионов одинакового заряда) Кинетические кривые сорбции H2PtCl6 (1,2) и HReO4 (3,4) на -Al2O3 из одно-компонентных (1,3) и бинарных (2,4) водных растворов. Расчетное содержание Pt и Re 0,6 мас.% Концентрационные профили распределения ме-таллов по радиальному сечению гранул носителя в Pt-Re катализаторах, приготовленных совместной сорбцией H2PtCl6 и HReO4 а - без конкурента; б - в смеси с 0.3М CH3COOH; в - в смеси с 0.3М HCl; г - -Al2O3 обработан 0.3М HCl
Пример: [PtCl6]2 + [ReO4] + Al2O3 → → Pt-Re/-Al2O3 (совместная сорбция ионов одинакового заряда) Кинетические кривые сорбции H2PtCl6 (1,2) и HReO4 (3,4) на -Al2O3 из одно-компонентных (1,3) и бинарных (2,4) водных растворов. Расчетное содержание Pt и Re 0,6 мас.% Концентрационные профили распределения ме-таллов по радиальному сечению гранул носителя в Pt-Re катализаторах, приготовленных совместной сорбцией H2PtCl6 и HReO4 а - без конкурента; б - в смеси с 0.3М CH3COOH; в - в смеси с 0.3М HCl; г - -Al2O3 обработан 0.3М HCl
 II) Нанесение из биметаллических предшественников Гетероядерные ацетаты металлов PdCu(OAc)4 (необратимо адсорбируется из C2H5OH на Al2O3) Гетерополиядерные карбонильные кластеры Fe2Pt(CO)12, [Fe4Pt(CO)16]2, [Fe3Pt3(CO)15]2 IrPt(CO)12(PPh3) Mn2Pt(CO)12 [Rh4Pt(CO)12]2, Pt2Ru(CO)18 Kомплексы (Pt-SnCl3, Pd-SnCl3, Ir-SnCl3, Ru-SnCl3) PtCl3SnCl3]2 - Pt-Sn1 [PtCl2(SnCl3)2]2 - Pt-Sn2 [Pt(SnCl3)5]3 - Pt-Sn5 [Pt3(0)Sn8Cl20]4 - Pt3-Sn8
II) Нанесение из биметаллических предшественников Гетероядерные ацетаты металлов PdCu(OAc)4 (необратимо адсорбируется из C2H5OH на Al2O3) Гетерополиядерные карбонильные кластеры Fe2Pt(CO)12, [Fe4Pt(CO)16]2, [Fe3Pt3(CO)15]2 IrPt(CO)12(PPh3) Mn2Pt(CO)12 [Rh4Pt(CO)12]2, Pt2Ru(CO)18 Kомплексы (Pt-SnCl3, Pd-SnCl3, Ir-SnCl3, Ru-SnCl3) PtCl3SnCl3]2 - Pt-Sn1 [PtCl2(SnCl3)2]2 - Pt-Sn2 [Pt(SnCl3)5]3 - Pt-Sn5 [Pt3(0)Sn8Cl20]4 - Pt3-Sn8
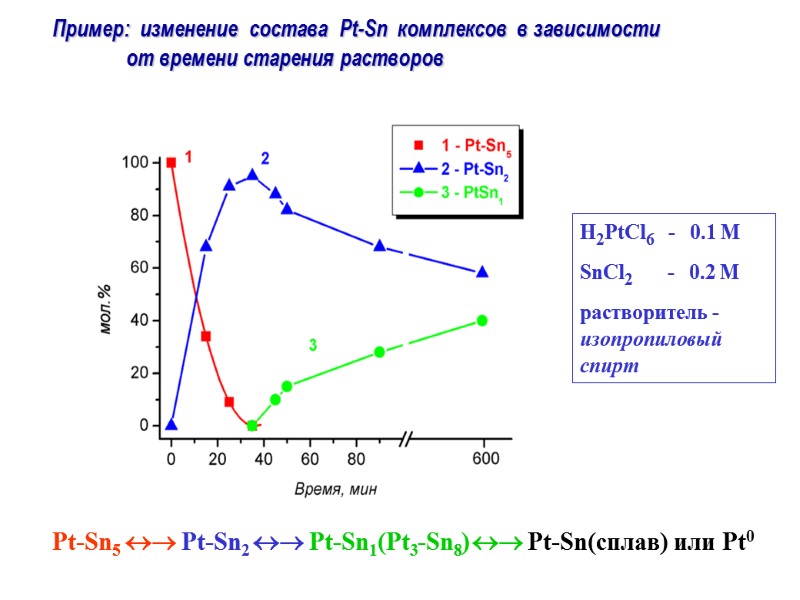
 Pt-Sn5 Pt-Sn2 Pt-Sn1(Pt3-Sn8) Pt-Sn(сплав) или Pt0 H2PtCl6 - 0.1 M SnCl2 - 0.2 М растворитель - изопропиловый спирт Пример: изменение состава Pt-Sn комплексов в зависимости от времени старения растворов
Pt-Sn5 Pt-Sn2 Pt-Sn1(Pt3-Sn8) Pt-Sn(сплав) или Pt0 H2PtCl6 - 0.1 M SnCl2 - 0.2 М растворитель - изопропиловый спирт Пример: изменение состава Pt-Sn комплексов в зависимости от времени старения растворов
 Полиметаллические золи Совместное восстановление солей металлов сильным восстановителем в присутствии ПАВ с последующим нанесением золя на носитель. Дисперсность регулируется: концентрацией реагентов и природой ПАВ, технологическими приёмами (например, созданием микроэмульсий) Смешанные полиядерные гидроксокомплексы Совместный гидролиз растворов хлоридов Pd и Pt или Pt и Ru, сопровождающийся адсорбцией ПГК (PtPd/C, PtRu/C) Смешанные соли металлов с органическими поликислотами Использование Co2[Mo4Cit2O11] xH2O для синтеза Co-Mo-S/-Al2O3 (достигнуто минимальное взаимодействие Со с носителем и максимально смешаны ионы Со и Мо). Метод Пекини Двойные комплексные соли (может осложняться раздельной сорбцией составляющих соль ионов)
Полиметаллические золи Совместное восстановление солей металлов сильным восстановителем в присутствии ПАВ с последующим нанесением золя на носитель. Дисперсность регулируется: концентрацией реагентов и природой ПАВ, технологическими приёмами (например, созданием микроэмульсий) Смешанные полиядерные гидроксокомплексы Совместный гидролиз растворов хлоридов Pd и Pt или Pt и Ru, сопровождающийся адсорбцией ПГК (PtPd/C, PtRu/C) Смешанные соли металлов с органическими поликислотами Использование Co2[Mo4Cit2O11] xH2O для синтеза Co-Mo-S/-Al2O3 (достигнуто минимальное взаимодействие Со с носителем и максимально смешаны ионы Со и Мо). Метод Пекини Двойные комплексные соли (может осложняться раздельной сорбцией составляющих соль ионов)
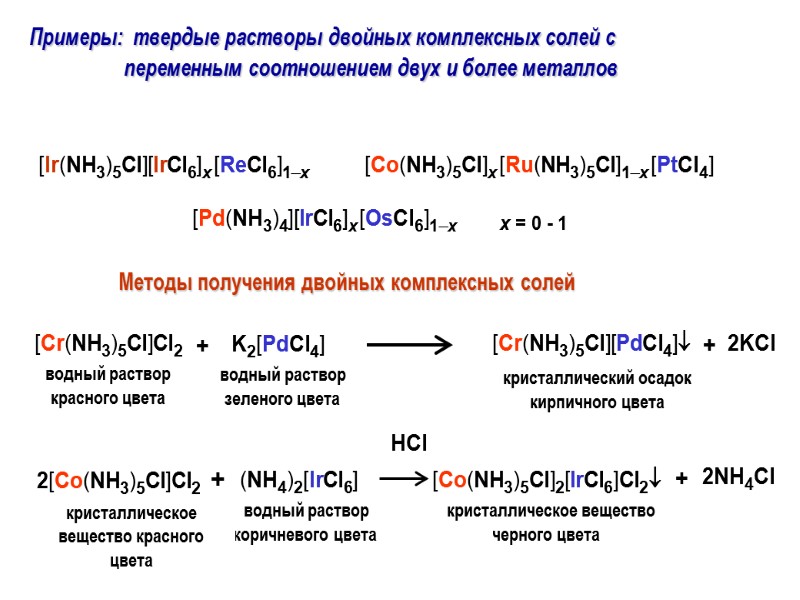
 Примеры: твердые растворы двойных комплексных солей с переменным соотношением двух и более металлов
Примеры: твердые растворы двойных комплексных солей с переменным соотношением двух и более металлов
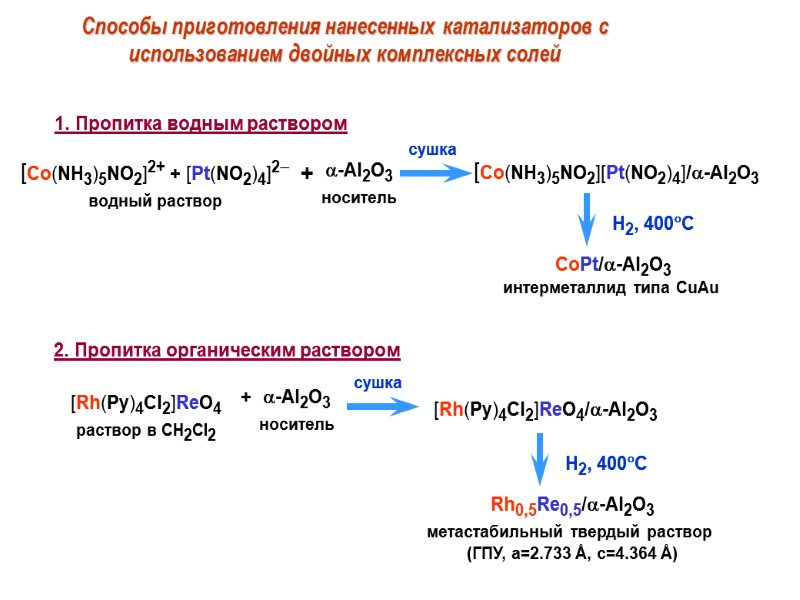
 Способы приготовления нанесенных катализаторов с использованием двойных комплексных солей 2. Пропитка органическим раствором Rh0,5Re0,5/-Al2O3 метастабильный твердый раствор (ГПУ, a=2.733 Å, c=4.364 Å) H2, 400С
Способы приготовления нанесенных катализаторов с использованием двойных комплексных солей 2. Пропитка органическим раствором Rh0,5Re0,5/-Al2O3 метастабильный твердый раствор (ГПУ, a=2.733 Å, c=4.364 Å) H2, 400С
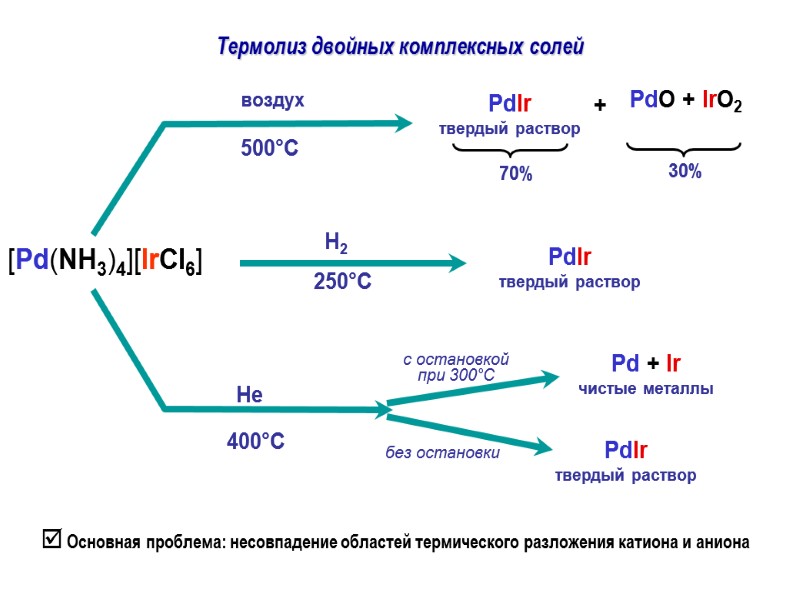
 Термолиз двойных комплексных солей Основная проблема: несовпадение областей термического разложения катиона и аниона
Термолиз двойных комплексных солей Основная проблема: несовпадение областей термического разложения катиона и аниона
 1-я стадия – нанесение модифицирующего элемента Синтез с использованием металлоорганических соединений а) закрепление соединения модифицирующего элемента ( S–OH)m + ЭRn → ( S–O)mЭRnm + HRm (S – поверхность Al2O3, SiO2; Э Mo, W, Re, Sn; R 3-C3H5, OC2H5, OAc) б) восстановление (S–O)mЭRnm + H2 → ( S–O)mЭn+ + nHRm в) закрепление Pt, Pd, Ni… на низковалентных ионах (S–O)m– Эn+ + Pt(-C3H5)2 (S–O)m– Эn+ --- Pt(-C3H5)2 (S–O)m–Э----Pt0 Нанесение из неорганических соединений а) сорбция (или пропитка) соединения добавки б) прокалка или восстановление в) сорбция соединения основного металла г) прокалка или восстановление для получения конечного катализатора 12.2.2. Особенности формирования нанесенных катализаторов при раздельном нанесении компонентов
1-я стадия – нанесение модифицирующего элемента Синтез с использованием металлоорганических соединений а) закрепление соединения модифицирующего элемента ( S–OH)m + ЭRn → ( S–O)mЭRnm + HRm (S – поверхность Al2O3, SiO2; Э Mo, W, Re, Sn; R 3-C3H5, OC2H5, OAc) б) восстановление (S–O)mЭRnm + H2 → ( S–O)mЭn+ + nHRm в) закрепление Pt, Pd, Ni… на низковалентных ионах (S–O)m– Эn+ + Pt(-C3H5)2 (S–O)m– Эn+ --- Pt(-C3H5)2 (S–O)m–Э----Pt0 Нанесение из неорганических соединений а) сорбция (или пропитка) соединения добавки б) прокалка или восстановление в) сорбция соединения основного металла г) прокалка или восстановление для получения конечного катализатора 12.2.2. Особенности формирования нанесенных катализаторов при раздельном нанесении компонентов
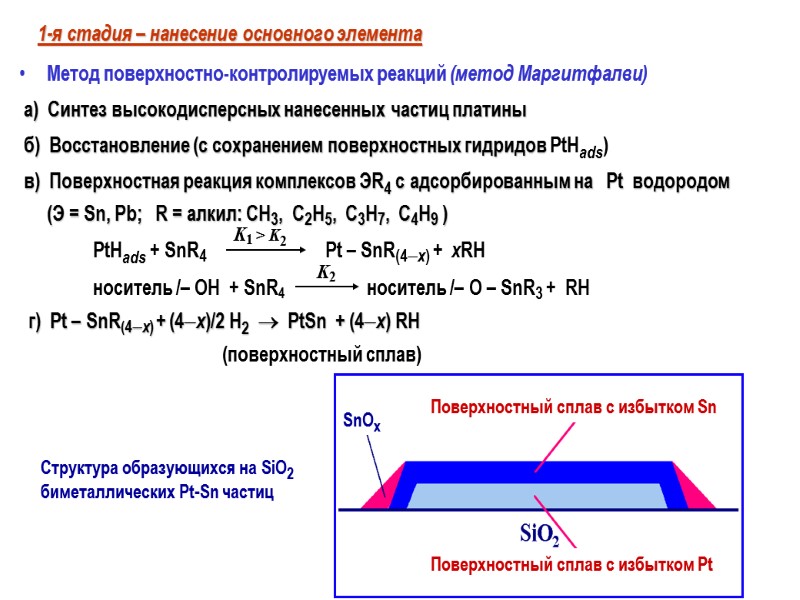
 1-я стадия – нанесение основного элемента Метод поверхностно-контролируемых реакций (метод Маргитфалви) а) Синтез высокодисперсных нанесенных частиц платины б) Восстановление (с сохранением поверхностных гидридов PtHads) в) Поверхностная реакция комплексов ЭR4 c адсорбированным на Pt водородом (Э = Sn, Pb; R = алкил: CH3, C2H5, C3H7, C4H9 ) PtHads + SnR4 Pt – SnR(4x) + xRH носитель /– OH + SnR4 носитель /– O – SnR3 + RH г) Pt – SnR(4x) + (4x)/2 H2 PtSn + (4x) RH (поверхностный сплав) K1 > K2 K2 Структура образующихся на SiO2 биметаллических Pt-Sn частиц
1-я стадия – нанесение основного элемента Метод поверхностно-контролируемых реакций (метод Маргитфалви) а) Синтез высокодисперсных нанесенных частиц платины б) Восстановление (с сохранением поверхностных гидридов PtHads) в) Поверхностная реакция комплексов ЭR4 c адсорбированным на Pt водородом (Э = Sn, Pb; R = алкил: CH3, C2H5, C3H7, C4H9 ) PtHads + SnR4 Pt – SnR(4x) + xRH носитель /– OH + SnR4 носитель /– O – SnR3 + RH г) Pt – SnR(4x) + (4x)/2 H2 PtSn + (4x) RH (поверхностный сплав) K1 > K2 K2 Структура образующихся на SiO2 биметаллических Pt-Sn частиц
 Метод Стыценко – Розовского (блокировка поверхностных дефектов, ответственных за осуществление побочных реакций, путём гидрогенолиза SnR4 на дефектных участках поверхности - активных центрах гидрогенолиза углеводородов) Ni + 2H2 + SnR4 NiSn + 4HR
Метод Стыценко – Розовского (блокировка поверхностных дефектов, ответственных за осуществление побочных реакций, путём гидрогенолиза SnR4 на дефектных участках поверхности - активных центрах гидрогенолиза углеводородов) Ni + 2H2 + SnR4 NiSn + 4HR
 Условия приготовления и эксплуатации катализатора: - условия и последовательность нанесения компонентов - концентрация и соотношение наносимых компонентов - природа используемого носителя, соединений элемента и модифицирующей добавки; - среда предварительной обработки и условия активации; - состав реакционной среды и условия проведения каталитических экспериментов. Физико-химические свойства тройной системы носитель – предшественник активного металла – соединение добавки - определяющим звеном в процессе формирования нанесенных сплавов и их предшественников является протекание двух параллельных процессов: взаимодействие наносимых компонентов с носителем и между собой на различных этапах приготовления катализаторов Факторы, определяющие формирование нанесенного сплава заданного состава и структуры
Условия приготовления и эксплуатации катализатора: - условия и последовательность нанесения компонентов - концентрация и соотношение наносимых компонентов - природа используемого носителя, соединений элемента и модифицирующей добавки; - среда предварительной обработки и условия активации; - состав реакционной среды и условия проведения каталитических экспериментов. Физико-химические свойства тройной системы носитель – предшественник активного металла – соединение добавки - определяющим звеном в процессе формирования нанесенных сплавов и их предшественников является протекание двух параллельных процессов: взаимодействие наносимых компонентов с носителем и между собой на различных этапах приготовления катализаторов Факторы, определяющие формирование нанесенного сплава заданного состава и структуры

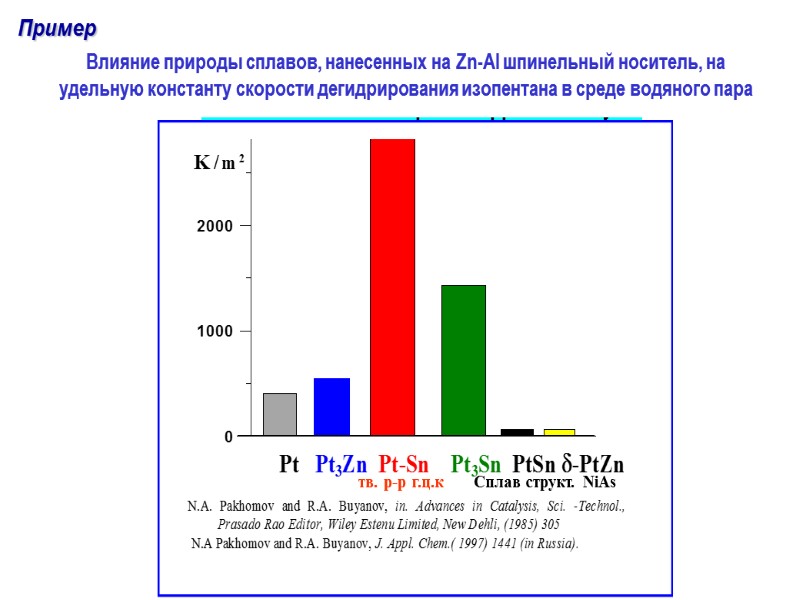
 Влияние природы сплавов, нанесенных на Zn-Al шпинельный носитель, на удельную константу скорости дегидрирования изопентана в среде водяного пара Пример
Влияние природы сплавов, нанесенных на Zn-Al шпинельный носитель, на удельную константу скорости дегидрирования изопентана в среде водяного пара Пример

