биофизика 10.ppt
- Количество слайдов: 13

12 ЛЕКЦИЯ ПРЕДМЕТ - БИОФИЗИКА Лучевая терапия 1. 2. 3. 4. Получение изображений с помощью радиоизотопов; Аппаратура для радионуклидной диагностики; Способы облучения и источники излучения, используемые в лучевой терапии; Способы повышения эффективности лучевой терапии.

Получение изображений с помощью радиоизотопов В ядерной медицине наиболее распространённым методом клинической диагностики является статическая изотопная визуализация в плоскости, называемая планарной сцинтиграфией. n Планарные сцинтиграммы - двумерные распределения (проекции) трёхмерного распределения активности изотопов, находящихся в поле зрения детектора. В отличие от рентгенографии, в которой точно известно начальное и конечное положения каждого рентгеновского луча, при визуализации радиоизотопного источника можно определить положение лишь регистрируемого γ -излучения. Временные изменения пространственного распределения РФП можно регистрировать, регистрируя многократные изображения за промежутки времени от нескольких миллисекунд до сотен секунд. Этот способ визуализации называемый динамической сцинтиграфией и является основным при исследованиях внутренних органов и систем организма. n На планарных сцинтиграммах во многих случаях трудно точно определить функциональные изменения в тканях, расположенных в глубине тела, однако томографические исследования с применением системы многоракурсного сбора информации об объекте позволяют преодолеть большинство проблем, связанных с наложением информации при одноракурсном способе сбора данных. Метод эмиссионной компьютерной томографии (ЭКТ) имеет ряд аналогий с рентгеновской компьютерной томографией (РКТ); однако существуют и отличия: 1. РКТ основана на определении степени ослабления излучения тканями организма, тогда как при ЭКТ требуется коррекция ослабления гамма-излучения для регистрации распределения радиоактивности внутри тела; 2. ограниченность скорости счёта при радиоизотопных исследованиях ведёт к ухудшению качества изображения по сравнению с изображением в рентгеновской компьютерной томографии.

В последние годы в медицине нашла применение однофотонная эмиссионная компьютерная томография (ОФЭКТ или SPECT) – метод полипозиционной регистрации сцинтиграфического изображения, более информативный по сравнению с традиционной планарной сцинтиграфией. Современное программное обеспечение радиодиагностических приборов позволяет рассчитывать объем исследуемого объекта (например, селезенки) на основе трехмерной реконструкции сцинтиграфических изображений, полученных в режиме SPECT. Гамма-камера. n Изображения планарной, динамической сцинтиграфии и ОФЕКТ получают на гамма-камерах. n Гамма-камеры предназначены для визуализации и исследования метаболизма РФП во внутренних органах и физиологических системах организма пациента с целью ранней диагностики онкологических, сердечно-сосудистых и других заболеваний человека. n Помимо диагностических исследований щитовидной железы, почек, печени и желчного пузыря, головного мозга, легких, сердца и др. , современные гаммакамеры обеспечивают сканирование всего тела пациента (скелета) и компьютерную томографию внутренних органов для получения трехмерной информации о распределении в тканях РФП. n Функционально гамма-камера представляет собой совокупность четырех основных блоков: коллиматора, позиционно-чувствительного детектора гаммаквантов, электронной системы формирования координатных сигналов и блока вывода и регистрации изображения. Все указанный компоненты заключены в свинцовый экран достаточной толщины, чтобы свести к минимуму фон от источников радиации, находящихся вне поля зрения камеры. n

Позиционно-чувствительный детектор (ПЧД) – блок гамма-камеры определяющий качество получаемого изображения. Основные требования предъявляемые ПЧД: эффективность регистрации детектора и площадь чувствительной поверхности детектора. n Эффективность регистрации детектора - отношение числа гамма-квантов поглощенных в рабочем объеме детектора к числу гамма-квантов попавших на его чувствительную поверхность. Основные метрологические характеристики гамма-камеры: 1. чувствительность; 2. пространственное разрешение; 3. энергетическое разрешение; 4. характеристика скорости счета; 5. однородность и линейность изображения. n Все характеристики гамма-камеры подразделяются на системные (детектор с коллиматором) и собственные (детектор без коллиматора). Системные характеристики: n Чувствительность – отношение наблюдаемой скорости счета к активности плоского источника, расположенного перпендикулярно оси коллиматора (с1*Бк-1). Зависит от: типа коллиматора, ширины окна анализатора, расстояния между источником и коллиматором и собственных характеристик камеры. n Пространственное разрешение – наименьшее расстояние между двумя параллельными линейными источниками, при котором на изображении они воспринимаются раздельно.

Характеристика скорости счета – измеряется с помощью цилиндрического фантома, заполненного РФП имеющего калибровочную активность. Зависимость наблюдаемой скорости счета от истинной скорости счета. n Контрастность изображения – зависит от проницаемости радиационной защиты и септы коллиматора, интенсивности и энергетического спектра рассеянного излучения. Собственные характеристики: n Пространственное разрешение – точечный коллимированный источник помещают на входное окно сцинтилляционного кристалла. Пространственное разрешение определяется как ширина амплитудного распределения координатного сигнала гамма-камеры на половине максимальной высоты. n Энергетическое разрешение – измеряется с помощью точечного коллимированного источника, помещенного на входное окно сцинтилляционного кристалла. Отношение ширины пика на половине максимального значения амплитудного распределения энергетического спектра на выходе детектора камеры к положению фотопика в процентах. n Неоднородность и нелинейность изображения – искажения изображения присущие сцинтилляционным камерам из-за образования кусочнонепрерывного фотокатода на поверхности непрерывного кристалла. n Геометрические искажения изображения – абсолютное максимальное отклонение изображения щели фантома от прямой линии. n Характеристика скорости счета – облучают детектор гамма-камеры точечным источником, отнесенным на расстояние 1, 5 м от чувствительной поверхности детектора. Интенсивность гамма-излучения измеряют с помощью набора медных пластин различной толщины с известным коэффициентом ослабления. n

Коллиматор. Всего применяют 4 типа коллиматоров: параллельный, пинхольный, коллиматор со сходящимися каналами (сходящийся) и коллиматор с расходящимися каналами (расходящийся). Пинхольный коллиматор – представляет собой свинцовую (или из другого тяжелого элемента) конусообразную полую конструкцию с небольшим отверстием на конце конуса, на расстоянии примерно (20 - 25)см от детектора. Размер отверстия можно менять специальными вставками диаметром приблизительно в несколько сантиметров. Изображение получается перевернутым и увеличенным. Такой коллиматор используют обычно для регистрации малых объектов. Пусть b - расстояние от отверстия до источника, f - расстояние от отверстия до детектора, I - размер изображения, O – размер источника, тогда справедливо следующие соотношение: I/O=f/b Также существует пинхольный коллиматор со множеством (обычно 7) отверстий. Его используют в компьютерной томографии малых органов. Расходящийся коллиматор – представляет собой свинцовую плоскую конструкцию со множеством отверстий которые сходятся в точке за коллиматором (и за детектором) на расстоянии 40 – 50 см от поверхности детектора. Изображение получается уменьшенное и неперевернутое. Справедливо следующее соотношение: I / О = (f – t)/(f + b), где t – толщина коллиматора. Сходящийся коллиматор - представляет собой свинцовую плоскую конструкцию со множеством отверстий которые сходятся в точке перед коллиматором (в сторону источника) на расстоянии 40 – 50 см от поверхности детектора. Изображение получается увеличенное и неперевернутое. Справедливо следующее соотношение: I / О = (f + t)/(f + t - b), где t – толщина коллиматора.
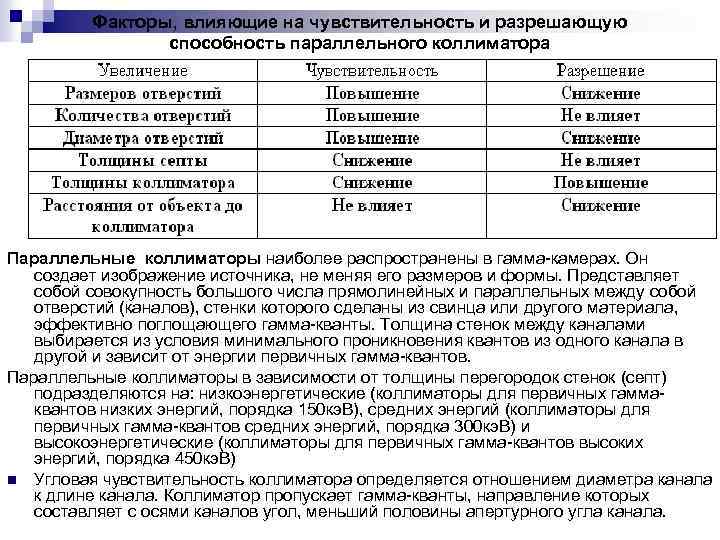
Факторы, влияющие на чувствительность и разрешающую способность параллельного коллиматора Параллельные коллиматоры наиболее распространены в гамма-камерах. Он создает изображение источника, не меняя его размеров и формы. Представляет собой совокупность большого числа прямолинейных и параллельных между собой отверстий (каналов), стенки которого сделаны из свинца или другого материала, эффективно поглощающего гамма-кванты. Толщина стенок между каналами выбирается из условия минимального проникновения квантов из одного канала в другой и зависит от энергии первичных гамма-квантов. Параллельные коллиматоры в зависимости от толщины перегородок стенок (септ) подразделяются на: низкоэнергетические (коллиматоры для первичных гаммаквантов низких энергий, порядка 150 кэ. В), средних энергий (коллиматоры для первичных гамма-квантов средних энергий, порядка 300 кэ. В) и высокоэнергетические (коллиматоры для первичных гамма-квантов высоких энергий, порядка 450 кэ. В) n Угловая чувствительность коллиматора определяется отношением диаметра канала к длине канала. Коллиматор пропускает гамма-кванты, направление которых составляет с осями каналов угол, меньший половины апертурного угла канала.
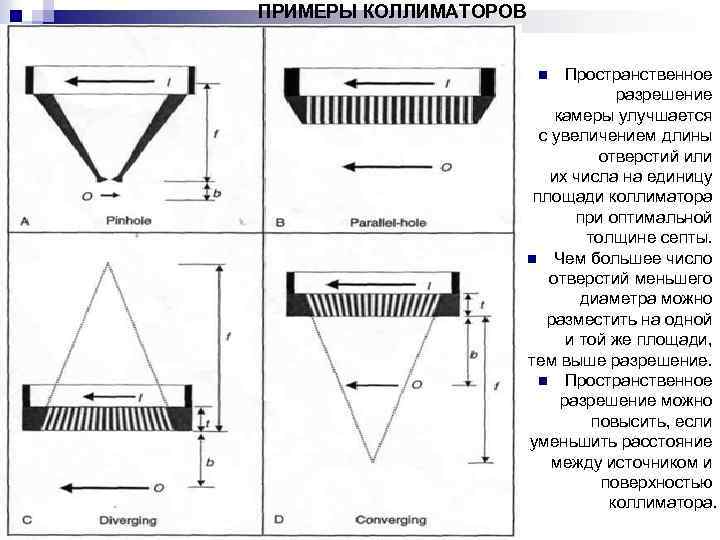
ПРИМЕРЫ КОЛЛИМАТОРОВ Пространственное разрешение камеры улучшается с увеличением длины отверстий или их числа на единицу площади коллиматора при оптимальной толщине септы. n Чем большее число отверстий меньшего диаметра можно разместить на одной и той же площади, тем выше разрешение. n Пространственное разрешение можно повысить, если уменьшить расстояние между источником и поверхностью коллиматора. n

Лучевая терапия. До 70% онкологических больных нуждаются в том или ином виде лучевой терапии, которые весьма многообразны. Основные способы облучения в лучевой терапии: n Дистанционная терапия - источники излучения находятся на определенном расстоянии от тела больного. n Контактная терапия – источники помещаются на поверхность тела пациента (аппликационная терапия) или в какую-либо полость тела – пищевод, прямую кишку, мочевой пузырь и др. (внутриполостная терапия). n Внутритканевая (интерстициальная) терапия – в ткани, содержащие опухолевый очаг, вводятся закрытые источники в виде проволок, игл, капсул, сборок из шариков или открытые источники, растворы которых непосредственно вводятся в организм через рот, в полость, опухоль или сосуд. Применение растворов основано на способности некоторых радионуклидов накапливаться преимущественно в определенных тканях (йод – в щитовидной железе, фосфор – в костном мозге и др. ). Контактную и внутритканевую терапию также называют брахитерапией. В зависимости от конкретного целевого назначения лучевая терапия подразделяется на ряд видов: n Радикальная лучевая терапия. Проводится с целью практически полного излечения больного за счет лучевого разрушения опухоли. Конечно, эта цель не всегда достигается, но предполагается, исходя из исходных данных о состоянии больного. Диапазон доз на опухоль 55 -80 Гр. n Предоперационная лучевая терапия. Проводится перед оперативным вмешательством с целью улучшения условий его проведения (уменьшение размера опухоли, перевод ее в операбельную форму) и уменьшения риска развития рецидивов. Диапазон доз 40 -50 Гр.

n n Интраоперационная лучевая терапия. Проводится в процессе оперативного вмешательства. Облучается либо опухоль, либо так называемое «открытое поле» , ложе опухоли после ее удаления. Это дает возможность добиться минимального облучения нормальных тканей и максимального - опухоли и зон регионарного метастазирования. Последнее должно обеспечить снижение частоты местных рецидивов, метастазов и послеоперационных осложнений. Диапазон доз 10 -20 Гр. Послеоперационная лучевая терапия. Проводится для достижения «стерилизации» операционного поля от рассеянных в процессе операции злокачественных клеток, а также разрушения оставшихся злокачественных тканей после неполного удаления опухоли и метастазов. Диапазон - 45 -55 Гр. Паллиативная терапия. Излучения позволяют решать и ряд вспомогательных задач терапии рака. Данная лучевая терапия не предполагает радикального излечения, учитывая состояние больного, характеристики опухоли и прогноз развития заболевания, и направлена на увеличение продолжительности жизни и относительное улучшение ее качества (снятие болей, отеков, облегчение подвижности и т. п. ). Диапазон доз 45 -55 Гр. Симптоматическая терапия. Близка по значению к паллиативной, чаще всего проводится для обезболивания. Суммарная очаговая доза менее 40 Гр. Основными методами лечения онкологических заболеваний в настоящее время считаются хирургический, лучевой и химиотерапевтический. Вспомогательную роль играют гормонотерапия и иммунотерапия. Активно развиваются генная и фотодинамическая терапия (воздействие на опухоль лазерного излучения и фотосенсибилизаторов).
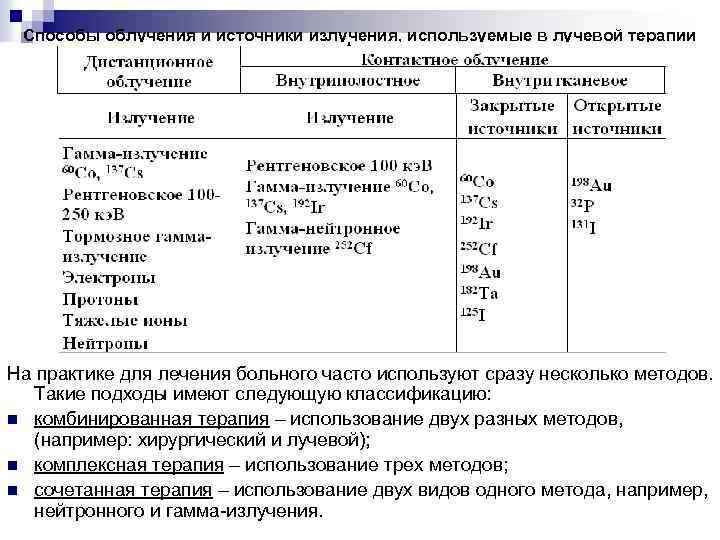
Способы облучения и источники излучения, используемые в лучевой терапии На практике для лечения больного часто используют сразу несколько методов. Такие подходы имеют следующую классификацию: n комбинированная терапия – использование двух разных методов, (например: хирургический и лучевой); n комплексная терапия – использование трех методов; n сочетанная терапия – использование двух видов одного метода, например, нейтронного и гамма-излучения.

При планировании курса лучевой терапии проводится определение областей, где доза может превысить толерантность нормальных тканей, и по возможности минимизируется область таких площадей. n Под толерантной (переносимой) дозой обычно понимают дозу, при которой частота поздних осложнений не превышает 5%. n Толерантная доза зависит от типа ткани, режима облучения и объема (площади) облучаемой ткани (для соединительной ткани это значение принято равным 60 Гр при площади облучения 100 см 2 и ежедневном облучении по 2 Гр). Существуют различные физические, химические и биологические способы модификации радиочувствительности нормальных и опухолевых тканей. n Для количественной оценки действия того или иного радиомодификатора используется так называемый фактор изменения дозы (ФИД), представляющий собой отношение доз ионизирующего излучения, вызывающих равные эффекты в условиях использования радиомодифицирующего агента и в контроле, без применения последнего. n Универсальным радиомодифицирующим агентом является кислород. Дозы, необходимые для одинакового снижения выживаемости клеток при их облучении в среде без кислорода почти в 3 раза выше, чем при хорошей оксигенации. n ФИД при использовании в качестве агента - кислорода называют коэффициентом кислородного усиления (ККУ).

Защита нормальных тканей n Химические радиозащитные препараты (радиопротекторы) пока не нашли широкого применения в клинической практике из-за небольшой широты их терапевтического действия (дозы препаратов, оказывающих заметное радиозащитное действие, вызывают выраженный побочный эффект, а применение их в нетоксичных дозах малоэффективно). n Наиболее перспективный в этом отношении метод – гипоксирадиотерапия. Он заключается в том, что на время проведения сеанса лучевой терапии больного переводят на дыхание газовыми смесями, в которых содержание кислорода ниже, чем в воздухе. Развивающаяся при этом общая гипоксия в организме позволяет осуществлять лечение любых форм и локализаций опухолей, резистентность, которых обусловлена наличием в них гипоксических клеток. Усиление лучевого поражения опухолей Среди многих более или менее успешных способов повышения радиочувствительности опухолевых клеток и тканей наиболее приемлемым для клинической практики оказался метод гипертермии, состоящий в нагревании опухолей с целью усиления их радиационного поражения. Чаще всего проводится дистанционный локальный нагрев опухоли с помощью генераторов электромагнитных излучений СВЧ-, УВЧ- и ВЧ-диапазонов (от 8 да 2450 МГц), реже применяют региональную и общую гипертермию. Еще один подход к решению центральной задачи лучевой терапии связан с вовлечением в клиническую практику так называемых плотноионизирующих излучений — нейтронов, протонов, π-мезонов, тяжелых ионов. Соответствующий тип лучевой терапий получил название адронной терапии. При этом ставка делается как на высокие параметры энерговыделения этими излучениями в тканях, так и на преимуществах пространственного распределения поглощенной дозы. При терапевтическом использовании таких излучений существенную роль начинает играть экономический фактор.
биофизика 10.ppt