биофизика 9.ppt
- Количество слайдов: 15

11 ЛЕКЦИЯ ПРЕДМЕТ - БИОФИЗИКА РАДИОФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ 1. 2. 3. 4. 5. Особенности радионуклидной диагностики; Основные направления и характеристики РНТ; Использование радиофармпрепаратов для радионуклидной терапии; Ядерно-физические данные радионуклидов, используемых для терапевтических РФП; Дозиметрическое обеспечение РНТ (MIRD -формализм).

Ядерная медицина – область медицины, где получила развитие клиническая диагностика заболеваний человека с помощью введения в его организм радиоизотопов в индикаторных количествах. Современная ядерная медицина состоит из: 1. радионуклидной диагностики (РНД); 2. радионуклидной терапии (РНТ). l Сущность РНТ состоит в лечебном воздействии на организм больного терапевтического радиофармпрепарата (РФП) путем введения его в организм (внутривенно, перорально или прицельно в патологический очаг). l Используя РНД производят анализ информации, полученной после введения в организм пациента определенного химического или биохимического соединения, меченного гамма-излучающим радионуклидом, с последующей регистрацией пространственновременного распределения этого соединения в организме с помощью позиционно-чувствительного детектора гамма-излучения. Полученные в лаборатории статические изображения изучаемого органа свидетельствуют о наличии и размере патологической области с аномальным распределением радиофармпрепарата. Изображения органов, избирательно концентрирующих препарат, получают методом сцинтиграфии. Пространственно – временная картина распределения радионуклида дает представление о топографии, форме и размерах органа, а также о наличии в нем патологических очагов. Радиоизотопная диагностика даёт менее чёткое изображение, чем КТ, ЯМР или УЗИ и имеет меньшее разрешение.

l l l l Распределение РФП зависит от кровотока и метаболической активности, поэтому РНД в большей степени направлена на функциональное исследование активности органов и систем, и в меньшей - на анализ их анатомо-морфологических особенностей. Функциональные изменения, намного опережающие анатомические, делают РНД уникальной как в ранней диагностике заболеваний, так и при динамическом наблюдении, при этом разовая лучевая нагрузка на пациента приблизительно в 100 раз меньше, чем при обычном рентгенологическом обследовании. Прямое отображение кровотока, микроциркуляции и метаболизма миокарда и головного мозга методом РНД обеспечило стремительный прогресс кардиологии и неврологии. РФП дают возможность получать изображения мест с аномальным метаболизмом, что позволяет визуализировать опухоли, воспаления или места тромбоза. Объективно обработать сцинтиграммы возможна только если знать процесс транспорта используемого РФП в организме, то есть иметь соответствующую математическую модель обращения данного РФП. Поэтому перспективы развития функциональной радионуклидной диагностики, связаны с созданием методов математического моделирования процессов транспорта РФП. На сегодняшний день разрабатывается комплекс математических моделей для исследований печени, костной системы, органной и тканевой гемоциркуляции; создается универсальный динамический фантом для проверки адекватности моделей

l l l l l Современное развитие ядерной медицины характеризуется прежде всего разработкой уникальных новых РФП, которые позволяют оценивать состояние различных органов и тканей организма на клеточном уровне. Наиболее перспективным является создание пептидных препаратов, меток рецепторов, которые позволяют проводить исследования патогенных заболеваний. Еще одним направлением является использование специализированных веществ для доставки терапевтических и диагностических доз лекарств непосредственно в нужное место. Использование таких РФП требует оснащения медицинских учреждений соответствующей техникой: эмиссионными и, особенно, позитронными томографами. В мире активно развивается позитронная томография, где существует около 30 наименований коммерческих препаратов для исследования в: кардиологии, онкологии, неврологии. Разрабатываются новые эмиссионные томографы с двумя-тремя детекторами, которые позволяют проводить эмиссионную томографию за минимальное время и с высоким разрешением. Слабым местом в радионуклидной диагностике является относительно невысокое пространственное разрешение аппаратуры. В первую очередь это относится к эмиссионным томографам и в меньшей степени к позитронным. Поэтому тенденцией в развитии методов диагностики и аппаратуры является появление комбинированных методов и аппаратуры, соединяющей эмиссионную томографию с рентгеновской и с ЯМРтомографией. Сегодня в мире появились первые подобные аппараты для пациентов эмиссионный томограф совмещенный с рентгеновским томографом.

Вторая разработка – эмиссионный томограф совмещенный с ЯМР томографом, позволяет одномоментно видеть не только включение исследуемого РФП в метаболический процесс, но и точно определить пространственную локализацию, по картине томографического среза. l К настоящему времени уже разработано свыше сотни терапевтических РФП, хотя в научно-клинических исследованиях используются десятки, а в терапии - всего лишь 10 – 15 подобных РФП. l Наиболее широко РНТ применяется в онкологии при ДРЩЖ ( 131 I ), для обезболивающей паллиативной терапии при костных метастазах рака предстательной железы, молочной железы, легких и других органов 89 Sr, 153 Sm и др. ), для локального послеоперационного облучения головного мозга при глиомах и т. д. l Широко используется РНТ в эндокринологии при ДТЗ (131 I), в ревматологии при артритах различной этиологии (186 Re- и 188 Re), а также при некоторых заболеваниях в гематологии, гастроэнтерологии и т. д. l Терапевтические РФП обычно метятся либо "чистыми" β-излучающими радионуклидами (32 P, 33 P, 89 Sr, 90 Y, 169 Er), либо "смешанными" β-γизлучателями (131 I, 153 Sm, 165 Dy, 166 Но, 177 Lu, 186 Re, 188 Re, и др. ) или α-γизлучающими радионуклидами (211 At, 213 Bi). Основными критерием выбора радионуклида-метки для терапевтических и диагностических РФП является: 1. Чем выше отношение уровней накопления РФП патологический очаг / нормальные ткани, тем выше доза внутреннего облучения патологического очага при заданном уровне толерантного облучения нормальных тканей. Именно поэтому терапевтические РФП метятся радионуклидами, которые при распаде испускают малопроникающее излучение (α- и β-частицы, электроны Оже и внутренней конверсии). l

2. Желательно, чтобы радионуклид также имел малоинтенсивное γизлучение. Хотя это и приводит к сравнительно небольшому дополнительному облучению всех нормальных тканей организма больного, зато позволяет методами планарной сцинтиграфии или ОФЭКТ осуществлять дозиметрическое планирование РНТ, контролировать распределение РФП в теле больного и определять дозу облучения в очагах. 3. Определяющими факторами, влияющими на степень радиационной безопасности конкретного РФП, являются период физического полураспада нуклида (Т 1/2), а также время биологического полувыведения РФП из организма (Tб), комбинируемые в комплексную величину Тэфф: Большое значение Тэфф может вызвать нежелательное хроническое облучение нормальных органов и тканей, куда он может попасть за длительное время вследствие медленных метаболических процессов; малое Тэфф создает крайне неравномерный режим облучения, который приводит к снижению терапевтической эффективности РНТ. Оптимальным значением периода полураспада для РНТ считают время от нескольких часов до нескольких суток. 4. В настоящее время стало возможным включать радионуклиды в состав различных химических соединений, биологические свойства которых резко отличаются от используемого нуклида (распределение в организме 99 Тс в соединении с технефитом, пентатехом и др. иное, чем собственно 99 Тс) которые доставляют РФП в нужный орган или ткань. 5. РФП, вводимые внутрь организма, не должны содержать токсических примесей или радиоактивных веществ, образующих дочерние ядра.
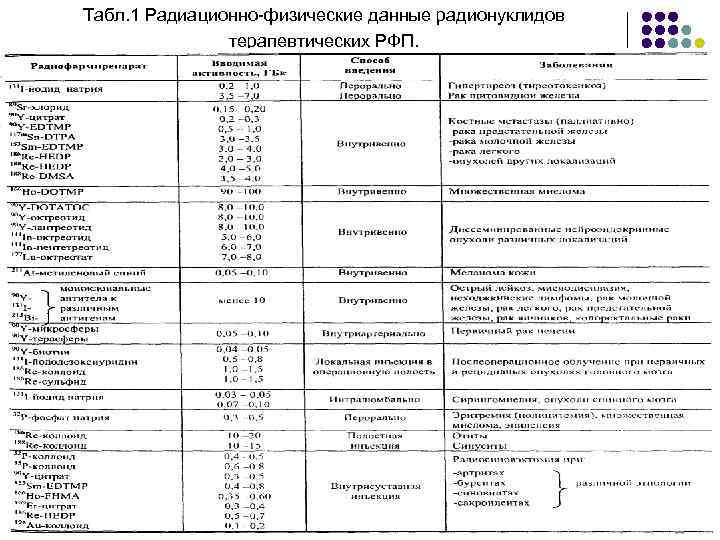
Табл. 1 Радиационно-физические данные радионуклидов терапевтических РФП.
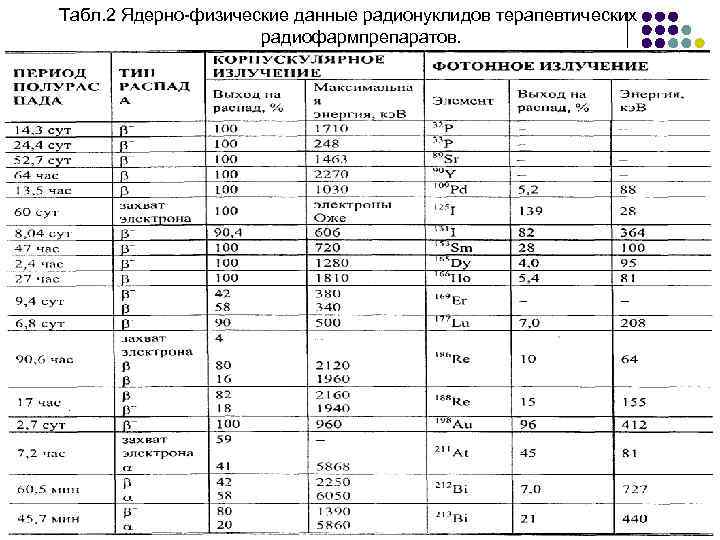
Табл. 2 Ядерно-физические данные радионуклидов терапевтических радиофармпрепаратов.

Критический орган - это орган, ткань, часть тела, облучение которых причиняет наибольший ущерб здоровью данного лица или его потомству. Золото (198 Аu). Препарат быстро поглощается из кровяного русла печенью, селезенкой и красным костным мозгом. Выведения не происходит, он остается в клетках до полного распада (12 -15 дней). Относительно высокая степень лучевой нагрузки на больного. Применяется для сканирования печени, селезенки, лимфоузлов (в случае их опухолевого поражения); определения кровотока в печени. l Индий (133 м. In). При внутривенном введении прочно связывается с gглобулинами крови и циркулирует в организме. 113 м. In является токсичным продуктом поэтому в клинической практике его используют в виде солей металлов. Редко используется в чистом виде, обычно входит в состав специальных меченых химических соединений – радиофармпрепаратов, получаемых на изотопных генераторах на территории госпиталя. l Йод (125 I). Является источником чистого гамма-излучения. Из-за большого периода полураспада применяется для метки гормонов, определяемых в сыворотке крови больного in vitro. Используют в брахитерапии простаты. l Йод (131 I). Источник b-частиц и гамма-квантов с различным уровнем энергий. Участвует в обменных процессах в организме. Критическим органом является щитовидная железа. Применяется в более чем в 90% всех терапевтических и диагностических процедур ядерной медицины, в частности, для определения функционального состояния и морфологических особенностей щитовидной железы. l Бенгальская роза - 131 I. После введения препарат поглощается из крови клетками печени и вместе с желчью выводится в кишечник. Критические органы - печень и желчный пузырь. Применяется для изучения функционального состояния печени при гепатитах, циррозах, желтухах и опухолях. l 131 I-BSCN используется в качестве меченого препарата для определения содержания бора в опухоли in vivo и для диагностики опухолей.

l l l Альбумин человеческой сыворотки, меченный изотопом 131 I или 99 м. Тс. Выпускается в виде микро и макроагрегатов с величиной частиц 20 -80 мкм, которые задерживаются в капиллярах легких. Через 3 -4 часа микроагрегаты под действием ферментов крови разрушаются и выводятся из организма. Применяется для определения показателей центральной и мозговой гемодинамики: минутного и ударного объемов сердца, скорости кровотока в большом и малом круге кровообращения, объема крови в легких, периферического кровотока, кровотока в головном мозге, скорости лимфотока. Гиппуран - 131 I после внутривенного введения быстро и избирательно выводится почками. Критические органы: почки и мочевой пузырь. Применение: оценка секреторно-выделительной функции почек, проходимости мочевыводящих путей, выявление количества остаточной мочи. Йод (132 I) излучает только гамма-кванты с энергией 0, 31 Мэ. В. Короткий период полураспада и отсутствие b-излучения уменьшает лучевую нагрузку на щитовидную железу почти в 200 раз по сравнению с 131 I, что позволяет применять его у детей. Ксенон (133 Хе). Источник гамма-квантов. Воздушно-ксенововая смесь применяется для определения нарушений проходимости спинного мозга при опухоли, менингите, сколиозе, объема остаточного воздуха в легких; регионарной вентиляции легких. Самарий-153 -оксабифор – фармпрепарат для лучевой терапии метастатических поражений скелета. Бета излучатель. Стронций-89. Источник b-частиц. Препарат «хлорид стронция-89» , «МЕТАСТРОН» - паллиативное средство при костных метастазах. 89 Sr является одним из наиболее современных и эффективных терапевтических радиоизотопов, который используется в онкологии для обезболивания, позволяя отказаться от наркотических веществ.

l l l Таллий (199 Tl). Предназначен для сцинтиграфии с целью диагностики инфаркта миокарда (Т 1 -199 -хлорид) и исследования кровоснабжения головного мозга (ДДК-Т 1 -199) в кардиологии. РФП способен стойко фиксироваться в структурах центральной нервной системы пропорционально кровотоку; используется для проведения томосцинтиграфии головного мозга с целью диагностики цереброваскулярной недостаточности. Этот индикатор дает возможность значительного снижения лучевой нагрузки на пациента. Технеций (99 м. Тс). Источник только g-квантов с энергией 140 Кэ. B. Технеций (99 м. Тс) пертехнетат проявляет себя в организме подобно йоду. Отличие заключается в том, что 99 м. Тс - пертехнетат не включается в синтез гормонов, поэтому его можно использовать для определения функции щитовидной железы на фоне применения с лечебной целью препаратов, блокирующих синтез гормонов. В последние годы в радионуклидной диагностике широко используются стандартные наборы реагентов, связывающиеся с 99 м. Тс и поставляющие его после внутривенного введения в определенный орган. Примером является реагент 99 м. Tc на основе альбумина крови человека. 99 м. Тс - ХИДА (ТСК-15) отличается быстрым прохждением и высокой концентрацией в желчевыводящих протоках и желчном пузыре, что обусловливает их хорошую визуализацию при минимальной лучевой нагрузке. Критические органы: печень, желчный пузырь и кишечник. Применяется для динамической гепатосцинтиграфии в диагностике желчнокаменной болезни, холецистита, холангита, желчевыводящих путей. 99 м. Тс - фитон избирательно накапливается в клетках печени и селезенки. При введении быстро выводится из крови с достижением максимального накопления в печени через 10 -15 -й мин. Критические органы: печень, селезенка и красный костный мозг. Применяется в диагностике очаговых поражений и цирроза печени. 99 м. Тс - цитон - нефротропный препарат. Крические органы - почки и мочевой пузырь. Применяется для статической диагностики опухолей и пороков развития почек.

99 м. Тс - ДТПА (ТСК) - нефротропный препарат. При внутри венном введении быстро фильтруется почками и полностью выводится из организма за 24 часа. Максимальная концентрация препарата в почках достигается через 5 -6 минут. Критические органы: почки и мочевой пузырь. Применяется для динамической сцинтиграфии почек в изучении клубочковой фильтрации и морфологии почек, мочекаменной болезни, туберкулезе почек, пиелонефрите, сахарном диабете. l 99 м. Тс - пирофосфат (ТСК-8) накапливается в костях, некротических тканях. Максимальная l концентрация в костях достигается через 4 часа. Выводится почками. Критические органы: скелет и почки. Применяется в диагностике метастазов в кости, инфаркте миокарда. l 99 м. Тс-МАА. Макроагрегаты альбумина сыворотки человеческой крови после внутри венного введения задерживаются в капиллярах легких. При внутриартериальном введении фиксируется в капиллярах того органа, который снабжается кровью из данной артерии. Критическим органом являются легкие или исследуемый орган. Применяется для выявления нарушений микроциркуляции артерии, закрытой травме груди. l Фосфор (32 Р). Источник b-частиц с максимальной энергией 1, 7 Мэ. В и наибольшей длиной пробега в тканях 8 мм. Используется для диагностики злокачественных новообразований глаз, кожи слизистых оболочек, молочной железы, головного мозга (во время операции). В настоящее время бурно развиваются исследования с препаратами на основе антител, пептидов и нуклеатидов, меченных различными радионуклидами, в основном 131 I, 90 Y, 111 In. В развитии радиофармпромышленности можно выделить два этапа. Первый производство готовых радиофармпрепаратов. Второй начался в связи с появлением генераторных систем, которые дали возможность получать радиофармпрепарат с заданными свойствами непосредственно в лаборатории, — из сочетания радионуклида с набором реагентов. l

Дозиметрическое обеспечение РНТ. MIRD-формализм. В отличие от традиционных методов дистанционного и контактного терапевтического облучения дозиметрическое обеспечение РНТ пока сильно отстает от клинических требований и не поспевает за интенсивной разработкой новых терапевтических РФП. l Проблема дозиметрического обеспечения распадается на две взаимосвязанные задачи – собственно дозиметрическое планирование РНТ (посредством РНД) и контроль очаговых и органных доз после введения терапевтической активности РФП. В основе дозиметрического планирования лежит так называемый MIRDформализм, т. е. математический аппарат дозиметрии внутреннего облучения от РФП, который был предложен еще в 1965 - 1969 гг. Использование описанного MIRD-формализма обусловливает следующую технологическую схему дозиметрического планирования РНТ с введением РФП, меченных "смешанными" β-γ-излучателями типа 131 I, 153 Sm, 186 Re и т. п. : l Больному сначала вводится диагностическая активность используемого терапевтического РФП, которая в 100 - 200 раз ниже терапевтической активности. l В течение нескольких дней неоднократно в динамике проводится in vivo радиометрия всего тела и (или) отдельных органов, например щитовидной железы при 131 I -РНТ гипертиреоза. Вместо радиометрии чаще используют планарную сцинтиграфию или однофотонную эмиссионную компьютерную томографию (ОФЭКТ), причем гамма-камера или радиометр должны быть предварительно откалиброваны в фантомных экспериментах. Желательно, чтобы фантом обладал наиболее возможной степенью антропоморфности с имитацией указанных органов. In vivo измерения иногда дополняются in vitro радиометрией серии биопроб, отбираемых у больного за тот же интервал времени (кровь, моча).

l l l По результатам радиометрии формируются функции удержания РФП в патологических очагах и в других органах-источниках, накапливающих РФП, а также, при необходимости, во всем теле. Больному проводят рентгенографию, КТ, УЗИ или какое-либо другое исследование для определения значений массы органов-мишеней и облучаемых патологических очагов. Для патологических очагов и остальных органов-источников (они одновременно являются и органами-мишенями) поглощенные фракции принимаются равными 1. Для органов-мишеней, не накапливающих РФП, поглощенные фракции определяются по табулированным данным, которые были рассчитаны в рамках MIRD-формализма методом Монте. Карло для математических антропоморфных фантомов различной степени сложности и которые приведены в официальных публикациях МКРЗ. По результатам определения функций удержания, массы облучаемого органа (патологического очага) и поглощенных фракций рассчитывают значение удельной дозы внутреннего облучения органа-мишени в единицах Гр/МБк, (дозы на единицу введенной диагностической активности РФП). При упрощенном дозиметрическом планировании по полученному значению удельной дозы и заданному врачом-радиологом значению суммарной очаговой дозы рассчитывается величина терапевтической активности РФП, которая и должна быть введена больному. При более точном дозиметрическом планировании учитывают лучевую нагрузку на критические по радиочувствительности органы-мишени, не накапливающие или частично накапливающие РФП: вводимая терапевтическая активность должна обеспечивать клинически приемлемый компромисс между терапевтически эффективной очаговой дозой и толерантной дозой наиболее радиочувствительного органамишени.

l l l Если в качестве радионуклида-метки для РФП используется "чистый" βизлучатель (32 P, 89 Sr, 90 Y, 169 Er), описанная схема планирования оказывается непригодной, так как нельзя проведения in vivo измерения функций удержания РФП. Чтобы обойти такую принципиальную трудность, больному вводят диагностическую активность того же РФП, но меченную не "чистым" β-излучателем, а "смешанным" β-γ-излучающим изотопом того же основного β-излучающего радионуклида. Тогда описанная выше технологическая схема дозиметрического планирования остается в силе, только в последней процедуре вычисления терапевтической активности необходимо ввести поправку на различие схем радиоактивного распада основного радионуклида и его изотопа-имитатора. Аналогичным образом, контроль реальных очаговых и органных доз после введения терапевтической активности РФП также требует проведения сложных измерений и расчетов ( непосредственные измерения доз облучения с внедрением миниатюрных дозиметров β-излучения в тело пациента крайне затруднены). Используют метод косвенного контроля доз внутреннего облучения. Для "смешанных" β-γ- и α-γ-излучающих РФП конкретная технология контроля зависит от того, проводилось или нет дозиметрическое планирование РНТ еще до введения терапевтической активности. Если предварительное дозиметрическое планирование не проводилось, то дополнительно проводят измерения по определению масс органов-мишеней, а значения поглощенных фракций для не накапливающих РФП органов-мишеней берут из таблиц в публикациях МКРЗ. Косвенный контроль очаговых и органных доз от "чистых" β-излучающих РФП вполне реален, если больному введена достаточно высокая терапевтическая активность подобного РФП. Тогда радиометрию патологических очагов можно проводить по тормозному излучению, создаваемому β-частицами при их замедлении в тканях тела больного. Радиационный выход тормозного излучения прямо пропорционален эффективному атомному номеру материала источника, и такая технология контроля наиболее приемлема для РНТ костных метастазов со 89 Sr и 90 Y.
биофизика 9.ppt