 1 Химия органических соединений
1 Химия органических соединений
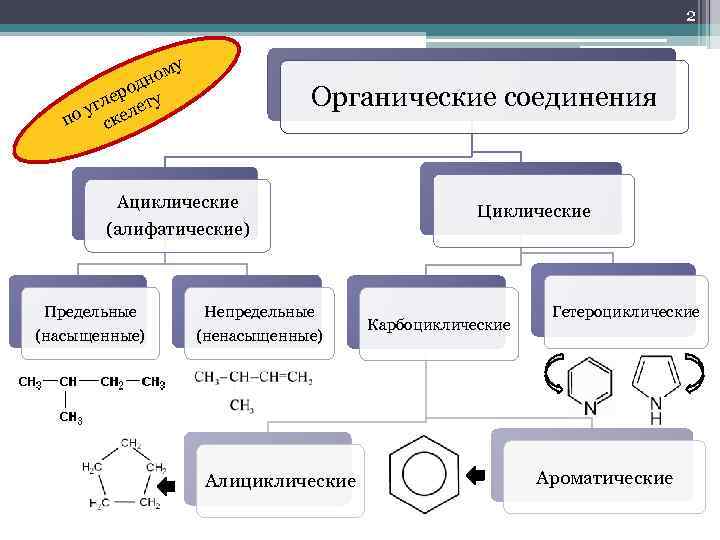 2 у ом н род у е угл елет по ск Органические соединения Ациклические (алифатические) Предельные (насыщенные) Непредельные (ненасыщенные) Алициклические Циклические Карбоциклические Гетероциклические Ароматические
2 у ом н род у е угл елет по ск Органические соединения Ациклические (алифатические) Предельные (насыщенные) Непредельные (ненасыщенные) Алициклические Циклические Карбоциклические Гетероциклические Ароматические
 3 о ьным п л а он ам ци нк рупп фу г спирты, фенолы - NH 2 амины (первичные) - NO 2 нитросоединения - C ≡N нитрилы -C =O H = галогенопроизводные -OH R- - Hal альдегиды кетоны -COOH карбоновые кислоты -COOR сложные эфиры - CONH 2 амиды - SO 3 H сульфокислоты -C – R O
3 о ьным п л а он ам ци нк рупп фу г спирты, фенолы - NH 2 амины (первичные) - NO 2 нитросоединения - C ≡N нитрилы -C =O H = галогенопроизводные -OH R- - Hal альдегиды кетоны -COOH карбоновые кислоты -COOR сложные эфиры - CONH 2 амиды - SO 3 H сульфокислоты -C – R O
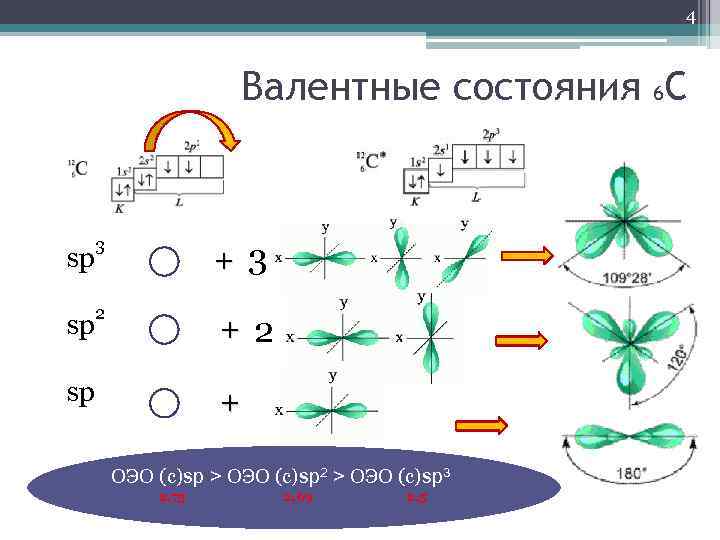 4 Валентные состояния 6 С sp 3 sp 2 + 3 + 2 sp + ОЭО (с)sp > ОЭО (с)sp 2 > ОЭО (с)sp 3 2, 75 2, 69 2, 5
4 Валентные состояния 6 С sp 3 sp 2 + 3 + 2 sp + ОЭО (с)sp > ОЭО (с)sp 2 > ОЭО (с)sp 3 2, 75 2, 69 2, 5
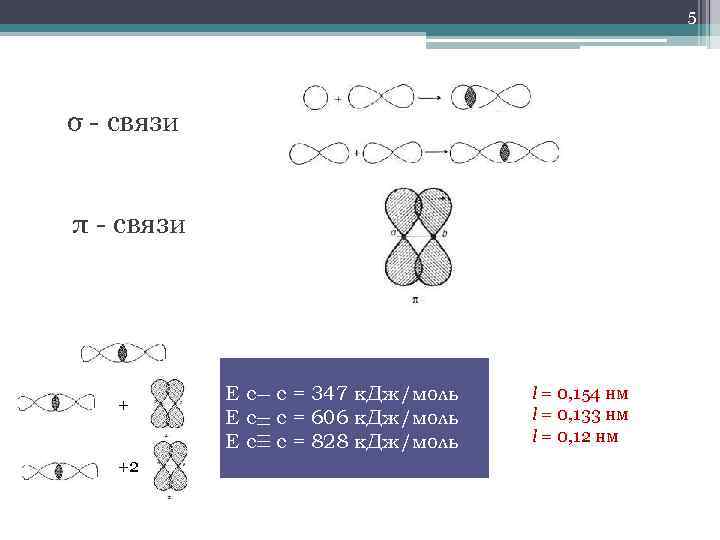 5 σ - связи π - связи + +2 Е с с = 347 к. Дж/моль Е с с = 606 к. Дж/моль Е с с = 828 к. Дж/моль l = 0, 154 нм l = 0, 133 нм l = 0, 12 нм
5 σ - связи π - связи + +2 Е с с = 347 к. Дж/моль Е с с = 606 к. Дж/моль Е с с = 828 к. Дж/моль l = 0, 154 нм l = 0, 133 нм l = 0, 12 нм
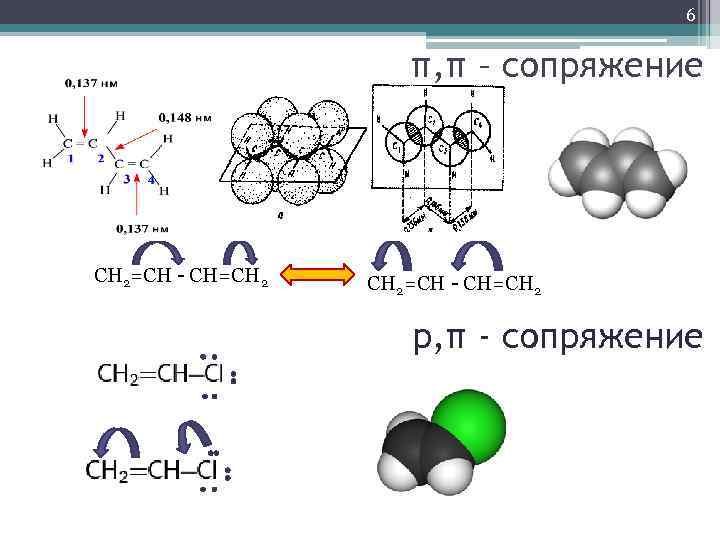 6 π, π – сопряжение СН 2=СН - СН=СН 2 р, π - сопряжение
6 π, π – сопряжение СН 2=СН - СН=СН 2 р, π - сопряжение
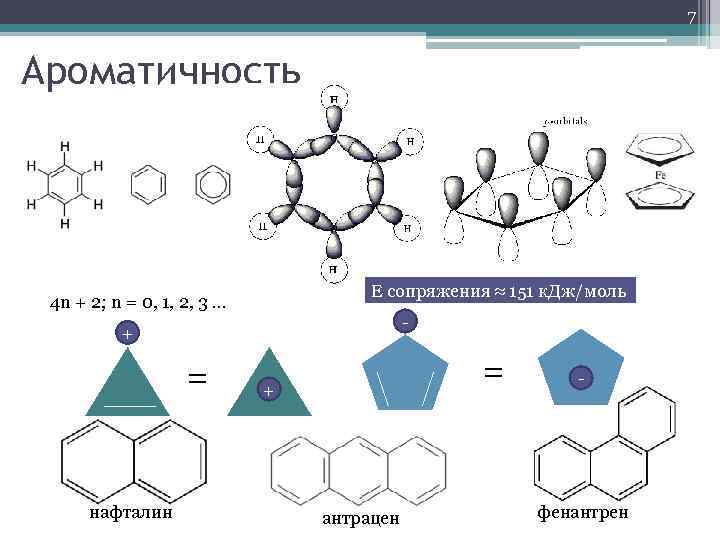 7 Ароматичность Е сопряжения ≈ 151 к. Дж/моль 4 n + 2; n = 0, 1, 2, 3 … - + = нафталин = + антрацен - фенантрен
7 Ароматичность Е сопряжения ≈ 151 к. Дж/моль 4 n + 2; n = 0, 1, 2, 3 … - + = нафталин = + антрацен - фенантрен
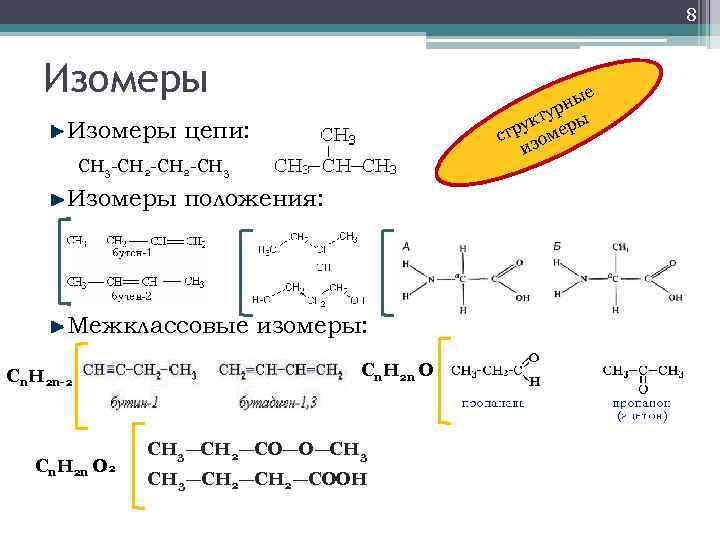 8 Изомеры е ны р кту ры у стр зоме и Изомеры цепи: CH 3 -CH 2 -CH 3 Изомеры положения: Межклассовые изомеры: Cn. H 2 n-2 Cn. H 2 n О СН 3—СН 2—СО—О—СН 3—СН 2—СООН
8 Изомеры е ны р кту ры у стр зоме и Изомеры цепи: CH 3 -CH 2 -CH 3 Изомеры положения: Межклассовые изомеры: Cn. H 2 n-2 Cn. H 2 n О СН 3—СН 2—СО—О—СН 3—СН 2—СООН
 Стереоизомеры Конформационные (“поворотные”) Конфигурационные: • Энантиомеры (“зеркальные”) • Диастереомеры • σ—диастереомерия: π—диастереомерия (геометрическая изомерия): ры о ере ст е зом и
Стереоизомеры Конформационные (“поворотные”) Конфигурационные: • Энантиомеры (“зеркальные”) • Диастереомеры • σ—диастереомерия: π—диастереомерия (геометрическая изомерия): ры о ере ст е зом и
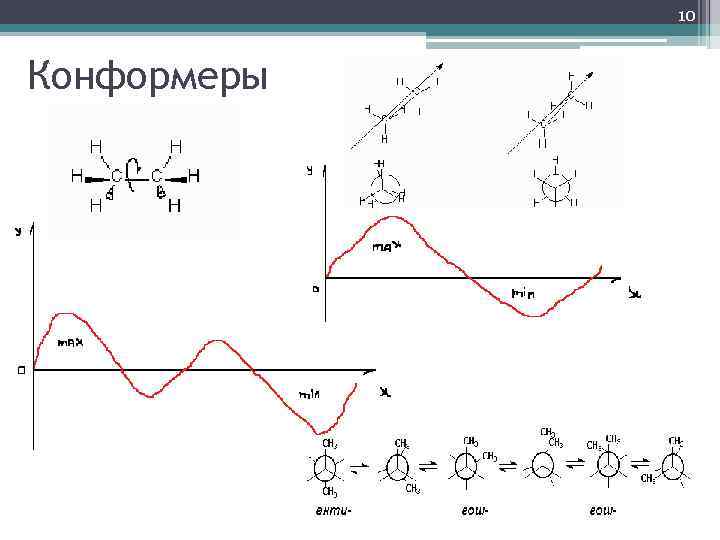 10 Конформеры
10 Конформеры
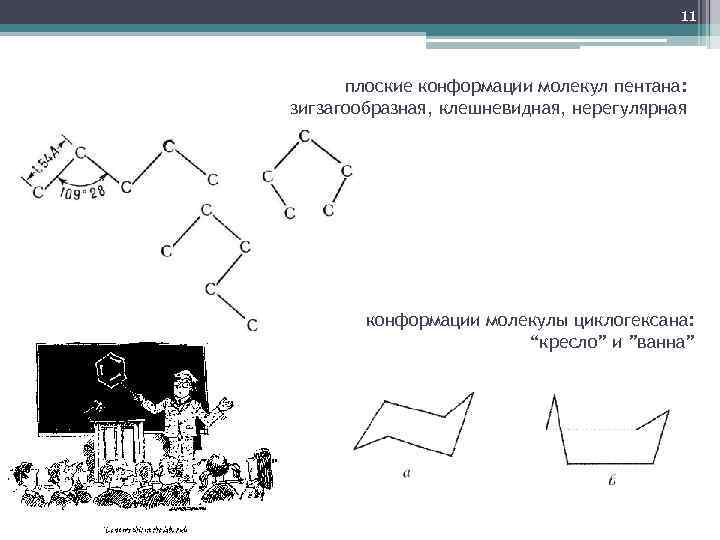 11 плоские конформации молекул пентана: зигзагообразная, клешневидная, нерегулярная конформации молекулы циклогексана: “кресло” и ”ванна”
11 плоские конформации молекул пентана: зигзагообразная, клешневидная, нерегулярная конформации молекулы циклогексана: “кресло” и ”ванна”
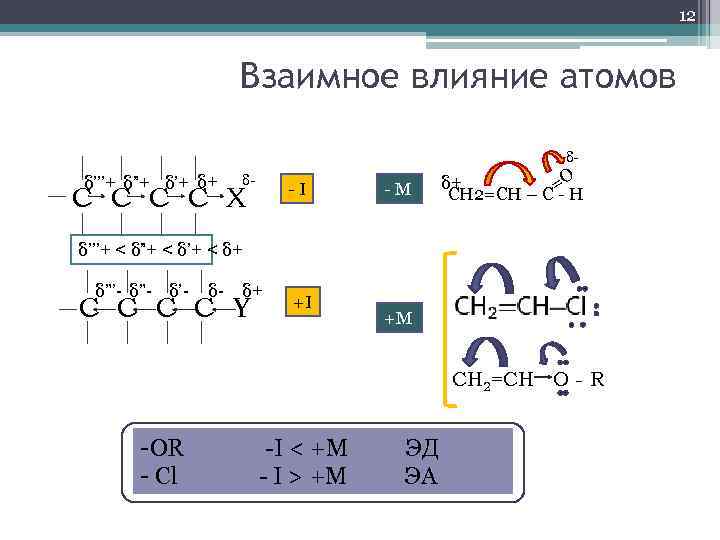 12 Взаимное влияние атомов δ- δ’’’+ δ”+ δ’+ δ+ δ- С C C C X - I - M δ+ =O CH 2=CH – C - H δ’’’+ < δ”+ < δ’+ < δ+ δ”’- δ”- δ’- δ- δ+ C C Y +I +M CH 2=CH O - R -OR -I < +M ЭД - Cl - I > +M ЭА
12 Взаимное влияние атомов δ- δ’’’+ δ”+ δ’+ δ+ δ- С C C C X - I - M δ+ =O CH 2=CH – C - H δ’’’+ < δ”+ < δ’+ < δ+ δ”’- δ”- δ’- δ- δ+ C C Y +I +M CH 2=CH O - R -OR -I < +M ЭД - Cl - I > +M ЭА
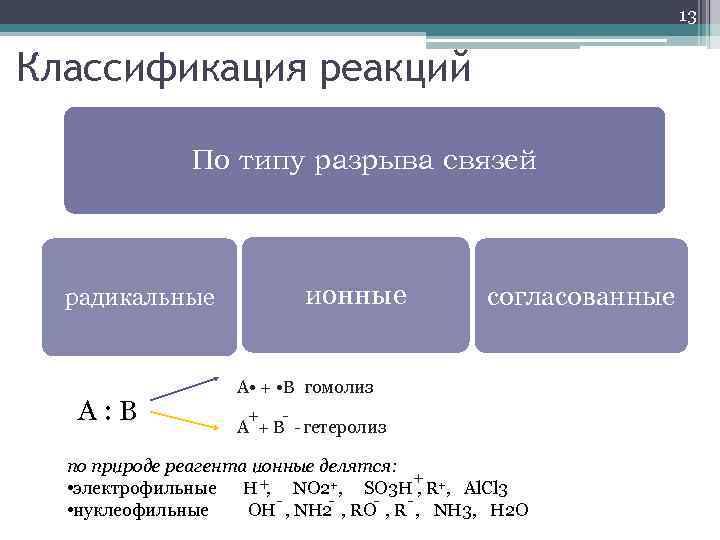 13 Классификация реакций По типу разрыва связей радикальные A : B ионные согласованные A • + • B гомолиз + A + B гетеролиз - по природе реагента ионные делятся: + + • электрофильные H , NO 2+, SO 3 H , R+, Al. Cl 3 • нуклеофильные OH , NH 2 , RO , R , NH 3, H 2 O
13 Классификация реакций По типу разрыва связей радикальные A : B ионные согласованные A • + • B гомолиз + A + B гетеролиз - по природе реагента ионные делятся: + + • электрофильные H , NO 2+, SO 3 H , R+, Al. Cl 3 • нуклеофильные OH , NH 2 , RO , R , NH 3, H 2 O
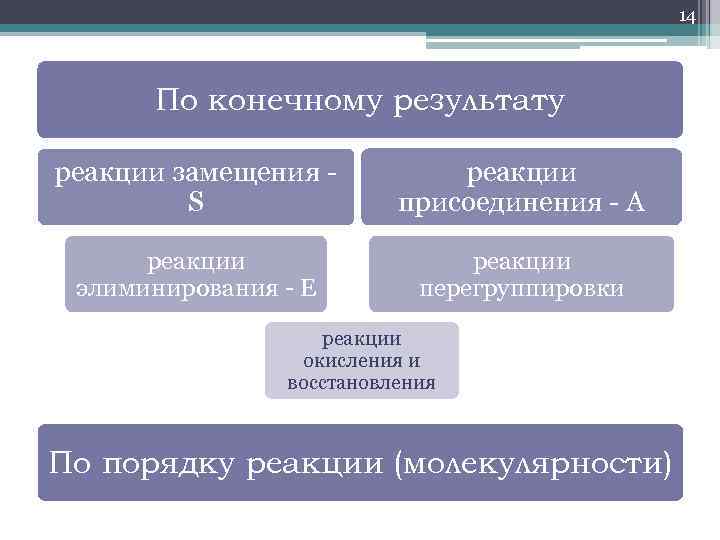 14 По конечному результату реакции замещения - S реакции присоединения - A реакции элиминирования - E реакции перегруппировки реакции окисления и восстановления По порядку реакции (молекулярности)
14 По конечному результату реакции замещения - S реакции присоединения - A реакции элиминирования - E реакции перегруппировки реакции окисления и восстановления По порядку реакции (молекулярности)
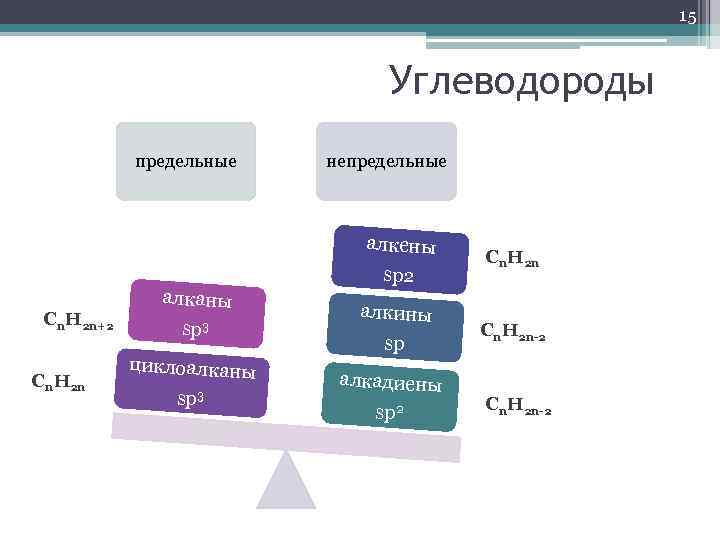 15 Углеводороды предельные непредельные алкены Cn. H 2 n+2 Cn. H 2 n алканы sp 3 циклоалканы sp 3 sp 2 алкины sp алкадиены sp 2 Cn. H 2 n-2
15 Углеводороды предельные непредельные алкены Cn. H 2 n+2 Cn. H 2 n алканы sp 3 циклоалканы sp 3 sp 2 алкины sp алкадиены sp 2 Cn. H 2 n-2
 16 Механизм радикального замещения SR (sp³) 1. инициирование ( T, hν, радиация) 2. рост цепи 3. обрыв цепи
16 Механизм радикального замещения SR (sp³) 1. инициирование ( T, hν, радиация) 2. рост цепи 3. обрыв цепи
 17 hν + Cl 2 смесь продуктов -Hl +Br 2 -HBr Е Сперв. –Н = 406 к. Дж/моль E Cвтор. –Н = 393, 5 к. Дж/моль Е Стрет. –Н = 381 к. Дж/моль Устойчивость CH 3 < Alk CH 2 < Alk CH Alk < Alk C Alk = CH 3, C 2 H 5. . Alk
17 hν + Cl 2 смесь продуктов -Hl +Br 2 -HBr Е Сперв. –Н = 406 к. Дж/моль E Cвтор. –Н = 393, 5 к. Дж/моль Е Стрет. –Н = 381 к. Дж/моль Устойчивость CH 3 < Alk CH 2 < Alk CH Alk < Alk C Alk = CH 3, C 2 H 5. . Alk
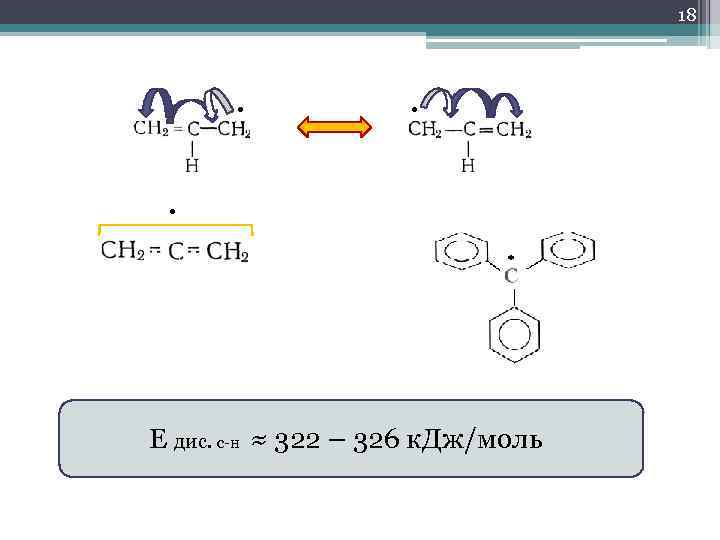 18 • • • Е дис. с-н ≈ 322 – 326 к. Дж/моль
18 • • • Е дис. с-н ≈ 322 – 326 к. Дж/моль
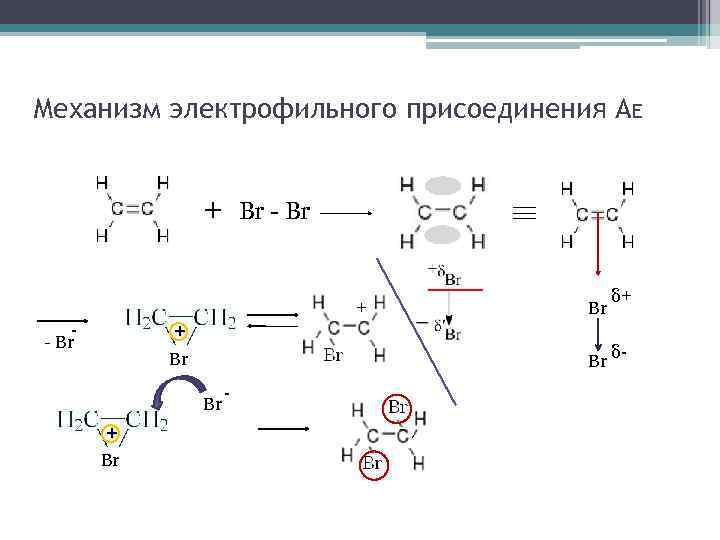 Механизм электрофильного присоединения АE + Br - Br + Br Br δ+ Br δ- Br + Br
Механизм электрофильного присоединения АE + Br - Br + Br Br δ+ Br δ- Br + Br
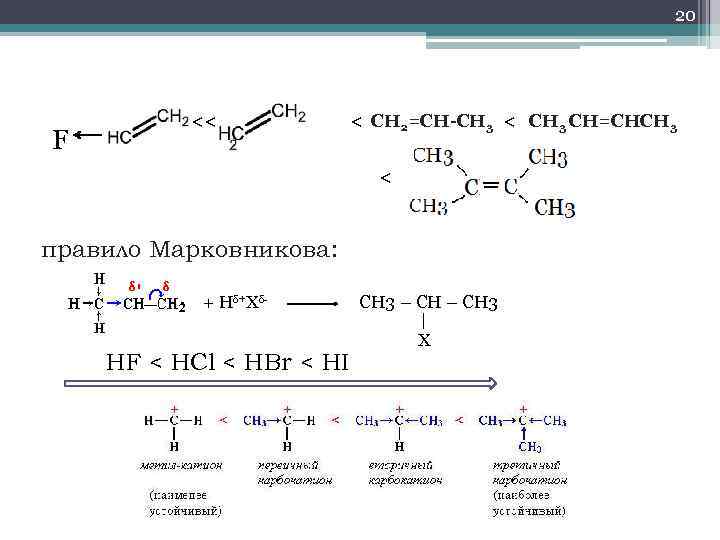 20 F << < СН 2=СН-СН 3 < СН 3 СН=СНСН 3 < правило Марковникова: + Hδ+Xδ- CH 3 – CH 3 X HF < HCl < HBr < HI
20 F << < СН 2=СН-СН 3 < СН 3 СН=СНСН 3 < правило Марковникова: + Hδ+Xδ- CH 3 – CH 3 X HF < HCl < HBr < HI
 21 AR (против правила Марковникова)
21 AR (против правила Марковникова)
 22 AE (кислотный катализ) + H CH 3 – CH = CH 2 + H 2 O CH 3 – CH(OH) – CH 3 + + CH 3 – CH = CH 2 + CH 3 – CH 3 H карбкатион HOH
22 AE (кислотный катализ) + H CH 3 – CH = CH 2 + H 2 O CH 3 – CH(OH) – CH 3 + + CH 3 – CH = CH 2 + CH 3 – CH 3 H карбкатион HOH
 23 Окисление алкенов “мягкое” окисление “жесткое” окисление
23 Окисление алкенов “мягкое” окисление “жесткое” окисление
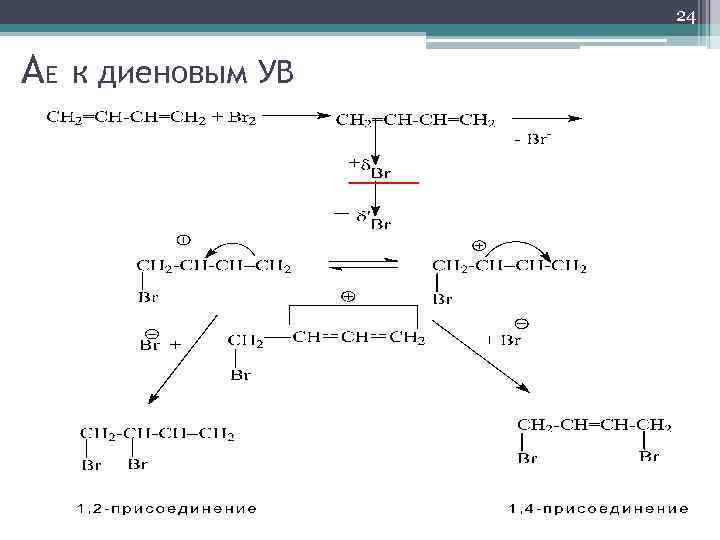 24 AE к диеновым УВ
24 AE к диеновым УВ
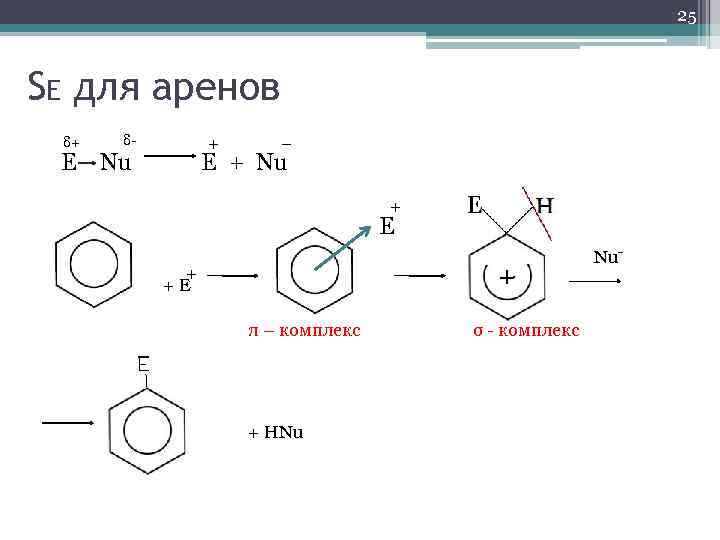 25 SE для аренов δ+ δ- + – E Nu E + Nu + E Nu- + + E π – комплекс σ - комплекс + HNu
25 SE для аренов δ+ δ- + – E Nu E + Nu + E Nu- + + E π – комплекс σ - комплекс + HNu
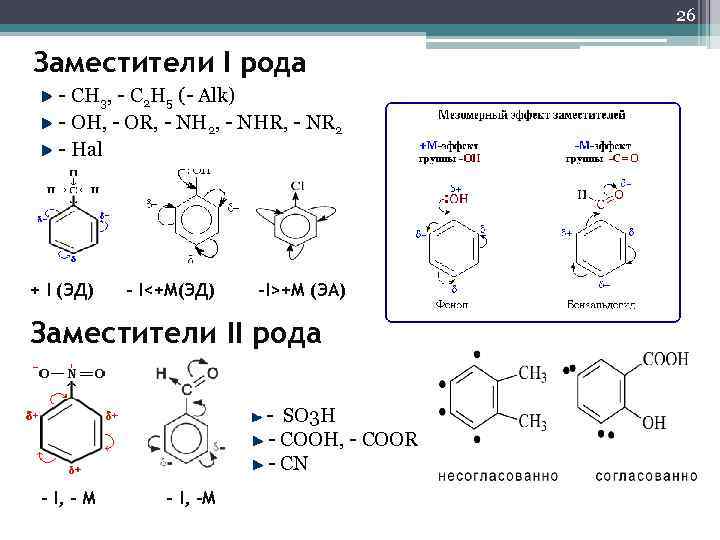 26 Заместители I рода - CH 3, - C 2 H 5 (- Alk) - OH, - OR, - NH 2, - NHR, - NR 2 - Hal + I (ЭД) - I<+M(ЭД) –I>+M (ЭА) Заместители II рода - SO 3 H - COOH, - COOR - CN - I, - М - I, -M
26 Заместители I рода - CH 3, - C 2 H 5 (- Alk) - OH, - OR, - NH 2, - NHR, - NR 2 - Hal + I (ЭД) - I<+M(ЭД) –I>+M (ЭА) Заместители II рода - SO 3 H - COOH, - COOR - CN - I, - М - I, -M
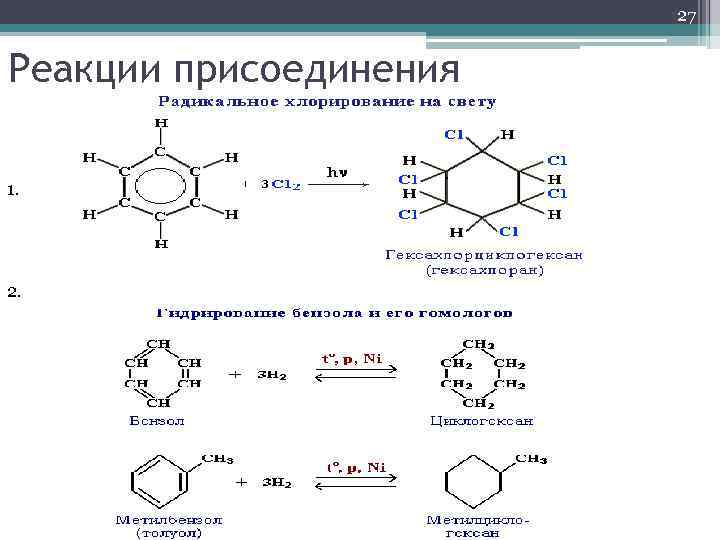 27 Реакции присоединения 1. 2.
27 Реакции присоединения 1. 2.
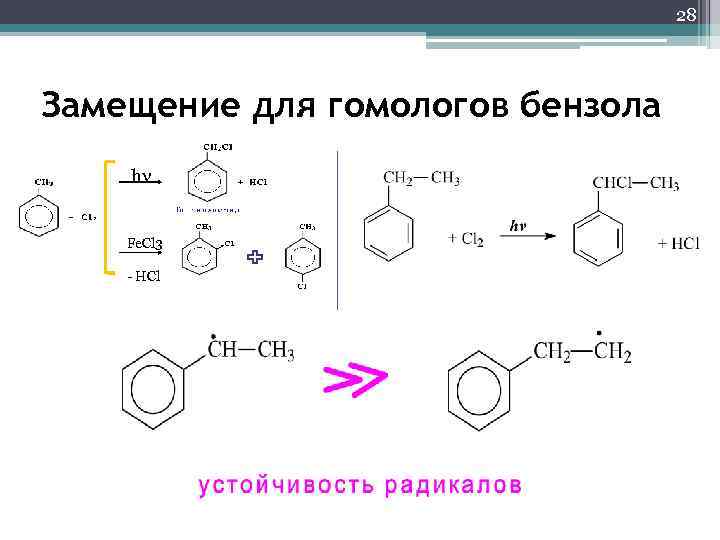 28 Замещение для гомологов бензола hν Fe. Cl 3 - HCl
28 Замещение для гомологов бензола hν Fe. Cl 3 - HCl
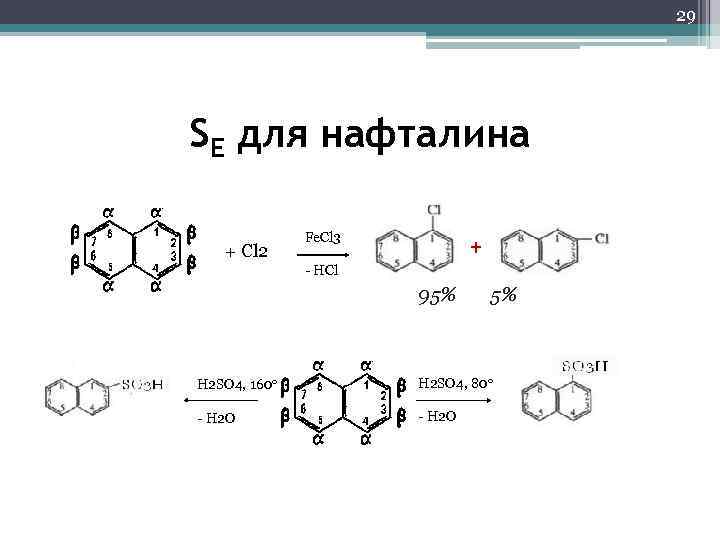 29 SE для нафталина + Сl 2 Fe. Cl 3 + - HCl 95% 5% H 2 SO 4, 160 H 2 SO 4, 80 - H 2 O
29 SE для нафталина + Сl 2 Fe. Cl 3 + - HCl 95% 5% H 2 SO 4, 160 H 2 SO 4, 80 - H 2 O
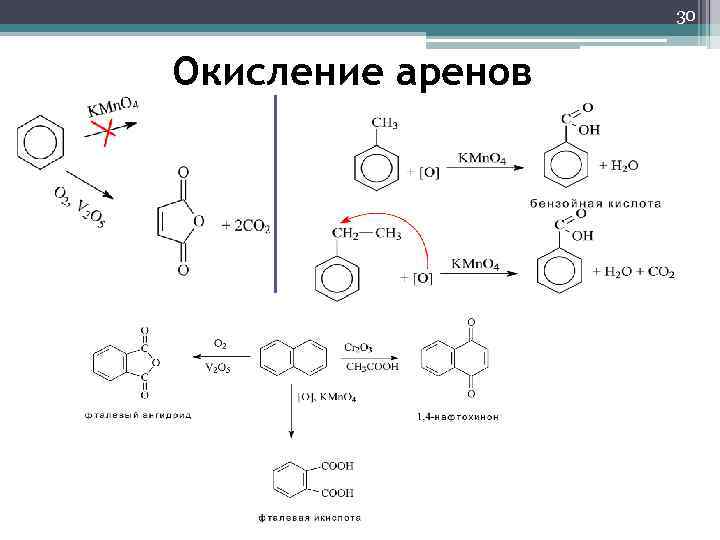 30 Окисление аренов
30 Окисление аренов
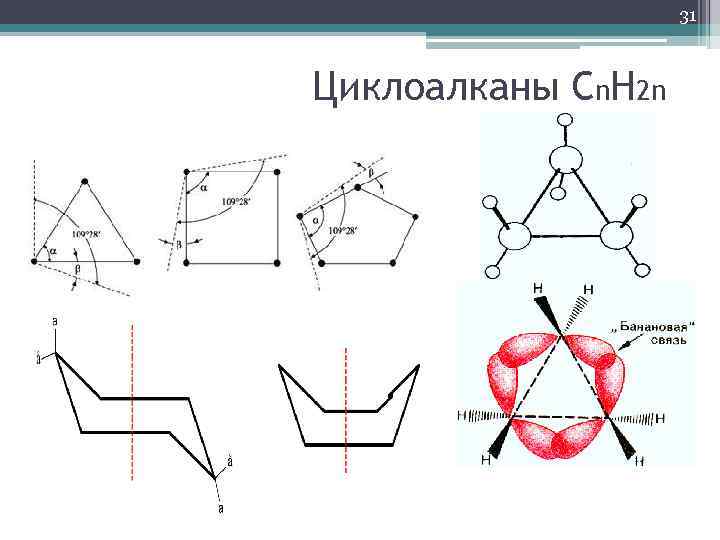 31 Циклоалканы Сn. H 2 n
31 Циклоалканы Сn. H 2 n
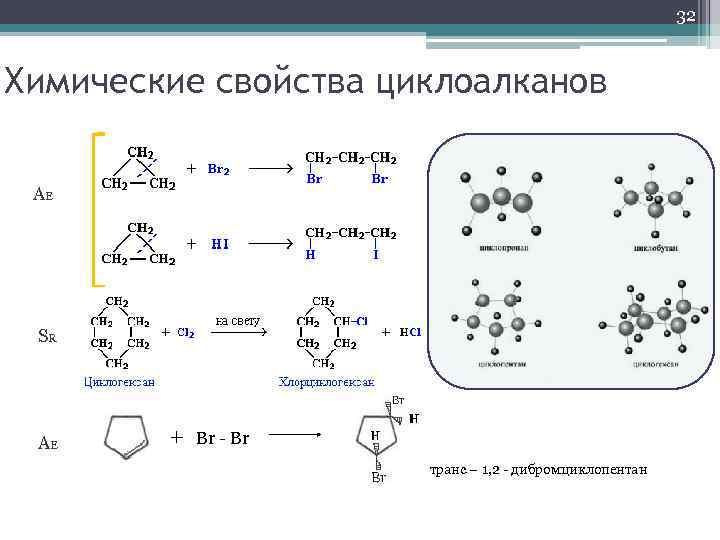 32 Химические свойства циклоалканов AE SR AE + Br - Br транс – 1, 2 - дибромциклопентан
32 Химические свойства циклоалканов AE SR AE + Br - Br транс – 1, 2 - дибромциклопентан
 33
33


