1 ТВЕРДЫЕ ТЕЛА 2 Кристаллические решетки 5 типов















38902-phys_chem_biol_2_2012.ppt
- Количество слайдов: 35
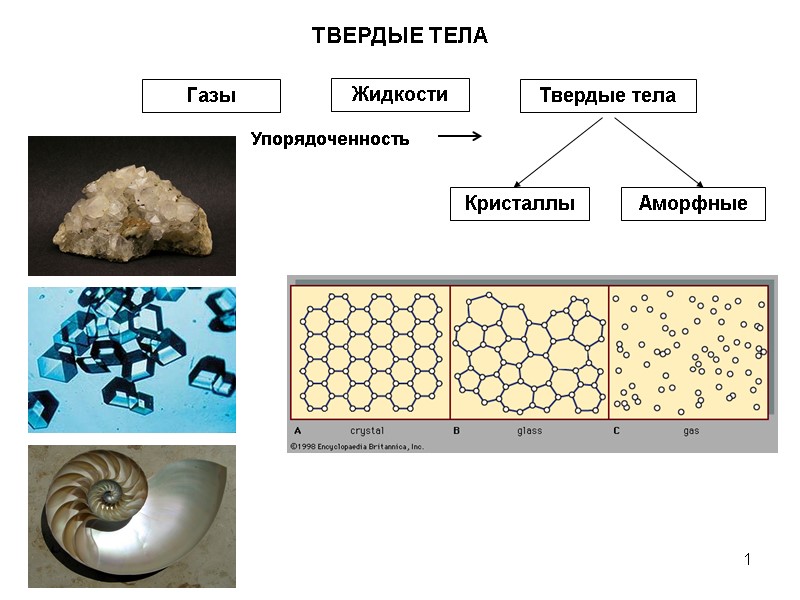
 1 ТВЕРДЫЕ ТЕЛА
1 ТВЕРДЫЕ ТЕЛА
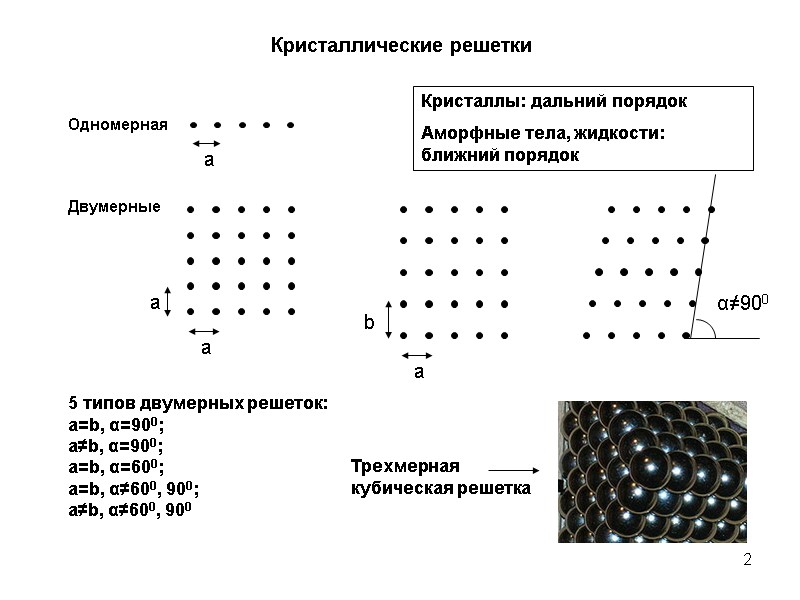
 2 Кристаллические решетки 5 типов двумерных решеток: a=b, α=900; a≠b, α=900; a=b, α=600; a=b, α≠600, 900; a≠b, α≠600, 900 Кристаллы: дальний порядок Аморфные тела, жидкости: ближний порядок
2 Кристаллические решетки 5 типов двумерных решеток: a=b, α=900; a≠b, α=900; a=b, α=600; a=b, α≠600, 900; a≠b, α≠600, 900 Кристаллы: дальний порядок Аморфные тела, жидкости: ближний порядок
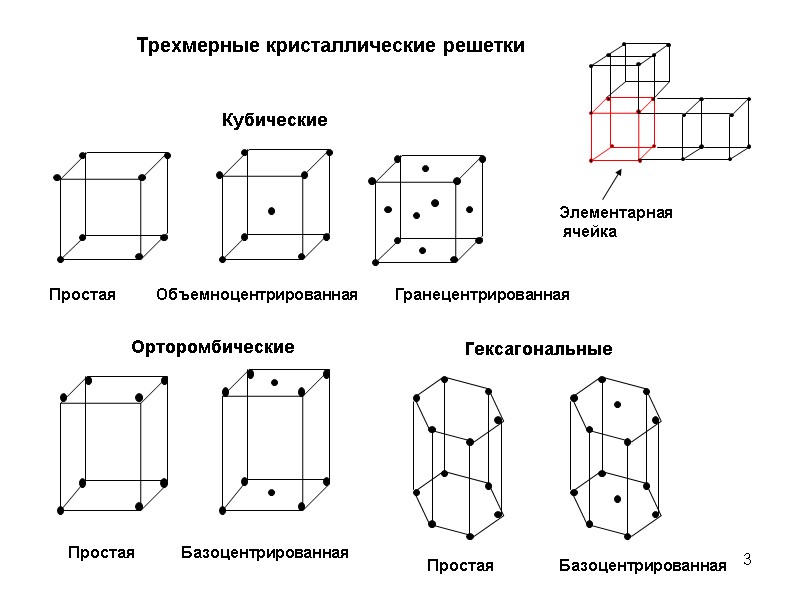
 3 Трехмерные кристаллические решетки Простая Кубические Объемноцентрированная Гранецентрированная Орторомбические Простая Базоцентрированная Гексагональные Простая Базоцентрированная Элементарная ячейка
3 Трехмерные кристаллические решетки Простая Кубические Объемноцентрированная Гранецентрированная Орторомбические Простая Базоцентрированная Гексагональные Простая Базоцентрированная Элементарная ячейка
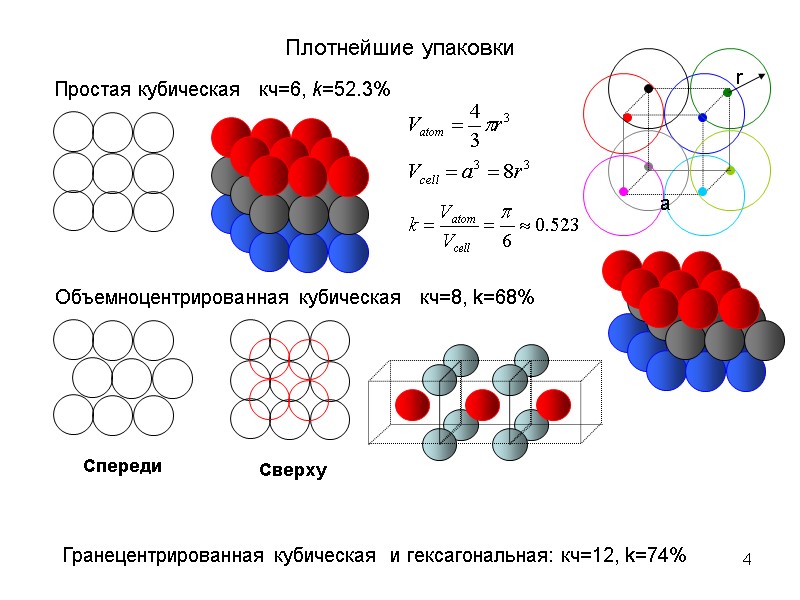
 4 Плотнейшие упаковки Простая кубическая кч=6, k=52.3% Объемноцентрированная кубическая кч=8, k=68% Гранецентрированная кубическая и гексагональная: кч=12, k=74%
4 Плотнейшие упаковки Простая кубическая кч=6, k=52.3% Объемноцентрированная кубическая кч=8, k=68% Гранецентрированная кубическая и гексагональная: кч=12, k=74%
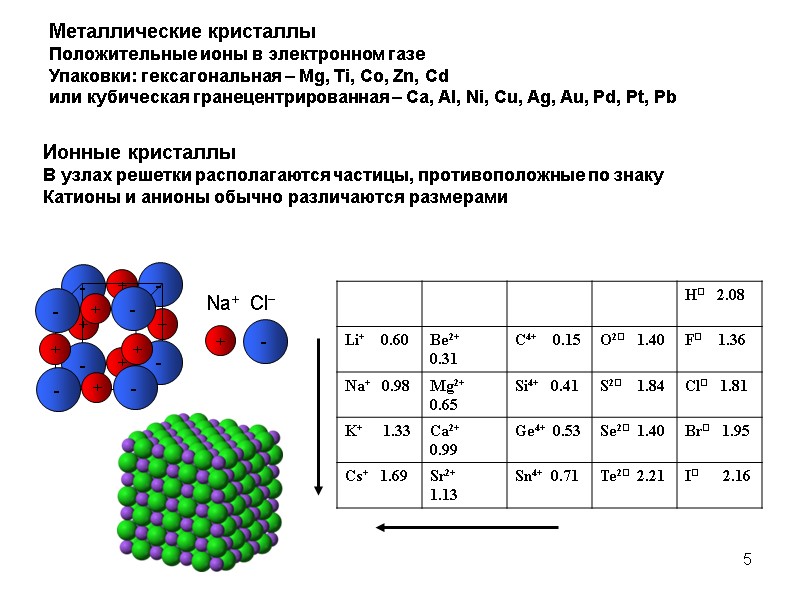
 5 Металлические кристаллы Положительные ионы в электронном газе Упаковки: гексагональная – Mg, Ti, Co, Zn, Cd или кубическая гранецентрированная – Ca, Al, Ni, Cu, Ag, Au, Pd, Pt, Pb Ионные кристаллы В узлах решетки располагаются частицы, противоположные по знаку Катионы и анионы обычно различаются размерами
5 Металлические кристаллы Положительные ионы в электронном газе Упаковки: гексагональная – Mg, Ti, Co, Zn, Cd или кубическая гранецентрированная – Ca, Al, Ni, Cu, Ag, Au, Pd, Pt, Pb Ионные кристаллы В узлах решетки располагаются частицы, противоположные по знаку Катионы и анионы обычно различаются размерами
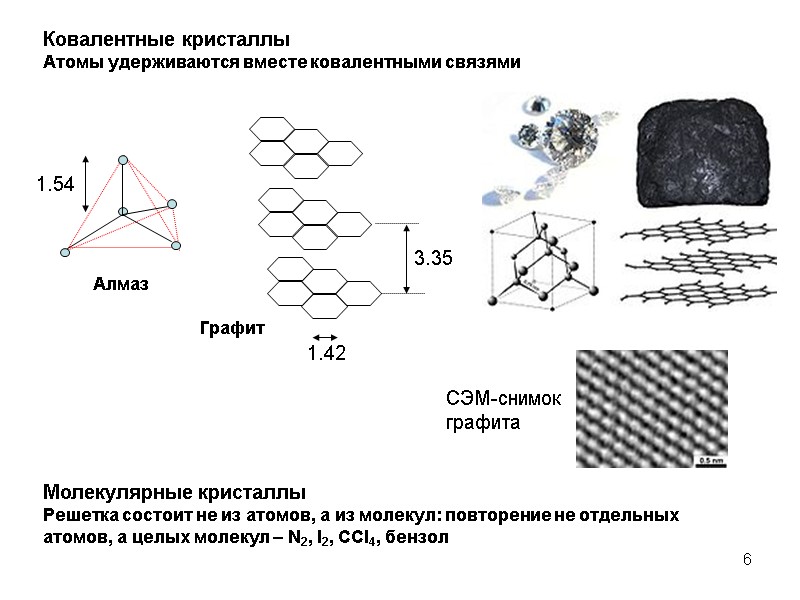
 6 Ковалентные кристаллы Атомы удерживаются вместе ковалентными связями Алмаз Графит Молекулярные кристаллы Решетка состоит не из атомов, а из молекул: повторение не отдельных атомов, а целых молекул – N2, I2, CCl4, бензол СЭМ-снимок графита
6 Ковалентные кристаллы Атомы удерживаются вместе ковалентными связями Алмаз Графит Молекулярные кристаллы Решетка состоит не из атомов, а из молекул: повторение не отдельных атомов, а целых молекул – N2, I2, CCl4, бензол СЭМ-снимок графита
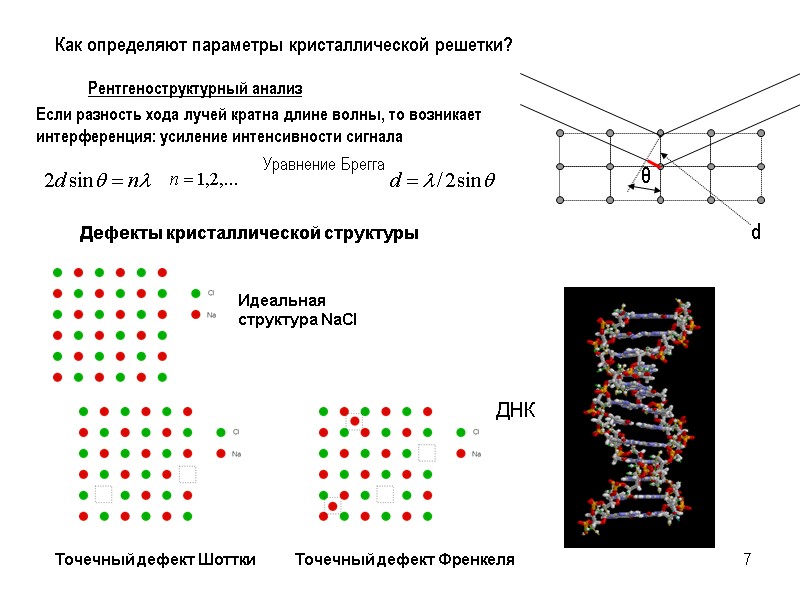
 7 Как определяют параметры кристаллической решетки? Рентгеноструктурный анализ ДНК Дефекты кристаллической структуры Идеальная структура NaCl Точечный дефект Шоттки Точечный дефект Френкеля
7 Как определяют параметры кристаллической решетки? Рентгеноструктурный анализ ДНК Дефекты кристаллической структуры Идеальная структура NaCl Точечный дефект Шоттки Точечный дефект Френкеля
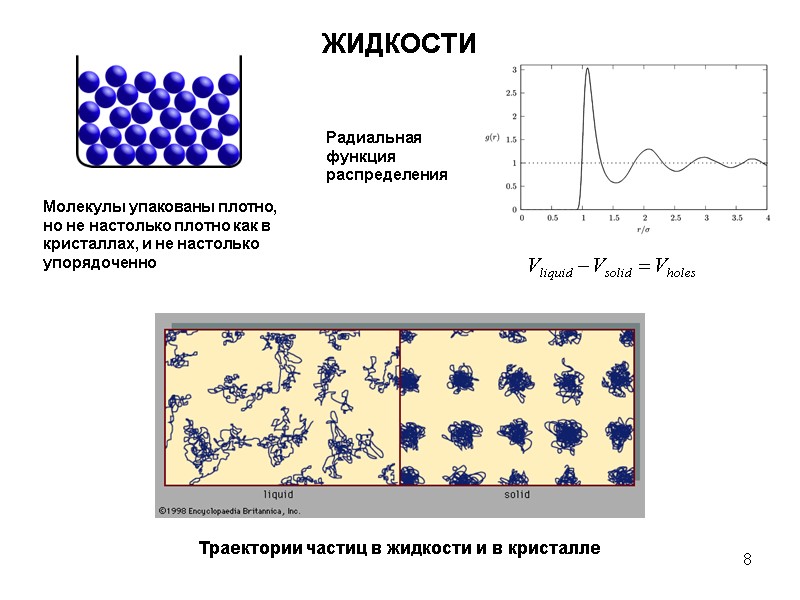
 8 ЖИДКОСТИ Радиальная функция распределения Траектории частиц в жидкости и в кристалле
8 ЖИДКОСТИ Радиальная функция распределения Траектории частиц в жидкости и в кристалле
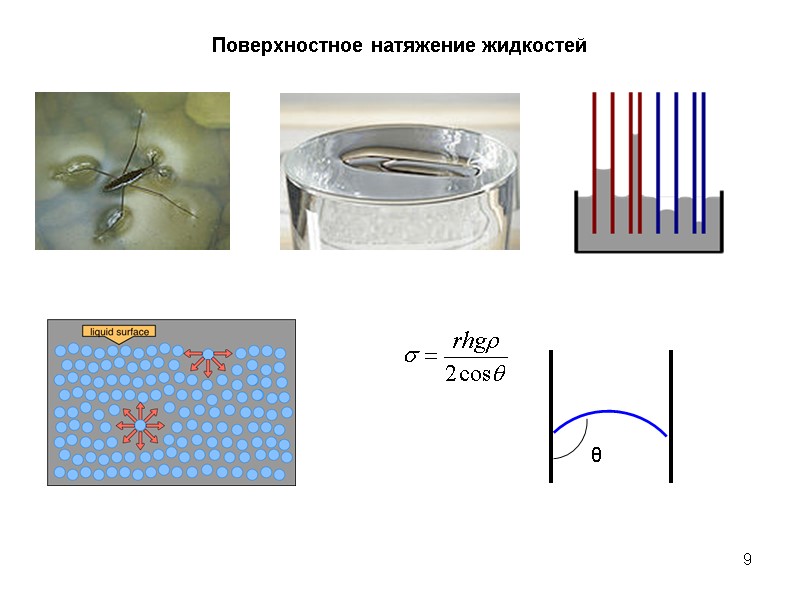
 9 Поверхностное натяжение жидкостей
9 Поверхностное натяжение жидкостей
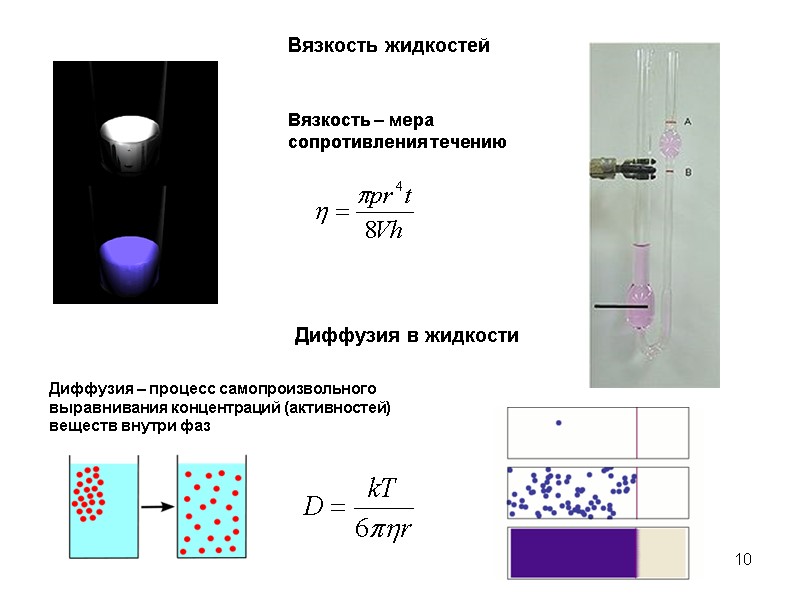
 10 Вязкость жидкостей Вязкость – мера сопротивления течению Диффузия в жидкости Диффузия – процесс самопроизвольного выравнивания концентраций (активностей) веществ внутри фаз
10 Вязкость жидкостей Вязкость – мера сопротивления течению Диффузия в жидкости Диффузия – процесс самопроизвольного выравнивания концентраций (активностей) веществ внутри фаз
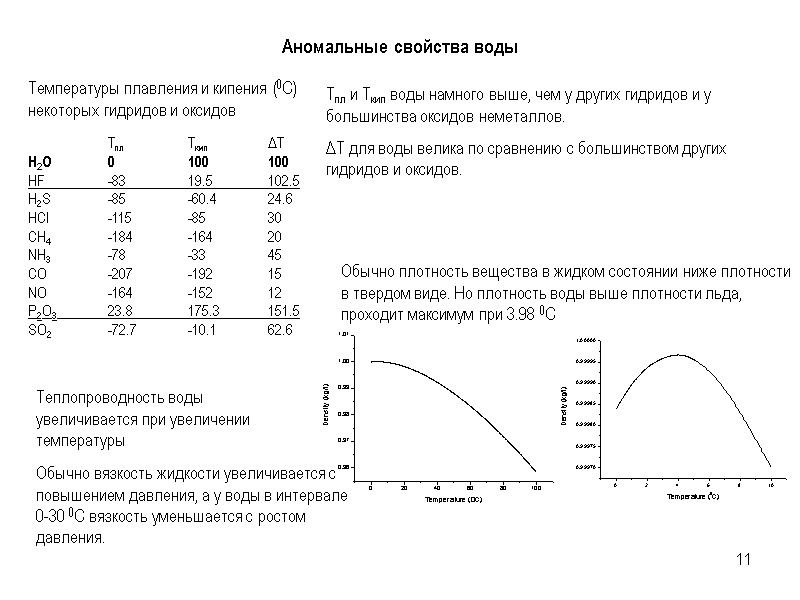
 11 Аномальные свойства воды Температуры плавления и кипения (0C) некоторых гидридов и оксидов Tпл Tкип ΔT H2O 0 100 100 HF -83 19.5 102.5 H2S -85 -60.4 24.6 HCl -115 -85 30 CH4 -184 -164 20 NH3 -78 -33 45 CO -207 -192 15 NO -164 -152 12 P2O3 23.8 175.3 151.5 SO2 -72.7 -10.1 62.6 Тпл и Ткип воды намного выше, чем у других гидридов и у большинства оксидов неметаллов. ΔТ для воды велика по сравнению с большинством других гидридов и оксидов. Теплопроводность воды увеличивается при увеличении температуры Обычно вязкость жидкости увеличивается с повышением давления, а у воды в интервале 0-30 0С вязкость уменьшается с ростом давления.
11 Аномальные свойства воды Температуры плавления и кипения (0C) некоторых гидридов и оксидов Tпл Tкип ΔT H2O 0 100 100 HF -83 19.5 102.5 H2S -85 -60.4 24.6 HCl -115 -85 30 CH4 -184 -164 20 NH3 -78 -33 45 CO -207 -192 15 NO -164 -152 12 P2O3 23.8 175.3 151.5 SO2 -72.7 -10.1 62.6 Тпл и Ткип воды намного выше, чем у других гидридов и у большинства оксидов неметаллов. ΔТ для воды велика по сравнению с большинством других гидридов и оксидов. Теплопроводность воды увеличивается при увеличении температуры Обычно вязкость жидкости увеличивается с повышением давления, а у воды в интервале 0-30 0С вязкость уменьшается с ростом давления.
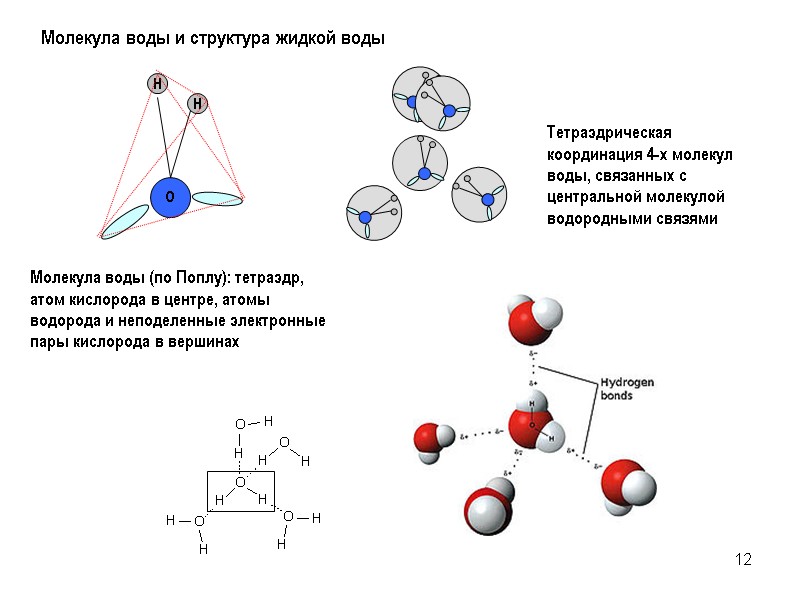
 12 Молекула воды и структура жидкой воды Тетраэдрическая координация 4-х молекул воды, связанных с центральной молекулой водородными связями Молекула воды (по Поплу): тетраэдр, атом кислорода в центре, атомы водорода и неподеленные электронные пары кислорода в вершинах
12 Молекула воды и структура жидкой воды Тетраэдрическая координация 4-х молекул воды, связанных с центральной молекулой водородными связями Молекула воды (по Поплу): тетраэдр, атом кислорода в центре, атомы водорода и неподеленные электронные пары кислорода в вершинах
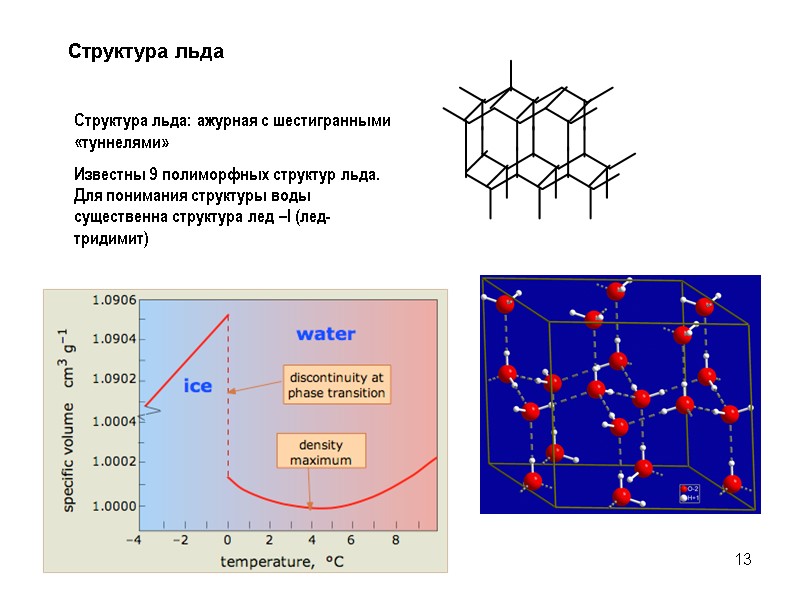
 13 Структура льда: ажурная с шестигранными «туннелями» Известны 9 полиморфных структур льда. Для понимания структуры воды существенна структура лед –I (лед-тридимит) Структура льда
13 Структура льда: ажурная с шестигранными «туннелями» Известны 9 полиморфных структур льда. Для понимания структуры воды существенна структура лед –I (лед-тридимит) Структура льда
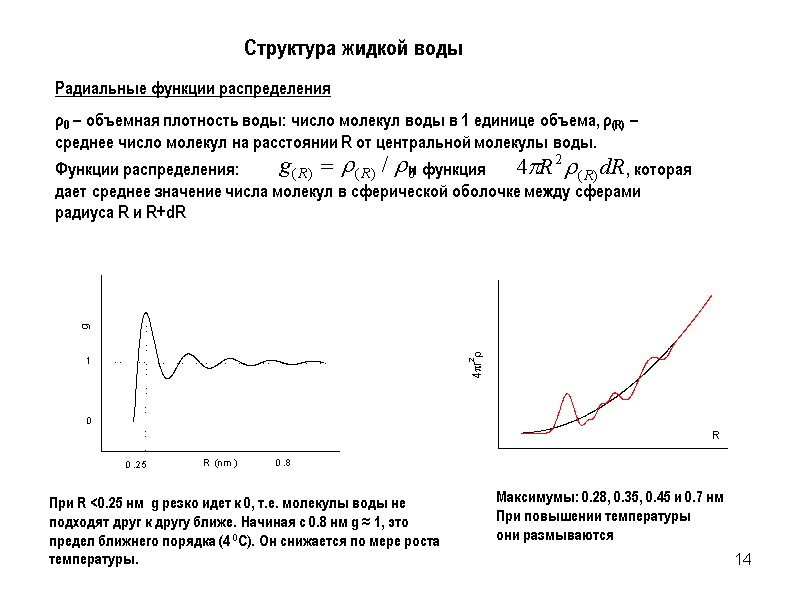
 14 Структура жидкой воды Радиальные функции распределения ρ0 – объемная плотность воды: число молекул воды в 1 единице объема, ρ(R) – среднее число молекул на расстоянии R от центральной молекулы воды. Функции распределения: и функция , которая дает среднее значение числа молекул в сферической оболочке между сферами радиуса R и R+dR При R <0.25 нм g резко идет к 0, т.е. молекулы воды не подходят друг к другу ближе. Начиная с 0.8 нм g ≈ 1, это предел ближнего порядка (4 0С). Он снижается по мере роста температуры. Максимумы: 0.28, 0.35, 0.45 и 0.7 нм При повышении температуры они размываются
14 Структура жидкой воды Радиальные функции распределения ρ0 – объемная плотность воды: число молекул воды в 1 единице объема, ρ(R) – среднее число молекул на расстоянии R от центральной молекулы воды. Функции распределения: и функция , которая дает среднее значение числа молекул в сферической оболочке между сферами радиуса R и R+dR При R <0.25 нм g резко идет к 0, т.е. молекулы воды не подходят друг к другу ближе. Начиная с 0.8 нм g ≈ 1, это предел ближнего порядка (4 0С). Он снижается по мере роста температуры. Максимумы: 0.28, 0.35, 0.45 и 0.7 нм При повышении температуры они размываются
 15 Представления о структуре жидкой воды Трехструктурная модель Бернала и Фаулера: Cосуществуют 3 структуры: вода I со структурой лед- I, вода II со структурой кварца (более плотной) и плотно упакованная кубическая вода III. В каждый момент времени какие-то области в выбранном объеме воды соответствуют структуре вода I, другие - вода II и третьи - вода III. Все три структуры находятся в динамическом равновесии и вода в целом гомогенна. Доля каждой из структур зависит от температуры. Структура вода I существует при температурах ниже 4 0С, структура II преобладает при температурах от 4 до 200 0С. При более высоких температурах доминирует плотная упаковка. Поэтому вода при температурах 0 – 4 0С плотнее льда, а при более высоких температурах начинает сказываться увеличение межмолекулярных расстояний и постепенная потеря ближнего порядка Двухструктурная модель Холла – т.к. уточненные данные показали, что максимум при 4 0С и выше находится при 0.45 нм (как во льду), а не 0.42 нм (как в кварце). 2 структуры - вода I со структурой лед- I и плотно упакованная вода. По мере размывания структуры лед- I плотность увеличивается до 4 0С , а при дальнейшем увеличении температуры плотность снижается. Модель «мерцающих кластеров» Френка и Вина: Кластеры тетраэдрически-координированных молекул воды плавают (при этом также распадясь и вновь образуясь) в плотной кубической структуре.
15 Представления о структуре жидкой воды Трехструктурная модель Бернала и Фаулера: Cосуществуют 3 структуры: вода I со структурой лед- I, вода II со структурой кварца (более плотной) и плотно упакованная кубическая вода III. В каждый момент времени какие-то области в выбранном объеме воды соответствуют структуре вода I, другие - вода II и третьи - вода III. Все три структуры находятся в динамическом равновесии и вода в целом гомогенна. Доля каждой из структур зависит от температуры. Структура вода I существует при температурах ниже 4 0С, структура II преобладает при температурах от 4 до 200 0С. При более высоких температурах доминирует плотная упаковка. Поэтому вода при температурах 0 – 4 0С плотнее льда, а при более высоких температурах начинает сказываться увеличение межмолекулярных расстояний и постепенная потеря ближнего порядка Двухструктурная модель Холла – т.к. уточненные данные показали, что максимум при 4 0С и выше находится при 0.45 нм (как во льду), а не 0.42 нм (как в кварце). 2 структуры - вода I со структурой лед- I и плотно упакованная вода. По мере размывания структуры лед- I плотность увеличивается до 4 0С , а при дальнейшем увеличении температуры плотность снижается. Модель «мерцающих кластеров» Френка и Вина: Кластеры тетраэдрически-координированных молекул воды плавают (при этом также распадясь и вновь образуясь) в плотной кубической структуре.
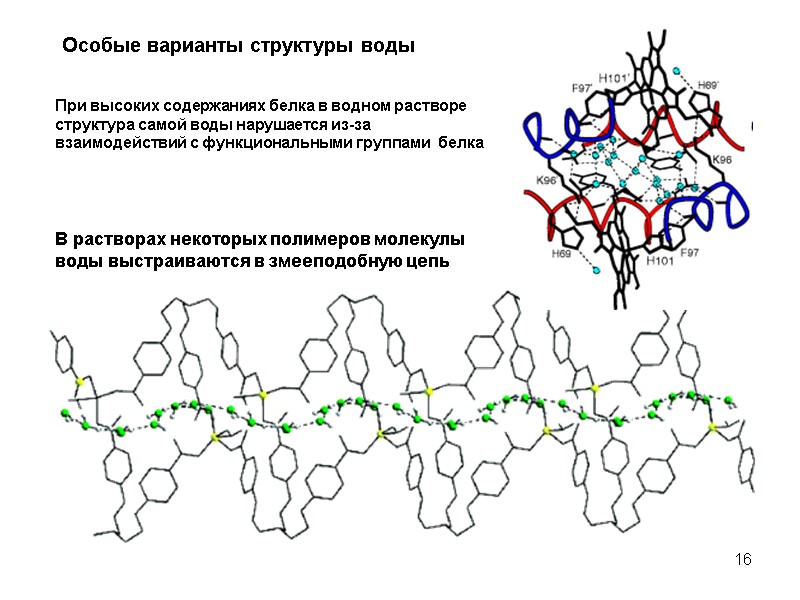
 16 Особые варианты структуры воды При высоких содержаниях белка в водном растворе структура самой воды нарушается из-за взаимодействий с функциональными группами белка В растворах некоторых полимеров молекулы воды выстраиваются в змееподобную цепь
16 Особые варианты структуры воды При высоких содержаниях белка в водном растворе структура самой воды нарушается из-за взаимодействий с функциональными группами белка В растворах некоторых полимеров молекулы воды выстраиваются в змееподобную цепь
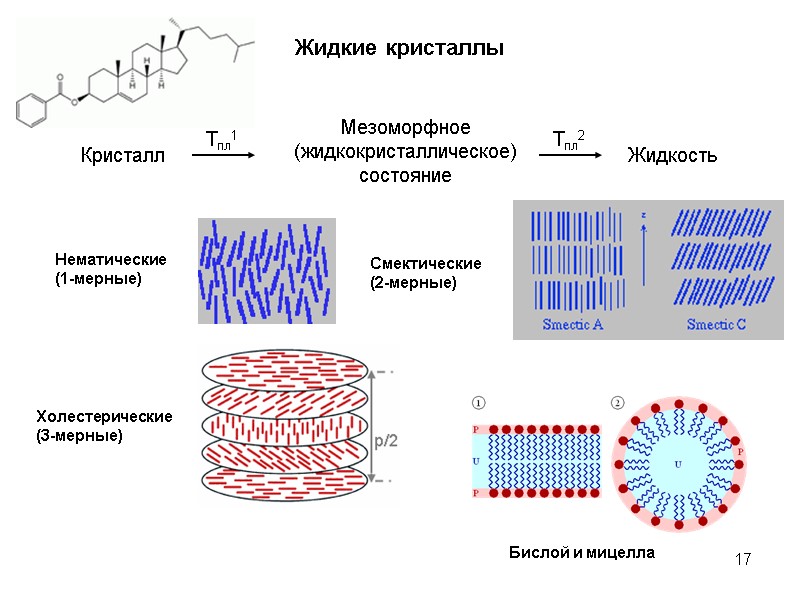
 17 Жидкие кристаллы Нематические (1-мерные) Смектические (2-мерные) Холестерические (3-мерные) Бислой и мицелла
17 Жидкие кристаллы Нематические (1-мерные) Смектические (2-мерные) Холестерические (3-мерные) Бислой и мицелла
 18 Термодинамика – область науки, связанная с переходами энергии из одной формы в другую Термодинамика Общая Техническая Химическая Классическая термодинамика имеет дело с макроскопическими объектами, в условиях «обычных» пространств, скоростей и времени. Термодинамика оперирует только начальными и конечными состояниями, ничего не говоря о механизме процессов. В классической термодинамике вообще отсутствует время как параметр. Вместе с тем, в неявном виде время всегда подразумевается т.к. обсуждаются медленные и быстрые процессы. Само понятие «состояния системы» подразумевает что состояние этой ее части такое-то, другой – такое-то, когда – в данный момент времени. Химическая термодинамика
18 Термодинамика – область науки, связанная с переходами энергии из одной формы в другую Термодинамика Общая Техническая Химическая Классическая термодинамика имеет дело с макроскопическими объектами, в условиях «обычных» пространств, скоростей и времени. Термодинамика оперирует только начальными и конечными состояниями, ничего не говоря о механизме процессов. В классической термодинамике вообще отсутствует время как параметр. Вместе с тем, в неявном виде время всегда подразумевается т.к. обсуждаются медленные и быстрые процессы. Само понятие «состояния системы» подразумевает что состояние этой ее части такое-то, другой – такое-то, когда – в данный момент времени. Химическая термодинамика
 19 Понятие температуры («нулевой» закон термодинамики) Температура – интуитивно «понятный и простой» параметр системы, на самом деле – нечто очень сложное. В сущности, температура некоего тела – это мера средней кинетической энергии молекул, составляющих данное тело. Способов прямого определения температуры не существует. Температура системы может быть измерена только с помощью какой-то другой системы, причем эти две системы должны достичь состояния теплового равновесия, т.е. переход тепла от более горячей системы к более холодной на момент измерения должен прекратиться. Формализация понятия температуры основана на экспериментальных законах, установленных для газов, находящихся при небольших давлениях и температурах: pV=RT, т.е. T=pV/R. Идеальный газ – это газ, для которого выполняется соотношение pV=RT. Для реальных систем можно записать: fA(pA,VA)=fB(pB,VB), где f(p,V) – эмпирическая температура. Важнейшие параметры: объем, давление, температура. Как их измерять? Давление и объем можно измерить непосредственно, а температуру?
19 Понятие температуры («нулевой» закон термодинамики) Температура – интуитивно «понятный и простой» параметр системы, на самом деле – нечто очень сложное. В сущности, температура некоего тела – это мера средней кинетической энергии молекул, составляющих данное тело. Способов прямого определения температуры не существует. Температура системы может быть измерена только с помощью какой-то другой системы, причем эти две системы должны достичь состояния теплового равновесия, т.е. переход тепла от более горячей системы к более холодной на момент измерения должен прекратиться. Формализация понятия температуры основана на экспериментальных законах, установленных для газов, находящихся при небольших давлениях и температурах: pV=RT, т.е. T=pV/R. Идеальный газ – это газ, для которого выполняется соотношение pV=RT. Для реальных систем можно записать: fA(pA,VA)=fB(pB,VB), где f(p,V) – эмпирическая температура. Важнейшие параметры: объем, давление, температура. Как их измерять? Давление и объем можно измерить непосредственно, а температуру?
 20 Температура системы может быть измерена лишь по изменению какого-либо свойства второй системы, находящейся с первой в тепловом равновесии. Это свойство должно поддаваться измерению, например - объем, электрическое сопротивление, светоотражение, светорассеяние. Эмпирические температурные шкалы Произвольный выбор: размер градуса, положение нуля Необходимое допущение: линейность изменения измеряемого свойства по мере изменения температуры Опорные точки: экспериментально воспроизводимые явления, происходящие с неким стандартным веществом при неких стандартных условиях. Шкала Цельсия: стандартное вещество: чистая вода, стандартные условия: давление равно 1 атм., опорные точки: плавление/кристаллизация – 0 0С, испарение/конденсация – 100 0С. Измеряемое свойство: объем ртути, находящейся в тепловом равновесии с телом (высота ртутного столбика).
20 Температура системы может быть измерена лишь по изменению какого-либо свойства второй системы, находящейся с первой в тепловом равновесии. Это свойство должно поддаваться измерению, например - объем, электрическое сопротивление, светоотражение, светорассеяние. Эмпирические температурные шкалы Произвольный выбор: размер градуса, положение нуля Необходимое допущение: линейность изменения измеряемого свойства по мере изменения температуры Опорные точки: экспериментально воспроизводимые явления, происходящие с неким стандартным веществом при неких стандартных условиях. Шкала Цельсия: стандартное вещество: чистая вода, стандартные условия: давление равно 1 атм., опорные точки: плавление/кристаллизация – 0 0С, испарение/конденсация – 100 0С. Измеряемое свойство: объем ртути, находящейся в тепловом равновесии с телом (высота ртутного столбика).
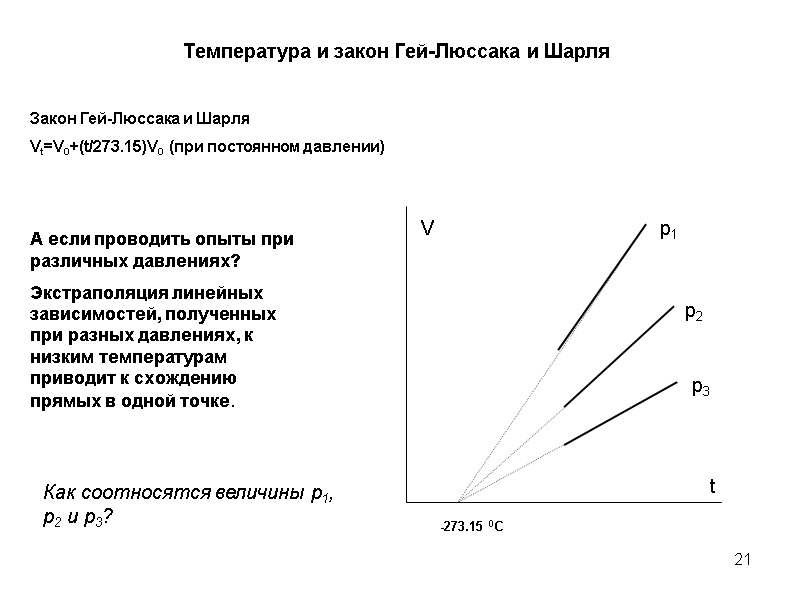
 21 Температура и закон Гей-Люссака и Шарля Закон Гей-Люссака и Шарля Vt=V0+(t/273.15)V0 (при постоянном давлении) А если проводить опыты при различных давлениях? Экстраполяция линейных зависимостей, полученных при разных давлениях, к низким температурам приводит к схождению прямых в одной точке. Как соотносятся величины p1, p2 и p3?
21 Температура и закон Гей-Люссака и Шарля Закон Гей-Люссака и Шарля Vt=V0+(t/273.15)V0 (при постоянном давлении) А если проводить опыты при различных давлениях? Экстраполяция линейных зависимостей, полученных при разных давлениях, к низким температурам приводит к схождению прямых в одной точке. Как соотносятся величины p1, p2 и p3?
 22 Соотношение между шкалами Цельсия, Кельвина и Фаренгейта Шкала Цельсия Переход лед/жидкая вода при 1 атм. – 00, переход жидкая вода/пар – 1000 Шкала Кельвина: Переход лед/жидкая вода при 1 атм. – 273.150, переход жидкая вода/пар – 373.150 Шкала Фаренгейта: Переход лед/жидкая вода при 1 атм. – 320, переход жидкая вода/пар – 2120
22 Соотношение между шкалами Цельсия, Кельвина и Фаренгейта Шкала Цельсия Переход лед/жидкая вода при 1 атм. – 00, переход жидкая вода/пар – 1000 Шкала Кельвина: Переход лед/жидкая вода при 1 атм. – 273.150, переход жидкая вода/пар – 373.150 Шкала Фаренгейта: Переход лед/жидкая вода при 1 атм. – 320, переход жидкая вода/пар – 2120
 23 Функции состояния Функция состояния это такая действительная непрерывная функция, которая обладает следующими свойствами Изменение функции состояния с изменением аргументов зависит лишь от начальных и конечных значений аргументов, но не зависит от их промежуточных значений 2. Для функции состояния круговой интеграл равен нулю: 3. От всякой ФС может может быть взят полный дифференциал:
23 Функции состояния Функция состояния это такая действительная непрерывная функция, которая обладает следующими свойствами Изменение функции состояния с изменением аргументов зависит лишь от начальных и конечных значений аргументов, но не зависит от их промежуточных значений 2. Для функции состояния круговой интеграл равен нулю: 3. От всякой ФС может может быть взят полный дифференциал:
 24 1-й закон (1-е начало) термодинамики – закон сохранения энергии Энергия – функция состояния системы, такая, что ее изменение при переходе системы из состояния 1 в состояние 2 равно работе, затраченной для осуществления этого перехода или произведенной системой при этом переходе. Энергия: потенциальная, кинетическая, тепловая, электрическая, и т.д. Сохранение энергии – закон, следующий из всего опыта человечества. Радиоактивный распад: кажется, что энергия распада возникает из ничего. На самом деле масса немного уменьшается: E=mc2. Термодинамика рассматривает прежде всего внутреннюю энергию и тепловую энергию (теплоту). Внутренняя энергия системы – совокупность всех видов энергии всех частиц, составляющих систему. Однако внутренняя энергия не зависит от положения системы в пространстве (в отличие от потенциальной энергии). Различаются или нет величины теплоты, полученной при сжигании одного и того же количества дров на 1-м и на 101-м этаже небоскреба?
24 1-й закон (1-е начало) термодинамики – закон сохранения энергии Энергия – функция состояния системы, такая, что ее изменение при переходе системы из состояния 1 в состояние 2 равно работе, затраченной для осуществления этого перехода или произведенной системой при этом переходе. Энергия: потенциальная, кинетическая, тепловая, электрическая, и т.д. Сохранение энергии – закон, следующий из всего опыта человечества. Радиоактивный распад: кажется, что энергия распада возникает из ничего. На самом деле масса немного уменьшается: E=mc2. Термодинамика рассматривает прежде всего внутреннюю энергию и тепловую энергию (теплоту). Внутренняя энергия системы – совокупность всех видов энергии всех частиц, составляющих систему. Однако внутренняя энергия не зависит от положения системы в пространстве (в отличие от потенциальной энергии). Различаются или нет величины теплоты, полученной при сжигании одного и того же количества дров на 1-м и на 101-м этаже небоскреба?
 25 Формулировки 1-го начала термодинамики В изолированной системе общее количество энергии постоянно, несмотря на все превращения одного вида энергии в другой, которые могут происходить в этой системе. Изменение энергии системы в данный промежуток времени равно количеству энергии, поступающей в систему из окружающей среды (или уходящей из системы в окружающую среду) в тот же промежуток времени. Вечный двигатель 1-го рода невозможен. Вечный двигатель 1-го рода – это гипотетическая машина, которая, получив некий «начальный толчок», далее может совершать работу бесконечно долго без пополнения запаса энергии. Внутренняя энергия системы – совокупность всех видов энергии всех частиц, составляющих систему. Что, в частности, входит во внутреннюю энергию? – это кинетическая энергия частиц, энергия их взаимодействий (специфических и неспецифических), внутримолекулярная энергия, внутриатомная энергия, внутриядерная, … В зависимости от конкретной ситуации «подключаются» те или иные виды энергии. Если просто нагреть газ, причем не слишком сильно, изменится только кинетическая энергия его молекул. Но можно дойти до E=mc2.
25 Формулировки 1-го начала термодинамики В изолированной системе общее количество энергии постоянно, несмотря на все превращения одного вида энергии в другой, которые могут происходить в этой системе. Изменение энергии системы в данный промежуток времени равно количеству энергии, поступающей в систему из окружающей среды (или уходящей из системы в окружающую среду) в тот же промежуток времени. Вечный двигатель 1-го рода невозможен. Вечный двигатель 1-го рода – это гипотетическая машина, которая, получив некий «начальный толчок», далее может совершать работу бесконечно долго без пополнения запаса энергии. Внутренняя энергия системы – совокупность всех видов энергии всех частиц, составляющих систему. Что, в частности, входит во внутреннюю энергию? – это кинетическая энергия частиц, энергия их взаимодействий (специфических и неспецифических), внутримолекулярная энергия, внутриатомная энергия, внутриядерная, … В зависимости от конкретной ситуации «подключаются» те или иные виды энергии. Если просто нагреть газ, причем не слишком сильно, изменится только кинетическая энергия его молекул. Но можно дойти до E=mc2.
 26 Внутренняя энергия как функция состояния Пусть U – внутренняя энергия системы, dU – ее бесконечно малое изменение. Бесконечно малое количество тепла, поглощаемое или выделяемое системой – δQ. Бесконечно малая механическая работа (расширение или сжатие системы) совершаемая при этом: δA. Тогда dU= δQ-δA. Если δA=0, то dU= δQ – т.е. изменение внутренней энергии системы в процессе, когда не совершается работа, равно теплоте, выделенной или полученной системой. Теплота – мера передачи энергии путем теплопроводности или излучения, без непосредственного совершения работы. Работа и теплота зависят от пути процесса, а не только от начального и конечного состояния систем. Работа и теплота при переходе из состояния a в состояние b по пути c и по пути d не одинаковы. Поэтому и в круговом процессе , . Однако, как показали опыты Джоуля: Т.е. работа и теплота циклического процесса одинаковы, хотя и не равны нулю.
26 Внутренняя энергия как функция состояния Пусть U – внутренняя энергия системы, dU – ее бесконечно малое изменение. Бесконечно малое количество тепла, поглощаемое или выделяемое системой – δQ. Бесконечно малая механическая работа (расширение или сжатие системы) совершаемая при этом: δA. Тогда dU= δQ-δA. Если δA=0, то dU= δQ – т.е. изменение внутренней энергии системы в процессе, когда не совершается работа, равно теплоте, выделенной или полученной системой. Теплота – мера передачи энергии путем теплопроводности или излучения, без непосредственного совершения работы. Работа и теплота зависят от пути процесса, а не только от начального и конечного состояния систем. Работа и теплота при переходе из состояния a в состояние b по пути c и по пути d не одинаковы. Поэтому и в круговом процессе , . Однако, как показали опыты Джоуля: Т.е. работа и теплота циклического процесса одинаковы, хотя и не равны нулю.
 27 Таким образом, внутренняя энергия – функция состояния системы, такая, что увеличение внутренней энергии системы равно разности тепла, переданного системе от окружающей среды и работы, совершенной системой над окружающей средой. А как обстоит дело с внутренней энергией? Снова рассмотрим тот же круговой процесс. Учтем, что dU= δQ-δA. Следовательно, изменение внутренней энергии в круговом процессе равно нулю. Выделим произвольные точки a, b, c, d. Изменение энергии в круговом процессе равно сумме изменения энергии системы при переходе из a в b через с и обратно через d, и эта сумма равна нулю:
27 Таким образом, внутренняя энергия – функция состояния системы, такая, что увеличение внутренней энергии системы равно разности тепла, переданного системе от окружающей среды и работы, совершенной системой над окружающей средой. А как обстоит дело с внутренней энергией? Снова рассмотрим тот же круговой процесс. Учтем, что dU= δQ-δA. Следовательно, изменение внутренней энергии в круговом процессе равно нулю. Выделим произвольные точки a, b, c, d. Изменение энергии в круговом процессе равно сумме изменения энергии системы при переходе из a в b через с и обратно через d, и эта сумма равна нулю:
 28 Пример: изменение внутренней энергии идеального газа при его расширении. Почему снова об идеальном газе? Идеальный газ – математически простая система (подчиняется простому уравнению состояния: pV=nRT), но на примере идеального газа можно продемонстрировать (в том или ином приближении) свойства реальных систем. 1. Изотермическое расширение, т.е. T=Const pV=Const’. При T=Const кинетическая энергия газа постоянна, а для идеального газа вся внутренняя энергия – это кинетическая т.к. молекулы не взаимодействуют. Поэтому ΔU=0 и Q=-A. Однако, расширение может происходить несколькими способами. 1.1. Расширение в вакуум – работа не производится, A=0 Q=0. Газ Вакуум
28 Пример: изменение внутренней энергии идеального газа при его расширении. Почему снова об идеальном газе? Идеальный газ – математически простая система (подчиняется простому уравнению состояния: pV=nRT), но на примере идеального газа можно продемонстрировать (в том или ином приближении) свойства реальных систем. 1. Изотермическое расширение, т.е. T=Const pV=Const’. При T=Const кинетическая энергия газа постоянна, а для идеального газа вся внутренняя энергия – это кинетическая т.к. молекулы не взаимодействуют. Поэтому ΔU=0 и Q=-A. Однако, расширение может происходить несколькими способами. 1.1. Расширение в вакуум – работа не производится, A=0 Q=0. Газ Вакуум
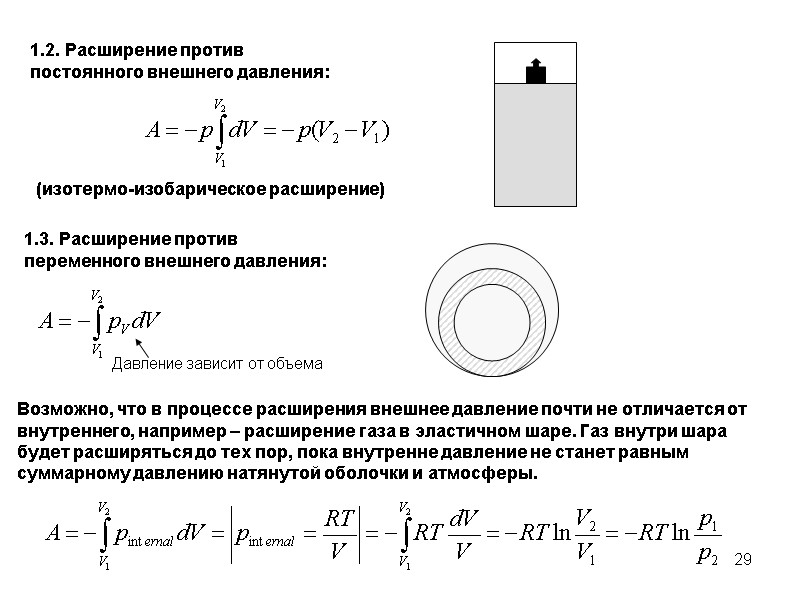
 29 1.2. Расширение против постоянного внешнего давления: 1.3. Расширение против переменного внешнего давления: (изотермо-изобарическое расширение) Давление зависит от объема Возможно, что в процессе расширения внешнее давление почти не отличается от внутреннего, например – расширение газа в эластичном шаре. Газ внутри шара будет расширяться до тех пор, пока внутренне давление не станет равным суммарному давлению натянутой оболочки и атмосферы.
29 1.2. Расширение против постоянного внешнего давления: 1.3. Расширение против переменного внешнего давления: (изотермо-изобарическое расширение) Давление зависит от объема Возможно, что в процессе расширения внешнее давление почти не отличается от внутреннего, например – расширение газа в эластичном шаре. Газ внутри шара будет расширяться до тех пор, пока внутренне давление не станет равным суммарному давлению натянутой оболочки и атмосферы.
 30 Энтальпия Рассмотрим изобарный процесс (p=Const), работа – только расширение. Но система – произвольная, не только идеальный газ. Изменение внутренней энергии ΔU=Q+pΔV, U2-U1=Q+p(V2-V1) Q=(U2+pV2)-(U1+pV1) Таким образом, поглощенная (выделенная) теплота Q равна разности двух величин, которые сами по себе являются комбинациями функций состояния. Есть смысл ввести новую функцию состояния – энтальпию: H=U+pV Если совершается только механическая работа, то поглощенная (выделенная) системой теплота равна изменению энтальпии. Изменение энтальпии в широком интервале Т может быть сложной функцией из-за фазовых переходов. Например, для воды при нагреве от 0 до 400 K:
30 Энтальпия Рассмотрим изобарный процесс (p=Const), работа – только расширение. Но система – произвольная, не только идеальный газ. Изменение внутренней энергии ΔU=Q+pΔV, U2-U1=Q+p(V2-V1) Q=(U2+pV2)-(U1+pV1) Таким образом, поглощенная (выделенная) теплота Q равна разности двух величин, которые сами по себе являются комбинациями функций состояния. Есть смысл ввести новую функцию состояния – энтальпию: H=U+pV Если совершается только механическая работа, то поглощенная (выделенная) системой теплота равна изменению энтальпии. Изменение энтальпии в широком интервале Т может быть сложной функцией из-за фазовых переходов. Например, для воды при нагреве от 0 до 400 K:
 31 Закон Гесса Теплота, выделяемая в химическом процессе при постоянном давлении, не зависит от количества стадий и способа проведения процесса. Если тепло выделяется, то процесс наз. экзотермическим, если поглощается – эндотермическим. Этот закон – прямое следствие того обстоятельства, что энтальпия – функция состояния. Энтальпия образования вещества: тепло, поглощенное или выделенное в процессе синтеза 1 моля вещества из его элементов при стандартном состоянии. Стандартное состояние элемента – его наиболее устойчивая форма при 25 0С и p=1 атм. Например, для Br2ж ΔHобр0=0, а для Br2г ΔHобр0=+7.4 ккал/моль. Выбор стандартного состояния достаточно однозначен для всех элементов, кроме углерода: алмаз и графит. Термохимия Закон Лавуазье-Лапласа Теплота, необходимая для разложения химического соединения, равна теплоте, выделяемой при его образовании
31 Закон Гесса Теплота, выделяемая в химическом процессе при постоянном давлении, не зависит от количества стадий и способа проведения процесса. Если тепло выделяется, то процесс наз. экзотермическим, если поглощается – эндотермическим. Этот закон – прямое следствие того обстоятельства, что энтальпия – функция состояния. Энтальпия образования вещества: тепло, поглощенное или выделенное в процессе синтеза 1 моля вещества из его элементов при стандартном состоянии. Стандартное состояние элемента – его наиболее устойчивая форма при 25 0С и p=1 атм. Например, для Br2ж ΔHобр0=0, а для Br2г ΔHобр0=+7.4 ккал/моль. Выбор стандартного состояния достаточно однозначен для всех элементов, кроме углерода: алмаз и графит. Термохимия Закон Лавуазье-Лапласа Теплота, необходимая для разложения химического соединения, равна теплоте, выделяемой при его образовании
 32 Энтальпия химической реакции (при стандартных условиях) определяется разностью суммарных стандартных энтальпий образования продуктов и реагентов (исходных веществ): Энтальпии многих процессов можно измерить непосредственно (прямой калориметрией). Например, нам известны стандартные энтальпии след. реакций: Csol+O2gas CO2gas ΔH0=-94.1 ккал/моль COgas+(1/2)O2gas CO2gas ΔH0=-67.7 ккал/моль Вычтем нижнее уравнение из верхнего, и второе значение ΔH0 из первого, получим: Csol+(1/2)O2gas COgas ΔH0=-26.4 ккал/моль Мы не просто «сэкономили» эксперимент, мы получили (пользуясь законом Гесса) энтальпию реакции, которую невозможно провести экспериментально! В реальном опыте часть углерода неизбежно окислилась бы до CO2, а не только до CO.
32 Энтальпия химической реакции (при стандартных условиях) определяется разностью суммарных стандартных энтальпий образования продуктов и реагентов (исходных веществ): Энтальпии многих процессов можно измерить непосредственно (прямой калориметрией). Например, нам известны стандартные энтальпии след. реакций: Csol+O2gas CO2gas ΔH0=-94.1 ккал/моль COgas+(1/2)O2gas CO2gas ΔH0=-67.7 ккал/моль Вычтем нижнее уравнение из верхнего, и второе значение ΔH0 из первого, получим: Csol+(1/2)O2gas COgas ΔH0=-26.4 ккал/моль Мы не просто «сэкономили» эксперимент, мы получили (пользуясь законом Гесса) энтальпию реакции, которую невозможно провести экспериментально! В реальном опыте часть углерода неизбежно окислилась бы до CO2, а не только до CO.
 33 Зависимость теплоты химической реакции от температуры, уравнения Кирхгофа Мы знаем теплоты химических реакций при стандартных условиях (25 0С). Можно ли, не проводя опытов, теоретически рассчитать теплоты тех же реакций при других температурах? Теплота произвольного процесса, проходящего при постоянном объеме равна разности внутренних энергий исходного и конечного состояний, а при постоянном давлении – разности энтальпий. Таким образом, температурная зависимость тепловых эффектов может быть вычислена, если известна теплоемкость. Обратимся к произвольной химической реакции, в которой n видов исходных веществ A превращаются в k видов продуктов B: ν – стехиометрические коэффициенты.
33 Зависимость теплоты химической реакции от температуры, уравнения Кирхгофа Мы знаем теплоты химических реакций при стандартных условиях (25 0С). Можно ли, не проводя опытов, теоретически рассчитать теплоты тех же реакций при других температурах? Теплота произвольного процесса, проходящего при постоянном объеме равна разности внутренних энергий исходного и конечного состояний, а при постоянном давлении – разности энтальпий. Таким образом, температурная зависимость тепловых эффектов может быть вычислена, если известна теплоемкость. Обратимся к произвольной химической реакции, в которой n видов исходных веществ A превращаются в k видов продуктов B: ν – стехиометрические коэффициенты.
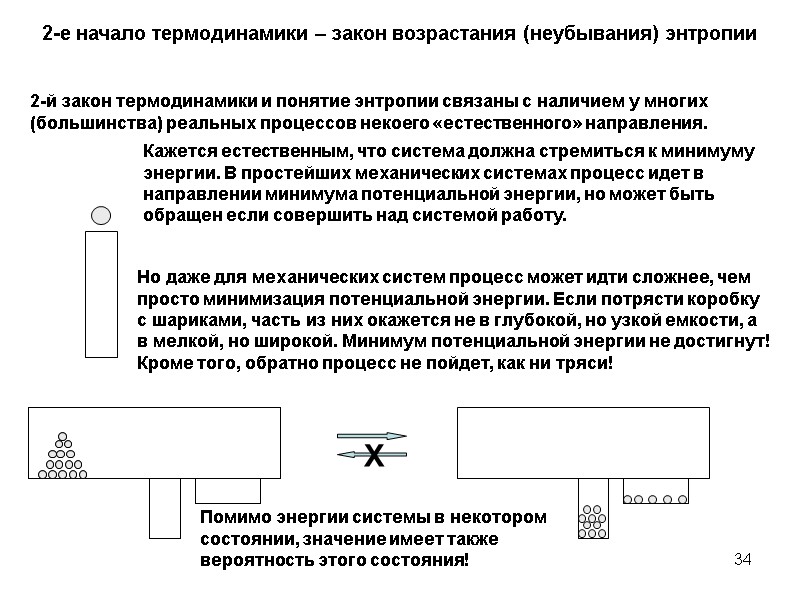
 34 2-е начало термодинамики – закон возрастания (неубывания) энтропии 2-й закон термодинамики и понятие энтропии связаны с наличием у многих (большинства) реальных процессов некоего «естественного» направления. Кажется естественным, что система должна стремиться к минимуму энергии. В простейших механических системах процесс идет в направлении минимума потенциальной энергии, но может быть обращен если совершить над системой работу. Но даже для механических систем процесс может идти сложнее, чем просто минимизация потенциальной энергии. Если потрясти коробку с шариками, часть из них окажется не в глубокой, но узкой емкости, а в мелкой, но широкой. Минимум потенциальной энергии не достигнут! Кроме того, обратно процесс не пойдет, как ни тряси! Помимо энергии системы в некотором состоянии, значение имеет также вероятность этого состояния!
34 2-е начало термодинамики – закон возрастания (неубывания) энтропии 2-й закон термодинамики и понятие энтропии связаны с наличием у многих (большинства) реальных процессов некоего «естественного» направления. Кажется естественным, что система должна стремиться к минимуму энергии. В простейших механических системах процесс идет в направлении минимума потенциальной энергии, но может быть обращен если совершить над системой работу. Но даже для механических систем процесс может идти сложнее, чем просто минимизация потенциальной энергии. Если потрясти коробку с шариками, часть из них окажется не в глубокой, но узкой емкости, а в мелкой, но широкой. Минимум потенциальной энергии не достигнут! Кроме того, обратно процесс не пойдет, как ни тряси! Помимо энергии системы в некотором состоянии, значение имеет также вероятность этого состояния!
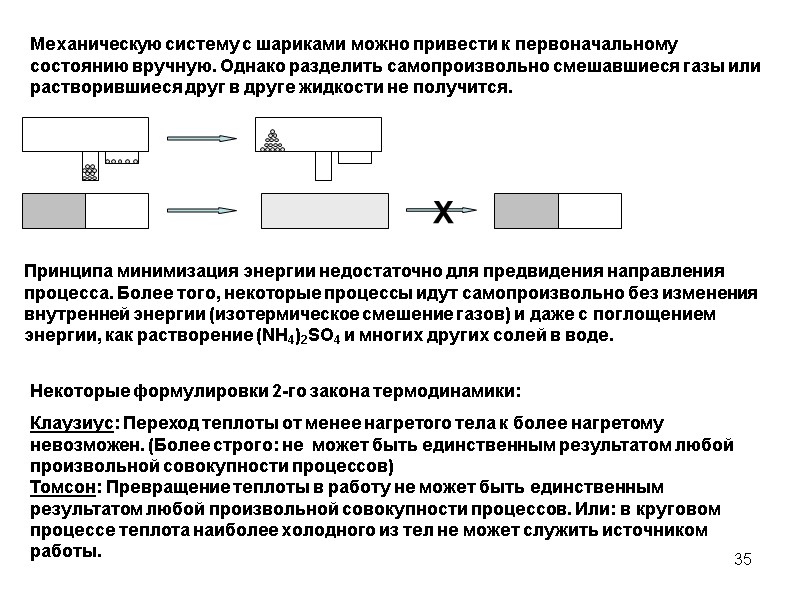
 35 Механическую систему с шариками можно привести к первоначальному состоянию вручную. Однако разделить самопроизвольно смешавшиеся газы или растворившиеся друг в друге жидкости не получится. Некоторые формулировки 2-го закона термодинамики: Клаузиус: Переход теплоты от менее нагретого тела к более нагретому невозможен. (Более строго: не может быть единственным результатом любой произвольной совокупности процессов) Томсон: Превращение теплоты в работу не может быть единственным результатом любой произвольной совокупности процессов. Или: в круговом процессе теплота наиболее холодного из тел не может служить источником работы. Принципа минимизация энергии недостаточно для предвидения направления процесса. Более того, некоторые процессы идут самопроизвольно без изменения внутренней энергии (изотермическое смешение газов) и даже с поглощением энергии, как растворение (NH4)2SO4 и многих других солей в воде.
35 Механическую систему с шариками можно привести к первоначальному состоянию вручную. Однако разделить самопроизвольно смешавшиеся газы или растворившиеся друг в друге жидкости не получится. Некоторые формулировки 2-го закона термодинамики: Клаузиус: Переход теплоты от менее нагретого тела к более нагретому невозможен. (Более строго: не может быть единственным результатом любой произвольной совокупности процессов) Томсон: Превращение теплоты в работу не может быть единственным результатом любой произвольной совокупности процессов. Или: в круговом процессе теплота наиболее холодного из тел не может служить источником работы. Принципа минимизация энергии недостаточно для предвидения направления процесса. Более того, некоторые процессы идут самопроизвольно без изменения внутренней энергии (изотермическое смешение газов) и даже с поглощением энергии, как растворение (NH4)2SO4 и многих других солей в воде.

