 1. Триклинная - все три оси симметрии имеют разную длину и расположены под разными углами. 2. Моноклинная - есть три оси симметрии: две образуют между собой прямой угол, а третья, перпендикулярная к одной из них, лежит в другой плоскости. 3. Ромбическая - при различной длине оси симметрии взаимно перпендикулярны. 4. Гексагональная - три одинаковой длины оси симметрии в одной плоскости образуют равные углы по 60°, четвертая ось им перпендикулярна. 5. Тригональная, или ромбоэдрическая – три оси одинаковой длины пересекаются под равными острыми углами. 6. Тетрагональная - все оси симметрии взаимно перпендикулярны, но только две равны. 7. Кубическая - все три оси симметрии равны между собой и пересекаются под прямым углом.
1. Триклинная - все три оси симметрии имеют разную длину и расположены под разными углами. 2. Моноклинная - есть три оси симметрии: две образуют между собой прямой угол, а третья, перпендикулярная к одной из них, лежит в другой плоскости. 3. Ромбическая - при различной длине оси симметрии взаимно перпендикулярны. 4. Гексагональная - три одинаковой длины оси симметрии в одной плоскости образуют равные углы по 60°, четвертая ось им перпендикулярна. 5. Тригональная, или ромбоэдрическая – три оси одинаковой длины пересекаются под равными острыми углами. 6. Тетрагональная - все оси симметрии взаимно перпендикулярны, но только две равны. 7. Кубическая - все три оси симметрии равны между собой и пересекаются под прямым углом.
 Некоторые вещества близкой химической природы образуют одинаковые кристаллические структуры. Такие вещества называются изоморфными.
Некоторые вещества близкой химической природы образуют одинаковые кристаллические структуры. Такие вещества называются изоморфными.
 n Многие соединения могут существовать в двух или более кристаллических структурах, устойчивых при различных температурах и давлениях. Такое явление называется полиморфизмом, а отвечающие им кристаллические структуры называют полиморфными формами.
n Многие соединения могут существовать в двух или более кристаллических структурах, устойчивых при различных температурах и давлениях. Такое явление называется полиморфизмом, а отвечающие им кристаллические структуры называют полиморфными формами.
 Так как монокристаллы анизотропны, то для того чтобы правильно разрезать полупроводниковый монокристалл на пластинки с одинаковыми свойствами, надо различать не только параллельные или непараллельные направления, но и симметричные и несимметричные, т. е. разбираться в теории симметрии кристаллов. А при определении электрических, механических и других свойств необходимо указывать расположение кристаллографических плоскостей и направления в кристаллах. Для этого используют индексы Миллера.
Так как монокристаллы анизотропны, то для того чтобы правильно разрезать полупроводниковый монокристалл на пластинки с одинаковыми свойствами, надо различать не только параллельные или непараллельные направления, но и симметричные и несимметричные, т. е. разбираться в теории симметрии кристаллов. А при определении электрических, механических и других свойств необходимо указывать расположение кристаллографических плоскостей и направления в кристаллах. Для этого используют индексы Миллера.
 Индексы Миллера n n В кубических кристаллах индексы (100) относятся к плоскости, параллельной осям Y и Z; индексы (010) - к плоскости, параллельной осям X и Z, а (001) - к плоскости, параллельной осям X и Y. В кристаллах с ортогональными осями эти плоскости вместе с тем перпендикулярны соответственно осям X, Y, Z.
Индексы Миллера n n В кубических кристаллах индексы (100) относятся к плоскости, параллельной осям Y и Z; индексы (010) - к плоскости, параллельной осям X и Z, а (001) - к плоскости, параллельной осям X и Y. В кристаллах с ортогональными осями эти плоскости вместе с тем перпендикулярны соответственно осям X, Y, Z.
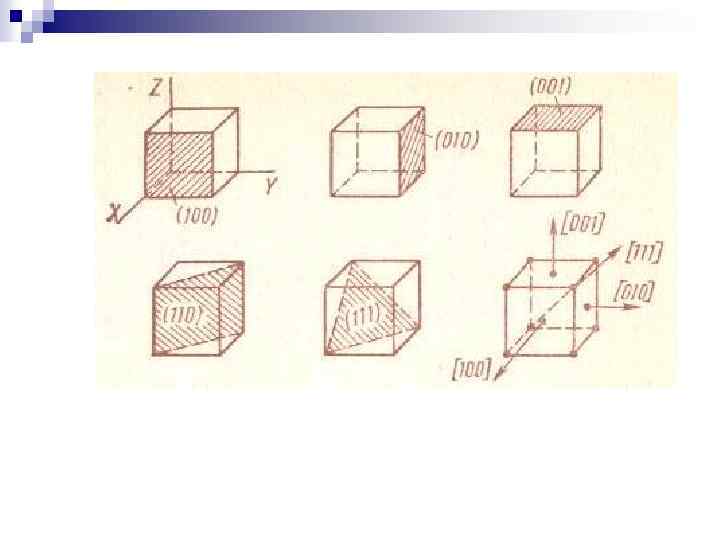
 n В кубических кристаллах эти направления перпендикулярны плоскости с теми же индексами. Положительное направление оси X обозначают [100], положительное направление оси Y - [010], отрицательное направление оси Z - [001], диагональ куба - [111] и т. д.
n В кубических кристаллах эти направления перпендикулярны плоскости с теми же индексами. Положительное направление оси X обозначают [100], положительное направление оси Y - [010], отрицательное направление оси Z - [001], диагональ куба - [111] и т. д.
 Нанокристаллы n n В промежуточной области между аморфным и кристаллическим состоянием вещества находится нанокристаллическое состояние. Нанокристаллы - это кристаллы размером от 0, 1 до 10 нм (в среднем 1 нм).
Нанокристаллы n n В промежуточной области между аморфным и кристаллическим состоянием вещества находится нанокристаллическое состояние. Нанокристаллы - это кристаллы размером от 0, 1 до 10 нм (в среднем 1 нм).
 n Характерной чертой нанокристаллических материалов является разупорядоченность (хаотичность) границ между кристаллами. В 1 см 3 число таких разнообразных границ может быть около 1019. ● - атомы нанокристалла; ○ - атомы, находящиеся на границах между нанокристаллами.
n Характерной чертой нанокристаллических материалов является разупорядоченность (хаотичность) границ между кристаллами. В 1 см 3 число таких разнообразных границ может быть около 1019. ● - атомы нанокристалла; ○ - атомы, находящиеся на границах между нанокристаллами.
 Лекция 2 Химическая связь и типы кристаллов.
Лекция 2 Химическая связь и типы кристаллов.
 План Химическая связь и типы кристаллов. n Дефекты в кристаллах. n Жидкие кристаллы. n
План Химическая связь и типы кристаллов. n Дефекты в кристаллах. n Жидкие кристаллы. n
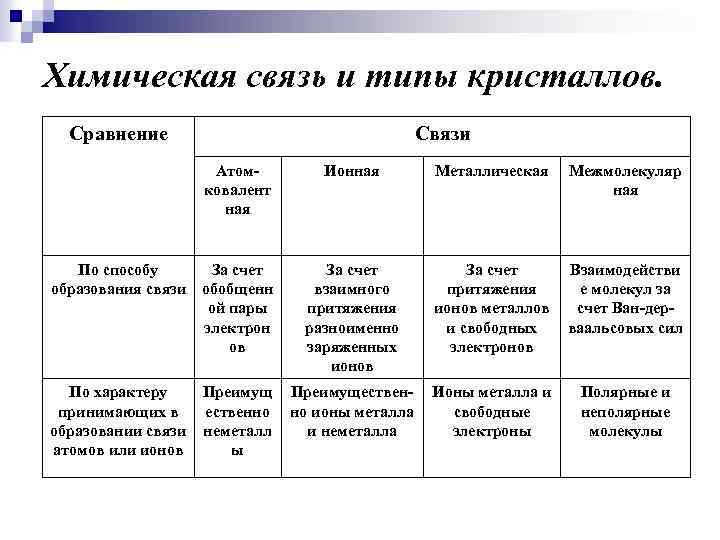 Химическая связь и типы кристаллов. Сравнение Связи Атомковалент ная Ионная Металлическая Межмолекуляр ная По способу образования связи За счет обобщенн ой пары электрон ов За счет взаимного притяжения разноименно заряженных ионов За счет притяжения ионов металлов и свободных электронов Взаимодействи е молекул за счет Ван-дерваальсовых сил По характеру принимающих в образовании связи атомов или ионов Преимущ ественно неметалл ы Преимущественно ионы металла и неметалла Ионы металла и свободные электроны Полярные и неполярные молекулы
Химическая связь и типы кристаллов. Сравнение Связи Атомковалент ная Ионная Металлическая Межмолекуляр ная По способу образования связи За счет обобщенн ой пары электрон ов За счет взаимного притяжения разноименно заряженных ионов За счет притяжения ионов металлов и свободных электронов Взаимодействи е молекул за счет Ван-дерваальсовых сил По характеру принимающих в образовании связи атомов или ионов Преимущ ественно неметалл ы Преимущественно ионы металла и неметалла Ионы металла и свободные электроны Полярные и неполярные молекулы
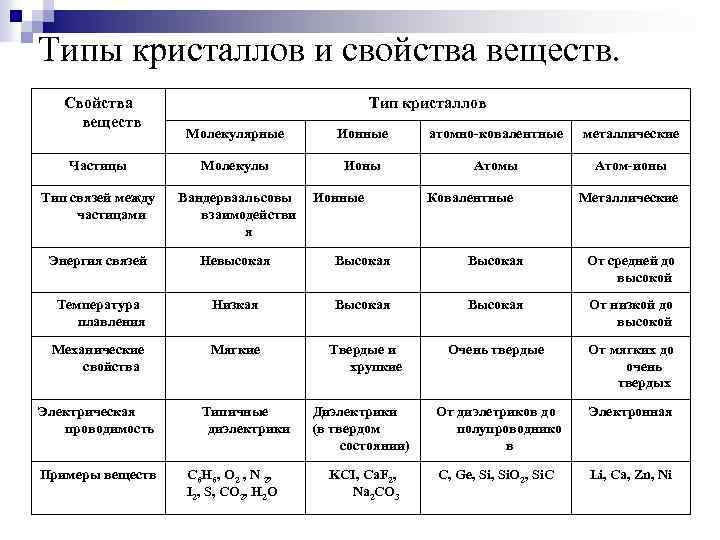 Типы кристаллов и свойства веществ. Свойства веществ Тип кристаллов Молекулярные Ионные атомно-ковалентные металлические Частицы Молекулы Ионы Атом-ионы Тип связей между частицами Вандерваальсовы взаимодействи я Энергия связей Невысокая Высокая От средней до высокой Температура плавления Низкая Высокая От низкой до высокой Механические свойства Мягкие Твердые и хрупкие Очень твердые От мягких до очень твердых Диэлектрики (в твердом состоянии) От диэлетриков до полупроводнико в Электронная KCI, Ca. F 2, Na 2 CO 3 С, Ge, Si. O 2, Si. C Li, Ca, Zn, Ni Электрическая проводимость Примеры веществ Типичные диэлектрики C 6 H 6 , О 2 , N 2 , I 2, S, CO 2, H 2 O Ионные Ковалентные Металлические
Типы кристаллов и свойства веществ. Свойства веществ Тип кристаллов Молекулярные Ионные атомно-ковалентные металлические Частицы Молекулы Ионы Атом-ионы Тип связей между частицами Вандерваальсовы взаимодействи я Энергия связей Невысокая Высокая От средней до высокой Температура плавления Низкая Высокая От низкой до высокой Механические свойства Мягкие Твердые и хрупкие Очень твердые От мягких до очень твердых Диэлектрики (в твердом состоянии) От диэлетриков до полупроводнико в Электронная KCI, Ca. F 2, Na 2 CO 3 С, Ge, Si. O 2, Si. C Li, Ca, Zn, Ni Электрическая проводимость Примеры веществ Типичные диэлектрики C 6 H 6 , О 2 , N 2 , I 2, S, CO 2, H 2 O Ионные Ковалентные Металлические
 Характеристики некоторых веществ Вещество Вид кристалла Энергия решетки, к. Дж/Моль Температура плавлени я, °С Электрическая проводимость при 298 К, (Ом*м)− 1 НСl Молекулярный 21, 3 -112 - H 20 Молекулярный 50, 2 0 - С (алмаз) Атомно-ковалентный 715 3500 1 -10 -13 Ge Атомно-ковалентный 369 938 1 -2 Na. CI Ионный 775 801 1*10 -15 Na Металлический 108, 3 98 2, 4 • 107 А] Металлический 310 660 3. 8 - 107 Мо Металлический 651 2620 1, 3 • 107
Характеристики некоторых веществ Вещество Вид кристалла Энергия решетки, к. Дж/Моль Температура плавлени я, °С Электрическая проводимость при 298 К, (Ом*м)− 1 НСl Молекулярный 21, 3 -112 - H 20 Молекулярный 50, 2 0 - С (алмаз) Атомно-ковалентный 715 3500 1 -10 -13 Ge Атомно-ковалентный 369 938 1 -2 Na. CI Ионный 775 801 1*10 -15 Na Металлический 108, 3 98 2, 4 • 107 А] Металлический 310 660 3. 8 - 107 Мо Металлический 651 2620 1, 3 • 107
 Дефекты в кристаллах. n Дефекты подразделяют на динамические (временные) и статистические (постоянные).
Дефекты в кристаллах. n Дефекты подразделяют на динамические (временные) и статистические (постоянные).
 Дефекты в кристаллах. Динамические дефекты возникают при механических, тепловых или электромагнитных воздействиях на кристалл. n Среди статистических дефектов различают протяженные (линейные и плоские) и атомные (точечные) несовершенства структуры. n
Дефекты в кристаллах. Динамические дефекты возникают при механических, тепловых или электромагнитных воздействиях на кристалл. n Среди статистических дефектов различают протяженные (линейные и плоские) и атомные (точечные) несовершенства структуры. n
 n Линейные дефекты, или дислокации (слово «дислокация» в переводе на русский означает «смещение» ), - это нарушения идеального расположения групп частиц, которые можно расположить вдоль воображаемой прямой или кривой, например винтовой, линии. Плоские дефекты - это смещение положения групп частиц, которые можно расположить на какой-либо плоскости.
n Линейные дефекты, или дислокации (слово «дислокация» в переводе на русский означает «смещение» ), - это нарушения идеального расположения групп частиц, которые можно расположить вдоль воображаемой прямой или кривой, например винтовой, линии. Плоские дефекты - это смещение положения групп частиц, которые можно расположить на какой-либо плоскости.
 Точечные дефекты – это: n а) отсутствие иона или атома в узлах решетки (так называемые вакансии, называемые дефектом Шоттки по имени описавшего этот тип дефекта немецкого физика), n б) смещение ионов или атомов из узла в междоузлие (дефект Френкеля); n в) внедрение в междоузлие или узел решетки чужеродного атома или иона (примесный дефект).
Точечные дефекты – это: n а) отсутствие иона или атома в узлах решетки (так называемые вакансии, называемые дефектом Шоттки по имени описавшего этот тип дефекта немецкого физика), n б) смещение ионов или атомов из узла в междоузлие (дефект Френкеля); n в) внедрение в междоузлие или узел решетки чужеродного атома или иона (примесный дефект).
 Точечные дефекты в кристаллической решетке. а - вакансия; б - междоузельный атом; в - примесный атом внедрения
Точечные дефекты в кристаллической решетке. а - вакансия; б - междоузельный атом; в - примесный атом внедрения
 Жидкие кристаллы. n n Жидкие кристаллы (ЖК) - это жидкости с упорядоченной молекулярной структурой, благодаря чему они занимают промежуточное положение между кристаллами и обычными жидкостями с беспорядочным расположением молекул. Жидкие кристаллы текучи, как обычные жидкости, но в то же время обладают анизотропией свойств, как кристаллы.
Жидкие кристаллы. n n Жидкие кристаллы (ЖК) - это жидкости с упорядоченной молекулярной структурой, благодаря чему они занимают промежуточное положение между кристаллами и обычными жидкостями с беспорядочным расположением молекул. Жидкие кристаллы текучи, как обычные жидкости, но в то же время обладают анизотропией свойств, как кристаллы.
 Типы структур жидких кристаллов. а) нематические; б) смектические; в) холестерические.
Типы структур жидких кристаллов. а) нематические; б) смектические; в) холестерические.
 Жидкие кристаллы. n Ориентационный порядок в жидких кристаллах легко изменяется под действием давления, электрического и магнитного полей, нагрева. Это явление дает возможность управлять их векторными свойствами (электропроводностью, магнитной восприимчивостью, диэлектрической проницаемостью и др. ) путем слабых воздействий и делает жидкие кристаллы незаменимыми материалами для изготовления особо чувствительных индикаторов.
Жидкие кристаллы. n Ориентационный порядок в жидких кристаллах легко изменяется под действием давления, электрического и магнитного полей, нагрева. Это явление дает возможность управлять их векторными свойствами (электропроводностью, магнитной восприимчивостью, диэлектрической проницаемостью и др. ) путем слабых воздействий и делает жидкие кристаллы незаменимыми материалами для изготовления особо чувствительных индикаторов.


