Миома матки..ppt
- Количество слайдов: 94
 1
1
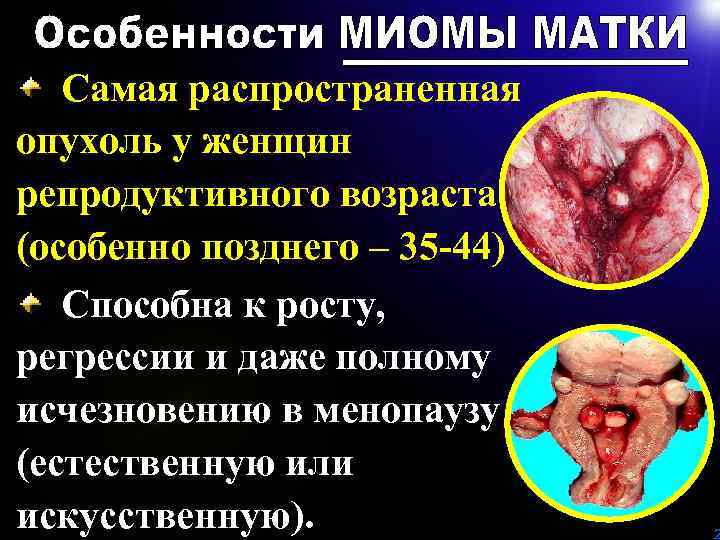 Самая распространенная опухоль у женщин репродуктивного возраста (особенно позднего – 35 -44) Способна к росту, регрессии и даже полному исчезновению в менопаузу (естественную или искусственную). 2
Самая распространенная опухоль у женщин репродуктивного возраста (особенно позднего – 35 -44) Способна к росту, регрессии и даже полному исчезновению в менопаузу (естественную или искусственную). 2
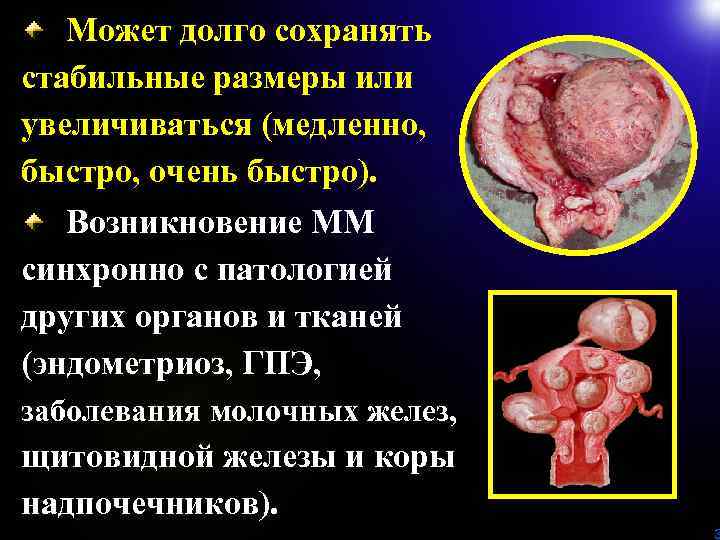 Может долго сохранять стабильные размеры или увеличиваться (медленно, быстро, очень быстро). Возникновение ММ синхронно с патологией других органов и тканей (эндометриоз, ГПЭ, заболевания молочных желез, щитовидной железы и коры надпочечников). 3
Может долго сохранять стабильные размеры или увеличиваться (медленно, быстро, очень быстро). Возникновение ММ синхронно с патологией других органов и тканей (эндометриоз, ГПЭ, заболевания молочных желез, щитовидной железы и коры надпочечников). 3
 Чаще множественная, но может быть одиночной В развитии играет роль не только гиперэстрогения и прогестерон дефицитные состоянии, но и прогестерон, пролактин и количество рецепторов к гормонам ММ – гетерогенная, вариабельная, способна накапливать или не накапливать гормоны. 4
Чаще множественная, но может быть одиночной В развитии играет роль не только гиперэстрогения и прогестерон дефицитные состоянии, но и прогестерон, пролактин и количество рецепторов к гормонам ММ – гетерогенная, вариабельная, способна накапливать или не накапливать гормоны. 4
 соматические, воспалительные, нейроэндокринные заболевания; опухоли яичников; эндометриоз (аденомиоз); гиперплазия эндометрия; стрессы; прерывание беременности (аборты); повреждение микроструктуры матки и отдельных миоцитов соматическая мутация клеток нарушение репродуктивной функции (отсутствие родов, лактации) 5
соматические, воспалительные, нейроэндокринные заболевания; опухоли яичников; эндометриоз (аденомиоз); гиперплазия эндометрия; стрессы; прерывание беременности (аборты); повреждение микроструктуры матки и отдельных миоцитов соматическая мутация клеток нарушение репродуктивной функции (отсутствие родов, лактации) 5
 6
6
 В зависимости от клетки-родоначальницы миома матки может быть: § лейомиомой, § фибромой, § эпителиоидной, § аденоматозной, § интравенозной. Имеет автономный рост (аутокринный и паракринный). 7
В зависимости от клетки-родоначальницы миома матки может быть: § лейомиомой, § фибромой, § эпителиоидной, § аденоматозной, § интравенозной. Имеет автономный рост (аутокринный и паракринный). 7
 Для своего роста и развития выделяет ФРФ, ЭРФ, СФР и образует новые сосуды (процесс неоангиогенеза). Строение сосудов – синусоидное с низко резистентным кровотоком. Митотическая активность низкая, но имеет место экспрессия пролиферирующих генов. В патогенезе развития играет роль сниженный АПОПТОЗ и генетические нарушения. 8
Для своего роста и развития выделяет ФРФ, ЭРФ, СФР и образует новые сосуды (процесс неоангиогенеза). Строение сосудов – синусоидное с низко резистентным кровотоком. Митотическая активность низкая, но имеет место экспрессия пролиферирующих генов. В патогенезе развития играет роль сниженный АПОПТОЗ и генетические нарушения. 8
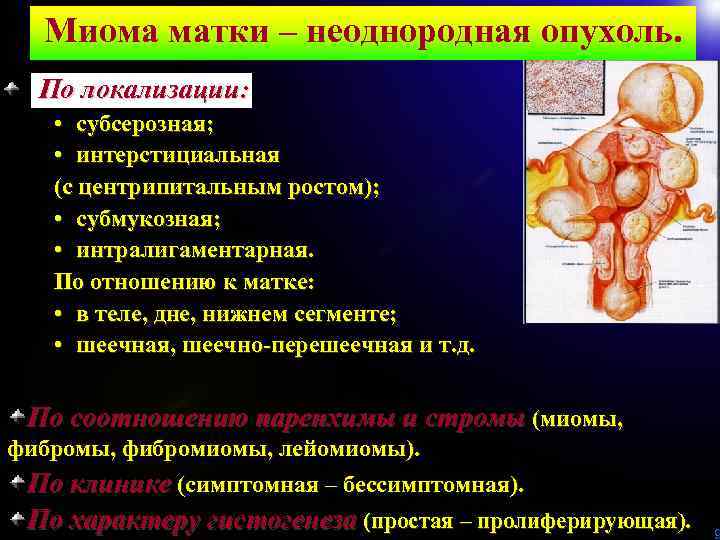 Миома матки – неоднородная опухоль. По локализации: • субсерозная; • интерстициальная (с центрипитальным ростом); • субмукозная; • интралигаментарная. По отношению к матке: • в теле, дне, нижнем сегменте; • шеечная, шеечно-перешеечная и т. д. По соотношению паренхимы и стромы (миомы, фибромиомы, лейомиомы). По клинике (симптомная – бессимптомная). По характеру гистогенеза (простая – пролиферирующая). 9
Миома матки – неоднородная опухоль. По локализации: • субсерозная; • интерстициальная (с центрипитальным ростом); • субмукозная; • интралигаментарная. По отношению к матке: • в теле, дне, нижнем сегменте; • шеечная, шеечно-перешеечная и т. д. По соотношению паренхимы и стромы (миомы, фибромиомы, лейомиомы). По клинике (симптомная – бессимптомная). По характеру гистогенеза (простая – пролиферирующая). 9
 Что нового в этой проблеме? 1. Доказана опухолевая природа ММмоноклональность. 2. Пересмотрены позиции о ведущей роли гиперэстрогении и прогестерон дефицитных состояний в возникновении опухоли. 3. Выявлена определяющая роль прогестерона в развитии ММ. 10
Что нового в этой проблеме? 1. Доказана опухолевая природа ММмоноклональность. 2. Пересмотрены позиции о ведущей роли гиперэстрогении и прогестерон дефицитных состояний в возникновении опухоли. 3. Выявлена определяющая роль прогестерона в развитии ММ. 10
 4. Подтверждены стадии развития ММ: Ø образование «активной» зоны роста Ø рост опухоли без признаков ее дифференцировки Ø рост опухоли с дифференцировкой и созреванием Ø клинически незначимый Ø клинически значимый Ø автономный рост (регуляция роста на ауто- и паракринном уровне) 11
4. Подтверждены стадии развития ММ: Ø образование «активной» зоны роста Ø рост опухоли без признаков ее дифференцировки Ø рост опухоли с дифференцировкой и созреванием Ø клинически незначимый Ø клинически значимый Ø автономный рост (регуляция роста на ауто- и паракринном уровне) 11
 1. Образование зачатка роста из незрелой ГМ клетки, из перицита. 2. Активная зона роста без признаков дифференцировки. 3. Рост опухоли с дифференцировкой и созреванием миоцитов. 4. Изменение функциональной активности миоцита (из сократительного → синтетический и продуци-рует коллаген, гликопротеиды, протеингликаны). 5. Разобщенность клеточного сообщества вызывает активный синтез ЭЦМ, гипертрофию и экспрессию ФР – переносчиков митогенных сигналов, которые усиливают деление и дифференцировку клеток. Через ФР опосредуется действие Э, П, Гт. Г и стрессовых гормонов (кортикостероиды). 12
1. Образование зачатка роста из незрелой ГМ клетки, из перицита. 2. Активная зона роста без признаков дифференцировки. 3. Рост опухоли с дифференцировкой и созреванием миоцитов. 4. Изменение функциональной активности миоцита (из сократительного → синтетический и продуци-рует коллаген, гликопротеиды, протеингликаны). 5. Разобщенность клеточного сообщества вызывает активный синтез ЭЦМ, гипертрофию и экспрессию ФР – переносчиков митогенных сигналов, которые усиливают деление и дифференцировку клеток. Через ФР опосредуется действие Э, П, Гт. Г и стрессовых гормонов (кортикостероиды). 12
 6. Запускается процесс неоангиогенеза, подавление иммунологической защиты. 7. Факторы роста: – – – ИПФР – инсулиноподобный; ЭФР – эпидермальный; СЭФР – сосудисто-эндотелиальный; ТФР – тромбоцитарный; ФРФ – фактор роста фибробластов. ФР, гормоны – составляют молекулярную основу многих процессов: воспаление, опухоль, неоангиогенез. 8. Нарушение соотношения пролиферации (↑) и апоптоза (↓). ↑ BCL-2, Bax, C-myc, P-53. 13
6. Запускается процесс неоангиогенеза, подавление иммунологической защиты. 7. Факторы роста: – – – ИПФР – инсулиноподобный; ЭФР – эпидермальный; СЭФР – сосудисто-эндотелиальный; ТФР – тромбоцитарный; ФРФ – фактор роста фибробластов. ФР, гормоны – составляют молекулярную основу многих процессов: воспаление, опухоль, неоангиогенез. 8. Нарушение соотношения пролиферации (↑) и апоптоза (↓). ↑ BCL-2, Bax, C-myc, P-53. 13
 Классификация миом матки в основном анатомическая и морфологическая. Классификация ВОЗ (1994 г. ): Ø Ø Ø обычная (зрелая доброкачественная опухоль); причудливая; внутрисосудистый лейомиоматоз; растущая (пролиферирующая); малигнизирующая (предсаркоматозная); эпителиоидная. 14
Классификация миом матки в основном анатомическая и морфологическая. Классификация ВОЗ (1994 г. ): Ø Ø Ø обычная (зрелая доброкачественная опухоль); причудливая; внутрисосудистый лейомиоматоз; растущая (пролиферирующая); малигнизирующая (предсаркоматозная); эпителиоидная. 14
 Гистологическая Простая, Клеточная, Митотически активная. (по классификации ВОЗ, 2003 г. , World Health Organization Classification of Tumors). Клинико-гистохимическая Простая, Пролиферирующая (клеточная, митотически активная). (Сидорова И. С. , Коган Е. А. , Зайратьянц О. В. , 2001 г. ) 15
Гистологическая Простая, Клеточная, Митотически активная. (по классификации ВОЗ, 2003 г. , World Health Organization Classification of Tumors). Клинико-гистохимическая Простая, Пролиферирующая (клеточная, митотически активная). (Сидорова И. С. , Коган Е. А. , Зайратьянц О. В. , 2001 г. ) 15
 Клинико-морфологическая характеристика простой и пролиферирующей миомы матки (крайние варианты развития). И. С. Сидорова. Признак Возраст Простая м. Пролиферирующая м. Поздний репродуктивный (35 -45 лет). Молодой (20 -29 лет), постменопаузальный (5255 лет). Наследственность + Особенности анамнеза Отягощен (высокая соматическая и гинекологическая заболеваемость, бесплодие). +++ Отягощен (сочетание с эндометриозом, гиперплазией эндометрия; сах. диабет, ожирение). 16
Клинико-морфологическая характеристика простой и пролиферирующей миомы матки (крайние варианты развития). И. С. Сидорова. Признак Возраст Простая м. Пролиферирующая м. Поздний репродуктивный (35 -45 лет). Молодой (20 -29 лет), постменопаузальный (5255 лет). Наследственность + Особенности анамнеза Отягощен (высокая соматическая и гинекологическая заболеваемость, бесплодие). +++ Отягощен (сочетание с эндометриозом, гиперплазией эндометрия; сах. диабет, ожирение). 16
 Признак Простая м. Пролиферирующая м. Клинические проявления Бессимптомная. Симптомная. Характеристика роста Медленный. Быстрый. Локализация Преимущественно побрюшинная и межмышечная. Межмышечная с центрипетальным ростом, подслизистая. Трубные углы, ребра матки, шеечно-перешеечная область, между листками широких связок. Преимущественное Дно и тело матки. расположение Количество узлов Единичные (1 -4). Размеры Небольшие (до 5). (диаметр – см) Множественные (5 и >). Большие (> 5). 17
Признак Простая м. Пролиферирующая м. Клинические проявления Бессимптомная. Симптомная. Характеристика роста Медленный. Быстрый. Локализация Преимущественно побрюшинная и межмышечная. Межмышечная с центрипетальным ростом, подслизистая. Трубные углы, ребра матки, шеечно-перешеечная область, между листками широких связок. Преимущественное Дно и тело матки. расположение Количество узлов Единичные (1 -4). Размеры Небольшие (до 5). (диаметр – см) Множественные (5 и >). Большие (> 5). 17
 Признак Особенности роста Простая м. Пролиферирующая м. За счет усиленного синтеза элементов ЭЦМ, вторичные изменения (отек, фиброз). Преобладание клеточного компонента; активный неоангиогенез; «миома из миомы» ; конгломерат узлов. Митотическая Низкая (0 -1 в 10 активность полях зрения). Особенности морфогистохимии Хаотичное расположенные ГМК, плотно оплетенные соед. ткан. каркасом. Преобладают миоциты средних и крупных размеров. Низкая (2 -5 в 10 полях зрения) Митозы растянуты. Множество зачатков роста. Миоциты крупные и маленькие (постаревшие). Выраженная «клеточность» . Преобладает мышечный компонент. 18
Признак Особенности роста Простая м. Пролиферирующая м. За счет усиленного синтеза элементов ЭЦМ, вторичные изменения (отек, фиброз). Преобладание клеточного компонента; активный неоангиогенез; «миома из миомы» ; конгломерат узлов. Митотическая Низкая (0 -1 в 10 активность полях зрения). Особенности морфогистохимии Хаотичное расположенные ГМК, плотно оплетенные соед. ткан. каркасом. Преобладают миоциты средних и крупных размеров. Низкая (2 -5 в 10 полях зрения) Митозы растянуты. Множество зачатков роста. Миоциты крупные и маленькие (постаревшие). Выраженная «клеточность» . Преобладает мышечный компонент. 18
 Признак Особенности морфогистохимии Простая м. Пролиферирующая м. Ядра крупные, гиперхромные (большое Клетки сморщенные, ядра маленькие. количество ДНК). Коллагеноз, гиалиноз. Очаги пролиферации опухолевых миоцитов Отсутствие признаков активного локализуются вокруг сосудов. роста. Клетки полигональной Преобладают формы с 2 -3 ядрами компоненты ЭЦМ. Сосудов мало. Чаще полиплоидия, свидетельствующая о нарушении отек, нарушение кариотипа и хромосомной питания, гиалиноз, изменчивости. кальциноз, дегеративно. Признаки дистрофические пролиферации: высокая изменения. клеточность, крупные ядра. 19
Признак Особенности морфогистохимии Простая м. Пролиферирующая м. Ядра крупные, гиперхромные (большое Клетки сморщенные, ядра маленькие. количество ДНК). Коллагеноз, гиалиноз. Очаги пролиферации опухолевых миоцитов Отсутствие признаков активного локализуются вокруг сосудов. роста. Клетки полигональной Преобладают формы с 2 -3 ядрами компоненты ЭЦМ. Сосудов мало. Чаще полиплоидия, свидетельствующая о нарушении отек, нарушение кариотипа и хромосомной питания, гиалиноз, изменчивости. кальциноз, дегеративно. Признаки дистрофические пролиферации: высокая изменения. клеточность, крупные ядра. 19
 Признак Особенности морфогистохимии Простая м. Пролиферирующая м. В отдельных участках миометрия – множество «активных зачатков роста» . Повышенная В отдельных экспрессия PCNA, участках миометрия онкогена Cerb-2, изменений нет. антионкогена р-53, Ki-67. Увеличение плоидности ядер (полиплоидия). Высокая экспрессия ТФР, СЭФР. 20
Признак Особенности морфогистохимии Простая м. Пролиферирующая м. В отдельных участках миометрия – множество «активных зачатков роста» . Повышенная В отдельных экспрессия PCNA, участках миометрия онкогена Cerb-2, изменений нет. антионкогена р-53, Ki-67. Увеличение плоидности ядер (полиплоидия). Высокая экспрессия ТФР, СЭФР. 20
 Признак Состояние эндометрия Простая м. Пролиферирующая м. Отражение возраста, Гиперплазия эндометрия гормонального баланса. – до 65 -87% во все Гиперпластические возрастные периоды. процессы в 20 -2%. Менопауза 52 -53 года. В первые После 54 лет. Регрессия (время 2 года – регрессия узлов отсутствует. наступления) опухоли. 21
Признак Состояние эндометрия Простая м. Пролиферирующая м. Отражение возраста, Гиперплазия эндометрия гормонального баланса. – до 65 -87% во все Гиперпластические возрастные периоды. процессы в 20 -2%. Менопауза 52 -53 года. В первые После 54 лет. Регрессия (время 2 года – регрессия узлов отсутствует. наступления) опухоли. 21
 Общая характеристика крайних вариантов развития ММ ПРОСТАЯ МИОМА МАТКИ Не активная, растет медленно. Преобладают элементы внеклеточного матрикса. Кровоснабжение снижено. Опухоль белесоватого цвета, плотная, с четкими контурами. ПРОЛИФЕРИРУЮЩАЯ МИОМА МАТКИ Активная, множественная, быстрорастущая, клеточная. Повышен пролиферативный потенциал. Часто сочетается с аденомиозом и гиперпластическими процессами эндометрия. 22
Общая характеристика крайних вариантов развития ММ ПРОСТАЯ МИОМА МАТКИ Не активная, растет медленно. Преобладают элементы внеклеточного матрикса. Кровоснабжение снижено. Опухоль белесоватого цвета, плотная, с четкими контурами. ПРОЛИФЕРИРУЮЩАЯ МИОМА МАТКИ Активная, множественная, быстрорастущая, клеточная. Повышен пролиферативный потенциал. Часто сочетается с аденомиозом и гиперпластическими процессами эндометрия. 22
 Ø Гиперэхогенное изображение новообразования с эффектом дистального поглощения звука, появление периферического уплотнения в виде капсулы (73%). Ø Сниженный внутриопухолевый кровоток миоматозного узла с единичными цветовыми сигналами по периферии. Ø ИР: § в миометрии – 0, 63+0, 05, § в миом. узлах – 0, 59+0, 06. Ø Максимальная систолическая скорость – 18, 7 см/сек. 23
Ø Гиперэхогенное изображение новообразования с эффектом дистального поглощения звука, появление периферического уплотнения в виде капсулы (73%). Ø Сниженный внутриопухолевый кровоток миоматозного узла с единичными цветовыми сигналами по периферии. Ø ИР: § в миометрии – 0, 63+0, 05, § в миом. узлах – 0, 59+0, 06. Ø Максимальная систолическая скорость – 18, 7 см/сек. 23
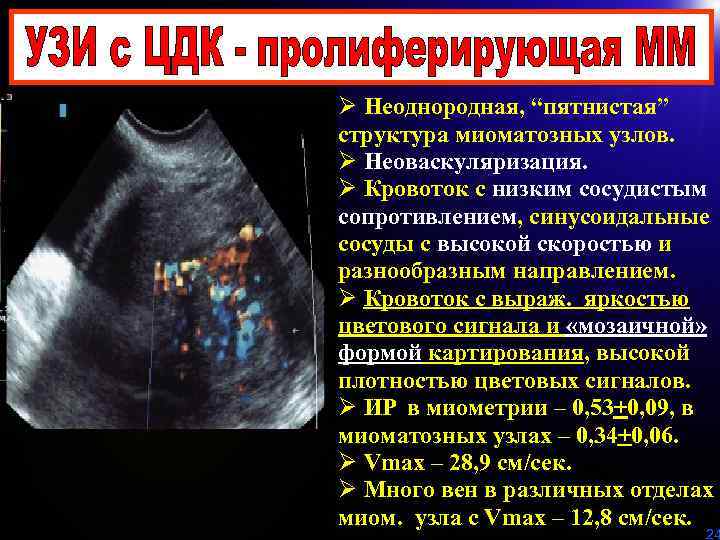 Ø Неоднородная, “пятнистая” структура миоматозных узлов. Ø Неоваскуляризация. Ø Кровоток с низким сосудистым сопротивлением, синусоидальные сосуды с высокой скоростью и разнообразным направлением. Ø Кровоток с выраж. яркостью цветового сигнала и «мозаичной» формой картирования, высокой плотностью цветовых сигналов. Ø ИР в миометрии – 0, 53+0, 09, в миоматозных узлах – 0, 34+0, 06. Ø Vmax – 28, 9 см/сек. Ø Много вен в различных отделах миом. узла с Vmax – 12, 8 см/сек. 24
Ø Неоднородная, “пятнистая” структура миоматозных узлов. Ø Неоваскуляризация. Ø Кровоток с низким сосудистым сопротивлением, синусоидальные сосуды с высокой скоростью и разнообразным направлением. Ø Кровоток с выраж. яркостью цветового сигнала и «мозаичной» формой картирования, высокой плотностью цветовых сигналов. Ø ИР в миометрии – 0, 53+0, 09, в миоматозных узлах – 0, 34+0, 06. Ø Vmax – 28, 9 см/сек. Ø Много вен в различных отделах миом. узла с Vmax – 12, 8 см/сек. 24
 • на ангиограммах хорошо регистрируются магистральные маточные сосуды (правая и левая маточные артерии) • прослеживается крупная ветвь одной из маточных артерий, питающая миоматозный узел • кровеносные сосуды самого миоматозного узла немногочисленны, средних калибров и располагаются по периферии, как бы огибая его контур • такой тип можно охарактеризовать как «периферически» , умеренно выраженный. Артериальная реконструктивная фаза исследования. 25
• на ангиограммах хорошо регистрируются магистральные маточные сосуды (правая и левая маточные артерии) • прослеживается крупная ветвь одной из маточных артерий, питающая миоматозный узел • кровеносные сосуды самого миоматозного узла немногочисленны, средних калибров и располагаются по периферии, как бы огибая его контур • такой тип можно охарактеризовать как «периферически» , умеренно выраженный. Артериальная реконструктивная фаза исследования. 25
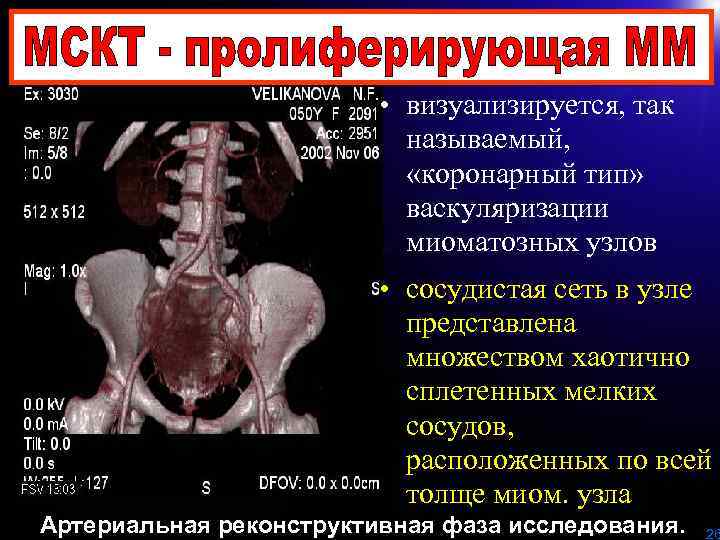 • визуализируется, так называемый, «коронарный тип» васкуляризации миоматозных узлов • сосудистая сеть в узле представлена множеством хаотично сплетенных мелких сосудов, расположенных по всей толще миом. узла Артериальная реконструктивная фаза исследования. 26
• визуализируется, так называемый, «коронарный тип» васкуляризации миоматозных узлов • сосудистая сеть в узле представлена множеством хаотично сплетенных мелких сосудов, расположенных по всей толще миом. узла Артериальная реконструктивная фаза исследования. 26
 Макроскопическая характеристика Простая миома Размеры не превышали 4 -5 см в диаметре. В виде единичных узлов (1 – 4 узла). Плотной белесоватой волокнистой структуры с четкими границами. Сосуды располагаются по Пролиферирующая миома Большие размеры (7 см в диаметре и больше). Множественный характер. Консистенция мягкая. На разрезах – неоднородной структуры розоватого цвета, с множественными периферии узла, в небольшом кровоизлияниями, полостями, количестве, среднего калибра. обильной васкуляризацией. 27
Макроскопическая характеристика Простая миома Размеры не превышали 4 -5 см в диаметре. В виде единичных узлов (1 – 4 узла). Плотной белесоватой волокнистой структуры с четкими границами. Сосуды располагаются по Пролиферирующая миома Большие размеры (7 см в диаметре и больше). Множественный характер. Консистенция мягкая. На разрезах – неоднородной структуры розоватого цвета, с множественными периферии узла, в небольшом кровоизлияниями, полостями, количестве, среднего калибра. обильной васкуляризацией. 27
 ПРОСТАЯ ММ ПРОЛИФЕРИРУЮЩАЯ М М ТЕЛО МАТКИ УЗЛЫ МИОМЫ 28
ПРОСТАЯ ММ ПРОЛИФЕРИРУЮЩАЯ М М ТЕЛО МАТКИ УЗЛЫ МИОМЫ 28
 • Выраженные дистрофические изменения, очаги некроза, отека, склероза • Преобладание соединительнотканной стромы с выраженным склерозом, гиалинозом на фоне отека и множественных участков некроза. Признаки нарушения кровообращения в миомах. • В участках некроза – скопление нейтрофильных лейкоцитов, лимфоцитов, формирование кистозных полостей в месте разрушения ткани миомы. 29
• Выраженные дистрофические изменения, очаги некроза, отека, склероза • Преобладание соединительнотканной стромы с выраженным склерозом, гиалинозом на фоне отека и множественных участков некроза. Признаки нарушения кровообращения в миомах. • В участках некроза – скопление нейтрофильных лейкоцитов, лимфоцитов, формирование кистозных полостей в месте разрушения ткани миомы. 29
 30
30
 • Во всех пролиферирующих узлах имеются множественные периваскулярные активные зоны роста. Миоциты полиморфны, единичные митозы. Сосуды синусоидного типа с низкорезистентным кровотоком. • Изменения в основном касаются клеточного компонента, сосудов, выражены признаки неоангиогенеза. 31
• Во всех пролиферирующих узлах имеются множественные периваскулярные активные зоны роста. Миоциты полиморфны, единичные митозы. Сосуды синусоидного типа с низкорезистентным кровотоком. • Изменения в основном касаются клеточного компонента, сосудов, выражены признаки неоангиогенеза. 31
 32
32
 33
33
 Э Ц М – ламинин, фибронектин, коллаген Ø определяет сохранение формы и функции окружающих клеток; Ø противостояние физическим воздействиям, которым подвергается матка (выскабливания, воспаления, метаболические нарушения); Ø сохраняют прочность органа препятствуя чрезмерному растяжению и сокращению матки; 34
Э Ц М – ламинин, фибронектин, коллаген Ø определяет сохранение формы и функции окружающих клеток; Ø противостояние физическим воздействиям, которым подвергается матка (выскабливания, воспаления, метаболические нарушения); Ø сохраняют прочность органа препятствуя чрезмерному растяжению и сокращению матки; 34
 Ø осуществляют диффузию питательных веществ, метаболитов и гормонов; Ø являются источником белка и ФР; Ø определяют энергию роста (сборка полисахаридных цепей); Ø выявлено до 400 вариантов мутаций генов ламинина, фибронектина и коллагенов, что нарушает образование сосудов (возникновение активного «зачатка» роста миоматозного узелка? ) 35
Ø осуществляют диффузию питательных веществ, метаболитов и гормонов; Ø являются источником белка и ФР; Ø определяют энергию роста (сборка полисахаридных цепей); Ø выявлено до 400 вариантов мутаций генов ламинина, фибронектина и коллагенов, что нарушает образование сосудов (возникновение активного «зачатка» роста миоматозного узелка? ) 35
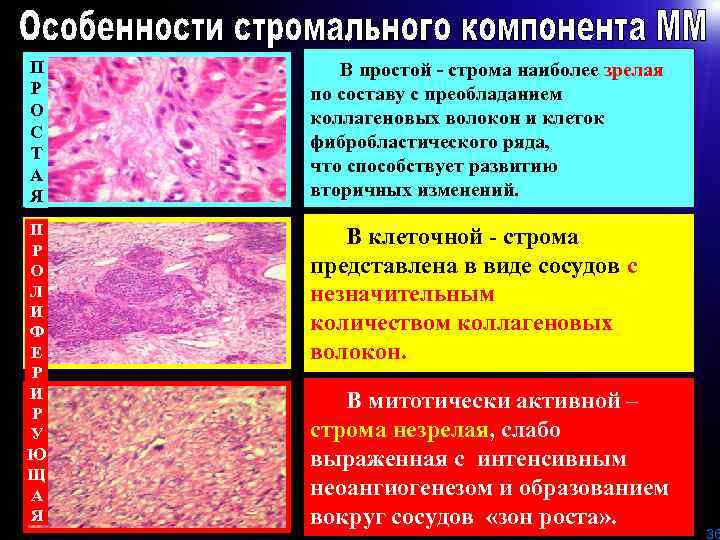 П Р О С Т А Я В простой - строма наиболее зрелая по составу с преобладанием коллагеновых волокон и клеток фибробластического ряда, что способствует развитию вторичных изменений. П Р О Л И Ф Е Р И Р У Ю Щ А Я В клеточной - строма представлена в виде сосудов с незначительным количеством коллагеновых волокон. В митотически активной – строма незрелая, слабо выраженная с интенсивным неоангиогенезом и образованием вокруг сосудов «зон роста» . 36
П Р О С Т А Я В простой - строма наиболее зрелая по составу с преобладанием коллагеновых волокон и клеток фибробластического ряда, что способствует развитию вторичных изменений. П Р О Л И Ф Е Р И Р У Ю Щ А Я В клеточной - строма представлена в виде сосудов с незначительным количеством коллагеновых волокон. В митотически активной – строма незрелая, слабо выраженная с интенсивным неоангиогенезом и образованием вокруг сосудов «зон роста» . 36
 APOP-DETEK ТЕСТ ФИБРОНЕКТИН ЛАМИНИН МАРКЕР АПОПТОЗА КОМПОНЕНТЫ ЭЦМ CD - 95 ПРОАПОПТОТИЧЕСКИЙ ФАКТОР KI- 67 МАРКЕР ПРОЛИФЕРАЦИИ BCL-2 FGF ИНГИБИТОР АПОПТОЗА ФАКТОР РОСТА ФИБРОБЛАСТОВ ВАХ EGF ИНДУКТОР АПОПТОЗА ЭПИДЕРМАЛЬНЫЙ ФАКТОР РОСТА C-MYC ФАКТОР ДЕЛЕНИЯ КЛЕТКИ EGFR CD-34 МАРКЕР НЕОАНГИОГЕНЕЗА ММРS и TIMP МАТРИКСНЫЕ МЕТАЛЛОПРОТЕИНАЗЫ РЕЦЕПТОР К ЭПИДЕРМАЛЬНОМУ ФАКТОРУ РОСТА и их ИНГИБИТОРЫ 37
APOP-DETEK ТЕСТ ФИБРОНЕКТИН ЛАМИНИН МАРКЕР АПОПТОЗА КОМПОНЕНТЫ ЭЦМ CD - 95 ПРОАПОПТОТИЧЕСКИЙ ФАКТОР KI- 67 МАРКЕР ПРОЛИФЕРАЦИИ BCL-2 FGF ИНГИБИТОР АПОПТОЗА ФАКТОР РОСТА ФИБРОБЛАСТОВ ВАХ EGF ИНДУКТОР АПОПТОЗА ЭПИДЕРМАЛЬНЫЙ ФАКТОР РОСТА C-MYC ФАКТОР ДЕЛЕНИЯ КЛЕТКИ EGFR CD-34 МАРКЕР НЕОАНГИОГЕНЕЗА ММРS и TIMP МАТРИКСНЫЕ МЕТАЛЛОПРОТЕИНАЗЫ РЕЦЕПТОР К ЭПИДЕРМАЛЬНОМУ ФАКТОРУ РОСТА и их ИНГИБИТОРЫ 37
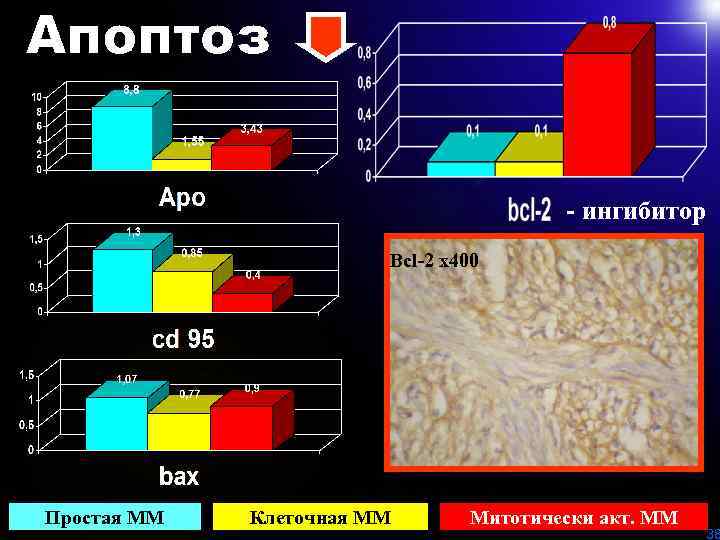 - ингибитор Bcl-2 х400 Рис. 6 Вcl-2 в клеточной миоме матки. Х 400 Простая ММ Клеточная ММ Митотически акт. ММ 38
- ингибитор Bcl-2 х400 Рис. 6 Вcl-2 в клеточной миоме матки. Х 400 Простая ММ Клеточная ММ Митотически акт. ММ 38
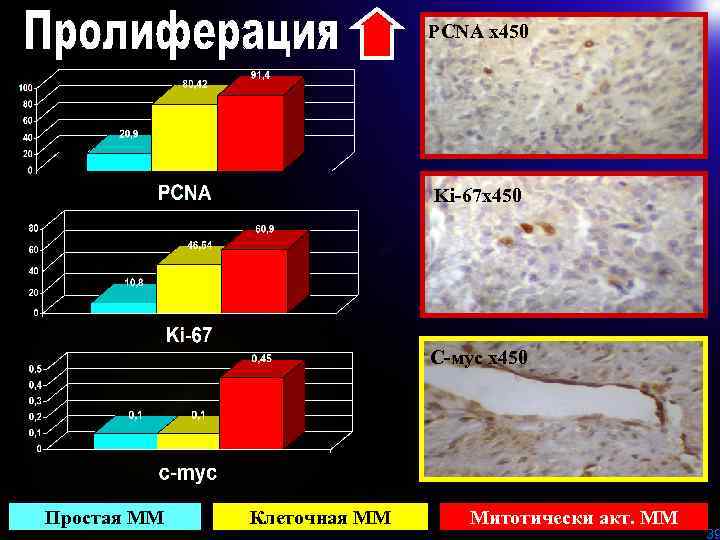 PCNA х450 Ki-67 х450 С-мус х450 Простая ММ Клеточная ММ Митотически акт. ММ 39
PCNA х450 Ki-67 х450 С-мус х450 Простая ММ Клеточная ММ Митотически акт. ММ 39
 CD-34 х200 Простая ММ Клеточная ММ Митотически акт. ММ 40
CD-34 х200 Простая ММ Клеточная ММ Митотически акт. ММ 40
 EGF х400 Простая ММ EGFR х400 Клеточная ММ Митотически акт. ММ 41
EGF х400 Простая ММ EGFR х400 Клеточная ММ Митотически акт. ММ 41
 Факторы роста способствуют : ü росту миомы за счет гипертрофии и пролиферации миоцитов. ü гипертрофии миометрия, что сопровождается увеличением толщины миометрия у больных с миомой матки. ü возникновению гиперпластических процессов эндометрия ü усилению неоангиогенеза, с формированием сосудов синусоидного типа с низкорезистентным кровотоком 42
Факторы роста способствуют : ü росту миомы за счет гипертрофии и пролиферации миоцитов. ü гипертрофии миометрия, что сопровождается увеличением толщины миометрия у больных с миомой матки. ü возникновению гиперпластических процессов эндометрия ü усилению неоангиогенеза, с формированием сосудов синусоидного типа с низкорезистентным кровотоком 42
 ПРОСТАЯ ПРОЛИФЕРИРУЮЩАЯ КЛЕТОЧНАЯ • Пролиферация низкая • Митотическая активность низкая • Увеличение компонентов ЭЦМ • Мало сосудов • Апоптоз высокий • Пролиферация повышена • Митозов мало • Компонентов ЭЦМ мало • Сосудов много • Апоптоз снижен МИТОТИЧЕСКИ АКТИВНАЯ • Пролиферация выраженная • Много митозов • Стромообразование снижено • Выраженный Ангиогенез • Множество зон роста • Низкий апоптоз 43
ПРОСТАЯ ПРОЛИФЕРИРУЮЩАЯ КЛЕТОЧНАЯ • Пролиферация низкая • Митотическая активность низкая • Увеличение компонентов ЭЦМ • Мало сосудов • Апоптоз высокий • Пролиферация повышена • Митозов мало • Компонентов ЭЦМ мало • Сосудов много • Апоптоз снижен МИТОТИЧЕСКИ АКТИВНАЯ • Пролиферация выраженная • Много митозов • Стромообразование снижено • Выраженный Ангиогенез • Множество зон роста • Низкий апоптоз 43
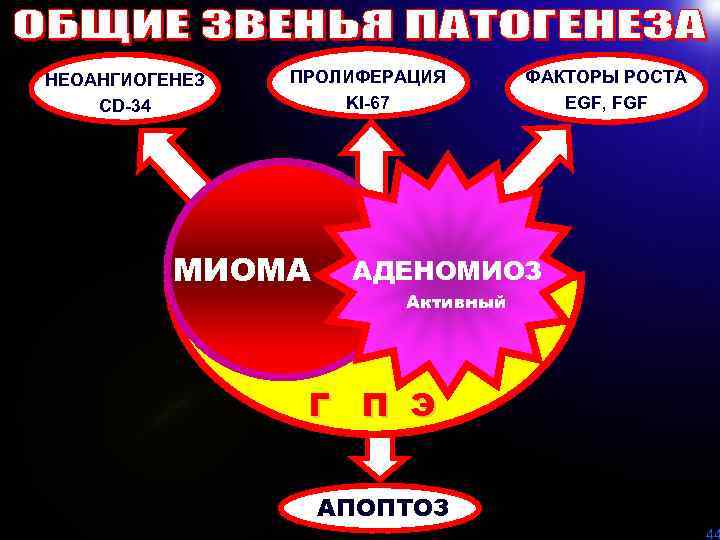 НЕОАНГИОГЕНЕЗ CD-34 ПРОЛИФЕРАЦИЯ KI-67 МИОМА ФАКТОРЫ РОСТА EGF, FGF АДЕНОМИОЗ Активный Г П Э АПОПТОЗ 44
НЕОАНГИОГЕНЕЗ CD-34 ПРОЛИФЕРАЦИЯ KI-67 МИОМА ФАКТОРЫ РОСТА EGF, FGF АДЕНОМИОЗ Активный Г П Э АПОПТОЗ 44
 ВОЗРАСТОМ ЖЕНЩИНЫ КЛИНИКО-МОРФОЛГИЧЕСКИМ ВАРИАНТОМ РАЗВИТИЯ ОПУХОЛИ 45
ВОЗРАСТОМ ЖЕНЩИНЫ КЛИНИКО-МОРФОЛГИЧЕСКИМ ВАРИАНТОМ РАЗВИТИЯ ОПУХОЛИ 45
 Репродуктивный 15 - 44 лет Пременопаузальный 45 - 50 лет Менопауза – 50, 8 лет Постменопаузальный 46
Репродуктивный 15 - 44 лет Пременопаузальный 45 - 50 лет Менопауза – 50, 8 лет Постменопаузальный 46
 Все изменения в организме женщины направлены на осуществление и реализацию репродуктивной функции. I РОДОВ - 20 – 22 лет II РОДОВ - 25 лет III РОДОВ - 28 – 30 лет Наличие ММ у молодой женщины (20 -29 лет) свидетельствует о: q наследственном заболевании; q пролиферирующем варианте развития ММ. 47
Все изменения в организме женщины направлены на осуществление и реализацию репродуктивной функции. I РОДОВ - 20 – 22 лет II РОДОВ - 25 лет III РОДОВ - 28 – 30 лет Наличие ММ у молодой женщины (20 -29 лет) свидетельствует о: q наследственном заболевании; q пролиферирующем варианте развития ММ. 47
 ЛЕЧИТЬ БЕСПЛОДИЕ КОРРИГИРОВАТЬ ГОРМОНАЛЬНЫЕ НАРУШЕНИЯ (НЛФ цикла, ановуляцию) СОХРАНЯТЬ БЕРЕМЕННОСТЬ 48
ЛЕЧИТЬ БЕСПЛОДИЕ КОРРИГИРОВАТЬ ГОРМОНАЛЬНЫЕ НАРУШЕНИЯ (НЛФ цикла, ановуляцию) СОХРАНЯТЬ БЕРЕМЕННОСТЬ 48
 О С О Б Е Н Н О С Т И: Ø Постепенно снижается гормональная функция яичников и соответственно для её поддержания повышается синтез гонадотропных гормонов. Ø Накапливаются последствия перенесенных и сопутствующих экстрагенитальных и гинекологических заболеваний. Ø Суммируются гормональные нарушения. 49
О С О Б Е Н Н О С Т И: Ø Постепенно снижается гормональная функция яичников и соответственно для её поддержания повышается синтез гонадотропных гормонов. Ø Накапливаются последствия перенесенных и сопутствующих экстрагенитальных и гинекологических заболеваний. Ø Суммируются гормональные нарушения. 49
 О С О Б Е Н Н О С Т И: Ø Нарушаются клеточно-межклеточные отношения в органах репродуктивной системы – ↑ процессы пролиферации, ↓ апоптоз; Ø Возникают мутации белка р-53 – гена-супрессора опухолевого роста. На поздний репродуктивный возраст приходится «пик» гинекологической заболеваемости (в том числе и ММ). Через 10 -15 лет у большинства пациенток с ММ возникнут показания к удалению органа. 50
О С О Б Е Н Н О С Т И: Ø Нарушаются клеточно-межклеточные отношения в органах репродуктивной системы – ↑ процессы пролиферации, ↓ апоптоз; Ø Возникают мутации белка р-53 – гена-супрессора опухолевого роста. На поздний репродуктивный возраст приходится «пик» гинекологической заболеваемости (в том числе и ММ). Через 10 -15 лет у большинства пациенток с ММ возникнут показания к удалению органа. 50
 Пременопаузальный возраст (46 -50 лет) О С О Б Е Н Н О С Т И: Постепенное прекращение репродуктивной функции и циклической деятельности Г–Г–Я– М системы. Снижение чувствительности яичников к гонадотропной стимуляции (к концу этого периода секреция ФСГ возрастает в 10 -14 раз, ЛГ – в 3 -4 раза). Увеличение продукции стрессовых гормонов (реакция «льва и кролика» ). Уменьшение синтеза антистрессовых нейрогормонов (эндорфинов). 51
Пременопаузальный возраст (46 -50 лет) О С О Б Е Н Н О С Т И: Постепенное прекращение репродуктивной функции и циклической деятельности Г–Г–Я– М системы. Снижение чувствительности яичников к гонадотропной стимуляции (к концу этого периода секреция ФСГ возрастает в 10 -14 раз, ЛГ – в 3 -4 раза). Увеличение продукции стрессовых гормонов (реакция «льва и кролика» ). Уменьшение синтеза антистрессовых нейрогормонов (эндорфинов). 51
 Повышенная лабильность ССС, показателей гемо- и гомеостаза. Возрастание размеров яичников и матки, снижение их кровоснабжения. Активизация пролиферативных процессов в органах репродуктивной системы (гиперплазия эндометрия, аденомиоз, эндометриоз, кисты и опухоли яичников). 52
Повышенная лабильность ССС, показателей гемо- и гомеостаза. Возрастание размеров яичников и матки, снижение их кровоснабжения. Активизация пролиферативных процессов в органах репродуктивной системы (гиперплазия эндометрия, аденомиоз, эндометриоз, кисты и опухоли яичников). 52
 У большинства пациенток в этом возрасте наблюдается быстрый рост миоматозных узлов, которые в совокупности с гиперплазией эндометрия, эндометриозом являются основным показанием к удалению матки. Маточные кровотечения (32 -48%). Анемия (37 -54%). Кисты и кистомы яичников (18 -27%). Гиперплазия и рак эндометрия (42%). ГОРМОНАЛЬНАЯ ТЕРАПИЯ АБЛАЦИЯ ЭНДОМЕТРИЯ УДАЛЕНИЕ МАТКИ 53
У большинства пациенток в этом возрасте наблюдается быстрый рост миоматозных узлов, которые в совокупности с гиперплазией эндометрия, эндометриозом являются основным показанием к удалению матки. Маточные кровотечения (32 -48%). Анемия (37 -54%). Кисты и кистомы яичников (18 -27%). Гиперплазия и рак эндометрия (42%). ГОРМОНАЛЬНАЯ ТЕРАПИЯ АБЛАЦИЯ ЭНДОМЕТРИЯ УДАЛЕНИЕ МАТКИ 53
 Постменопаузальный возраст. Менопауза у здоровых – 50, 8 ± 0, 9 лет При миоме матки – 53, 6 ± 1, 1 лет О С О Б Е Н Н О С Т И: Ø Практическое прекращение секреторной функции яичников, их атрофия. Ø Атрофия эндометрия и других гормонально зависимых тканей. 54
Постменопаузальный возраст. Менопауза у здоровых – 50, 8 ± 0, 9 лет При миоме матки – 53, 6 ± 1, 1 лет О С О Б Е Н Н О С Т И: Ø Практическое прекращение секреторной функции яичников, их атрофия. Ø Атрофия эндометрия и других гормонально зависимых тканей. 54
 Ø Эстрон (Э 1) – на молекулярном уровне может усиливать экспрессию онкогенов, ФР и опухолевую трансформацию клеток (ожирение, гипотиреоз, гиперплазия коры надпочечников). Ø Инволюция и апоптоз органов и тканей. Ø Уменьшение размеров матки (30 лет – 120 г, 65 лет – 30 г) и одновременно – миоматозных узлов. 55
Ø Эстрон (Э 1) – на молекулярном уровне может усиливать экспрессию онкогенов, ФР и опухолевую трансформацию клеток (ожирение, гипотиреоз, гиперплазия коры надпочечников). Ø Инволюция и апоптоз органов и тканей. Ø Уменьшение размеров матки (30 лет – 120 г, 65 лет – 30 г) и одновременно – миоматозных узлов. 55
 Клинические проявления нерегрессирующей ММ в постменопаузе: ü Отсутствие уменьшения размеров матки ü Кровянистые выделения. ü Патология эндометрия (гиперплазия, отсутствие атрофии – М-эхо до 8 мм и более). ü Сочетание ММ с эндометриозом и ГПЭ. ü Хроническая анемия. ü Отсутствие физиологической атрофии яичников (в норме 3, 6± 1, 4 см). В первые 5 лет постменопаузы их размеры уменьшаются на 20%, после 10 лет – на 30 -35%, в 70 лет – на 50% (маленькие сморщенные яичники). 56
Клинические проявления нерегрессирующей ММ в постменопаузе: ü Отсутствие уменьшения размеров матки ü Кровянистые выделения. ü Патология эндометрия (гиперплазия, отсутствие атрофии – М-эхо до 8 мм и более). ü Сочетание ММ с эндометриозом и ГПЭ. ü Хроническая анемия. ü Отсутствие физиологической атрофии яичников (в норме 3, 6± 1, 4 см). В первые 5 лет постменопаузы их размеры уменьшаются на 20%, после 10 лет – на 30 -35%, в 70 лет – на 50% (маленькие сморщенные яичники). 56
 Нерегрессирующая миома матки в постменопаузальном возрасте является маркером онкопатологии органов репродуктивной системы (опухоль яичников, гиперплазия или рак эндометрия). Продукция Э столь низкая, что удаление яичников не сопровождается снижением его содержания в крови и моче. В организме повышается содержание тестостерона и андростендиона (андрогенное воздействие). Стабильно высокая продукция гонадотропинов (в десятки раз!) – «пиковая флюктуация» . Гонадотропины – ингибиторы апоптоза и индукторы-посредники пролиферации. 57
Нерегрессирующая миома матки в постменопаузальном возрасте является маркером онкопатологии органов репродуктивной системы (опухоль яичников, гиперплазия или рак эндометрия). Продукция Э столь низкая, что удаление яичников не сопровождается снижением его содержания в крови и моче. В организме повышается содержание тестостерона и андростендиона (андрогенное воздействие). Стабильно высокая продукция гонадотропинов (в десятки раз!) – «пиковая флюктуация» . Гонадотропины – ингибиторы апоптоза и индукторы-посредники пролиферации. 57
 Основным методом лечения больных с ММ в постменопаузе является оперативное - удаление матки. В пери- и постменопаузальном возрасте – соблюдать разумную онкологическую настороженность (саркома в узле, рак эндометрия, опухоль яичника). 58
Основным методом лечения больных с ММ в постменопаузе является оперативное - удаление матки. В пери- и постменопаузальном возрасте – соблюдать разумную онкологическую настороженность (саркома в узле, рак эндометрия, опухоль яичника). 58
 ХИРУРГИЧЕСКИЕ КОНСЕРВАТИВНЫЕ ü Миомэктомия при простой миоме. ü Миомэктомия с гормональной терапией. ü Эмболизация сосудов матки (эффективнее при пролиферирующей). 59
ХИРУРГИЧЕСКИЕ КОНСЕРВАТИВНЫЕ ü Миомэктомия при простой миоме. ü Миомэктомия с гормональной терапией. ü Эмболизация сосудов матки (эффективнее при пролиферирующей). 59
 Под «истинным ростом» понимают количественное увеличение мышечной массы, размеров миоцитов, их ядер, разрастание стромы, формирование новых «зон роста» миом. «Ложный рост» происходит за счет отека, нарушения кровоснабжения в миоматозных узлах. Истинный рост наблюдается в 15, 7%, ложный – в 62, 2% случаев. 60
Под «истинным ростом» понимают количественное увеличение мышечной массы, размеров миоцитов, их ядер, разрастание стромы, формирование новых «зон роста» миом. «Ложный рост» происходит за счет отека, нарушения кровоснабжения в миоматозных узлах. Истинный рост наблюдается в 15, 7%, ложный – в 62, 2% случаев. 60
 Консервативное лечение Позволяет в ряде случаев избежать удаления матки, так как в первые 2 года постменопаузы миома матки регрессирует или даже полностью исчезает. Консервативная терапия нередко позволяет затормозить дальнейший рост опухоли, нормализовать гормональные нарушения. 61
Консервативное лечение Позволяет в ряде случаев избежать удаления матки, так как в первые 2 года постменопаузы миома матки регрессирует или даже полностью исчезает. Консервативная терапия нередко позволяет затормозить дальнейший рост опухоли, нормализовать гормональные нарушения. 61
 Гормональная терапия ПРОГЕСТАГЕНЫ Производные прогестерона, тестостерона, нороксипрогестерона: – Норколут; – Прималют-нор; – Норэтистерон ацетат. Эффект сомнительный нередко противоположный, побочные явления (неврологические, нейро-эндокринные). В патогенезе ММ прогестерон играет ключевую роль. Прогестероны блокируют рецепторы к прогестерону 62
Гормональная терапия ПРОГЕСТАГЕНЫ Производные прогестерона, тестостерона, нороксипрогестерона: – Норколут; – Прималют-нор; – Норэтистерон ацетат. Эффект сомнительный нередко противоположный, побочные явления (неврологические, нейро-эндокринные). В патогенезе ММ прогестерон играет ключевую роль. Прогестероны блокируют рецепторы к прогестерону 62
 Гормональная терапия АНТИПРОГЕСТАГЕНЫ Мифепристон (блокирует действие П на уровне рецепторов, уменьшает кровоснабжение узлов опухоли) – по 50 мг – 30 дней. Противопоказания: надпочечниковая и печеночная недостаточность, длительное применение глюкокортикоидов, воспалительные заболевания, гиперплазия эндометрия, заболевания почек, беременность. 63
Гормональная терапия АНТИПРОГЕСТАГЕНЫ Мифепристон (блокирует действие П на уровне рецепторов, уменьшает кровоснабжение узлов опухоли) – по 50 мг – 30 дней. Противопоказания: надпочечниковая и печеночная недостаточность, длительное применение глюкокортикоидов, воспалительные заболевания, гиперплазия эндометрия, заболевания почек, беременность. 63
 Гормональная терапия Антагонисты гонадолиберина qоказывает обратимое угнетающее воздействие на гипофизарно-яичниковую систему; qснижает уровень гонадотропных гормонов; qдействует на уровне гипоталамуса; qподавляет клеточную пролиферацию; qоказывает антиэстрогенный и антипрогестероновый эффект. Назначают по 200 -400 мг/сут. однократно 4 -6 мес. – назначают по 2, 5 мг* 2 раза в сут – 6 мес Под действием препаратов этой группы происходит значительное уменьшение внутриопухолевого кровотока, количества микрососудов, повышается индекс резистентности. 64
Гормональная терапия Антагонисты гонадолиберина qоказывает обратимое угнетающее воздействие на гипофизарно-яичниковую систему; qснижает уровень гонадотропных гормонов; qдействует на уровне гипоталамуса; qподавляет клеточную пролиферацию; qоказывает антиэстрогенный и антипрогестероновый эффект. Назначают по 200 -400 мг/сут. однократно 4 -6 мес. – назначают по 2, 5 мг* 2 раза в сут – 6 мес Под действием препаратов этой группы происходит значительное уменьшение внутриопухолевого кровотока, количества микрососудов, повышается индекс резистентности. 64
 Гормональная терапия Агонисты гонадолиберина - Гн. РГ q Гозерелин; q Нафарелин; q Бусерелин – 0, 2% р-р в носовые ходы * 3 раза в день 4 -6 мес. q Золадекс – 3, 6 мг/28 дн. *3 -6 мес. +премарин 0, 3 мг/сут. с 1 -25 д. ц. Пульсирующий выброс гонадолиберина поддерживает секрецию гонадотропинов. Длительное – приводит к десентизации и псевдоменопаузе (гипоэстрогения), снижению кровоснабжения матки, подавлению неоангиогенеза. Гн. РГ – уменьшают размеры миом, снижают васкуляризацию, подавляют активность неоангиогенеза путем склеротических изменений в активных зонах роста. 65
Гормональная терапия Агонисты гонадолиберина - Гн. РГ q Гозерелин; q Нафарелин; q Бусерелин – 0, 2% р-р в носовые ходы * 3 раза в день 4 -6 мес. q Золадекс – 3, 6 мг/28 дн. *3 -6 мес. +премарин 0, 3 мг/сут. с 1 -25 д. ц. Пульсирующий выброс гонадолиберина поддерживает секрецию гонадотропинов. Длительное – приводит к десентизации и псевдоменопаузе (гипоэстрогения), снижению кровоснабжения матки, подавлению неоангиогенеза. Гн. РГ – уменьшают размеры миом, снижают васкуляризацию, подавляют активность неоангиогенеза путем склеротических изменений в активных зонах роста. 65
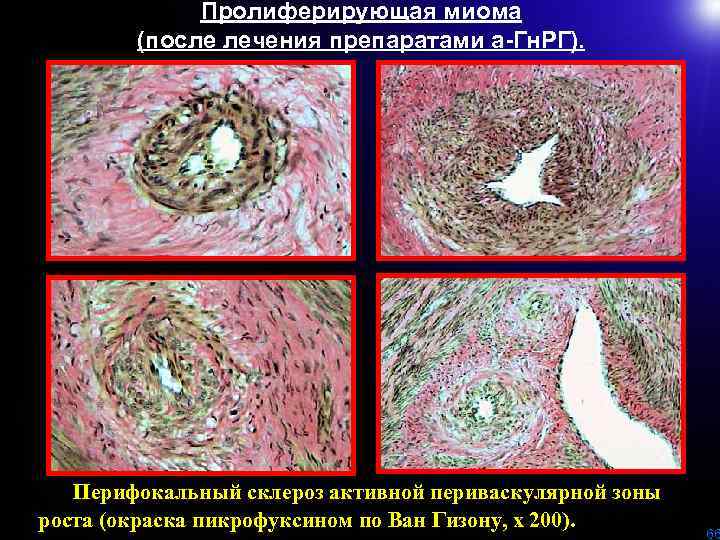 Пролиферирующая миома (после лечения препаратами а-Гн. РГ). Перифокальный склероз активной периваскулярной зоны роста (окраска пикрофуксином по Ван Гизону, х 200). 66
Пролиферирующая миома (после лечения препаратами а-Гн. РГ). Перифокальный склероз активной периваскулярной зоны роста (окраска пикрофуксином по Ван Гизону, х 200). 66
 Лечение в зависимости от клинико-морфологического варианта развития миомы матки. ПРОСТАЯ МИОМА МАТКИ 1. МИОМЭКТОМИЯ 2. ПРОФИЛАКТИКА НАРУШЕНИЯ ПИТАНИЯ В УЗЛАХ (СПАЗМОЛИТИКИ, АНТИАГЕГАНТЫ) ПРОЛИФЕРИРУЮЩАЯ МИОМА МАТКИ 1. МИОМЭКТОМИЯ ДОМИНИРУЮЩЕГО УЗЛА 2. ГОРМОНАЛЬНАЯ ТЕРАПИЯ 3. ЭМБОЛИЗАЦИЯ СОСУДОВ МАТКИ 4 ФУЗ Консервативная миомэктомия эффективна при простой миоме. При пролиферирующей миоме матки – возможны рецидивы. 67
Лечение в зависимости от клинико-морфологического варианта развития миомы матки. ПРОСТАЯ МИОМА МАТКИ 1. МИОМЭКТОМИЯ 2. ПРОФИЛАКТИКА НАРУШЕНИЯ ПИТАНИЯ В УЗЛАХ (СПАЗМОЛИТИКИ, АНТИАГЕГАНТЫ) ПРОЛИФЕРИРУЮЩАЯ МИОМА МАТКИ 1. МИОМЭКТОМИЯ ДОМИНИРУЮЩЕГО УЗЛА 2. ГОРМОНАЛЬНАЯ ТЕРАПИЯ 3. ЭМБОЛИЗАЦИЯ СОСУДОВ МАТКИ 4 ФУЗ Консервативная миомэктомия эффективна при простой миоме. При пролиферирующей миоме матки – возможны рецидивы. 67
 Лечение больных с миомой матки является не простой проблемой… 68
Лечение больных с миомой матки является не простой проблемой… 68
 v Гормональная терапия в лечении миомы матки недостаточно эффективна и сопровождается существенными отрицательными эффектами, ограничивающими их применение. v Подавляет овуляцию, выключает механизм образования желтого тела v Эндометрий длительно существует без влияния прогестерона v Атрофия эндометрия v Отрицательное влияние на систему гемостаза (гиперкоагуляция, венозные тромбозы) v Отр. влияние на структуру молочных желез v Склероз стенок сосудов матки и др. 69
v Гормональная терапия в лечении миомы матки недостаточно эффективна и сопровождается существенными отрицательными эффектами, ограничивающими их применение. v Подавляет овуляцию, выключает механизм образования желтого тела v Эндометрий длительно существует без влияния прогестерона v Атрофия эндометрия v Отрицательное влияние на систему гемостаза (гиперкоагуляция, венозные тромбозы) v Отр. влияние на структуру молочных желез v Склероз стенок сосудов матки и др. 69
 Ø Операции миомэктомии небольших миоматозных узлов сопровождаются травмой миометрия, спаечным процессом, дефектами стенки матки, наличием рубца, коагуляционным ожогом и т. д. Ø Главное в лечении остановить дальнейший рост и развитие миоматозных узлов на стадии клинически незначимых, но это не гормональная терапия и не эмболизация узлов небольших размеров. 70
Ø Операции миомэктомии небольших миоматозных узлов сопровождаются травмой миометрия, спаечным процессом, дефектами стенки матки, наличием рубца, коагуляционным ожогом и т. д. Ø Главное в лечении остановить дальнейший рост и развитие миоматозных узлов на стадии клинически незначимых, но это не гормональная терапия и не эмболизация узлов небольших размеров. 70
 q Необходим поиск и оценка эффективности новых ЛС, влияющих на основные молекулярно-биологические процессы, которые сопровождают развитие ММ: Ø индукция апоптоза Øингибирование пролиферации и ангиогенеза Øподавление экспрессии ФР Ø угнетение активности ММРs 71
q Необходим поиск и оценка эффективности новых ЛС, влияющих на основные молекулярно-биологические процессы, которые сопровождают развитие ММ: Ø индукция апоптоза Øингибирование пролиферации и ангиогенеза Øподавление экспрессии ФР Ø угнетение активности ММРs 71
 НЕОАНГИОГЕНЕЗ ФАКТОРЫ РОСТА АПОПТОЗ ПРОЛИФЕРАЦИЯ ИНВАЗИЯ 72
НЕОАНГИОГЕНЕЗ ФАКТОРЫ РОСТА АПОПТОЗ ПРОЛИФЕРАЦИЯ ИНВАЗИЯ 72
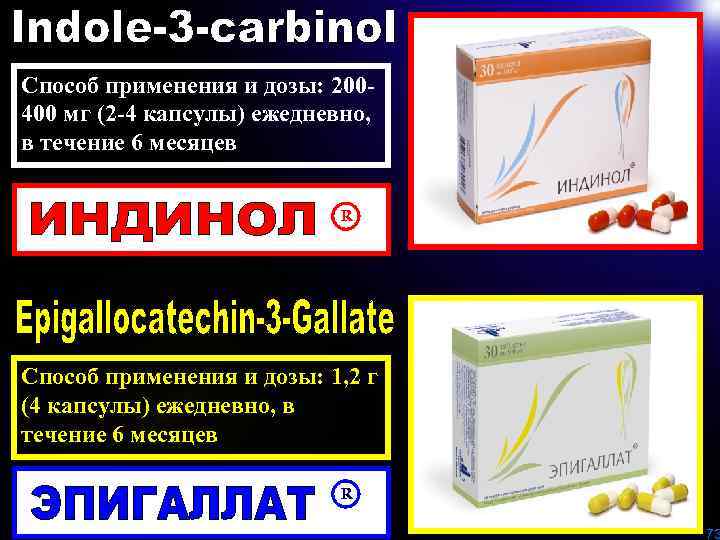 Способ применения и дозы: 200400 мг (2 -4 капсулы) ежедневно, в течение 6 месяцев R Способ применения и дозы: 1, 2 г (4 капсулы) ежедневно, в течение 6 месяцев R R 73
Способ применения и дозы: 200400 мг (2 -4 капсулы) ежедневно, в течение 6 месяцев R Способ применения и дозы: 1, 2 г (4 капсулы) ежедневно, в течение 6 месяцев R R 73
 Всего: 96 пациенток с миомой матки, средний возраст – 29, 4 +/- 1, 7 лет Критерии отбора Миома матки небольших размеров. Молодой возраст. Отсутствие показаний к операции Отказ от лечения гормональными препаратами 6 месяцев 74
Всего: 96 пациенток с миомой матки, средний возраст – 29, 4 +/- 1, 7 лет Критерии отбора Миома матки небольших размеров. Молодой возраст. Отсутствие показаний к операции Отказ от лечения гормональными препаратами 6 месяцев 74
 КЛИНИЧЕСКИЕ СИМПТОМЫ ПРИ МИОМЕ МАТКИ (ДО И ПОСЛЕ ЛЕЧЕНИЯ) БОЛЬ не связанная с менструальным циклом ГИПЕРПОЛИМЕНОРЕЯ МЕТРОРРАГИЯ АНЕМИЯ ДИЗУРИЯ Психоэмоциональные нарушения До лечения После лечения % 75
КЛИНИЧЕСКИЕ СИМПТОМЫ ПРИ МИОМЕ МАТКИ (ДО И ПОСЛЕ ЛЕЧЕНИЯ) БОЛЬ не связанная с менструальным циклом ГИПЕРПОЛИМЕНОРЕЯ МЕТРОРРАГИЯ АНЕМИЯ ДИЗУРИЯ Психоэмоциональные нарушения До лечения После лечения % 75
 Динамика размеров матки, узлов миом и участков аденомиоза у обследованных больных до и после лечения ИНДИНОЛОМ и ЭПИГАЛЛАТОМ ДО ЛЕЧЕНИЯ ОБЪЕМ МАТКИ ОБЪЕМ УЗЛОВ ТОЛЩИНА СТЕНКИ МАТКИ С АДЕНОМИОЗОМ 196 см³ 85 см³ 29 мм ЧЕРЕЗ 3 МЕСЯЦА 191 см³ 82 см³ 29 мм ЧЕРЕЗ 6 МЕСЯЦЕВ 180 см³ 78 см³ 25 мм ПОСЛЕ ЛЕЧЕНИЯ 76
Динамика размеров матки, узлов миом и участков аденомиоза у обследованных больных до и после лечения ИНДИНОЛОМ и ЭПИГАЛЛАТОМ ДО ЛЕЧЕНИЯ ОБЪЕМ МАТКИ ОБЪЕМ УЗЛОВ ТОЛЩИНА СТЕНКИ МАТКИ С АДЕНОМИОЗОМ 196 см³ 85 см³ 29 мм ЧЕРЕЗ 3 МЕСЯЦА 191 см³ 82 см³ 29 мм ЧЕРЕЗ 6 МЕСЯЦЕВ 180 см³ 78 см³ 25 мм ПОСЛЕ ЛЕЧЕНИЯ 76
 Степень уменьшения размеров (%) миоматозных узлов (диаметр до 4 см) в зависимости от морфотипа после лечения Индинолом и Эпигаллатом. Морфотип опухоли Через 6 месяцев Через 1 год Пролиферирующая ММ (n=18) 12, 3± 4, 6% 18, 1± 3, 9% Простая ММ (n=7) 7, 1± 1, 2% 9, 2± 1, 1% 77
Степень уменьшения размеров (%) миоматозных узлов (диаметр до 4 см) в зависимости от морфотипа после лечения Индинолом и Эпигаллатом. Морфотип опухоли Через 6 месяцев Через 1 год Пролиферирующая ММ (n=18) 12, 3± 4, 6% 18, 1± 3, 9% Простая ММ (n=7) 7, 1± 1, 2% 9, 2± 1, 1% 77
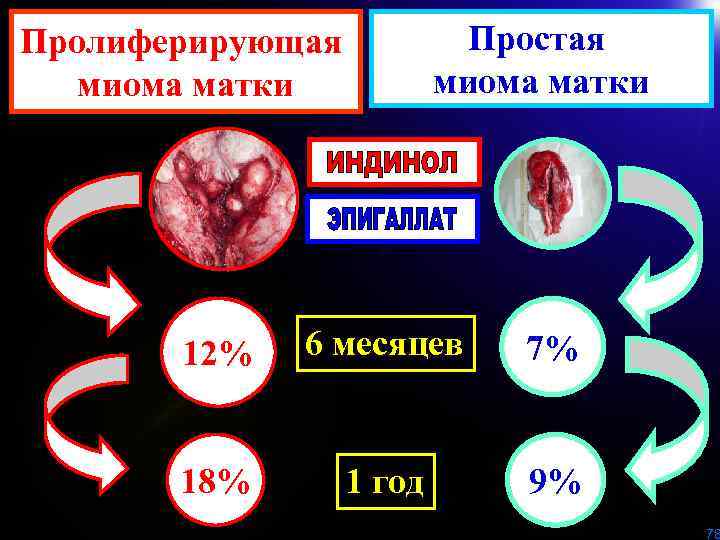 Простая миома матки Пролиферирующая миома матки 12% 6 месяцев 7% 18% 1 год 9% 78
Простая миома матки Пролиферирующая миома матки 12% 6 месяцев 7% 18% 1 год 9% 78
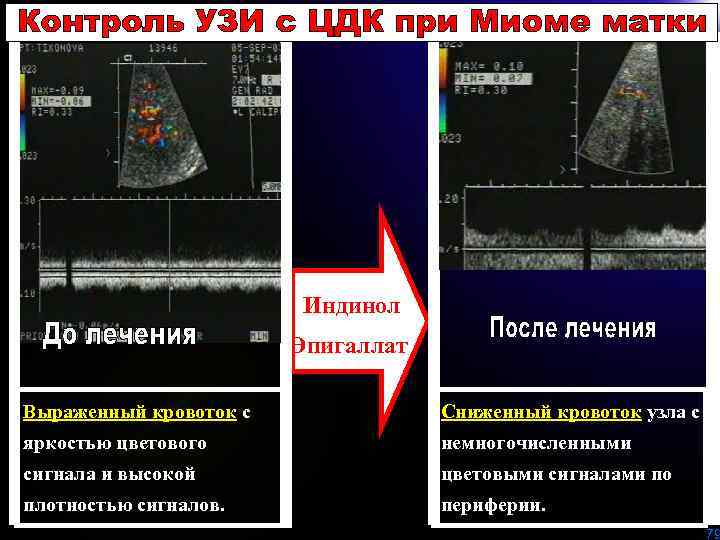 Индинол Эпигаллат Выраженный кровоток с Сниженный кровоток узла с яркостью цветового немногочисленными сигнала и высокой цветовыми сигналами по плотностью сигналов. периферии. 79
Индинол Эпигаллат Выраженный кровоток с Сниженный кровоток узла с яркостью цветового немногочисленными сигнала и высокой цветовыми сигналами по плотностью сигналов. периферии. 79
 R Контроль R R После лечения 80
R Контроль R R После лечения 80
 R Контроль R R После лечения 81
R Контроль R R После лечения 81
 R Контроль R R После лечения 82
R Контроль R R После лечения 82
 R Контроль R R После лечения 83
R Контроль R R После лечения 83
 Во всех случаях миомы матки, при отсутствии показаний к оперативному лечению. При профилактике рецидивирования и роста узлов после миомэктомии. 84
Во всех случаях миомы матки, при отсутствии показаний к оперативному лечению. При профилактике рецидивирования и роста узлов после миомэктомии. 84
 В чем заключается концепция будущей стратегии в терапии миомы матки? 85
В чем заключается концепция будущей стратегии в терапии миомы матки? 85
 (от англ. target — цель, мишень) 86
(от англ. target — цель, мишень) 86
 - принципиально новый метод терапии молекулярнонацеленного действия, точечным, прицельным образом воздействующий на ключевые звенья патогенетической цепи опухолевого и опухолевидного процессов. 87
- принципиально новый метод терапии молекулярнонацеленного действия, точечным, прицельным образом воздействующий на ключевые звенья патогенетической цепи опухолевого и опухолевидного процессов. 87
 - выгодно отличаются от классических лекарственных средств, оказывая патогенетически обоснованное действие лишь на опухолевые клетки. 88
- выгодно отличаются от классических лекарственных средств, оказывая патогенетически обоснованное действие лишь на опухолевые клетки. 88
 Результаты внедрения в клиническую практику первых таргетных препаратов доказали перспективность данного направления, способного значительно повысить эффективность медикаментозного лечения миомы матки. 89
Результаты внедрения в клиническую практику первых таргетных препаратов доказали перспективность данного направления, способного значительно повысить эффективность медикаментозного лечения миомы матки. 89
 90
90
 91
91
 Этапы миомэктомии 92
Этапы миомэктомии 92
 Этапы миомэктомии 93
Этапы миомэктомии 93
 Результат комплексного лечения миомы матки 94
Результат комплексного лечения миомы матки 94


