1 Алканы_2011.ppt
- Количество слайдов: 65
 1 Предмет и пути развития органической химии 1
1 Предмет и пути развития органической химии 1
 ПРЕДМЕТ И ПУТИ РАЗВИТИЯ ОРГАНИЧЕСКОЙ ХИМИИ Органическая химия изучает соединения углерода – углеводороды и их производные, в состав которых могут входить почти все элементы периодической системы. Углерод – это единственный элемент периодической системы, который образует самое большое число соединений. Это связано со способностью углеродных атомов соединяться не только с другими элементами, но и друг с другом. В результате образуются прямые, разветвленные и замкнутые (циклические) цепи. Причина этого состоит в том, что Есв между атомами С примерно такая же, как и у атома С с 2 другими элементами.
ПРЕДМЕТ И ПУТИ РАЗВИТИЯ ОРГАНИЧЕСКОЙ ХИМИИ Органическая химия изучает соединения углерода – углеводороды и их производные, в состав которых могут входить почти все элементы периодической системы. Углерод – это единственный элемент периодической системы, который образует самое большое число соединений. Это связано со способностью углеродных атомов соединяться не только с другими элементами, но и друг с другом. В результате образуются прямые, разветвленные и замкнутые (циклические) цепи. Причина этого состоит в том, что Есв между атомами С примерно такая же, как и у атома С с 2 другими элементами.
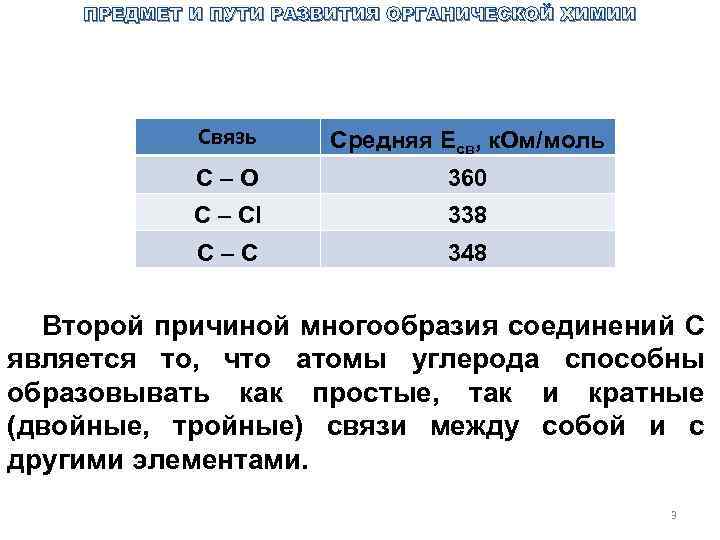 ПРЕДМЕТ И ПУТИ РАЗВИТИЯ ОРГАНИЧЕСКОЙ ХИМИИ Связь Средняя Есв, к. Ом/моль С – О 360 С – Сl 338 С – С 348 Второй причиной многообразия соединений С является то, что атомы углерода способны образовывать как простые, так и кратные (двойные, тройные) связи между собой и с другими элементами. 3
ПРЕДМЕТ И ПУТИ РАЗВИТИЯ ОРГАНИЧЕСКОЙ ХИМИИ Связь Средняя Есв, к. Ом/моль С – О 360 С – Сl 338 С – С 348 Второй причиной многообразия соединений С является то, что атомы углерода способны образовывать как простые, так и кратные (двойные, тройные) связи между собой и с другими элементами. 3
 ИСТОРИЯ РАЗВИТИЯ ОРГАНИЧЕСКОЙ ХИМИИ Строение и соединений классификация органических У любого органического соединения можно выделить две структурных части – углеродный скелет и функциональную группу. Углеродный скелет образуют атомы С, связанные между собой. Функциональная группа – это один атом или группа атомов, присоединенных к углеродному скелету. Они являются реакционноспособными центрами органической молекулы и определяют ее физические и химические свойства. 4
ИСТОРИЯ РАЗВИТИЯ ОРГАНИЧЕСКОЙ ХИМИИ Строение и соединений классификация органических У любого органического соединения можно выделить две структурных части – углеродный скелет и функциональную группу. Углеродный скелет образуют атомы С, связанные между собой. Функциональная группа – это один атом или группа атомов, присоединенных к углеродному скелету. Они являются реакционноспособными центрами органической молекулы и определяют ее физические и химические свойства. 4
 ИСТОРИЯ РАЗВИТИЯ ОРГАНИЧЕСКОЙ ХИМИИ Часто атом С, соединенный с функциональной группой, может входить в состав как углеродного скелета, так и функциональной группы. Кратные связи между атомами С в силу своей высокой реакционной способности также могут рассматриваться как функциональные группы. Известно более 100 различных 5 функциональных групп.
ИСТОРИЯ РАЗВИТИЯ ОРГАНИЧЕСКОЙ ХИМИИ Часто атом С, соединенный с функциональной группой, может входить в состав как углеродного скелета, так и функциональной группы. Кратные связи между атомами С в силу своей высокой реакционной способности также могут рассматриваться как функциональные группы. Известно более 100 различных 5 функциональных групп.
 ИСТОРИЯ РАЗВИТИЯ ОРГАНИЧЕСКОЙ ХИМИИ Классическая органическая химия рассматривает соединения, в молекулах которых атомы С соединены с атомами Hal, О, N, S и Р. Соединения С с другими элементами относятся к элементоорганической химии. Классификацию органических соединений можно провести по углеродному скелету или по функциональной группе. Изучая строение углеводорода используют классификацию органических соединений по структуре его углеродного скелета. 6
ИСТОРИЯ РАЗВИТИЯ ОРГАНИЧЕСКОЙ ХИМИИ Классическая органическая химия рассматривает соединения, в молекулах которых атомы С соединены с атомами Hal, О, N, S и Р. Соединения С с другими элементами относятся к элементоорганической химии. Классификацию органических соединений можно провести по углеродному скелету или по функциональной группе. Изучая строение углеводорода используют классификацию органических соединений по структуре его углеродного скелета. 6
 КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 7
КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 7
 РЕАКЦИИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ ТИПЫ РАЗРЫВА ХИМИЧЕСКИХ СВЯЗЕЙ В органических соединениях химическая связь образуется пары валентных электронов (ē↑↓). Химическая реакция – это процесс, в котором распадаются одни химические связи и образуются новые. При этом число валентных электронов, участвующих в химической связи, остается постоянным. Поэтому число вновь образовавшихся связей равно числу распавшихся. Углеводороды обычно имеют ковалентный тип связи. Существуют два типа разрыва химической связи: 1) гомолитический разрыв – электронная пара, образующая связь, делится поровну между полученными частями молекулы, т. е. каждая часть приобретает по 1ē. Полученные части молекулы являются электронейтральными и очень реакционноспособными, т. к. имеют неспаренный ē. 8
РЕАКЦИИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ ТИПЫ РАЗРЫВА ХИМИЧЕСКИХ СВЯЗЕЙ В органических соединениях химическая связь образуется пары валентных электронов (ē↑↓). Химическая реакция – это процесс, в котором распадаются одни химические связи и образуются новые. При этом число валентных электронов, участвующих в химической связи, остается постоянным. Поэтому число вновь образовавшихся связей равно числу распавшихся. Углеводороды обычно имеют ковалентный тип связи. Существуют два типа разрыва химической связи: 1) гомолитический разрыв – электронная пара, образующая связь, делится поровну между полученными частями молекулы, т. е. каждая часть приобретает по 1ē. Полученные части молекулы являются электронейтральными и очень реакционноспособными, т. к. имеют неспаренный ē. 8
 РЕАКЦИИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ СН 3 – СН 2 – СН 3 – СН 2* + СН 3* этильный радикал метильный радикал Радикал – это частица, обладающая неспаренным ē. Cl 2 Cl* + Cl* Такие реакции протекают, как правило, в газовой среде или в неполярных растворителях. Чтобы разорвать связь необходимо сообщить молекуле определенное количество энергии (Е), превышающее энергию связи (Есв). Эта энергия распределена между радикалами. 9
РЕАКЦИИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ СН 3 – СН 2 – СН 3 – СН 2* + СН 3* этильный радикал метильный радикал Радикал – это частица, обладающая неспаренным ē. Cl 2 Cl* + Cl* Такие реакции протекают, как правило, в газовой среде или в неполярных растворителях. Чтобы разорвать связь необходимо сообщить молекуле определенное количество энергии (Е), превышающее энергию связи (Есв). Эта энергия распределена между радикалами. 9
 СЫРЬЕВЫЕ ИСТОЧНИКИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 1. Природные газы – обычно сопутствуют нефти. Они содержат ~ 95 % метана (СН 4) и ~ 2 % других углеводородов (этана, пропана, бутана и др. ). Их разделяют на компоненты фракционной перегонкой при низких температурах. Основные направления переработки природных газов: – пиролиз (термическое разложение) на ацетилен, водород и газовую сажу; – неполное окисление до оксида углерода (СО); – хлорирование с целью получения хлорсодержащих растворителей. 2. Нефть – это геохимические остатки растений и животных. Месторождения нефти находятся в России, США, Южной и Центральной Америке, Иране и Румынии. 10
СЫРЬЕВЫЕ ИСТОЧНИКИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 1. Природные газы – обычно сопутствуют нефти. Они содержат ~ 95 % метана (СН 4) и ~ 2 % других углеводородов (этана, пропана, бутана и др. ). Их разделяют на компоненты фракционной перегонкой при низких температурах. Основные направления переработки природных газов: – пиролиз (термическое разложение) на ацетилен, водород и газовую сажу; – неполное окисление до оксида углерода (СО); – хлорирование с целью получения хлорсодержащих растворителей. 2. Нефть – это геохимические остатки растений и животных. Месторождения нефти находятся в России, США, Южной и Центральной Америке, Иране и Румынии. 10
 СЫРЬЕВЫЕ ИСТОЧНИКИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Нефть состоит из углеводородов с небольшой примесью кислородных, сернистых, азотистых и других соединений. По составу различают нефти парафиновые, нафтеновые и ароматические. Разгонкой при обычном давлении нефть разделяют на 3 фракции: бензин (30 – 180 C), керосин (180 – 300 C) и мазут (остаток от перегонки). Из этих основных фракций нефти выделяют более узкие фракции: петролейный (нефтяной) эфир (30 – 180 C), лигроин (110 – 140 C), уайт-спирит (150 – 210 C) и газойль (270 – 300 C). Из мазута перегонкой под низким давлением получают соляровое масло, смазочные масла, вазелин и твердый парафин. Основной способ переработки нефти – крекинг. Это термическое разложение углеводородов и других составных частей нефти. Чем выше температура, тем больше скорость крекинга и больше выход газов и 11 ароматических углеводородов.
СЫРЬЕВЫЕ ИСТОЧНИКИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Нефть состоит из углеводородов с небольшой примесью кислородных, сернистых, азотистых и других соединений. По составу различают нефти парафиновые, нафтеновые и ароматические. Разгонкой при обычном давлении нефть разделяют на 3 фракции: бензин (30 – 180 C), керосин (180 – 300 C) и мазут (остаток от перегонки). Из этих основных фракций нефти выделяют более узкие фракции: петролейный (нефтяной) эфир (30 – 180 C), лигроин (110 – 140 C), уайт-спирит (150 – 210 C) и газойль (270 – 300 C). Из мазута перегонкой под низким давлением получают соляровое масло, смазочные масла, вазелин и твердый парафин. Основной способ переработки нефти – крекинг. Это термическое разложение углеводородов и других составных частей нефти. Чем выше температура, тем больше скорость крекинга и больше выход газов и 11 ароматических углеводородов.
 СЫРЬЕВЫЕ ИСТОЧНИКИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 3. Каменный уголь и другие виды ископаемых углей. В промышленности используют следующие способы переработки каменного угля: сухая перегонка (коксование, полукоксование), гидрирование, неполное сгорание, получение карбида кальция. Сухую перегонку применяют для получения кокса или бытового газа. Газы коксования содержат этан, этилен, водород и углекислый газ. Гидрирование угля проводят при 400 – 600 C под давлением водорода 250 атм на катализаторе – оксидах железа. Образуется жидкая смесь углеводородов, которую гидрируют на никелевом катализаторе с получением простейших углеводородов. Неполное сгорание угля дает оксид углерода (СО). В технике используют три типа газообразных смесей, содержащих СО: 12
СЫРЬЕВЫЕ ИСТОЧНИКИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 3. Каменный уголь и другие виды ископаемых углей. В промышленности используют следующие способы переработки каменного угля: сухая перегонка (коксование, полукоксование), гидрирование, неполное сгорание, получение карбида кальция. Сухую перегонку применяют для получения кокса или бытового газа. Газы коксования содержат этан, этилен, водород и углекислый газ. Гидрирование угля проводят при 400 – 600 C под давлением водорода 250 атм на катализаторе – оксидах железа. Образуется жидкая смесь углеводородов, которую гидрируют на никелевом катализаторе с получением простейших углеводородов. Неполное сгорание угля дает оксид углерода (СО). В технике используют три типа газообразных смесей, содержащих СО: 12
 СЫРЬЕВЫЕ ИСТОЧНИКИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ – генераторный газ С + О 2 = СО 2 СО 2 + С = 2 СО – водяной газ С + Н 2 О = Н 2 + СО – синтез-газ образуется при каталитическом взаимодействии природного газа (метана) с водяным паром, диоксидом углерода или кислородом при 800 – 900 C с катализатором Ni. O или Al 2 O 3: СН 4 + Н 2 О = СО + 3 Н 2 СН 4 + СО 2 = 2 СО + 2 Н 2 2 СН 4 + О 2 = 2 СО + 4 Н 2 СО используют в технике для получения смесей углеводородов при обычном давлении или спиртов при повышенном давлении. Карбид кальция (Ca. C 2) получают из угля и извести. В дальнейшем он перерабатывается в ацетилен (C 2 Н 2). 13
СЫРЬЕВЫЕ ИСТОЧНИКИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ – генераторный газ С + О 2 = СО 2 СО 2 + С = 2 СО – водяной газ С + Н 2 О = Н 2 + СО – синтез-газ образуется при каталитическом взаимодействии природного газа (метана) с водяным паром, диоксидом углерода или кислородом при 800 – 900 C с катализатором Ni. O или Al 2 O 3: СН 4 + Н 2 О = СО + 3 Н 2 СН 4 + СО 2 = 2 СО + 2 Н 2 2 СН 4 + О 2 = 2 СО + 4 Н 2 СО используют в технике для получения смесей углеводородов при обычном давлении или спиртов при повышенном давлении. Карбид кальция (Ca. C 2) получают из угля и извести. В дальнейшем он перерабатывается в ацетилен (C 2 Н 2). 13
 СЫРЬЕВЫЕ ИСТОЧНИКИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 4. Сланцы. Их перерабатывают в высококалорийный бытовой газ. Смолу, образующуюся при пиролизе сланцев, используют для получения фенолов. Органическую составляющую сланцев – кероген – перерабатывают в двухосновные кислоты. 5. Продукты сельского и лесного хозяйства. Этиловый спирт получают при брожении глюкозы, которая образуется при гидролитическом расщеплении клетчатки (из древесины) или крахмала (из хлебных злаков и картофеля). Из глюкозы синтезируют витамин С и лимонную кислоту. Скипидар и канифоль производят из живицы или древесины хвойных пород. Из эфирных масел получают витамин А, цитраль и другие душистые вещества. 14
СЫРЬЕВЫЕ ИСТОЧНИКИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 4. Сланцы. Их перерабатывают в высококалорийный бытовой газ. Смолу, образующуюся при пиролизе сланцев, используют для получения фенолов. Органическую составляющую сланцев – кероген – перерабатывают в двухосновные кислоты. 5. Продукты сельского и лесного хозяйства. Этиловый спирт получают при брожении глюкозы, которая образуется при гидролитическом расщеплении клетчатки (из древесины) или крахмала (из хлебных злаков и картофеля). Из глюкозы синтезируют витамин С и лимонную кислоту. Скипидар и канифоль производят из живицы или древесины хвойных пород. Из эфирных масел получают витамин А, цитраль и другие душистые вещества. 14
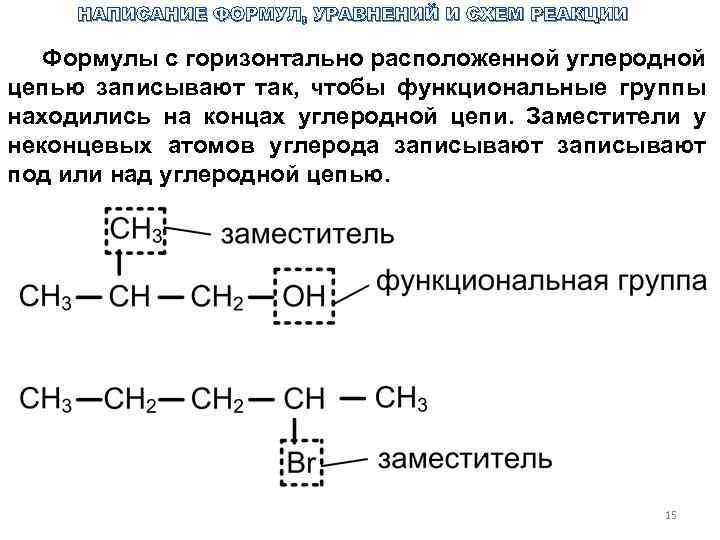 НАПИСАНИЕ ФОРМУЛ, УРАВНЕНИЙ И СХЕМ РЕАКЦИИ Формулы с горизонтально расположенной углеродной цепью записывают так, чтобы функциональные группы находились на концах углеродной цепи. Заместители у неконцевых атомов углерода записывают под или над углеродной цепью. 15
НАПИСАНИЕ ФОРМУЛ, УРАВНЕНИЙ И СХЕМ РЕАКЦИИ Формулы с горизонтально расположенной углеродной цепью записывают так, чтобы функциональные группы находились на концах углеродной цепи. Заместители у неконцевых атомов углерода записывают под или над углеродной цепью. 15
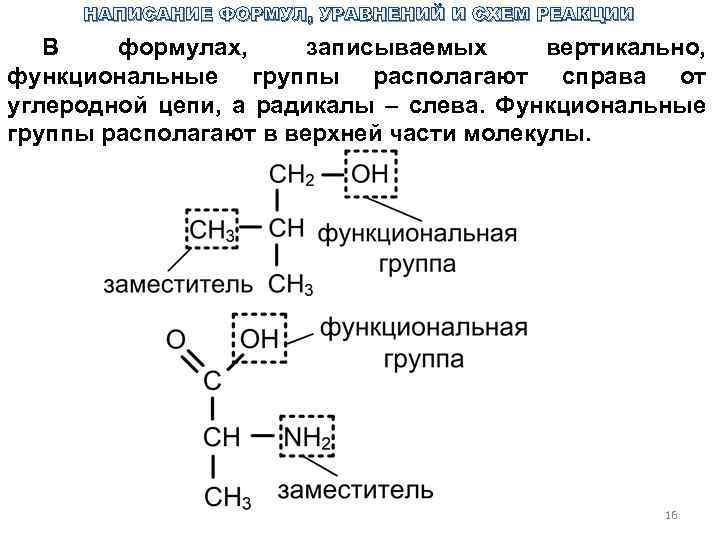 НАПИСАНИЕ ФОРМУЛ, УРАВНЕНИЙ И СХЕМ РЕАКЦИИ В формулах, записываемых вертикально, функциональные группы располагают справа от углеродной цепи, а радикалы – слева. Функциональные группы располагают в верхней части молекулы. 16
НАПИСАНИЕ ФОРМУЛ, УРАВНЕНИЙ И СХЕМ РЕАКЦИИ В формулах, записываемых вертикально, функциональные группы располагают справа от углеродной цепи, а радикалы – слева. Функциональные группы располагают в верхней части молекулы. 16
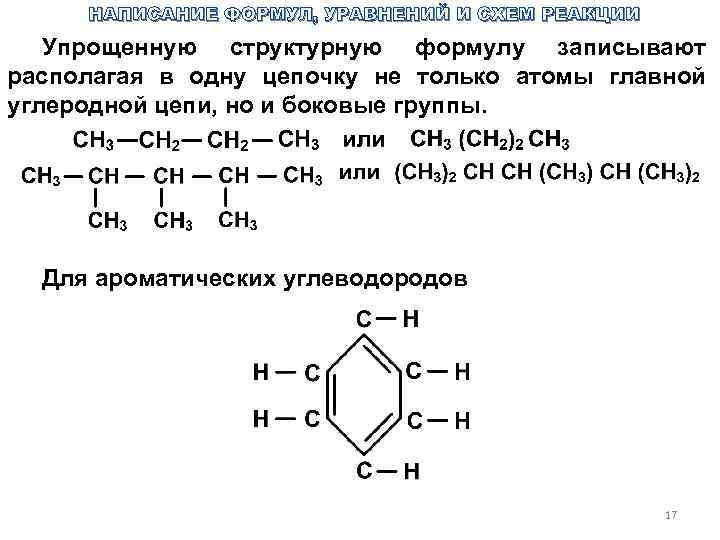 НАПИСАНИЕ ФОРМУЛ, УРАВНЕНИЙ И СХЕМ РЕАКЦИИ Упрощенную структурную формулу записывают располагая в одну цепочку не только атомы главной углеродной цепи, но и боковые группы. Для ароматических углеводородов 17
НАПИСАНИЕ ФОРМУЛ, УРАВНЕНИЙ И СХЕМ РЕАКЦИИ Упрощенную структурную формулу записывают располагая в одну цепочку не только атомы главной углеродной цепи, но и боковые группы. Для ароматических углеводородов 17
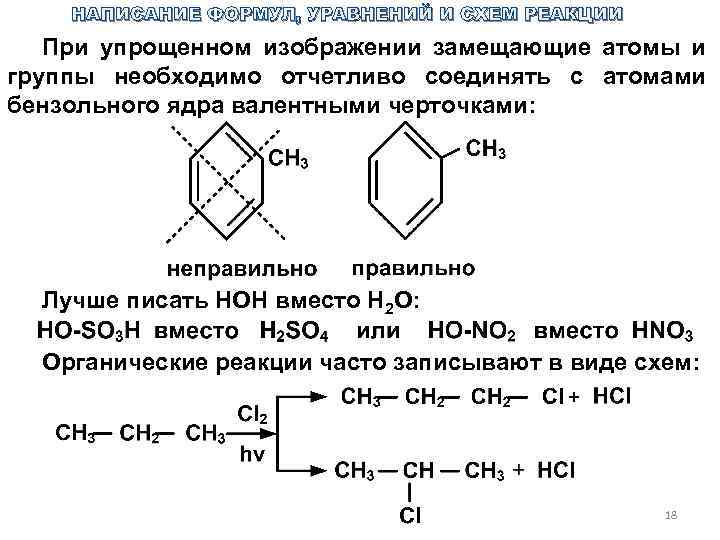 НАПИСАНИЕ ФОРМУЛ, УРАВНЕНИЙ И СХЕМ РЕАКЦИИ При упрощенном изображении замещающие атомы и группы необходимо отчетливо соединять с атомами бензольного ядра валентными черточками: Лучше писать НОН вместо Н 2 О: Органические реакции часто записывают в виде схем: 18
НАПИСАНИЕ ФОРМУЛ, УРАВНЕНИЙ И СХЕМ РЕАКЦИИ При упрощенном изображении замещающие атомы и группы необходимо отчетливо соединять с атомами бензольного ядра валентными черточками: Лучше писать НОН вместо Н 2 О: Органические реакции часто записывают в виде схем: 18
 . НАПИСАНИЕ ФОРМУЛ, УРАВНЕНИЙ И СХЕМ РЕАКЦИИ или Коэффициенты в схемах не проставляют. Некоторые вещества, например H 2, HCl, H 2 O, Na. Cl, образующиеся в реакциях, указывают над или под стрелкой. Под стрелкой указывают условия реакции, катализатор и другие параметры. Иногда под стрелкой в схемах указывают исходные вещества, которые в результате взаимодействия образуют реагент, обозначаемый над стрелкой: 19
. НАПИСАНИЕ ФОРМУЛ, УРАВНЕНИЙ И СХЕМ РЕАКЦИИ или Коэффициенты в схемах не проставляют. Некоторые вещества, например H 2, HCl, H 2 O, Na. Cl, образующиеся в реакциях, указывают над или под стрелкой. Под стрелкой указывают условия реакции, катализатор и другие параметры. Иногда под стрелкой в схемах указывают исходные вещества, которые в результате взаимодействия образуют реагент, обозначаемый над стрелкой: 19
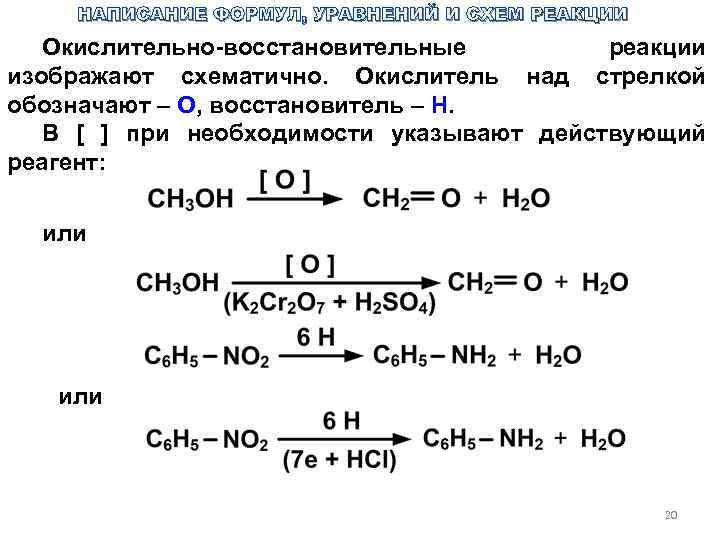 НАПИСАНИЕ ФОРМУЛ, УРАВНЕНИЙ И СХЕМ РЕАКЦИИ Окислительно-восстановительные реакции изображают схематично. Окислитель над стрелкой обозначают – О, восстановитель – Н. В [ ] при необходимости указывают действующий реагент: или 20
НАПИСАНИЕ ФОРМУЛ, УРАВНЕНИЙ И СХЕМ РЕАКЦИИ Окислительно-восстановительные реакции изображают схематично. Окислитель над стрелкой обозначают – О, восстановитель – Н. В [ ] при необходимости указывают действующий реагент: или 20
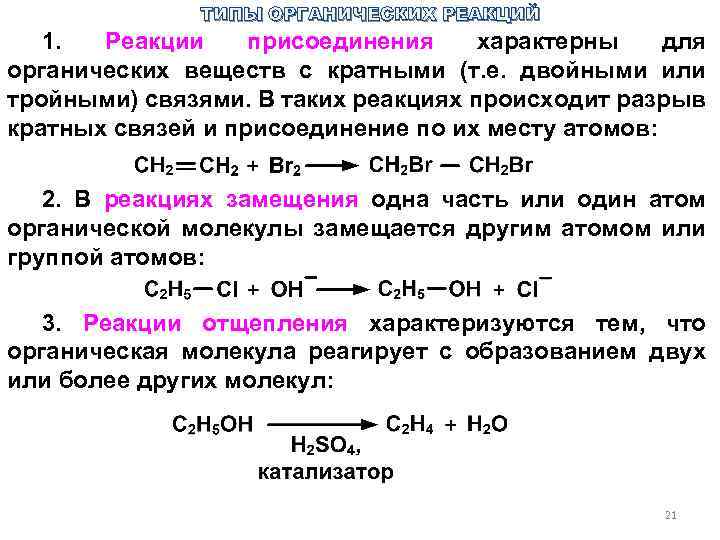 ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ 1. Реакции присоединения характерны для органических веществ с кратными (т. е. двойными или тройными) связями. В таких реакциях происходит разрыв кратных связей и присоединение по их месту атомов: 2. В реакциях замещения одна часть или один атом органической молекулы замещается другим атомом или группой атомов: 3. Реакции отщепления характеризуются тем, что органическая молекула реагирует с образованием двух или более других молекул: 21
ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ 1. Реакции присоединения характерны для органических веществ с кратными (т. е. двойными или тройными) связями. В таких реакциях происходит разрыв кратных связей и присоединение по их месту атомов: 2. В реакциях замещения одна часть или один атом органической молекулы замещается другим атомом или группой атомов: 3. Реакции отщепления характеризуются тем, что органическая молекула реагирует с образованием двух или более других молекул: 21
 ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ Химические реакции в органической химии, как правило, протекают в одну сторону необратимо, т. е. из продуктов реакции нельзя восстановить исходные вещества. Поэтому для этих реакций Кр не имеет смысла. Органические реакции характеризуются энергией и скоростью процесса, т. е. константой скорости (К) и энергией активации (Еа). 4. Реакции перегруппировки или изомерного перехода, в которых меняется структура молекул, но не происходит отщепления или присоединения атомов или групп атомов: 22
ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ Химические реакции в органической химии, как правило, протекают в одну сторону необратимо, т. е. из продуктов реакции нельзя восстановить исходные вещества. Поэтому для этих реакций Кр не имеет смысла. Органические реакции характеризуются энергией и скоростью процесса, т. е. константой скорости (К) и энергией активации (Еа). 4. Реакции перегруппировки или изомерного перехода, в которых меняется структура молекул, но не происходит отщепления или присоединения атомов или групп атомов: 22
 ТИПЫ РЕАГЕНТОВ Чтобы произошла реакция, реагирующие молекулы должны столкнуться. Условно можно считать, что одна молекула атакует другую. Атакуемая молекула называется субстратом, а атакующая – реагентом. Пусть молекула-субстрат имеет полярную связь. В ту сторону, куда смещается электронная пара в туже сторону смещается отрицательный «–» электрический заряд. Положительный «+» электрический заряд смещается в противоположную сторону. Такая молекула называется полярной. Её электрический заряд распределен неравномерно. 23
ТИПЫ РЕАГЕНТОВ Чтобы произошла реакция, реагирующие молекулы должны столкнуться. Условно можно считать, что одна молекула атакует другую. Атакуемая молекула называется субстратом, а атакующая – реагентом. Пусть молекула-субстрат имеет полярную связь. В ту сторону, куда смещается электронная пара в туже сторону смещается отрицательный «–» электрический заряд. Положительный «+» электрический заряд смещается в противоположную сторону. Такая молекула называется полярной. Её электрический заряд распределен неравномерно. 23
 ТИПЫ РЕАГЕНТОВ Реагенты могут быть также заряженными или полярными. Они делятся на нуклеофилы и электрофилы. Нуклеофилы стремятся к «+» : ОН–, CN–, Br–, : NH 3, H 2 O: Электрофилы стремятся к «–» : NO 2+, SO 3+, H 3 O+ 24
ТИПЫ РЕАГЕНТОВ Реагенты могут быть также заряженными или полярными. Они делятся на нуклеофилы и электрофилы. Нуклеофилы стремятся к «+» : ОН–, CN–, Br–, : NH 3, H 2 O: Электрофилы стремятся к «–» : NO 2+, SO 3+, H 3 O+ 24
 УГЛЕВОДОРОДЫ Это вещества, состоящие из двух элементов – углерода (С) и водорода (Н). При этом атом углерода образует углеродную цепь – скелет молекулы, а атом водорода присоединяется к этой цепи, дополняя свободные валентности углерода до четырех. Если в молекуле углеводорода все связи одинарные или простые, то такие углеводороды называются насыщенными или алканами. Все связи носят ковалентный характер. Чтобы понять характер связи рассмотрим электронную структуру атома С. С 1 s 2 2 p 4 25
УГЛЕВОДОРОДЫ Это вещества, состоящие из двух элементов – углерода (С) и водорода (Н). При этом атом углерода образует углеродную цепь – скелет молекулы, а атом водорода присоединяется к этой цепи, дополняя свободные валентности углерода до четырех. Если в молекуле углеводорода все связи одинарные или простые, то такие углеводороды называются насыщенными или алканами. Все связи носят ковалентный характер. Чтобы понять характер связи рассмотрим электронную структуру атома С. С 1 s 2 2 p 4 25
 УГЛЕВОДОРОДЫ Исходя из электронной структуры, атом С должен проявлять валентность +2, однако известно, что в органических молекулах атом С проявляет валентность +4. Объяснение этому дает теория гибридизации связей. В молекулах алканов атом С находится в sp 3 гибридном состоянии, т. е. 2 s и 2 p орбитали принимают одинаковую конфигурацию, энергетически уравновешиваются и 2 s и 2 p электроны равномерно распределены между этими орбиталями. В итоге получаем: 26
УГЛЕВОДОРОДЫ Исходя из электронной структуры, атом С должен проявлять валентность +2, однако известно, что в органических молекулах атом С проявляет валентность +4. Объяснение этому дает теория гибридизации связей. В молекулах алканов атом С находится в sp 3 гибридном состоянии, т. е. 2 s и 2 p орбитали принимают одинаковую конфигурацию, энергетически уравновешиваются и 2 s и 2 p электроны равномерно распределены между этими орбиталями. В итоге получаем: 26
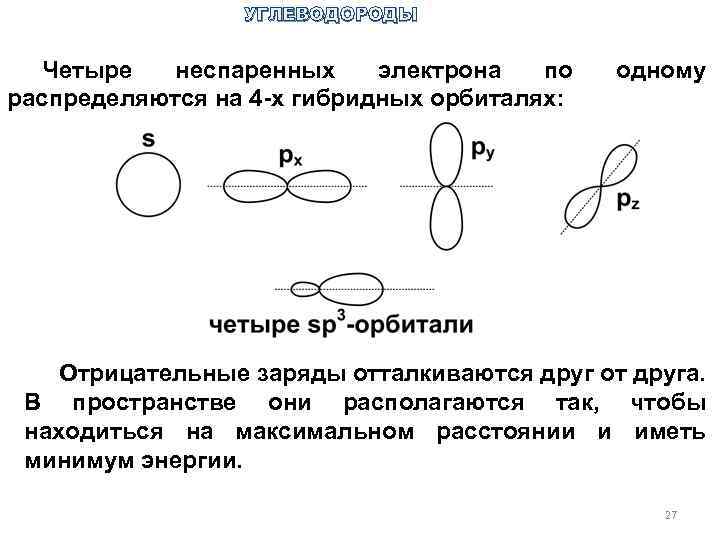 УГЛЕВОДОРОДЫ Четыре неспаренных электрона по распределяются на 4 -х гибридных орбиталях: одному Отрицательные заряды отталкиваются друг от друга. В пространстве они располагаются так, чтобы находиться на максимальном расстоянии и иметь минимум энергии. 27
УГЛЕВОДОРОДЫ Четыре неспаренных электрона по распределяются на 4 -х гибридных орбиталях: одному Отрицательные заряды отталкиваются друг от друга. В пространстве они располагаются так, чтобы находиться на максимальном расстоянии и иметь минимум энергии. 27
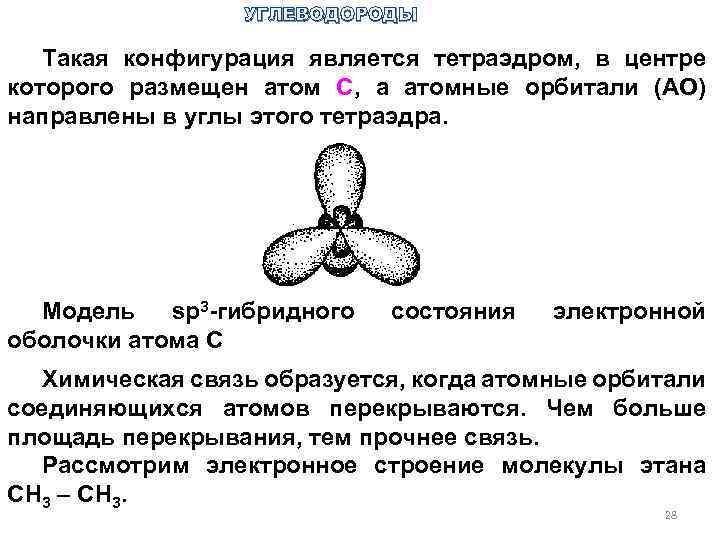 УГЛЕВОДОРОДЫ Такая конфигурация является тетраэдром, в центре которого размещен атом С, а атомные орбитали (АО) направлены в углы этого тетраэдра. Модель sp 3 -гибридного оболочки атома С состояния электронной Химическая связь образуется, когда атомные орбитали соединяющихся атомов перекрываются. Чем больше площадь перекрывания, тем прочнее связь. Рассмотрим электронное строение молекулы этана СН 3 – СН 3. 28
УГЛЕВОДОРОДЫ Такая конфигурация является тетраэдром, в центре которого размещен атом С, а атомные орбитали (АО) направлены в углы этого тетраэдра. Модель sp 3 -гибридного оболочки атома С состояния электронной Химическая связь образуется, когда атомные орбитали соединяющихся атомов перекрываются. Чем больше площадь перекрывания, тем прочнее связь. Рассмотрим электронное строение молекулы этана СН 3 – СН 3. 28
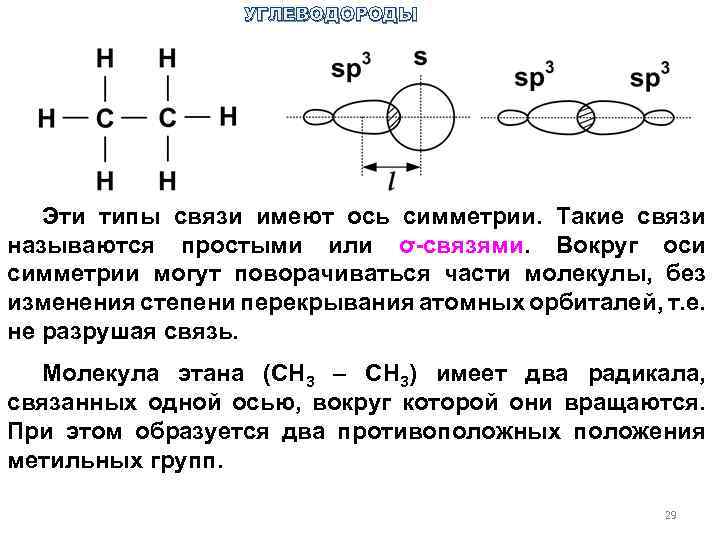 УГЛЕВОДОРОДЫ Эти типы связи имеют ось симметрии. Такие связи называются простыми или σ-связями. Вокруг оси симметрии могут поворачиваться части молекулы, без изменения степени перекрывания атомных орбиталей, т. е. не разрушая связь. Молекула этана (СН 3 – СН 3) имеет два радикала, связанных одной осью, вокруг которой они вращаются. При этом образуется два противоположных положения метильных групп. 29
УГЛЕВОДОРОДЫ Эти типы связи имеют ось симметрии. Такие связи называются простыми или σ-связями. Вокруг оси симметрии могут поворачиваться части молекулы, без изменения степени перекрывания атомных орбиталей, т. е. не разрушая связь. Молекула этана (СН 3 – СН 3) имеет два радикала, связанных одной осью, вокруг которой они вращаются. При этом образуется два противоположных положения метильных групп. 29
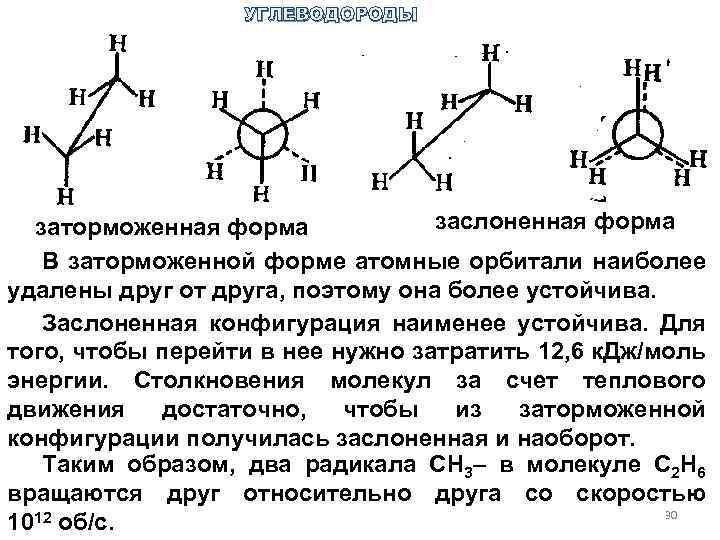 УГЛЕВОДОРОДЫ заслоненная форма заторможенная форма В заторможенной форме атомные орбитали наиболее удалены друг от друга, поэтому она более устойчива. Заслоненная конфигурация наименее устойчива. Для того, чтобы перейти в нее нужно затратить 12, 6 к. Дж/моль энергии. Столкновения молекул за счет теплового движения достаточно, чтобы из заторможенной конфигурации получилась заслоненная и наоборот. Таким образом, два радикала СН 3– в молекуле С 2 Н 6 вращаются друг относительно друга со скоростью 30 1012 об/с.
УГЛЕВОДОРОДЫ заслоненная форма заторможенная форма В заторможенной форме атомные орбитали наиболее удалены друг от друга, поэтому она более устойчива. Заслоненная конфигурация наименее устойчива. Для того, чтобы перейти в нее нужно затратить 12, 6 к. Дж/моль энергии. Столкновения молекул за счет теплового движения достаточно, чтобы из заторможенной конфигурации получилась заслоненная и наоборот. Таким образом, два радикала СН 3– в молекуле С 2 Н 6 вращаются друг относительно друга со скоростью 30 1012 об/с.
 АЛКАНЫ Их называют насыщенные, предельные, инертные, малоактивные углеводороды или парафины. СН 4 – метан – родоначальник гомологического ряда. Каждый последующий член ряда отличается от предыдущего на группу – СН 2 –. Это метильная группа. ИЗОМЕРИЯ. НОМЕНКЛАТУРА Для молекулы алканов характерно явление изомерии – молекулы алкана, имеющие одинаковую эмпирическую формулу различаются по строению. Явление изомерии начинается с четвертого члена ряда – бутана С 4 Н 10. 31
АЛКАНЫ Их называют насыщенные, предельные, инертные, малоактивные углеводороды или парафины. СН 4 – метан – родоначальник гомологического ряда. Каждый последующий член ряда отличается от предыдущего на группу – СН 2 –. Это метильная группа. ИЗОМЕРИЯ. НОМЕНКЛАТУРА Для молекулы алканов характерно явление изомерии – молекулы алкана, имеющие одинаковую эмпирическую формулу различаются по строению. Явление изомерии начинается с четвертого члена ряда – бутана С 4 Н 10. 31
 АЛКАНЫ Алканы называют по двум систематической и рациональной. номенклатурам: При названии по систематической (ИЮПАК) номенклатуре: 1. В формуле молекулы выбирают главную цепь – самую длинную. 2. Эту цепь нумеруют с того конца, к которому ближе расположен заместитель (радикал). Если заместителей несколько, то алкан нумеруют с того конца, к которому ближе радикал. 32
АЛКАНЫ Алканы называют по двум систематической и рациональной. номенклатурам: При названии по систематической (ИЮПАК) номенклатуре: 1. В формуле молекулы выбирают главную цепь – самую длинную. 2. Эту цепь нумеруют с того конца, к которому ближе расположен заместитель (радикал). Если заместителей несколько, то алкан нумеруют с того конца, к которому ближе радикал. 32
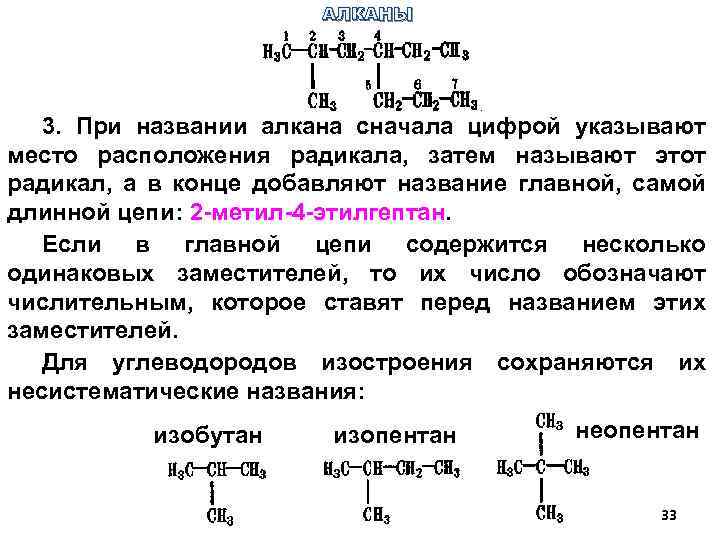 АЛКАНЫ 3. При названии алкана сначала цифрой указывают место расположения радикала, затем называют этот радикал, а в конце добавляют название главной, самой длинной цепи: 2 -метил-4 -этилгептан. Если в главной цепи содержится несколько одинаковых заместителей, то их число обозначают числительным, которое ставят перед названием этих заместителей. Для углеводородов изостроения сохраняются их несистематические названия: изобутан изопентан неопентан 33
АЛКАНЫ 3. При названии алкана сначала цифрой указывают место расположения радикала, затем называют этот радикал, а в конце добавляют название главной, самой длинной цепи: 2 -метил-4 -этилгептан. Если в главной цепи содержится несколько одинаковых заместителей, то их число обозначают числительным, которое ставят перед названием этих заместителей. Для углеводородов изостроения сохраняются их несистематические названия: изобутан изопентан неопентан 33
 АЛКАНЫ По рациональной номенклатуре алканы рассматривают как производные простейшего углеводорода – метана, в молекуле которого один или несколько водородных атомов замещены на радикалы. Эти радикалы называют по старшинству – от менее сложных к более сложным. Если эти заместители одинаковые, то указывают их количество. В основу названия включают слово “метан”: тетраметилметан (2, 2 -диметилпропан) метилэтилизопропилметан (2, 3 -диметилпентан) 34
АЛКАНЫ По рациональной номенклатуре алканы рассматривают как производные простейшего углеводорода – метана, в молекуле которого один или несколько водородных атомов замещены на радикалы. Эти радикалы называют по старшинству – от менее сложных к более сложным. Если эти заместители одинаковые, то указывают их количество. В основу названия включают слово “метан”: тетраметилметан (2, 2 -диметилпропан) метилэтилизопропилметан (2, 3 -диметилпентан) 34
 АЛКАНЫ Свою номенклатуру имеют углеводородные радикалы. Одновалентные радикалы называют алкилами. Их общая формула Сn. H 2 n+1. Названия радикалов составляют из названий соответствующих углеводородов заменой суффикса –ан на –ил. Двухвалентные радикалы называют, заменяя суффикс –ан на –илиден. Исключение – радикал метилен = СН 2. СПОСОБЫ ПОЛУЧЕНИЯ Основным источником насыщенных углеводородов является природный газ и сырая нефть. Природной смесью твердых высокомолекулярных алканов является горный воск (озокерит) – разновидность твердого природного битума. 1. Многократная фракционная перегонка природного газа или бензиновой фракции нефти. 35
АЛКАНЫ Свою номенклатуру имеют углеводородные радикалы. Одновалентные радикалы называют алкилами. Их общая формула Сn. H 2 n+1. Названия радикалов составляют из названий соответствующих углеводородов заменой суффикса –ан на –ил. Двухвалентные радикалы называют, заменяя суффикс –ан на –илиден. Исключение – радикал метилен = СН 2. СПОСОБЫ ПОЛУЧЕНИЯ Основным источником насыщенных углеводородов является природный газ и сырая нефть. Природной смесью твердых высокомолекулярных алканов является горный воск (озокерит) – разновидность твердого природного битума. 1. Многократная фракционная перегонка природного газа или бензиновой фракции нефти. 35
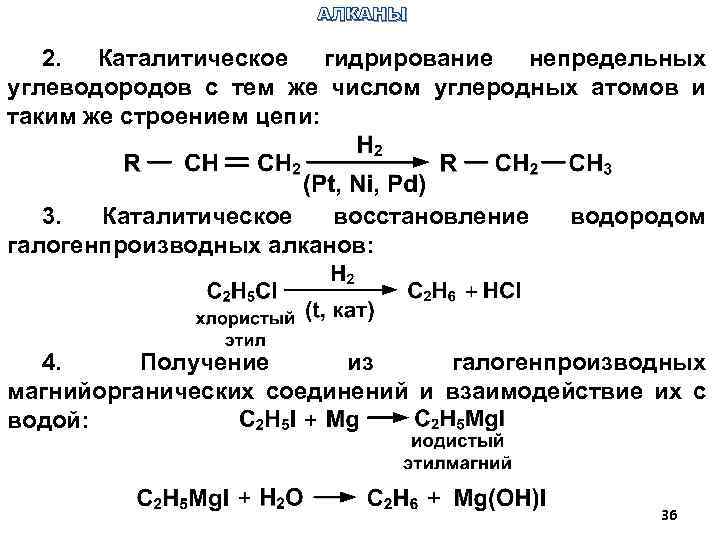 АЛКАНЫ 2. Каталитическое гидрирование непредельных углеводородов с тем же числом углеродных атомов и таким же строением цепи: 3. Каталитическое восстановление галогенпроизводных алканов: водородом 4. Получение из галогенпроизводных магнийорганических соединений и взаимодействие их с водой: 36
АЛКАНЫ 2. Каталитическое гидрирование непредельных углеводородов с тем же числом углеродных атомов и таким же строением цепи: 3. Каталитическое восстановление галогенпроизводных алканов: водородом 4. Получение из галогенпроизводных магнийорганических соединений и взаимодействие их с водой: 36
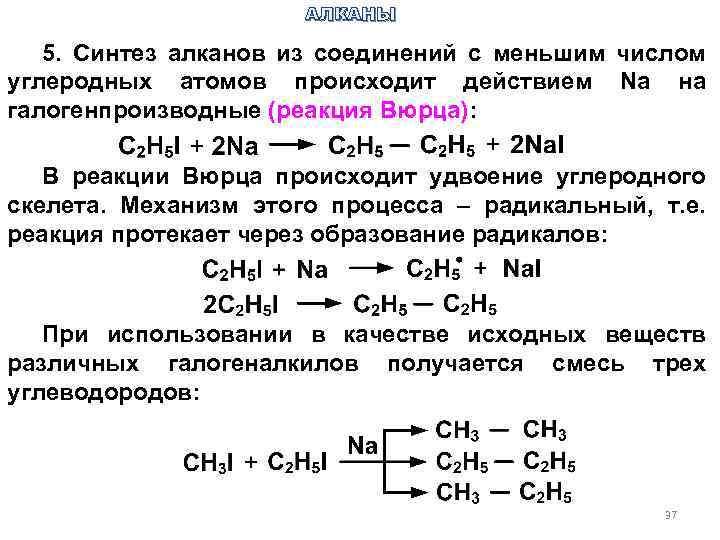 АЛКАНЫ 5. Синтез алканов из соединений с меньшим числом углеродных атомов происходит действием Na на галогенпроизводные (реакция Вюрца): В реакции Вюрца происходит удвоение углеродного скелета. Механизм этого процесса – радикальный, т. е. реакция протекает через образование радикалов: При использовании в качестве исходных веществ различных галогеналкилов получается смесь трех углеводородов: 37
АЛКАНЫ 5. Синтез алканов из соединений с меньшим числом углеродных атомов происходит действием Na на галогенпроизводные (реакция Вюрца): В реакции Вюрца происходит удвоение углеродного скелета. Механизм этого процесса – радикальный, т. е. реакция протекает через образование радикалов: При использовании в качестве исходных веществ различных галогеналкилов получается смесь трех углеводородов: 37
 АЛКАНЫ 6. Электролиз солей карбоновых кислот (реакция Кольбе). Соли карбоновых кислот в водном растворе диссоциируют: Под действием напряжения начинается диффузия ионов к катоду и аноду с образованием радикалов. На аноде: У каждого радикала углеродный скелет уменьшается на одну единицу и получается алкан с удвоенным числом атомов углерода (С – 2). Если используется смесь солей, то образуется смесь углеводородов аналогично реакции Вюрца. 38
АЛКАНЫ 6. Электролиз солей карбоновых кислот (реакция Кольбе). Соли карбоновых кислот в водном растворе диссоциируют: Под действием напряжения начинается диффузия ионов к катоду и аноду с образованием радикалов. На аноде: У каждого радикала углеродный скелет уменьшается на одну единицу и получается алкан с удвоенным числом атомов углерода (С – 2). Если используется смесь солей, то образуется смесь углеводородов аналогично реакции Вюрца. 38
 АЛКАНЫ ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ В ряду углеводородов с нормальной цепью алканы с числом атомов углерода 1 – 4 при нормальных условиях – газы, алканы с С 5 – С 15 – жидкости и, начиная с С 16 – твердые вещества. Алканы – это жирные углеводороды, не растворяются в воде, т. к. полярные молекулы воды притягиваются друг к другу сильнее, чем неполярные молекулы алканов. ХИМИЧЕСКИЕ СВОЙСТВА АЛКАНОВ Алканы обладают сравнительно низкой активностью. Они имеет два типа связей: С – С и С – Н. Низкая активность определяется прочностью этих связей ~ 350 к. Дж/моль и 414 к. Дж/моль. Связи являются ковалентными и молекулы алканов неполярны, что определяет их низкую активность. 39
АЛКАНЫ ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ В ряду углеводородов с нормальной цепью алканы с числом атомов углерода 1 – 4 при нормальных условиях – газы, алканы с С 5 – С 15 – жидкости и, начиная с С 16 – твердые вещества. Алканы – это жирные углеводороды, не растворяются в воде, т. к. полярные молекулы воды притягиваются друг к другу сильнее, чем неполярные молекулы алканов. ХИМИЧЕСКИЕ СВОЙСТВА АЛКАНОВ Алканы обладают сравнительно низкой активностью. Они имеет два типа связей: С – С и С – Н. Низкая активность определяется прочностью этих связей ~ 350 к. Дж/моль и 414 к. Дж/моль. Связи являются ковалентными и молекулы алканов неполярны, что определяет их низкую активность. 39
 АЛКАНЫ Атомы С находятся в sp 3 -гибридном состоянии, все атомные орбитали у атома С заняты. Для sp 3 -гибридизации необходимо затратить энергию, в количестве 406 к. Дж/моль. При этом валентность углерода увеличивается с 2 -х до 4 -х, что дает возможность образования 2 -х связей С – Н. В результате выделяется энергия 828 к. Дж/моль. Энергетически sp 3 -гибридизация очень выгодна. У алканов всего два типа связей, поэтому для них характерны 2 -а типа реакций: 1) реакция замещения связана с разрывом связи С – Н. При этом углеродный скелет остается без изменения; 40
АЛКАНЫ Атомы С находятся в sp 3 -гибридном состоянии, все атомные орбитали у атома С заняты. Для sp 3 -гибридизации необходимо затратить энергию, в количестве 406 к. Дж/моль. При этом валентность углерода увеличивается с 2 -х до 4 -х, что дает возможность образования 2 -х связей С – Н. В результате выделяется энергия 828 к. Дж/моль. Энергетически sp 3 -гибридизация очень выгодна. У алканов всего два типа связей, поэтому для них характерны 2 -а типа реакций: 1) реакция замещения связана с разрывом связи С – Н. При этом углеродный скелет остается без изменения; 40
 АЛКАНЫ 2) реакция расщепления связана с разрывом связи С – С, что ведет к изменению углеродного скелета молекулы. Хотя связи С – Н прочнее С – С, они легче вступают в реакцию. Химическая реакция – это процесс, связанный с разрывом одних связей и образованием других. В соответствии с законом сохранения энергии число электронов, дающих связи, остается постоянным. Поэтому число разрывающихся связей равно числу образующихся. Реакции могут быть простыми и сложными. В ходе смешивания, химической реакции и образования продуктов в сложных реакциях химическая система претерпевает ряд стадий. Цепь этих стадий образует механизм химической реакции. У простых реакций этот процесс протекает в одну стадию. 41
АЛКАНЫ 2) реакция расщепления связана с разрывом связи С – С, что ведет к изменению углеродного скелета молекулы. Хотя связи С – Н прочнее С – С, они легче вступают в реакцию. Химическая реакция – это процесс, связанный с разрывом одних связей и образованием других. В соответствии с законом сохранения энергии число электронов, дающих связи, остается постоянным. Поэтому число разрывающихся связей равно числу образующихся. Реакции могут быть простыми и сложными. В ходе смешивания, химической реакции и образования продуктов в сложных реакциях химическая система претерпевает ряд стадий. Цепь этих стадий образует механизм химической реакции. У простых реакций этот процесс протекает в одну стадию. 41
![АЛКАНЫ Скорость этой реакции записывается уравнением: ν = k [CH 3 CОCH 3]·[H 3 АЛКАНЫ Скорость этой реакции записывается уравнением: ν = k [CH 3 CОCH 3]·[H 3](https://present5.com/presentation/37730794_90882735/image-42.jpg) АЛКАНЫ Скорость этой реакции записывается уравнением: ν = k [CH 3 CОCH 3]·[H 3 O+] ν не зависит от [I 2], а зависит от [CH 3 COCH 3] и [H 3 O+], т. е. кислотности раствора, которая в уравнение реакции не входит. Поэтому реакция носит сложный, стадийный характер. Эта реакция протекает в 3 стадии: 42
АЛКАНЫ Скорость этой реакции записывается уравнением: ν = k [CH 3 CОCH 3]·[H 3 O+] ν не зависит от [I 2], а зависит от [CH 3 COCH 3] и [H 3 O+], т. е. кислотности раствора, которая в уравнение реакции не входит. Поэтому реакция носит сложный, стадийный характер. Эта реакция протекает в 3 стадии: 42
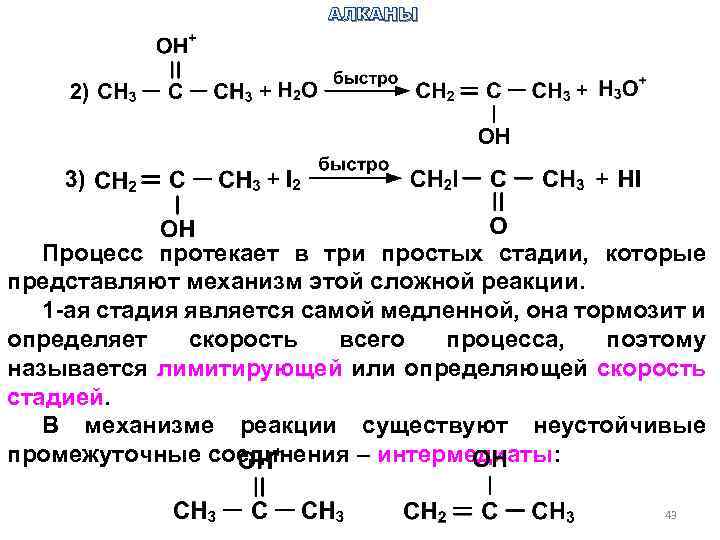 АЛКАНЫ Процесс протекает в три простых стадии, которые представляют механизм этой сложной реакции. 1 -ая стадия является самой медленной, она тормозит и определяет скорость всего процесса, поэтому называется лимитирующей или определяющей скорость стадией. В механизме реакции существуют неустойчивые промежуточные соединения – интермедиаты: 43
АЛКАНЫ Процесс протекает в три простых стадии, которые представляют механизм этой сложной реакции. 1 -ая стадия является самой медленной, она тормозит и определяет скорость всего процесса, поэтому называется лимитирующей или определяющей скорость стадией. В механизме реакции существуют неустойчивые промежуточные соединения – интермедиаты: 43
 АЛКАНЫ Обычно их так мало, что определить их каким либо методом анализа невозможно, но если их наличие установлено, то механизм реакции становится ясен. УСЛОВИЯ ПРОТЕКАНИЯ РЕАКЦИИ В ОДНУ СТАДИЮ Для протекания простой химической реакции необходимо 3 условия: 1) столкновение 2 -х реагирующих молекул (частиц) 2) каждое столкновение может быть результативным только в том случае, если Естолкн. > некоторого значения, которое называется Еактивации 3) чтобы столкновение было результативным, эти молекулы (частицы) должны быть ориентированы друг относительно друга вполне определенным образом. 44
АЛКАНЫ Обычно их так мало, что определить их каким либо методом анализа невозможно, но если их наличие установлено, то механизм реакции становится ясен. УСЛОВИЯ ПРОТЕКАНИЯ РЕАКЦИИ В ОДНУ СТАДИЮ Для протекания простой химической реакции необходимо 3 условия: 1) столкновение 2 -х реагирующих молекул (частиц) 2) каждое столкновение может быть результативным только в том случае, если Естолкн. > некоторого значения, которое называется Еактивации 3) чтобы столкновение было результативным, эти молекулы (частицы) должны быть ориентированы друг относительно друга вполне определенным образом. 44
 АЛКАНЫ Столкнувшиеся частицы на какое-то время образуют систему из этих частиц с определенным расположением атомов – конфигурацию. В этой конфигурации происходит ослабление и разрыв связей и образование и усиление других связей. В процессе конфигурации энергия (Еn) становится равной энергии столкновения (Ек). Если Еn > Eакт, то образовавшийся комплекс называется активированным (переходным) комплексом, который может распадаться на продукты реакции. Если система достигает активированного комплекса, она может распадаться на продукты реакции. 45
АЛКАНЫ Столкнувшиеся частицы на какое-то время образуют систему из этих частиц с определенным расположением атомов – конфигурацию. В этой конфигурации происходит ослабление и разрыв связей и образование и усиление других связей. В процессе конфигурации энергия (Еn) становится равной энергии столкновения (Ек). Если Еn > Eакт, то образовавшийся комплекс называется активированным (переходным) комплексом, который может распадаться на продукты реакции. Если система достигает активированного комплекса, она может распадаться на продукты реакции. 45
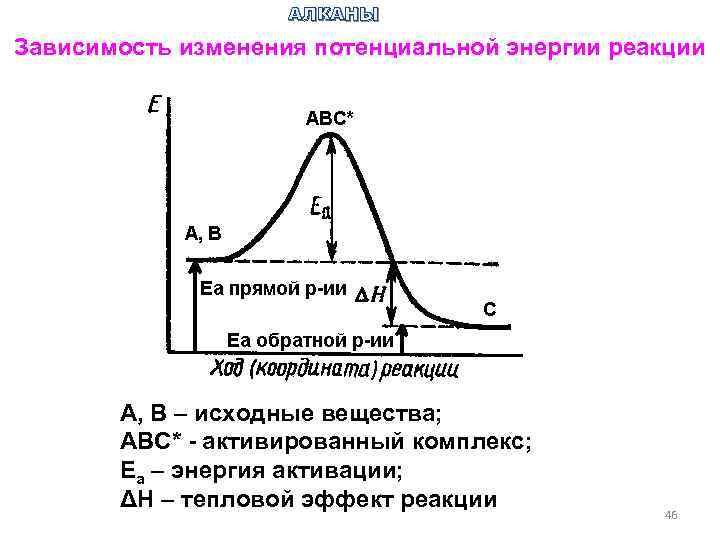 АЛКАНЫ Зависимость изменения потенциальной энергии реакции А, В – исходные вещества; АВС* - активированный комплекс; Еа – энергия активации; ΔН – тепловой эффект реакции 46
АЛКАНЫ Зависимость изменения потенциальной энергии реакции А, В – исходные вещества; АВС* - активированный комплекс; Еа – энергия активации; ΔН – тепловой эффект реакции 46
 АЛКАНЫ Тепловой эффект реакции (ΔН) равен разности между энергиями активации обратной и прямой реакций. ΔН = Еа прямой р-ии – Еа обратной р-ии. Все реакции, связанные с алканами, сопровождаются гомолитическим распадом связи, т. к. он наиболее выгоден. Поэтому в этих реакциях в качестве интермедиатов выступают радикалы, т. е. частицы с неспаренным ē. Механизм таких реакций радикальный. Есвязи между двумя атомами, в частности для связи С – Н, зависит от места ее положения, т. е. на нее влияют другие атомы. 47
АЛКАНЫ Тепловой эффект реакции (ΔН) равен разности между энергиями активации обратной и прямой реакций. ΔН = Еа прямой р-ии – Еа обратной р-ии. Все реакции, связанные с алканами, сопровождаются гомолитическим распадом связи, т. к. он наиболее выгоден. Поэтому в этих реакциях в качестве интермедиатов выступают радикалы, т. е. частицы с неспаренным ē. Механизм таких реакций радикальный. Есвязи между двумя атомами, в частности для связи С – Н, зависит от места ее положения, т. е. на нее влияют другие атомы. 47
 АЛКАНЫ Энергия связи (Есвязи) С – Н Соединения Есв, к. Дж/моль СН 3–Н 423 СН 3–СН 2–Н (СН 3)2–СН 2–Н (СН 3)3–С–Н 402 384 373 Поэтому реакции протекают избирательно, наиболее активные связи в молекулах с большим числом (порядком) связей С – С. ГАЛОГЕНИРОВАНИЕ АЛКАНОВ Реакция галогенирования – это процесс замещения атома Н атомами Hal при взаимодействии алканов с молекулами Hal. Скорость таких реакций определяется природой атома Hal в таком порядке: F > Cl > Br > I. 48
АЛКАНЫ Энергия связи (Есвязи) С – Н Соединения Есв, к. Дж/моль СН 3–Н 423 СН 3–СН 2–Н (СН 3)2–СН 2–Н (СН 3)3–С–Н 402 384 373 Поэтому реакции протекают избирательно, наиболее активные связи в молекулах с большим числом (порядком) связей С – С. ГАЛОГЕНИРОВАНИЕ АЛКАНОВ Реакция галогенирования – это процесс замещения атома Н атомами Hal при взаимодействии алканов с молекулами Hal. Скорость таких реакций определяется природой атома Hal в таком порядке: F > Cl > Br > I. 48
 АЛКАНЫ а) реакции со фтором протекают очень энергично, иногда со взрывом, в зависимости от количества фтора. Рассмотрим энергетический баланс реакции: СН 3 – СН 3 + F 2 → СН 3 – СН 2 F + HF 1) разрыв связи F – F ΔН = 160 к. Дж/моль 2) разрыв связи СН 3 СН 2–Н ΔН = 402 к. Дж/моль 3) образование связи С – FΔН = 412 к. Дж/моль 4) образование связи Н – FΔН = 570 к. Дж/моль ΔНреакции ΔН = – 460 к. Дж/моль Поскольку квант энергии элементарного взаимодействия, равный – 460 к. Дж/моль, превышает Есв С – С, то в избытке фтора процесс фторирования протекает с разрушением углеродного скелета и с образованием простых продуктов: СН 3 – СН 3 + 7 F 2 → 2 СF 4 + 6 HF 49
АЛКАНЫ а) реакции со фтором протекают очень энергично, иногда со взрывом, в зависимости от количества фтора. Рассмотрим энергетический баланс реакции: СН 3 – СН 3 + F 2 → СН 3 – СН 2 F + HF 1) разрыв связи F – F ΔН = 160 к. Дж/моль 2) разрыв связи СН 3 СН 2–Н ΔН = 402 к. Дж/моль 3) образование связи С – FΔН = 412 к. Дж/моль 4) образование связи Н – FΔН = 570 к. Дж/моль ΔНреакции ΔН = – 460 к. Дж/моль Поскольку квант энергии элементарного взаимодействия, равный – 460 к. Дж/моль, превышает Есв С – С, то в избытке фтора процесс фторирования протекает с разрушением углеродного скелета и с образованием простых продуктов: СН 3 – СН 3 + 7 F 2 → 2 СF 4 + 6 HF 49
 АЛКАНЫ Чтобы провести фторирование без разрушения углеродного скелета используют менее активные фторирующие реагенты, например Co. F 3: СН 4 + Co. F 3 → СН 3 F + Co. F 2 + HF б) хлорирование – реакция замещения атомов Н атомами Cl в молекуле углеводорода. Радикальный механизм характерен для всех реакций с участием алканов. Рассмотрим энергетический баланс реакции хлорирования: 1) разрыв связи Cl – Cl ΔН = + 249 к. Дж/моль 2) разрыв связи СН 3–Н ΔН = + 427 к. Дж/моль 3) образование связи С – Cl ΔН = – 348 к. Дж/моль 4) образование связи Н – Cl ΔН = – 431 к. Дж/моль ΔНреакции ΔН = – 109 к. Дж/моль 50
АЛКАНЫ Чтобы провести фторирование без разрушения углеродного скелета используют менее активные фторирующие реагенты, например Co. F 3: СН 4 + Co. F 3 → СН 3 F + Co. F 2 + HF б) хлорирование – реакция замещения атомов Н атомами Cl в молекуле углеводорода. Радикальный механизм характерен для всех реакций с участием алканов. Рассмотрим энергетический баланс реакции хлорирования: 1) разрыв связи Cl – Cl ΔН = + 249 к. Дж/моль 2) разрыв связи СН 3–Н ΔН = + 427 к. Дж/моль 3) образование связи С – Cl ΔН = – 348 к. Дж/моль 4) образование связи Н – Cl ΔН = – 431 к. Дж/моль ΔНреакции ΔН = – 109 к. Дж/моль 50
 АЛКАНЫ Выделяемый квант энергии Е при хлорировании алканов недостаточен для разрыва связи С – C, поэтому в процессе хлорирования углеродный скелет алкана остается без изменения. Реакция хлорирования имеет радикальный механизм, который развивается по типу цепной реакции, т. е. необходимо получение радикалов – активных частиц (интермедиатов). Такие частицы можно получить при распаде молекулы хлора. Газообразная смесь алкана с хлором может стоять в темноте длительное время без признаков реакции, однако на свету реакция быстро начинается и заканчивается. Эквимолярная смесь Cl 2 с СН 4 на свету может взорваться. 51
АЛКАНЫ Выделяемый квант энергии Е при хлорировании алканов недостаточен для разрыва связи С – C, поэтому в процессе хлорирования углеродный скелет алкана остается без изменения. Реакция хлорирования имеет радикальный механизм, который развивается по типу цепной реакции, т. е. необходимо получение радикалов – активных частиц (интермедиатов). Такие частицы можно получить при распаде молекулы хлора. Газообразная смесь алкана с хлором может стоять в темноте длительное время без признаков реакции, однако на свету реакция быстро начинается и заканчивается. Эквимолярная смесь Cl 2 с СН 4 на свету может взорваться. 51
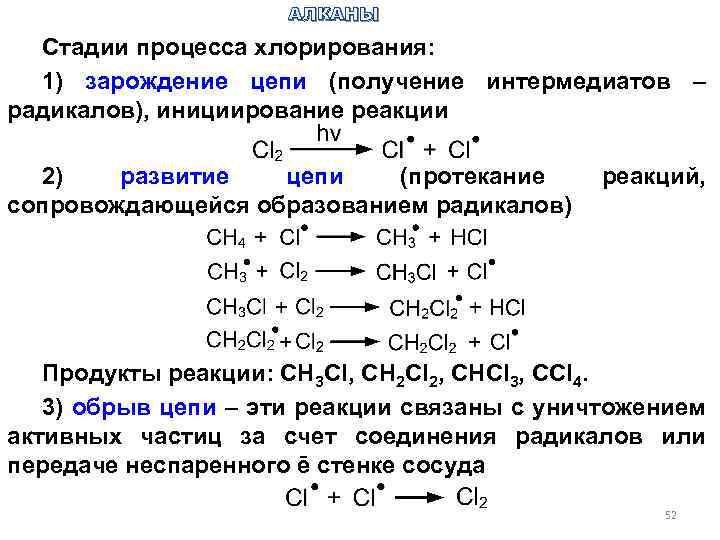 АЛКАНЫ Стадии процесса хлорирования: 1) зарождение цепи (получение интермедиатов – радикалов), инициирование реакции 2) развитие цепи (протекание сопровождающейся образованием радикалов) реакций, Продукты реакции: СН 3 Cl, СН 2 Cl 2, СНCl 3, СCl 4. 3) обрыв цепи – эти реакции связаны с уничтожением активных частиц за счет соединения радикалов или передаче неспаренного ē стенке сосуда 52
АЛКАНЫ Стадии процесса хлорирования: 1) зарождение цепи (получение интермедиатов – радикалов), инициирование реакции 2) развитие цепи (протекание сопровождающейся образованием радикалов) реакций, Продукты реакции: СН 3 Cl, СН 2 Cl 2, СНCl 3, СCl 4. 3) обрыв цепи – эти реакции связаны с уничтожением активных частиц за счет соединения радикалов или передаче неспаренного ē стенке сосуда 52
 АЛКАНЫ Неспаренный ē взаимодействует со стенкой сосуда гораздо реже, чем происходит соединение радикалов. в) бромирование протекает по типу хлорирования, только медленнее. Смесь С 6 Н 14 и паров Br 2 в темноте долго остается рыжей, а на свету окраска быстро исчезает за счет исчезновения атомов Br 2. С 6 Н 14 + Br 2 → С 6 Н 13 Br + НBr жидкость г) иодирование происходит очень медленно и обратимо. ОКИСЛЕНИЕ АЛКАНОВ а) горение При высокой температуре алканы энергично окисляются с выделением большого количества тепла, т. е. горят. 53
АЛКАНЫ Неспаренный ē взаимодействует со стенкой сосуда гораздо реже, чем происходит соединение радикалов. в) бромирование протекает по типу хлорирования, только медленнее. Смесь С 6 Н 14 и паров Br 2 в темноте долго остается рыжей, а на свету окраска быстро исчезает за счет исчезновения атомов Br 2. С 6 Н 14 + Br 2 → С 6 Н 13 Br + НBr жидкость г) иодирование происходит очень медленно и обратимо. ОКИСЛЕНИЕ АЛКАНОВ а) горение При высокой температуре алканы энергично окисляются с выделением большого количества тепла, т. е. горят. 53
 АЛКАНЫ Механизм горения – цепной, радикальный, протекает с разрывом связи С – С. CH 4(г) + 2 O 2(г) → CO 2(г) + 2 H 2 O(г) ΔH= – 890 к. Дж/моль C 8 H 18(ж)+12, 5 O 2(г)→ 8 CO 2(г)+9 H 2 O(г) ΔH= – 3511 к. Дж/моль бензин Алканы окисляются в паровой фазе, в которой и происходит хорошее смешивание с кислородом. При избытке O 2 алканы горят очень бледным незаметным пламенем с образованием углекислого газа (CO 2) и воды (H 2 O). При недостатке О 2 процесс может протекать с образованием продуктов неполного окисления углерода. CH 4 + 1, 5 O 2 → CO + 2 H 2 O CH 4 + O 2 → C + 2 H 2 O 54
АЛКАНЫ Механизм горения – цепной, радикальный, протекает с разрывом связи С – С. CH 4(г) + 2 O 2(г) → CO 2(г) + 2 H 2 O(г) ΔH= – 890 к. Дж/моль C 8 H 18(ж)+12, 5 O 2(г)→ 8 CO 2(г)+9 H 2 O(г) ΔH= – 3511 к. Дж/моль бензин Алканы окисляются в паровой фазе, в которой и происходит хорошее смешивание с кислородом. При избытке O 2 алканы горят очень бледным незаметным пламенем с образованием углекислого газа (CO 2) и воды (H 2 O). При недостатке О 2 процесс может протекать с образованием продуктов неполного окисления углерода. CH 4 + 1, 5 O 2 → CO + 2 H 2 O CH 4 + O 2 → C + 2 H 2 O 54
 АЛКАНЫ Раскаленные частицы несгоревшего углерода придают пламени яркую окраску (пламя светится). б) частичное окисление В промышленности в органическом синтезе очень часто приходится получать продукты частичного окисления алканов. Для этого используется окисление при 150 C в присутствии катализатора – перманганата калия (KMn. O 4) или оксида марганца (Mn. O 2). Эти условия способствуют образованию из алканов перекисных радикалов, а из них гидроперекисей: Дальнейшее взаимодействие гидроперекисей зависит от их строения. 55
АЛКАНЫ Раскаленные частицы несгоревшего углерода придают пламени яркую окраску (пламя светится). б) частичное окисление В промышленности в органическом синтезе очень часто приходится получать продукты частичного окисления алканов. Для этого используется окисление при 150 C в присутствии катализатора – перманганата калия (KMn. O 4) или оксида марганца (Mn. O 2). Эти условия способствуют образованию из алканов перекисных радикалов, а из них гидроперекисей: Дальнейшее взаимодействие гидроперекисей зависит от их строения. 55
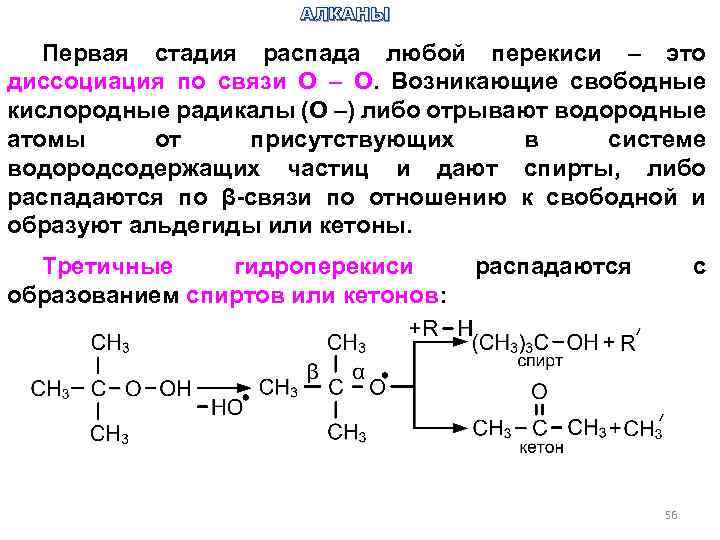 АЛКАНЫ Первая стадия распада любой перекиси – это диссоциация по связи О – О. Возникающие свободные кислородные радикалы (О –) либо отрывают водородные атомы от присутствующих в системе водородсодержащих частиц и дают спирты, либо распадаются по β-связи по отношению к свободной и образуют альдегиды или кетоны. Третичные гидроперекиси образованием спиртов или кетонов: распадаются с 56
АЛКАНЫ Первая стадия распада любой перекиси – это диссоциация по связи О – О. Возникающие свободные кислородные радикалы (О –) либо отрывают водородные атомы от присутствующих в системе водородсодержащих частиц и дают спирты, либо распадаются по β-связи по отношению к свободной и образуют альдегиды или кетоны. Третичные гидроперекиси образованием спиртов или кетонов: распадаются с 56
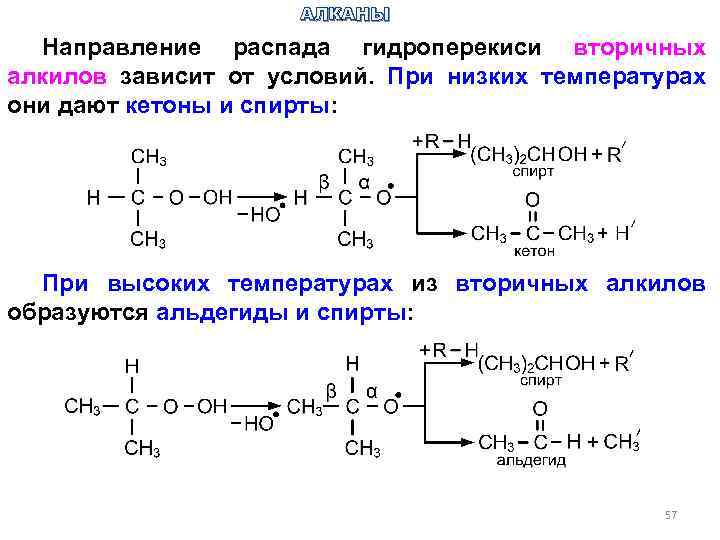 АЛКАНЫ Направление распада гидроперекиси вторичных алкилов зависит от условий. При низких температурах они дают кетоны и спирты: При высоких температурах из вторичных алкилов образуются альдегиды и спирты: 57
АЛКАНЫ Направление распада гидроперекиси вторичных алкилов зависит от условий. При низких температурах они дают кетоны и спирты: При высоких температурах из вторичных алкилов образуются альдегиды и спирты: 57
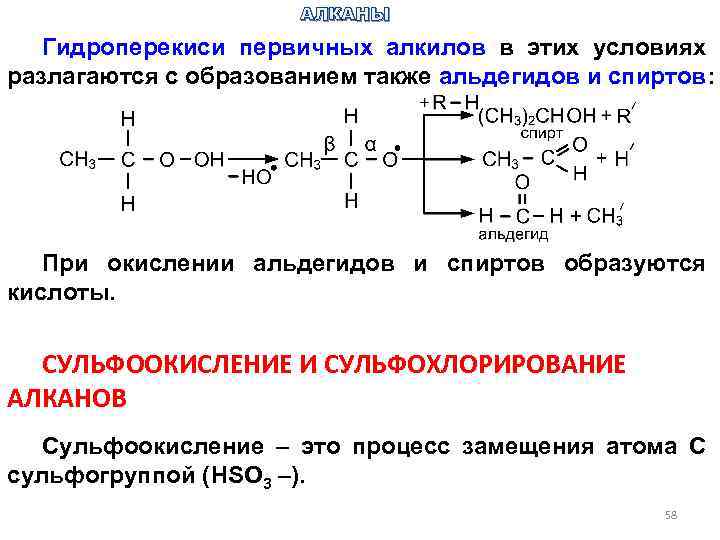 АЛКАНЫ Гидроперекиси первичных алкилов в этих условиях разлагаются с образованием также альдегидов и спиртов: При окислении альдегидов и спиртов образуются кислоты. СУЛЬФООКИСЛЕНИЕ И СУЛЬФОХЛОРИРОВАНИЕ АЛКАНОВ Сульфоокисление – это процесс замещения атома С сульфогруппой (HSO 3 –). 58
АЛКАНЫ Гидроперекиси первичных алкилов в этих условиях разлагаются с образованием также альдегидов и спиртов: При окислении альдегидов и спиртов образуются кислоты. СУЛЬФООКИСЛЕНИЕ И СУЛЬФОХЛОРИРОВАНИЕ АЛКАНОВ Сульфоокисление – это процесс замещения атома С сульфогруппой (HSO 3 –). 58
 АЛКАНЫ Алканы с H 2 SO 4 реагируют только при высокой температуре и с концентрированной кислотой: При высокой температуре с участием сернистого газа (SO 2) и хлора можно осуществить процесс сульфохлорирования: 59
АЛКАНЫ Алканы с H 2 SO 4 реагируют только при высокой температуре и с концентрированной кислотой: При высокой температуре с участием сернистого газа (SO 2) и хлора можно осуществить процесс сульфохлорирования: 59
 АЛКАНЫ Аналогичный процесс в присутствии SO 2 можно осуществить при участии О 2: Из хлорангидрида сульфокислоты взаимодействием со щелочью получают стиральный порошок: НИТРОВАНИЕ АЛКАНОВ Это процесс замещения атома водорода нитрогруппой (NO 2). Реакция протекает только при высокой температуре (300 C) в паровой фазе, т. к. только при этой температуре образуются активные частицы – радикалы. 60
АЛКАНЫ Аналогичный процесс в присутствии SO 2 можно осуществить при участии О 2: Из хлорангидрида сульфокислоты взаимодействием со щелочью получают стиральный порошок: НИТРОВАНИЕ АЛКАНОВ Это процесс замещения атома водорода нитрогруппой (NO 2). Реакция протекает только при высокой температуре (300 C) в паровой фазе, т. к. только при этой температуре образуются активные частицы – радикалы. 60
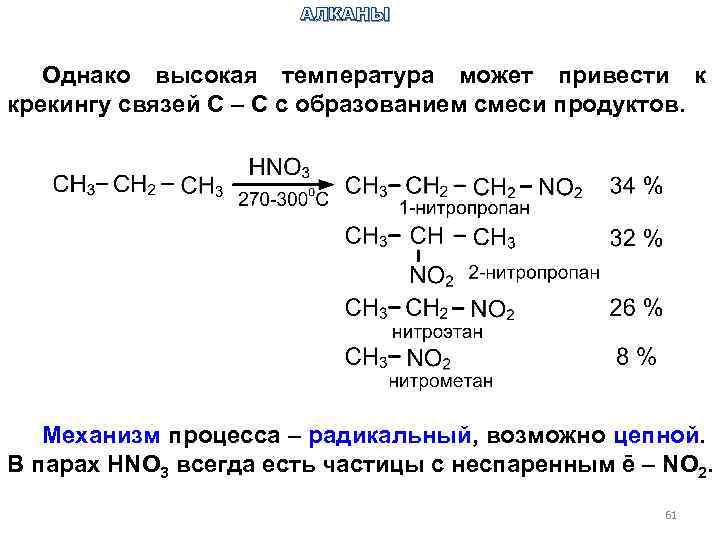 АЛКАНЫ Однако высокая температура может привести к крекингу связей С – С с образованием смеси продуктов. Механизм процесса – радикальный, возможно цепной. В парах HNO 3 всегда есть частицы с неспаренным ē – NO 2. 61
АЛКАНЫ Однако высокая температура может привести к крекингу связей С – С с образованием смеси продуктов. Механизм процесса – радикальный, возможно цепной. В парах HNO 3 всегда есть частицы с неспаренным ē – NO 2. 61
 АЛКАНЫ Начальная стадия нитрования – взаимодействие диоксида азота с углеводородом, в результате которого образуются свободные радикалы. С диоксидом азота эти радикалы дают нитросоединения или эфиры азотистой кислоты: КРЕКИНГ АЛКАНОВ При ~1000 C все связи в молекуле алкана разрываются с выделением водорода и эквивалентного количества угля (С): 62
АЛКАНЫ Начальная стадия нитрования – взаимодействие диоксида азота с углеводородом, в результате которого образуются свободные радикалы. С диоксидом азота эти радикалы дают нитросоединения или эфиры азотистой кислоты: КРЕКИНГ АЛКАНОВ При ~1000 C все связи в молекуле алкана разрываются с выделением водорода и эквивалентного количества угля (С): 62
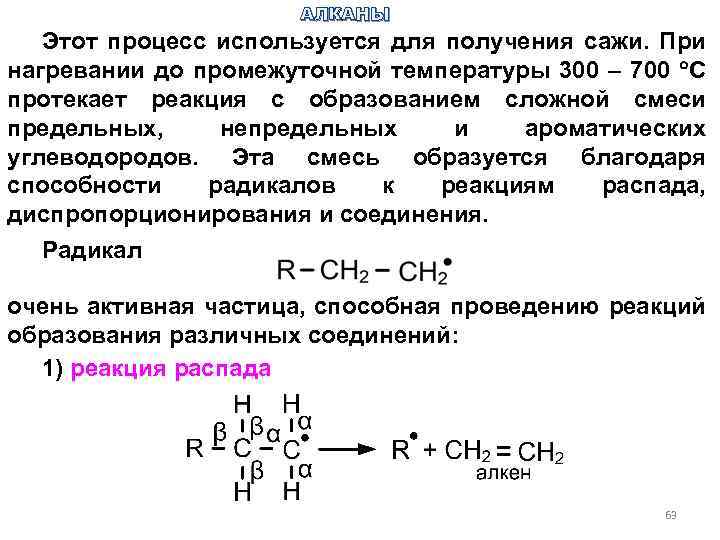 АЛКАНЫ Этот процесс используется для получения сажи. При нагревании до промежуточной температуры 300 – 700 C протекает реакция с образованием сложной смеси предельных, непредельных и ароматических углеводородов. Эта смесь образуется благодаря способности радикалов к реакциям распада, диспропорционирования и соединения. Радикал очень активная частица, способная проведению реакций образования различных соединений: 1) реакция распада 63
АЛКАНЫ Этот процесс используется для получения сажи. При нагревании до промежуточной температуры 300 – 700 C протекает реакция с образованием сложной смеси предельных, непредельных и ароматических углеводородов. Эта смесь образуется благодаря способности радикалов к реакциям распада, диспропорционирования и соединения. Радикал очень активная частица, способная проведению реакций образования различных соединений: 1) реакция распада 63
 АЛКАНЫ 2) диспропорционирование 3) соединение двух радикалов Распад свободных радикалов всегда идет по β-связи по отношению к атому со свободным электроном. Соединение свободных радикалов играет небольшую роль, т. к. их концентрация ничтожна и вероятность столкновения двух свободных радикалов мала. Главными являются два первых процесса. 64
АЛКАНЫ 2) диспропорционирование 3) соединение двух радикалов Распад свободных радикалов всегда идет по β-связи по отношению к атому со свободным электроном. Соединение свободных радикалов играет небольшую роль, т. к. их концентрация ничтожна и вероятность столкновения двух свободных радикалов мала. Главными являются два первых процесса. 64
 АЛКАНЫ Введением в зону реакции катализаторов можно изменить направление крекинга. Например, на некоторых катализаторах можно получать из предельных углеводородов олефины, т. е. осуществлять процесс дегидрогенизации. В присутствии Al. Cl 3 протекают процессы изомеризации. На платине осуществляют процессы ароматизации – образования ароматических углеводородов. 65
АЛКАНЫ Введением в зону реакции катализаторов можно изменить направление крекинга. Например, на некоторых катализаторах можно получать из предельных углеводородов олефины, т. е. осуществлять процесс дегидрогенизации. В присутствии Al. Cl 3 протекают процессы изомеризации. На платине осуществляют процессы ароматизации – образования ароматических углеводородов. 65


