соединения галогенов с кислородом.ppt
- Количество слайдов: 29

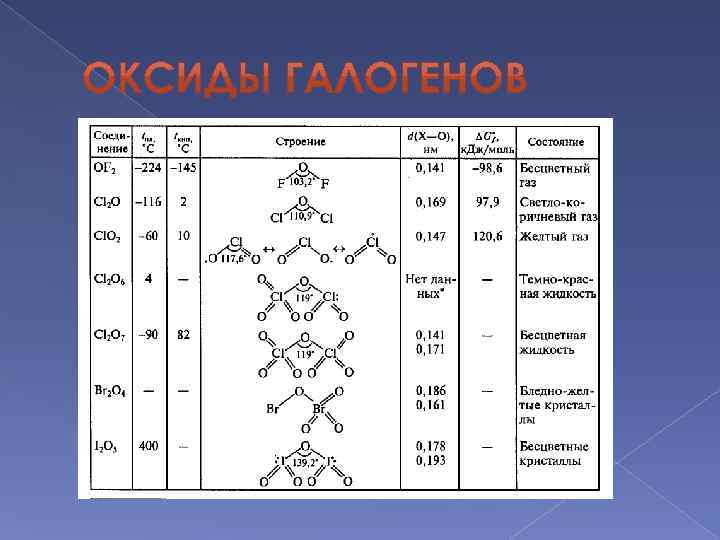
 1. Получают, пропуская фтор через 2% раствор гидроксида натрия: 2 F 2 + 2 Na. OH = OF 2 + 2 Na. F + H 2 O 2. Сильный окислитель, используется для синтеза фторидов благородных газов: Xe + OF 2 = Xe. F 2 + 1/2 O 2 3. При пропускании электрического разряда через охлажденную смесь фтора и кислорода получается другой фторид O 2 F 2. Он содержит связь О-О, как в пероксидах.
1. Получают, пропуская фтор через 2% раствор гидроксида натрия: 2 F 2 + 2 Na. OH = OF 2 + 2 Na. F + H 2 O 2. Сильный окислитель, используется для синтеза фторидов благородных газов: Xe + OF 2 = Xe. F 2 + 1/2 O 2 3. При пропускании электрического разряда через охлажденную смесь фтора и кислорода получается другой фторид O 2 F 2. Он содержит связь О-О, как в пероксидах.
 Оксид хлора (I) Cl 2 O (закись хлора) – желтокоричневый газ с неприятным запахом Получают: 3 Hg. O + 2 Cl 2 = Hg 3 O 2 Cl 2↓ + Cl 2 O↑ Соединение крайне неустойчиво, при повышенной температуре разлагается со взрывом Хорошо растворим в воде с образованием слабой кислоты HCl. O Сильный окислитель: 3 Cl 2 O + 10 NH 3 = N 2 + 6 NH 4 Cl + 3 H 2 O Производится в промышленных масштабах , используется как отбеливатель и для обеззараживания воды
Оксид хлора (I) Cl 2 O (закись хлора) – желтокоричневый газ с неприятным запахом Получают: 3 Hg. O + 2 Cl 2 = Hg 3 O 2 Cl 2↓ + Cl 2 O↑ Соединение крайне неустойчиво, при повышенной температуре разлагается со взрывом Хорошо растворим в воде с образованием слабой кислоты HCl. O Сильный окислитель: 3 Cl 2 O + 10 NH 3 = N 2 + 6 NH 4 Cl + 3 H 2 O Производится в промышленных масштабах , используется как отбеливатель и для обеззараживания воды
 Оксид хлора (|||) Cl 2 O 3 образуется при озонолизе оксида хлора (|), неустойчивое соединение Высший оксид хлора (Vll) Cl 2 O 7 Маслянистая, бесцветная жидкость, легко взрывается, молекула построена из 2 -х тетраэдров Cl. O 4, имеющих общую вершину Получают из концентрированной хлорной кислоты: 2 HCl. O 4 + P 2 O 5 = Cl 2 O 7 + 2 HPO 3
Оксид хлора (|||) Cl 2 O 3 образуется при озонолизе оксида хлора (|), неустойчивое соединение Высший оксид хлора (Vll) Cl 2 O 7 Маслянистая, бесцветная жидкость, легко взрывается, молекула построена из 2 -х тетраэдров Cl. O 4, имеющих общую вершину Получают из концентрированной хлорной кислоты: 2 HCl. O 4 + P 2 O 5 = Cl 2 O 7 + 2 HPO 3
 I 2 O 5 – единственный термодинамически устойчивый оксид галогенов Получают дегидратацией йодноватой кислоты HIO 3
I 2 O 5 – единственный термодинамически устойчивый оксид галогенов Получают дегидратацией йодноватой кислоты HIO 3

 Гипогалогенитные кислоты. HXO известны лишь в разбавленных водных растворах. Их получают взаимодействием галогена с суспензией оксида ртути. Гипогалогенитные кислоты являются слабыми. При переходе от хлора к иоду по мере увеличения радиуса и уменьшения электроотрицательности атом галогена слабее смещает электронную плотность от атома кислорода и, тем самым, слабее поляризует связь Н-О. В результате кислотные свойства в ряду HCl. O - HBr. O - HIO ослабляются. Окислительная способность кислот HXO и ионов XO- в том же ряду с термодинамической точки зрения уменьшается. Это следует из сравнения величин стандартных потенциалов Ео.
Гипогалогенитные кислоты. HXO известны лишь в разбавленных водных растворах. Их получают взаимодействием галогена с суспензией оксида ртути. Гипогалогенитные кислоты являются слабыми. При переходе от хлора к иоду по мере увеличения радиуса и уменьшения электроотрицательности атом галогена слабее смещает электронную плотность от атома кислорода и, тем самым, слабее поляризует связь Н-О. В результате кислотные свойства в ряду HCl. O - HBr. O - HIO ослабляются. Окислительная способность кислот HXO и ионов XO- в том же ряду с термодинамической точки зрения уменьшается. Это следует из сравнения величин стандартных потенциалов Ео.
 Свойства HCl. O HBr. O HIO E 0 (p. H = 0) HXO + H+ + ℮ = ½ X 2 + H 2 O 1, 63 1, 59 1, 45 p. Ka процесса HXO = H+ + XO- 7, 25 8, 7 11 константа равновесия 3 XO- = 2 X- + XO 3 - 1027 1015 1020 Бромноватистая кислота
Свойства HCl. O HBr. O HIO E 0 (p. H = 0) HXO + H+ + ℮ = ½ X 2 + H 2 O 1, 63 1, 59 1, 45 p. Ka процесса HXO = H+ + XO- 7, 25 8, 7 11 константа равновесия 3 XO- = 2 X- + XO 3 - 1027 1015 1020 Бромноватистая кислота
 Гипогалогенит-ионы неустойчивы и легко диспропорционируют на галогенид и галогенат-ионы. Скорость диспропорционирования возрастает в ряду: Cl. O- - Br. O- - IOКислотные свойства в ряду HCl. O-HBr. O-HIO ослабляются, также как и окислительные свойсства (первые две характеристики в таблице) Из значений констант равновесия следует, что ионы Br. O- и IOтермодинамически более стабильны, чем Cl. OУстойчивость гипогалогенидов понижается вниз по группе
Гипогалогенит-ионы неустойчивы и легко диспропорционируют на галогенид и галогенат-ионы. Скорость диспропорционирования возрастает в ряду: Cl. O- - Br. O- - IOКислотные свойства в ряду HCl. O-HBr. O-HIO ослабляются, также как и окислительные свойсства (первые две характеристики в таблице) Из значений констант равновесия следует, что ионы Br. O- и IOтермодинамически более стабильны, чем Cl. OУстойчивость гипогалогенидов понижается вниз по группе
 Высокую окислительную способность гипохлоритов иллюстрируют следующие реакции: Na. Сl. O +2 Na. I + H 2 O = Na. Cl + I 2 + 2 Na. OH 2 Na. Cl. O + Mn. Cl 2 + 4 Na. OH = Na 2 Mn. O 4 + 4 Na. Cl + 2 H 2 O.
Высокую окислительную способность гипохлоритов иллюстрируют следующие реакции: Na. Сl. O +2 Na. I + H 2 O = Na. Cl + I 2 + 2 Na. OH 2 Na. Cl. O + Mn. Cl 2 + 4 Na. OH = Na 2 Mn. O 4 + 4 Na. Cl + 2 H 2 O.
 Известна лишь хлористая кислота HCl. O 2 Водные растворы получают обработкой суспензии хлорита бария разбавленной серной кислотой: Ba(Cl. O 2)2 + H 2 SO 4 = Ba. SO 4↓ + 2 HCl. O 2 Кислота средней силы (р. Ка = 2) Соли (хлориты) используют для отбеливания 2 Cl. O 2 + Ba(OH)2 + H 2 O 2 = Ba(Cl. O 2)2 + 2 H 2 O + O 2
Известна лишь хлористая кислота HCl. O 2 Водные растворы получают обработкой суспензии хлорита бария разбавленной серной кислотой: Ba(Cl. O 2)2 + H 2 SO 4 = Ba. SO 4↓ + 2 HCl. O 2 Кислота средней силы (р. Ка = 2) Соли (хлориты) используют для отбеливания 2 Cl. O 2 + Ba(OH)2 + H 2 O 2 = Ba(Cl. O 2)2 + 2 H 2 O + O 2
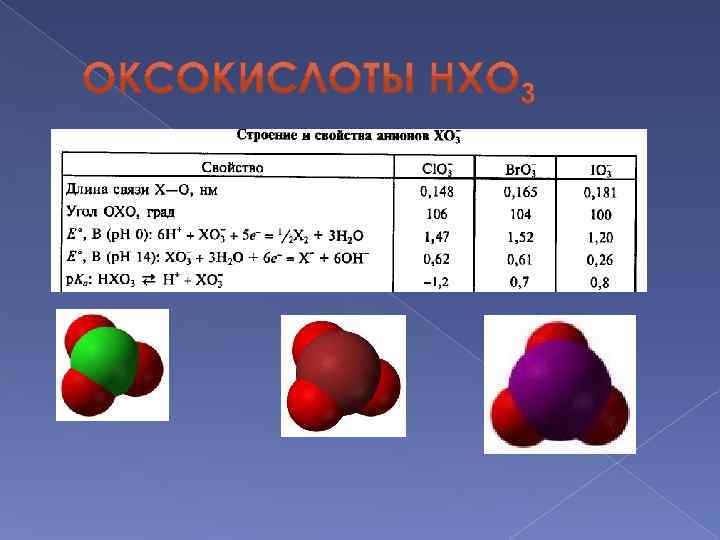
 В водных растворах HXO 3 являются сильными кислотами Сила кислот снижается в ряду: хлорноватая кислота > бромноватая кислота > йодноватая кислота Твердые галогенаты – сильные окислители: 2 S + 2 KBr. O 3 = K 2 SO 4 + Br 2 + SO 2 Окислительная способность галогенат-ионов уменьшается в ряду: Br. O 3 - ≈ Cl. O 3 - > IO 3 – 2 Na. Br. O 3 + I 2 = 2 Na. IO 3 + Br 2 2 Na. Cl. O 3 + I 2 = 2 Na. IO 3 + Cl 2
В водных растворах HXO 3 являются сильными кислотами Сила кислот снижается в ряду: хлорноватая кислота > бромноватая кислота > йодноватая кислота Твердые галогенаты – сильные окислители: 2 S + 2 KBr. O 3 = K 2 SO 4 + Br 2 + SO 2 Окислительная способность галогенат-ионов уменьшается в ряду: Br. O 3 - ≈ Cl. O 3 - > IO 3 – 2 Na. Br. O 3 + I 2 = 2 Na. IO 3 + Br 2 2 Na. Cl. O 3 + I 2 = 2 Na. IO 3 + Cl 2

 Бертолетова соль - хлорат калия KCl. O 3. Открыта французским химиком Бертолле в результате действия хлора на горячий раствор щелочи ЗCl 2 + 6 KOH = 5 KCl+ KCl. O 3 + ЗH 2 O Эта соль богата кислородом и довольно легко отдает его при нагревании в твердом состоянии в соответствии с уравнением 2 KCl. O 3 = 2 KCl+ 3 O 2 Клод Луи Бертолле (1748 -1822)
Бертолетова соль - хлорат калия KCl. O 3. Открыта французским химиком Бертолле в результате действия хлора на горячий раствор щелочи ЗCl 2 + 6 KOH = 5 KCl+ KCl. O 3 + ЗH 2 O Эта соль богата кислородом и довольно легко отдает его при нагревании в твердом состоянии в соответствии с уравнением 2 KCl. O 3 = 2 KCl+ 3 O 2 Клод Луи Бертолле (1748 -1822)
 При смешении с органическими веществами, появляется опасность взрыва, особенно опасны смеси с сахаром, серой, крахмалом, сажей. В воде (при комнатной температуре), практически нерастворима. Сильный окислитель: 2 KCl. O 3 + 3 S = 2 KCl + 3 SO 2↑ 5 KCl. O 3 + 6 P = 5 KCl + 3 P 2 O 5
При смешении с органическими веществами, появляется опасность взрыва, особенно опасны смеси с сахаром, серой, крахмалом, сажей. В воде (при комнатной температуре), практически нерастворима. Сильный окислитель: 2 KCl. O 3 + 3 S = 2 KCl + 3 SO 2↑ 5 KCl. O 3 + 6 P = 5 KCl + 3 P 2 O 5
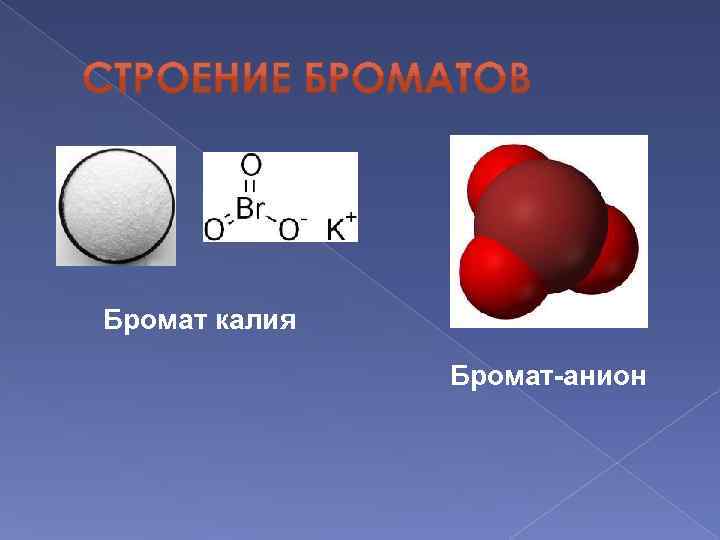 Бромат калия Бромат-анион
Бромат калия Бромат-анион
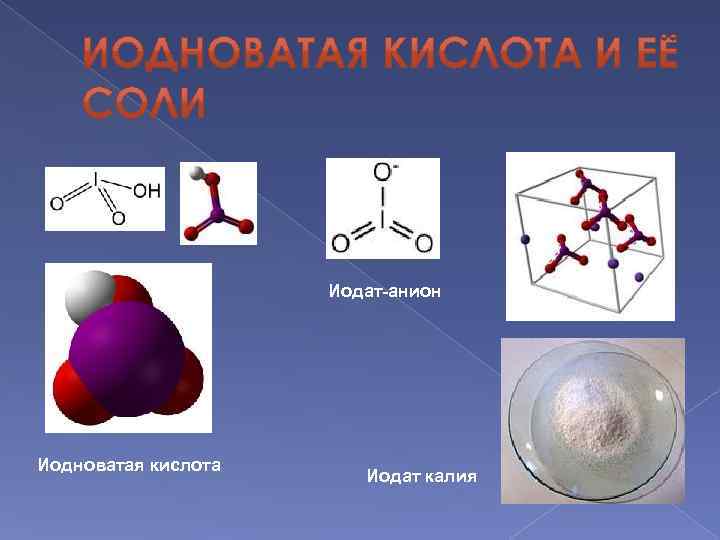 Иодат-анион Иодноватая кислота Иодат калия
Иодат-анион Иодноватая кислота Иодат калия

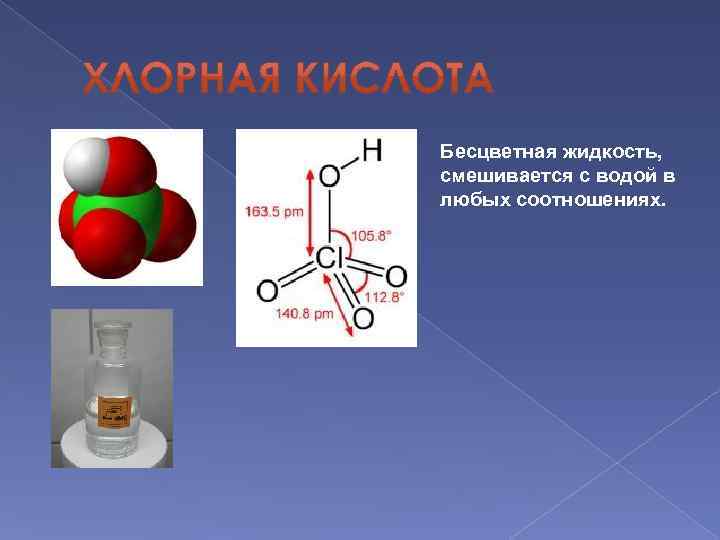 Бесцветная жидкость, смешивается с водой в любых соотношениях.
Бесцветная жидкость, смешивается с водой в любых соотношениях.
 Известна лишь в растворах. Ионы перхлорат Cl. O 4 - и пербромат Br. O 4 - имеют тетраэдрическое строение
Известна лишь в растворах. Ионы перхлорат Cl. O 4 - и пербромат Br. O 4 - имеют тетраэдрическое строение
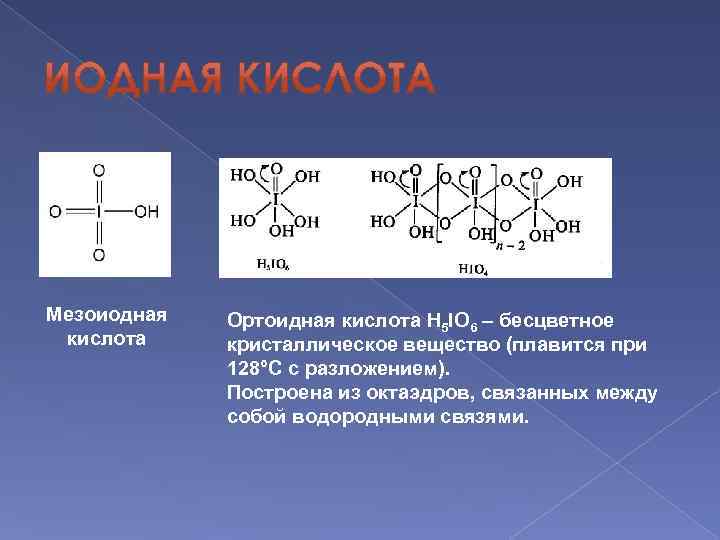 Мезоиодная кислота Ортоидная кислота H 5 IO 6 – бесцветное кристаллическое вещество (плавится при 128°С с разложением). Построена из октаэдров, связанных между собой водородными связями.
Мезоиодная кислота Ортоидная кислота H 5 IO 6 – бесцветное кристаллическое вещество (плавится при 128°С с разложением). Построена из октаэдров, связанных между собой водородными связями.
 Получают подкислением соответствующих пергалогенатов: Na. Cl. O 4 + HCl = HCl. O 4 + Na. Cl Окисление галогенатов: Na. Br. O 3 + F 2 + 2 Na. OH = Na. Br. O 4 + 2 Na. F + H 2 O
Получают подкислением соответствующих пергалогенатов: Na. Cl. O 4 + HCl = HCl. O 4 + Na. Cl Окисление галогенатов: Na. Br. O 3 + F 2 + 2 Na. OH = Na. Br. O 4 + 2 Na. F + H 2 O

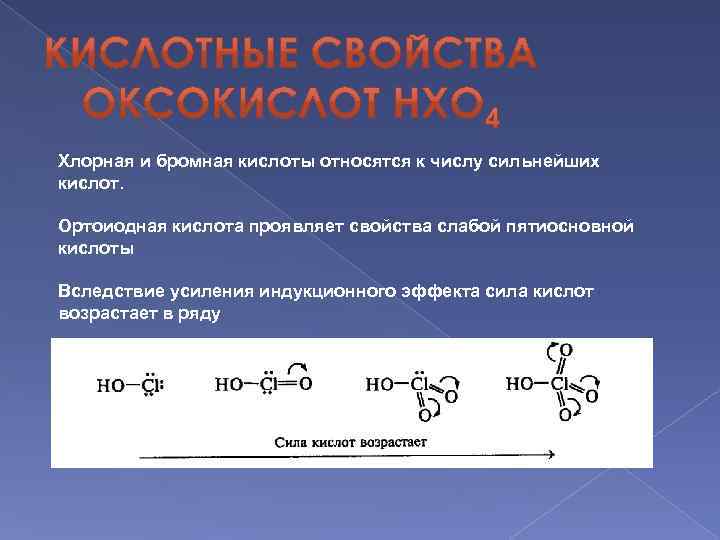 Хлорная и бромная кислоты относятся к числу сильнейших кислот. Ортоиодная кислота проявляет свойства слабой пятиосновной кислоты Вследствие усиления индукционного эффекта сила кислот возрастает в ряду
Хлорная и бромная кислоты относятся к числу сильнейших кислот. Ортоиодная кислота проявляет свойства слабой пятиосновной кислоты Вследствие усиления индукционного эффекта сила кислот возрастает в ряду
 Все оксокислоты являются сильными окислителями Наиболее сильными окислителями являются перброматы, а наиболее слабыми периодаты, что объясняется меньшей прочностью связи Br – O по сравнению с Cl – O Mg + 2 HCl. O 4 = Mg(Cl. O 4)2 + H 2↑ Периодаты отличаются наибольшей устойчивостью
Все оксокислоты являются сильными окислителями Наиболее сильными окислителями являются перброматы, а наиболее слабыми периодаты, что объясняется меньшей прочностью связи Br – O по сравнению с Cl – O Mg + 2 HCl. O 4 = Mg(Cl. O 4)2 + H 2↑ Периодаты отличаются наибольшей устойчивостью
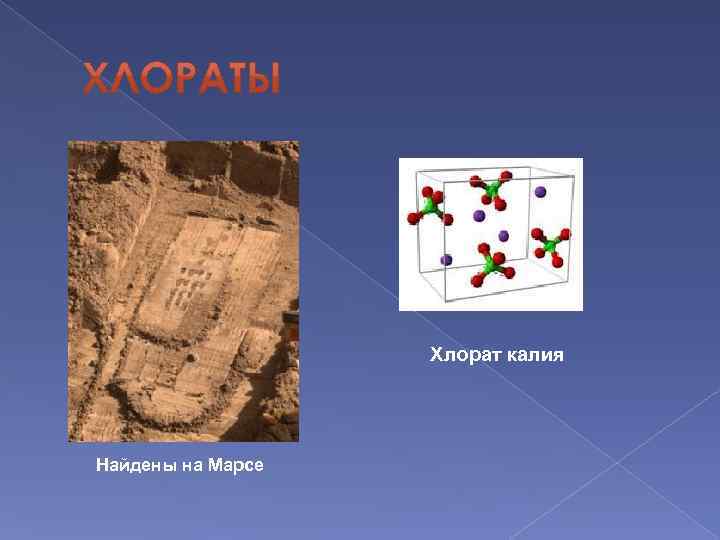 Хлорат калия Найдены на Марсе
Хлорат калия Найдены на Марсе
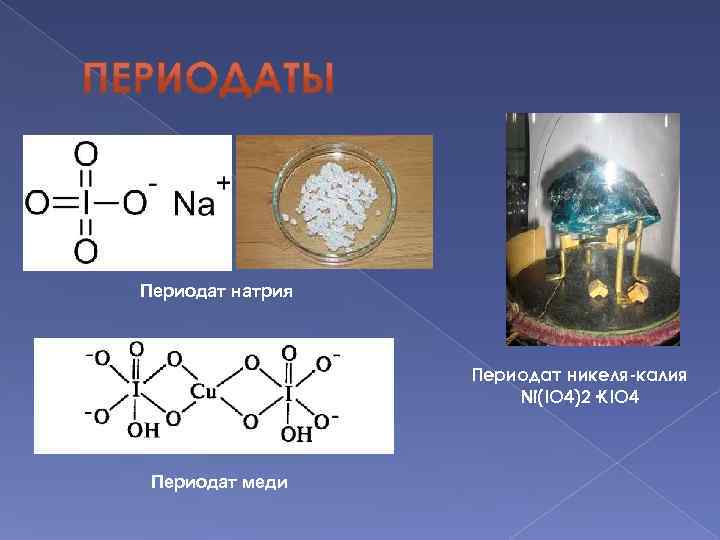 Периодат натрия Периодат никеля-калия Ni(IO 4)2·KIO 4 Периодат меди
Периодат натрия Периодат никеля-калия Ni(IO 4)2·KIO 4 Периодат меди


