1 ПЕПТИДЫ и белки Спирали встречаются во многих

1 ПЕПТИДЫ и белки Спирали встречаются во многих областях: в архитектуре, в макромолекулах белков, нуклеиновых кислот и даже в полисахаридах (Loretto Chapel, Santa Fe, NM/© Sarbo )

2 “Натура тем паче всего удивительна, что в простоте своей многохитростна и от малого числа причин производит неисчислимые образы свойств, перемен и явлений М.В. Ломоносов 1711-1765
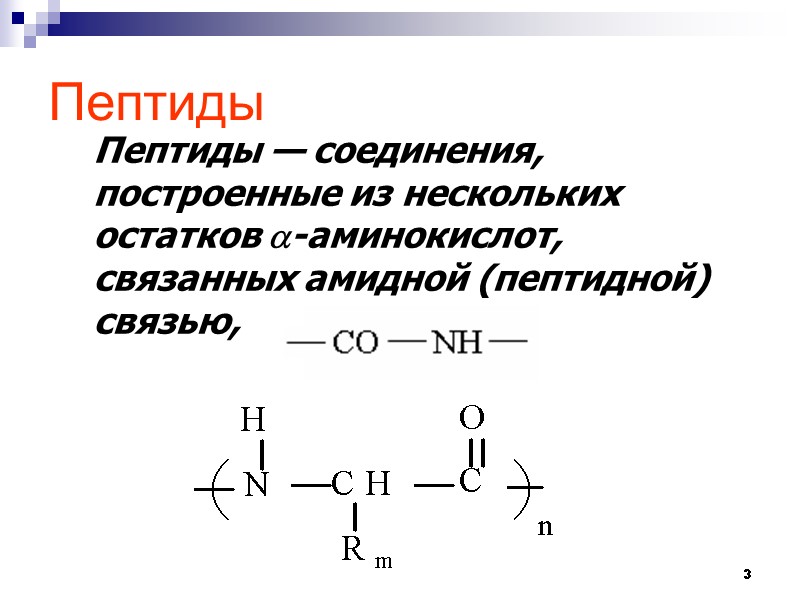
3 Пептиды Пептиды — соединения, построенные из нескольких остатков -аминокислот, связанных амидной (пептидной) связью,

4 Протяжённые межмолекулярные амиды, образовавшиеся в результате взаимодействия некоторого числа аминокислот, называются пептидами (греч. Πεπτος, peptós — сваренный, переваренный, питательный). Пептиды впервые были выделены из гидролизатов белков, полученных с помощью ферментирования. Термин «пептиды» был предложен известным химиком Эмилем Фишером (1852-1919).Слово образовано из первых четырёх букв названия пептоны (продукты расщепления белков пепсином) и конечных букв названия углеводов полисахариды. ФИШЕР (Fischer), Эмиль 9 октября 1852 г. – 15 июля 1919 г. Нобелевская премия по химии, 1902 г.
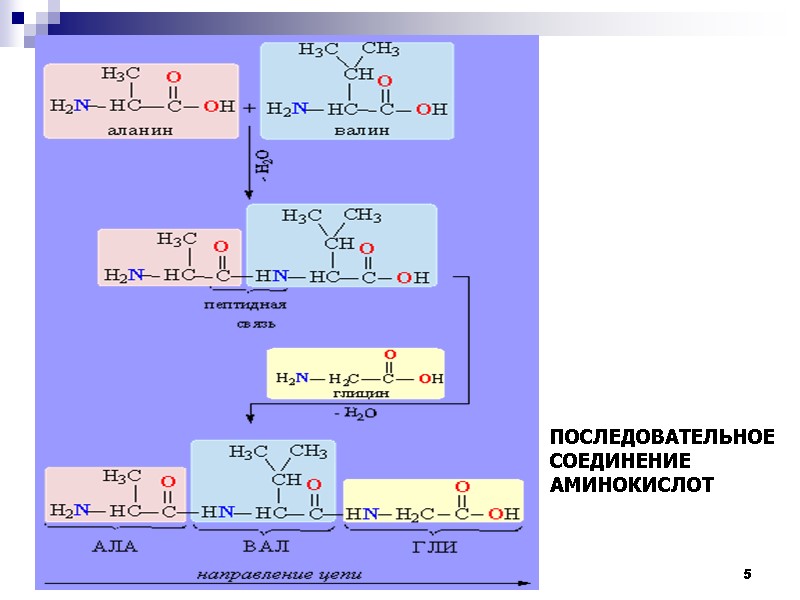
5 ПОСЛЕДОВАТЕЛЬНОЕ СОЕДИНЕНИЕ АМИНОКИСЛОТ
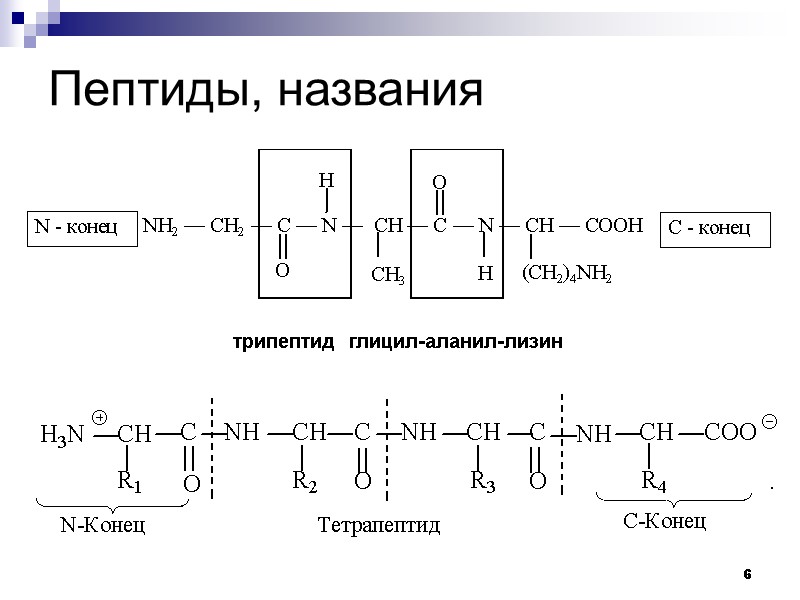
6 Пептиды, названия трипептид глицил-аланил-лизин
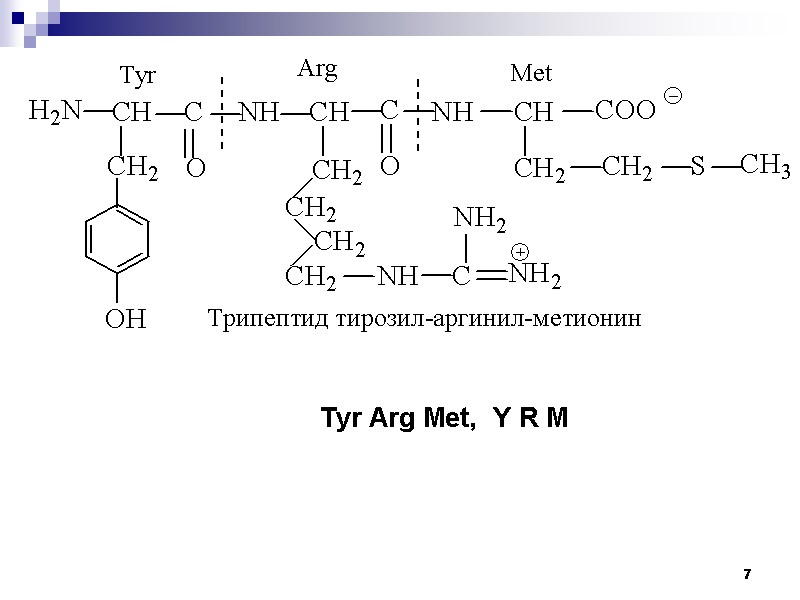
7 Tyr Arg Met, Y R M
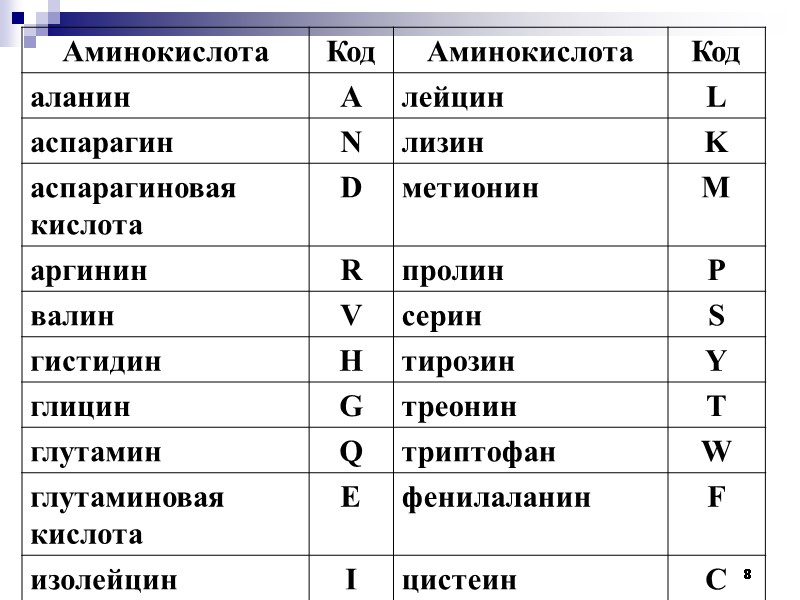
8
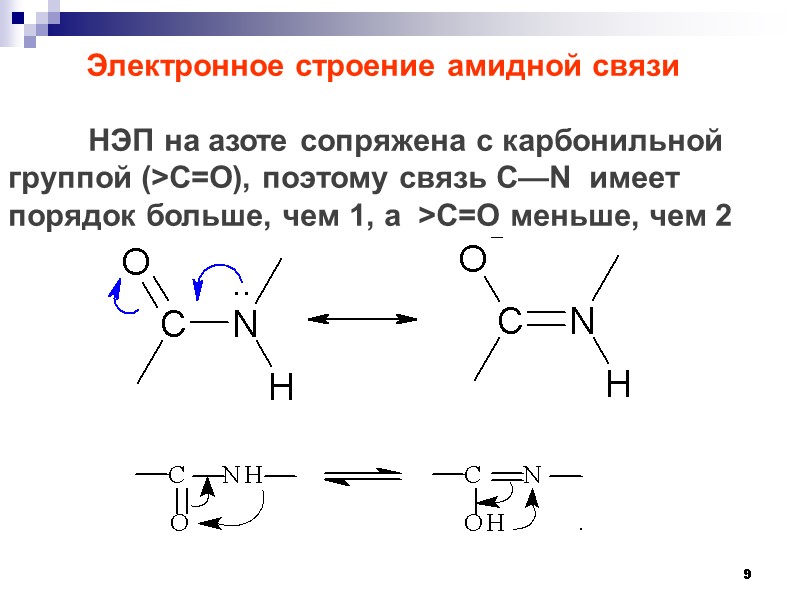
9 Электронное строение амидной связи НЭП на азоте сопряжена с карбонильной группой (>С=О), поэтому связь C—N имеет порядок больше, чем 1, а >С=О меньше, чем 2
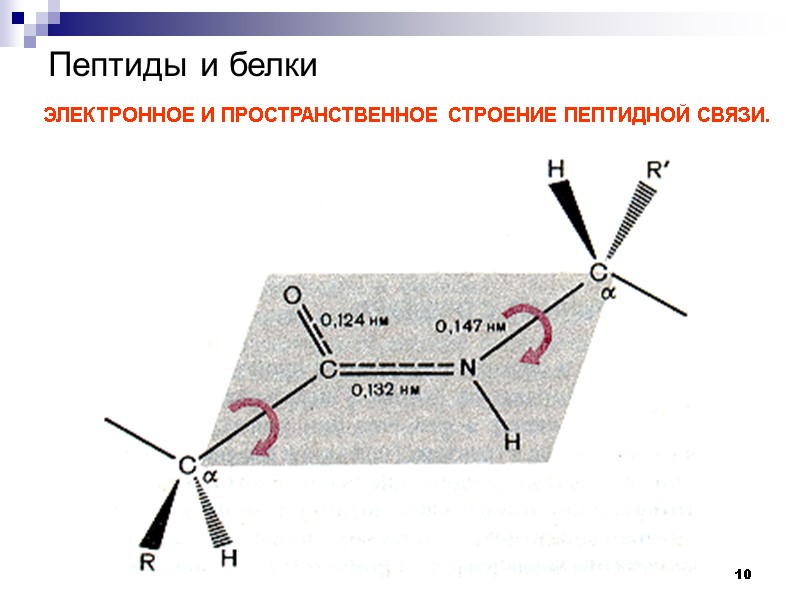
10 Пептиды и белки ЭЛЕКТРОННОЕ И ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПЕПТИДНОЙ СВЯЗИ.
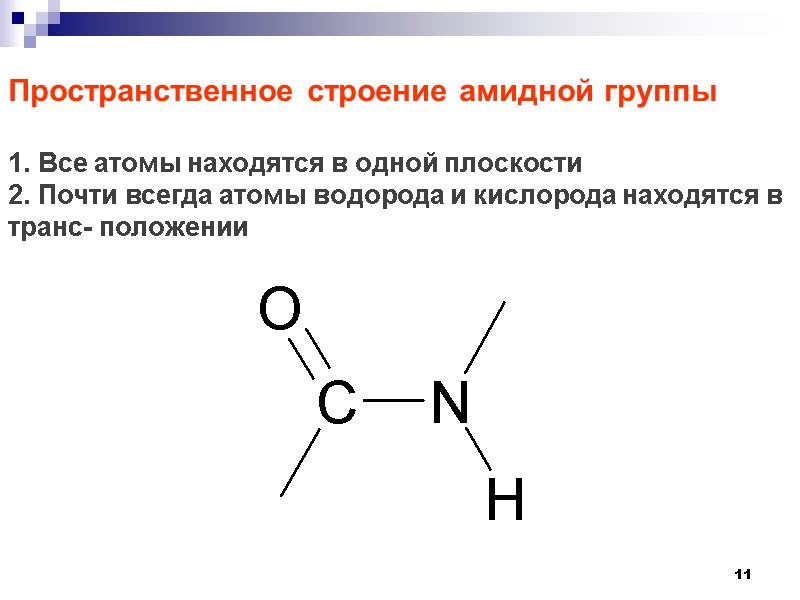
11 Пространственное строение амидной группы 1. Все атомы находятся в одной плоскости 2. Почти всегда атомы водорода и кислорода находятся в транс- положении
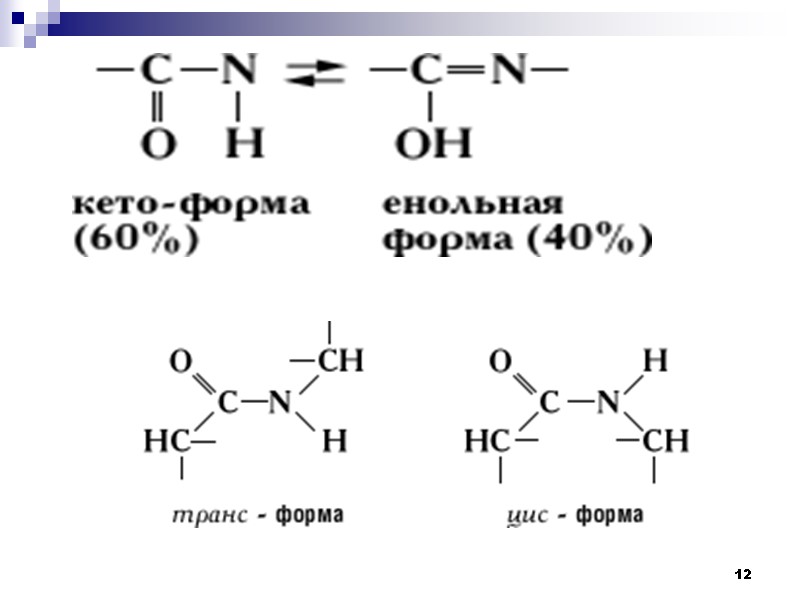
12
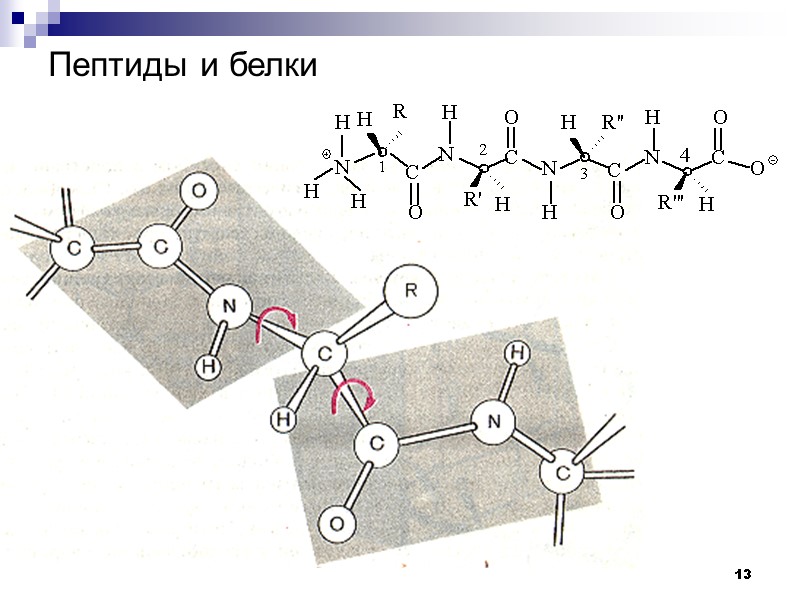
13 Пептиды и белки

14 Как и аминокислоты, пептиды и белки являются амфотерными соединениями, содержащими и кислотные группы (-COOH) и оснóвные группы (-NH2). ИЭТ зависит от их количества- если больше –COOH, чем NH2, то ИЭТ меньше 5-6, если, наоборот, то больше. Пептид: Тре-Фен-Тир. Содержит одну COOH и одну NH2 ИЭТ будет равна 5-6. Пептид: Гли-Лиз-Тир. Содержит одну COOH и две NH2 ИЭТ будет равна 8-11. Пептид: Глу-Ала-Цис. Содержит две COOH и одну NH2 ИЭТ будет равна 3.

15 Классификация пептидов. В зависимости от числа аминокислотных остатков различают ди-, три-, тетра-, пента- и тому подобные пептиды; пептиды с молекулярной массой не более 10 000 у.е. ,(не более 50-60 аминокислотных остатков) называют олигопептидами, а с молекулярной массой, большей 10 000 у.е. полипептидами, или белками.

16 Основные функции пептидов: регуляторная (рилизинг-факторы или либерины, нейромедиаторы); гормональная (окситоцин, вазопрессин, брадикинин, гастрин и др.); антибиотическая (грамицидин А, В, С, S; актиномицин D и др.); антиоксидантная (глутатион и др.); регуляторы митоза (факторы роста); функция витаминов (фолиевая кислота); пептидные алкалоиды (эрготамин и др.); токсическая (фаллоидин, аманитин и др.).
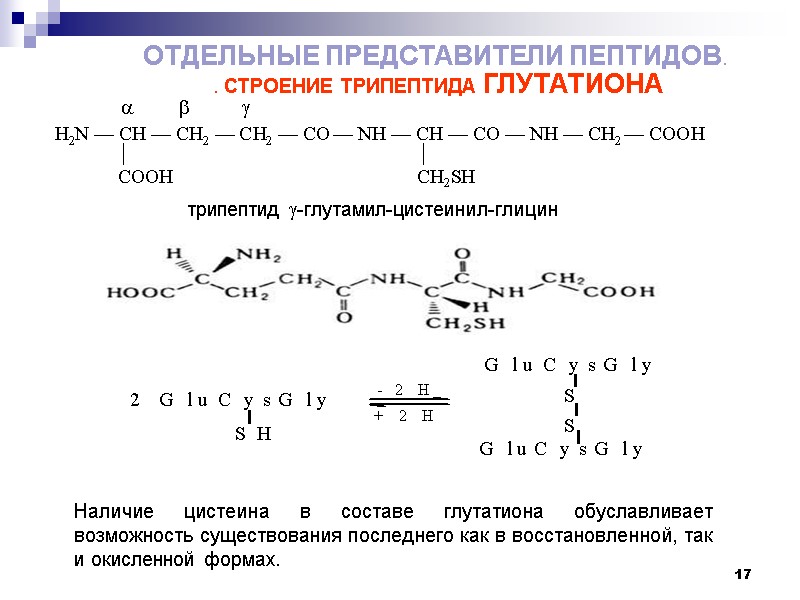
17 . СТРОЕНИЕ ТРИПЕПТИДА ГЛУТАТИОНА трипептид -глутамил-цистеинил-глицин Наличие цистеина в составе глутатиона обуславливает возможность существования последнего как в восстановленной, так и окисленной формах. ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ ПЕПТИДОВ.

18 Аспартам — дипептид, состоящий из остатков L-аспарагиновой кислоты и метилового эфира L-фенилаланина, используется в качестве заменителя сахара – низкокалорийной пищевой добавки. Почти в 200 раз слаще сахарозы. Изолированный из мясного сока октапептид Lys-Gly-Asp-Glu-Glu-Ser-Leu-Ala широко используются в пищевой промышленности для улучшения вкуса пищи

19 Нейропептиды (опиатные пептиды). К ним относятся пептиды, содержащиеся в головном мозге. Первые два представителя нейропептидов, названные энкефалинами, были выделены из мозга животных в 1975 г. Оба являются пентапептидами, отличающимися только С-концевой -аминокислотой TyrGlyGlyPheMet метионин-энкефалин TyrGlyGlyPheLeu лейцин-энкефалин Эти пептиды оказывают обезболивающее действие и используются как лекарственные средства.

20 Окситоцин вызывает сокращение гладких мышц матки и в меньшей степени — мышц мочевого пузыря и кишечника, стимулирует отделение молока молочными железами. Выделен в чистом виде из биологических объектов (1950) и получен синтетически (1954) В. Дю Виньо с сотрудниками (первый синтез биологически активного соединения, имеющего структуру белка) Вазопрессин (от лат. vas – cocyд и presso – давлю), гормон, выделяемый задней долей гипофиза,вызывает сужение сосудов (действуя на гладкие мышцы их стенок) и повышение кровяного давления (прессорный эффект), а также поддерживает на должном уровне обратное всасывание воды в прямых канальцах почек, то есть уменьшает количество выделяющейся мочи (антидиуретический эффект).
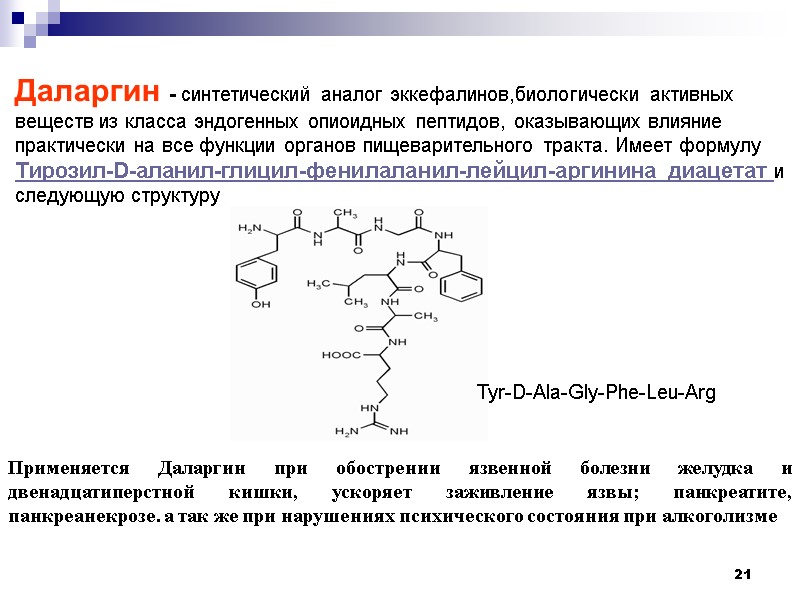
21 Даларгин - синтетический аналог эккефалинов,биологически активных веществ из класса эндогенных опиоидных пептидов, оказывающих влияние практически на все функции органов пищеварительного тракта. Имеет формулу Тирозил-D-аланил-глицил-фенилаланил-лейцил-аргинина диацетат и следующую структуру Tyr-D-Ala-Gly-Phe-Leu-Arg

22 Одним из современных перспективных лекарственных препаратов пептидной природы является отечественный препарат Семакс. Семакс - гептапептид метионил-глутамил-гистидил-фенилаланил-пролил-глицил-пролин, MetGluHisPheProGlyPro , — лекарственное средство, оказывающее ноотропное и нейропротективное действие
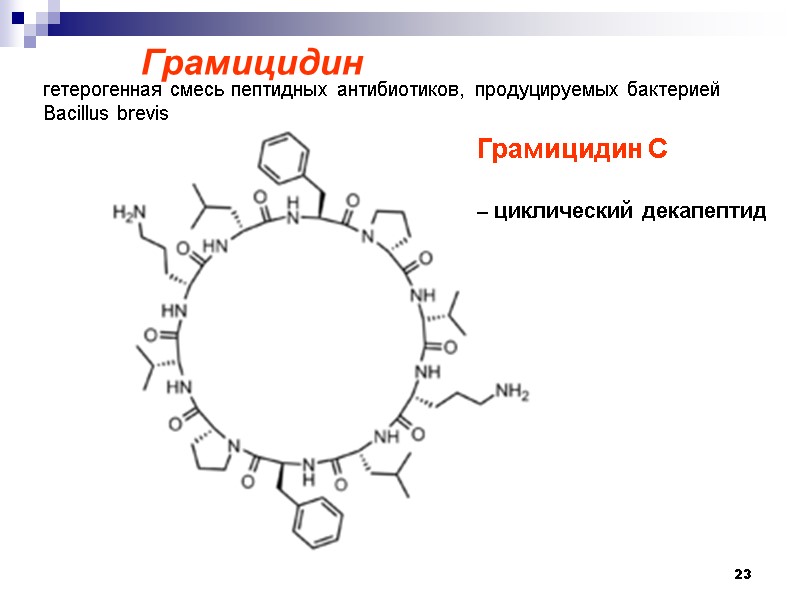
23 Грамицидин гетерогенная смесь пептидных антибиотиков, продуцируемых бактерией Bacillus brevis Грамицидин С – циклический декапептид
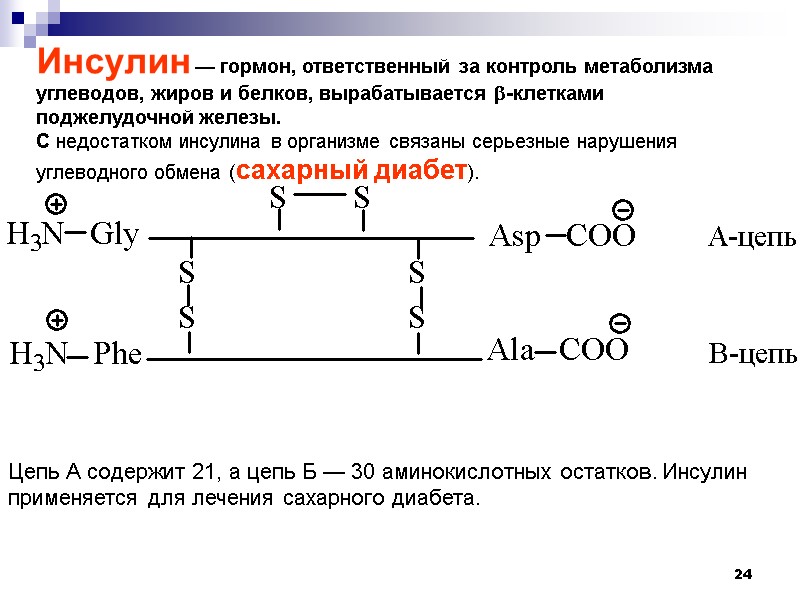
24 Инсулин — гормон, ответственный за контроль метаболизма углеводов, жиров и белков, вырабатывается -клетками поджелудочной железы. С недостатком инсулина в организме связаны серьезные нарушения углеводного обмена (сахарный диабет). Цепь А содержит 21, а цепь Б — 30 аминокислотных остатков. Инсулин применяется для лечения сахарного диабета.
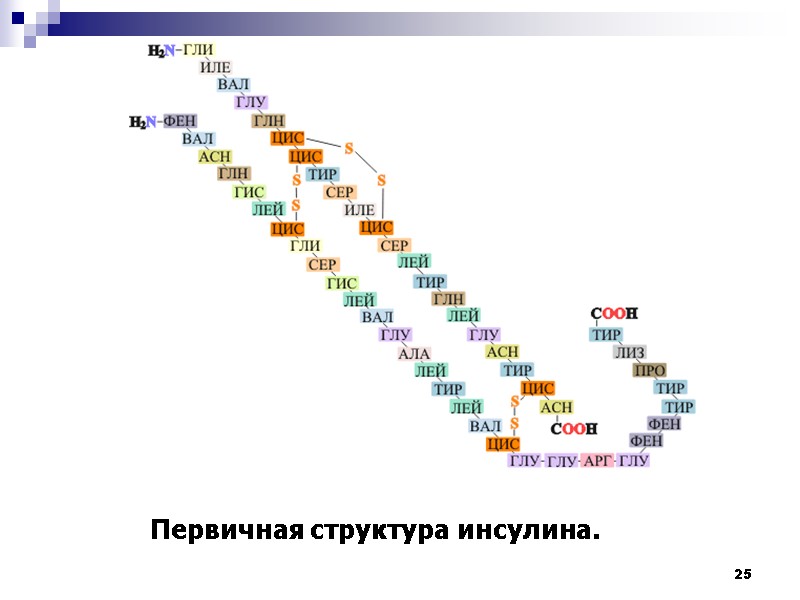
25 Первичная структура инсулина.

26 Биолан комплекс веществ пептидной группы, природных нейропротекторных аминокислот и пептидов, оптимально сбалансированных и необходимых для нормального и стабильного функционирования нервной системы и организма человека. - TrpAlaGlyGlyAspAlaSerGlyGlu - Delta sleep inducng peptide, DSIP -βAlaHis - карнозин - Gly - глицин

27 20 аминокислот могут дать примерно 100000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000 белков, состоящих из 150 остатков аминокислот. Это астрономическое число – число гугол умноженное на число гугол (число гугол – это 10100)

28 ИСКУССТВЕННЫЙ СИНТЕЗ ПЕПТИДОВ. Схема синтеза дипептида аланил-валина: Первый компонент – N-концевая аминокислота аланин I. Защита группы –NH2 II. Активация группы –СООН
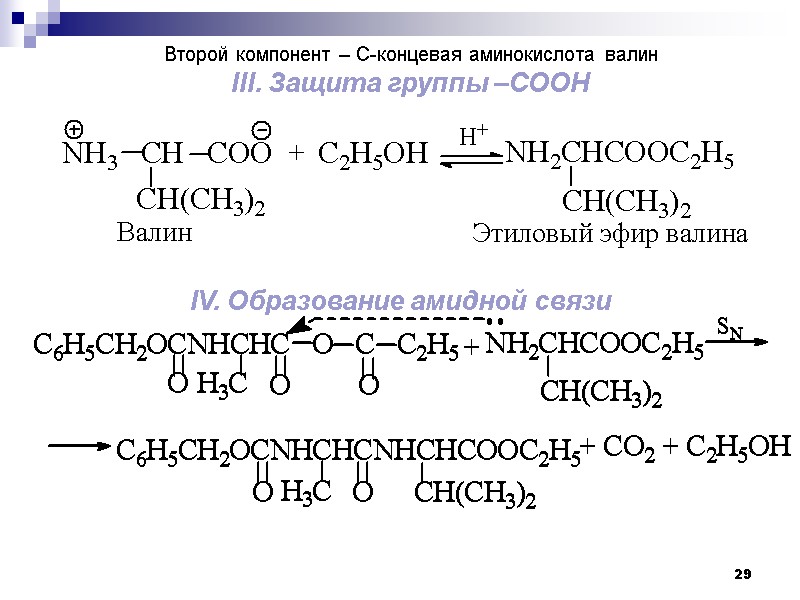
29 Второй компонент – С-концевая аминокислота валин III. Защита группы –СООН IV. Образование амидной связи

30 V. Удаление защиты
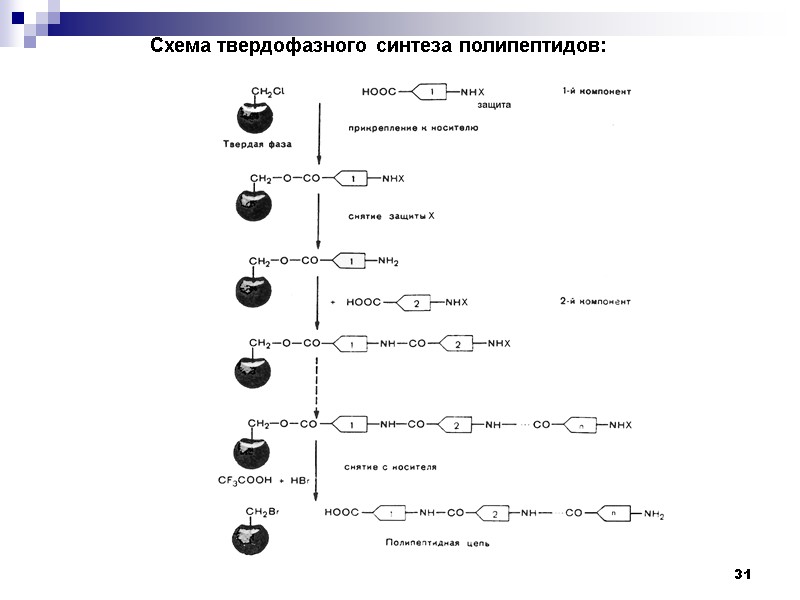
31 Схема твердофазного синтеза полипептидов:

32 Схема твёрдофазного синтеза полипептидов Первый компонент – прикрепление к носителю

33 Второй компонент (и дальнейшее наращивание цепи) Снятие с носителя

34 Содержание белков в различных тканях человека В мышцах – до 80%; в селезенке, крови, легких – около 72%; в коже – 63%; в печени – 57%; в мозге – 15%; жировая ткань, костная и ткань зубов содержат от 14 до 28% белков.
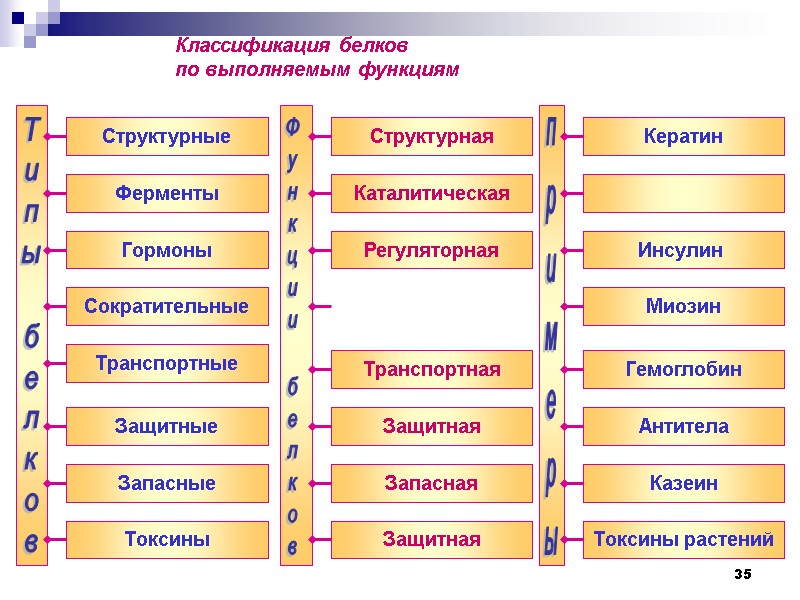
35 Типы белков Ферменты Гормоны Транспортные Защитные Запасные Токсины Структурные Структурная Каталитическая Регуляторная Сократительные Транспортная Защитная Запасная Защитная Кератин Инсулин Миозин Гемоглобин Антитела Казеин Токсины растений Функции белков примеры Классификация белков по выполняемым функциям

36 Строительная (пластическая) – белки участвуют в образовании оболочки клетки, органоидов и мембран клетки. Каталитическая – все клеточные катализаторы – белки (активные центры фермента). Двигательная – сократительные белки вызывают всякое движение. Транспортная – белок крови гемоглобин присоединяет кислород и разносит его по всем тканям. Защитная – выработка белковых тел и антител для обезвреживания чужеродных веществ. Энергетическая – 1 г белка эквивалентен 17,6 кДж. Рецепторная – реакция на внешний раздражитель Функции белков
37 Функции белков
38 Степень организации белковых молекул

39 Пептиды и белки Структура белков Первичная структура пептидов и белков — это последовательность аминокислотных остатков в полипептидной цепи. Первичная структура определяет все остальные уровни структурной организации белка
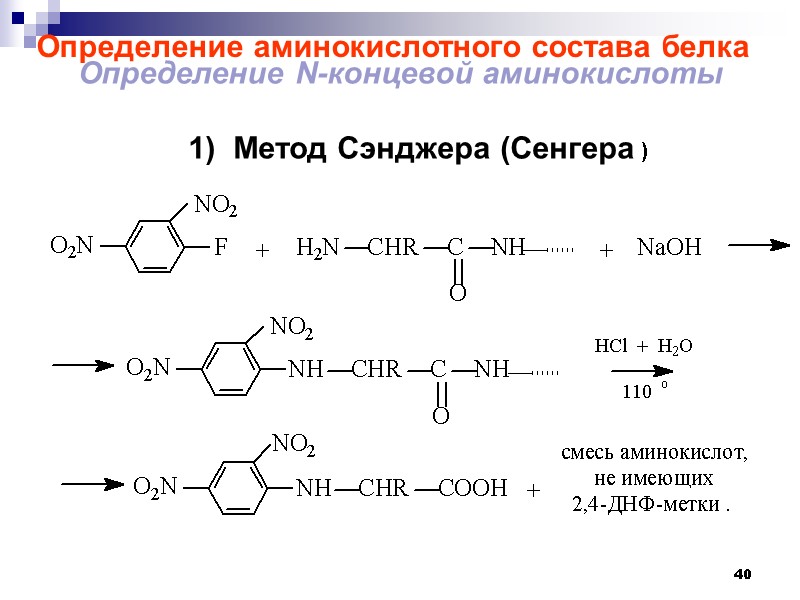
40 Определение аминокислотного состава белка Определение N-концевой аминокислоты 1) Метод Сэнджера (Сенгера )
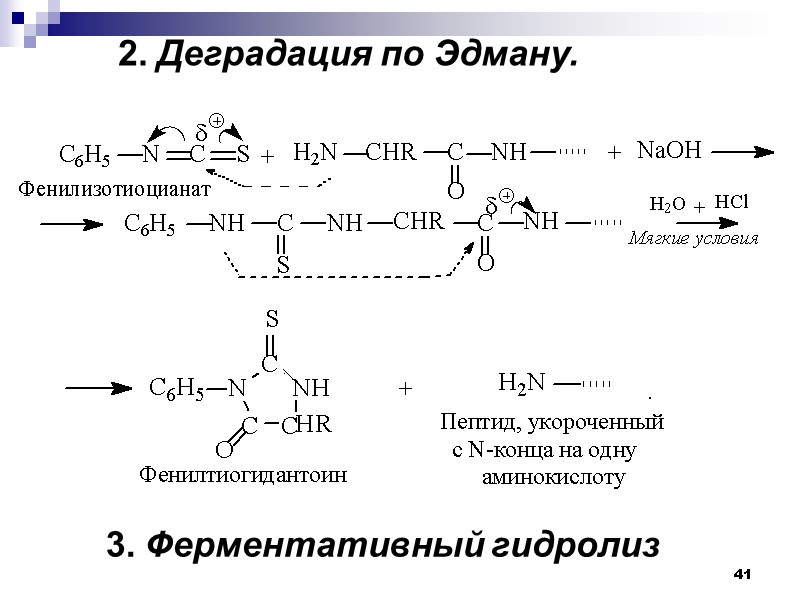
41 2. Деградация по Эдману. 3. Ферментативный гидролиз

42 Пептиды и белки Вторичная структура белков Вторичная структура белка — это более высокий уровень структурной организации, в котором закрепление конформации происходит за счет водородных связей между пептидными группами.
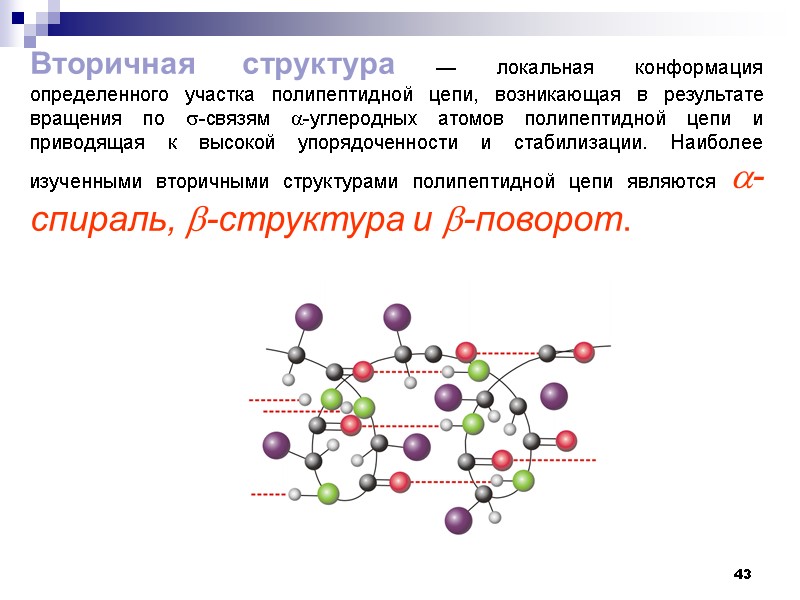
43 Вторичная структура — локальная конформация определенного участка полипептидной цепи, возникающая в результате вращения по -связям -углеродных атомов полипептидной цепи и приводящая к высокой упорядоченности и стабилизации. Наиболее изученными вторичными структурами полипептидной цепи являются -спираль, -структура и -поворот.
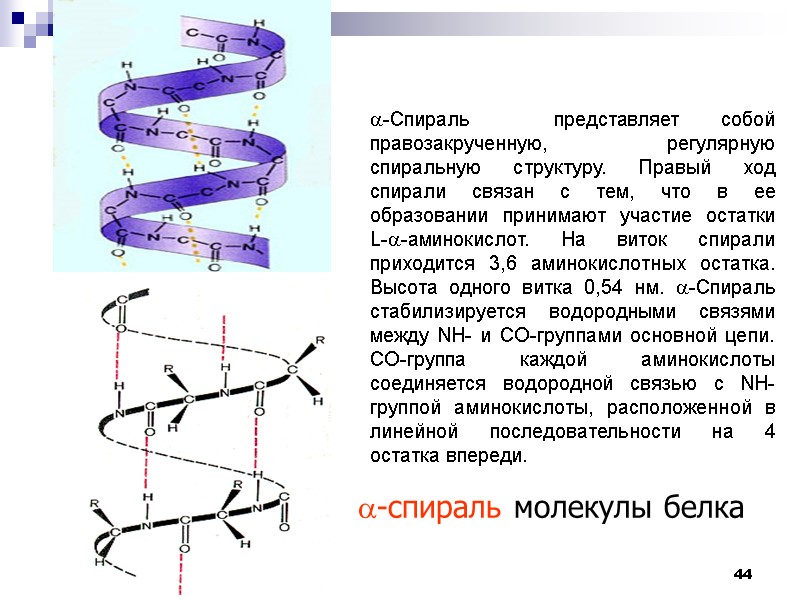
44 a-спираль молекулы белка -Спираль представляет собой правозакрученную, регулярную спиральную структуру. Правый ход спирали связан с тем, что в ее образовании принимают участие остатки L--аминокислот. На виток спирали приходится 3,6 аминокислотных остатка. Высота одного витка 0,54 нм. -Спираль стабилизируется водородными связями между NH- и CO-группами основной цепи. СО-группа каждой аминокислоты соединяется водородной связью с NН-группой аминокислоты, расположенной в линейной последовательности на 4 остатка впереди.
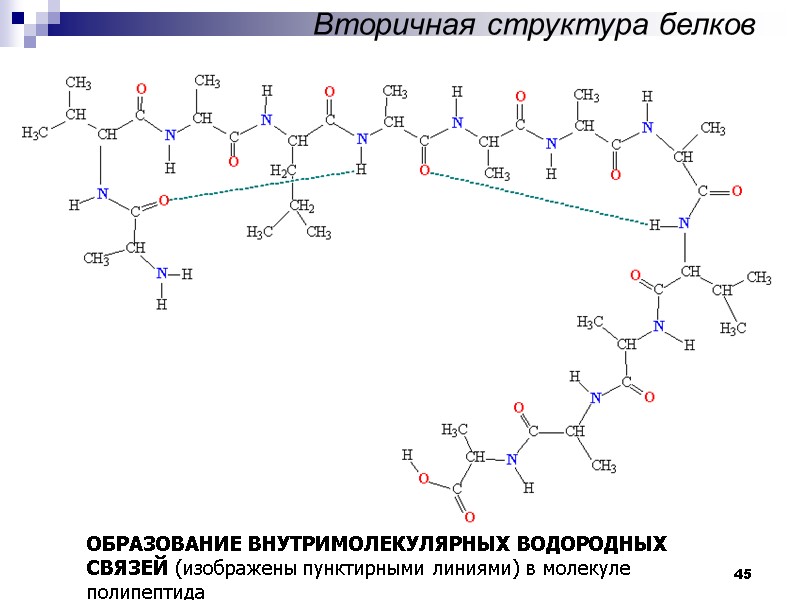
45 Вторичная структура белков ОБРАЗОВАНИЕ ВНУТРИМОЛЕКУЛЯРНЫХ ВОДОРОДНЫХ СВЯЗЕЙ (изображены пунктирными линиями) в молекуле полипептида

46
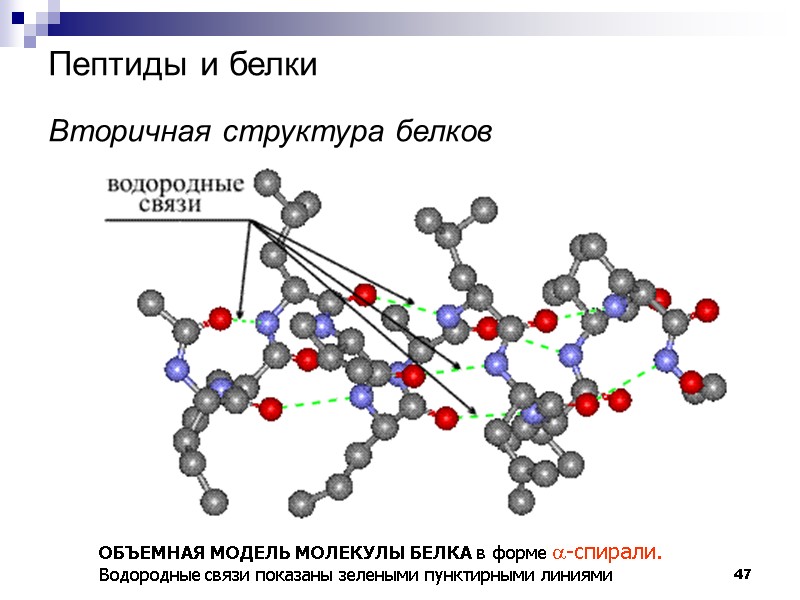
47 Пептиды и белки Вторичная структура белков ОБЪЕМНАЯ МОДЕЛЬ МОЛЕКУЛЫ БЕЛКА в форме a-спирали. Водородные связи показаны зелеными пунктирными линиями

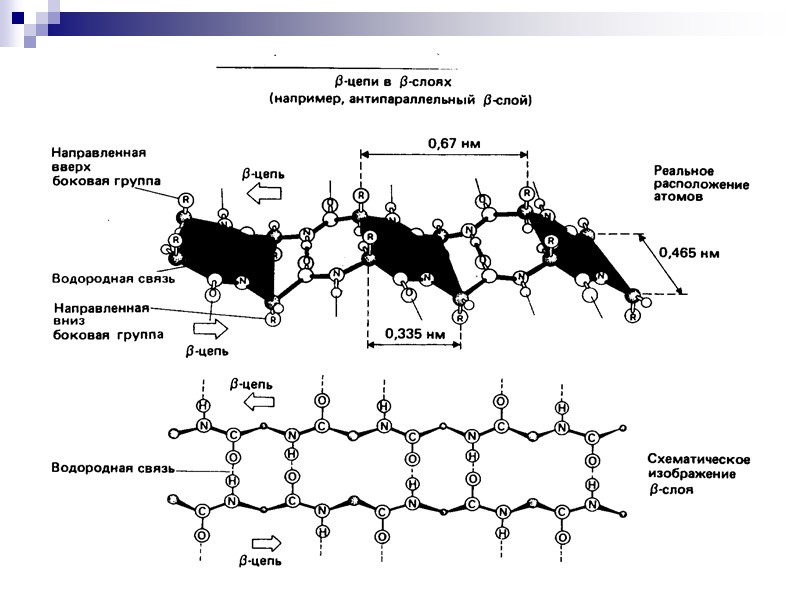
48 -Структура образуется из довольно вытянутых полипептидных цепей. -Структура бывает двух видов: а) параллельный -складчатый слой, если направление полипептидных цепей одинаково и б) антипараллельный, если полипептидные цепи направлены противоположно. Этот тип конформации стабилизирован водородными связями между NH- и CO-группами разных полипептидных цепей в фибриллярных белках или различными участками одной и той же полипептидной цепи в глобулярных белках.
49
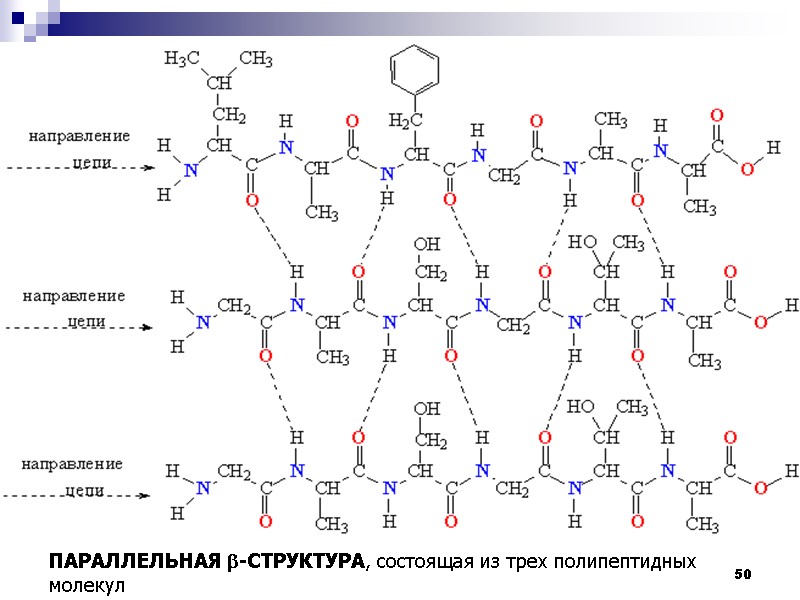
50 ПАРАЛЛЕЛЬНАЯ b-СТРУКТУРА, состоящая из трех полипептидных молекул
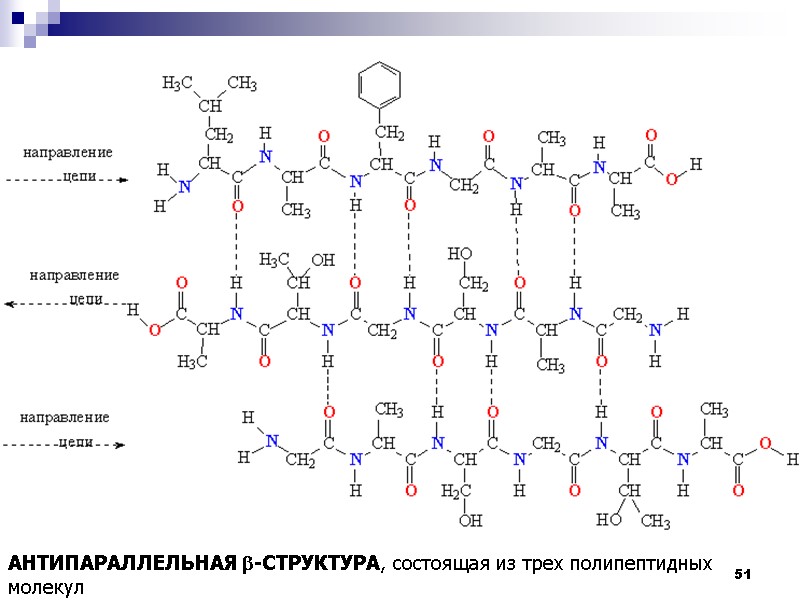
51 АНТИПАРАЛЛЕЛЬНАЯ b-СТРУКТУРА, состоящая из трех полипептидных молекул
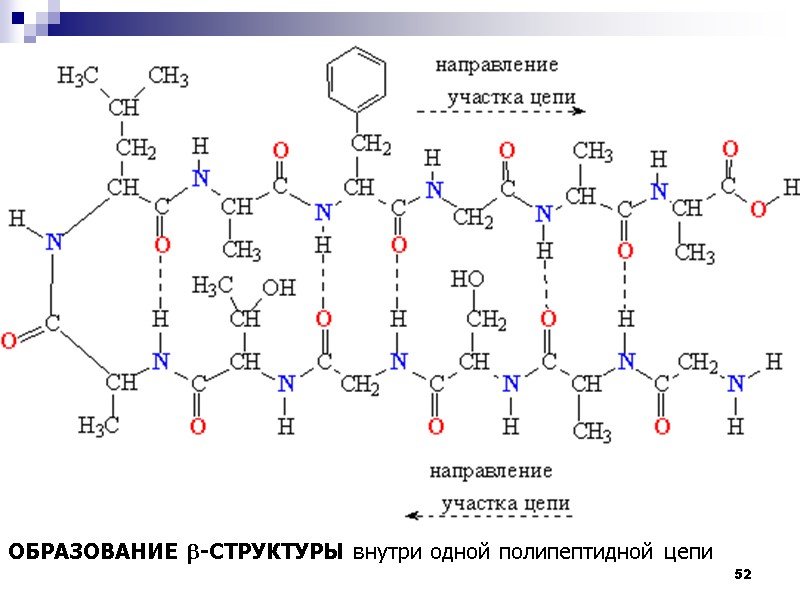
52 ОБРАЗОВАНИЕ b-СТРУКТУРЫ внутри одной полипептидной цепи
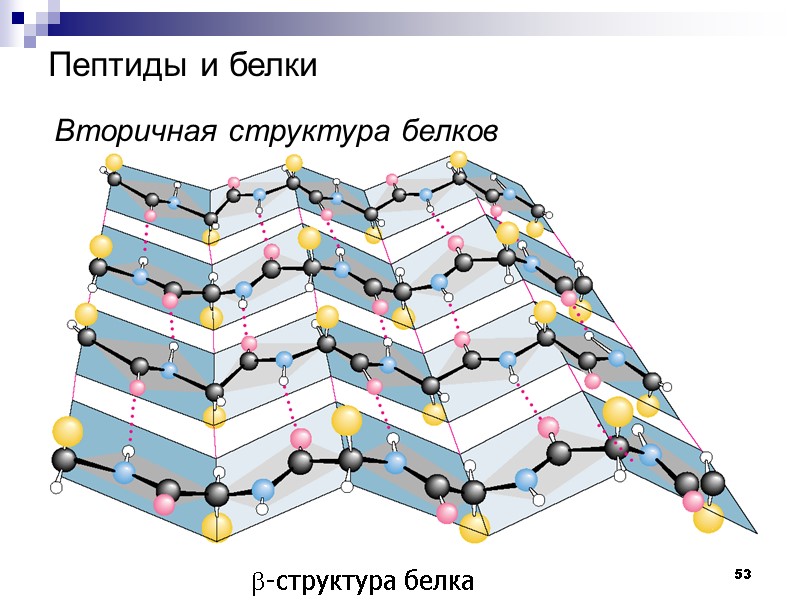
53 Пептиды и белки Вторичная структура белков b-структура белка
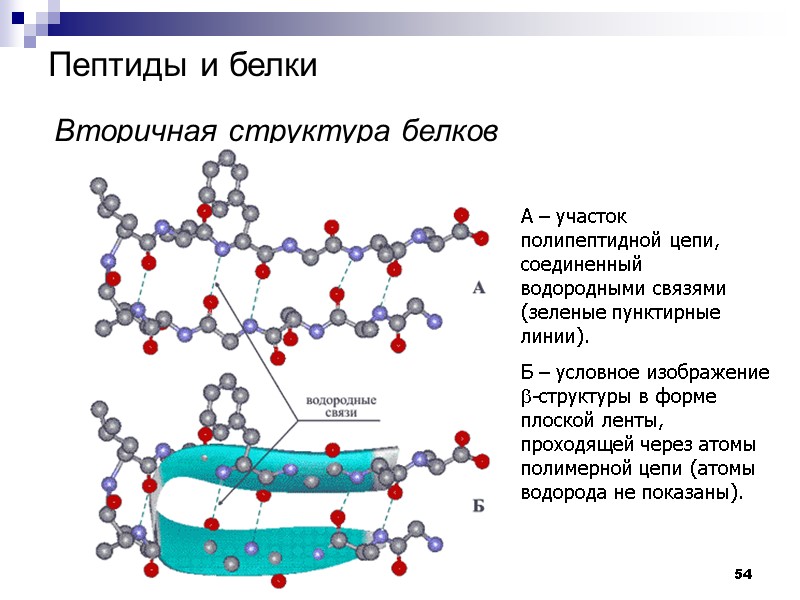
54 Пептиды и белки Вторичная структура белков А – участок полипептидной цепи, соединенный водородными связями (зеленые пунктирные линии). Б – условное изображение b-структуры в форме плоской ленты, проходящей через атомы полимерной цепи (атомы водорода не показаны).
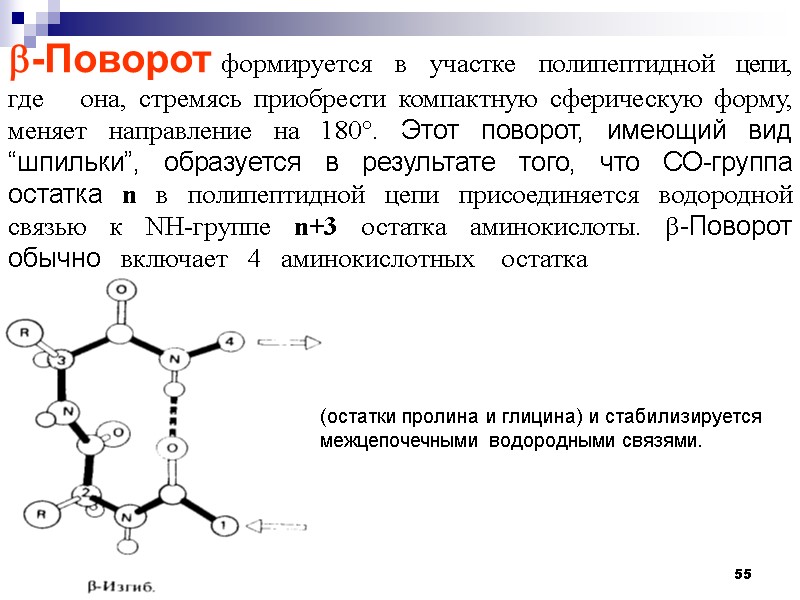
55 -Поворот формируется в участке полипептидной цепи, где она, стремясь приобрести компактную сферическую форму, меняет направление на 180. Этот поворот, имеющий вид “шпильки”, образуется в результате того, что СО-группа остатка n в полипептидной цепи присоединяется водородной связью к NH-группе n+3 остатка аминокислоты. -Поворот обычно включает 4 аминокислотных остатка (остатки пролина и глицина) и стабилизируется межцепочечными водородными связями.
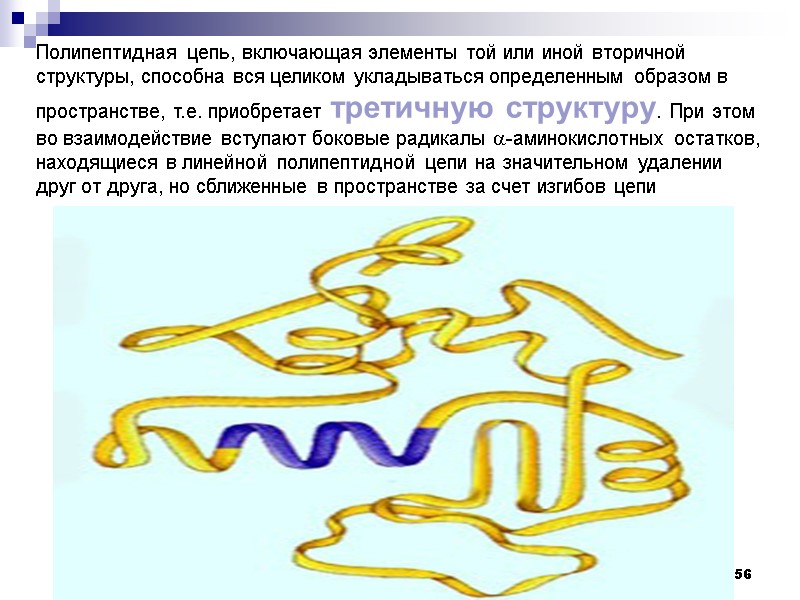
56 Полипептидная цепь, включающая элементы той или иной вторичной структуры, способна вся целиком укладываться определенным образом в пространстве, т.е. приобретает третичную структуру. При этом во взаимодействие вступают боковые радикалы -аминокислотных остатков, находящиеся в линейной полипептидной цепи на значительном удалении друг от друга, но сближенные в пространстве за счет изгибов цепи
57
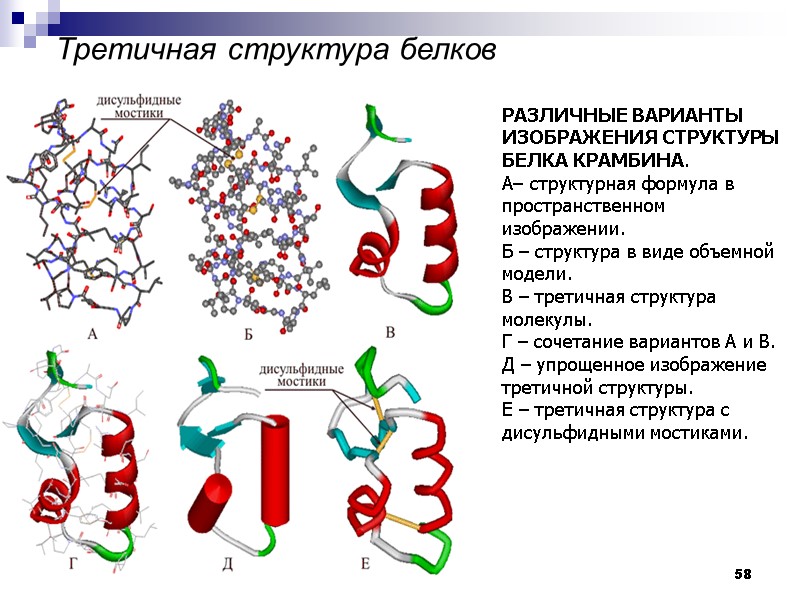
58 Третичная структура белков РАЗЛИЧНЫЕ ВАРИАНТЫ ИЗОБРАЖЕНИЯ СТРУКТУРЫ БЕЛКА КРАМБИНА. А– структурная формула в пространственном изображении. Б – структура в виде объемной модели. В – третичная структура молекулы. Г – сочетание вариантов А и В. Д – упрощенное изображение третичной структуры. Е – третичная структура с дисульфидными мостиками.

59 Глобулярные белки ГЛОБУЛЯРНАЯ СТРУКТУРА АЛЬБУМИНА (белок куриного яйца). В структуре помимо дисульфидных мостиков присутствуют свободные сульфгидридные HS-группы цистеина, которые в процессе разложения белка легко образуют сероводород – источник запаха тухлых яиц. Дисульфидные мостики намного более устойчивы и при разложении белка сероводород не образуют
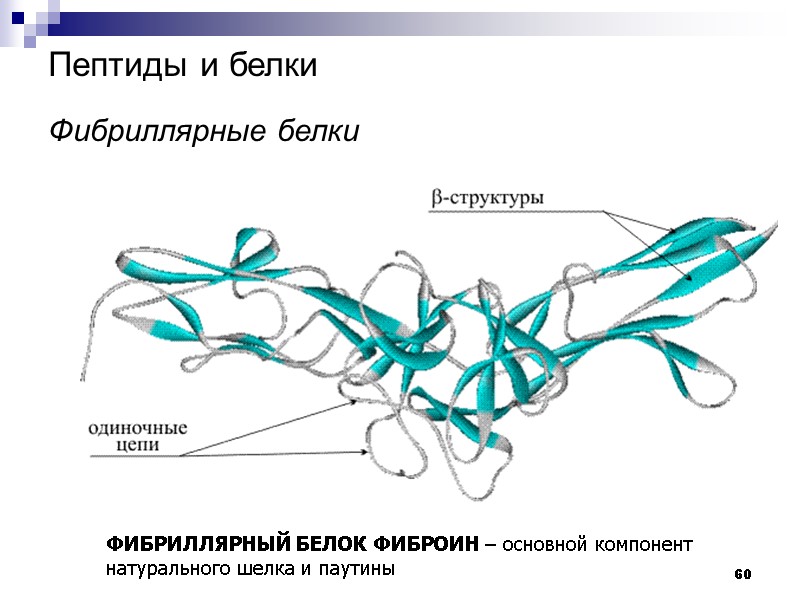
60 Пептиды и белки Фибриллярные белки ФИБРИЛЛЯРНЫЙ БЕЛОК ФИБРОИН – основной компонент натурального шелка и паутины
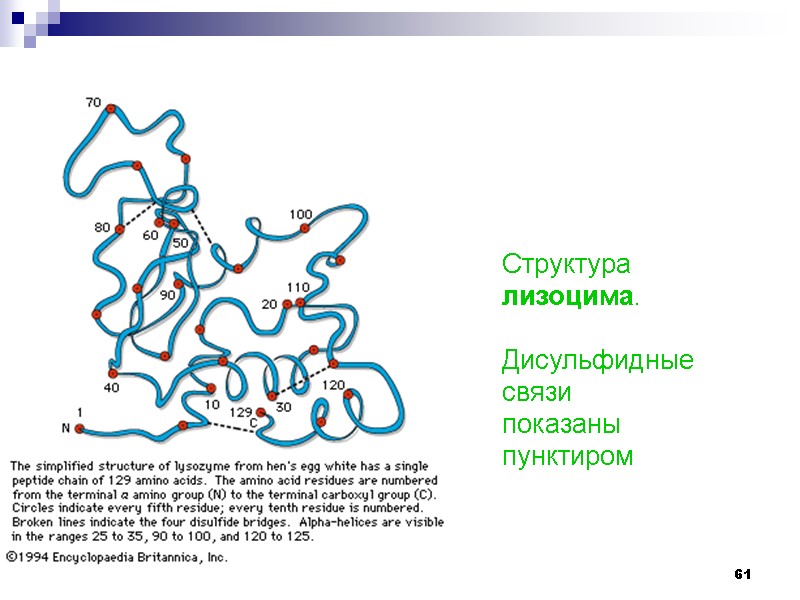
61 Структура лизоцима. Дисульфидные связи показаны пунктиром
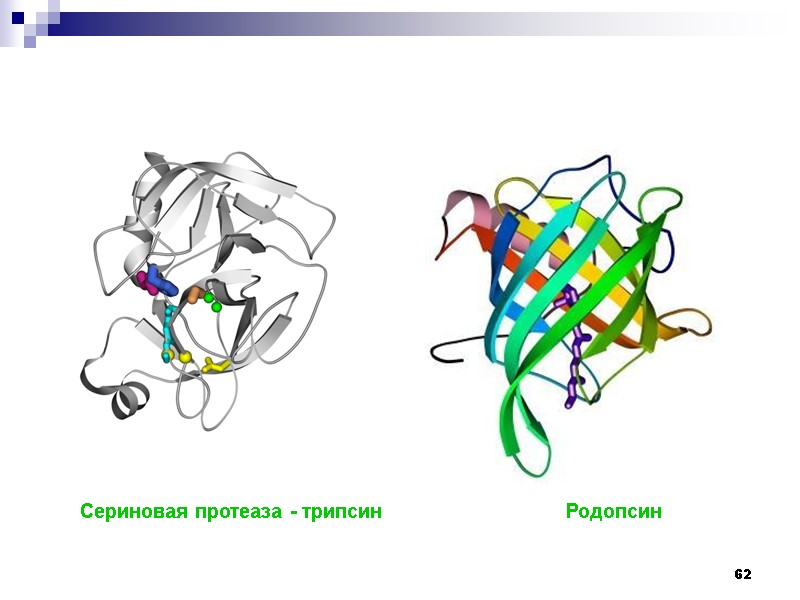
62 Сериновая протеаза - трипсин Родопсин
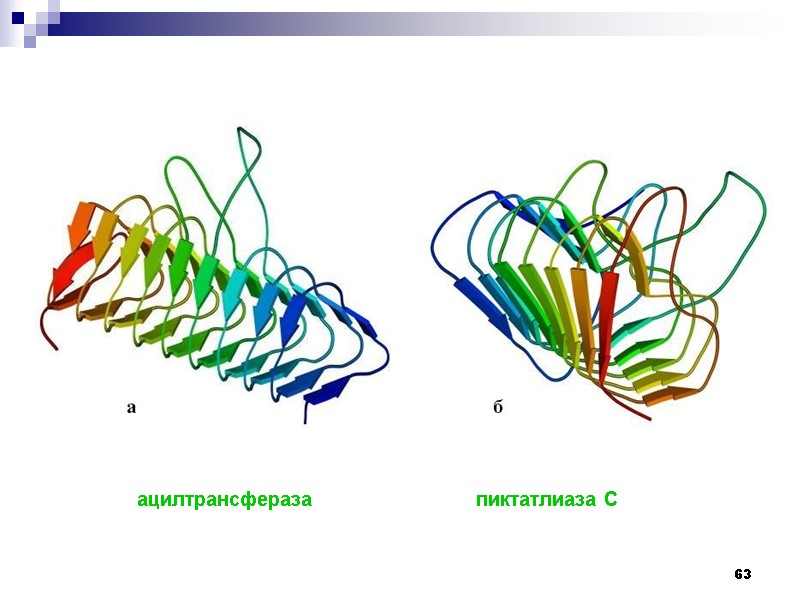
63 ацилтрансфераза пиктатлиаза С
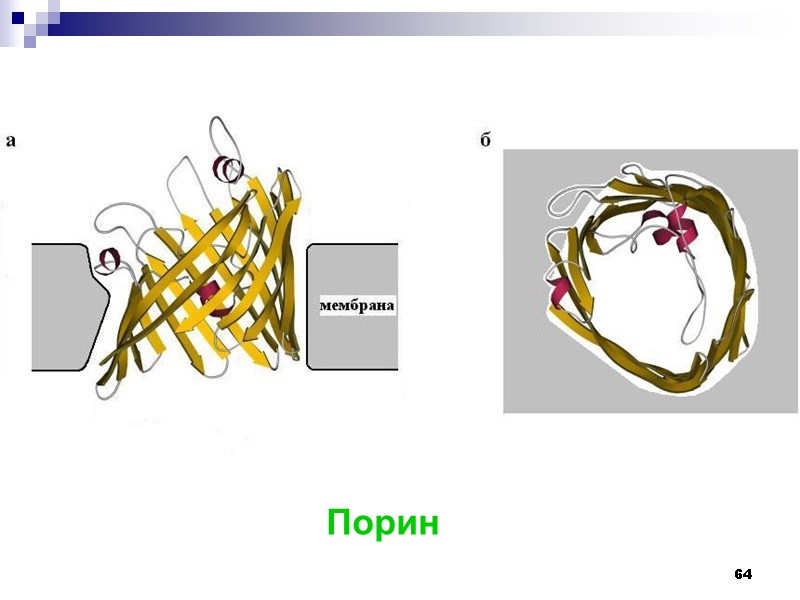
64 Порин

65
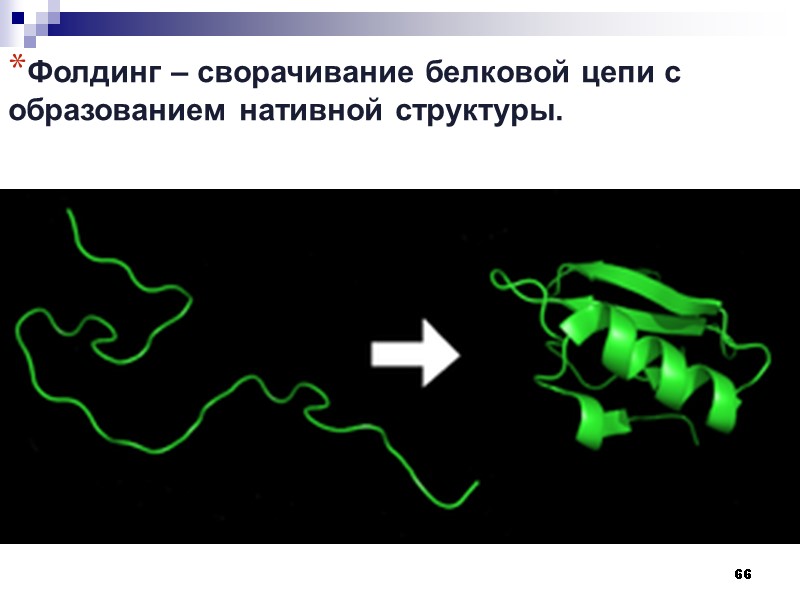
66 Фолдинг – сворачивание белковой цепи с образованием нативной структуры.
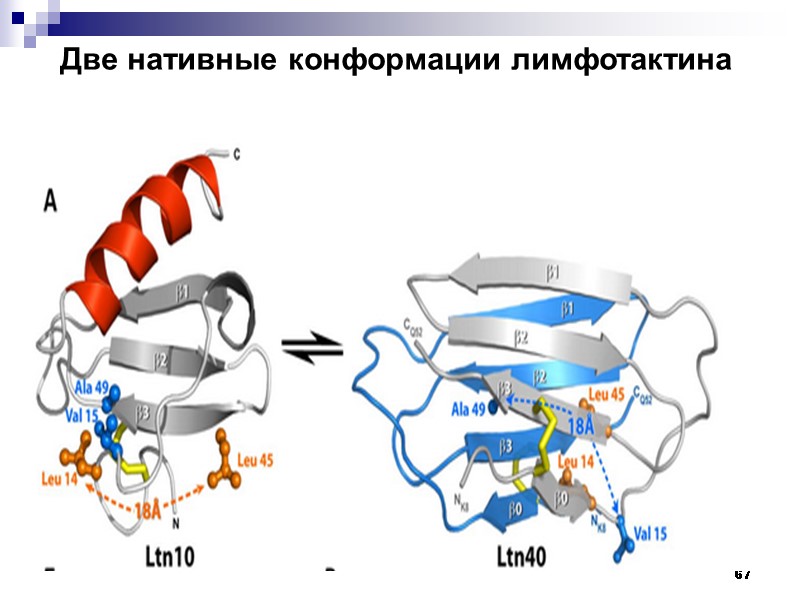
67 Две нативные конформации лимфотактина

68 Оловянная “чума” – переход белого олова (b-формы) в серое (a-форму)

69 Этот белок может существовать в двух конформациях – “здоровой” PrPC, которую можно обнаружить в здоровых клетках и “патологической” – PrPSc, которая является прионом. Для PrPC формы характерно преобладание a-спиралей, а для PrPSc – наличие b–складчатых слоёв. Белок PrPC

70 губчатые энцефалопатии Синдром Крейцфельда-Якоба Новый вариант Крейцфельда-Якоба – коровье бешенство синдром Герсманна–Штройслера–Шейнкера хроническая семейная бессонница, куру, скрепи
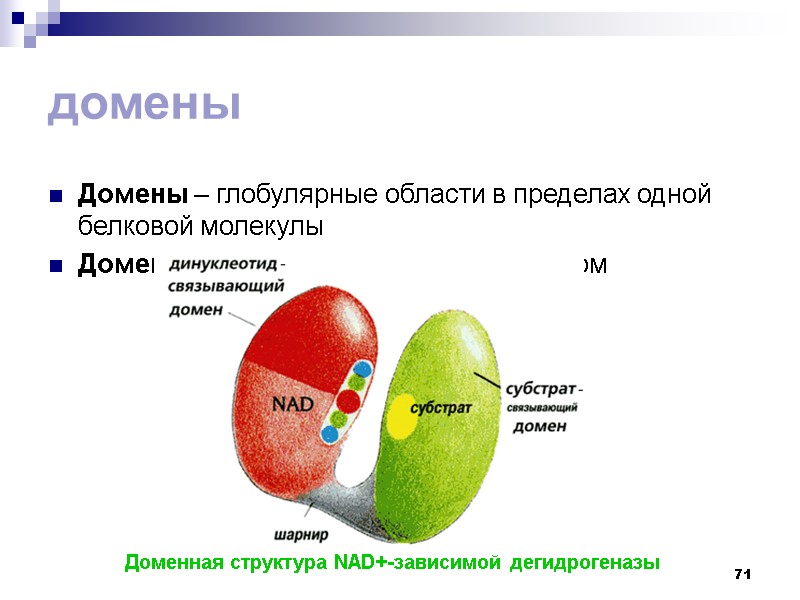
71 домены Домены – глобулярные области в пределах одной белковой молекулы Домены соединены шарнирным участком Доменная структура NAD+-зависимой дегидрогеназы

72 Под четвертичной структурой подразумевают способ укладки в пространстве отдельных полипептидных цепей (одинаковых или разных) с третичной структурой, приводящий к формированию единого в структурном и функциональном отношениях макромолекулярного образования (мультимера). Каждая отдельная полипептидная цепь в структуре мультимера называется протомером. Протомеры комплементарны и связываются в единую надмолекулярную структуру нековалентными связями. Самостоятельный протомер чаще всего не обладает биологической активностью.
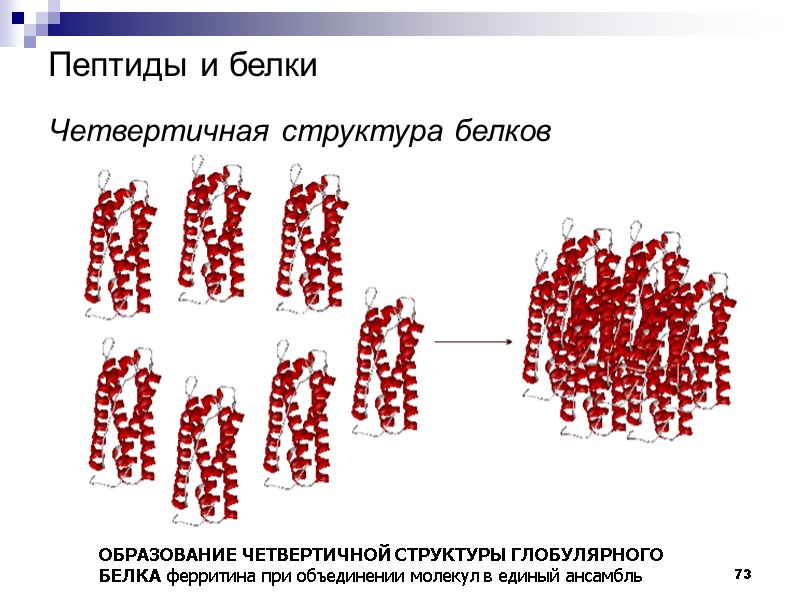
73 Пептиды и белки Четвертичная структура белков ОБРАЗОВАНИЕ ЧЕТВЕРТИЧНОЙ СТРУКТУРЫ ГЛОБУЛЯРНОГО БЕЛКА ферритина при объединении молекул в единый ансамбль
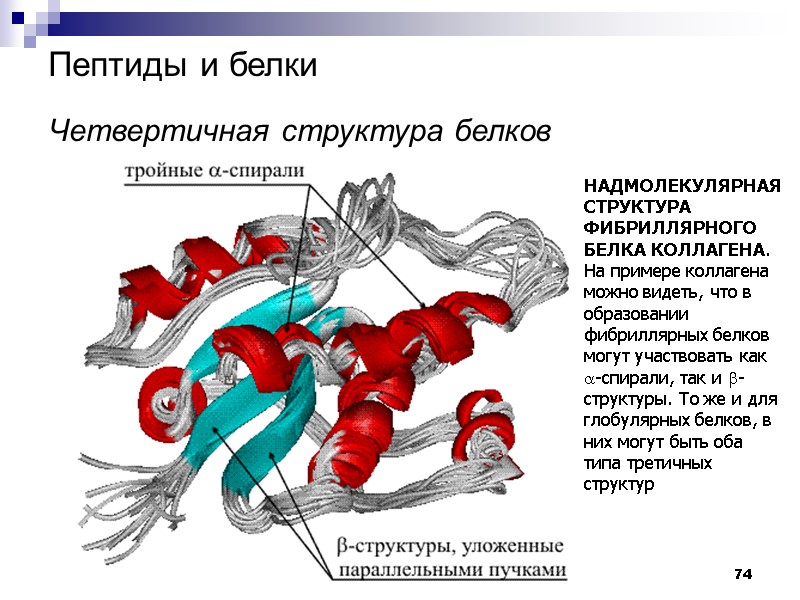
74 Пептиды и белки Четвертичная структура белков НАДМОЛЕКУЛЯРНАЯ СТРУКТУРА ФИБРИЛЛЯРНОГО БЕЛКА КОЛЛАГЕНА. На примере коллагена можно видеть, что в образовании фибриллярных белков могут участвовать как a-спирали, так и b-структуры. То же и для глобулярных белков, в них могут быть оба типа третичных структур
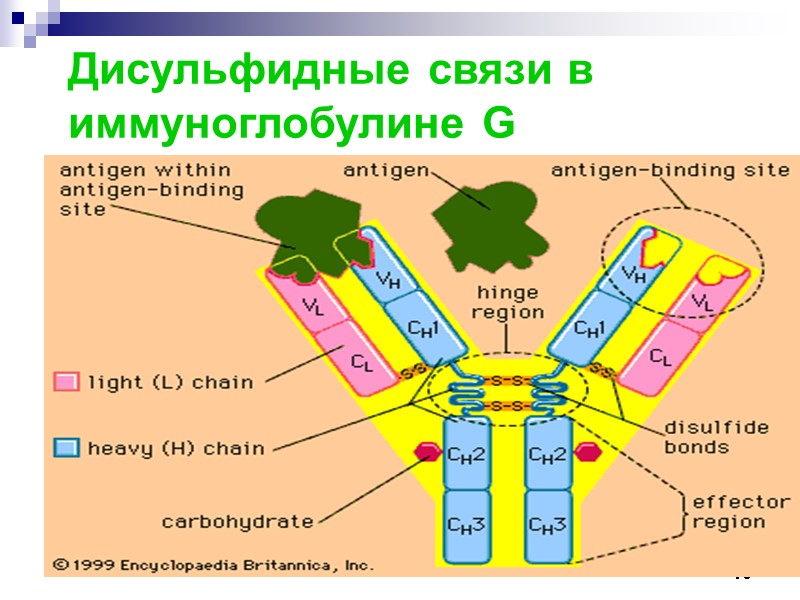
75 Дисульфидные связи в иммуноглобулине G

76 Четвертичная структура Пример четвертичной структуры - вирус табачной мозаики: 2130 одинаковых молекул белка расположены вокруг РНК вируса
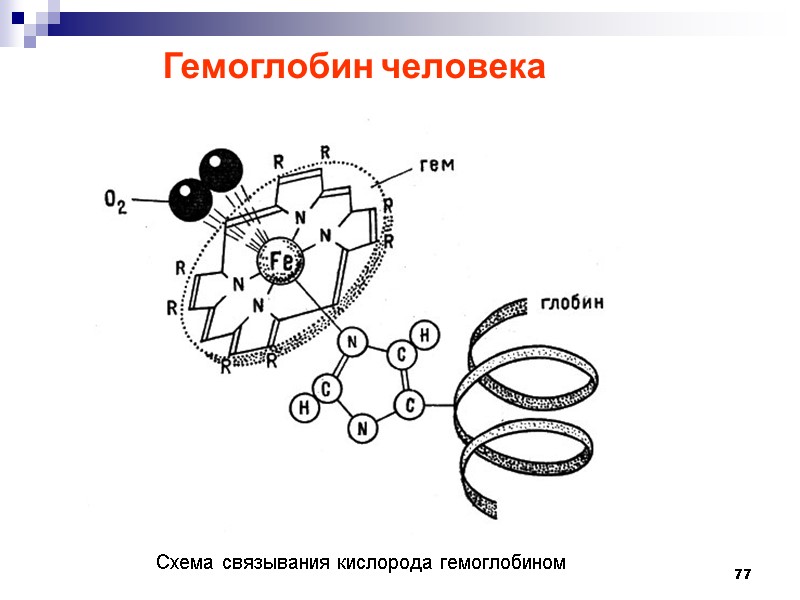
77 Гемоглобин человека Схема связывания кислорода гемоглобином

78 Гемоглобин выполняет роль переносчика кислорода от лёгких к клеткам Четвертичная структура гемоглобина. Чёрные диски обозначают молекулы гема.
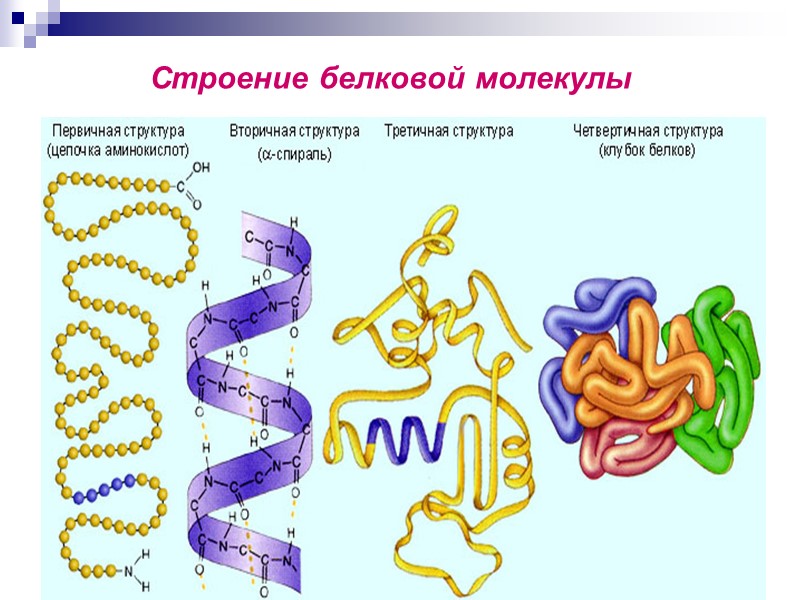
79 Строение белковой молекулы
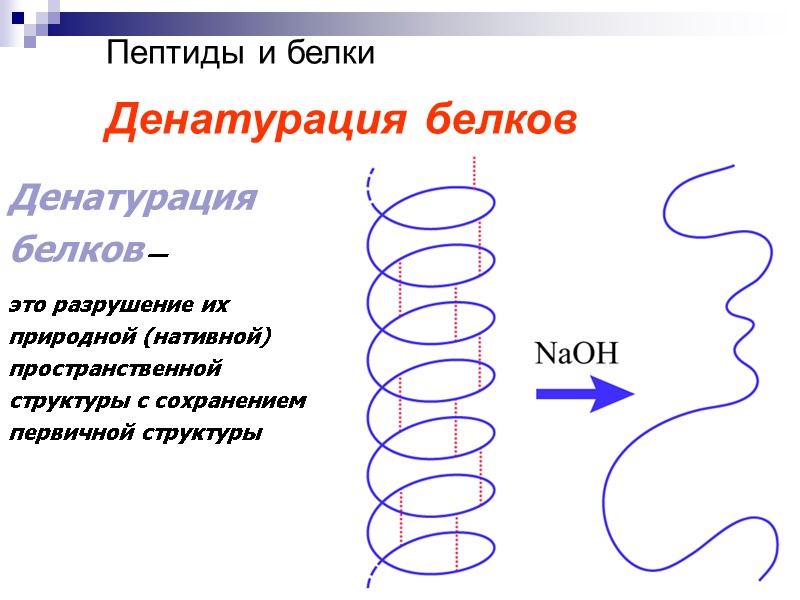
80 Пептиды и белки Денатурация белков Денатурация белков — это разрушение их природной (нативной) пространственной структуры с сохранением первичной структуры

81 Денатурированный белок теряет свои биологические свойства.
82 По данным Всемирной организации здравоохранения примерно половина населения земного шара находится в состоянии белкового голодания, а мировая нехватка пищевого белка составляет около 15 млн. тонн в год при норме потребления белка в сутки взрослым человеком 115 грамм

83 Цветные реакции на белки 1. Ксантопротеиновая – взаимодействие с концентрированной азотной кислотой, которое сопровождается появлением желтой окраски. 2. Биуретовая – взаимодействие слабощелочных растворов белков с раствором сульфата меди (II), в результате которой появляется фиолетово-синяя окраска.
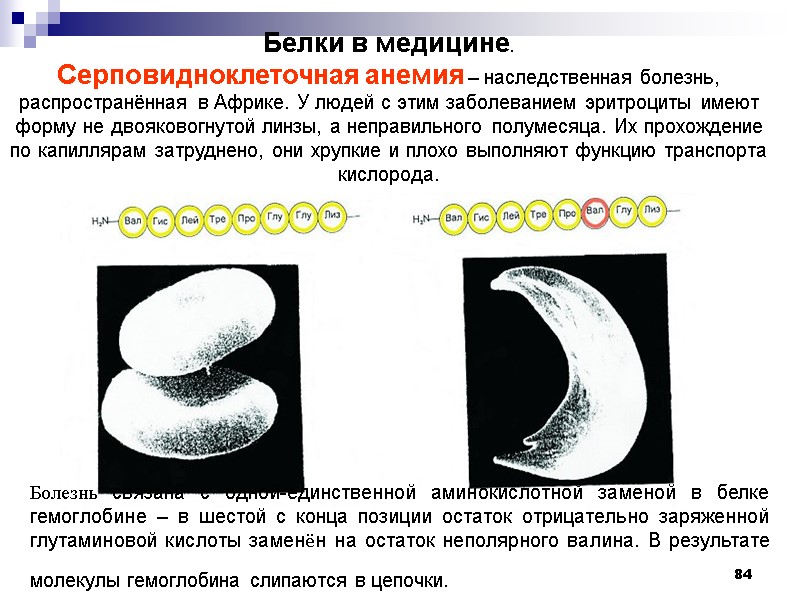
84 Белки в медицине. Серповидноклеточная анемия – наследственная болезнь, распространённая в Африке. У людей с этим заболеванием эритроциты имеют форму не двояковогнутой линзы, а неправильного полумесяца. Их прохождение по капиллярам затруднено, они хрупкие и плохо выполняют функцию транспорта кислорода. Болезнь связана с одной-единственной аминокислотной заменой в белке гемоглобине – в шестой с конца позиции остаток отрицательно заряженной глутаминовой кислоты заменён на остаток неполярного валина. В результате молекулы гемоглобина слипаются в цепочки.
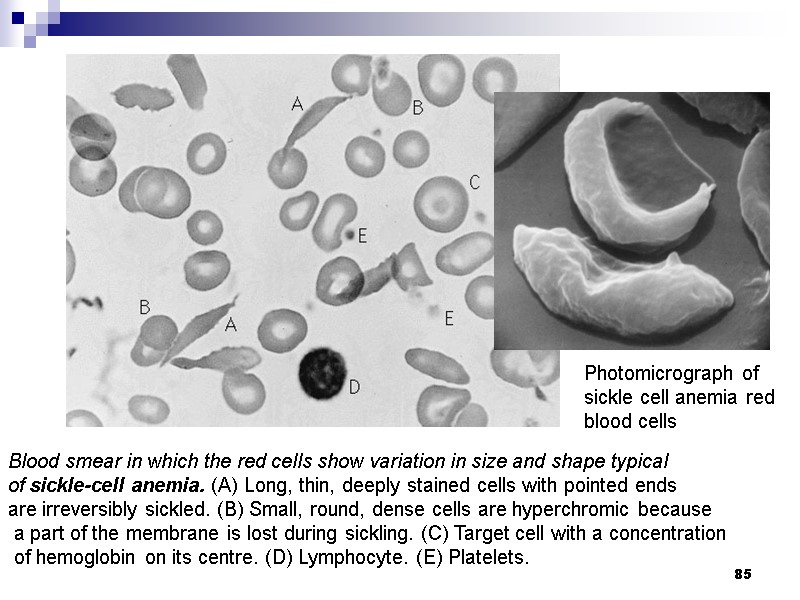
85 Photomicrograph of sickle cell anemia red blood cells Blood smear in which the red cells show variation in size and shape typical of sickle-cell anemia. (A) Long, thin, deeply stained cells with pointed ends are irreversibly sickled. (B) Small, round, dense cells are hyperchromic because a part of the membrane is lost during sickling. (C) Target cell with a concentration of hemoglobin on its centre. (D) Lymphocyte. (E) Platelets.

86 Спасибо!!!
34936-16_peptidy_belki.ppt
- Количество слайдов: 86

