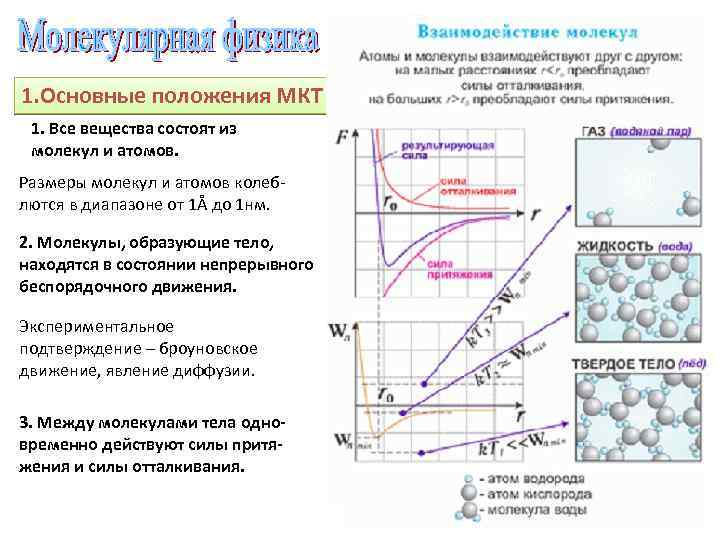
 1. Основные положения МКТ 1. Все вещества состоят из молекул и атомов. Размеры молекул и атомов колеблются в диапазоне от 1Å до 1 нм. 2. Молекулы, образующие тело, находятся в состоянии непрерывного беспорядочного движения. Экспериментальное подтверждение – броуновское движение, явление диффузии. 3. Между молекулами тела одновременно действуют силы притяжения и силы отталкивания.
1. Основные положения МКТ 1. Все вещества состоят из молекул и атомов. Размеры молекул и атомов колеблются в диапазоне от 1Å до 1 нм. 2. Молекулы, образующие тело, находятся в состоянии непрерывного беспорядочного движения. Экспериментальное подтверждение – броуновское движение, явление диффузии. 3. Между молекулами тела одновременно действуют силы притяжения и силы отталкивания.
 Основные понятия Атомная единица массы вещества Относительная молекулярная (атомная) массы вещества Моль – количество вещества, в котором содержится столько же молекул (атомов), сколько содержится в 0, 012 кг углерода Молярная масса Количество вещества Моль любого идеального газа при нормальных условиях (Т=273 К, р=101, 3 к. Па) занимает объем V=22. 4 л. 2. Уравнение состояния идеального газа Клапейрон, 1834 г. - для произвольной массы газа: Менделеев, 1874 г. - для моля ( =1 моль) газа В = R. Для произвольной массы газа:
Основные понятия Атомная единица массы вещества Относительная молекулярная (атомная) массы вещества Моль – количество вещества, в котором содержится столько же молекул (атомов), сколько содержится в 0, 012 кг углерода Молярная масса Количество вещества Моль любого идеального газа при нормальных условиях (Т=273 К, р=101, 3 к. Па) занимает объем V=22. 4 л. 2. Уравнение состояния идеального газа Клапейрон, 1834 г. - для произвольной массы газа: Менделеев, 1874 г. - для моля ( =1 моль) газа В = R. Для произвольной массы газа:
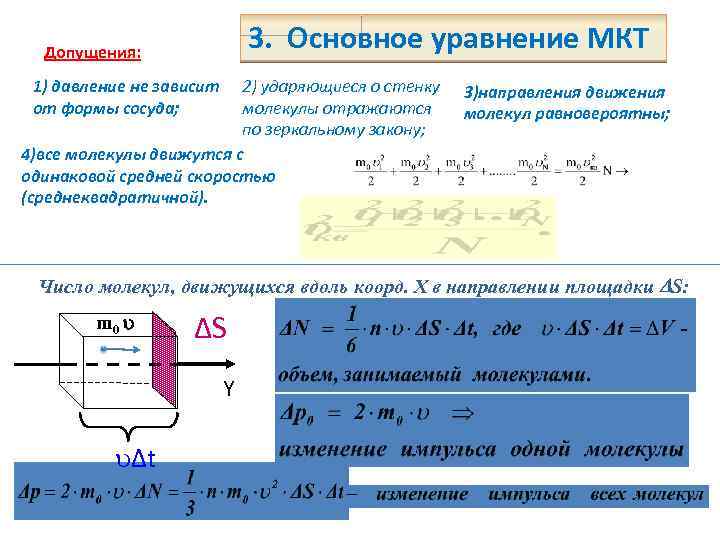 3. Основное уравнение МКТ Допущения: 1) давление не зависит от формы сосуда; 2) ударяющиеся о стенку молекулы отражаются по зеркальному закону; 4)все молекулы движутся с одинаковой средней скоростью (среднеквадратичной). 3)направления движения молекул равновероятны; Число молекул, движущихся вдоль коорд. Х в направлении площадки S: m 0 ΔS Y Δt
3. Основное уравнение МКТ Допущения: 1) давление не зависит от формы сосуда; 2) ударяющиеся о стенку молекулы отражаются по зеркальному закону; 4)все молекулы движутся с одинаковой средней скоростью (среднеквадратичной). 3)направления движения молекул равновероятны; Число молекул, движущихся вдоль коорд. Х в направлении площадки S: m 0 ΔS Y Δt
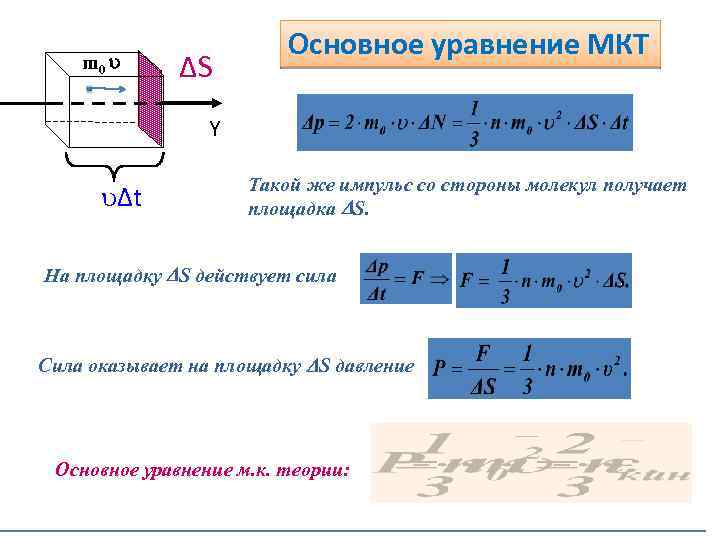 m 0 ΔS Основное уравнение МКТ Y Δt Такой же импульс со стороны молекул получает площадка S. На площадку S действует сила Сила оказывает на площадку S давление Основное уравнение м. к. теории:
m 0 ΔS Основное уравнение МКТ Y Δt Такой же импульс со стороны молекул получает площадка S. На площадку S действует сила Сила оказывает на площадку S давление Основное уравнение м. к. теории:
 4. Следствия из основного уравнения МКТ 1. Физический смысл температуры газа Из уравнения состояния идеального газа и основного уравнения МКТ следует, что (1) Абсолютная температура газа является мерой средней кинетической энергии теплового движения молекул. Из уравнения (1) следует, что в природе существует минимальная температура – абсолютный ноль Т=0.
4. Следствия из основного уравнения МКТ 1. Физический смысл температуры газа Из уравнения состояния идеального газа и основного уравнения МКТ следует, что (1) Абсолютная температура газа является мерой средней кинетической энергии теплового движения молекул. Из уравнения (1) следует, что в природе существует минимальная температура – абсолютный ноль Т=0.
 4. Следствия из основного уравнения МКТ 2. Средняя квадратичная скорость молекул (1) Учитывая, что кинетическая энергия поступательного движения молекул равна из уравнения (1) определим среднюю квадратичную скорость 3. Закон Дальтона Давление идеального газа при Т=const зависит от и не зависит от их строения: концентрации молекул Давление смеси газов равно сумме их парциальных давлений где рi - парциальное давление i-го газа.
4. Следствия из основного уравнения МКТ 2. Средняя квадратичная скорость молекул (1) Учитывая, что кинетическая энергия поступательного движения молекул равна из уравнения (1) определим среднюю квадратичную скорость 3. Закон Дальтона Давление идеального газа при Т=const зависит от и не зависит от их строения: концентрации молекул Давление смеси газов равно сумме их парциальных давлений где рi - парциальное давление i-го газа.
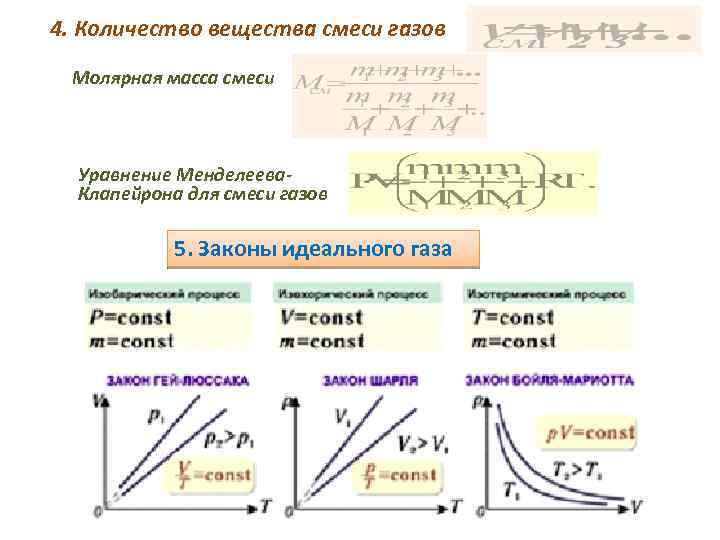 4. Количество вещества смеси газов Молярная масса смеси Уравнение Менделеева. Клапейрона для смеси газов 5. Законы идеального газа
4. Количество вещества смеси газов Молярная масса смеси Уравнение Менделеева. Клапейрона для смеси газов 5. Законы идеального газа
 Предположим, что мы сделали «моментальную фотографию» небольшого объема газа, на которой указаны скорости каждой молекулы. Расположим молекулы вдоль координаты скорости в виде точек. 6. Распределение Максвелла f( ) N + Скорости большинства молекул группируются в основном вблизи наиболее вероятного значения. Близкие к нулю и очень большие значения скорости встречаются сравнительно редко. Число молекул N, скорости которых лежат в интервале от до + , зависит от общего количества молекул N в выбранном объеме. Относительное число молекул N/N, скорости которых попадают внутрь интервала , называется функцией распределения молекул по скоростям: Функцию распределения молекул по скоростям теоретически нашел Максвелл в 1860 году. где А- множитель, не зависящий от скорости, m – масса молекулы, k – постоянная Больцмана, Т – абсолютная температура.
Предположим, что мы сделали «моментальную фотографию» небольшого объема газа, на которой указаны скорости каждой молекулы. Расположим молекулы вдоль координаты скорости в виде точек. 6. Распределение Максвелла f( ) N + Скорости большинства молекул группируются в основном вблизи наиболее вероятного значения. Близкие к нулю и очень большие значения скорости встречаются сравнительно редко. Число молекул N, скорости которых лежат в интервале от до + , зависит от общего количества молекул N в выбранном объеме. Относительное число молекул N/N, скорости которых попадают внутрь интервала , называется функцией распределения молекул по скоростям: Функцию распределения молекул по скоростям теоретически нашел Максвелл в 1860 году. где А- множитель, не зависящий от скорости, m – масса молекулы, k – постоянная Больцмана, Т – абсолютная температура.
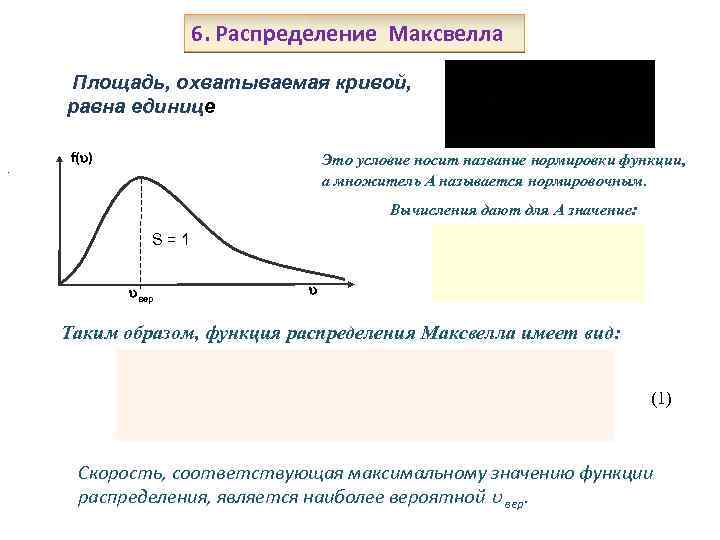 6. Распределение Максвелла Площадь, охватываемая кривой, равна единице. f( ) Это условие носит название нормировки функции, а множитель А называется нормировочным. Вычисления дают для А значение: S=1 вер Таким образом, функция распределения Максвелла имеет вид: (1) Скорость, соответствующая максимальному значению функции распределения, является наиболее вероятной вер.
6. Распределение Максвелла Площадь, охватываемая кривой, равна единице. f( ) Это условие носит название нормировки функции, а множитель А называется нормировочным. Вычисления дают для А значение: S=1 вер Таким образом, функция распределения Максвелла имеет вид: (1) Скорость, соответствующая максимальному значению функции распределения, является наиболее вероятной вер.
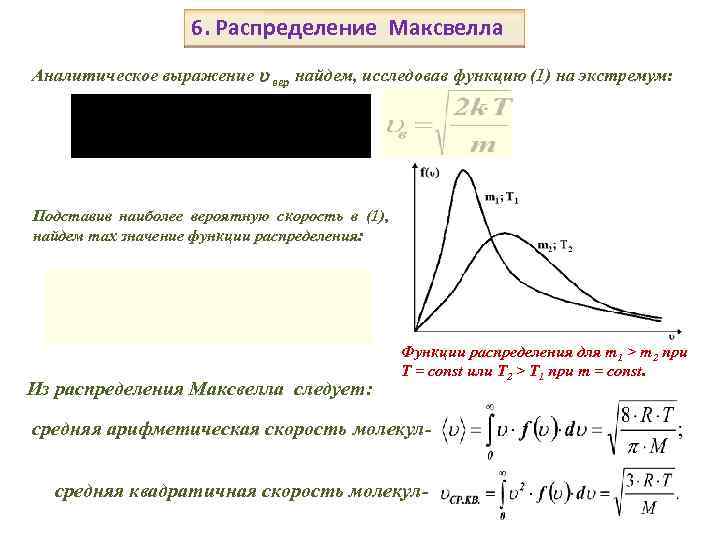 6. Распределение Максвелла Аналитическое выражение вер найдем, исследовав функцию (1) на экстремум: Подставив наиболее вероятную скорость в (1), найдем max значение функции распределения: Из распределения Максвелла следует: Функции распределения для m 1 > m 2 при Т = const или Т 2 > T 1 при m = const. средняя арифметическая скорость молекулсредняя квадратичная скорость молекул-
6. Распределение Максвелла Аналитическое выражение вер найдем, исследовав функцию (1) на экстремум: Подставив наиболее вероятную скорость в (1), найдем max значение функции распределения: Из распределения Максвелла следует: Функции распределения для m 1 > m 2 при Т = const или Т 2 > T 1 при m = const. средняя арифметическая скорость молекулсредняя квадратичная скорость молекул-
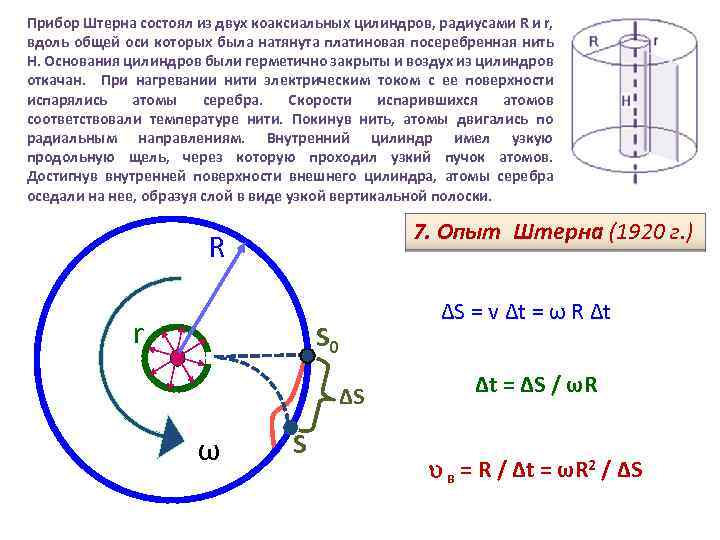 Прибор Штерна состоял из двух коаксиальных цилиндров, радиусами R и r, вдоль общей оси которых была натянута платиновая посеребренная нить Н. Основания цилиндров были герметично закрыты и воздух из цилиндров откачан. При нагревании нити электрическим током с ее поверхности испарялись атомы серебра. Скорости испарившихся атомов соответствовали температуре нити. Покинув нить, атомы двигались по радиальным направлениям. Внутренний цилиндр имел узкую продольную щель, через которую проходил узкий пучок атомов. Достигнув внутренней поверхности внешнего цилиндра, атомы серебра оседали на нее, образуя слой в виде узкой вертикальной полоски. 7. Опыт Штерна (1920 г. ) R r ΔS = v Δt = ω R Δt S 0 ΔS ω S Δt = ΔS / ωR в = R / Δt = ωR 2 / ΔS
Прибор Штерна состоял из двух коаксиальных цилиндров, радиусами R и r, вдоль общей оси которых была натянута платиновая посеребренная нить Н. Основания цилиндров были герметично закрыты и воздух из цилиндров откачан. При нагревании нити электрическим током с ее поверхности испарялись атомы серебра. Скорости испарившихся атомов соответствовали температуре нити. Покинув нить, атомы двигались по радиальным направлениям. Внутренний цилиндр имел узкую продольную щель, через которую проходил узкий пучок атомов. Достигнув внутренней поверхности внешнего цилиндра, атомы серебра оседали на нее, образуя слой в виде узкой вертикальной полоски. 7. Опыт Штерна (1920 г. ) R r ΔS = v Δt = ω R Δt S 0 ΔS ω S Δt = ΔS / ωR в = R / Δt = ωR 2 / ΔS
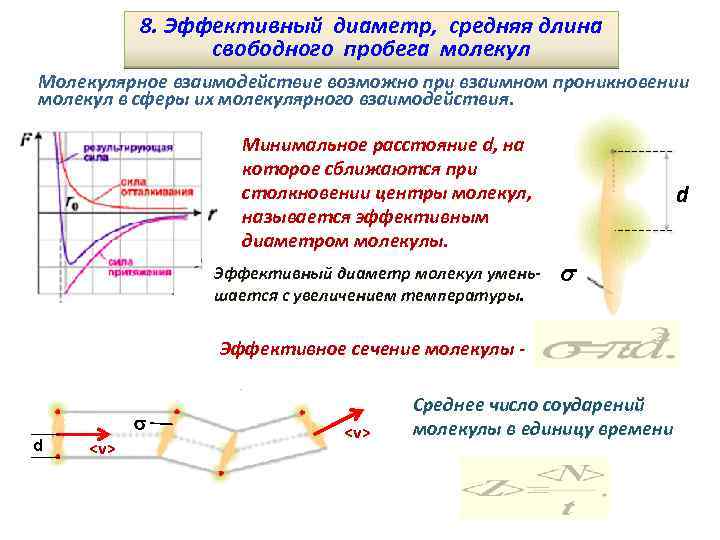 8. Эффективный диаметр, средняя длина свободного пробега молекул Молекулярное взаимодействие возможно при взаимном проникновении молекул в сферы их молекулярного взаимодействия. Минимальное расстояние d, на которое сближаются при столкновении центры молекул, называется эффективным диаметром молекулы. Эффективный диаметр молекул уменьшается с увеличением температуры. d Эффективное сечение молекулы d
8. Эффективный диаметр, средняя длина свободного пробега молекул Молекулярное взаимодействие возможно при взаимном проникновении молекул в сферы их молекулярного взаимодействия. Минимальное расстояние d, на которое сближаются при столкновении центры молекул, называется эффективным диаметром молекулы. Эффективный диаметр молекул уменьшается с увеличением температуры. d Эффективное сечение молекулы d
 Эффективный диаметр, средняя длина свободного пробега молекул С учетом относительного движения молекул среднее число столкновений Среднее расстояние, проходимое молекулой между двумя последовательными столкновениями, называется средней длиной свободного пробега Совместное решение уравнений позволяет найти : С учетом уравнения состояния идеального газа p=nk. T
Эффективный диаметр, средняя длина свободного пробега молекул С учетом относительного движения молекул среднее число столкновений Среднее расстояние, проходимое молекулой между двумя последовательными столкновениями, называется средней длиной свободного пробега Совместное решение уравнений позволяет найти : С учетом уравнения состояния идеального газа p=nk. T
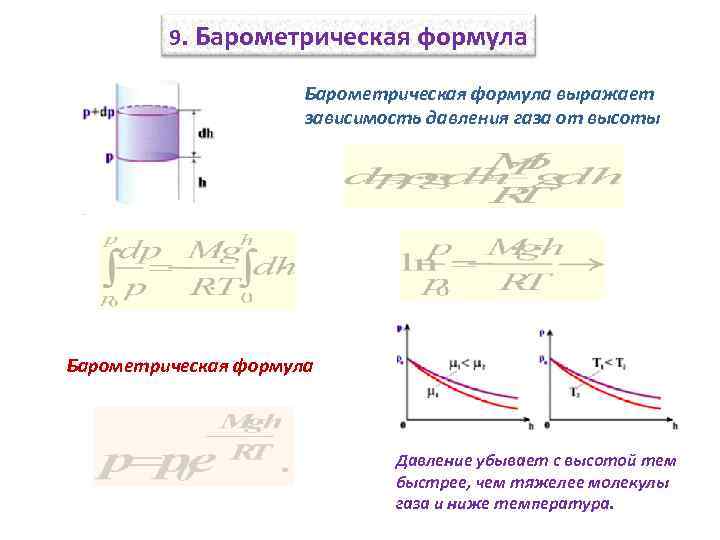 9. Барометрическая формула выражает зависимость давления газа от высоты Барометрическая формула Давление убывает с высотой тем быстрее, чем тяжелее молекулы газа и ниже температура.
9. Барометрическая формула выражает зависимость давления газа от высоты Барометрическая формула Давление убывает с высотой тем быстрее, чем тяжелее молекулы газа и ниже температура.
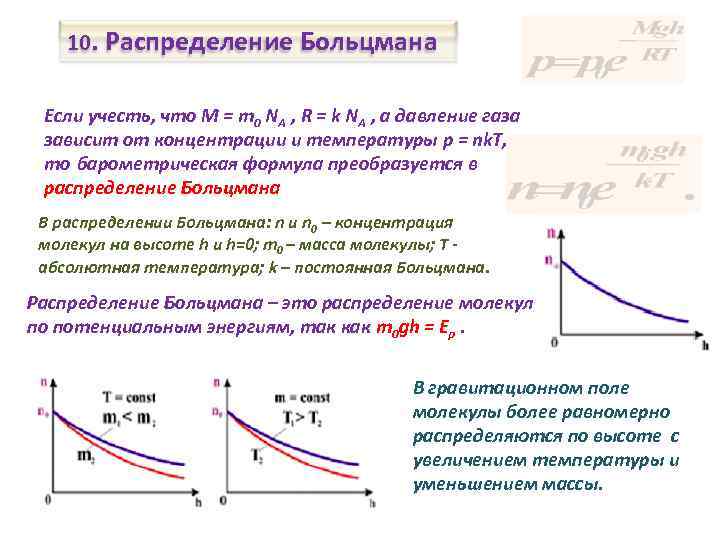 10. Распределение Больцмана Если учесть, что M = m 0 NA , R = k NA , а давление газа зависит от концентрации и температуры p = nk. T, то барометрическая формула преобразуется в распределение Больцмана В распределении Больцмана: n и n 0 – концентрация молекул на высоте h и h=0; m 0 – масса молекулы; Т абсолютная температура; k – постоянная Больцмана. Распределение Больцмана – это распределение молекул по потенциальным энергиям, так как m 0 gh = Ep. В гравитационном поле молекулы более равномерно распределяются по высоте с увеличением температуры и уменьшением массы.
10. Распределение Больцмана Если учесть, что M = m 0 NA , R = k NA , а давление газа зависит от концентрации и температуры p = nk. T, то барометрическая формула преобразуется в распределение Больцмана В распределении Больцмана: n и n 0 – концентрация молекул на высоте h и h=0; m 0 – масса молекулы; Т абсолютная температура; k – постоянная Больцмана. Распределение Больцмана – это распределение молекул по потенциальным энергиям, так как m 0 gh = Ep. В гравитационном поле молекулы более равномерно распределяются по высоте с увеличением температуры и уменьшением массы.
 11. Явления переноса Наука, изучающая процессы возникающие при нарушениях равновесия, называется физической кинетикой. Нарушение равновесия приводит к переносу из одних слоев среды в другие либо энергии, либо вещества , либо импульса. Теплопроводность При теплопроводности происходит перенос молекулами энергии из одних слоев в другие, что приводит к выравниванию температуры. - закон Фурье, 1822 г. градиент температуры. - коэффициент теплопроводности. где: - плотность вещества; с. V - удельная теплоемкость при постоянном объеме; < > -средняя арифметическая скорость; < > - средняя длина свободного пробега молекул.
11. Явления переноса Наука, изучающая процессы возникающие при нарушениях равновесия, называется физической кинетикой. Нарушение равновесия приводит к переносу из одних слоев среды в другие либо энергии, либо вещества , либо импульса. Теплопроводность При теплопроводности происходит перенос молекулами энергии из одних слоев в другие, что приводит к выравниванию температуры. - закон Фурье, 1822 г. градиент температуры. - коэффициент теплопроводности. где: - плотность вещества; с. V - удельная теплоемкость при постоянном объеме; < > -средняя арифметическая скорость; < > - средняя длина свободного пробега молекул.
 Диффузия При диффузии происходит перенос молекулами массы из одних слоев в другие, что приводит к выравниванию плотности. - закон Фика, 1895 г. градиент плотности. D - коэффициент диффузии. где: < > -средняя арифметическая скорость; < > - средняя длина свободного пробега молекул.
Диффузия При диффузии происходит перенос молекулами массы из одних слоев в другие, что приводит к выравниванию плотности. - закон Фика, 1895 г. градиент плотности. D - коэффициент диффузии. где: < > -средняя арифметическая скорость; < > - средняя длина свободного пробега молекул.
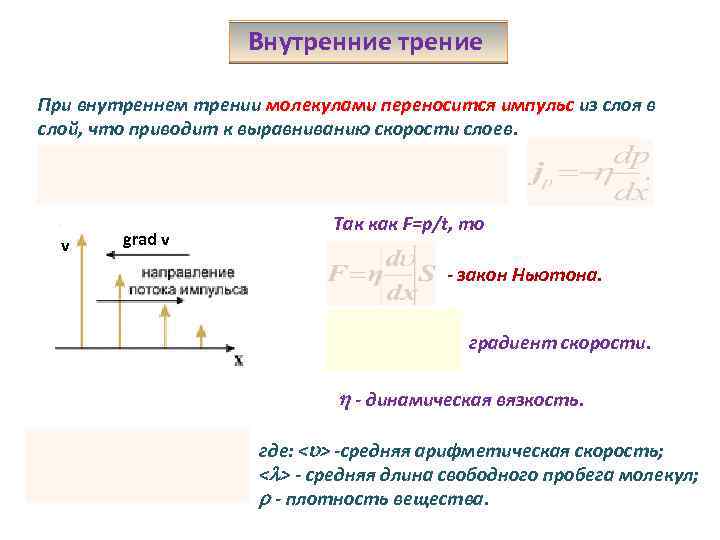 Внутренние трение При внутреннем трении молекулами переносится импульс из слоя в слой, что приводит к выравниванию скорости слоев. v grad v Так как F=p/t, то - закон Ньютона. градиент скорости. - динамическая вязкость. где: < > -средняя арифметическая скорость; < > - средняя длина свободного пробега молекул; - плотность вещества.
Внутренние трение При внутреннем трении молекулами переносится импульс из слоя в слой, что приводит к выравниванию скорости слоев. v grad v Так как F=p/t, то - закон Ньютона. градиент скорости. - динамическая вязкость. где: < > -средняя арифметическая скорость; < > - средняя длина свободного пробега молекул; - плотность вещества.


