05Дыхание 2012 Bio.ppt
- Количество слайдов: 77

1. Окисление органических веществ (углеводы, липиды, белки). Регуляция Red. Ox-статуса клетки! 2. Энегрообеспечение (субстратное+мембранное фосфорилирование) 3. Создание разнообразных углеродных скелетов для биосинтеза (автотрофность!) 4. Термогенез 5. Окислительная детоксикация

Уравнение фотосинтеза сахара (углеводы) кислород (побочный продукт) 6 CO 2 + 6 H 2 O + свет = C 6 H 12 O 6 + 6 O 2 Уравнение дыхания C 6 H 12 O 6 + 6 O 2 = 6 CO 2 + 6 H 2 O + энергия
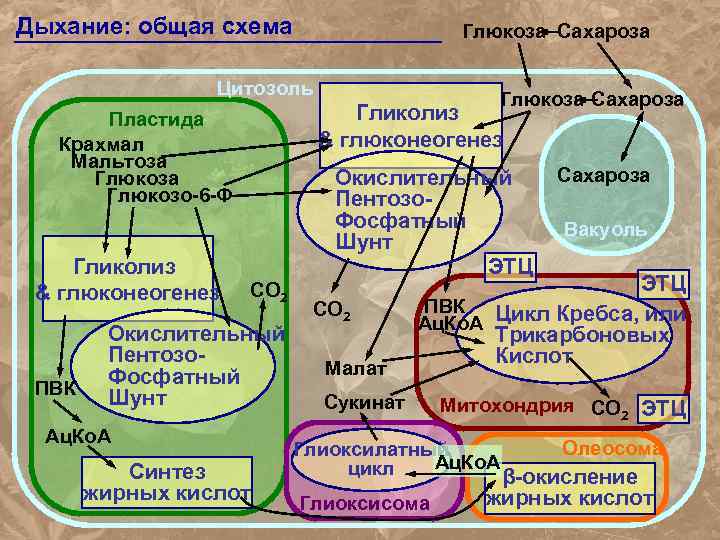
Дыхание: общая схема Глюкоза Сахароза Цитозоль Гликолиз & глюконеогенез Пластида Крахмал Мальтоза Глюкозо-6 -Ф Гликолиз & глюконеогенез ПВК Глюкоза Сахароза Окислительный Пентозо. Фосфатный Шунт ЭТЦ СО 2 Окислительный Пентозо. Фосфатный Шунт Ац. Ко. А Синтез жирных кислот СО 2 Малат Сахароза Вакуоль ЭТЦ ПВК Цикл Кребса, или Ац. Ко. А Трикарбоновых Кислот Сукинат Митохондрия СО 2 ЭТЦ Олеосома Глиоксилатный Ац. Ко. А цикл β-окисление Глиоксисома жирных кислот
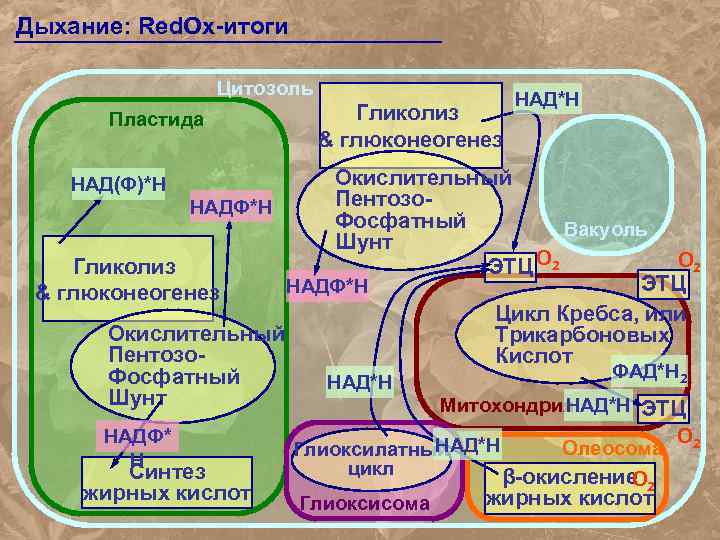
Дыхание: Red. Ox-итоги Цитозоль Пластида Гликолиз & глюконеогенез НАД*Н Окислительный Пентозо. НАДФ*Н Фосфатный Вакуоль Шунт О 2 Гликолиз ЭТЦ О 2 ЭТЦ НАДФ*Н & глюконеогенез Цикл Кребса, или Окислительный Трикарбоновых Пентозо. Кислот ФАД*Н 2 Фосфатный НАД*Н Шунт Митохондрия НАД*Н ЭТЦ НАД(Ф)*Н НАДФ* Н Синтез жирных кислот О НАД*Н Олеосома 2 Глиоксилатный цикл β-окисление 2 О жирных кислот Глиоксисома
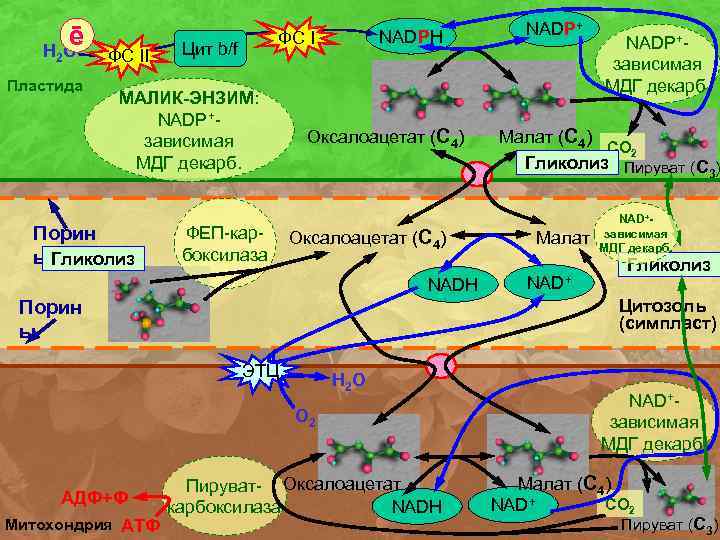
ē НО 2 Пластида ФC II ФC I Цит b/f МАЛИК-ЭНЗИМ: NADP+зависимая МДГ декарб. Порин ы. Гликолиз NADPH ФЕП-карбоксилаза Оксалоацетат (С 4) NADH ЭТЦ Н 2 О О 2 Митохондрия АТФ NADP+зависимая МДГ декарб. Малат (С 4) СО 2 Гликолиз Пируват (С ) 3 Малат NAD+зависимая МДГ декарб. Гликолиз Цитозоль (симпласт) Порин ы АДФ+Ф NADP+ Пируват- Оксалоацетат NADH карбоксилаза NAD+зависимая МДГ декарб. Малат (С 4) СО 2 NAD+ Пируват (С 3)
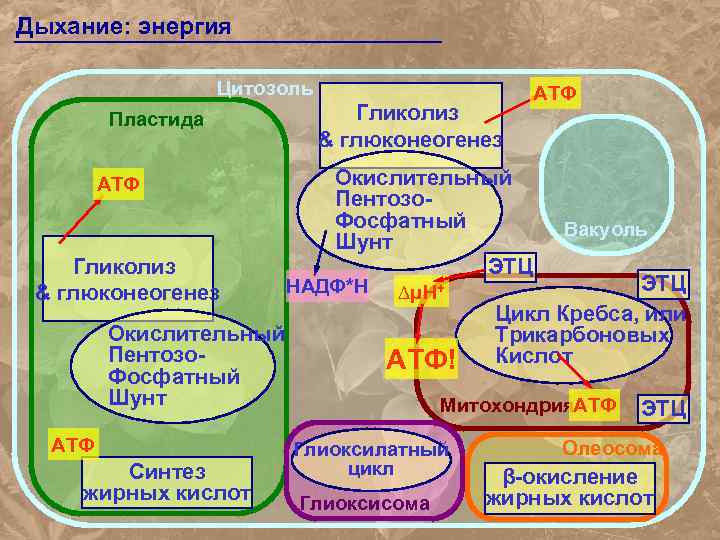
Дыхание: энергия Цитозоль Пластида АТФ Гликолиз & глюконеогенез Окислительный Пентозо. Фосфатный Шунт АТФ Синтез жирных кислот Гликолиз & глюконеогенез Окислительный Пентозо. Фосфатный Шунт ЭТЦ НАДФ*Н ∆μН+ АТФ! АТФ Вакуоль ЭТЦ Цикл Кребса, или Трикарбоновых Кислот Митохондрия. АТФ Глиоксилатный цикл Глиоксисома ЭТЦ Олеосома β-окисление жирных кислот
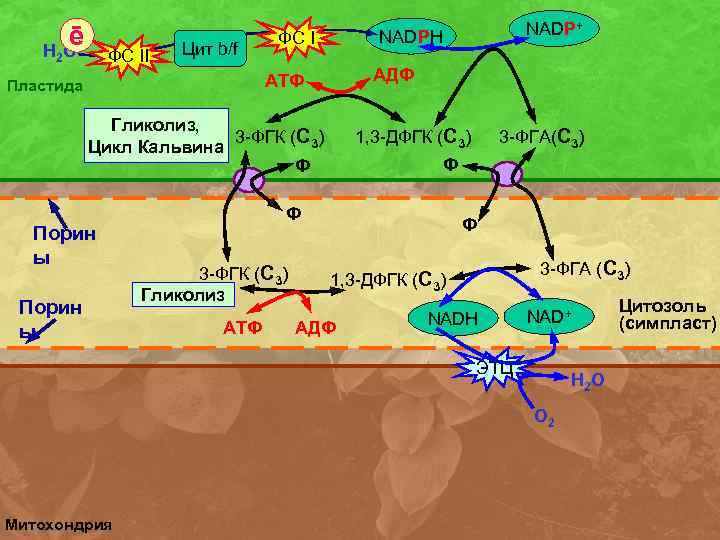
ē Н 2 О ФC II Цит b/f ФC I АДФ АТФ Пластида Гликолиз, 3 -ФГК (С 3) Цикл Кальвина Ф Порин ы NADP+ NADPH 1, 3 -ДФГК (С 3) Ф Ф 3 -ФГК (С 3) Гликолиз АТФ 3 -ФГА(С 3) Ф 3 -ФГА (С 3) 1, 3 -ДФГК (С 3) АДФ NADH NAD+ ЭТЦ Н 2 О О 2 Митохондрия Цитозоль (симпласт)

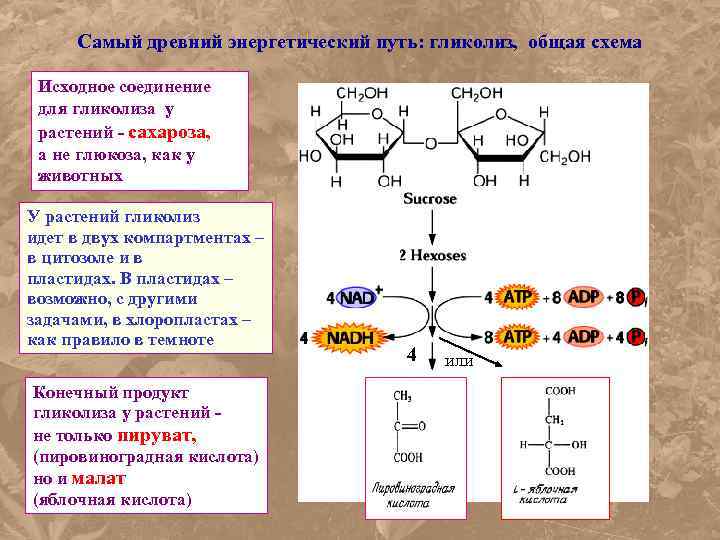
Самый древний энергетический путь: гликолиз, общая схема Исходное соединение для гликолиза у растений - сахароза, а не глюкоза, как у животных У растений гликолиз идет в двух компартментах – в цитозоле и в пластидах. В пластидах – возможно, с другими задачами, в хлоропластах – как правило в темноте Конечный продукт гликолиза у растений не только пируват, (пировиноградная кислота) но и малат (яблочная кислота) 4 или
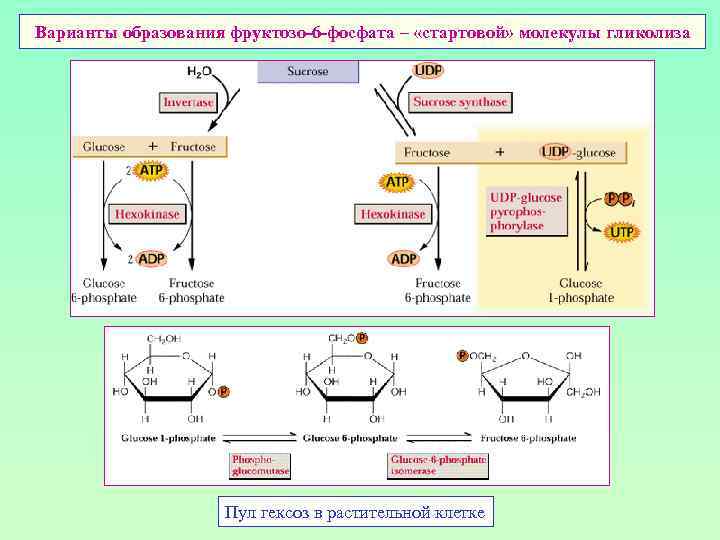
Варианты образования фруктозо-6 -фосфата – «стартовой» молекулы гликолиза Пул гексоз в растительной клетке

Основные стадии гликолиза и их «шунты» в растительной клетке АТФ-зависимая фосфофоруктокиназа Альдолаза Глицеральдегид 3 -Ф-дегидрогеназа Фософоглицераткиназа ФЕПкарбоксилаза Пируваткиназа Активируются при недостатке фосфора

Активация спиртового брожения наблюдается при аноксии НАДН НАД+ АЦЕТАЛЬДЕГИД АЛКОГОЛЬДЕГИДРОГЕН АЗА СО 2 ФЕП ЭТАНОЛ ПИРУВАТДЕКАРБОКСИ ЛАЗА ПИРУВАТ НАДН ФЕПКАРБОКСИЛАЗА НСО 3– ЛАКТАТДЕГИДРОГЕН АЗА НАД+ ЛАКТАТ НАДН ОКСАЛОАЦЕТАТ НАД+ МАЛАТ
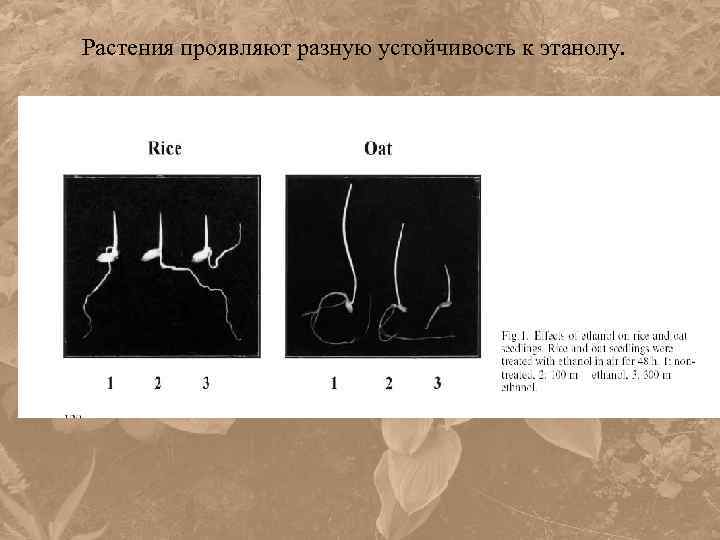
Растения проявляют разную устойчивость к этанолу.

Обращение реакции, катализируемой пируваткиназой СН 3 С=О С ОО- пируваткиназа СН 2 С-О~ Р С ОО- фосфоенолпируват АДФ пируват АТФ СО 2 АТФ ФЕП-КАРБОКСИКИНАЗА СО 2 пируваткарбоксилаза АДФ СОО С=О С Н 2 СОО- НАД-МДГ оксалоацетат НАДН цитозоль НАД+ СОО НОСН С Н 2 СОО- малат НАД-МДГ НАДН НАД+ СОО С=О С Н 2 СОО- оксалоацетат митохондрии

Регуляция гликолиза Животные Пластидный гликолиз Растения фруктозо-6 -Ф АТФ-ФФ-киназа ФФ АДФ Фруктозо-1, 6 -Ф ФЕП пируваткиназа ПВК
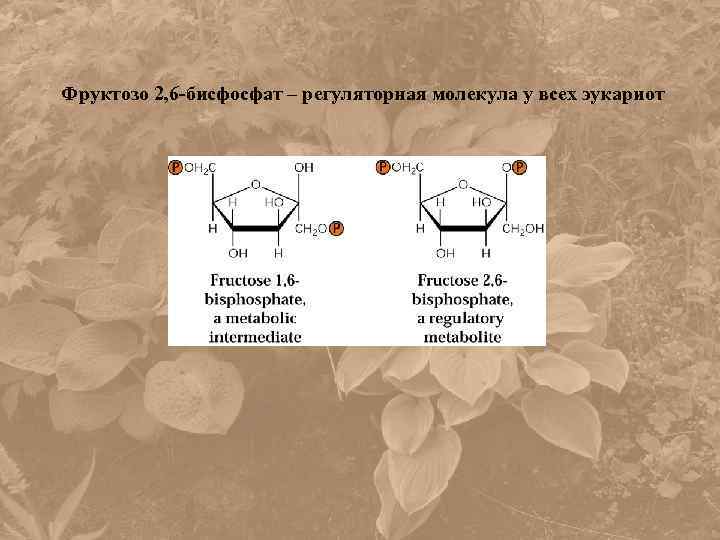
Фруктозо 2, 6 -бисфосфат – регуляторная молекула у всех эукариот

Ключевое место регуляции гликолиза: отношение С 6 / С 3 киназы фруктозо-6 -фосфат фруктозо-1. 6–бисфосфат ФГА , ФГК фосфатаза Фн фруктозо-6 -фосфат-2 -киназа фруктозо-6 -фосфат фруктозо-2. 6–бисфосфат фруктозо-2, 6 -бисфосфат-2 -фосфатаза Фн Фр-2, 6 -бф АТФ-ФФК АДФ Фр-2, 6 -бф ФФн-ФФК Фр-6 -ф фосфатаза АТФ Цитрат Фр-1. 6 -бф ФЕП, ФГК

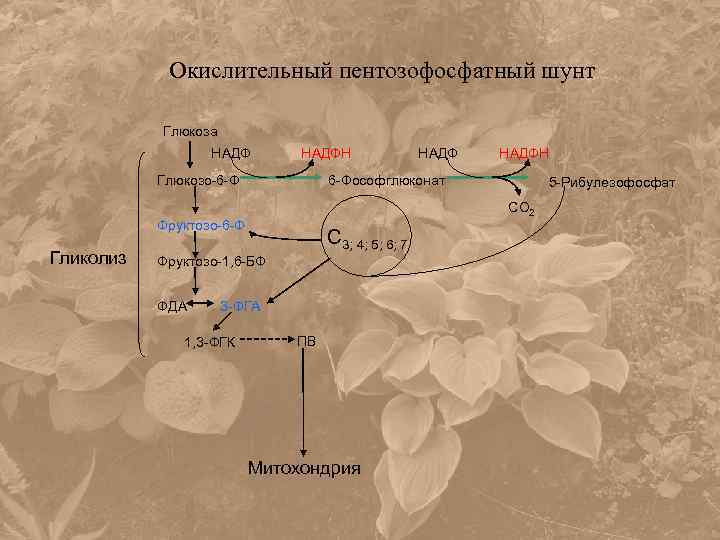
Окислительный пентозофосфатный шунт Глюкоза НАДФН Глюкозо-6 -Ф С 3; 4; 5; 6; 7 3 -ФГА 1, 3 -ФГК 5 -Рибулезофосфат СО 2 Фруктозо-1, 6 -БФ ФДА НАДФН 6 -Фософглюконат Фруктозо-6 -Ф Гликолиз НАДФ ПВ Митохондрия

Первые две реакции пентозофосфатного цикла необратимы и сопровождаются образованием НАДФН и рибулозо-5 -фосфата. СН 2 О(Р) 6 НАДФ+ О 6 х ОН ОН Глюкозо-6 -фосфат 6 НАДФН 6 Н 2 О 6 х COOH CНOH НOCH CНOH CH 2 O P 6 -фосфоглюконовая кислота 6 НАДФ+ 6 НАДФН 6 СО 2 6 х CH 2 ОН C =O CHOH CH 2 O P Рибулозо-5 -фосфат
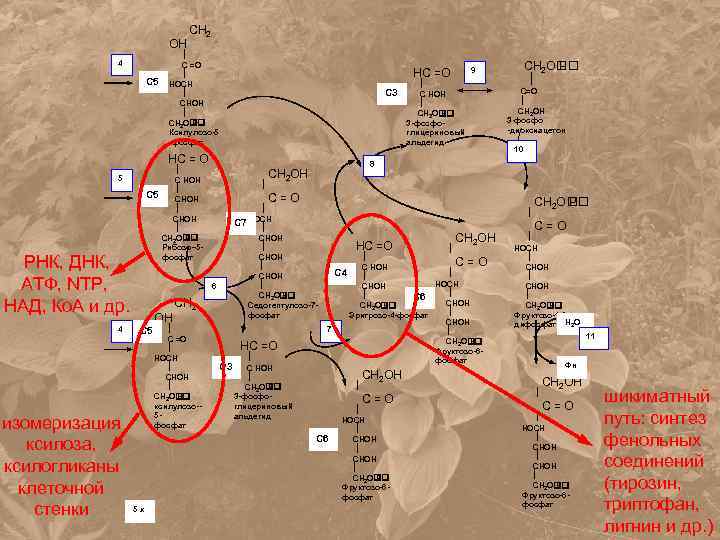
ОН 4 С 5 CH 2 C =O НОCH CHOH CH 2 O P Ксилулозо-5 -фосфат НС =О С 3 НC = О 5 С 5 РНК, ДНК, АТФ, NTP, НАД, Ко. А и др. 4 изомеризация ксилоза, ксилогликаны клеточной стенки C НOН CHOH CH 2 O P Рибозо--5 фосфат ОН СН 2 ОН 10 НС =О С 3 C НОН CH 2 O P 3 -фосфоглицериновый альдегид НС =О СН 2 ОН C=О C НОН С 4 НОCH СНОН С 6 CHOH CH 2 O P Эритрозо-4 -фосфат СНОН 7 CH 2 O P Фруктозо-6 фосфат СН 2 О Р C=О НОCH CHOH СНОН CH 2 O P Фруктозо-1. 6 дифосфат Н 2 О 11 Фн СН 2 ОН C=О С 6 5 х C=О CH 2 OН 3 -фосфо -диоксиацетон C=О СН 2 C =O НОCH CHOH CH 2 O P ксилулозо-5 фосфат C НОН CH 2 O P 3 -фосфоглицериновый альдегид 8 С 7 НОCH CHOH СНОН CH 2 O P Седогептулозо-7 фосфат 6 С 5 СН 2 О Р 9 НОCH CHOH СНОН CH 2 O P Фруктозо-6 фосфат СН 2 ОН C=О НОCH CHOH СНОН CH 2 O P Фруктозо-6 фосфат шикиматный путь: синтез фенольных соединений (тирозин, триптофан, лигнин и др. )

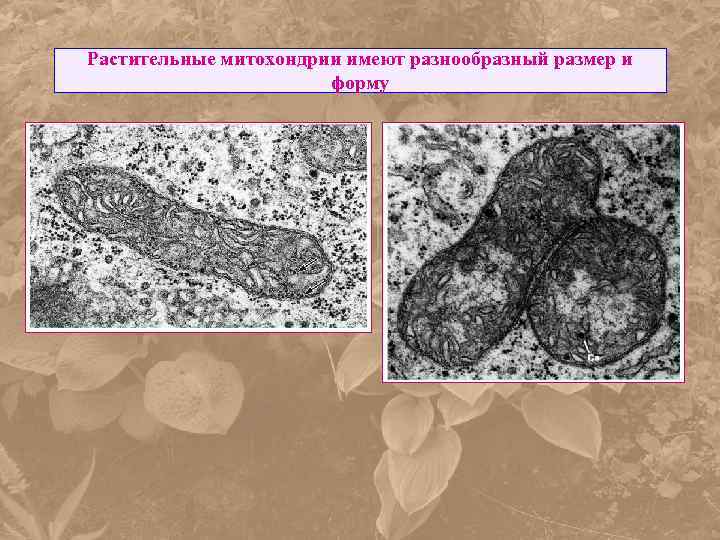
Растительные митохондрии имеют разнообразный размер и форму
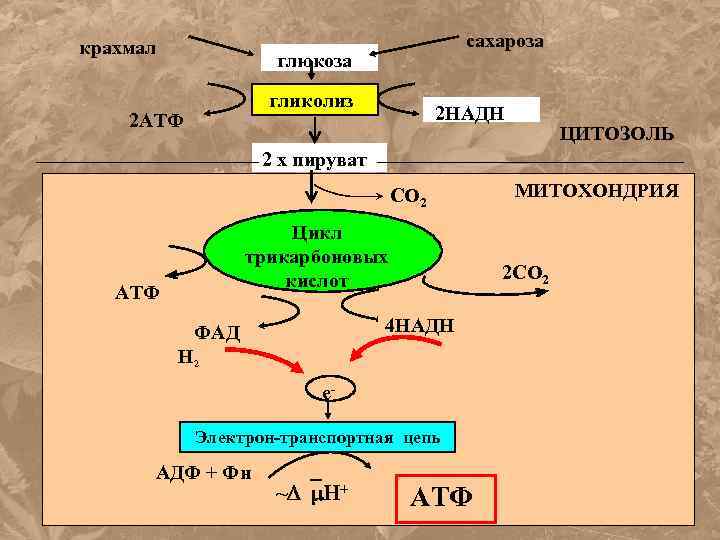
крахмал сахароза глюкоза гликолиз 2 АТФ 2 НАДН ЦИТОЗОЛЬ 2 х пируват СО 2 Цикл трикарбоновых кислот АТФ 2 СО 2 4 НАДН ФАД Н 2 e- Электрон-транспортная цепь АДФ + Фн ~ + МИТОХОНДРИЯ АТФ

Пируватдегидрогеназный комплекс SH-Со. А СО 2 пируват О СН 3 С S Со. А НАДН Ацетил Со. А Ацетил-S- Со. А НАД+ • Е 1 – пируватдегидрогеназа • Е 2 –дигидролипоилацетил трансфераза • Е 3 –дигидролипоил дегидрогеназа • Тиаминпирофосфат • Липоевая кислота НАД+, ФАД, Со. А

Ацетил-кофермент А (Acet-Co. A) – восстановленный углеводный фрагмент, который окисляется в митохондриях для восстановления НАДН Кофермент А - универсальный переносчик и “активатор” ацильных (жирнокислотных) групп Со. А-SH + CH 3 СOOH ↔ O || Co. A-S~C-CH 3 + Н 2 О. HH | | OHH || | | O H CH 3 H || | H 3 C~ S-C-C-N-C-C– C — АДФ – 3’Ф || O | | | H HH | | | HHH | | | OH CH 3 H ¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯ пантетеин: пантоевая к-та + β-аланин + цистеамин
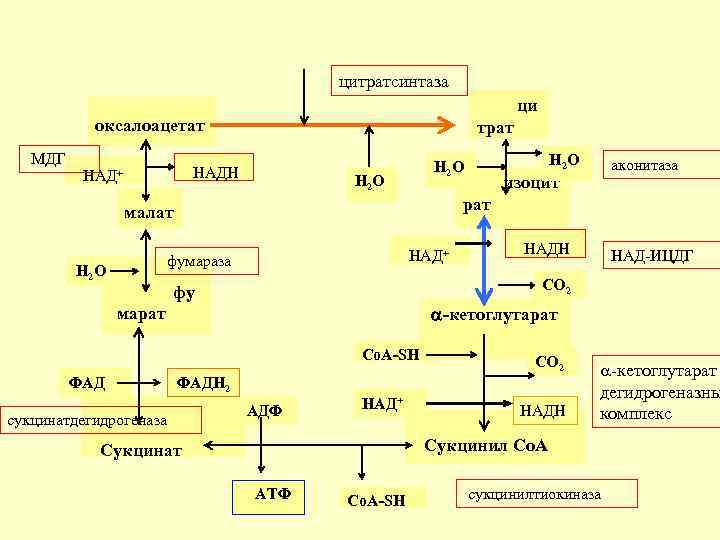
цитратсинтаза ци оксалоацетат МДГ трат НАДН НАД+ Н 2 О НАД+ фумараза изоцит НАДН -кетоглутарат Сo. A-SH СО 2 ФАДН 2 сукцинатдегидрогеназа НАД-ИЦДГ СО 2 фу фу марат ФАД аконитаза рат малат Н 2 О АДФ НАД+ НАДН -кетоглутарат дегидрогеназны комплекс Сукцинил Со. А Сукцинат АТФ Сo. A-SH сукцинилтиокиназа
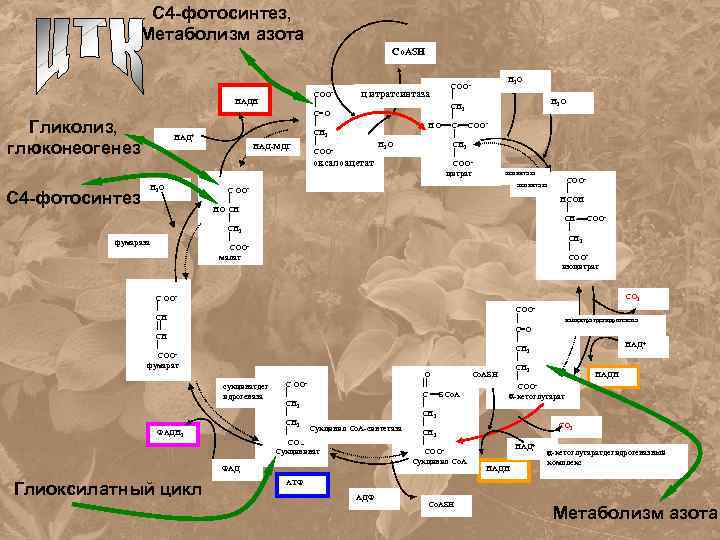
С 4 -фотосинтез, Метаболизм азота Co. ASH НАДН Гликолиз, глюконеогенез С 4 -фотосинтез НАД+ НАД-МДГ Н 2 О фумараза СООц итратсинтаза СН 2 С=О НО С- СООСН 2 Н 2 О СОО оксалоацетат СООцитрат Н 2 О аконитаза С ОО НО СН 2 СООмалат СОО НСОН СН- СОО СН 2 СООизоцитрат СО 2 С ОО СН СООфумарат СОО- сукцинатдег идрогеназа ФАДН 2 С ОО СН 2 Сукцинил Со. А-синтетаза СОО Сукцининат ФАД Глиоксилатный цикл Н 2 О СОО- изоцитратдегидрогеназа С О НАД+ СН 2 НАДН СОО -кетоглутарат О Co. ASH С SCo. A СН 2 НАД+ СООСукцинил Со. А НАДН СО 2 -кетоглутаратдегидрогеназный комплекс АТФ АДФ Co. ASH Метаболизм азота
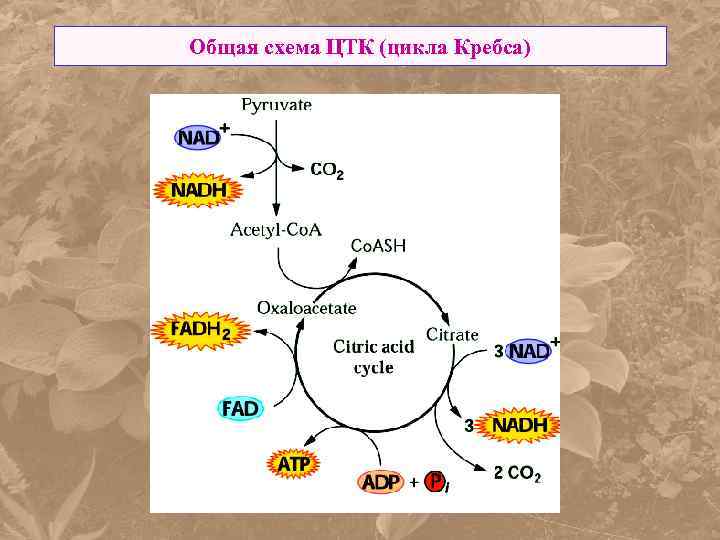
Общая схема ЦТК (цикла Кребса)
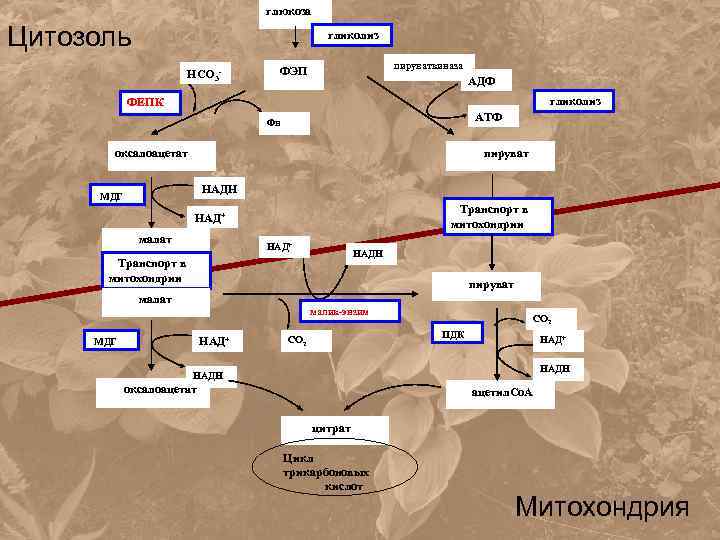
глюкоза Цитозоль гликолиз НСО 3 - пируваткиназа ФЭП АДФ гликолиз ФЕПК АТФ Фн оксалоацетат пируват НАДН МДГ Транспорт в митохондрии НАД+ малат НАД+ НАДН Транспорт в митохондрии пируват малик-энзим НАД+ МДГ СО 2 ПДК СО 2 НАД+ НАДН оксалоацетат ацетил. Со. А цитрат Цикл трикарбоновых кислот Митохондрия


Конверсия жиров в углеводы включает три этапа: Распад жиров и -окисление жирных кислот Глиоксилатный цикл в глиоксисомах Глюконеогенез

• В клетках животных жирные кислоты подвергаются -окислению в митохондриях • В клетках растений жирные кислоты подвергаются -окислению в глиоксисомах, которые являются разновидностью пероксисом. Глиоксисомы впервые были выделены Биверсом в 1967 г. (Beevers)
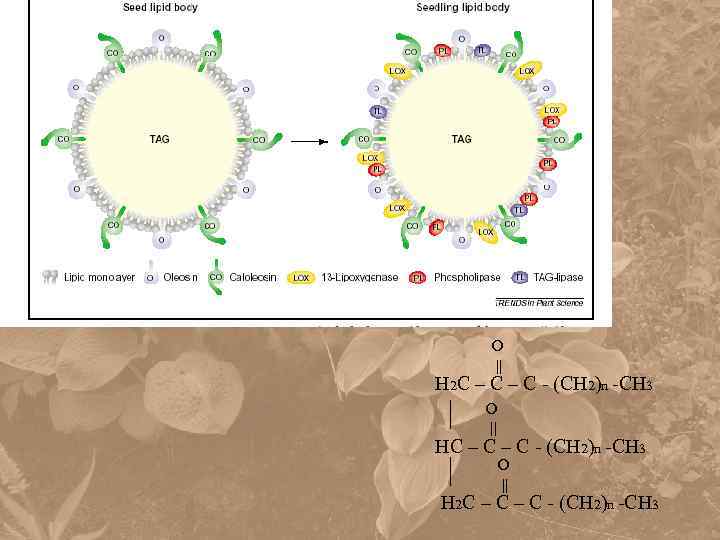
О || Н 2 С – С – С - (СН 2)n -СН 3 О || Н 2 С – С - (СН 2)n -СН 3
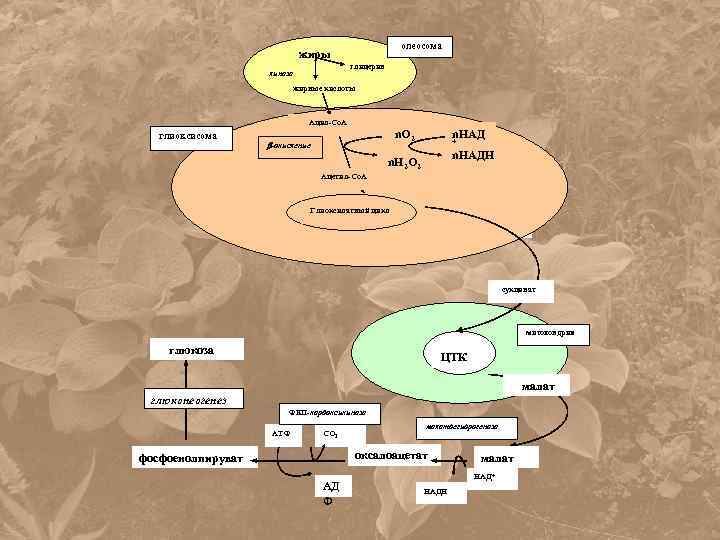
олеосома жиры глицерин липаза жирные кислоты Ацил-Со. А глиоксисома n. O 2 -окисление Ацетил-Со. А Глиоксилатный цикл n. НАД + n. НАДH n. H 2 O 2 Глиоксилатный цикл сукцинат митохондрия глюкоза ЦТК малат глюконеогенез ФЕП-карбоксикиназа АТФ СО 2 малатдегидрогеназа оксалоацетат фосфоенолпируват АД Ф малат НАД+ НАДН
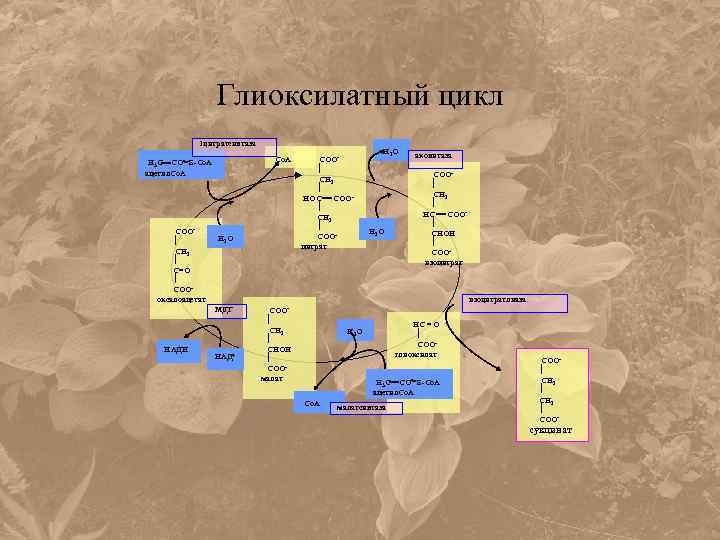
Глиоксилатный цикл 1 цитратсинтаза Н 3 С СО S-Co. A ацетил. Со. А СОО СН 2 С=О СООоксалоацетат Co. A Н 2 О аконитаза СОО СН 2 НС СОО СНОН СООизоцитратлиаза МДГ НАДН СОО СН 2 НОС СОО СН 2 СООцитрат НАД+ СОО СН 2 СНОН СООмалат НС = О СООглиоксилат Н 2 О Н 3 С СО S-Co. A ацетил. Со. А Co. A малатсинтаза СОО СН 2 СОО- сукцинат
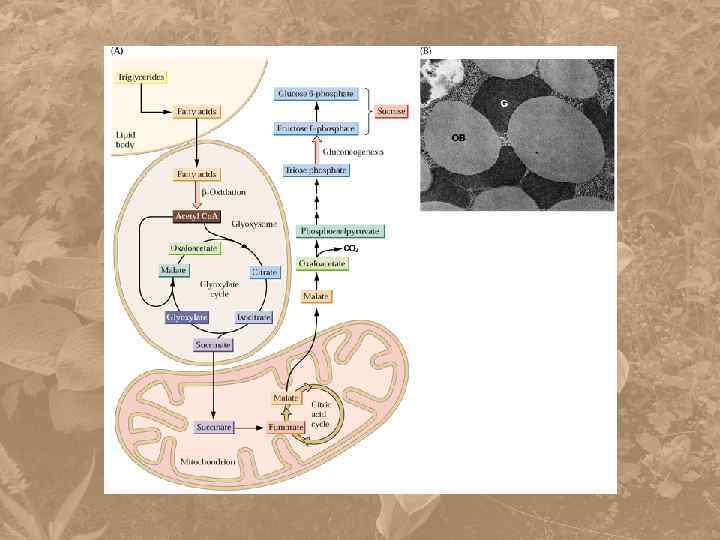
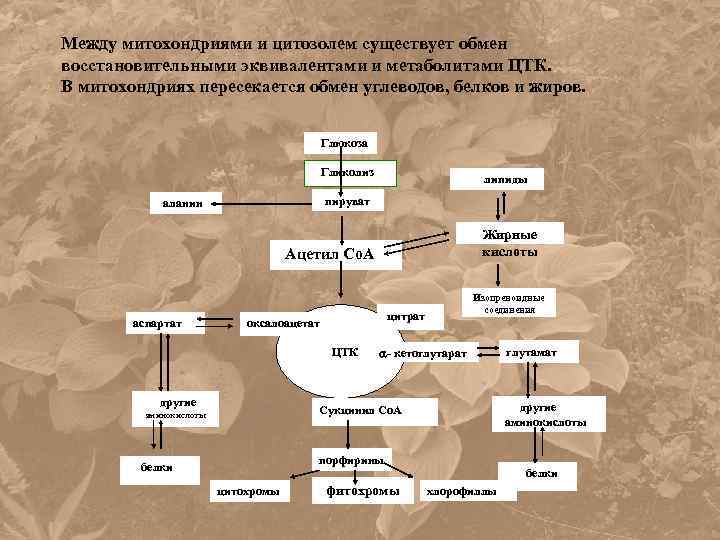
Между митохондриями и цитозолем существует обмен восстановительными эквивалентами и метаболитами ЦТК. В митохондриях пересекается обмен углеводов, белков и жиров. Глюкоза Гликолиз липиды пируват аланин Жирные кислоты Ацетил Со. А аспартат цитрат оксалоацетат ЦТК другие Изопреноидные соединения - кетоглутарат другие аминокислоты Сукцинил Со. А аминокислоты порфирины белки цитохромы фитохромы глутамат белки хлорофиллы
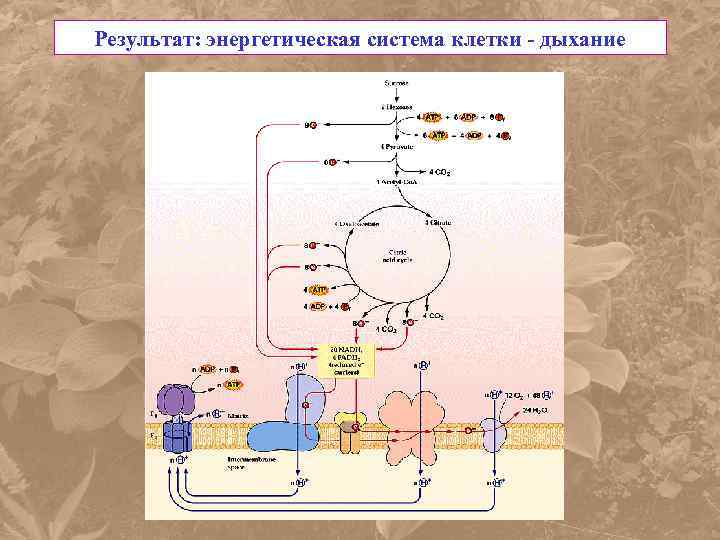
Результат: энергетическая система клетки - дыхание
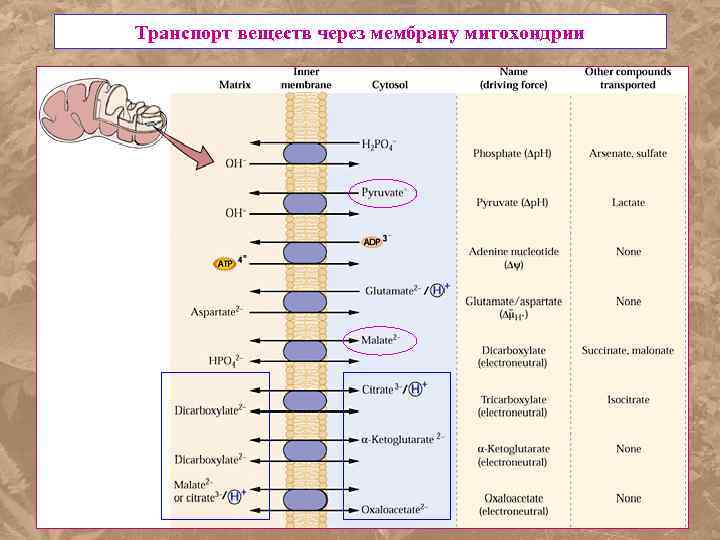
Транспорт веществ через мембрану митохондрии


Мх-ЭТЦ основные компоненты + 4 Н + 2 Н+ Межмембранное пространство 4 Н e- III I Q e- НАДН ротенон Цит с НАД Сукцинат IV e- О 2 АНТИМИЦИН А Н 2 О СО CN- матрикс

У растений работают дополнительно 4 НАД(Ф)Н-редуктазы 4 Н+ НАДН НАДФН I ДГex + ДГex e- НАДН ротенон n. Н+ e- Цит с III II ДГin 2 Н+ 4 Н Q IV e- ДГin НАДН НАДФНСукцинат АТФ синтаза О 2 АНТИМИЦИН А Н 2 О СО CN- АДФ АТФ ОЛИГОМИЦИН

Мх-ЭТЦ у растений 4 Н+ НАДН НАДФН I ДГex + ДГex e- Q ротенон IV e- АО ДГin НАДН НАДФНСукцинат Цит с III e- НАДН n. Н+ e- II ДГin 2 Н+ 4 Н АТФ синтаза О 2 Н 2 О SHAM О 2 АНТИМИЦИН А Н 2 О СО CN- АДФ АТФ ОЛИГОМИЦИН
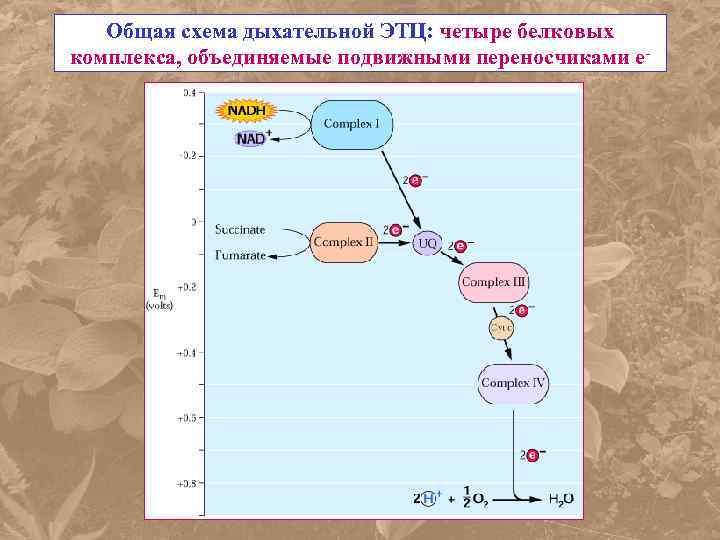
Общая схема дыхательной ЭТЦ: четыре белковых комплекса, объединяемые подвижными переносчиками е-
Комплекс I: НАДН-дегидрогеназа. Старый башмак…
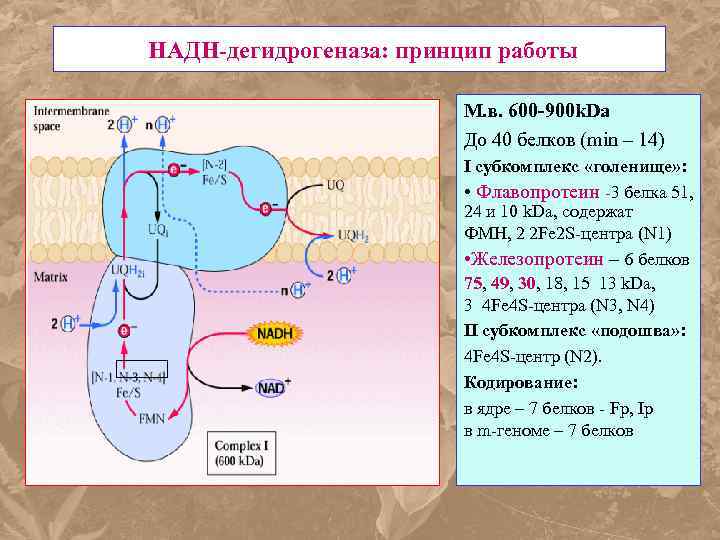
НАДН-дегидрогеназа: принцип работы М. в. 600 -900 k. Da До 40 белков (min – 14) I субкомплекс «голенище» : • Флавопротеин -3 белка 51, 24 и 10 k. Da, содержат ФМН, 2 2 Fe 2 S-центра (N 1) • Железопротеин – 6 белков 75, 49, 30, 18, 15 13 k. Da, 3 4 Fe 4 S-центра (N 3, N 4) II субкомплекс «подошва» : 4 Fe 4 S-центр (N 2). Кодирование: в ядре – 7 белков - Fp, Ip в m-геноме – 7 белков
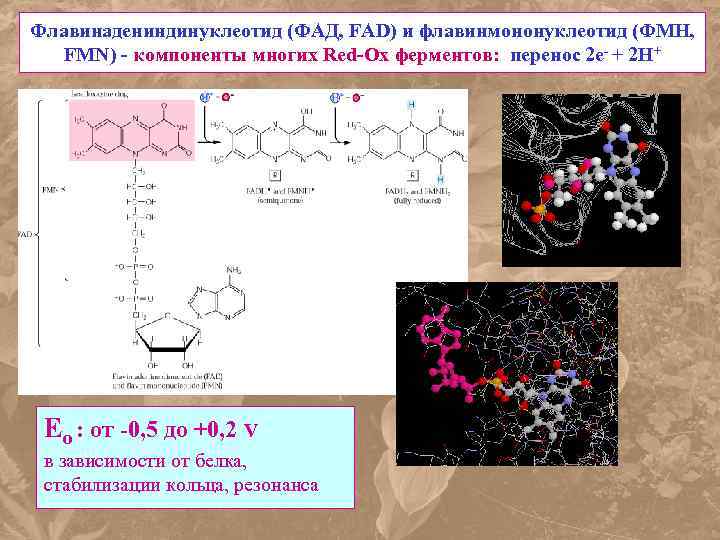
Флавинадениндинуклеотид (ФАД, FAD) и флавинмононуклеотид (ФМН, FMN) - компоненты многих Red-Ox ферментов: перенос 2 е- + 2 Н+ Eo : от -0, 5 до +0, 2 V в зависимости от белка, стабилизации кольца, резонанса
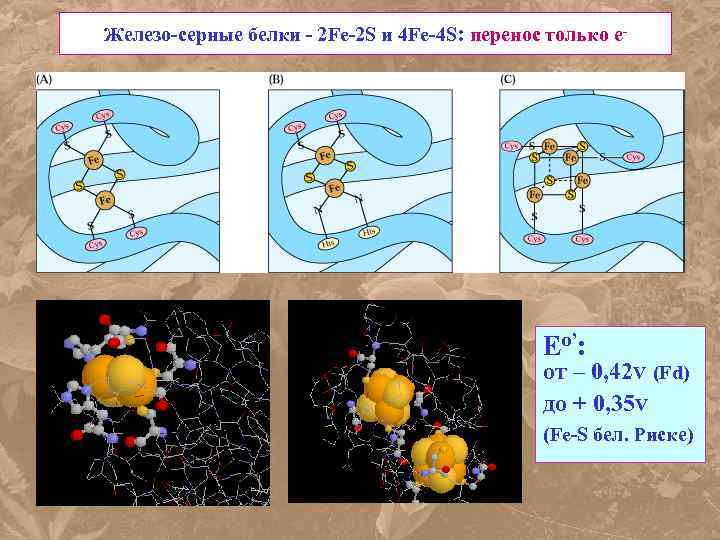
Железо-серные белки - 2 Fe-2 S и 4 Fe-4 S: перенос только е- Eо’: от – 0, 42 V (Fd) до + 0, 35 V (Fe-S бел. Риске)
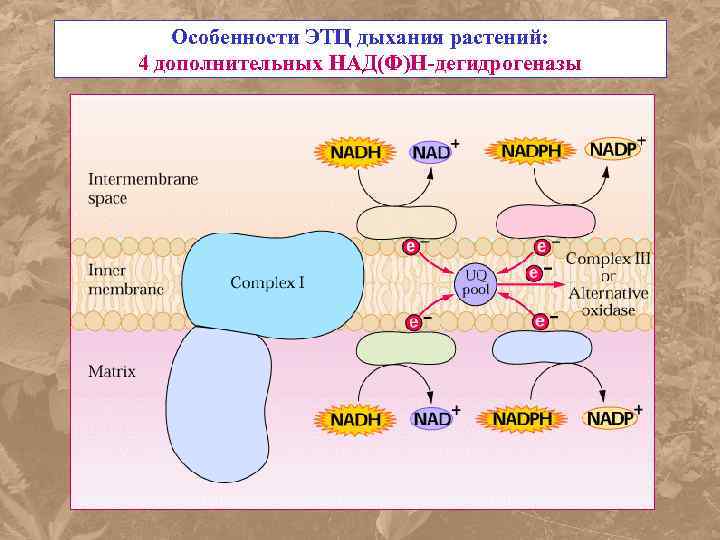
Особенности ЭТЦ дыхания растений: 4 дополнительных НАД(Ф)Н-дегидрогеназы
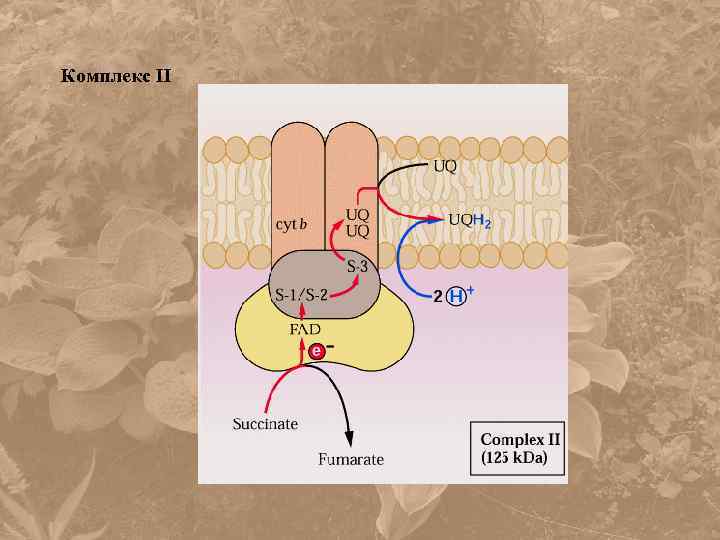
Комплекс II
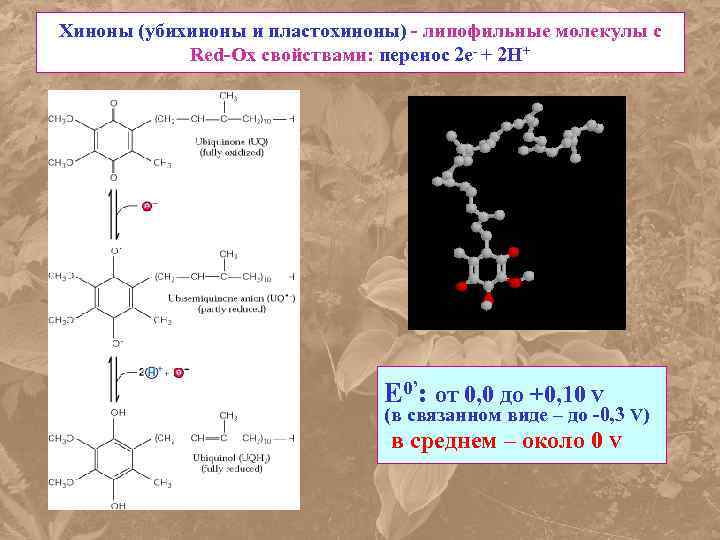
Хиноны (убихиноны и пластохиноны) - липофильные молекулы с Red-Ox свойствами: перенос 2 е- + 2 Н+ E 0’: от 0, 0 до +0, 10 V (в связанном виде – до -0, 3 V) в среднем – около 0 V
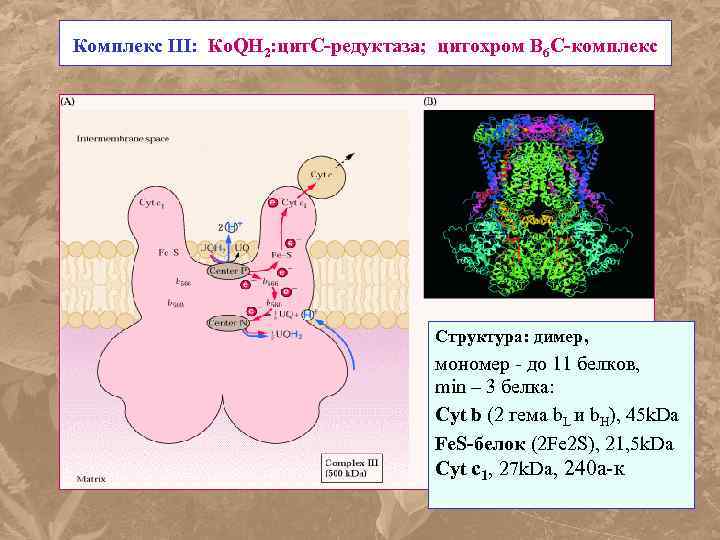
Комплекс III: Ко. QН 2: цит. С-редуктаза; цитохром В 6 С-комплекс Структура: димер, мономер - до 11 белков, min – 3 белка: Cyt b (2 гема b. L и b. H), 45 k. Da Fe. S-белок (2 Fe 2 S), 21, 5 k. Da Cyt c 1, 27 k. Da, 240 а-к
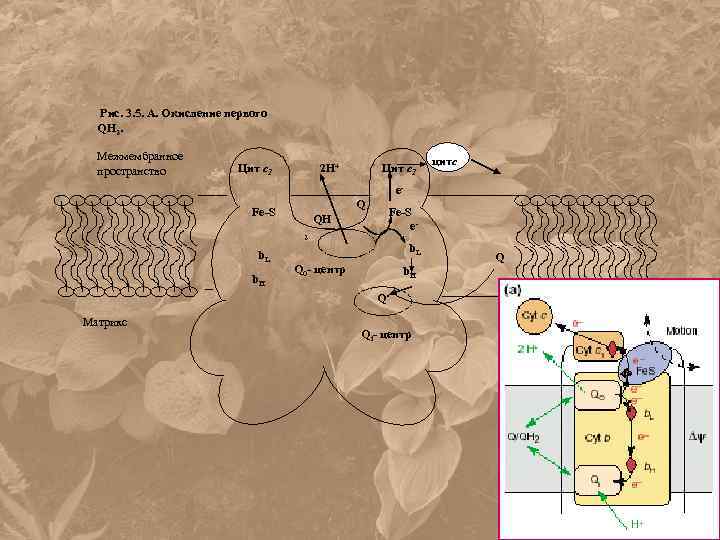
Рис. 3. 5. А. Окисление первого QH 2. Межмембранное пространство Цит с1 2 H+ Цит с1 цитс e. Q Fe-S QH Fe-S e- 2 b. L b. H b. L Q 0 - центр b. H Q. - Матрикс Qi- центр Q
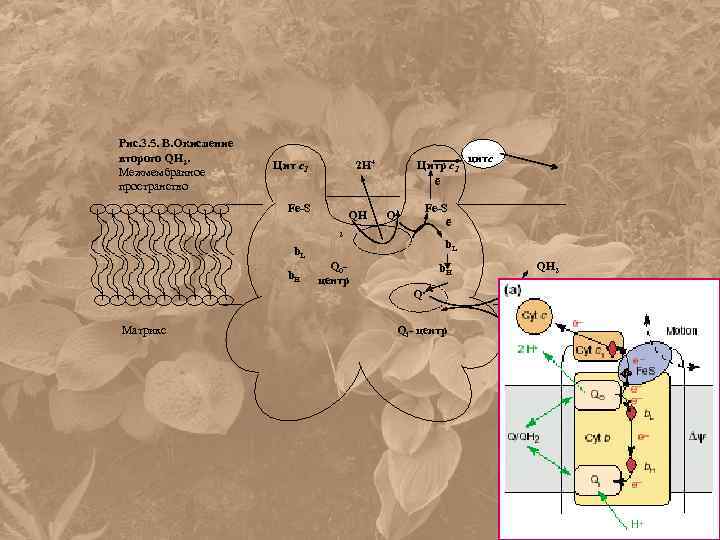
Рис. 3. 5. В. Окисление второго QH 2. Межмембранное пространство Цит с1 2 H+ Fe-S QH Цитр с1 ē Q Fe-S ē 2 b. L b. H Матрикс Q 0 центр цитс b. L b. H QH 2 Q. Qi- центр 2 Н+
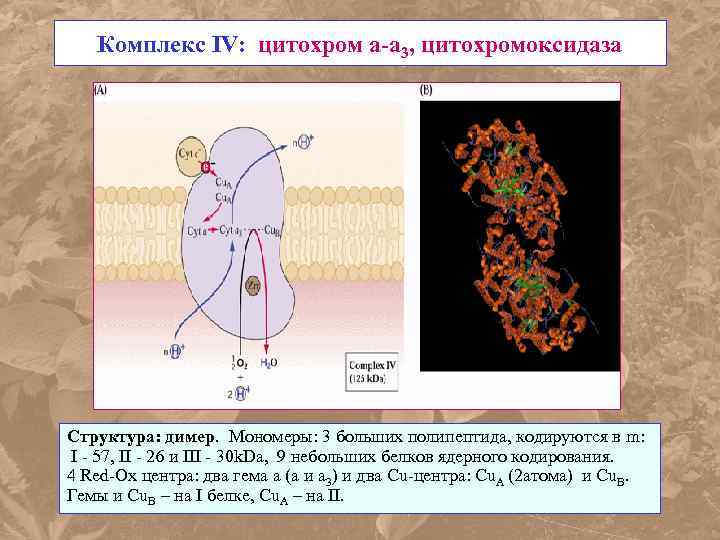
Комплекс IV: цитохром а-а 3, цитохромоксидаза Структура: димер. Мономеры: 3 больших полипептида, кодируются в m: I - 57, II - 26 и III - 30 k. Da, 9 небольших белков ядерного кодирования. 4 Red-Ox центра: два гема а (a и a 3) и два Cu-центра: Сu. А (2 атома) и Cu. В. Гемы и Cu. B – на I белке, Cu. A – на II.
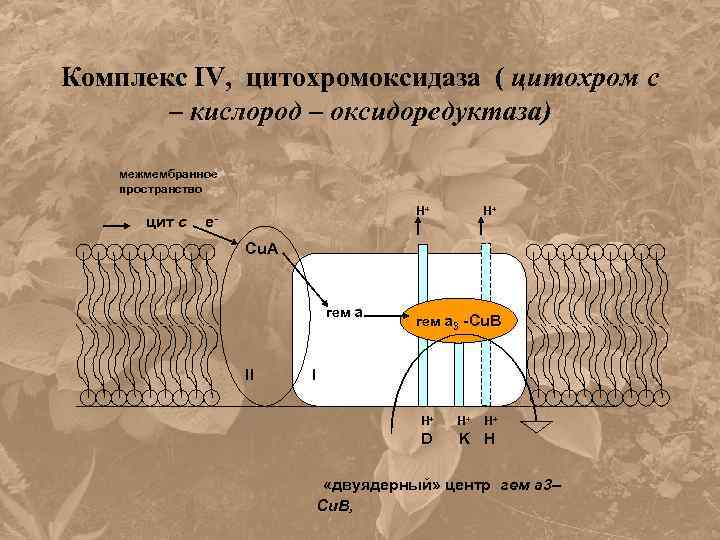
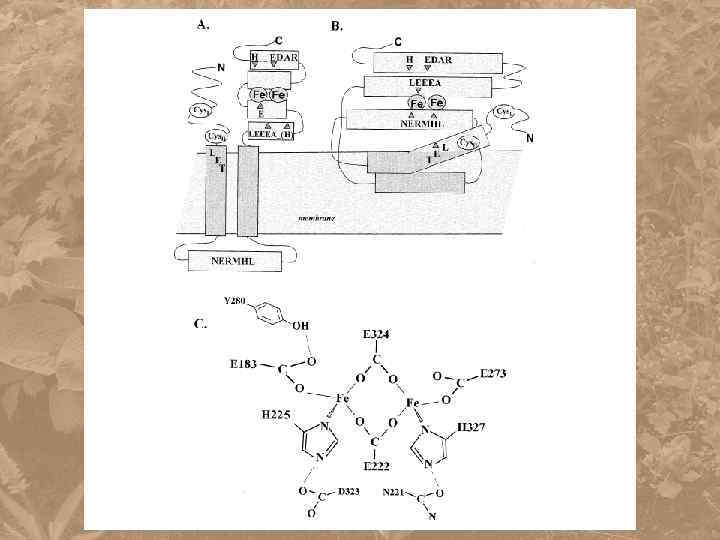
Комплекс IV, цитохромоксидаза ( цитохром с – кислород – оксидоредуктаза) межмембранное пространство цит с H+ e- H+ Cu. A гем а II гем а 3 -Сu. B I H+ H+ H+ D K H «двуядерный» центр гем а 3– Сu. В,
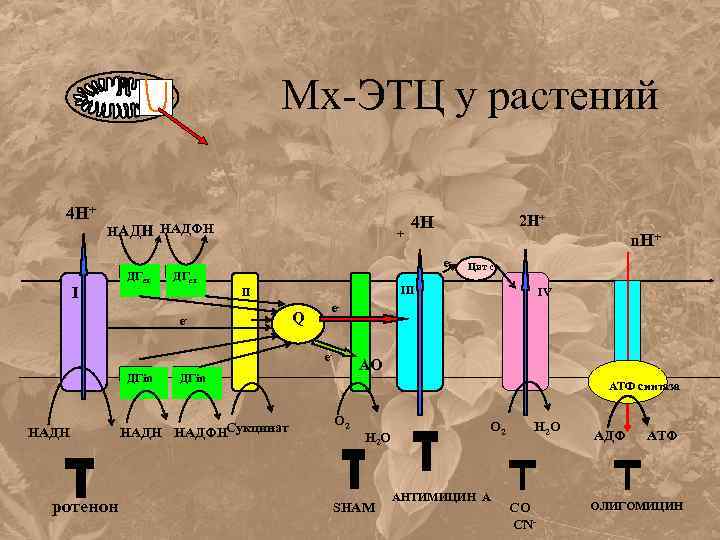
Мх-ЭТЦ у растений 4 Н+ НАДН НАДФН I ДГex + ДГex e- Q ротенон IV e- АО ДГin НАДН НАДФНСукцинат Цит с III e- НАДН n. Н+ e- II ДГin 2 Н+ 4 Н АТФ синтаза О 2 Н 2 О SHAM О 2 АНТИМИЦИН А Н 2 О СО CN- АДФ АТФ ОЛИГОМИЦИН

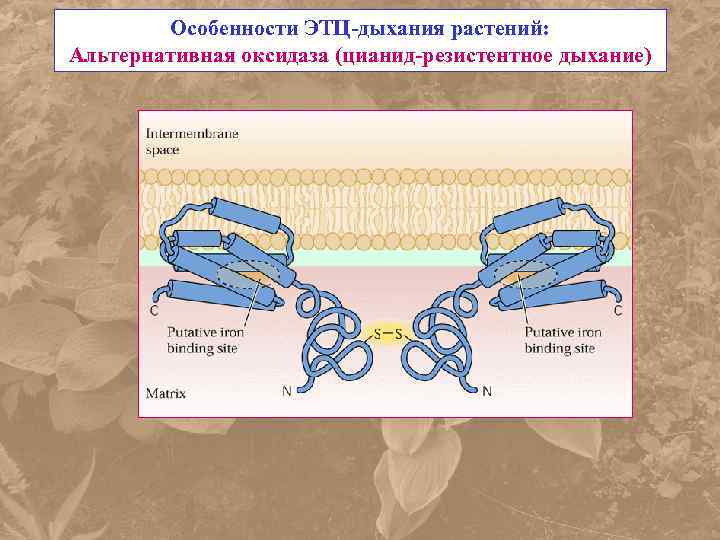
Особенности ЭТЦ-дыхания растений: Альтернативная оксидаза (цианид-резистентное дыхание)

AO относится к семейству di-iron белков R-2 типа Обнаружена у E. coli, Paracoccus denitrificans, простейших Trypanosoma, водорослей и всех семенных растений. Впервые белок АО был получен из мтх Sauromatum guttatum

Цианидрезистентное дыхание Термогенез ароидных растений Arum maculatum, Symplocarpus foetidis, Sauromatum guttatum, Philodendron selloum. Альтернативная оксидаза один полипептид ( М. В. ~ 32 к. Да) один ядерный ген АОХ 1 В мембране Мх: мономерная или димерная форма Впервые белок АО был получен из мтх Sauromatum guttatum 2 QH 2 +O 2 → 2 Q + 2 H 2 O

• Термогенез в цветках некоторых растений связан с терморегуляцией: • При понижении температуры воздуха температура тканей цветка остается постоянной , а скорость поглощения кислорода возрастает. При повышении температуры воздуха скорость дыхания падает

• t воздуха t цветка • Symplocarpus foetidis +3 -+240 +16 -+ 260 • Philodendron selloum +4 -+390 +39 -+ 440 • Существуют точки, (switchig temperature) за пределами которых «терморегуляция» не действует

Sauromatum guttatum

Symplocarpus foetidus

Helicodeceros muscivorus
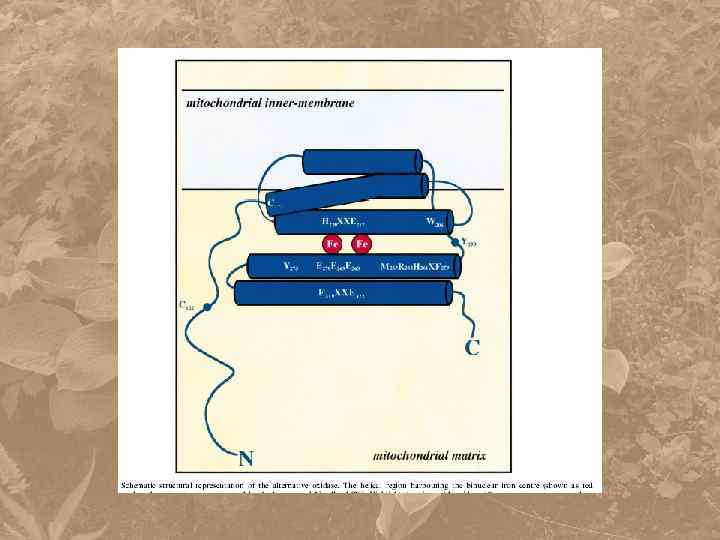
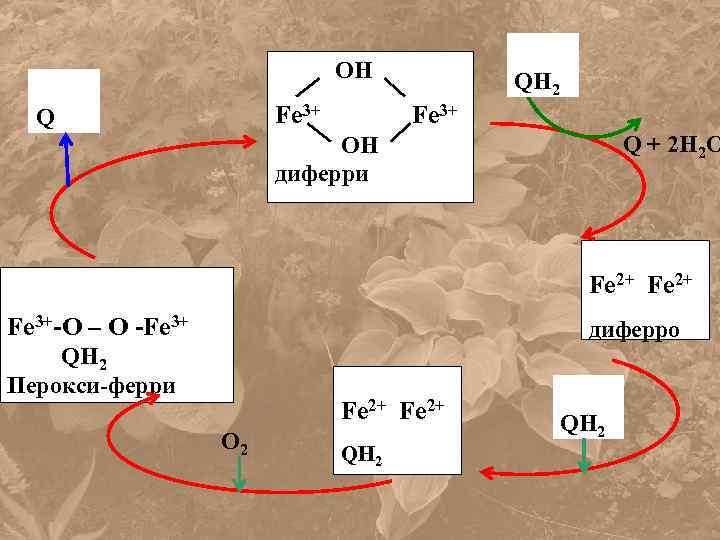
OH Fe 3+ Q QH 2 Fe 3+ Q + 2 H 2 O OH диферри Fe 2+ Fe 3+-O – O -Fe 3+ диферро QH 2 Перокси-ферри Fe 2+ O 2 QH 2
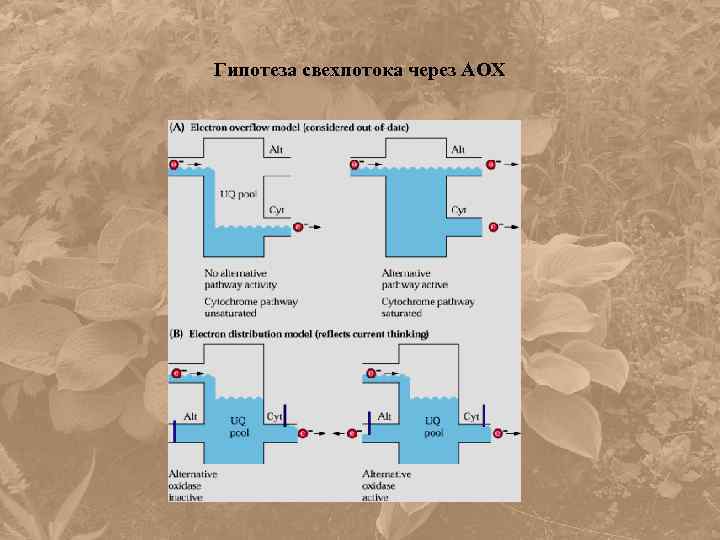
Гипотеза свехпотока через АОХ
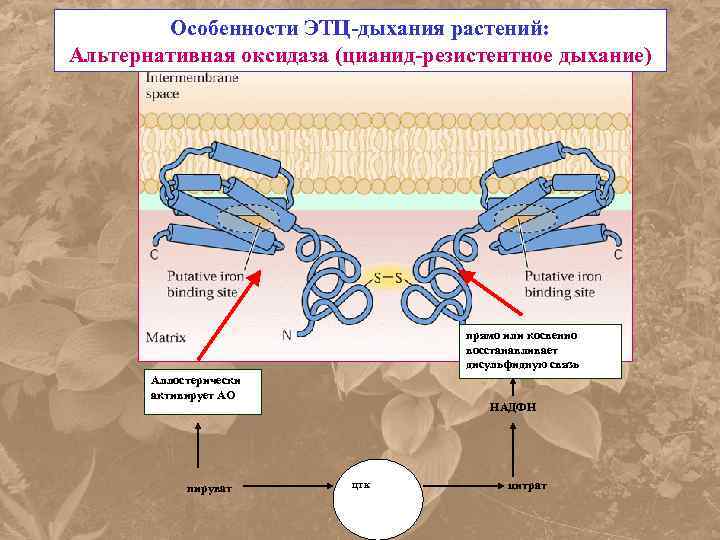
Особенности ЭТЦ-дыхания растений: Альтернативная оксидаза (цианид-резистентное дыхание) прямо или косвенно восстанавливает дисульфидную связь Аллостерически активирует АО пируват НАДФН ЦТК цитрат
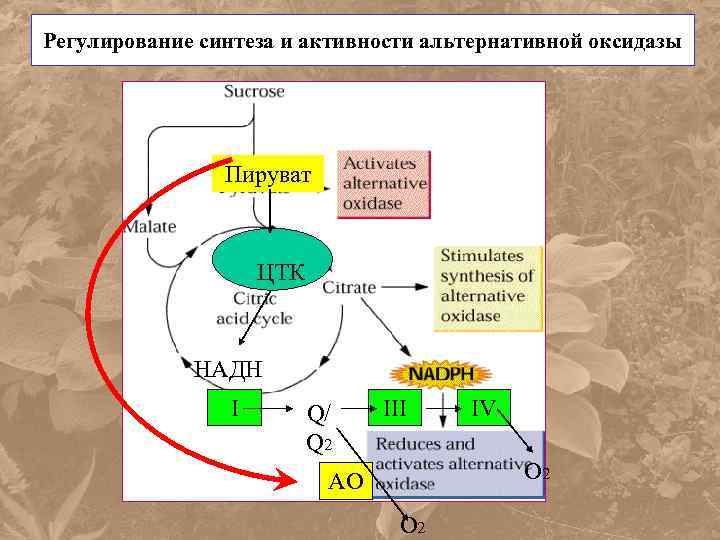
Регулирование синтеза и активности альтернативной оксидазы Пируват ЦТК НАДН I Q/ Q 2 III IV O 2 AO O 2

Регуляция активности АО • Электронные потоки в дыхательной цепи распределяются по цитохромному и альтернативному пути согласно активности двух терминальных оксидаз, которые конкурируют за электроны.
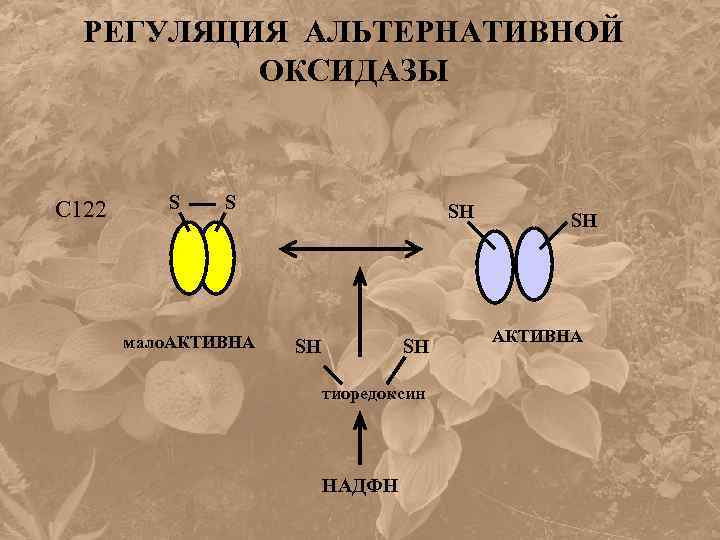
РЕГУЛЯЦИЯ АЛЬТЕРНАТИВНОЙ ОКСИДАЗЫ С 122 S S мало. АКТИВНА SH SH SH тиоредоксин НАДФН SH АКТИВНА
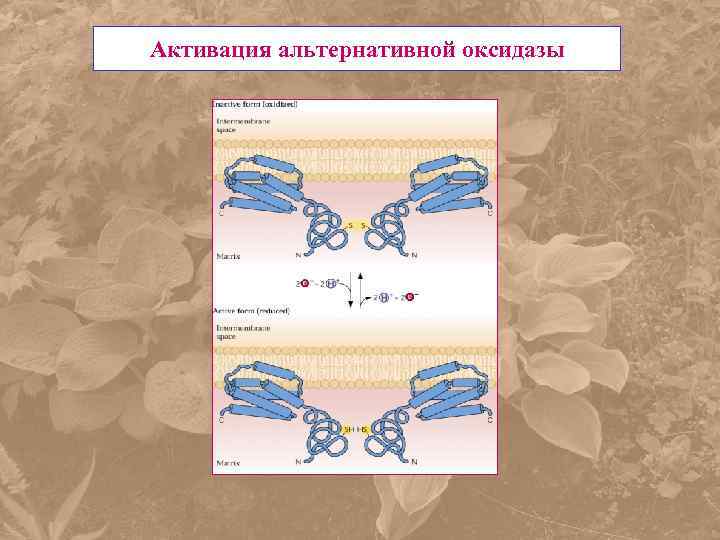
Активация альтернативной оксидазы

• В восстановленном состоянии АО аллостерически активируется пируватом и другими кетокислотами.
05Дыхание 2012 Bio.ppt