2 Алкены.pptx
- Количество слайдов: 33
 1 НЕНАСЫЩЕННЫЕ, НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ 1
1 НЕНАСЫЩЕННЫЕ, НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ 1
 АЛКЕНЫ Это соединения, в углеродном скелете которых есть кратные двойные связи. Алкены имеют свой гомологический ряд, начальный представитель которого этилен – СН 2 = СН 2. Общая формула алкенов Сn. H 2 n. Атом углерода, который имеет двойную связь, находится в sp 2 -гибридном состоянии. В этом состоянии происходит взаимодействие одной s- и двух р-орбиталей с равноценной энергией с образованием трех эквивалентных гибридных орбиталей. 2
АЛКЕНЫ Это соединения, в углеродном скелете которых есть кратные двойные связи. Алкены имеют свой гомологический ряд, начальный представитель которого этилен – СН 2 = СН 2. Общая формула алкенов Сn. H 2 n. Атом углерода, который имеет двойную связь, находится в sp 2 -гибридном состоянии. В этом состоянии происходит взаимодействие одной s- и двух р-орбиталей с равноценной энергией с образованием трех эквивалентных гибридных орбиталей. 2
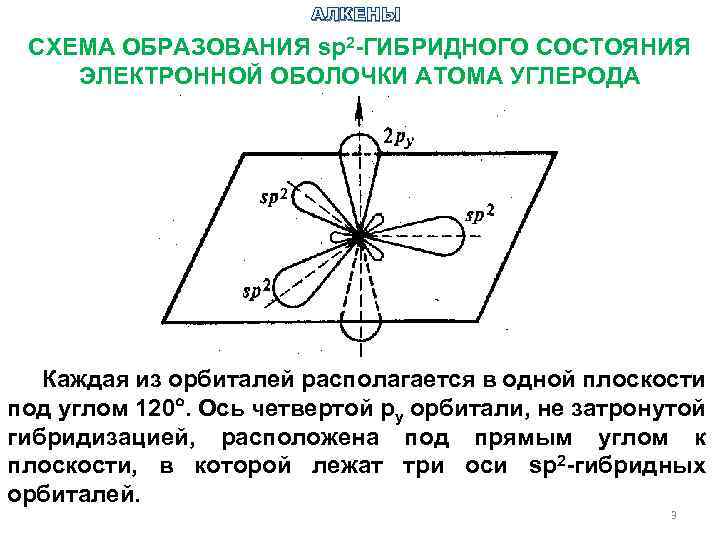 АЛКЕНЫ СХЕМА ОБРАЗОВАНИЯ sp 2 -ГИБРИДНОГО СОСТОЯНИЯ ЭЛЕКТРОННОЙ ОБОЛОЧКИ АТОМА УГЛЕРОДА Каждая из орбиталей располагается в одной плоскости под углом 120. Ось четвертой ру орбитали, не затронутой гибридизацией, расположена под прямым углом к плоскости, в которой лежат три оси sp 2 -гибридных орбиталей. 3
АЛКЕНЫ СХЕМА ОБРАЗОВАНИЯ sp 2 -ГИБРИДНОГО СОСТОЯНИЯ ЭЛЕКТРОННОЙ ОБОЛОЧКИ АТОМА УГЛЕРОДА Каждая из орбиталей располагается в одной плоскости под углом 120. Ось четвертой ру орбитали, не затронутой гибридизацией, расположена под прямым углом к плоскости, в которой лежат три оси sp 2 -гибридных орбиталей. 3
 АЛКЕНЫ Образовавшиеся гибридные орбитали, перекрываясь с орбиталями других атомов, образуют простые σ-связи. Неизменившиеся ру орбитали двух атомов углерода, образующих σ-связи, также могут перекрываться над и под плоскостью, в которой лежат sp 2 -гибридные орбитали, образуя сложную π-связь. 4
АЛКЕНЫ Образовавшиеся гибридные орбитали, перекрываясь с орбиталями других атомов, образуют простые σ-связи. Неизменившиеся ру орбитали двух атомов углерода, образующих σ-связи, также могут перекрываться над и под плоскостью, в которой лежат sp 2 -гибридные орбитали, образуя сложную π-связь. 4
 АЛКЕНЫ Кратная связь между двумя атомами состоит из двух частей: простой σ-связи и сложной π-связи за счет двукратного перекрывания py орбиталями. Условием для образования π-связи является параллельность р орбиталей соединяющихся атомов и их перпендикулярность к плоскости молекулы. Молекулы, имеющие кратную связь по месту этой связи образуют плоскость симметрии. Поэтому вокруг кратной связи не может происходить свободного вращения частей молекулы, т. е. это жесткая связь. Например, молекула этилена имеет две области высокой электронной плотности по одной с каждой стороны плоскости, образованной двумя связями. Она антисимметрична относительно оси, соединяющей оба ядра, и симметрична относительно зеркальной плоскости между ними. 5
АЛКЕНЫ Кратная связь между двумя атомами состоит из двух частей: простой σ-связи и сложной π-связи за счет двукратного перекрывания py орбиталями. Условием для образования π-связи является параллельность р орбиталей соединяющихся атомов и их перпендикулярность к плоскости молекулы. Молекулы, имеющие кратную связь по месту этой связи образуют плоскость симметрии. Поэтому вокруг кратной связи не может происходить свободного вращения частей молекулы, т. е. это жесткая связь. Например, молекула этилена имеет две области высокой электронной плотности по одной с каждой стороны плоскости, образованной двумя связями. Она антисимметрична относительно оси, соединяющей оба ядра, и симметрична относительно зеркальной плоскости между ними. 5
 АЛКЕНЫ СХЕМА МОЛЕКУЛЫ ЭТИЛЕНА ИЗОМЕРИЯ И НОМЕНКЛАТУРА АЛКЕНОВ У алкенов существует три вида изомерии: 1) структурная – связана со структурой углеродного скелета, начинается с бутена С 4 Н 8. 2) позиционная – связана с расположением кратной связи в углеродном скелете 3) цис-транс-изомерия (пространственная, 6 геометрическая).
АЛКЕНЫ СХЕМА МОЛЕКУЛЫ ЭТИЛЕНА ИЗОМЕРИЯ И НОМЕНКЛАТУРА АЛКЕНОВ У алкенов существует три вида изомерии: 1) структурная – связана со структурой углеродного скелета, начинается с бутена С 4 Н 8. 2) позиционная – связана с расположением кратной связи в углеродном скелете 3) цис-транс-изомерия (пространственная, 6 геометрическая).
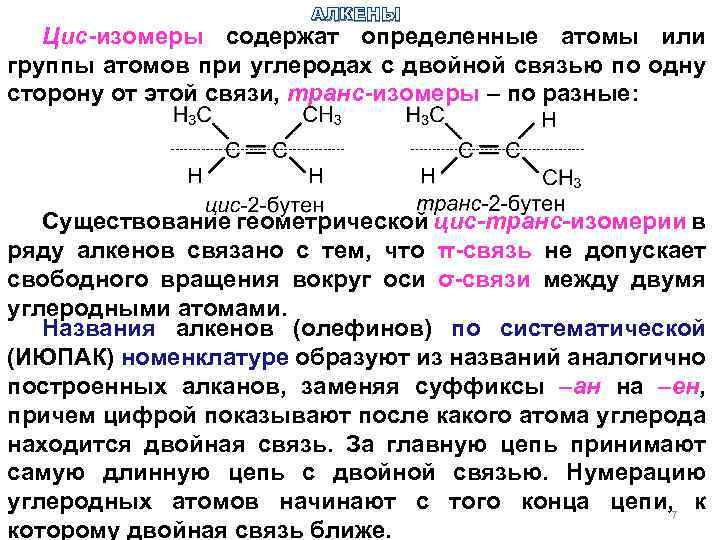 АЛКЕНЫ Цис-изомеры содержат определенные атомы или группы атомов при углеродах с двойной связью по одну сторону от этой связи, транс-изомеры – по разные: Существование геометрической цис-транс-изомерии в ряду алкенов связано с тем, что π-связь не допускает свободного вращения вокруг оси σ-связи между двумя углеродными атомами. Названия алкенов (олефинов) по систематической (ИЮПАК) номенклатуре образуют из названий аналогично построенных алканов, заменяя суффиксы –ан на –ен, причем цифрой показывают после какого атома углерода находится двойная связь. За главную цепь принимают самую длинную цепь с двойной связью. Нумерацию углеродных атомов начинают с того конца цепи, к 7 которому двойная связь ближе.
АЛКЕНЫ Цис-изомеры содержат определенные атомы или группы атомов при углеродах с двойной связью по одну сторону от этой связи, транс-изомеры – по разные: Существование геометрической цис-транс-изомерии в ряду алкенов связано с тем, что π-связь не допускает свободного вращения вокруг оси σ-связи между двумя углеродными атомами. Названия алкенов (олефинов) по систематической (ИЮПАК) номенклатуре образуют из названий аналогично построенных алканов, заменяя суффиксы –ан на –ен, причем цифрой показывают после какого атома углерода находится двойная связь. За главную цепь принимают самую длинную цепь с двойной связью. Нумерацию углеродных атомов начинают с того конца цепи, к 7 которому двойная связь ближе.
 АЛКЕНЫ По рациональной номенклатуре алкены называют как алкилзамещенные родоначальника ряда – этилена. Непредельные углеводородные радикалы называют, добавляя к корню суффикс –енил: 8
АЛКЕНЫ По рациональной номенклатуре алкены называют как алкилзамещенные родоначальника ряда – этилена. Непредельные углеводородные радикалы называют, добавляя к корню суффикс –енил: 8
 АЛКЕНЫ Эмпирические названия радикалов: СПОСОБЫ ПОЛУЧЕНИЯ АЛКЕНОВ 1) первые четыре члена ряда алкенов получают разгонкой под давлением или при низкой температуре газообразной части продуктов крекинга нефтяных дистиллятов 2) дегидрогенизация алканов 9
АЛКЕНЫ Эмпирические названия радикалов: СПОСОБЫ ПОЛУЧЕНИЯ АЛКЕНОВ 1) первые четыре члена ряда алкенов получают разгонкой под давлением или при низкой температуре газообразной части продуктов крекинга нефтяных дистиллятов 2) дегидрогенизация алканов 9
 АЛКЕНЫ 3) дегидратация спиртов (отщепление воды) В качестве катализаторов дегидратации используют: – серную или фосфорную кислоты, – кислые соли (KHSO 4), – оксиды фосфора (P 2 O 5), алюминия (Al 2 O 3). Условия дегидратации зависят от природы спирта. Порядок отщепления воды определяется правилом Зайцева: при образовании воды наиболее отщепляется водород от наименее гидрогенезированного атома углерода. 10
АЛКЕНЫ 3) дегидратация спиртов (отщепление воды) В качестве катализаторов дегидратации используют: – серную или фосфорную кислоты, – кислые соли (KHSO 4), – оксиды фосфора (P 2 O 5), алюминия (Al 2 O 3). Условия дегидратации зависят от природы спирта. Порядок отщепления воды определяется правилом Зайцева: при образовании воды наиболее отщепляется водород от наименее гидрогенезированного атома углерода. 10
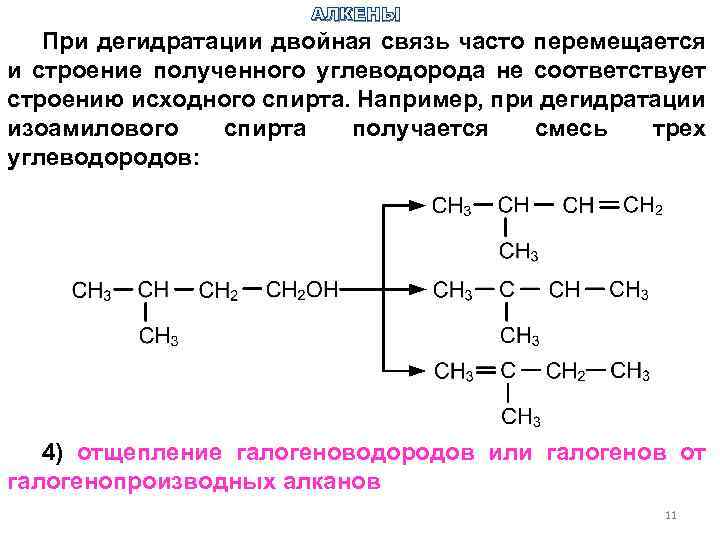 АЛКЕНЫ При дегидратации двойная связь часто перемещается и строение полученного углеводорода не соответствует строению исходного спирта. Например, при дегидратации изоамилового спирта получается смесь трех углеводородов: 4) отщепление галогеноводородов или галогенов от галогенопроизводных алканов 11
АЛКЕНЫ При дегидратации двойная связь часто перемещается и строение полученного углеводорода не соответствует строению исходного спирта. Например, при дегидратации изоамилового спирта получается смесь трех углеводородов: 4) отщепление галогеноводородов или галогенов от галогенопроизводных алканов 11
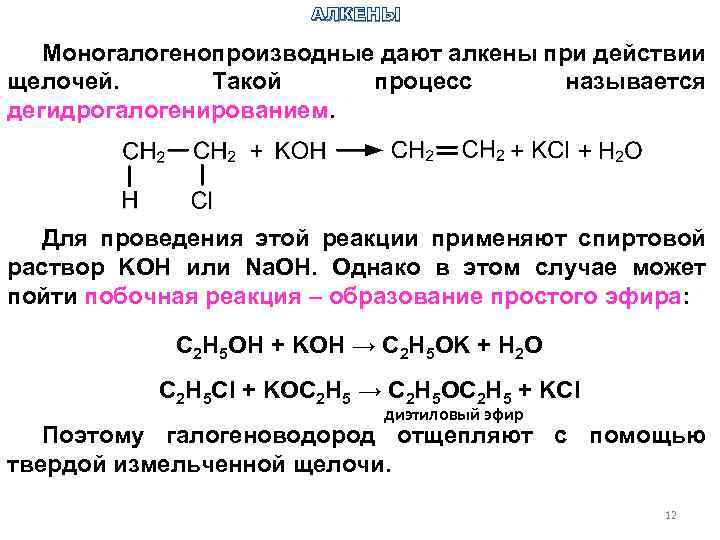 АЛКЕНЫ Моногалогенопроизводные дают алкены при действии щелочей. Такой процесс называется дегидрогалогенированием. Для проведения этой реакции применяют спиртовой раствор KОН или Na. OH. Однако в этом случае может пойти побочная реакция – образование простого эфира: C 2 H 5 OH + KOH → C 2 H 5 OK + H 2 O C 2 H 5 Cl + KOC 2 H 5 → C 2 H 5 OC 2 H 5 + KCl диэтиловый эфир Поэтому галогеноводород отщепляют с помощью твердой измельченной щелочи. 12
АЛКЕНЫ Моногалогенопроизводные дают алкены при действии щелочей. Такой процесс называется дегидрогалогенированием. Для проведения этой реакции применяют спиртовой раствор KОН или Na. OH. Однако в этом случае может пойти побочная реакция – образование простого эфира: C 2 H 5 OH + KOH → C 2 H 5 OK + H 2 O C 2 H 5 Cl + KOC 2 H 5 → C 2 H 5 OC 2 H 5 + KCl диэтиловый эфир Поэтому галогеноводород отщепляют с помощью твердой измельченной щелочи. 12
 АЛКЕНЫ Дегидрогалогенирование Зайцева: протекает по правилу 5) из дигалогенидов Для этого используют метод отщепления галогенов от дигалогенпроизводных с атомами галогенов у соседних углеродных атомов. Для отщепления применяют цинковую пыль или стружку в водно-спиртовой среде: ФИЗИЧЕСКИЕ СВОЙСТВА АЛКЕНОВ По физическим свойствам алкены мало отличаются от алканов. Первые три члена ряда этиленовых (С 1 – С 4) – газы. Алкены с числом углеродных атомов от 5 до 17 (С 5 – С 17) 13 – жидкости, остальные – твердые тела.
АЛКЕНЫ Дегидрогалогенирование Зайцева: протекает по правилу 5) из дигалогенидов Для этого используют метод отщепления галогенов от дигалогенпроизводных с атомами галогенов у соседних углеродных атомов. Для отщепления применяют цинковую пыль или стружку в водно-спиртовой среде: ФИЗИЧЕСКИЕ СВОЙСТВА АЛКЕНОВ По физическим свойствам алкены мало отличаются от алканов. Первые три члена ряда этиленовых (С 1 – С 4) – газы. Алкены с числом углеродных атомов от 5 до 17 (С 5 – С 17) 13 – жидкости, остальные – твердые тела.
 АЛКЕНЫ Алкены с нормальной цепью углеродных атомов кипят при более высокой температуре, чем их изомеры с разветвленной цепью. Перемещение двойной связи в центр молекулы вызывает повышение температуры кипения алкена. Цис-изомеры кипят при более высокой температуре, чем транс-изомеры. Алкены плохо растворяются в воде, но хорошо растворяются в органических ратворителях и растворах солей тяжелых металлов, например Cu 2 Cl 2, образуя с ними комплексные соединения. ХИМИЧЕСКИЕ СВОЙСТВА АЛКЕНОВ В молекулах алкенов сильное влияние на их реакционную способность оказывают электронные эффекты. 14
АЛКЕНЫ Алкены с нормальной цепью углеродных атомов кипят при более высокой температуре, чем их изомеры с разветвленной цепью. Перемещение двойной связи в центр молекулы вызывает повышение температуры кипения алкена. Цис-изомеры кипят при более высокой температуре, чем транс-изомеры. Алкены плохо растворяются в воде, но хорошо растворяются в органических ратворителях и растворах солей тяжелых металлов, например Cu 2 Cl 2, образуя с ними комплексные соединения. ХИМИЧЕСКИЕ СВОЙСТВА АЛКЕНОВ В молекулах алкенов сильное влияние на их реакционную способность оказывают электронные эффекты. 14
 АЛКЕНЫ Если в молекуле имеются только ковалентные связи и нет смещений электрических зарядов, то такая молекула малоактивна. Более химически активна молекула, в которой наблюдается смещение электрического заряда, т. е. появляются атомы с большей или меньшей плотностью электронного облака. Реагенты, которые отдают свою электронную пару для образования связи с атомными ядрами других молекул, называются нуклеофильными или электронодонорными. Реагенты, действие которых связано с приобретением электронов, т. е. с частичным приобретением электронной пары, которая ранее принадлежала полностью другой молекуле, называют электрофильными или электроноакцепторными. 15
АЛКЕНЫ Если в молекуле имеются только ковалентные связи и нет смещений электрических зарядов, то такая молекула малоактивна. Более химически активна молекула, в которой наблюдается смещение электрического заряда, т. е. появляются атомы с большей или меньшей плотностью электронного облака. Реагенты, которые отдают свою электронную пару для образования связи с атомными ядрами других молекул, называются нуклеофильными или электронодонорными. Реагенты, действие которых связано с приобретением электронов, т. е. с частичным приобретением электронной пары, которая ранее принадлежала полностью другой молекуле, называют электрофильными или электроноакцепторными. 15
 АЛКЕНЫ На неравномерное распределение электронной плотности молекулы могут влиять следующие факторы: 1) индуктивный эффект – обычно влияет на молекулы с простыми связями (σ-σ взаимодействие). Если к углеродному скелету присоединить атом или группу с электроотрицательностью (ЭО), отличной от атома углерода С (ЭО=2, 5), то в этой связи наблюдается смещение электронной плотности в сторону более электроотрицательного атома, например: Если электронная плотность оттягивается от атома С, такой эффект называется отрицательным индуктивным эффектом (– Iэф). 16
АЛКЕНЫ На неравномерное распределение электронной плотности молекулы могут влиять следующие факторы: 1) индуктивный эффект – обычно влияет на молекулы с простыми связями (σ-σ взаимодействие). Если к углеродному скелету присоединить атом или группу с электроотрицательностью (ЭО), отличной от атома углерода С (ЭО=2, 5), то в этой связи наблюдается смещение электронной плотности в сторону более электроотрицательного атома, например: Если электронная плотность оттягивается от атома С, такой эффект называется отрицательным индуктивным эффектом (– Iэф). 16
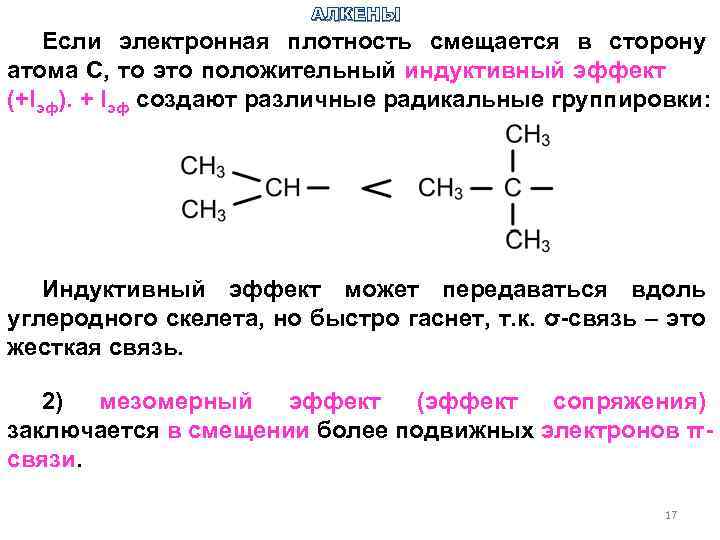 АЛКЕНЫ Если электронная плотность смещается в сторону атома С, то это положительный индуктивный эффект (+Iэф). + Iэф создают различные радикальные группировки: Индуктивный эффект может передаваться вдоль углеродного скелета, но быстро гаснет, т. к. σ-связь – это жесткая связь. 2) мезомерный эффект (эффект сопряжения) заключается в смещении более подвижных электронов πсвязи. 17
АЛКЕНЫ Если электронная плотность смещается в сторону атома С, то это положительный индуктивный эффект (+Iэф). + Iэф создают различные радикальные группировки: Индуктивный эффект может передаваться вдоль углеродного скелета, но быстро гаснет, т. к. σ-связь – это жесткая связь. 2) мезомерный эффект (эффект сопряжения) заключается в смещении более подвижных электронов πсвязи. 17
 АЛКЕНЫ Эти электроны находятся как бы во внешнем положении и легко могут смещаться в сторону, особенно легко в сопряженных связях. Сопряженные связи – такая система связей, в которой кратные связи разделены простыми связями: π-электроны легко смещаются, а заряды концентрируются на концах сопряженных связей. При этом электронная плотность кратных связей несколько уменьшается и они становятся длиннее, а электронная плотность простых связей несколько увеличивается (С – С 0, 154 нм, С = С 0, 134 нм). 18
АЛКЕНЫ Эти электроны находятся как бы во внешнем положении и легко могут смещаться в сторону, особенно легко в сопряженных связях. Сопряженные связи – такая система связей, в которой кратные связи разделены простыми связями: π-электроны легко смещаются, а заряды концентрируются на концах сопряженных связей. При этом электронная плотность кратных связей несколько уменьшается и они становятся длиннее, а электронная плотность простых связей несколько увеличивается (С – С 0, 154 нм, С = С 0, 134 нм). 18
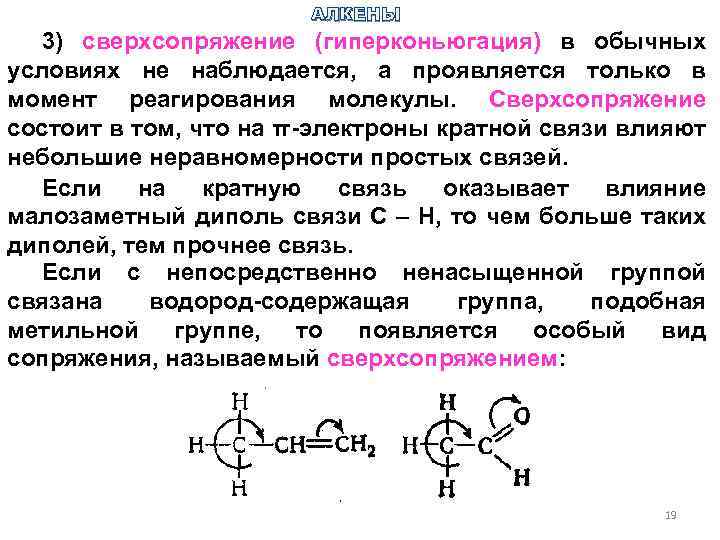 АЛКЕНЫ 3) сверхсопряжение (гиперконьюгация) в обычных условиях не наблюдается, а проявляется только в момент реагирования молекулы. Сверхсопряжение состоит в том, что на π-электроны кратной связи влияют небольшие неравномерности простых связей. Если на кратную связь оказывает влияние малозаметный диполь связи С – Н, то чем больше таких диполей, тем прочнее связь. Если с непосредственно ненасыщенной группой связана водород-содержащая группа, подобная метильной группе, то появляется особый вид сопряжения, называемый сверхсопряжением: 19
АЛКЕНЫ 3) сверхсопряжение (гиперконьюгация) в обычных условиях не наблюдается, а проявляется только в момент реагирования молекулы. Сверхсопряжение состоит в том, что на π-электроны кратной связи влияют небольшие неравномерности простых связей. Если на кратную связь оказывает влияние малозаметный диполь связи С – Н, то чем больше таких диполей, тем прочнее связь. Если с непосредственно ненасыщенной группой связана водород-содержащая группа, подобная метильной группе, то появляется особый вид сопряжения, называемый сверхсопряжением: 19
 АЛКЕНЫ Сверхсопряжение (гиперконьюгация) проявляется в том, что атомы водорода радикала, связанного с ненасыщенной группой, являются активированными (протонизированными): электронная плотность связей С – Н метильной группы смещается в сторону двойной связи. Сверхсопряжение описывается как частичное, слабое перекрывание орбиталей С – Н связей (σ-связей) с πорбиталями кратной связи: 20
АЛКЕНЫ Сверхсопряжение (гиперконьюгация) проявляется в том, что атомы водорода радикала, связанного с ненасыщенной группой, являются активированными (протонизированными): электронная плотность связей С – Н метильной группы смещается в сторону двойной связи. Сверхсопряжение описывается как частичное, слабое перекрывание орбиталей С – Н связей (σ-связей) с πорбиталями кратной связи: 20
 АЛКЕНЫ Хотя для алкенов возможны реакции замещения, протекающие по радикальному механизму, основной тип реакций алкенов – реакции присоединения по месту кратной связи. При этом происходит разрыв π-связей, а σ -связи остаются без изменения. РЕАКЦИИ АЛКЕНОВ 1. Гидрогенизация – присоединение водорода по месту кратной связи в присутствии катализатора – Pd, Pt, Ni: Поскольку для гидрирования необходима адсорбция молекулы алкена на катализаторе по двойной связи, алкены гидрируются тем легче, чем меньше заместителей имеется у двойной связи – правило Лебедева. 21
АЛКЕНЫ Хотя для алкенов возможны реакции замещения, протекающие по радикальному механизму, основной тип реакций алкенов – реакции присоединения по месту кратной связи. При этом происходит разрыв π-связей, а σ -связи остаются без изменения. РЕАКЦИИ АЛКЕНОВ 1. Гидрогенизация – присоединение водорода по месту кратной связи в присутствии катализатора – Pd, Pt, Ni: Поскольку для гидрирования необходима адсорбция молекулы алкена на катализаторе по двойной связи, алкены гидрируются тем легче, чем меньше заместителей имеется у двойной связи – правило Лебедева. 21
 АЛКЕНЫ 2. Алкилирование – процесс, протекающий с удлинением углеродной цепи, т. е присоединение алкильной группы. К таким процессам относится алкилирование алкенов парафинами в присутствии H 3 PO 4 или H 2 SO 4: Этим путем можно получать алканы с изостроением, например изооктан, которые используют как высокооктановое моторное топливо. 3. Галогенирование Галогены легко присоединяются по месту двойной связи. Например, если барботировать алкены через бромную воду, она обесцвечивается за счет присоединения атомов Br по месту кратной связи. Это качественная и количественная реакция на алкены. По количеству поглощенного брома можно установить 22 содержание алкена.
АЛКЕНЫ 2. Алкилирование – процесс, протекающий с удлинением углеродной цепи, т. е присоединение алкильной группы. К таким процессам относится алкилирование алкенов парафинами в присутствии H 3 PO 4 или H 2 SO 4: Этим путем можно получать алканы с изостроением, например изооктан, которые используют как высокооктановое моторное топливо. 3. Галогенирование Галогены легко присоединяются по месту двойной связи. Например, если барботировать алкены через бромную воду, она обесцвечивается за счет присоединения атомов Br по месту кратной связи. Это качественная и количественная реакция на алкены. По количеству поглощенного брома можно установить 22 содержание алкена.
 АЛКЕНЫ Этот процесс может протекать по двум механизмам: – радикальному – электрофильному или ионному (наиболее вероятному). При радикальном присоединении атомы галогена, получающиеся по схеме: присоединяются к наиболее доступному из атомов углерода с образованием наиболее стабильного из возможных радикалов. При галогенировании пропилена возможно образование двух радикалов: 23
АЛКЕНЫ Этот процесс может протекать по двум механизмам: – радикальному – электрофильному или ионному (наиболее вероятному). При радикальном присоединении атомы галогена, получающиеся по схеме: присоединяются к наиболее доступному из атомов углерода с образованием наиболее стабильного из возможных радикалов. При галогенировании пропилена возможно образование двух радикалов: 23
 АЛКЕНЫ Легче образуется и более стабилен радикал (1). В этом радикале свободный электрон сопряжен с электронами пяти С – Н - связей. В радикале (2) электрон сопряжен только с электронами одной С – Н – связи. Кроме того крайний углеродный атом более доступен для взаимодействия. Радикал (1) далее реагирует с молекулой галогена с образованием нового атома галогена: Чаще происходит присоединение по ионному электрофильному механизму. Молекула галогена атакует двойную связь, захватывая электроны и образуя πкомплекс. Затем отделяется отрицательный ион галогена. К образовавшемуся карбониевому или бромониевому катиону присоединяется отрицательный ион галогена: 24
АЛКЕНЫ Легче образуется и более стабилен радикал (1). В этом радикале свободный электрон сопряжен с электронами пяти С – Н - связей. В радикале (2) электрон сопряжен только с электронами одной С – Н – связи. Кроме того крайний углеродный атом более доступен для взаимодействия. Радикал (1) далее реагирует с молекулой галогена с образованием нового атома галогена: Чаще происходит присоединение по ионному электрофильному механизму. Молекула галогена атакует двойную связь, захватывая электроны и образуя πкомплекс. Затем отделяется отрицательный ион галогена. К образовавшемуся карбониевому или бромониевому катиону присоединяется отрицательный ион галогена: 24
 АЛКЕНЫ 4. Гидрогалогенирование В этих реакциях молекула гидрогалогена присоединяется по месту кратной связи. В ряду гидрогалогенов существует закономерность: HF < HCl < HBr < HI У HI максимальная скорость взаимодействия, т. е. способность отдавать катион Н+. Присоединение галогеноводородов к несимметричным алкенам происходит по правилу Марковникова: присоединении молекулы галогеноводорода по месту кратной связи алкена атом Н присоединяется к тому атому С кратной связи, который имеет больше атомов Н. Такой атом С называется наиболее гидрогенезированным. 25
АЛКЕНЫ 4. Гидрогалогенирование В этих реакциях молекула гидрогалогена присоединяется по месту кратной связи. В ряду гидрогалогенов существует закономерность: HF < HCl < HBr < HI У HI максимальная скорость взаимодействия, т. е. способность отдавать катион Н+. Присоединение галогеноводородов к несимметричным алкенам происходит по правилу Марковникова: присоединении молекулы галогеноводорода по месту кратной связи алкена атом Н присоединяется к тому атому С кратной связи, который имеет больше атомов Н. Такой атом С называется наиболее гидрогенезированным. 25
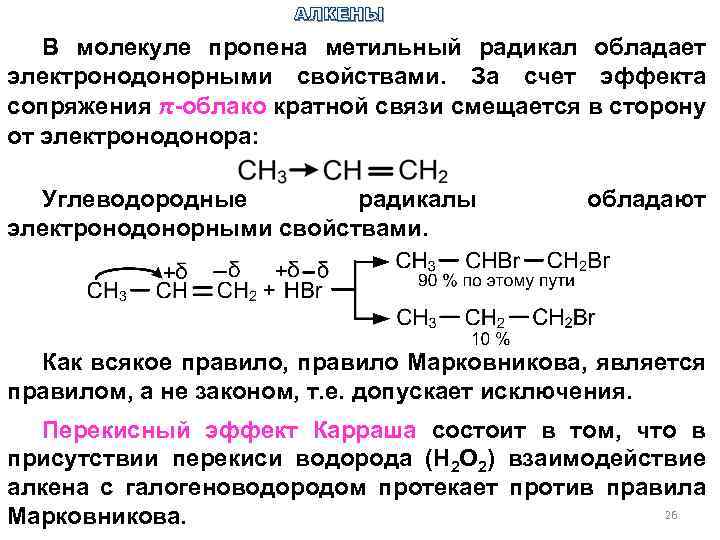 АЛКЕНЫ В молекуле пропена метильный радикал обладает электронодонорными свойствами. За счет эффекта сопряжения π-облако кратной связи смещается в сторону от электронодонора: Углеводородные радикалы электронодонорными свойствами. обладают Как всякое правило, правило Марковникова, является правилом, а не законом, т. е. допускает исключения. Перекисный эффект Карраша состоит в том, что в присутствии перекиси водорода (Н 2 О 2) взаимодействие алкена с галогеноводородом протекает против правила 26 Марковникова.
АЛКЕНЫ В молекуле пропена метильный радикал обладает электронодонорными свойствами. За счет эффекта сопряжения π-облако кратной связи смещается в сторону от электронодонора: Углеводородные радикалы электронодонорными свойствами. обладают Как всякое правило, правило Марковникова, является правилом, а не законом, т. е. допускает исключения. Перекисный эффект Карраша состоит в том, что в присутствии перекиси водорода (Н 2 О 2) взаимодействие алкена с галогеноводородом протекает против правила 26 Марковникова.
 АЛКЕНЫ Н 2 О 2 взаимодействует с галогеноводородом и освобождает атомы галогена, которые присоединяются по месту двойной связи к крайнему атому С, т. к. при этом образуется более стабильный радикал, который взаимодействует с алкеном: 5. Гипогалогенирование – это взаимодействие молекулы алкена с хлорноватистой или бромноватистой кислотой. Процесс протекает по правилу Марковникова: электроотрицательный гидроксид-ион направляется к наименее гидрогенезированному атому углерода: 6. Окисление. Направление окисления алкенов зависит от условий реакции и выбора окислителя: 27
АЛКЕНЫ Н 2 О 2 взаимодействует с галогеноводородом и освобождает атомы галогена, которые присоединяются по месту двойной связи к крайнему атому С, т. к. при этом образуется более стабильный радикал, который взаимодействует с алкеном: 5. Гипогалогенирование – это взаимодействие молекулы алкена с хлорноватистой или бромноватистой кислотой. Процесс протекает по правилу Марковникова: электроотрицательный гидроксид-ион направляется к наименее гидрогенезированному атому углерода: 6. Окисление. Направление окисления алкенов зависит от условий реакции и выбора окислителя: 27
 АЛКЕНЫ 1) алкены при высокой температуре без катализатора сгорают с образованием Н 2 О и СО 2, т. е. с разрушением углеродного скелета. Пламя имеет желтый цвет по сравнению с пламенем алканов, т. к. образуется больше твердых частиц несгоревшего углерода. Это происходит потому, что доля атомов углерода в молекуле алкена больше, чем у алкана. 2) молекула алкена в присутствии окислителей способна окисляться с разрывом кратной связи. Окислители: KMn. O 4, K 2 Cr 2 O 7, HNO 3. При барботировании алкена через раствор KMn. O 4 происходит его обесцвечивание. Это качественная реакция на алкен. Состав продуктов реакции окисления зависит от природы раствора окислителя: 28
АЛКЕНЫ 1) алкены при высокой температуре без катализатора сгорают с образованием Н 2 О и СО 2, т. е. с разрушением углеродного скелета. Пламя имеет желтый цвет по сравнению с пламенем алканов, т. к. образуется больше твердых частиц несгоревшего углерода. Это происходит потому, что доля атомов углерода в молекуле алкена больше, чем у алкана. 2) молекула алкена в присутствии окислителей способна окисляться с разрывом кратной связи. Окислители: KMn. O 4, K 2 Cr 2 O 7, HNO 3. При барботировании алкена через раствор KMn. O 4 происходит его обесцвечивание. Это качественная реакция на алкен. Состав продуктов реакции окисления зависит от природы раствора окислителя: 28
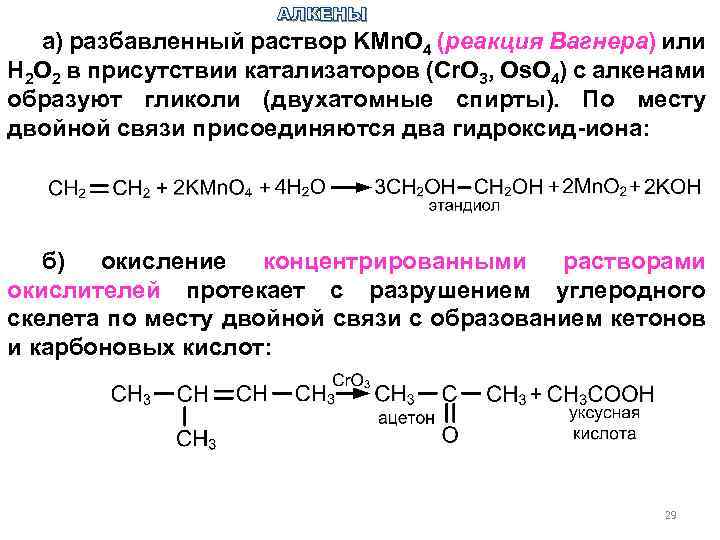 АЛКЕНЫ а) разбавленный раствор KMn. O 4 (реакция Вагнера) или Н 2 О 2 в присутствии катализаторов (Cr. O 3, Os. O 4) с алкенами образуют гликоли (двухатомные спирты). По месту двойной связи присоединяются два гидроксид-иона: б) окисление концентрированными растворами окислителей протекает с разрушением углеродного скелета по месту двойной связи с образованием кетонов и карбоновых кислот: 29
АЛКЕНЫ а) разбавленный раствор KMn. O 4 (реакция Вагнера) или Н 2 О 2 в присутствии катализаторов (Cr. O 3, Os. O 4) с алкенами образуют гликоли (двухатомные спирты). По месту двойной связи присоединяются два гидроксид-иона: б) окисление концентрированными растворами окислителей протекает с разрушением углеродного скелета по месту двойной связи с образованием кетонов и карбоновых кислот: 29
 АЛКЕНЫ 7. Озонирование. При определении строения алкенов в качестве специфического окислителя используется озон. Это реакция озонирования Гарриеса. Озон присоединяется по месту двойной связи, образуя нестойкие, взрывчатые озониды (особые перекиси): При взаимодействии воды с озонидом он разрушается, т. е. происходит озонидное расщепление с образованием альдегида и кетона: 30
АЛКЕНЫ 7. Озонирование. При определении строения алкенов в качестве специфического окислителя используется озон. Это реакция озонирования Гарриеса. Озон присоединяется по месту двойной связи, образуя нестойкие, взрывчатые озониды (особые перекиси): При взаимодействии воды с озонидом он разрушается, т. е. происходит озонидное расщепление с образованием альдегида и кетона: 30
 АЛКЕНЫ 8. Сульфатизация (гидролиз). При барботировании алкена через раствор H 2 SO 4 происходит его растворение. Молекула H 2 SO 4 присоединяется по месту двойной связи по правилу Марковникова. Образуется сложный эфир серной кислоты. При нагревании полученного раствора из эфира образуется спирт, который улетучивается или возгоняется. Процесс протекает в две стадии: 31
АЛКЕНЫ 8. Сульфатизация (гидролиз). При барботировании алкена через раствор H 2 SO 4 происходит его растворение. Молекула H 2 SO 4 присоединяется по месту двойной связи по правилу Марковникова. Образуется сложный эфир серной кислоты. При нагревании полученного раствора из эфира образуется спирт, который улетучивается или возгоняется. Процесс протекает в две стадии: 31
 АЛКЕНЫ H 2 SO 4 является катализатором. В промышленных условиях гидролиз проводят по схеме: 9. Полимеризация. Это процесс объединения простых молекул (мономеров) в длинную цепь – полимер – за счет двойных связей: 32
АЛКЕНЫ H 2 SO 4 является катализатором. В промышленных условиях гидролиз проводят по схеме: 9. Полимеризация. Это процесс объединения простых молекул (мономеров) в длинную цепь – полимер – за счет двойных связей: 32
 АЛКЕНЫ 10. Изомеризация. При высоких температурах или в присутствии катализаторов длинные молекулы алкенов могут подвергаться изометрзации за счет изменения структуры углеродного скелета и передвижения двойной связи по цепочке: 33
АЛКЕНЫ 10. Изомеризация. При высоких температурах или в присутствии катализаторов длинные молекулы алкенов могут подвергаться изометрзации за счет изменения структуры углеродного скелета и передвижения двойной связи по цепочке: 33


