 1 Лекция 6 1. Типы химических связей в кристаллах, электроотрицательность. Кристаллохимические радиусы, поляризация ионов. 2. Потенциальная энергия ионной решетки, константа Маделунга. 3. Гомодесмические и гетеродесмические структуры, структурные единицы кристалла. Основные структурные мотивы.
1 Лекция 6 1. Типы химических связей в кристаллах, электроотрицательность. Кристаллохимические радиусы, поляризация ионов. 2. Потенциальная энергия ионной решетки, константа Маделунга. 3. Гомодесмические и гетеродесмические структуры, структурные единицы кристалла. Основные структурные мотивы.
 Типы сильной химической связи 2 Валентные связи – ионные, ковалентные и металлические, их энергии связи обычно десятки и сотни к. Дж/моль Типы сильной связи Особенности Перенос валентных электронов от одних атомов к другим с образованием катионов и анионов Ионная Ковалентная спаренные электроны Металлическая электроны катионы Обобществление двумя или большим числом атомов валентных электронных пар (двухцентровая и многоцентровая связи). Если электроны предоставлены одним из атомов, то говорят о наличии координационной связи Распределение части внешних электронов атомов металла по всей решетке кристалла
Типы сильной химической связи 2 Валентные связи – ионные, ковалентные и металлические, их энергии связи обычно десятки и сотни к. Дж/моль Типы сильной связи Особенности Перенос валентных электронов от одних атомов к другим с образованием катионов и анионов Ионная Ковалентная спаренные электроны Металлическая электроны катионы Обобществление двумя или большим числом атомов валентных электронных пар (двухцентровая и многоцентровая связи). Если электроны предоставлены одним из атомов, то говорят о наличии координационной связи Распределение части внешних электронов атомов металла по всей решетке кристалла
 Зонная теория 3 E Зона проводимости (пустые уровни) E Запрещенная зона Валентная зона (заполненные уровни) Валентные связи можно сравнивать в единой энергетической шкале в рамках зонной теории твердого тела, которая рассматривает коллективизированные электронные уровни взаимодействующих в решетке атомов – энергетические зоны. Для ионных и ковалентных кристаллов – диэлектриков характерно наличие щели шириной > 3 э. В между нижней заполненной (валентной) зоной и верхней свободной зоной (зоной проводимости), а в металлах такой щели нет. Возможен непрерывный переход от ионной к ковалентной и далее к металлической связи (например, под давлением)
Зонная теория 3 E Зона проводимости (пустые уровни) E Запрещенная зона Валентная зона (заполненные уровни) Валентные связи можно сравнивать в единой энергетической шкале в рамках зонной теории твердого тела, которая рассматривает коллективизированные электронные уровни взаимодействующих в решетке атомов – энергетические зоны. Для ионных и ковалентных кристаллов – диэлектриков характерно наличие щели шириной > 3 э. В между нижней заполненной (валентной) зоной и верхней свободной зоной (зоной проводимости), а в металлах такой щели нет. Возможен непрерывный переход от ионной к ковалентной и далее к металлической связи (например, под давлением)
 4 Электроотрицательность ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ – способность связанного атома притягивать к себе электроны. H 2. 20 Л. Полинг (1901 – 1994) ЭО по Р. Малликену (1934): I – первый потенциал ионизации, F – сродство к электрону. Li Be 0. 98 1. 57 Na Mg 0. 93 1. 31 K Ca Sc Ti V Cr Mn Fe Co Ni Cu 0. 82 1. 00 1. 36 1. 54 1. 63 1. 66 1. 55 1. 83 1. 88 1. 91 Rb Sr Y Zr Nb Mo Tc Ru Rh 0. 82 0. 95 1. 22 1. 33 1. 6 2. 16 1. 9 2. 2 Cs Ba La* Hf Ta W Re 0. 79 0. 89 1. 1 1. 3 1. 5 2. 36 Fr Ra Ac* Rf Db 0. 7 0. 9 1. 1 La Актиноиды He B C N O F Ne 2. 04 2. 55 3. 04 3. 44 3. 98 Al Si P S Cl Ar 1. 61 1. 90 2. 19 2. 58 3. 16 Zn Ga Ge As Se Br Kr 1. 90 1. 65 1. 81 2. 01 2. 18 2. 55 2. 96 3. 00 Pd Ag Cd In Sn Sb Te I Xe 2. 28 2. 20 1. 93 1. 69 1. 78 1. 96 2. 05 2. 1 2. 66 2. 60 Os Ir Pt Au Hg Tl Pb Bi Po At Rn 1. 9 2. 20 2. 28 2. 54 2. 00 1. 62 2. 33 2. 02 2. 0 2. 2 Sg Bh Hs Mt Ds Rg Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu 1. 12 1. 13 1. 14 1. 13 1. 17 1. 2 1. 1 1. 22 1. 23 1. 24 1. 25 1. 1 1. 27 Ac Th Pa U Pu Am Cm Bk Cf Es Fm Md No Lr 1. 1 1. 3 1. 5 1. 38 Np 1. 36 1. 28 1. 13 1. 28 1. 3 1. 29 граница металлы–неметаллы Лантаноиды = (I + F) / 2
4 Электроотрицательность ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ – способность связанного атома притягивать к себе электроны. H 2. 20 Л. Полинг (1901 – 1994) ЭО по Р. Малликену (1934): I – первый потенциал ионизации, F – сродство к электрону. Li Be 0. 98 1. 57 Na Mg 0. 93 1. 31 K Ca Sc Ti V Cr Mn Fe Co Ni Cu 0. 82 1. 00 1. 36 1. 54 1. 63 1. 66 1. 55 1. 83 1. 88 1. 91 Rb Sr Y Zr Nb Mo Tc Ru Rh 0. 82 0. 95 1. 22 1. 33 1. 6 2. 16 1. 9 2. 2 Cs Ba La* Hf Ta W Re 0. 79 0. 89 1. 1 1. 3 1. 5 2. 36 Fr Ra Ac* Rf Db 0. 7 0. 9 1. 1 La Актиноиды He B C N O F Ne 2. 04 2. 55 3. 04 3. 44 3. 98 Al Si P S Cl Ar 1. 61 1. 90 2. 19 2. 58 3. 16 Zn Ga Ge As Se Br Kr 1. 90 1. 65 1. 81 2. 01 2. 18 2. 55 2. 96 3. 00 Pd Ag Cd In Sn Sb Te I Xe 2. 28 2. 20 1. 93 1. 69 1. 78 1. 96 2. 05 2. 1 2. 66 2. 60 Os Ir Pt Au Hg Tl Pb Bi Po At Rn 1. 9 2. 20 2. 28 2. 54 2. 00 1. 62 2. 33 2. 02 2. 0 2. 2 Sg Bh Hs Mt Ds Rg Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu 1. 12 1. 13 1. 14 1. 13 1. 17 1. 2 1. 1 1. 22 1. 23 1. 24 1. 25 1. 1 1. 27 Ac Th Pa U Pu Am Cm Bk Cf Es Fm Md No Lr 1. 1 1. 3 1. 5 1. 38 Np 1. 36 1. 28 1. 13 1. 28 1. 3 1. 29 граница металлы–неметаллы Лантаноиды = (I + F) / 2
 Электроотрицательность, типы связей и структурные карты 5 среднее главное квантовое число Ионной связи отвечает примерно Δ > 2, что характерно для связей между наиболее активными металлами и неметаллами. Для ковалентных связей верхняя граница Δ 1. 5, а наименьшие Δ характерны для ковалентных связей неметалл-неметалл или металлических связей. Металлическая связь встречается в сплавах, интерметаллидах и соединениях переходных металлов с наименее электроотрицательными неметаллами B, C, N, Si, P. Диаграмма Музера Пирсона Электроотрицательности полезны для соединений AB (1959) классификации структур по типам химической связи, которые часто Cs. Cl представляют в виде диаграмм. Одна из первых диаграмм предложена Na. Cl Музером и Пирсоном для соединений AB, которые хорошо разделяются на сфалерит вюрцит четыре структурные группы. Подобные увеличение ионности Δ диаграммы часто называют структурными картами.
Электроотрицательность, типы связей и структурные карты 5 среднее главное квантовое число Ионной связи отвечает примерно Δ > 2, что характерно для связей между наиболее активными металлами и неметаллами. Для ковалентных связей верхняя граница Δ 1. 5, а наименьшие Δ характерны для ковалентных связей неметалл-неметалл или металлических связей. Металлическая связь встречается в сплавах, интерметаллидах и соединениях переходных металлов с наименее электроотрицательными неметаллами B, C, N, Si, P. Диаграмма Музера Пирсона Электроотрицательности полезны для соединений AB (1959) классификации структур по типам химической связи, которые часто Cs. Cl представляют в виде диаграмм. Одна из первых диаграмм предложена Na. Cl Музером и Пирсоном для соединений AB, которые хорошо разделяются на сфалерит вюрцит четыре структурные группы. Подобные увеличение ионности Δ диаграммы часто называют структурными картами.
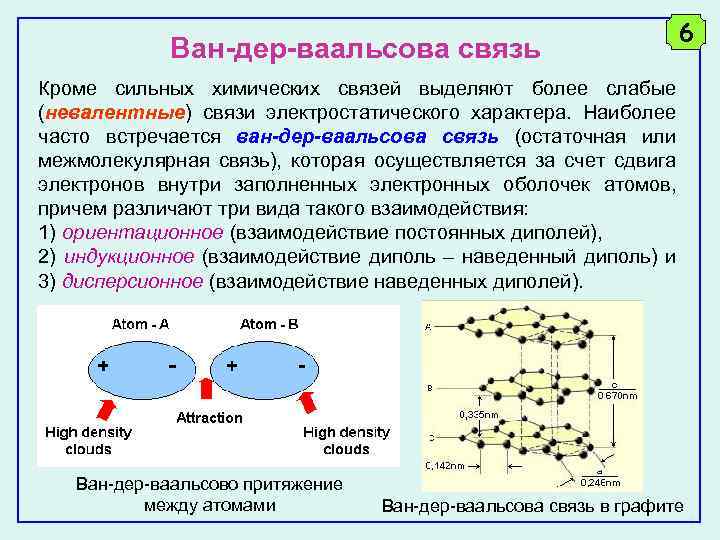 Ван-дер-ваальсова связь 6 Кроме сильных химических связей выделяют более слабые (невалентные) связи электростатического характера. Наиболее часто встречается ван-дер-ваальсова связь (остаточная или межмолекулярная связь), которая осуществляется за счет сдвига электронов внутри заполненных электронных оболочек атомов, причем различают три вида такого взаимодействия: 1) ориентационное (взаимодействие постоянных диполей), 2) индукционное (взаимодействие диполь – наведенный диполь) и 3) дисперсионное (взаимодействие наведенных диполей). Ван-дер-ваальсово притяжение между атомами Ван-дер-ваальсова связь в графите
Ван-дер-ваальсова связь 6 Кроме сильных химических связей выделяют более слабые (невалентные) связи электростатического характера. Наиболее часто встречается ван-дер-ваальсова связь (остаточная или межмолекулярная связь), которая осуществляется за счет сдвига электронов внутри заполненных электронных оболочек атомов, причем различают три вида такого взаимодействия: 1) ориентационное (взаимодействие постоянных диполей), 2) индукционное (взаимодействие диполь – наведенный диполь) и 3) дисперсионное (взаимодействие наведенных диполей). Ван-дер-ваальсово притяжение между атомами Ван-дер-ваальсова связь в графите
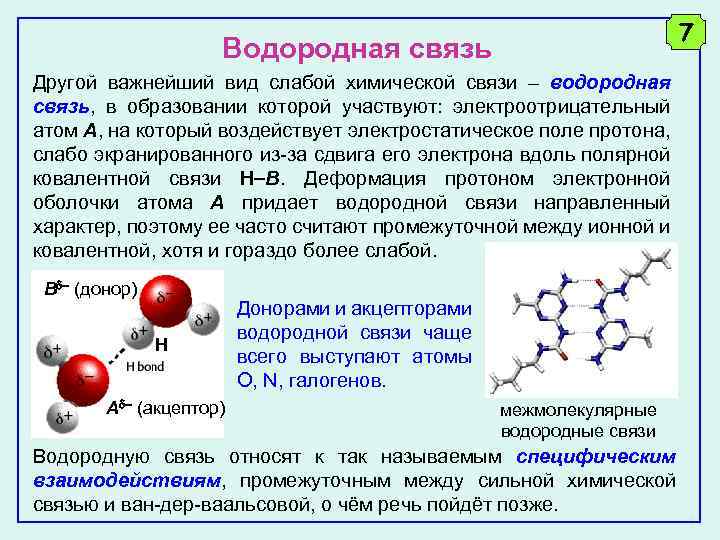 7 Водородная связь Другой важнейший вид слабой химической связи – водородная связь, в образовании которой участвуют: электроотрицательный атом A, на который воздействует электростатическое поле протона, слабо экранированного из-за сдвига его электрона вдоль полярной ковалентной связи H B. Деформация протоном электронной оболочки атома A придает водородной связи направленный характер, поэтому ее часто считают промежуточной между ионной и ковалентной, хотя и гораздо более слабой. B (донор) H A (акцептор) Донорами и акцепторами водородной связи чаще всего выступают атомы O, N, галогенов. межмолекулярные водородные связи Водородную связь относят к так называемым специфическим взаимодействиям, промежуточным между сильной химической связью и ван-дер-ваальсовой, о чём речь пойдёт позже.
7 Водородная связь Другой важнейший вид слабой химической связи – водородная связь, в образовании которой участвуют: электроотрицательный атом A, на который воздействует электростатическое поле протона, слабо экранированного из-за сдвига его электрона вдоль полярной ковалентной связи H B. Деформация протоном электронной оболочки атома A придает водородной связи направленный характер, поэтому ее часто считают промежуточной между ионной и ковалентной, хотя и гораздо более слабой. B (донор) H A (акцептор) Донорами и акцепторами водородной связи чаще всего выступают атомы O, N, галогенов. межмолекулярные водородные связи Водородную связь относят к так называемым специфическим взаимодействиям, промежуточным между сильной химической связью и ван-дер-ваальсовой, о чём речь пойдёт позже.
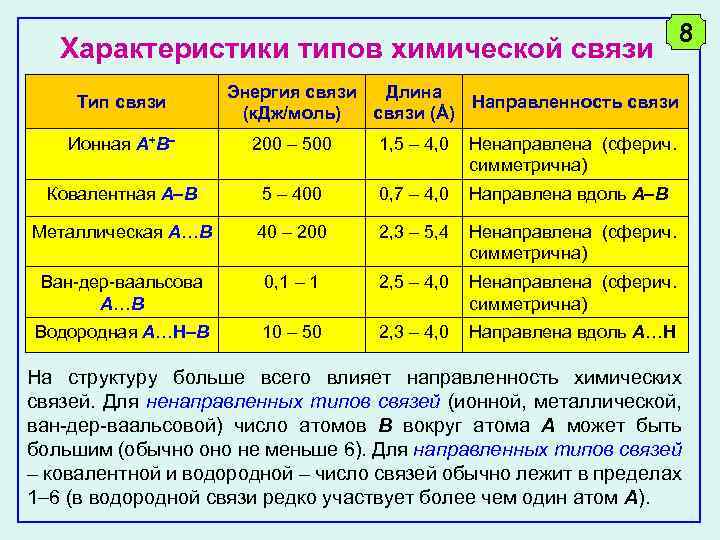 Характеристики типов химической связи Тип связи 8 Энергия связи Длина Направленность связи (к. Дж/моль) связи (Å) Ионная A+B 200 500 1, 5 4, 0 Ненаправлена (сферич. симметрична) Ковалентная A B 5 400 0, 7 4, 0 Направлена вдоль A B Металлическая A…B 40 200 2, 3 5, 4 Ненаправлена (сферич. симметрична) Ван-дер-ваальсова A…B 0, 1 1 2, 5 4, 0 Ненаправлена (сферич. симметрична) Водородная A…H B 10 50 2, 3 4, 0 Направлена вдоль A…H На структуру больше всего влияет направленность химических связей. Для ненаправленных типов связей (ионной, металлической, ван-дер-ваальсовой) число атомов B вокруг атома A может быть большим (обычно оно не меньше 6). Для направленных типов связей – ковалентной и водородной – число связей обычно лежит в пределах 1 6 (в водородной связи редко участвует более чем один атом A).
Характеристики типов химической связи Тип связи 8 Энергия связи Длина Направленность связи (к. Дж/моль) связи (Å) Ионная A+B 200 500 1, 5 4, 0 Ненаправлена (сферич. симметрична) Ковалентная A B 5 400 0, 7 4, 0 Направлена вдоль A B Металлическая A…B 40 200 2, 3 5, 4 Ненаправлена (сферич. симметрична) Ван-дер-ваальсова A…B 0, 1 1 2, 5 4, 0 Ненаправлена (сферич. симметрична) Водородная A…H B 10 50 2, 3 4, 0 Направлена вдоль A…H На структуру больше всего влияет направленность химических связей. Для ненаправленных типов связей (ионной, металлической, ван-дер-ваальсовой) число атомов B вокруг атома A может быть большим (обычно оно не меньше 6). Для направленных типов связей – ковалентной и водородной – число связей обычно лежит в пределах 1 6 (в водородной связи редко участвует более чем один атом A).
 Кристаллохимические радиусы 9 Несмотря на разнообразие типов химических связей и структур, при одинаковом типе и порядке связи расстояние d. AB для данной пары атомов выдерживается в разных структурах с точностью порядка 0, 05 0, 1 Å. Это позволяет в первом приближении приписать атомам для того или иного типа связей между ними приблизительно постоянные «размеры» – кристаллохимические радиусы. КРИСТАЛЛОХИМИЧЕСКИЕ РАДИУСЫ – размерные характеристики атомов, отвечающие определенному типу связи и основанные на классическом представлении о связанных атомах как соприкасающихся шарах. Главное свойство кристаллохимических радиусов – воспроизводить при суммировании длины соответствующих химических связей (аддитивность радиусов). В соответствии с основными типами химической связи различают четыре системы кристаллохимических радиусов: ионные, ковалентные, металлические и ван-дер-ваальсовы.
Кристаллохимические радиусы 9 Несмотря на разнообразие типов химических связей и структур, при одинаковом типе и порядке связи расстояние d. AB для данной пары атомов выдерживается в разных структурах с точностью порядка 0, 05 0, 1 Å. Это позволяет в первом приближении приписать атомам для того или иного типа связей между ними приблизительно постоянные «размеры» – кристаллохимические радиусы. КРИСТАЛЛОХИМИЧЕСКИЕ РАДИУСЫ – размерные характеристики атомов, отвечающие определенному типу связи и основанные на классическом представлении о связанных атомах как соприкасающихся шарах. Главное свойство кристаллохимических радиусов – воспроизводить при суммировании длины соответствующих химических связей (аддитивность радиусов). В соответствии с основными типами химической связи различают четыре системы кристаллохимических радиусов: ионные, ковалентные, металлические и ван-дер-ваальсовы.
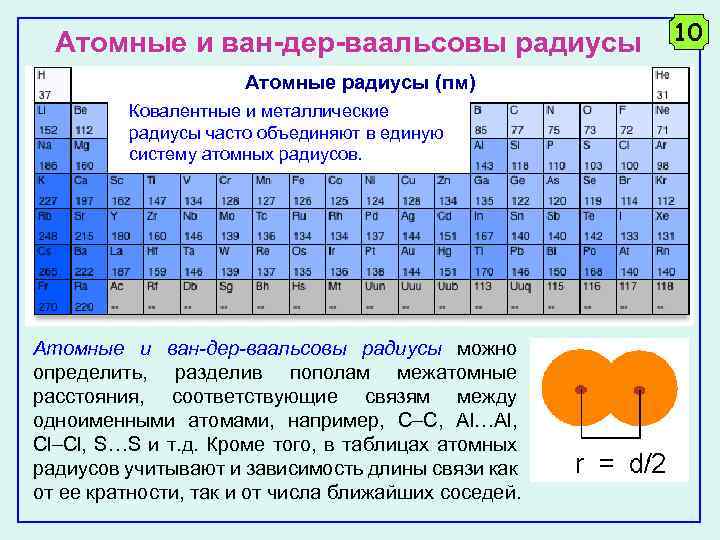 Атомные и ван-дер-ваальсовы радиусы 10 Атомные радиусы (пм) Ковалентные и металлические радиусы часто объединяют в единую систему атомных радиусов. Атомные и ван-дер-ваальсовы радиусы можно определить, разделив пополам межатомные расстояния, соответствующие связям между одноименными атомами, например, C C, Al…Al, Cl Cl, S…S и т. д. Кроме того, в таблицах атомных радиусов учитывают и зависимость длины связи как от ее кратности, так и от числа ближайших соседей.
Атомные и ван-дер-ваальсовы радиусы 10 Атомные радиусы (пм) Ковалентные и металлические радиусы часто объединяют в единую систему атомных радиусов. Атомные и ван-дер-ваальсовы радиусы можно определить, разделив пополам межатомные расстояния, соответствующие связям между одноименными атомами, например, C C, Al…Al, Cl Cl, S…S и т. д. Кроме того, в таблицах атомных радиусов учитывают и зависимость длины связи как от ее кратности, так и от числа ближайших соседей.
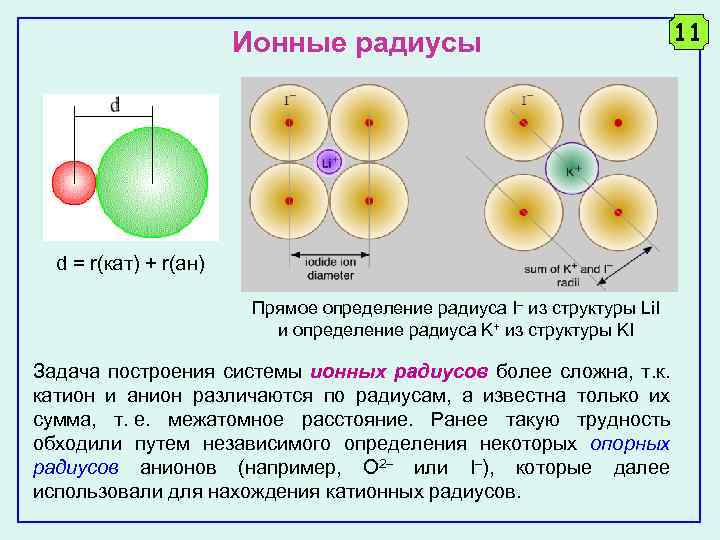 Ионные радиусы 11 d = r(кат) + r(ан) Прямое определение радиуса I из структуры Li. I и определение радиуса K+ из структуры KI Задача построения системы ионных радиусов более сложна, т. к. катион и анион различаются по радиусам, а известна только их сумма, т. е. межатомное расстояние. Ранее такую трудность обходили путем независимого определения некоторых опорных радиусов анионов (например, O 2 или I ), которые далее использовали для нахождения катионных радиусов.
Ионные радиусы 11 d = r(кат) + r(ан) Прямое определение радиуса I из структуры Li. I и определение радиуса K+ из структуры KI Задача построения системы ионных радиусов более сложна, т. к. катион и анион различаются по радиусам, а известна только их сумма, т. е. межатомное расстояние. Ранее такую трудность обходили путем независимого определения некоторых опорных радиусов анионов (например, O 2 или I ), которые далее использовали для нахождения катионных радиусов.
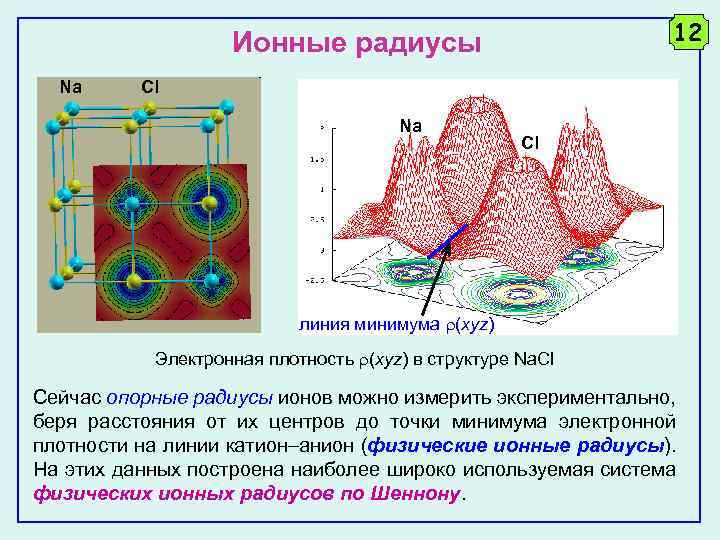 12 Ионные радиусы Na Cl линия минимума (xyz) Электронная плотность (xyz) в структуре Na. Cl Сейчас опорные радиусы ионов можно измерить экспериментально, беря расстояния от их центров до точки минимума электронной плотности на линии катион анион (физические ионные радиусы). На этих данных построена наиболее широко используемая система физических ионных радиусов по Шеннону.
12 Ионные радиусы Na Cl линия минимума (xyz) Электронная плотность (xyz) в структуре Na. Cl Сейчас опорные радиусы ионов можно измерить экспериментально, беря расстояния от их центров до точки минимума электронной плотности на линии катион анион (физические ионные радиусы). На этих данных построена наиболее широко используемая система физических ионных радиусов по Шеннону.
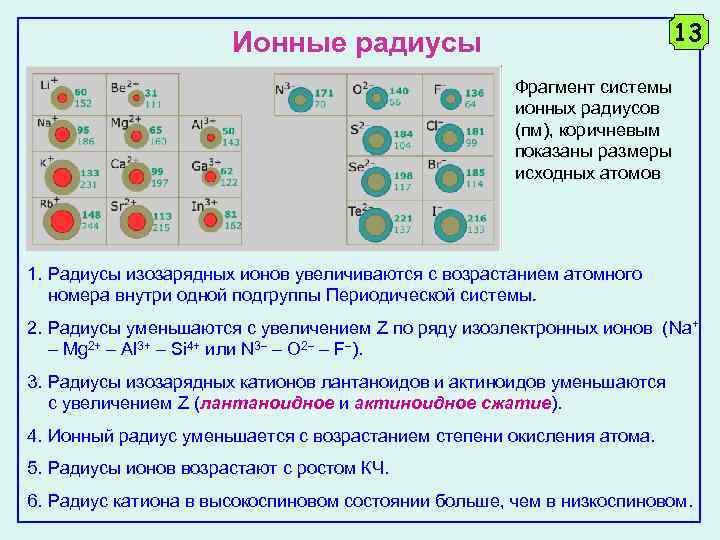 13 Ионные радиусы Фрагмент системы ионных радиусов (пм), коричневым показаны размеры исходных атомов 1. Радиусы изозарядных ионов увеличиваются с возрастанием атомного номера внутри одной подгруппы Периодической системы. 2. Радиусы уменьшаются с увеличением Z по ряду изоэлектронных ионов (Na+ Mg 2+ Al 3+ Si 4+ или N 3 O 2 F ). 3. Радиусы изозарядных катионов лантаноидов и актиноидов уменьшаются с увеличением Z (лантаноидное и актиноидное сжатие). 4. Ионный радиус уменьшается с возрастанием степени окисления атома. 5. Радиусы ионов возрастают с ростом КЧ. 6. Радиус катиона в высокоспиновом состоянии больше, чем в низкоспиновом.
13 Ионные радиусы Фрагмент системы ионных радиусов (пм), коричневым показаны размеры исходных атомов 1. Радиусы изозарядных ионов увеличиваются с возрастанием атомного номера внутри одной подгруппы Периодической системы. 2. Радиусы уменьшаются с увеличением Z по ряду изоэлектронных ионов (Na+ Mg 2+ Al 3+ Si 4+ или N 3 O 2 F ). 3. Радиусы изозарядных катионов лантаноидов и актиноидов уменьшаются с увеличением Z (лантаноидное и актиноидное сжатие). 4. Ионный радиус уменьшается с возрастанием степени окисления атома. 5. Радиусы ионов возрастают с ростом КЧ. 6. Радиус катиона в высокоспиновом состоянии больше, чем в низкоспиновом.
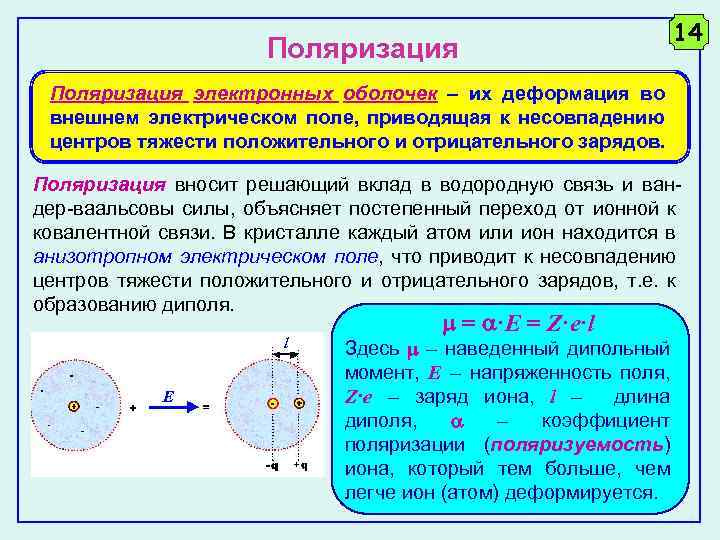 Поляризация 14 Поляризация электронных оболочек – их деформация во внешнем электрическом поле, приводящая к несовпадению центров тяжести положительного и отрицательного зарядов. Поляризация вносит решающий вклад в водородную связь и вандер-ваальсовы силы, объясняет постепенный переход от ионной к ковалентной связи. В кристалле каждый атом или ион находится в анизотропном электрическом поле, что приводит к несовпадению центров тяжести положительного и отрицательного зарядов, т. е. к образованию диполя. l E = ·E = Z·e·l Здесь – наведенный дипольный момент, E – напряженность поля, Z·e – заряд иона, l – длина диполя, – коэффициент поляризации (поляризуемость) иона, который тем больше, чем легче ион (атом) деформируется.
Поляризация 14 Поляризация электронных оболочек – их деформация во внешнем электрическом поле, приводящая к несовпадению центров тяжести положительного и отрицательного зарядов. Поляризация вносит решающий вклад в водородную связь и вандер-ваальсовы силы, объясняет постепенный переход от ионной к ковалентной связи. В кристалле каждый атом или ион находится в анизотропном электрическом поле, что приводит к несовпадению центров тяжести положительного и отрицательного зарядов, т. е. к образованию диполя. l E = ·E = Z·e·l Здесь – наведенный дипольный момент, E – напряженность поля, Z·e – заряд иона, l – длина диполя, – коэффициент поляризации (поляризуемость) иона, который тем больше, чем легче ион (атом) деформируется.
 Закономерности поляризации 15 Для поляризации ионов в кристалле установлены следующие закономерности (правила Фаянса, 1923): К. Фаянс (1887 -1975) d d d 1. Поляризуемость аниона тем больше, чем больше его радиус. 2. Поляризующее действие катиона тем больше, а его поляризуемость тем меньше, чем больше его заряд и меньше радиус. 3. Чем ближе электронная оболочка атома к оболочке инертного газа, тем меньше поляризационные эффекты. Под действием поляризации электронные оболочки атомов и ионов сминаются, электронная плотность аниона смещается к катиону, растёт ковалентность связи. Это приводит к уменьшению расстояний катион-анион и постепенному переходу от типично ионных структур (с высокими KЧ) к типично ковалентным (с низкими KЧ).
Закономерности поляризации 15 Для поляризации ионов в кристалле установлены следующие закономерности (правила Фаянса, 1923): К. Фаянс (1887 -1975) d d d 1. Поляризуемость аниона тем больше, чем больше его радиус. 2. Поляризующее действие катиона тем больше, а его поляризуемость тем меньше, чем больше его заряд и меньше радиус. 3. Чем ближе электронная оболочка атома к оболочке инертного газа, тем меньше поляризационные эффекты. Под действием поляризации электронные оболочки атомов и ионов сминаются, электронная плотность аниона смещается к катиону, растёт ковалентность связи. Это приводит к уменьшению расстояний катион-анион и постепенному переходу от типично ионных структур (с высокими KЧ) к типично ковалентным (с низкими KЧ).
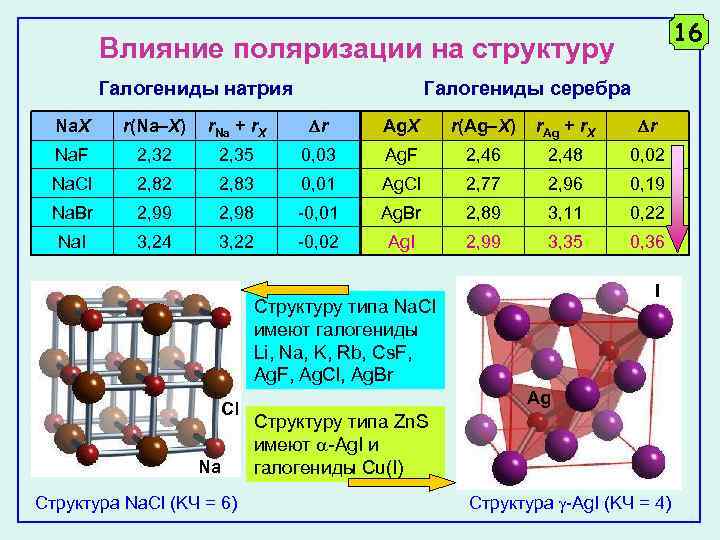 16 Влияние поляризации на структуру Галогениды натрия Галогениды серебра Na. X r(Na X) r. Na + r. X r Ag. X r(Ag X) r. Ag + r. X r Na. F 2, 32 2, 35 0, 03 Ag. F 2, 46 2, 48 0, 02 Na. Cl 2, 82 2, 83 0, 01 Ag. Cl 2, 77 2, 96 0, 19 Na. Br 2, 99 2, 98 -0, 01 Ag. Br 2, 89 3, 11 0, 22 Na. I 3, 24 3, 22 -0, 02 Ag. I 2, 99 3, 35 0, 36 I Структуру типа Na. Cl имеют галогениды Li, Na, K, Rb, Cs. F, Ag. F, Ag. Cl, Ag. Br Cl Na Структура Na. Cl (KЧ = 6) Ag Структуру типа Zn. S имеют -Ag. I и галогениды Cu(I) Структура -Ag. I (KЧ = 4)
16 Влияние поляризации на структуру Галогениды натрия Галогениды серебра Na. X r(Na X) r. Na + r. X r Ag. X r(Ag X) r. Ag + r. X r Na. F 2, 32 2, 35 0, 03 Ag. F 2, 46 2, 48 0, 02 Na. Cl 2, 82 2, 83 0, 01 Ag. Cl 2, 77 2, 96 0, 19 Na. Br 2, 99 2, 98 -0, 01 Ag. Br 2, 89 3, 11 0, 22 Na. I 3, 24 3, 22 -0, 02 Ag. I 2, 99 3, 35 0, 36 I Структуру типа Na. Cl имеют галогениды Li, Na, K, Rb, Cs. F, Ag. F, Ag. Cl, Ag. Br Cl Na Структура Na. Cl (KЧ = 6) Ag Структуру типа Zn. S имеют -Ag. I и галогениды Cu(I) Структура -Ag. I (KЧ = 4)
 Энергия сцепления кристалла 17 Энергия сцепления кристалла равна энергии образования кристалла из бесконечно разреженного газа атомов, ионов или молекул. Устойчивость кристалла определяется энергией разрыва его самых слабых связей: например, для того, чтобы разрушить органический кристалл, достаточно разорвать его ван-дер-ваальсовы или водородные межмолекулярные связи. Если же связи одного типа, их нужно разорвать по всему кристаллу. Если рассмотреть наиболее простой случай ионного кристалла, то его в первом приближении можно рассматривать как трёхмерную решётку точечных зарядов – катионов и анионов. Энергию образования ионного кристалла (энергию решётки) измеряют относительно бесконечно разреженного газа ионов. Энергия ионной решётки зависит от зарядов ионов, катионанионных расстояний и типа кристаллической структуры.
Энергия сцепления кристалла 17 Энергия сцепления кристалла равна энергии образования кристалла из бесконечно разреженного газа атомов, ионов или молекул. Устойчивость кристалла определяется энергией разрыва его самых слабых связей: например, для того, чтобы разрушить органический кристалл, достаточно разорвать его ван-дер-ваальсовы или водородные межмолекулярные связи. Если же связи одного типа, их нужно разорвать по всему кристаллу. Если рассмотреть наиболее простой случай ионного кристалла, то его в первом приближении можно рассматривать как трёхмерную решётку точечных зарядов – катионов и анионов. Энергию образования ионного кристалла (энергию решётки) измеряют относительно бесконечно разреженного газа ионов. Энергия ионной решётки зависит от зарядов ионов, катионанионных расстояний и типа кристаллической структуры.
 Энергия ионной решётки 18 В энергию решётки U основной вклад вносят электростатические силы и некулоновские силы отталкивания: U = – a/R + b·exp( R/ ), (уравнение Борна-Майера) где R – кратчайшее расстояние катион-анион; а, b, – константы. Константа а связана с энергией электростатического взаимодействия катионов MZ+ и анионов XZ , рассчитанной для всего кристалла. Для двух ближайших ионов сила притяжения равна = Z+Z e 2/R. Чтобы просуммировать остальные члены, нужно знать тип структуры. Например, в структуре Na. Cl каждый ион на расстоянии R = а/2 окружают 6 ближайших ионов (0 1) противоположного знака, на расстоянии R = a/ имеются 12 ионов того же знака (0 2), затем 8 ионов противоположного знака на расстоянии R = a /2 (0 3) и далее по другим координационным сферам.
Энергия ионной решётки 18 В энергию решётки U основной вклад вносят электростатические силы и некулоновские силы отталкивания: U = – a/R + b·exp( R/ ), (уравнение Борна-Майера) где R – кратчайшее расстояние катион-анион; а, b, – константы. Константа а связана с энергией электростатического взаимодействия катионов MZ+ и анионов XZ , рассчитанной для всего кристалла. Для двух ближайших ионов сила притяжения равна = Z+Z e 2/R. Чтобы просуммировать остальные члены, нужно знать тип структуры. Например, в структуре Na. Cl каждый ион на расстоянии R = а/2 окружают 6 ближайших ионов (0 1) противоположного знака, на расстоянии R = a/ имеются 12 ионов того же знака (0 2), затем 8 ионов противоположного знака на расстоянии R = a /2 (0 3) и далее по другим координационным сферам.
 19 Постоянная Маделунга Суммируя все кулоновские члены и умножая на число Авогадро в расчёте на моль MX, для структуры Na. Cl получаем: Uкул = –(Z+Z e 2 N/R)(6 – 12/ + 8/ – 6/ + 24/ –. . . ) = AZ+Z e 2 N/R. Сумма бесконечного ряда в скобках (A) называется постоянной Маделунга (1918), которая зависит от типа структуры, но не зависит от его масштаба. Структурный тип A Галит Na. Cl 1, 7476 Вюрцит Zn. S 1, 6407 Cs. Cl 1, 7627 Флюорит Ca. F 2 2, 5193 1, 6381 Рутил Ti. O 2 2, 3850 Э. Маделунг (1881 – 1972) Сфалерит Zn. S Кроме кулоновского члена, существенный вклад в энергию ионной решетки дает отталкивание ионов, описываемое членом b·exp( R/ ). Параметр определяют по сжимаемости кристалла, а константу b можно найти из условия равновесия кристалла d. U/d. R = 0.
19 Постоянная Маделунга Суммируя все кулоновские члены и умножая на число Авогадро в расчёте на моль MX, для структуры Na. Cl получаем: Uкул = –(Z+Z e 2 N/R)(6 – 12/ + 8/ – 6/ + 24/ –. . . ) = AZ+Z e 2 N/R. Сумма бесконечного ряда в скобках (A) называется постоянной Маделунга (1918), которая зависит от типа структуры, но не зависит от его масштаба. Структурный тип A Галит Na. Cl 1, 7476 Вюрцит Zn. S 1, 6407 Cs. Cl 1, 7627 Флюорит Ca. F 2 2, 5193 1, 6381 Рутил Ti. O 2 2, 3850 Э. Маделунг (1881 – 1972) Сфалерит Zn. S Кроме кулоновского члена, существенный вклад в энергию ионной решетки дает отталкивание ионов, описываемое членом b·exp( R/ ). Параметр определяют по сжимаемости кристалла, а константу b можно найти из условия равновесия кристалла d. U/d. R = 0.
 20 Энергия ионной решётки Простейший вид уравнения U = Z+Z e 2 A·N (1 – /R)/R Борна-Майера: Наибольший вклад в энергию решётки даёт кулоновский член, некулоновская энергия отталкивания составляет до 10 15 % общей энергии. В наиболее точных расчетах учитывают энергию ван-дерваальсового взаимодействия и энергию нулевых колебаний: U = Z+Z e 2 A·N/R + b·exp( R/ ) – c·N/R 6 + 2, 25 h 0 Вклад ван-дер-ваальсовых сил (до 10 % общей энергии) оказывается решающим для устойчивости структуры Cs. Cl по сравнению с Na. Cl. Измеренные и вычисленные энергии решёток (ккал/моль) Соед. Uэксп Uтеор Na. F 217 215 Ag. F 231 219 Ca. F 2 624 622 Na. Cl 185 184 Ag. Cl 219 203 Cd. F 2 662 634 Na. Br 178 176 Ag. Br 217 197 Cu. F 2 727 627 Na. I 167 164 Ag. I 214 190 Cd. I 2 576 477
20 Энергия ионной решётки Простейший вид уравнения U = Z+Z e 2 A·N (1 – /R)/R Борна-Майера: Наибольший вклад в энергию решётки даёт кулоновский член, некулоновская энергия отталкивания составляет до 10 15 % общей энергии. В наиболее точных расчетах учитывают энергию ван-дерваальсового взаимодействия и энергию нулевых колебаний: U = Z+Z e 2 A·N/R + b·exp( R/ ) – c·N/R 6 + 2, 25 h 0 Вклад ван-дер-ваальсовых сил (до 10 % общей энергии) оказывается решающим для устойчивости структуры Cs. Cl по сравнению с Na. Cl. Измеренные и вычисленные энергии решёток (ккал/моль) Соед. Uэксп Uтеор Na. F 217 215 Ag. F 231 219 Ca. F 2 624 622 Na. Cl 185 184 Ag. Cl 219 203 Cd. F 2 662 634 Na. Br 178 176 Ag. Br 217 197 Cu. F 2 727 627 Na. I 167 164 Ag. I 214 190 Cd. I 2 576 477
 «Десмическая» классификация структур 21 Гомодесмической называется структура, в которой все атомы связаны равноценными химическими связями одного типа (обычно близкой длины). Такими структурами являются структуры алмаза, Na. Cl, Zn. S, Ca. F 2, металлов, инертных газов. Гетеродесмической называется структура, в которой атомы связаны химическими связями различного типа (различной прочности) и/или длины. В гетеродесмических структурах можно выделить структурные единицы кристалла – устойчивые группы атомов, связанных наиболее прочными связями (обычно ковалентными), которые способны переходить из одной структуры в другую. Конфигурация структурных единиц кристалла и их взаимное расположение определяют характерные черты строения кристалла – мотив структуры.
«Десмическая» классификация структур 21 Гомодесмической называется структура, в которой все атомы связаны равноценными химическими связями одного типа (обычно близкой длины). Такими структурами являются структуры алмаза, Na. Cl, Zn. S, Ca. F 2, металлов, инертных газов. Гетеродесмической называется структура, в которой атомы связаны химическими связями различного типа (различной прочности) и/или длины. В гетеродесмических структурах можно выделить структурные единицы кристалла – устойчивые группы атомов, связанных наиболее прочными связями (обычно ковалентными), которые способны переходить из одной структуры в другую. Конфигурация структурных единиц кристалла и их взаимное расположение определяют характерные черты строения кристалла – мотив структуры.
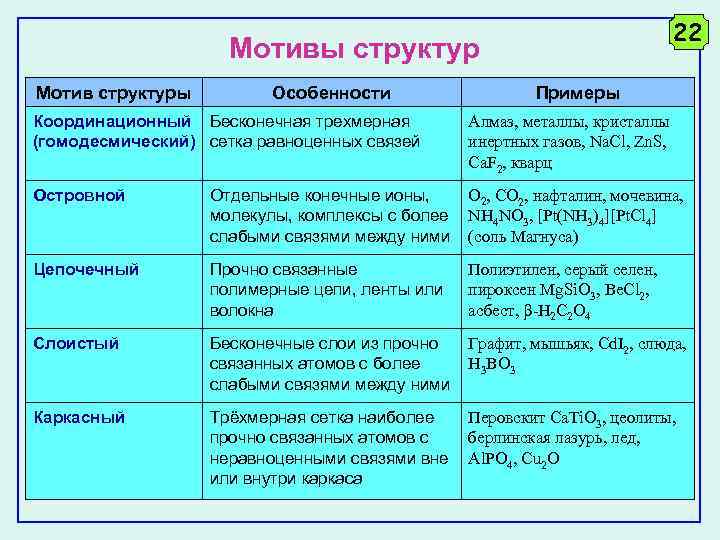 22 Мотивы структур Мотив структуры Особенности Координационный Бесконечная трехмерная (гомодесмический) сетка равноценных связей Примеры Алмаз, металлы, кристаллы инертных газов, Na. Cl, Zn. S, Ca. F 2, кварц Островной O 2, CO 2, нафталин, мочевина, Отдельные конечные ионы, молекулы, комплексы с более NH 4 NO 3, [Pt(NH 3)4][Pt. Cl 4] слабыми связями между ними (соль Магнуса) Цепочечный Прочно связанные полимерные цепи, ленты или волокна Полиэтилен, серый селен, пироксен Mg. Si. O 3, Be. Cl 2, асбест, -H 2 C 2 O 4 Слоистый Бесконечные слои из прочно связанных атомов с более слабыми связями между ними Графит, мышьяк, Cd. I 2, слюда, H 3 BO 3 Каркасный Перовскит Ca. Ti. O 3, цеолиты, Трёхмерная сетка наиболее берлинская лазурь, лед, прочно связанных атомов с неравноценными связями вне Al. PO 4, Cu 2 O или внутри каркаса
22 Мотивы структур Мотив структуры Особенности Координационный Бесконечная трехмерная (гомодесмический) сетка равноценных связей Примеры Алмаз, металлы, кристаллы инертных газов, Na. Cl, Zn. S, Ca. F 2, кварц Островной O 2, CO 2, нафталин, мочевина, Отдельные конечные ионы, молекулы, комплексы с более NH 4 NO 3, [Pt(NH 3)4][Pt. Cl 4] слабыми связями между ними (соль Магнуса) Цепочечный Прочно связанные полимерные цепи, ленты или волокна Полиэтилен, серый селен, пироксен Mg. Si. O 3, Be. Cl 2, асбест, -H 2 C 2 O 4 Слоистый Бесконечные слои из прочно связанных атомов с более слабыми связями между ними Графит, мышьяк, Cd. I 2, слюда, H 3 BO 3 Каркасный Перовскит Ca. Ti. O 3, цеолиты, Трёхмерная сетка наиболее берлинская лазурь, лед, прочно связанных атомов с неравноценными связями вне Al. PO 4, Cu 2 O или внутри каркаса
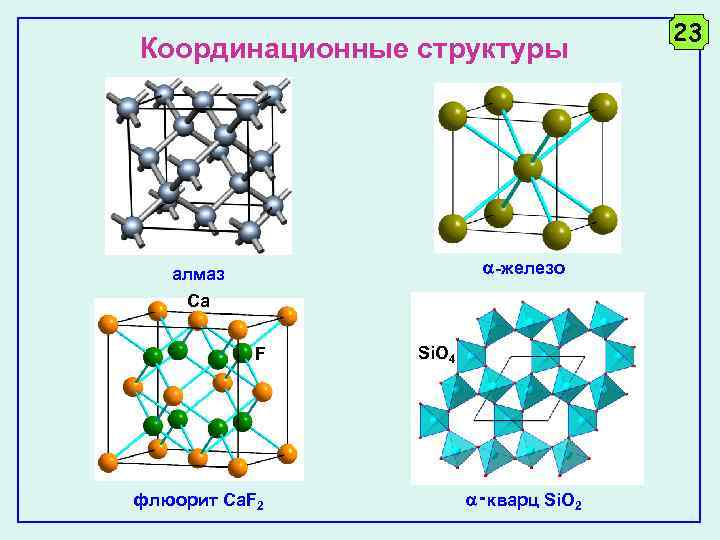 Координационные структуры -железо алмаз Ca F флюорит Ca. F 2 Si. O 4 ‑кварц Si. O 2 23
Координационные структуры -железо алмаз Ca F флюорит Ca. F 2 Si. O 4 ‑кварц Si. O 2 23
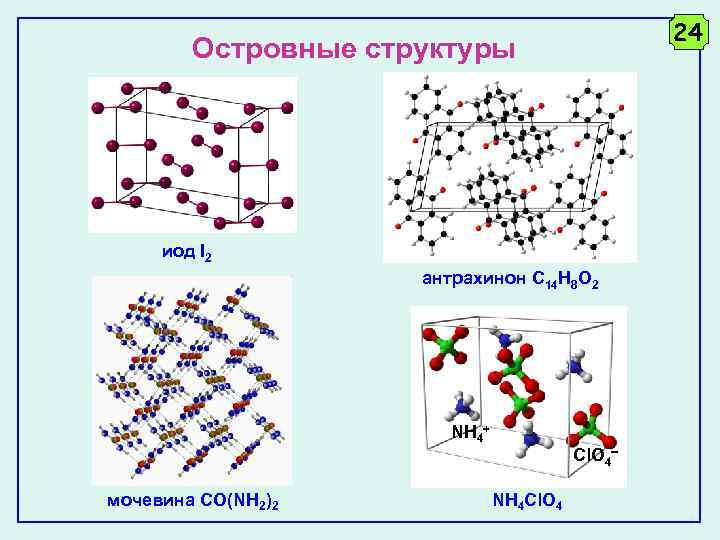 24 Островные структуры иод I 2 антрахинон C 14 H 8 O 2 NH 4+ мочевина CO(NH 2)2 Cl. O 4 NH 4 Cl. O 4
24 Островные структуры иод I 2 антрахинон C 14 H 8 O 2 NH 4+ мочевина CO(NH 2)2 Cl. O 4 NH 4 Cl. O 4
![Цепочечные структуры 25 Be Cl серый селен [Si. O 3] Be. Cl 2 Mg. Цепочечные структуры 25 Be Cl серый селен [Si. O 3] Be. Cl 2 Mg.](https://present5.com/presentation/5652994_169311216/image-25.jpg) Цепочечные структуры 25 Be Cl серый селен [Si. O 3] Be. Cl 2 Mg. O 6 одиночные цепочки [Si. O 3] в энстатите Mg. Si. O 3 двойные цепочки (ленты) [Si 4 O 11] в тремолите Ca 2 Mg 5 Si 8 O 22(OH)2
Цепочечные структуры 25 Be Cl серый селен [Si. O 3] Be. Cl 2 Mg. O 6 одиночные цепочки [Si. O 3] в энстатите Mg. Si. O 3 двойные цепочки (ленты) [Si 4 O 11] в тремолите Ca 2 Mg 5 Si 8 O 22(OH)2
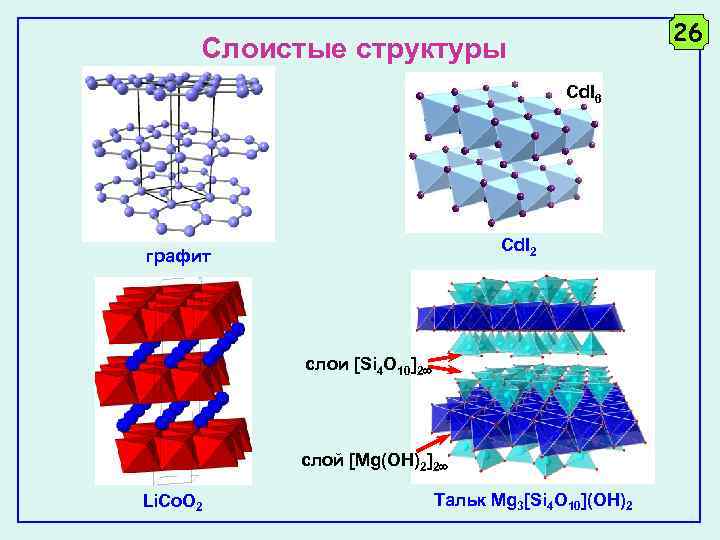 26 Слоистые структуры Cd. I 6 Cd. I 2 графит слои [Si 4 O 10]2 слой [Mg(OH)2]2 Li. Co. O 2 Тальк Mg 3[Si 4 O 10](OH)2
26 Слоистые структуры Cd. I 6 Cd. I 2 графит слои [Si 4 O 10]2 слой [Mg(OH)2]2 Li. Co. O 2 Тальк Mg 3[Si 4 O 10](OH)2
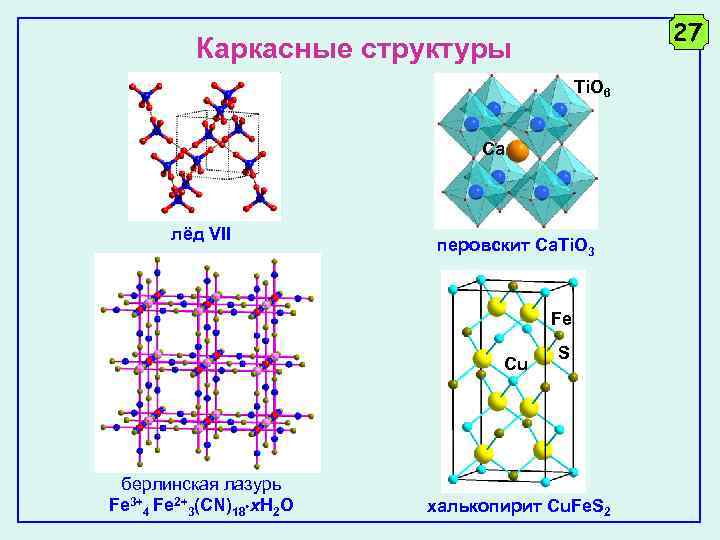 27 Каркасные структуры Ti. O 6 Ca лёд VII перовскит Ca. Ti. O 3 Fe Cu берлинская лазурь Fe 3+4 Fe 2+3(CN)18 x. H 2 O S халькопирит Cu. Fe. S 2
27 Каркасные структуры Ti. O 6 Ca лёд VII перовскит Ca. Ti. O 3 Fe Cu берлинская лазурь Fe 3+4 Fe 2+3(CN)18 x. H 2 O S халькопирит Cu. Fe. S 2
 Литература 28 1. Бокий Г. Б. Кристаллохимия. М. : Наука, 1971. 2. Современная кристаллография / Под ред. Б. К. Вайнштейна. М. : Наука, 1979. Т. 2. 3. Пенкаля Т. Очерки кристаллохимии. Л. : Химия, 1974. 4. Солодовников С. Ф. Основы кристаллохимии. Справочно-методические материалы к курсу. Новосибирск: НГУ, 2007. 5. Солодовников С. Ф. Основные термины и понятия структурной кристаллографии и кристаллохимии. Словарь-пособие. Новосибирск: ИНХ СО РАН, 2005. 6. Солодовников С. Ф. Основы кристаллохимии. Учебное пособие. Новосибирск: НГУ, 2012. Последние три пособия можно найти на сайте кафедры неорганической химии ФЕН НГУ: http: //icchair. niic. nsc. ru/ полезные файлы.
Литература 28 1. Бокий Г. Б. Кристаллохимия. М. : Наука, 1971. 2. Современная кристаллография / Под ред. Б. К. Вайнштейна. М. : Наука, 1979. Т. 2. 3. Пенкаля Т. Очерки кристаллохимии. Л. : Химия, 1974. 4. Солодовников С. Ф. Основы кристаллохимии. Справочно-методические материалы к курсу. Новосибирск: НГУ, 2007. 5. Солодовников С. Ф. Основные термины и понятия структурной кристаллографии и кристаллохимии. Словарь-пособие. Новосибирск: ИНХ СО РАН, 2005. 6. Солодовников С. Ф. Основы кристаллохимии. Учебное пособие. Новосибирск: НГУ, 2012. Последние три пособия можно найти на сайте кафедры неорганической химии ФЕН НГУ: http: //icchair. niic. nsc. ru/ полезные файлы.


