Lecture5_2013.ppt
- Количество слайдов: 25
 1 Лекция 5 1. Основные структурные параметры и основные стереохимические характеристики структуры. 2. Координационное число и координационные многогранники. 3. Упорядоченные, дефектные и разупорядоченные структуры. 4. Собственная симметрия координационных полиэдров, молекул и сложных ионов. 5. Структурный тип. Изоструктурность (изотипность), антиизоструктурность, гомеотипия, гетеротипия.
1 Лекция 5 1. Основные структурные параметры и основные стереохимические характеристики структуры. 2. Координационное число и координационные многогранники. 3. Упорядоченные, дефектные и разупорядоченные структуры. 4. Собственная симметрия координационных полиэдров, молекул и сложных ионов. 5. Структурный тип. Изоструктурность (изотипность), антиизоструктурность, гомеотипия, гетеротипия.
 Основные структурные параметры 2 Основными структурными параметрами можно назвать данные, однозначно описывающие кристаллическую структуру: – параметры решетки и пространственная группа, – координаты базисных атомов, – параметры тепловых колебаний базисных атомов: изотропные (сферически симметричные, 1 параметр/атом) или анизотропные (эллипсоидальные, 6 параметров/атом), – коэффициенты заполнения (заселенности) позиций: указывают проценты заселенности каждым сортом атомов. Эти данные являются исходными для вычисления всех нужных нам геометрических характеристик структуры и без них невозможно провести дальнейший анализ: определить ближайшее и более удаленное окружение каждого атома, выделить слагающие кристалл частицы (ионы, молекулы и более сложные образования) и выяснить их взаимное расположение.
Основные структурные параметры 2 Основными структурными параметрами можно назвать данные, однозначно описывающие кристаллическую структуру: – параметры решетки и пространственная группа, – координаты базисных атомов, – параметры тепловых колебаний базисных атомов: изотропные (сферически симметричные, 1 параметр/атом) или анизотропные (эллипсоидальные, 6 параметров/атом), – коэффициенты заполнения (заселенности) позиций: указывают проценты заселенности каждым сортом атомов. Эти данные являются исходными для вычисления всех нужных нам геометрических характеристик структуры и без них невозможно провести дальнейший анализ: определить ближайшее и более удаленное окружение каждого атома, выделить слагающие кристалл частицы (ионы, молекулы и более сложные образования) и выяснить их взаимное расположение.
 Основные структурные параметры 3 Структура твёрдого раствора Cd 0, 8 Mn 0, 2 S S (Cd, Mn) Атом (ПСТ) КР / СП Cd/Mn S Гексагональная сингония, a = 4. 1038(2); c = 6. 6588(2) Å параметры решётки Пр. гр. P 63 mc, Z = 2, R = 0. 061 Параметры: симметрия число R-фактор 1 – координатный, 1 – заселенность, формульных 2 – колебания единиц Координаты базисного атома Заселен. Параметр ность колебаний, Å2 x/a y/b z/c 2 / 3 m 1/3 2/3 0. 375(1) 0. 8/0. 2 2. 6(1) 2 / 3 m 1/3 2/3 0 1 2. 6(1) одна степень фиксированы (не уточняются) свободы уточняются (переменные)
Основные структурные параметры 3 Структура твёрдого раствора Cd 0, 8 Mn 0, 2 S S (Cd, Mn) Атом (ПСТ) КР / СП Cd/Mn S Гексагональная сингония, a = 4. 1038(2); c = 6. 6588(2) Å параметры решётки Пр. гр. P 63 mc, Z = 2, R = 0. 061 Параметры: симметрия число R-фактор 1 – координатный, 1 – заселенность, формульных 2 – колебания единиц Координаты базисного атома Заселен. Параметр ность колебаний, Å2 x/a y/b z/c 2 / 3 m 1/3 2/3 0. 375(1) 0. 8/0. 2 2. 6(1) 2 / 3 m 1/3 2/3 0 1 2. 6(1) одна степень фиксированы (не уточняются) свободы уточняются (переменные)
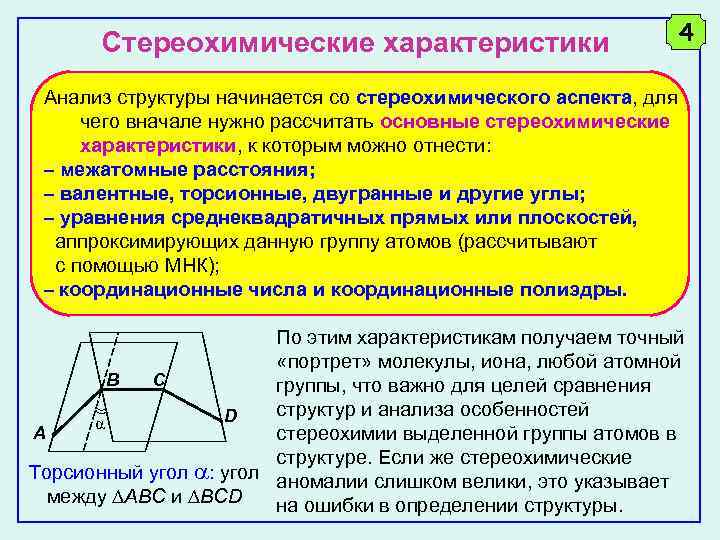 Стереохимические характеристики 4 Анализ структуры начинается со стереохимического аспекта, для чего вначале нужно рассчитать основные стереохимические характеристики, к которым можно отнести: – межатомные расстояния; – валентные, торсионные, двугранные и другие углы; – уравнения среднеквадратичных прямых или плоскостей, аппроксимирующих данную группу атомов (рассчитывают с помощью МНК); – координационные числа и координационные полиэдры. По этим характеристикам получаем точный «портрет» молекулы, иона, любой атомной B C группы, что важно для целей сравнения структур и анализа особенностей D α A стереохимии выделенной группы атомов в структуре. Если же стереохимические Торсионный угол : угол аномалии слишком велики, это указывает между ABC и BCD на ошибки в определении структуры.
Стереохимические характеристики 4 Анализ структуры начинается со стереохимического аспекта, для чего вначале нужно рассчитать основные стереохимические характеристики, к которым можно отнести: – межатомные расстояния; – валентные, торсионные, двугранные и другие углы; – уравнения среднеквадратичных прямых или плоскостей, аппроксимирующих данную группу атомов (рассчитывают с помощью МНК); – координационные числа и координационные полиэдры. По этим характеристикам получаем точный «портрет» молекулы, иона, любой атомной B C группы, что важно для целей сравнения структур и анализа особенностей D α A стереохимии выделенной группы атомов в структуре. Если же стереохимические Торсионный угол : угол аномалии слишком велики, это указывает между ABC и BCD на ошибки в определении структуры.
 Координационное число 5 Координационное число – число ближайших соседних атомов, окружающих данный атом (А. Вернер, 1893). Кроме ближайших соседей – первой координационной сферы можно рассматривать вторую, третью координационную сферы и т. д. КЧ определить довольно просто, если все расстояния до ближайших соседей примерно одинаковы. В более сложных структурах КЧ можно определить по разрыву в последовательности межатомных расстояний, в наиболее трудных случаях используют дополнительные графические или аналитические приемы. Если ближайшие соседи располагаются вокруг центрального атома неравномерно, образуя группы близких расстояний, по числу их значений в каждой группе пишут КЧ = 4 + 2, 8 + 6, 2 + 2 и т. д. Какими бывают координационные числа? КЧ = 0 в твердом теле практически недостижимо, поэтому минимальное КЧ = 1 (как для атома Н в углеводородах), а наибольшие КЧ могут достигать значений 20, 24 и даже выше (в интерметаллических соединениях).
Координационное число 5 Координационное число – число ближайших соседних атомов, окружающих данный атом (А. Вернер, 1893). Кроме ближайших соседей – первой координационной сферы можно рассматривать вторую, третью координационную сферы и т. д. КЧ определить довольно просто, если все расстояния до ближайших соседей примерно одинаковы. В более сложных структурах КЧ можно определить по разрыву в последовательности межатомных расстояний, в наиболее трудных случаях используют дополнительные графические или аналитические приемы. Если ближайшие соседи располагаются вокруг центрального атома неравномерно, образуя группы близких расстояний, по числу их значений в каждой группе пишут КЧ = 4 + 2, 8 + 6, 2 + 2 и т. д. Какими бывают координационные числа? КЧ = 0 в твердом теле практически недостижимо, поэтому минимальное КЧ = 1 (как для атома Н в углеводородах), а наибольшие КЧ могут достигать значений 20, 24 и даже выше (в интерметаллических соединениях).
 Координационный полиэдр 6 Координационный полиэдр – замкнутый выпуклый многогранник, вершинами которого являются ближайшие к данному атому соседние атомы (лиганды). Число вершин такого полиэдра всегда равно координационному числу. Для КЧ = 1, 2, 3 полиэдр из координационной сферы не получится, т. к. в любом полиэдре не менее 4 вершин. Многогранник может не получиться, если все атомы первой координационной сферы компланарны или расположены по одну сторону от центрального атома (такую конфигурацию называют зонтичной). В других случаях вокруг центрального атома можно построить замкнутый выпуклый многогранник (многовершинник), который характеризуется числом граней или вершин (КЧ), а также своей формой. Числа вершин v, ребер e и граней f выпуклого полиэдра связаны формулой Эйлера: v + f = e + 2.
Координационный полиэдр 6 Координационный полиэдр – замкнутый выпуклый многогранник, вершинами которого являются ближайшие к данному атому соседние атомы (лиганды). Число вершин такого полиэдра всегда равно координационному числу. Для КЧ = 1, 2, 3 полиэдр из координационной сферы не получится, т. к. в любом полиэдре не менее 4 вершин. Многогранник может не получиться, если все атомы первой координационной сферы компланарны или расположены по одну сторону от центрального атома (такую конфигурацию называют зонтичной). В других случаях вокруг центрального атома можно построить замкнутый выпуклый многогранник (многовершинник), который характеризуется числом граней или вершин (КЧ), а также своей формой. Числа вершин v, ребер e и граней f выпуклого полиэдра связаны формулой Эйлера: v + f = e + 2.
 Примеры координационных полиэдров тетраэдр Для большинства полиэдров характерны треугольные или четырёхугольные грани. Самыми распространенными полиэдрами являются тетраэдр и октаэдр 7
Примеры координационных полиэдров тетраэдр Для большинства полиэдров характерны треугольные или четырёхугольные грани. Самыми распространенными полиэдрами являются тетраэдр и октаэдр 7
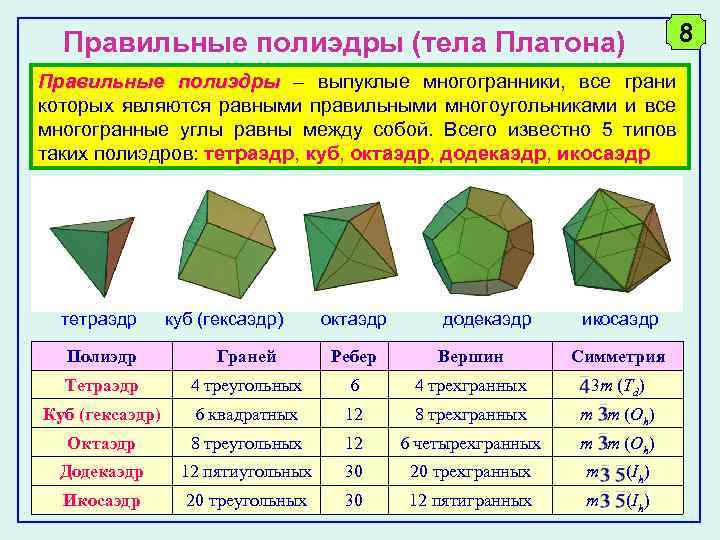 8 Правильные полиэдры (тела Платона) Правильные полиэдры – выпуклые многогранники, все грани полиэдры которых являются равными правильными многоугольниками и все многогранные углы равны между собой. Всего известно 5 типов таких полиэдров: тетраэдр, куб, октаэдр, додекаэдр, икосаэдр тетраэдр куб (гексаэдр) октаэдр додекаэдр икосаэдр Полиэдр Граней Ребер Вершин Симметрия Тетраэдр 4 треугольных 6 4 трехгранных 3 m (Td) Куб (гексаэдр) 6 квадратных 12 8 трехгранных m m (Oh) Октаэдр 8 треугольных 12 6 четырехгранных m m (Oh) Додекаэдр 12 пятиугольных 30 20 трехгранных m (Ih) Икосаэдр 20 треугольных 30 12 пятигранных m (Ih)
8 Правильные полиэдры (тела Платона) Правильные полиэдры – выпуклые многогранники, все грани полиэдры которых являются равными правильными многоугольниками и все многогранные углы равны между собой. Всего известно 5 типов таких полиэдров: тетраэдр, куб, октаэдр, додекаэдр, икосаэдр тетраэдр куб (гексаэдр) октаэдр додекаэдр икосаэдр Полиэдр Граней Ребер Вершин Симметрия Тетраэдр 4 треугольных 6 4 трехгранных 3 m (Td) Куб (гексаэдр) 6 квадратных 12 8 трехгранных m m (Oh) Октаэдр 8 треугольных 12 6 четырехгранных m m (Oh) Додекаэдр 12 пятиугольных 30 20 трехгранных m (Ih) Икосаэдр 20 треугольных 30 12 пятигранных m (Ih)
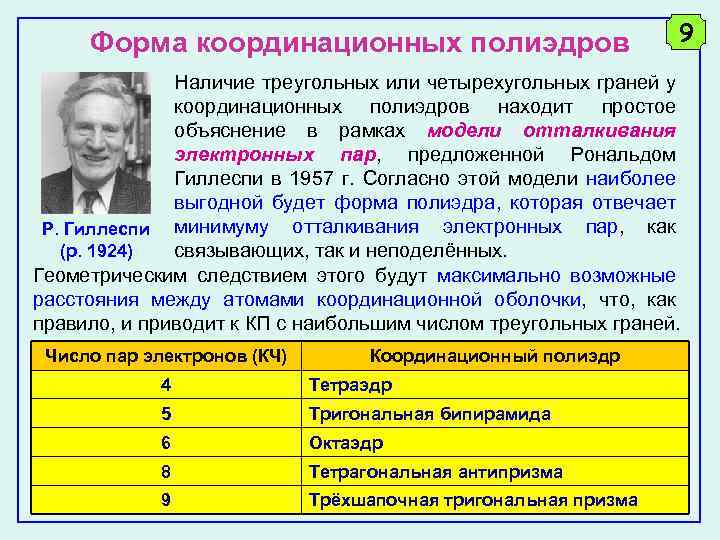 Форма координационных полиэдров 9 Наличие треугольных или четырехугольных граней у координационных полиэдров находит простое объяснение в рамках модели отталкивания электронных пар, предложенной Рональдом Гиллеспи в 1957 г. Согласно этой модели наиболее выгодной будет форма полиэдра, которая отвечает Р. Гиллеспи минимуму отталкивания электронных пар, как (р. 1924) связывающих, так и неподелённых. Геометрическим следствием этого будут максимально возможные расстояния между атомами координационной оболочки, что, как правило, и приводит к КП с наибольшим числом треугольных граней. Число пар электронов (КЧ) Координационный полиэдр 4 Тетраэдр 5 Тригональная бипирамида 6 Октаэдр 8 Тетрагональная антипризма 9 Трёхшапочная тригональная призма
Форма координационных полиэдров 9 Наличие треугольных или четырехугольных граней у координационных полиэдров находит простое объяснение в рамках модели отталкивания электронных пар, предложенной Рональдом Гиллеспи в 1957 г. Согласно этой модели наиболее выгодной будет форма полиэдра, которая отвечает Р. Гиллеспи минимуму отталкивания электронных пар, как (р. 1924) связывающих, так и неподелённых. Геометрическим следствием этого будут максимально возможные расстояния между атомами координационной оболочки, что, как правило, и приводит к КП с наибольшим числом треугольных граней. Число пар электронов (КЧ) Координационный полиэдр 4 Тетраэдр 5 Тригональная бипирамида 6 Октаэдр 8 Тетрагональная антипризма 9 Трёхшапочная тригональная призма
 Тепловое движение атомов 10 Параметры тепловых колебаний атомов сигнализируют о правильности учета поглощения и самой модели структуры. Параметры изотропных тепловых колебаний должны быть положительными, а параметры анизотропных тепловых колебаний должны приводить к эллипсоидам, а не к открытым поверхностям второго порядка. Тепловые параметры свидетельствуют о динамике структуры. Длинные полуоси эллипсоидов тепловых колебаний обычно перпендикулярны химическим связям, а их объем возрастает с возрастанием теплового движения, которое обычно выше на периферии молекулы, иона или комплекса. Повышенное тепловое движение приводит к сильно вытянутым или сплюснутым эллипсоидам тепловых колебаний.
Тепловое движение атомов 10 Параметры тепловых колебаний атомов сигнализируют о правильности учета поглощения и самой модели структуры. Параметры изотропных тепловых колебаний должны быть положительными, а параметры анизотропных тепловых колебаний должны приводить к эллипсоидам, а не к открытым поверхностям второго порядка. Тепловые параметры свидетельствуют о динамике структуры. Длинные полуоси эллипсоидов тепловых колебаний обычно перпендикулярны химическим связям, а их объем возрастает с возрастанием теплового движения, которое обычно выше на периферии молекулы, иона или комплекса. Повышенное тепловое движение приводит к сильно вытянутым или сплюснутым эллипсоидам тепловых колебаний.
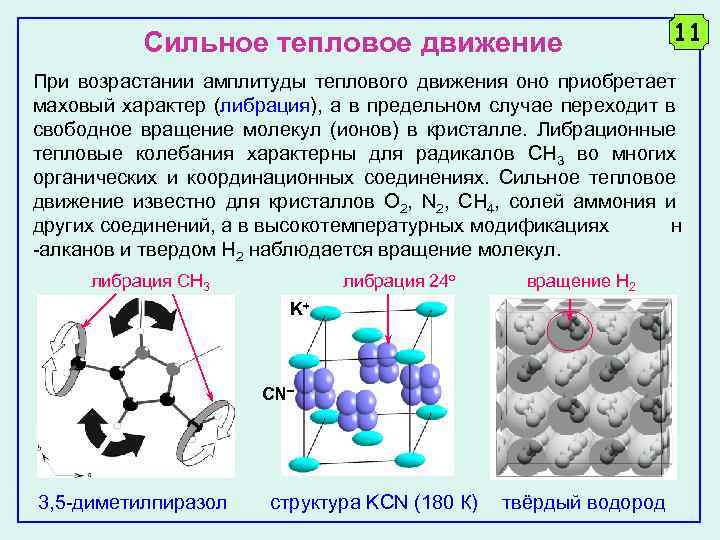 Сильное тепловое движение 11 При возрастании амплитуды теплового движения оно приобретает маховый характер (либрация), а в предельном случае переходит в свободное вращение молекул (ионов) в кристалле. Либрационные тепловые колебания характерны для радикалов CH 3 во многих органических и координационных соединениях. Сильное тепловое движение известно для кристаллов O 2, N 2, CH 4, солей аммония и других соединений, а в высокотемпературных модификациях н -алканов и твердом H 2 наблюдается вращение молекул. либрация CH 3 либрация 24 о вращение H 2 K+ CN 3, 5 -диметилпиразол структура KCN (180 К) твёрдый водород
Сильное тепловое движение 11 При возрастании амплитуды теплового движения оно приобретает маховый характер (либрация), а в предельном случае переходит в свободное вращение молекул (ионов) в кристалле. Либрационные тепловые колебания характерны для радикалов CH 3 во многих органических и координационных соединениях. Сильное тепловое движение известно для кристаллов O 2, N 2, CH 4, солей аммония и других соединений, а в высокотемпературных модификациях н -алканов и твердом H 2 наблюдается вращение молекул. либрация CH 3 либрация 24 о вращение H 2 K+ CN 3, 5 -диметилпиразол структура KCN (180 К) твёрдый водород
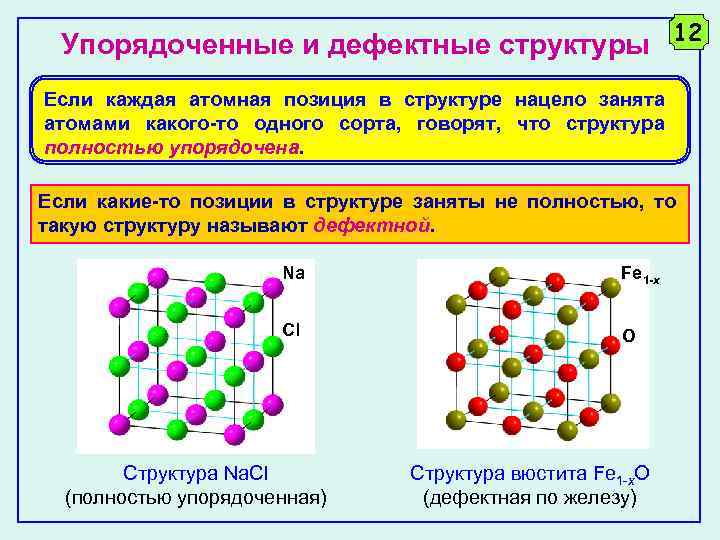 Упорядоченные и дефектные структуры 12 Если каждая атомная позиция в структуре нацело занята атомами какого-то одного сорта, говорят, что структура полностью упорядочена. Если какие-то позиции в структуре заняты не полностью, то такую структуру называют дефектной. Na Fe 1 -x Cl O Структура Na. Cl (полностью упорядоченная) Структура вюстита Fe 1 -x. O (дефектная по железу)
Упорядоченные и дефектные структуры 12 Если каждая атомная позиция в структуре нацело занята атомами какого-то одного сорта, говорят, что структура полностью упорядочена. Если какие-то позиции в структуре заняты не полностью, то такую структуру называют дефектной. Na Fe 1 -x Cl O Структура Na. Cl (полностью упорядоченная) Структура вюстита Fe 1 -x. O (дефектная по железу)
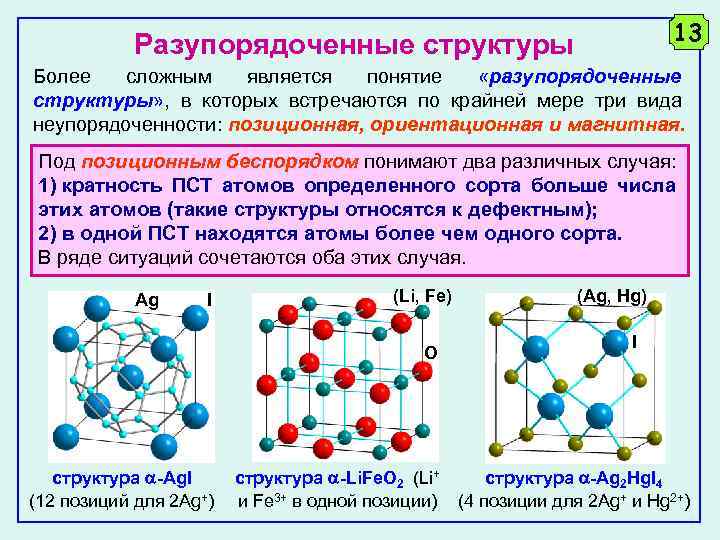 13 Разупорядоченные структуры Более сложным является понятие «разупорядоченные структуры» , в которых встречаются по крайней мере три вида неупорядоченности: позиционная, ориентационная и магнитная. Под позиционным беспорядком понимают два различных случая: 1) кратность ПСТ атомов определенного сорта больше числа этих атомов (такие структуры относятся к дефектным); 2) в одной ПСТ находятся атомы более чем одного сорта. В ряде ситуаций сочетаются оба этих случая. Ag I (Li, Fe) O (Ag, Hg) I структура -Ag. I структура -Li. Fe. O 2 (Li+ структура -Ag 2 Hg. I 4 (12 позиций для 2 Ag+) и Fe 3+ в одной позиции) (4 позиции для 2 Ag+ и Hg 2+)
13 Разупорядоченные структуры Более сложным является понятие «разупорядоченные структуры» , в которых встречаются по крайней мере три вида неупорядоченности: позиционная, ориентационная и магнитная. Под позиционным беспорядком понимают два различных случая: 1) кратность ПСТ атомов определенного сорта больше числа этих атомов (такие структуры относятся к дефектным); 2) в одной ПСТ находятся атомы более чем одного сорта. В ряде ситуаций сочетаются оба этих случая. Ag I (Li, Fe) O (Ag, Hg) I структура -Ag. I структура -Li. Fe. O 2 (Li+ структура -Ag 2 Hg. I 4 (12 позиций для 2 Ag+) и Fe 3+ в одной позиции) (4 позиции для 2 Ag+ и Hg 2+)
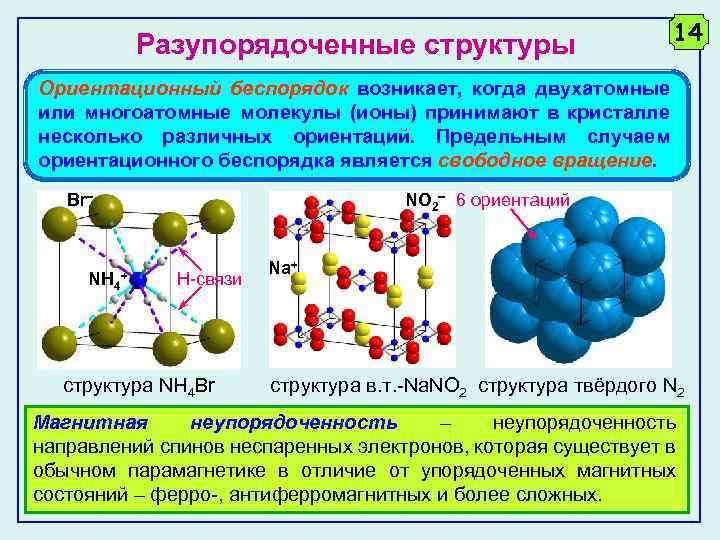 14 Разупорядоченные структуры Ориентационный беспорядок возникает, когда двухатомные или многоатомные молекулы (ионы) принимают в кристалле несколько различных ориентаций. Предельным случаем ориентационного беспорядка является свободное вращение. Br NH 4 NO 2 6 ориентаций + Н-связи cтруктура NH 4 Br Na+ cтруктура в. т. -Na. NO 2 cтруктура твёрдого N 2 Магнитная неупорядоченность – неупорядоченность направлений спинов неспаренных электронов, которая существует в обычном парамагнетике в отличие от упорядоченных магнитных состояний – ферро-, антиферромагнитных и более сложных.
14 Разупорядоченные структуры Ориентационный беспорядок возникает, когда двухатомные или многоатомные молекулы (ионы) принимают в кристалле несколько различных ориентаций. Предельным случаем ориентационного беспорядка является свободное вращение. Br NH 4 NO 2 6 ориентаций + Н-связи cтруктура NH 4 Br Na+ cтруктура в. т. -Na. NO 2 cтруктура твёрдого N 2 Магнитная неупорядоченность – неупорядоченность направлений спинов неспаренных электронов, которая существует в обычном парамагнетике в отличие от упорядоченных магнитных состояний – ферро-, антиферромагнитных и более сложных.
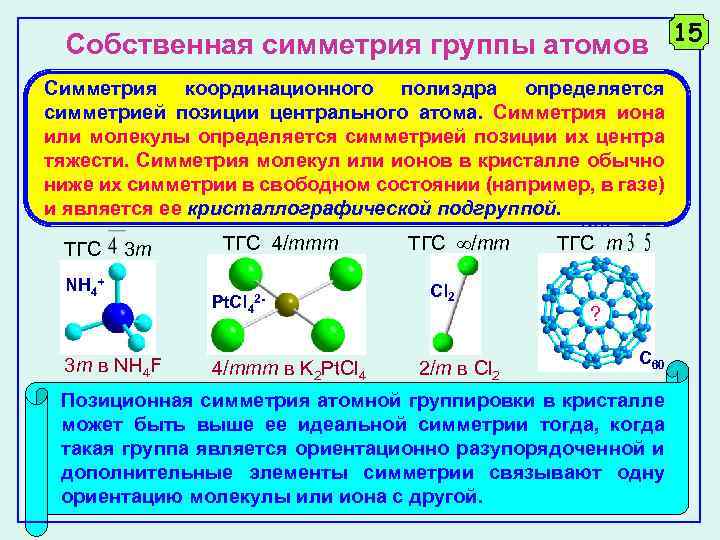 Собственная симметрия группы атомов 15 Симметрия координационного полиэдра определяется симметрией позиции центрального атома. Симметрия иона или молекулы определяется симметрией позиции их центра тяжести. Симметрия молекул или ионов в кристалле обычно ниже их симметрии в свободном состоянии (например, в газе) и является ее кристаллографической подгруппой. ТГС 3 m NH 4+ 3 m в NH 4 F ТГС 4/mmm Pt. Cl 42 - 4/mmm в K 2 Pt. Cl 4 ТГС /mm Cl 2 2/m в Cl 2 ТГС m ? C 60 Позиционная симметрия атомной группировки в кристалле может быть выше ее идеальной симметрии тогда, когда такая группа является ориентационно разупорядоченной и дополнительные элементы симметрии связывают одну ориентацию молекулы или иона с другой.
Собственная симметрия группы атомов 15 Симметрия координационного полиэдра определяется симметрией позиции центрального атома. Симметрия иона или молекулы определяется симметрией позиции их центра тяжести. Симметрия молекул или ионов в кристалле обычно ниже их симметрии в свободном состоянии (например, в газе) и является ее кристаллографической подгруппой. ТГС 3 m NH 4+ 3 m в NH 4 F ТГС 4/mmm Pt. Cl 42 - 4/mmm в K 2 Pt. Cl 4 ТГС /mm Cl 2 2/m в Cl 2 ТГС m ? C 60 Позиционная симметрия атомной группировки в кристалле может быть выше ее идеальной симметрии тогда, когда такая группа является ориентационно разупорядоченной и дополнительные элементы симметрии связывают одну ориентацию молекулы или иона с другой.
 Структурный тип 16 Как сравнивать разные структуры между собой? Говоря о структуре, кристаллохимики оперируют не абсолютными размерами атомных группировок или параметров решетки, а относительными, так как ни форма координационных полиэдров или молекул, ни их взаимное расположение не зависят от масштаба структуры. Отвлекаясь от метрических характеристик структуры и беря только ее топологические характеристики (симметрию структуры, наличие или отсутствие связей, взаимное расположение атомов), говорят о структурном типе кристалла. Структурный тип – вид относительного взаимного расположения атомов в кристалле, который характеризуется: 1) определенной пр. гр. и формой ячейки Браве; 2) определенным набором ПСТ и интервалами координат атомов; 3) определенными КЧ, формой и взаимным расположением материальных частиц.
Структурный тип 16 Как сравнивать разные структуры между собой? Говоря о структуре, кристаллохимики оперируют не абсолютными размерами атомных группировок или параметров решетки, а относительными, так как ни форма координационных полиэдров или молекул, ни их взаимное расположение не зависят от масштаба структуры. Отвлекаясь от метрических характеристик структуры и беря только ее топологические характеристики (симметрию структуры, наличие или отсутствие связей, взаимное расположение атомов), говорят о структурном типе кристалла. Структурный тип – вид относительного взаимного расположения атомов в кристалле, который характеризуется: 1) определенной пр. гр. и формой ячейки Браве; 2) определенным набором ПСТ и интервалами координат атомов; 3) определенными КЧ, формой и взаимным расположением материальных частиц.
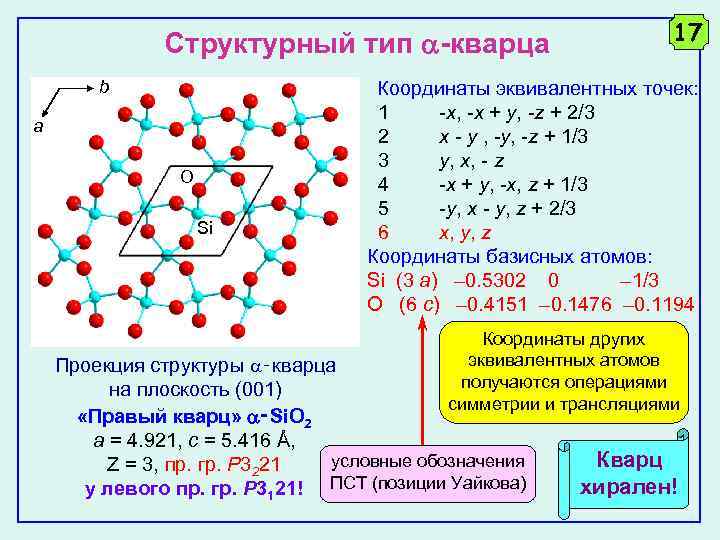 Структурный тип -кварца b 17 Координаты эквивалентных точек: a O Si 1 -x, -x + y, -z + 2/3 2 x - y , -y, -z + 1/3 3 y, x, - z 4 -x + y, -x, z + 1/3 5 -y, x - y, z + 2/3 6 x, y, z Координаты базисных атомов: Si (3 a) – 0. 5302 0 – 1/3 O (6 c) – 0. 4151 – 0. 1476 – 0. 1194 Координаты других эквивалентных атомов получаются операциями симметрии и трансляциями Проекция структуры ‑кварца на плоскость (001) «Правый кварц» ‑Si. O 2 a = 4. 921, c = 5. 416 Å, условные обозначения Z = 3, пр. гр. P 3221 у левого пр. гр. P 3121! ПСТ (позиции Уайкова) Кварц хирален!
Структурный тип -кварца b 17 Координаты эквивалентных точек: a O Si 1 -x, -x + y, -z + 2/3 2 x - y , -y, -z + 1/3 3 y, x, - z 4 -x + y, -x, z + 1/3 5 -y, x - y, z + 2/3 6 x, y, z Координаты базисных атомов: Si (3 a) – 0. 5302 0 – 1/3 O (6 c) – 0. 4151 – 0. 1476 – 0. 1194 Координаты других эквивалентных атомов получаются операциями симметрии и трансляциями Проекция структуры ‑кварца на плоскость (001) «Правый кварц» ‑Si. O 2 a = 4. 921, c = 5. 416 Å, условные обозначения Z = 3, пр. гр. P 3221 у левого пр. гр. P 3121! ПСТ (позиции Уайкова) Кварц хирален!
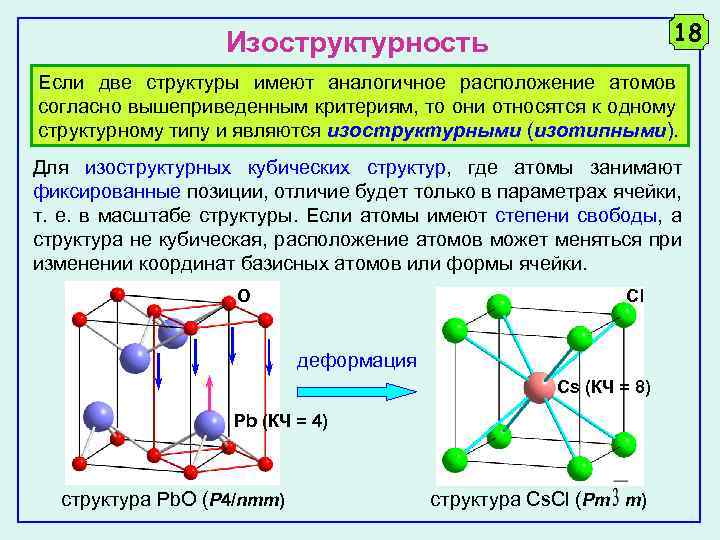 18 Изоструктурность Если две структуры имеют аналогичное расположение атомов согласно вышеприведенным критериям, то они относятся к одному структурному типу и являются изоструктурными (изотипными). Для изоструктурных кубических структур, где атомы занимают фиксированные позиции, отличие будет только в параметрах ячейки, т. е. в масштабе структуры. Если атомы имеют степени свободы, а структура не кубическая, расположение атомов может меняться при изменении координат базисных атомов или формы ячейки. O Cl деформация Cs (КЧ = 8) Pb (КЧ = 4) cтруктура Pb. O (P 4/nmm) cтруктура Cs. Cl (Pm m)
18 Изоструктурность Если две структуры имеют аналогичное расположение атомов согласно вышеприведенным критериям, то они относятся к одному структурному типу и являются изоструктурными (изотипными). Для изоструктурных кубических структур, где атомы занимают фиксированные позиции, отличие будет только в параметрах ячейки, т. е. в масштабе структуры. Если атомы имеют степени свободы, а структура не кубическая, расположение атомов может меняться при изменении координат базисных атомов или формы ячейки. O Cl деформация Cs (КЧ = 8) Pb (КЧ = 4) cтруктура Pb. O (P 4/nmm) cтруктура Cs. Cl (Pm m)
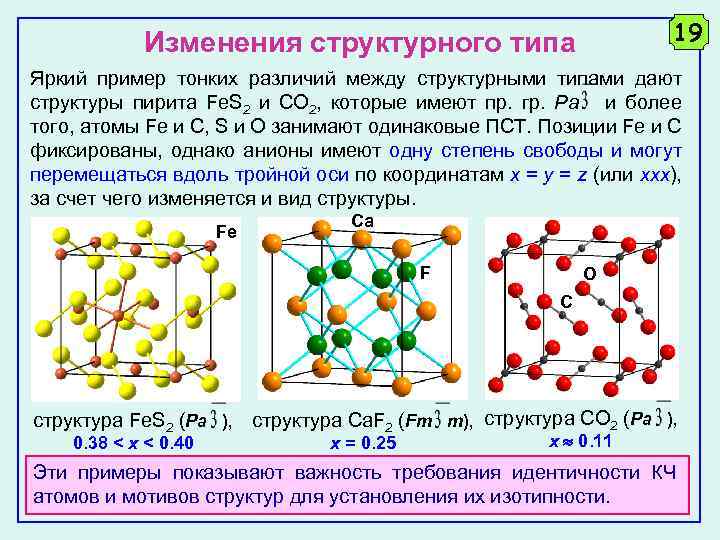 19 Изменения структурного типа Яркий пример тонких различий между структурными типами дают структуры пирита Fe. S 2 и CO 2, которые имеют пр. гр. Pa и более того, атомы Fe и C, S и O занимают одинаковые ПСТ. Позиции Fe и C фиксированы, однако анионы имеют одну степень свободы и могут перемещаться вдоль тройной оси по координатам x = y = z (или xxx), за счет чего изменяется и вид структуры. Fe Ca F O C cтруктура Fe. S 2 (Pa ), cтруктура Ca. F 2 (Fm m), cтруктура CO 2 (Pa ), 0. 38 < x < 0. 40 x = 0. 25 x 0. 11 Эти примеры показывают важность требования идентичности КЧ атомов и мотивов структур для установления их изотипности.
19 Изменения структурного типа Яркий пример тонких различий между структурными типами дают структуры пирита Fe. S 2 и CO 2, которые имеют пр. гр. Pa и более того, атомы Fe и C, S и O занимают одинаковые ПСТ. Позиции Fe и C фиксированы, однако анионы имеют одну степень свободы и могут перемещаться вдоль тройной оси по координатам x = y = z (или xxx), за счет чего изменяется и вид структуры. Fe Ca F O C cтруктура Fe. S 2 (Pa ), cтруктура Ca. F 2 (Fm m), cтруктура CO 2 (Pa ), 0. 38 < x < 0. 40 x = 0. 25 x 0. 11 Эти примеры показывают важность требования идентичности КЧ атомов и мотивов структур для установления их изотипности.
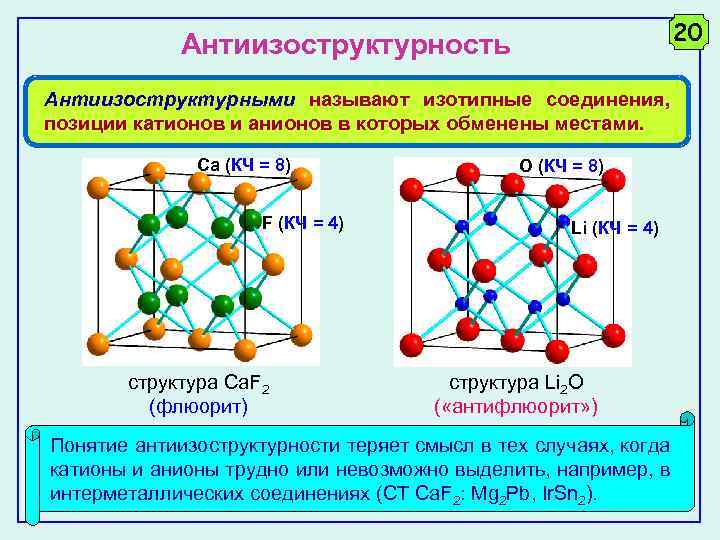 20 Антиизоструктурность Антиизоструктурными называют изотипные соединения, позиции катионов и анионов в которых обменены местами. Ca (КЧ = 8) F (КЧ = 4) cтруктура Ca. F 2 (флюорит) O (КЧ = 8) Li (КЧ = 4) cтруктура Li 2 O ( «антифлюорит» ) Понятие антиизоструктурности теряет смысл в тех случаях, когда катионы и анионы трудно или невозможно выделить, например, в интерметаллических соединениях (CT Ca. F 2: Mg 2 Pb, Ir. Sn 2).
20 Антиизоструктурность Антиизоструктурными называют изотипные соединения, позиции катионов и анионов в которых обменены местами. Ca (КЧ = 8) F (КЧ = 4) cтруктура Ca. F 2 (флюорит) O (КЧ = 8) Li (КЧ = 4) cтруктура Li 2 O ( «антифлюорит» ) Понятие антиизоструктурности теряет смысл в тех случаях, когда катионы и анионы трудно или невозможно выделить, например, в интерметаллических соединениях (CT Ca. F 2: Mg 2 Pb, Ir. Sn 2).
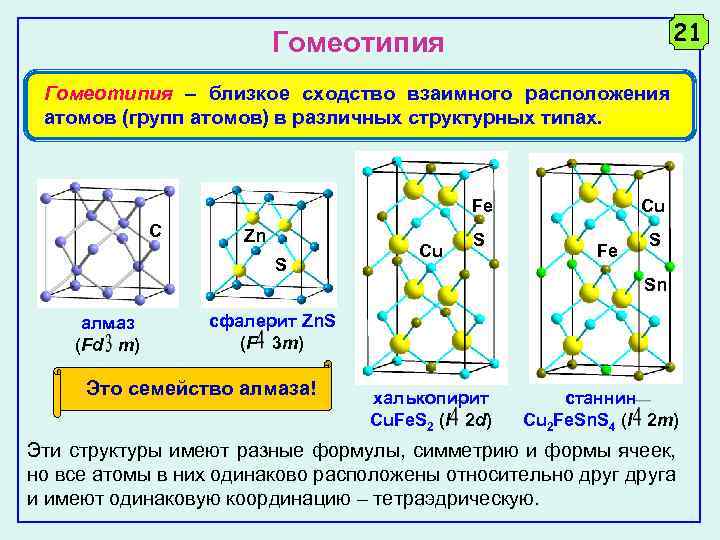 21 Гомеотипия – близкое сходство взаимного расположения атомов (групп атомов) в различных структурных типах. Fe C Zn S Cu Fe S Sn алмаз (Fd m) сфалерит Zn. S (F 3 m) Это семейство алмаза! халькопирит Cu. Fe. S 2 (I 2 d) станнин Cu 2 Fe. Sn. S 4 (I 2 m) Эти структуры имеют разные формулы, симметрию и формы ячеек, но все атомы в них одинаково расположены относительно друга и имеют одинаковую координацию – тетраэдрическую.
21 Гомеотипия – близкое сходство взаимного расположения атомов (групп атомов) в различных структурных типах. Fe C Zn S Cu Fe S Sn алмаз (Fd m) сфалерит Zn. S (F 3 m) Это семейство алмаза! халькопирит Cu. Fe. S 2 (I 2 d) станнин Cu 2 Fe. Sn. S 4 (I 2 m) Эти структуры имеют разные формулы, симметрию и формы ячеек, но все атомы в них одинаково расположены относительно друга и имеют одинаковую координацию – тетраэдрическую.
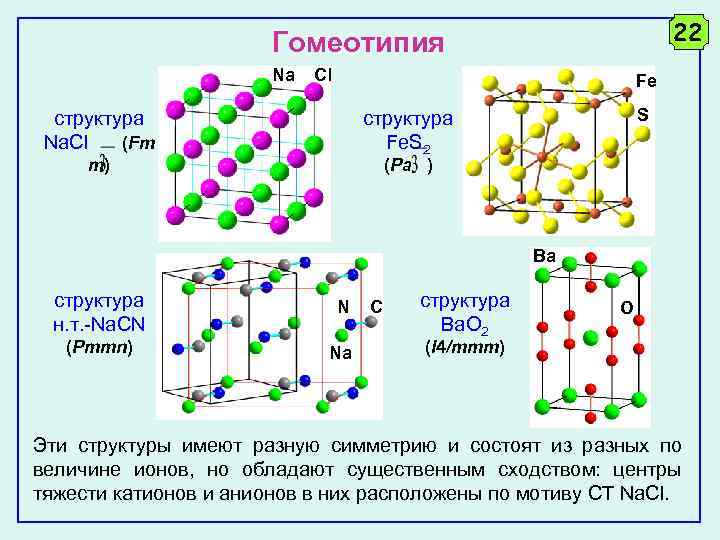 22 Гомеотипия Na Cl Fe cтруктура Na. Cl (Fm S cтруктура Fe. S 2 m) (Pa ) Ba cтруктура н. т. -Na. CN (Pmmn) N Na C cтруктура Ba. O 2 O (I 4/mmm) Эти структуры имеют разную симметрию и состоят из разных по величине ионов, но обладают существенным сходством: центры тяжести катионов и анионов в них расположены по мотиву CТ Na. Cl.
22 Гомеотипия Na Cl Fe cтруктура Na. Cl (Fm S cтруктура Fe. S 2 m) (Pa ) Ba cтруктура н. т. -Na. CN (Pmmn) N Na C cтруктура Ba. O 2 O (I 4/mmm) Эти структуры имеют разную симметрию и состоят из разных по величине ионов, но обладают существенным сходством: центры тяжести катионов и анионов в них расположены по мотиву CТ Na. Cl.
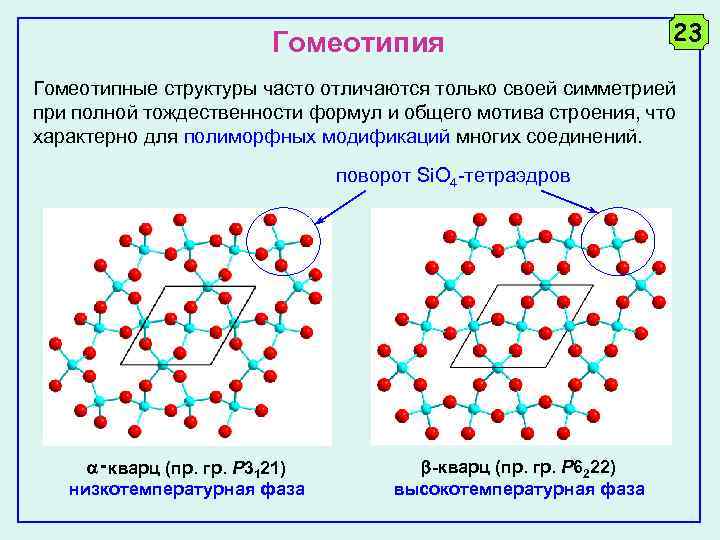 Гомеотипия 23 Гомеотипные структуры часто отличаются только своей симметрией при полной тождественности формул и общего мотива строения, что характерно для полиморфных модификаций многих соединений. поворот Si. O 4 -тетраэдров ‑кварц (пр. гр. P 3121) низкотемпературная фаза -кварц (пр. гр. P 6222) высокотемпературная фаза
Гомеотипия 23 Гомеотипные структуры часто отличаются только своей симметрией при полной тождественности формул и общего мотива строения, что характерно для полиморфных модификаций многих соединений. поворот Si. O 4 -тетраэдров ‑кварц (пр. гр. P 3121) низкотемпературная фаза -кварц (пр. гр. P 6222) высокотемпературная фаза
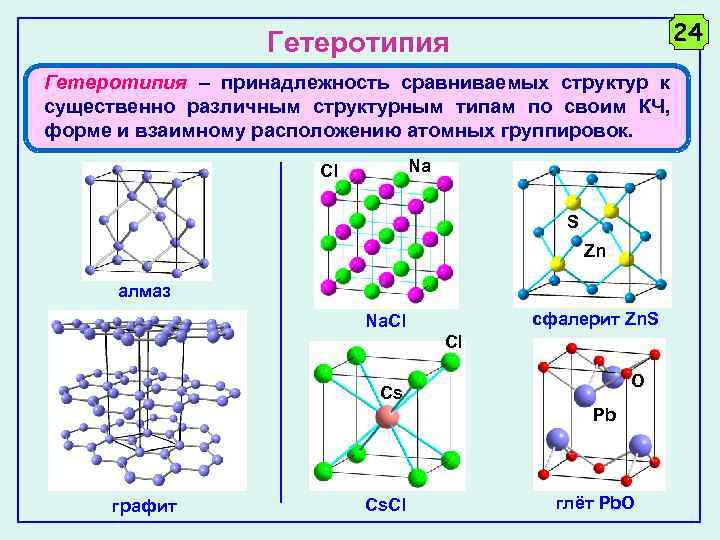 24 Гетеротипия – принадлежность сравниваемых структур к существенно различным структурным типам по своим КЧ, форме и взаимному расположению атомных группировок. Na Cl S Zn алмаз сфалерит Zn. S Na. Cl Cl O Cs Pb графит Cs. Cl глёт Pb. O
24 Гетеротипия – принадлежность сравниваемых структур к существенно различным структурным типам по своим КЧ, форме и взаимному расположению атомных группировок. Na Cl S Zn алмаз сфалерит Zn. S Na. Cl Cl O Cs Pb графит Cs. Cl глёт Pb. O
 Литература 25 1. Бокий Г. Б. Кристаллохимия. М. : Наука, 1971. 2. Современная кристаллография / Под ред. Б. К. Вайнштейна. М. : Наука, 1979. Т. 2. 3. Пенкаля Т. Очерки кристаллохимии. Л. : Химия, 1974. 4. Солодовников С. Ф. Основы кристаллохимии. Справочно-методические материалы к курсу. Новосибирск: НГУ, 2007. 5. Солодовников С. Ф. Основные термины и понятия структурной кристаллографии и кристаллохимии. Словарь-пособие. Новосибирск: ИНХ СО РАН, 2005. 6. Солодовников С. Ф. Основы кристаллохимии. Учебное пособие. Новосибирск: НГУ, 2012. Последние три пособия можно найти на сайте кафедры неорганической химии ФЕН НГУ: http: //icchair. niic. nsc. ru/ полезные файлы.
Литература 25 1. Бокий Г. Б. Кристаллохимия. М. : Наука, 1971. 2. Современная кристаллография / Под ред. Б. К. Вайнштейна. М. : Наука, 1979. Т. 2. 3. Пенкаля Т. Очерки кристаллохимии. Л. : Химия, 1974. 4. Солодовников С. Ф. Основы кристаллохимии. Справочно-методические материалы к курсу. Новосибирск: НГУ, 2007. 5. Солодовников С. Ф. Основные термины и понятия структурной кристаллографии и кристаллохимии. Словарь-пособие. Новосибирск: ИНХ СО РАН, 2005. 6. Солодовников С. Ф. Основы кристаллохимии. Учебное пособие. Новосибирск: НГУ, 2012. Последние три пособия можно найти на сайте кафедры неорганической химии ФЕН НГУ: http: //icchair. niic. nsc. ru/ полезные файлы.


