Lecture10_2013.ppt
- Количество слайдов: 31
 1 Лекция 10 1. Важнейшие структуры простых веществ – металлов и неметаллов. 2. Стехиометрическая классификация структур. Символ Пирсона. 3. Основные структурные типы бинарных соединений. 4. Структуры простых и сложных оксидов. 5. Силикаты. Фазы кремнезёма. Стишовит. 6. Структуры простых и сложных сульфидов.
1 Лекция 10 1. Важнейшие структуры простых веществ – металлов и неметаллов. 2. Стехиометрическая классификация структур. Символ Пирсона. 3. Основные структурные типы бинарных соединений. 4. Структуры простых и сложных оксидов. 5. Силикаты. Фазы кремнезёма. Стишовит. 6. Структуры простых и сложных сульфидов.
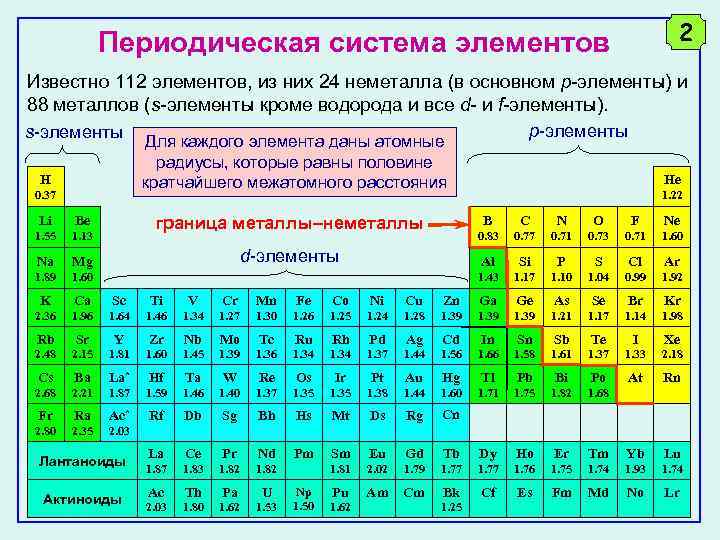 2 Периодическая система элементов Известно 112 элементов, из них 24 неметалла (в основном p-элементы) и 88 металлов (s-элементы кроме водорода и все d- и f-элементы). s-элементы H 0. 37 p-элементы Для каждого элемента даны атомные радиусы, которые равны половине кратчайшего межатомного расстояния граница металлы–неметаллы Li Be 1. 55 1. 13 Na Mg 1. 89 1. 60 K Ca Sc Ti V Cr Mn Fe Co Ni Cu 2. 36 1. 96 1. 64 1. 46 1. 34 1. 27 1. 30 1. 26 1. 25 1. 24 Rb Sr Y Zr Nb Mo Tc Ru Rh 2. 48 2. 15 1. 81 1. 60 1. 45 1. 39 1. 36 1. 34 Cs Ba La* Hf Ta W Re 2. 68 2. 21 1. 87 1. 59 1. 46 1. 40 Fr Ra Ac* Rf Db 2. 80 2. 35 2. 03 He 1. 22 B C N O F Ne 0. 83 0. 77 0. 71 0. 73 0. 71 1. 60 Al Si P S Cl Ar 1. 43 1. 17 1. 10 1. 04 0. 99 1. 92 Zn Ga Ge As Se Br Kr 1. 28 1. 39 1. 21 1. 17 1. 14 1. 98 Pd Ag Cd In Sn Sb Te I Xe 1. 34 1. 37 1. 44 1. 56 1. 66 1. 58 1. 61 1. 37 1. 33 2. 18 Os Ir Pt Au Hg Tl Pb Bi Po At Rn 1. 37 1. 35 1. 38 1. 44 1. 60 1. 71 1. 75 1. 82 1. 68 Sg Bh Hs Mt Ds Rg Cn La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu 1. 87 1. 83 1. 82 1. 81 2. 02 1. 79 1. 77 1. 76 1. 75 1. 74 1. 93 1. 74 Ac Th Pa U Pu Am Cm Bk Cf Es Fm Md No Lr 2. 03 1. 80 1. 62 1. 53 d-элементы Лантаноиды Актиноиды Np 1. 50 1. 62 1. 25
2 Периодическая система элементов Известно 112 элементов, из них 24 неметалла (в основном p-элементы) и 88 металлов (s-элементы кроме водорода и все d- и f-элементы). s-элементы H 0. 37 p-элементы Для каждого элемента даны атомные радиусы, которые равны половине кратчайшего межатомного расстояния граница металлы–неметаллы Li Be 1. 55 1. 13 Na Mg 1. 89 1. 60 K Ca Sc Ti V Cr Mn Fe Co Ni Cu 2. 36 1. 96 1. 64 1. 46 1. 34 1. 27 1. 30 1. 26 1. 25 1. 24 Rb Sr Y Zr Nb Mo Tc Ru Rh 2. 48 2. 15 1. 81 1. 60 1. 45 1. 39 1. 36 1. 34 Cs Ba La* Hf Ta W Re 2. 68 2. 21 1. 87 1. 59 1. 46 1. 40 Fr Ra Ac* Rf Db 2. 80 2. 35 2. 03 He 1. 22 B C N O F Ne 0. 83 0. 77 0. 71 0. 73 0. 71 1. 60 Al Si P S Cl Ar 1. 43 1. 17 1. 10 1. 04 0. 99 1. 92 Zn Ga Ge As Se Br Kr 1. 28 1. 39 1. 21 1. 17 1. 14 1. 98 Pd Ag Cd In Sn Sb Te I Xe 1. 34 1. 37 1. 44 1. 56 1. 66 1. 58 1. 61 1. 37 1. 33 2. 18 Os Ir Pt Au Hg Tl Pb Bi Po At Rn 1. 37 1. 35 1. 38 1. 44 1. 60 1. 71 1. 75 1. 82 1. 68 Sg Bh Hs Mt Ds Rg Cn La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu 1. 87 1. 83 1. 82 1. 81 2. 02 1. 79 1. 77 1. 76 1. 75 1. 74 1. 93 1. 74 Ac Th Pa U Pu Am Cm Bk Cf Es Fm Md No Lr 2. 03 1. 80 1. 62 1. 53 d-элементы Лантаноиды Актиноиды Np 1. 50 1. 62 1. 25
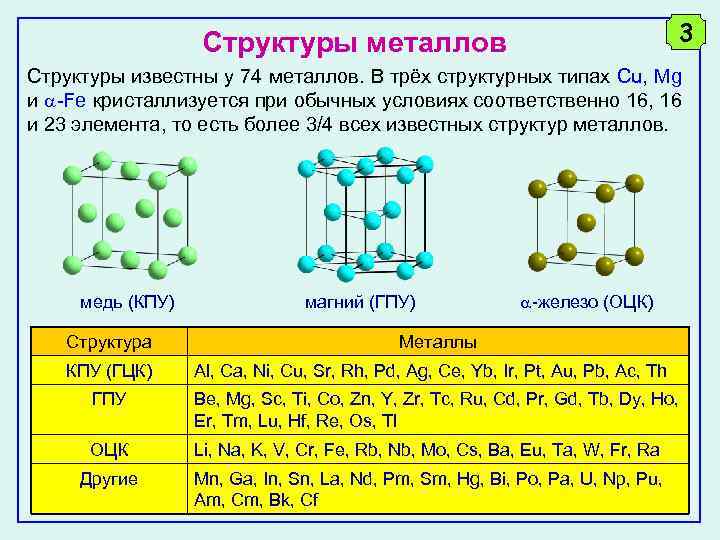 3 Структуры металлов Структуры известны у 74 металлов. В трёх структурных типах Cu, Mg и -Fe кристаллизуется при обычных условиях соответственно 16, 16 и 23 элемента, то есть более 3/4 всех известных структур металлов. медь (КПУ) Структура КПУ (ГЦК) магний (ГПУ) -железо (ОЦК) Металлы Al, Ca, Ni, Cu, Sr, Rh, Pd, Ag, Ce, Yb, Ir, Pt, Au, Pb, Ac, Th ГПУ Be, Mg, Sc, Ti, Co, Zn, Y, Zr, Tc, Ru, Cd, Pr, Gd, Tb, Dy, Ho, Er, Tm, Lu, Hf, Re, Os, Tl ОЦК Li, Na, K, V, Cr, Fe, Rb, Nb, Mo, Cs, Ba, Eu, Ta, W, Fr, Ra Другие Mn, Ga, In, Sn, La, Nd, Pm, Sm, Hg, Bi, Po, Pa, U, Np, Pu, Am, Cm, Bk, Cf
3 Структуры металлов Структуры известны у 74 металлов. В трёх структурных типах Cu, Mg и -Fe кристаллизуется при обычных условиях соответственно 16, 16 и 23 элемента, то есть более 3/4 всех известных структур металлов. медь (КПУ) Структура КПУ (ГЦК) магний (ГПУ) -железо (ОЦК) Металлы Al, Ca, Ni, Cu, Sr, Rh, Pd, Ag, Ce, Yb, Ir, Pt, Au, Pb, Ac, Th ГПУ Be, Mg, Sc, Ti, Co, Zn, Y, Zr, Tc, Ru, Cd, Pr, Gd, Tb, Dy, Ho, Er, Tm, Lu, Hf, Re, Os, Tl ОЦК Li, Na, K, V, Cr, Fe, Rb, Nb, Mo, Cs, Ba, Eu, Ta, W, Fr, Ra Другие Mn, Ga, In, Sn, La, Nd, Pm, Sm, Hg, Bi, Po, Pa, U, Np, Pu, Am, Cm, Bk, Cf
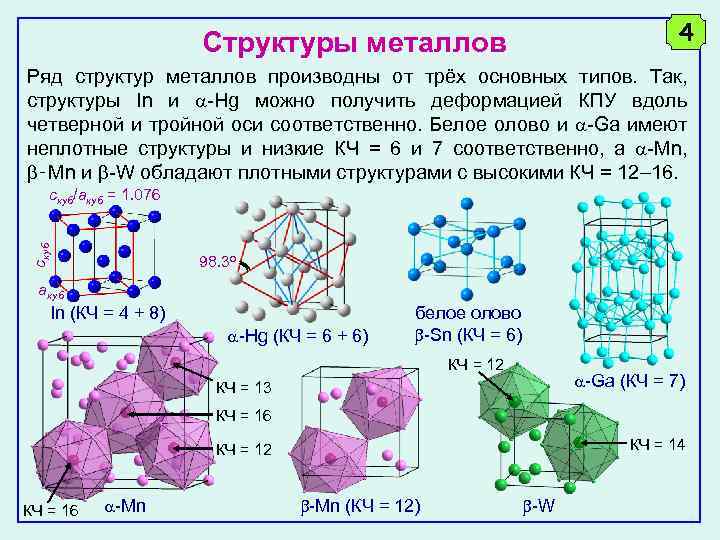 4 Структуры металлов Ряд структур металлов производны от трёх основных типов. Так, структуры In и -Hg можно получить деформацией КПУ вдоль четверной и тройной оси соответственно. Белое олово и -Ga имеют неплотные структуры и низкие КЧ = 6 и 7 соответственно, а -Mn, ‑Mn и -W обладают плотными структурами с высокими КЧ = 12 16. cкуб скуб/акуб = 1. 076 98. 3 o aкуб In (КЧ = 4 + 8) -Hg (КЧ = 6 + 6) белое олово -Sn (КЧ = 6) КЧ = 12 -Ga (КЧ = 7) КЧ = 13 КЧ = 16 КЧ = 14 КЧ = 12 КЧ = 16 -Mn (КЧ = 12) -W
4 Структуры металлов Ряд структур металлов производны от трёх основных типов. Так, структуры In и -Hg можно получить деформацией КПУ вдоль четверной и тройной оси соответственно. Белое олово и -Ga имеют неплотные структуры и низкие КЧ = 6 и 7 соответственно, а -Mn, ‑Mn и -W обладают плотными структурами с высокими КЧ = 12 16. cкуб скуб/акуб = 1. 076 98. 3 o aкуб In (КЧ = 4 + 8) -Hg (КЧ = 6 + 6) белое олово -Sn (КЧ = 6) КЧ = 12 -Ga (КЧ = 7) КЧ = 13 КЧ = 16 КЧ = 14 КЧ = 12 КЧ = 16 -Mn (КЧ = 12) -W
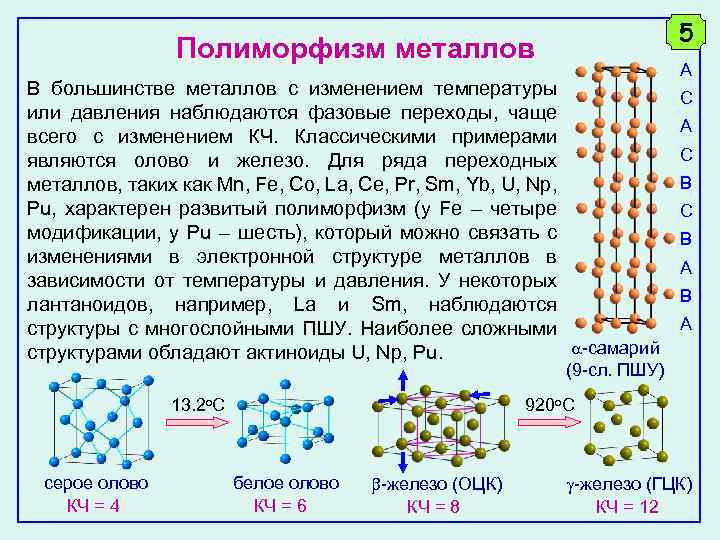 5 Полиморфизм металлов А В большинстве металлов с изменением температуры С или давления наблюдаются фазовые переходы, чаще А всего с изменением КЧ. Классическими примерами С являются олово и железо. Для ряда переходных В металлов, таких как Mn, Fe, Co, La, Ce, Pr, Sm, Yb, U, Np, Pu, характерен развитый полиморфизм (у Fe – четыре С модификации, у Pu – шесть), который можно связать с В изменениями в электронной структуре металлов в А зависимости от температуры и давления. У некоторых В лантаноидов, например, La и Sm, наблюдаются А структуры с многослойными ПШУ. Наиболее сложными -самарий структурами обладают актиноиды U, Np, Pu. (9 -сл. ПШУ) 920 o. C 13. 2 o. C серое олово КЧ = 4 белое олово КЧ = 6 -железо (ОЦК) КЧ = 8 -железо (ГЦК) КЧ = 12
5 Полиморфизм металлов А В большинстве металлов с изменением температуры С или давления наблюдаются фазовые переходы, чаще А всего с изменением КЧ. Классическими примерами С являются олово и железо. Для ряда переходных В металлов, таких как Mn, Fe, Co, La, Ce, Pr, Sm, Yb, U, Np, Pu, характерен развитый полиморфизм (у Fe – четыре С модификации, у Pu – шесть), который можно связать с В изменениями в электронной структуре металлов в А зависимости от температуры и давления. У некоторых В лантаноидов, например, La и Sm, наблюдаются А структуры с многослойными ПШУ. Наиболее сложными -самарий структурами обладают актиноиды U, Np, Pu. (9 -сл. ПШУ) 920 o. C 13. 2 o. C серое олово КЧ = 4 белое олово КЧ = 6 -железо (ОЦК) КЧ = 8 -железо (ГЦК) КЧ = 12
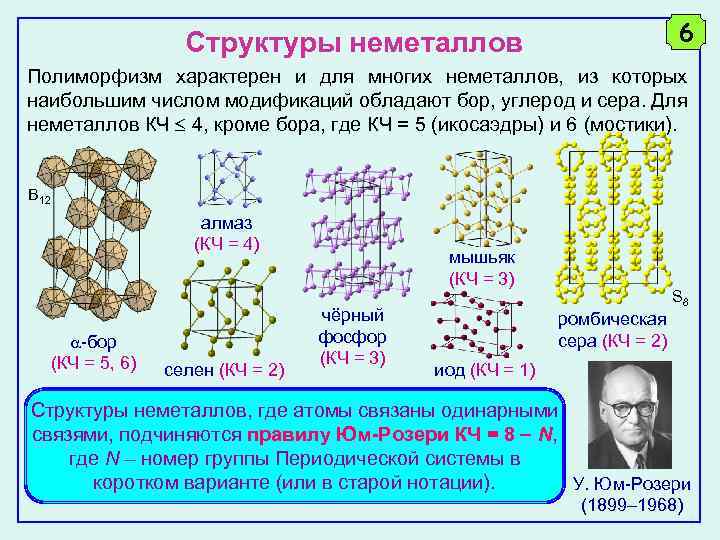 6 Структуры неметаллов Полиморфизм характерен и для многих неметаллов, из которых наибольшим числом модификаций обладают бор, углерод и сера. Для неметаллов КЧ 4, кроме бора, где КЧ = 5 (икосаэдры) и 6 (мостики). B 12 алмаз (КЧ = 4) -бор (КЧ = 5, 6) селен (КЧ = 2) мышьяк (КЧ = 3) чёрный фосфор (КЧ = 3) S 8 ромбическая сера (КЧ = 2) иод (КЧ = 1) Структуры неметаллов, где атомы связаны одинарными связями, подчиняются правилу Юм-Розери КЧ = 8 N, где N – номер группы Периодической системы в коротком варианте (или в старой нотации). У. Юм-Розери (1899– 1968)
6 Структуры неметаллов Полиморфизм характерен и для многих неметаллов, из которых наибольшим числом модификаций обладают бор, углерод и сера. Для неметаллов КЧ 4, кроме бора, где КЧ = 5 (икосаэдры) и 6 (мостики). B 12 алмаз (КЧ = 4) -бор (КЧ = 5, 6) селен (КЧ = 2) мышьяк (КЧ = 3) чёрный фосфор (КЧ = 3) S 8 ромбическая сера (КЧ = 2) иод (КЧ = 1) Структуры неметаллов, где атомы связаны одинарными связями, подчиняются правилу Юм-Розери КЧ = 8 N, где N – номер группы Периодической системы в коротком варианте (или в старой нотации). У. Юм-Розери (1899– 1968)
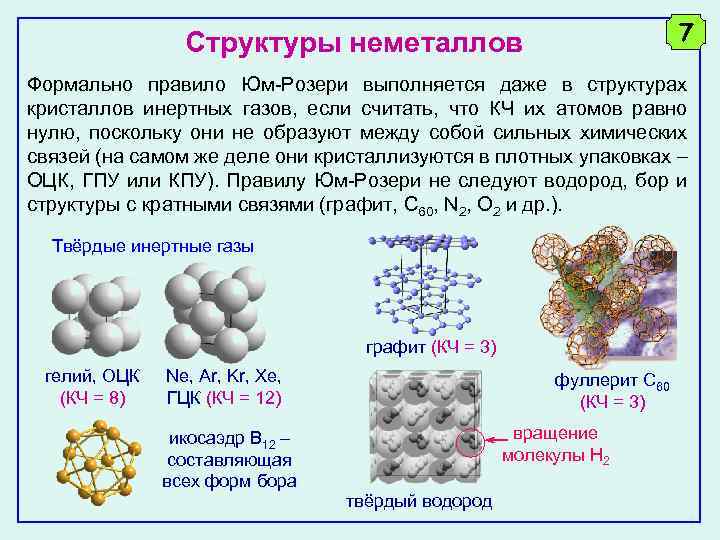 7 Структуры неметаллов Формально правило Юм-Розери выполняется даже в структурах кристаллов инертных газов, если считать, что КЧ их атомов равно нулю, поскольку они не образуют между собой сильных химических связей (на самом же деле они кристаллизуются в плотных упаковках ОЦК, ГПУ или КПУ). Правилу Юм-Розери не следуют водород, бор и структуры с кратными связями (графит, C 60, N 2, O 2 и др. ). Твёрдые инертные газы графит (КЧ = 3) гелий, ОЦК (КЧ = 8) Ne, Ar, Kr, Xe, ГЦК (КЧ = 12) икосаэдр B 12 – составляющая всех форм бора фуллерит C 60 (КЧ = 3) вращение молекулы H 2 твёрдый водород
7 Структуры неметаллов Формально правило Юм-Розери выполняется даже в структурах кристаллов инертных газов, если считать, что КЧ их атомов равно нулю, поскольку они не образуют между собой сильных химических связей (на самом же деле они кристаллизуются в плотных упаковках ОЦК, ГПУ или КПУ). Правилу Юм-Розери не следуют водород, бор и структуры с кратными связями (графит, C 60, N 2, O 2 и др. ). Твёрдые инертные газы графит (КЧ = 3) гелий, ОЦК (КЧ = 8) Ne, Ar, Kr, Xe, ГЦК (КЧ = 12) икосаэдр B 12 – составляющая всех форм бора фуллерит C 60 (КЧ = 3) вращение молекулы H 2 твёрдый водород
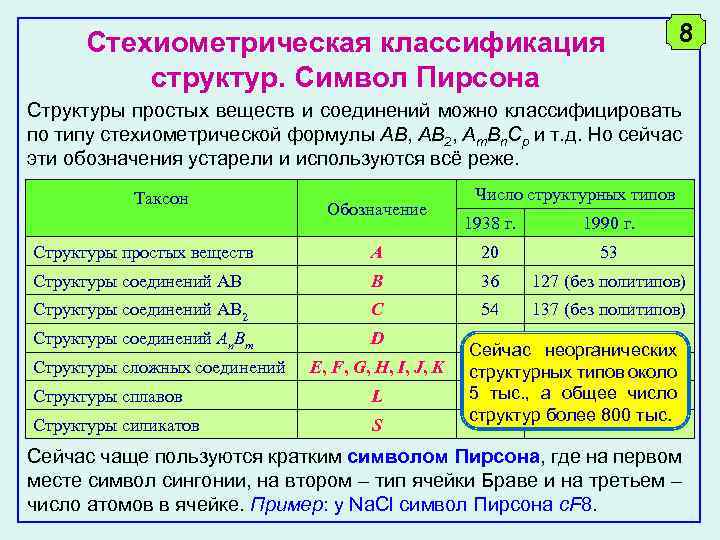 Стехиометрическая классификация структур. Символ Пирсона 8 Структуры простых веществ и соединений можно классифицировать по типу стехиометрической формулы АВ, AB 2, Am. Bn. Cp и т. д. Но сейчас эти обозначения устарели и используются всё реже. Таксон Обозначение Число структурных типов 1938 г. 1990 г. Структуры простых веществ A 20 53 Структуры соединений AB B 36 127 (без политипов) Структуры соединений AB 2 C 54 137 (без политипов) Структуры соединений An. Bm D Структуры сложных соединений E, F, G, H, I, J, K Структуры сплавов L Структуры силикатов S Сейчас неорганических структурных типов около 5 тыс. , а общее число структур более 800 тыс. Сейчас чаще пользуются кратким символом Пирсона, где на первом месте символ сингонии, на втором – тип ячейки Браве и на третьем – число атомов в ячейке. Пример: у Na. Cl символ Пирсона c. F 8.
Стехиометрическая классификация структур. Символ Пирсона 8 Структуры простых веществ и соединений можно классифицировать по типу стехиометрической формулы АВ, AB 2, Am. Bn. Cp и т. д. Но сейчас эти обозначения устарели и используются всё реже. Таксон Обозначение Число структурных типов 1938 г. 1990 г. Структуры простых веществ A 20 53 Структуры соединений AB B 36 127 (без политипов) Структуры соединений AB 2 C 54 137 (без политипов) Структуры соединений An. Bm D Структуры сложных соединений E, F, G, H, I, J, K Структуры сплавов L Структуры силикатов S Сейчас неорганических структурных типов около 5 тыс. , а общее число структур более 800 тыс. Сейчас чаще пользуются кратким символом Пирсона, где на первом месте символ сингонии, на втором – тип ячейки Браве и на третьем – число атомов в ячейке. Пример: у Na. Cl символ Пирсона c. F 8.
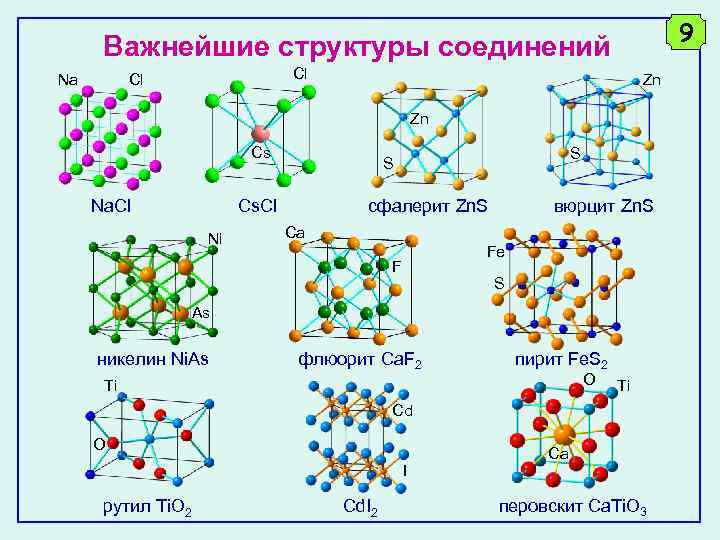 9 Важнейшие структуры соединений Na Cl Cl Zn Zn Cs Na. Cl Cs. Cl Ni S S сфалерит Zn. S вюрцит Zn. S Ca Fe F S As никелин Ni. As флюорит Ca. F 2 пирит Fe. S 2 O Ti Ti Cd O I рутил Ti. O 2 Cd. I 2 Ca перовскит Ca. Ti. O 3
9 Важнейшие структуры соединений Na Cl Cl Zn Zn Cs Na. Cl Cs. Cl Ni S S сфалерит Zn. S вюрцит Zn. S Ca Fe F S As никелин Ni. As флюорит Ca. F 2 пирит Fe. S 2 O Ti Ti Cd O I рутил Ti. O 2 Cd. I 2 Ca перовскит Ca. Ti. O 3
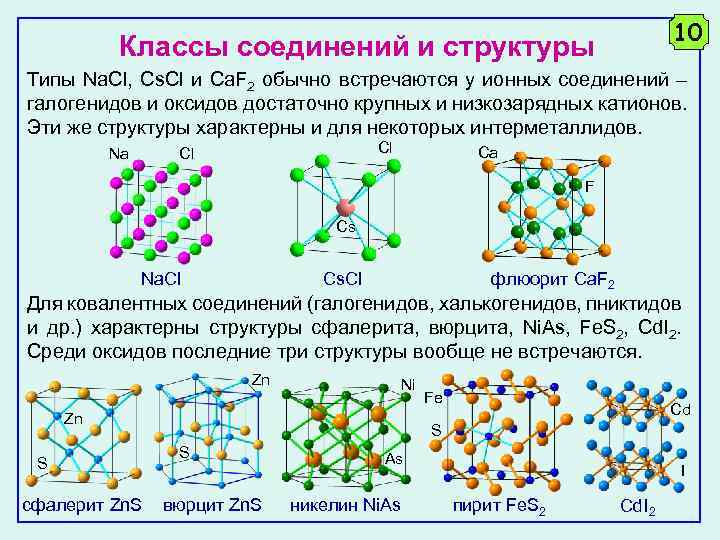 10 Классы соединений и структуры Типы Na. Cl, Cs. Cl и Ca. F 2 обычно встречаются у ионных соединений – галогенидов и оксидов достаточно крупных и низкозарядных катионов. Эти же структуры характерны и для некоторых интерметаллидов. Na Cl Cl Ca F Cs Na. Cl флюорит Ca. F 2 Cs. Cl Для ковалентных соединений (галогенидов, халькогенидов, пниктидов и др. ) характерны структуры сфалерита, вюрцита, Ni. As, Fe. S 2, Cd. I 2. Среди оксидов последние три структуры вообще не встречаются. Zn Ni Zn S сфалерит Zn. S Fe Cd S S вюрцит Zn. S As никелин Ni. As I пирит Fe. S 2 Cd. I 2
10 Классы соединений и структуры Типы Na. Cl, Cs. Cl и Ca. F 2 обычно встречаются у ионных соединений – галогенидов и оксидов достаточно крупных и низкозарядных катионов. Эти же структуры характерны и для некоторых интерметаллидов. Na Cl Cl Ca F Cs Na. Cl флюорит Ca. F 2 Cs. Cl Для ковалентных соединений (галогенидов, халькогенидов, пниктидов и др. ) характерны структуры сфалерита, вюрцита, Ni. As, Fe. S 2, Cd. I 2. Среди оксидов последние три структуры вообще не встречаются. Zn Ni Zn S сфалерит Zn. S Fe Cd S S вюрцит Zn. S As никелин Ni. As I пирит Fe. S 2 Cd. I 2
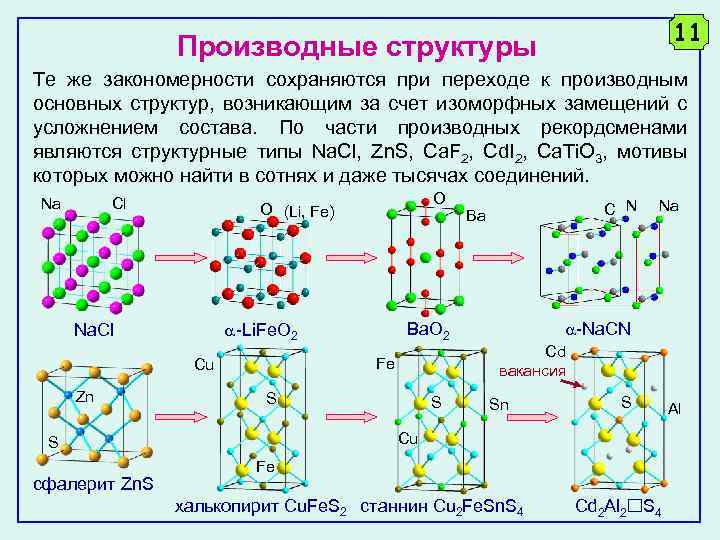 11 Производные структуры Те же закономерности сохраняются при переходе к производным основных структур, возникающим за счет изоморфных замещений с усложнением состава. По части производных рекордсменами являются структурные типы Na. Cl, Zn. S, Ca. F 2, Cd. I 2, Ca. Ti. O 3, мотивы которых можно найти в сотнях и даже тысячах соединений. Na Cl -Li. Fe. O 2 Na. Cl Na -Na. CN Cd вакансия S S Sn S Cu S сфалерит Zn. S C N Ba Ba. O 2 Fe Cu Zn O O (Li, Fe) Fe халькопирит Cu. Fe. S 2 станнин Cu 2 Fe. Sn. S 4 Cd 2 Al 2 S 4 Al
11 Производные структуры Те же закономерности сохраняются при переходе к производным основных структур, возникающим за счет изоморфных замещений с усложнением состава. По части производных рекордсменами являются структурные типы Na. Cl, Zn. S, Ca. F 2, Cd. I 2, Ca. Ti. O 3, мотивы которых можно найти в сотнях и даже тысячах соединений. Na Cl -Li. Fe. O 2 Na. Cl Na -Na. CN Cd вакансия S S Sn S Cu S сфалерит Zn. S C N Ba Ba. O 2 Fe Cu Zn O O (Li, Fe) Fe халькопирит Cu. Fe. S 2 станнин Cu 2 Fe. Sn. S 4 Cd 2 Al 2 S 4 Al
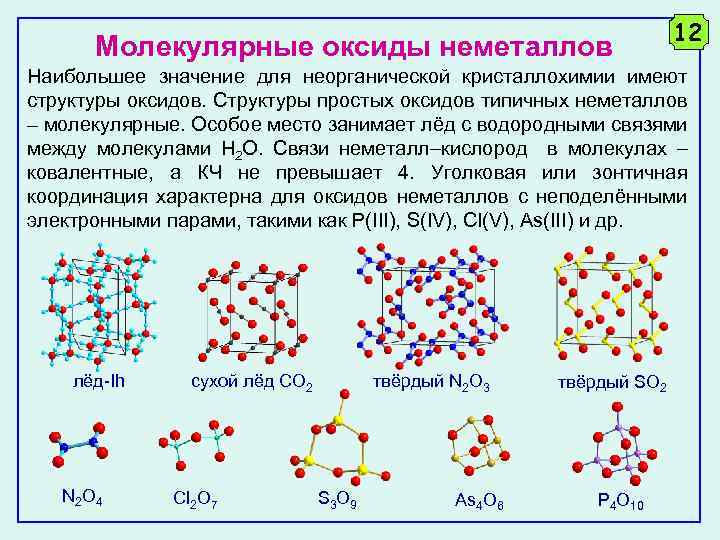 Молекулярные оксиды неметаллов 12 Наибольшее значение для неорганической кристаллохимии имеют структуры оксидов. Структуры простых оксидов типичных неметаллов – молекулярные. Особое место занимает лёд с водородными связями между молекулами H 2 O. Связи неметалл кислород в молекулах ковалентные, а КЧ не превышает 4. Уголковая или зонтичная координация характерна для оксидов неметаллов с неподелёнными электронными парами, такими как P(III), S(IV), Cl(V), As(III) и др. лёд-Ih N 2 O 4 сухой лёд CO 2 Cl 2 O 7 твёрдый N 2 O 3 S 3 O 9 As 4 O 6 твёрдый SO 2 P 4 O 10
Молекулярные оксиды неметаллов 12 Наибольшее значение для неорганической кристаллохимии имеют структуры оксидов. Структуры простых оксидов типичных неметаллов – молекулярные. Особое место занимает лёд с водородными связями между молекулами H 2 O. Связи неметалл кислород в молекулах ковалентные, а КЧ не превышает 4. Уголковая или зонтичная координация характерна для оксидов неметаллов с неподелёнными электронными парами, такими как P(III), S(IV), Cl(V), As(III) и др. лёд-Ih N 2 O 4 сухой лёд CO 2 Cl 2 O 7 твёрдый N 2 O 3 S 3 O 9 As 4 O 6 твёрдый SO 2 P 4 O 10
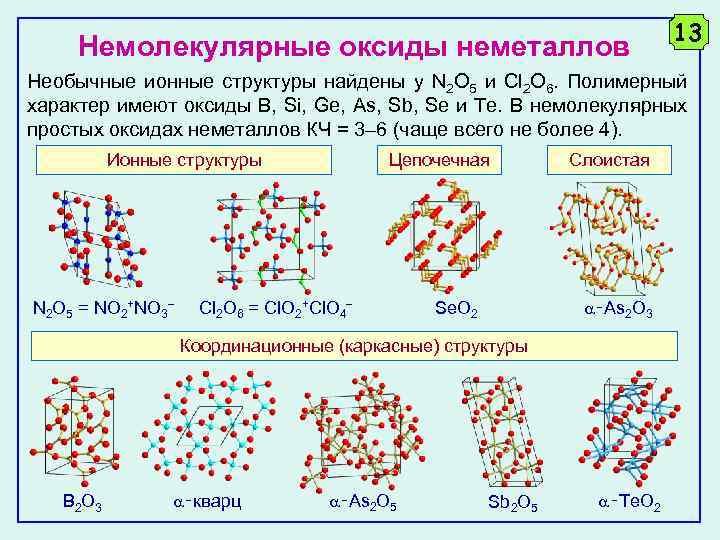 Немолекулярные оксиды неметаллов 13 Необычные ионные структуры найдены у N 2 O 5 и Cl 2 O 6. Полимерный характер имеют оксиды B, Si, Ge, As, Sb, Se и Te. В немолекулярных простых оксидах неметаллов КЧ = 3– 6 (чаще всего не более 4). Ионные структуры N 2 O 5 = NO 2+NO 3 Цепочечная Cl 2 O 6 = Cl. O 2+Cl. O 4 Слоистая ‑As 2 O 3 Se. O 2 Координационные (каркасные) структуры B 2 O 3 ‑кварц ‑As 2 O 5 Sb 2 O 5 ‑Te. O 2
Немолекулярные оксиды неметаллов 13 Необычные ионные структуры найдены у N 2 O 5 и Cl 2 O 6. Полимерный характер имеют оксиды B, Si, Ge, As, Sb, Se и Te. В немолекулярных простых оксидах неметаллов КЧ = 3– 6 (чаще всего не более 4). Ионные структуры N 2 O 5 = NO 2+NO 3 Цепочечная Cl 2 O 6 = Cl. O 2+Cl. O 4 Слоистая ‑As 2 O 3 Se. O 2 Координационные (каркасные) структуры B 2 O 3 ‑кварц ‑As 2 O 5 Sb 2 O 5 ‑Te. O 2
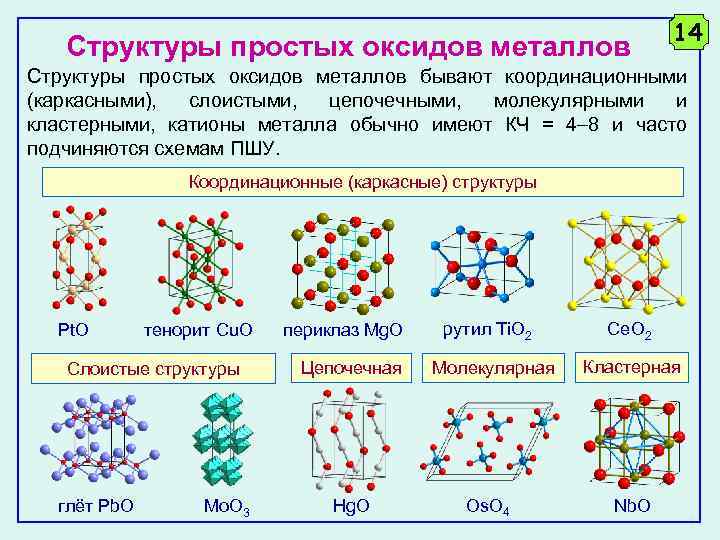 Структуры простых оксидов металлов 14 Структуры простых оксидов металлов бывают координационными (каркасными), слоистыми, цепочечными, молекулярными и кластерными, катионы металла обычно имеют КЧ = 4 8 и часто подчиняются схемам ПШУ. Координационные (каркасные) структуры Pt. O тенорит Cu. O Слоистые структуры глёт Pb. O Mo. O 3 периклаз Mg. O Цепочечная Hg. O рутил Ti. O 2 Молекулярная Os. O 4 Ce. O 2 Кластерная Nb. O
Структуры простых оксидов металлов 14 Структуры простых оксидов металлов бывают координационными (каркасными), слоистыми, цепочечными, молекулярными и кластерными, катионы металла обычно имеют КЧ = 4 8 и часто подчиняются схемам ПШУ. Координационные (каркасные) структуры Pt. O тенорит Cu. O Слоистые структуры глёт Pb. O Mo. O 3 периклаз Mg. O Цепочечная Hg. O рутил Ti. O 2 Молекулярная Os. O 4 Ce. O 2 Кластерная Nb. O
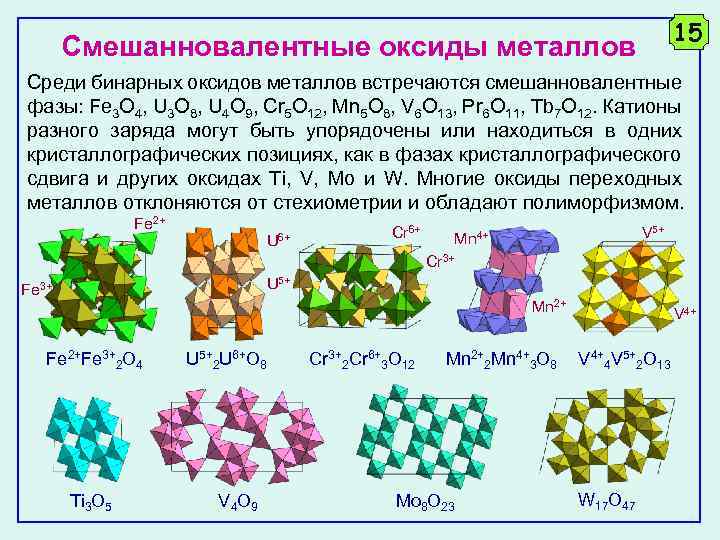 15 Смешанновалентные оксиды металлов Среди бинарных оксидов металлов встречаются смешанновалентные фазы: Fe 3 O 4, U 3 O 8, U 4 O 9, Cr 5 O 12, Mn 5 O 8, V 6 O 13, Pr 6 O 11, Tb 7 O 12. Катионы разного заряда могут быть упорядочены или находиться в одних кристаллографических позициях, как в фазах кристаллографического сдвига и других оксидах Ti, V, Mo и W. Многие оксиды переходных металлов отклоняются от стехиометрии и обладают полиморфизмом. Fe 2+ U 6+ Cr 6+ V 5+ Mn 4+ Cr 3+ U 5+ Fe 3+ Mn 2+ Fe 2+Fe 3+2 O 4 Ti 3 O 5 U 5+2 U 6+O 8 V 4 O 9 Cr 3+2 Cr 6+3 O 12 Mn 2+2 Mn 4+3 O 8 Mo 8 O 23 V 4+4 V 5+2 O 13 W 17 O 47
15 Смешанновалентные оксиды металлов Среди бинарных оксидов металлов встречаются смешанновалентные фазы: Fe 3 O 4, U 3 O 8, U 4 O 9, Cr 5 O 12, Mn 5 O 8, V 6 O 13, Pr 6 O 11, Tb 7 O 12. Катионы разного заряда могут быть упорядочены или находиться в одних кристаллографических позициях, как в фазах кристаллографического сдвига и других оксидах Ti, V, Mo и W. Многие оксиды переходных металлов отклоняются от стехиометрии и обладают полиморфизмом. Fe 2+ U 6+ Cr 6+ V 5+ Mn 4+ Cr 3+ U 5+ Fe 3+ Mn 2+ Fe 2+Fe 3+2 O 4 Ti 3 O 5 U 5+2 U 6+O 8 V 4 O 9 Cr 3+2 Cr 6+3 O 12 Mn 2+2 Mn 4+3 O 8 Mo 8 O 23 V 4+4 V 5+2 O 13 W 17 O 47
 Двойные оксиды металлов 16 Оксиды Ax. By. Oz можно классифицировать по электроотрицательностям элементов А и В. Так как оксидов с двумя электроотрицательными элементами А и В немного, можно выделить две основные группы. 1) Соли оксокислот: А – электроположительный элемент, В – электроотрицательный, катионы An+, анионы [By. Oz]n (обычно островные, реже полимерные), КЧ(А) 6, КЧ(В) 6. Примеры: Na. NO 3, Ba. SO 4, K 2 Cr 2 O 7, Na 5 P 3 O 10, Ag 8[W 4 O 16], Na[PO 3]. 2) Сложные оксиды: А и В – электроположительные элементы, полимерные постройки из связей В–О (КЧ(В) 6), дополненные катионами Аn+ (КЧ(А) 6) или полиэдрами АОn (КЧ(А) КЧ(В)). Примеры: Ca[Ti. O 3]3 , Cs[V 2 O 5]2 , Ba[Ni. O 3] , [Mg. IVAl. VI 2 O 4]3 (шпинель). Промежуточное положение между обеими группами занимают так называемые оксиды-оксосоли, в которых есть либо дискретные ионы О 2 , не связанные с неметаллом, либо устойчивые металлоксидные группировки: Bi 12 O 16(Si. O 4), Fe 3 O 2(BO 3), Cu 2 O(SO 4), Zr 2 O(PO 4)2, Mo. O(PO 4), Pb. O(Mo. O 4), UO 2(SO 4) и др.
Двойные оксиды металлов 16 Оксиды Ax. By. Oz можно классифицировать по электроотрицательностям элементов А и В. Так как оксидов с двумя электроотрицательными элементами А и В немного, можно выделить две основные группы. 1) Соли оксокислот: А – электроположительный элемент, В – электроотрицательный, катионы An+, анионы [By. Oz]n (обычно островные, реже полимерные), КЧ(А) 6, КЧ(В) 6. Примеры: Na. NO 3, Ba. SO 4, K 2 Cr 2 O 7, Na 5 P 3 O 10, Ag 8[W 4 O 16], Na[PO 3]. 2) Сложные оксиды: А и В – электроположительные элементы, полимерные постройки из связей В–О (КЧ(В) 6), дополненные катионами Аn+ (КЧ(А) 6) или полиэдрами АОn (КЧ(А) КЧ(В)). Примеры: Ca[Ti. O 3]3 , Cs[V 2 O 5]2 , Ba[Ni. O 3] , [Mg. IVAl. VI 2 O 4]3 (шпинель). Промежуточное положение между обеими группами занимают так называемые оксиды-оксосоли, в которых есть либо дискретные ионы О 2 , не связанные с неметаллом, либо устойчивые металлоксидные группировки: Bi 12 O 16(Si. O 4), Fe 3 O 2(BO 3), Cu 2 O(SO 4), Zr 2 O(PO 4)2, Mo. O(PO 4), Pb. O(Mo. O 4), UO 2(SO 4) и др.
 17 Многокомпонентные оксиды Понятия «соли оксокислот» и «сложные оксиды» обобщаются и на оксиды с большим числом компонентов (т. е. они содержат помимо кислорода атомы трёх и большего числа элементов). Mo. O 4 Na Fe. O 6 PO 4 Na. O 6 Cs BO 3 Na 2 Mo. O 4 Na[PO 3] Cs[V 2 O 5]2 [Fe 3 O 2]2 (BO 3) Между солями оксокислот и сложными оксидами нет строгих границ: ряд оксосолей имеет полимерную структуру, как и сложные оксиды, а некоторые из структур сложных оксидов известны для оксосолей (так, структуру шпинели Mg. Al 2 O 4 имеет типичная соль Na 2 Mo. O 4). Для многих сложных оксидов традиционно укоренились старые химические названия, аналогичные солям: титанаты, ниобаты, рутенаты и даже «купраты» , что кристаллохимически не обосновано.
17 Многокомпонентные оксиды Понятия «соли оксокислот» и «сложные оксиды» обобщаются и на оксиды с большим числом компонентов (т. е. они содержат помимо кислорода атомы трёх и большего числа элементов). Mo. O 4 Na Fe. O 6 PO 4 Na. O 6 Cs BO 3 Na 2 Mo. O 4 Na[PO 3] Cs[V 2 O 5]2 [Fe 3 O 2]2 (BO 3) Между солями оксокислот и сложными оксидами нет строгих границ: ряд оксосолей имеет полимерную структуру, как и сложные оксиды, а некоторые из структур сложных оксидов известны для оксосолей (так, структуру шпинели Mg. Al 2 O 4 имеет типичная соль Na 2 Mo. O 4). Для многих сложных оксидов традиционно укоренились старые химические названия, аналогичные солям: титанаты, ниобаты, рутенаты и даже «купраты» , что кристаллохимически не обосновано.
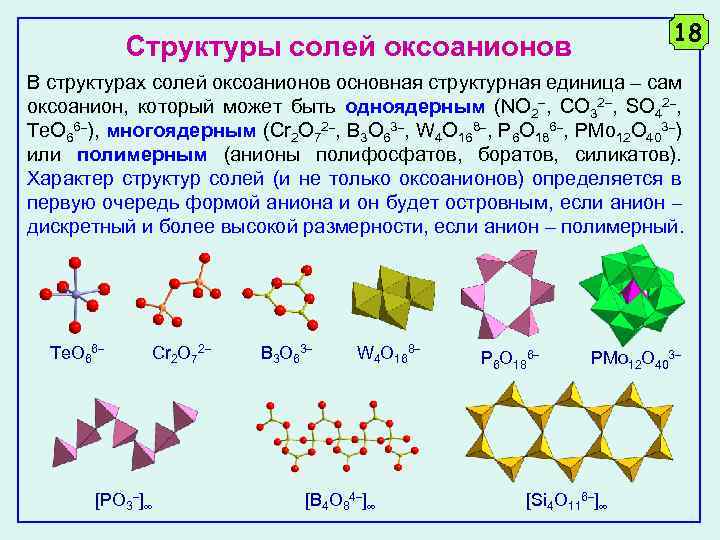 18 Структуры солей оксоанионов В структурах солей оксоанионов основная структурная единица – сам оксоанион, который может быть одноядерным (NO 2 , CO 32 , SO 42 , Te. O 66 ), многоядерным (Cr 2 O 72 , B 3 O 63 , W 4 O 168 , P 6 O 186 , PMo 12 O 403 ) или полимерным (анионы полифосфатов, боратов, силикатов). Характер структур солей (и не только оксоанионов) определяется в первую очередь формой аниона и он будет островным, если анион – дискретный и более высокой размерности, если анион – полимерный. Te. O 66 Cr 2 O 72 [PO 3 ] B 3 O 63 W 4 O 168 [B 4 O 84 ] P 6 O 186 PMo 12 O 403 [Si 4 O 116 ]
18 Структуры солей оксоанионов В структурах солей оксоанионов основная структурная единица – сам оксоанион, который может быть одноядерным (NO 2 , CO 32 , SO 42 , Te. O 66 ), многоядерным (Cr 2 O 72 , B 3 O 63 , W 4 O 168 , P 6 O 186 , PMo 12 O 403 ) или полимерным (анионы полифосфатов, боратов, силикатов). Характер структур солей (и не только оксоанионов) определяется в первую очередь формой аниона и он будет островным, если анион – дискретный и более высокой размерности, если анион – полимерный. Te. O 66 Cr 2 O 72 [PO 3 ] B 3 O 63 W 4 O 168 [B 4 O 84 ] P 6 O 186 PMo 12 O 403 [Si 4 O 116 ]
 Структуры силикатов 19 Примеры структур оксидов с различными мотивами дают силикаты, в которых при обычных условиях всегда присутствуют Si. O 4 -тетраэдры, изолированные или соединенные общими вершинами в различные постройки. Характерная черта силикатов – возможность замещения кремния на алюминий. Всего выделяют 4 основные группы силикатов. Группа Разновидность Островные Ортосиликаты Ионы Si. O 44 Диортосиликаты Ионы Si 2 O 76 Кольцевые Радикал Кольца в один [Sin. O 3 n]2 n и два [Si 2 n. O 5 n]2 n этажа Цепочечные Цепи [Si. O 3] , ленты [Sin. O 3 n-1] Слоистые Слои [Si 2 -x. Alx. O 5]2 Каркасные Модификации Si. O 2 Каркасы [Si. O 2]3 Полевые шпаты Каркасы [Si 1 -x. Alx. O 2]3 с 4 - и 8 -член. кольцами Микропористые Каркасы [Si 1 -x. Alx. O 2]3 с 5 -8 -членными кольцами Цеолиты Каркасы [Si 1 -x. Alx. O 2]3 с большими полостями и сквозными каналами
Структуры силикатов 19 Примеры структур оксидов с различными мотивами дают силикаты, в которых при обычных условиях всегда присутствуют Si. O 4 -тетраэдры, изолированные или соединенные общими вершинами в различные постройки. Характерная черта силикатов – возможность замещения кремния на алюминий. Всего выделяют 4 основные группы силикатов. Группа Разновидность Островные Ортосиликаты Ионы Si. O 44 Диортосиликаты Ионы Si 2 O 76 Кольцевые Радикал Кольца в один [Sin. O 3 n]2 n и два [Si 2 n. O 5 n]2 n этажа Цепочечные Цепи [Si. O 3] , ленты [Sin. O 3 n-1] Слоистые Слои [Si 2 -x. Alx. O 5]2 Каркасные Модификации Si. O 2 Каркасы [Si. O 2]3 Полевые шпаты Каркасы [Si 1 -x. Alx. O 2]3 с 4 - и 8 -член. кольцами Микропористые Каркасы [Si 1 -x. Alx. O 2]3 с 5 -8 -членными кольцами Цеолиты Каркасы [Si 1 -x. Alx. O 2]3 с большими полостями и сквозными каналами
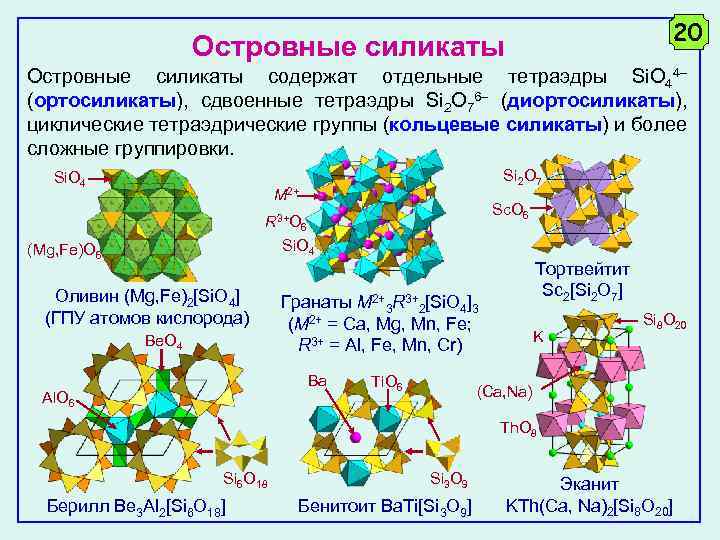 20 Островные силикаты содержат отдельные тетраэдры Si. O 44 (ортосиликаты), сдвоенные тетраэдры Si 2 O 76 (диортосиликаты), циклические тетраэдрические группы (кольцевые силикаты) и более сложные группировки. Si. O 4 Si 2 O 7 M 2+ Sc. O 6 R 3+O 6 Si. O 4 (Mg, Fe)O 6 Оливин (Mg, Fe)2[Si. O 4] (ГПУ атомов кислорода) Be. O 4 Гранаты M 2+3 R 3+2[Si. O 4]3 (M 2+ = Ca, Mg, Mn, Fe; R 3+ = Al, Fe, Mn, Cr) Ba Al. O 6 Тортвейтит Sc 2[Si 2 O 7] Ti. O 6 K Si 8 O 20 (Ca, Na) Th. O 8 Si 6 O 18 Берилл Be 3 Al 2[Si 6 O 18] Si 3 O 9 Бенитоит Ba. Ti[Si 3 O 9] Эканит KTh(Ca, Na)2[Si 8 O 20]
20 Островные силикаты содержат отдельные тетраэдры Si. O 44 (ортосиликаты), сдвоенные тетраэдры Si 2 O 76 (диортосиликаты), циклические тетраэдрические группы (кольцевые силикаты) и более сложные группировки. Si. O 4 Si 2 O 7 M 2+ Sc. O 6 R 3+O 6 Si. O 4 (Mg, Fe)O 6 Оливин (Mg, Fe)2[Si. O 4] (ГПУ атомов кислорода) Be. O 4 Гранаты M 2+3 R 3+2[Si. O 4]3 (M 2+ = Ca, Mg, Mn, Fe; R 3+ = Al, Fe, Mn, Cr) Ba Al. O 6 Тортвейтит Sc 2[Si 2 O 7] Ti. O 6 K Si 8 O 20 (Ca, Na) Th. O 8 Si 6 O 18 Берилл Be 3 Al 2[Si 6 O 18] Si 3 O 9 Бенитоит Ba. Ti[Si 3 O 9] Эканит KTh(Ca, Na)2[Si 8 O 20]
![21 Цепочечные силикаты содержат одиночные цепочки [Si. O 3] или ленты из таких цепочек, 21 Цепочечные силикаты содержат одиночные цепочки [Si. O 3] или ленты из таких цепочек,](https://present5.com/presentation/5652994_180087667/image-21.jpg) 21 Цепочечные силикаты содержат одиночные цепочки [Si. O 3] или ленты из таких цепочек, состоящие из двух, трёх и более рядов. Наиболее распространены силикаты с одиночными цепочками – пироксены (Mg, Ca, Fe, Mn, Al, Na, Li)[Si. O 3] и двухрядными лентами – амфиболы (Ca, Mg, Fe)7[Si 4 O 11]2(OH)2. Ca. O 7 Mg. O 6 [Si. O 3] Ca Mg. O 6 Ca. O 6 [Si 4 O 11] Цепочки [Si. O 3] в энстатите Mg[Si. O 3] Двухрядные ленты [Si 4 O 11] в тремолите Ca 2 Mg 5[Si 4 O 11]2(OH)2 Двухрядные ленты [Si 6 O 17] в ксонотлите Ca 6[Si 6 O 17](OH)2
21 Цепочечные силикаты содержат одиночные цепочки [Si. O 3] или ленты из таких цепочек, состоящие из двух, трёх и более рядов. Наиболее распространены силикаты с одиночными цепочками – пироксены (Mg, Ca, Fe, Mn, Al, Na, Li)[Si. O 3] и двухрядными лентами – амфиболы (Ca, Mg, Fe)7[Si 4 O 11]2(OH)2. Ca. O 7 Mg. O 6 [Si. O 3] Ca Mg. O 6 Ca. O 6 [Si 4 O 11] Цепочки [Si. O 3] в энстатите Mg[Si. O 3] Двухрядные ленты [Si 4 O 11] в тремолите Ca 2 Mg 5[Si 4 O 11]2(OH)2 Двухрядные ленты [Si 6 O 17] в ксонотлите Ca 6[Si 6 O 17](OH)2
![22 Слоистые силикаты и алюмосиликаты содержат слои [Si 2 O 5]2 и [(Si, Al)2 22 Слоистые силикаты и алюмосиликаты содержат слои [Si 2 O 5]2 и [(Si, Al)2](https://present5.com/presentation/5652994_180087667/image-22.jpg) 22 Слоистые силикаты и алюмосиликаты содержат слои [Si 2 O 5]2 и [(Si, Al)2 O 5]2 , которые связываются со слоями из полиэдров Mg 2+, Al 3+, Fe 3+ и др. в двух- и трёхэтажные пакеты. В природе обычно встречаются гексагональные слои, которые нейтральны и связаны ван-дер-ваальсовыми силами в глинистых минералах, а в слюдах отрицательный заряд слоёв компенсируют межслоевые катионы. Часто образуют смешаннослойные фазы слой [Si 2 O 5]2 слюда слой [Al. Si 3 O 10]2 слой [Al(OH)3]2 K слои [Mg(OH)2]2 Лизардит Mg 3[Si 2 O 5](OH)4 глины Тальк Mg 3[Si 4 O 10](OH)2 Мусковит KAl 2[Al. Si 3 O 10](OH)2
22 Слоистые силикаты и алюмосиликаты содержат слои [Si 2 O 5]2 и [(Si, Al)2 O 5]2 , которые связываются со слоями из полиэдров Mg 2+, Al 3+, Fe 3+ и др. в двух- и трёхэтажные пакеты. В природе обычно встречаются гексагональные слои, которые нейтральны и связаны ван-дер-ваальсовыми силами в глинистых минералах, а в слюдах отрицательный заряд слоёв компенсируют межслоевые катионы. Часто образуют смешаннослойные фазы слой [Si 2 O 5]2 слюда слой [Al. Si 3 O 10]2 слой [Al(OH)3]2 K слои [Mg(OH)2]2 Лизардит Mg 3[Si 2 O 5](OH)4 глины Тальк Mg 3[Si 4 O 10](OH)2 Мусковит KAl 2[Al. Si 3 O 10](OH)2
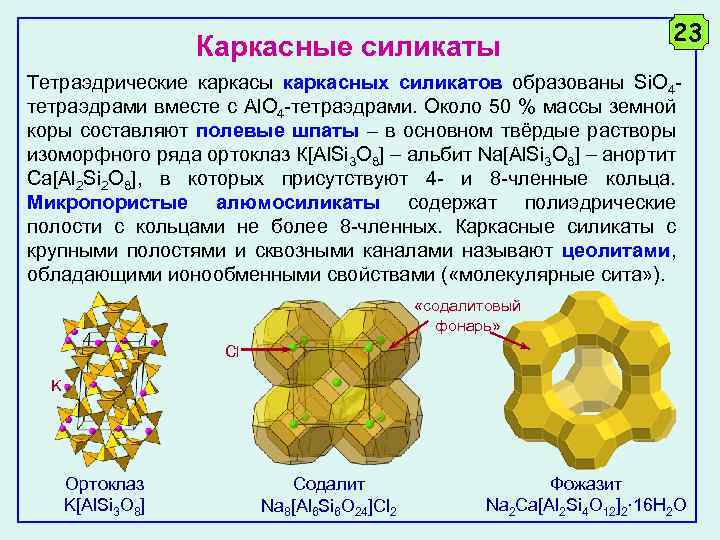 Каркасные силикаты 23 Тетраэдрические каркасы каркасных силикатов образованы Si. O 4 тетраэдрами вместе с Al. O 4 -тетраэдрами. Около 50 % массы земной коры составляют полевые шпаты – в основном твёрдые растворы изоморфного ряда ортоклаз К[Аl. Si 3 O 8] альбит Na[Аl. Si 3 O 8] анортит Са[Аl 2 Si 2 O 8], в которых присутствуют 4 - и 8 -членные кольца. Микропористые алюмосиликаты содержат полиэдрические полости с кольцами не более 8 -членных. Каркасные силикаты с крупными полостями и сквозными каналами называют цеолитами, обладающими ионообменными свойствами ( «молекулярные сита» ). «содалитовый фонарь» Cl K Ортоклаз K[Al. Si 3 O 8] Содалит Na 8[Al 6 Si 6 O 24]Cl 2 Фожазит Na 2 Ca[Al 2 Si 4 O 12]2· 16 H 2 O
Каркасные силикаты 23 Тетраэдрические каркасы каркасных силикатов образованы Si. O 4 тетраэдрами вместе с Al. O 4 -тетраэдрами. Около 50 % массы земной коры составляют полевые шпаты – в основном твёрдые растворы изоморфного ряда ортоклаз К[Аl. Si 3 O 8] альбит Na[Аl. Si 3 O 8] анортит Са[Аl 2 Si 2 O 8], в которых присутствуют 4 - и 8 -членные кольца. Микропористые алюмосиликаты содержат полиэдрические полости с кольцами не более 8 -членных. Каркасные силикаты с крупными полостями и сквозными каналами называют цеолитами, обладающими ионообменными свойствами ( «молекулярные сита» ). «содалитовый фонарь» Cl K Ортоклаз K[Al. Si 3 O 8] Содалит Na 8[Al 6 Si 6 O 24]Cl 2 Фожазит Na 2 Ca[Al 2 Si 4 O 12]2· 16 H 2 O
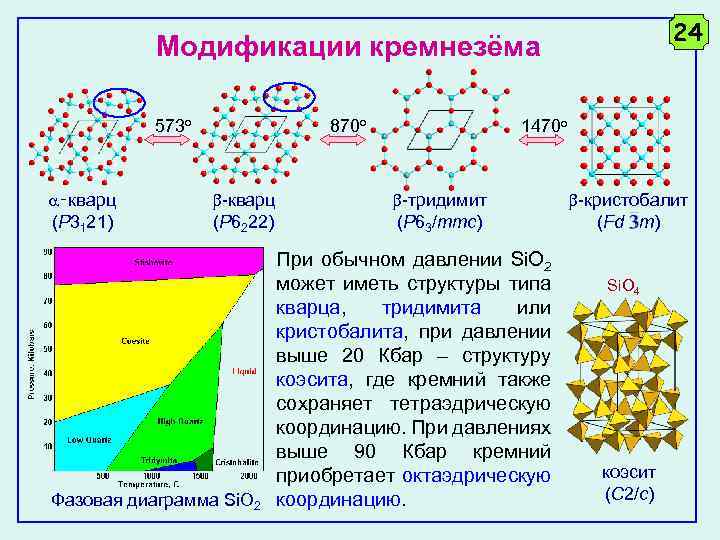 24 Модификации кремнезёма 573 о ‑кварц (P 3121) 870 о -кварц (P 6222) Фазовая диаграмма Si. O 2 1470 о -тридимит (P 63/mmc) При обычном давлении Si. O 2 может иметь структуры типа кварца, тридимита или кристобалита, при давлении выше 20 Кбар – структуру коэсита, где кремний также сохраняет тетраэдрическую координацию. При давлениях выше 90 Кбар кремний приобретает октаэдрическую координацию. -кристобалит (Fd m) Si. O 4 коэсит (C 2/c)
24 Модификации кремнезёма 573 о ‑кварц (P 3121) 870 о -кварц (P 6222) Фазовая диаграмма Si. O 2 1470 о -тридимит (P 63/mmc) При обычном давлении Si. O 2 может иметь структуры типа кварца, тридимита или кристобалита, при давлении выше 20 Кбар – структуру коэсита, где кремний также сохраняет тетраэдрическую координацию. При давлениях выше 90 Кбар кремний приобретает октаэдрическую координацию. -кристобалит (Fd m) Si. O 4 коэсит (C 2/c)
 Стишовит 25 Впервые фаза Si. O 2 с октаэдрической координацией кремния (тип рутила) открыта весной 1961 г. аспирантом Института физики высоких давлений С. М. Стишовым, сейчас он академик и директор этого института. В конце 1961 г. в Аризонском метеоритном кратере найден природный образец новой фазы, которая в честь С. М. Стишов молодого исследователя была названа стишовитом. (р. 1937) 90 Кбар ‑кварц (КЧ = 4) = 2. 65 г/см 3 Кристалл плотной фазы Si. O 2, фото из статьи С. М. Стишова, С. В. Поповой, 1961 г. стишовит (КЧ = 6) = 4. 29 г/см 3 Кристалл стишовита размером 2. 4 мм, выращенный в ИФВД РАН Аризонский метеоритный кратер, где был открыт стишовит
Стишовит 25 Впервые фаза Si. O 2 с октаэдрической координацией кремния (тип рутила) открыта весной 1961 г. аспирантом Института физики высоких давлений С. М. Стишовым, сейчас он академик и директор этого института. В конце 1961 г. в Аризонском метеоритном кратере найден природный образец новой фазы, которая в честь С. М. Стишов молодого исследователя была названа стишовитом. (р. 1937) 90 Кбар ‑кварц (КЧ = 4) = 2. 65 г/см 3 Кристалл плотной фазы Si. O 2, фото из статьи С. М. Стишова, С. В. Поповой, 1961 г. стишовит (КЧ = 6) = 4. 29 г/см 3 Кристалл стишовита размером 2. 4 мм, выращенный в ИФВД РАН Аризонский метеоритный кратер, где был открыт стишовит
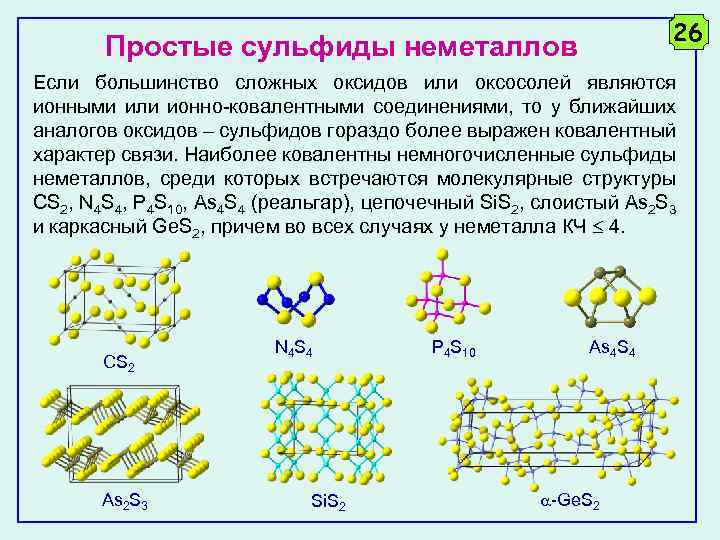 26 Простые сульфиды неметаллов Если большинство сложных оксидов или оксосолей являются ионными или ионно-ковалентными соединениями, то у ближайших аналогов оксидов – сульфидов гораздо более выражен ковалентный характер связи. Наиболее ковалентны немногочисленные сульфиды неметаллов, среди которых встречаются молекулярные структуры CS 2, N 4 S 4, P 4 S 10, As 4 S 4 (реальгар), цепочечный Si. S 2, слоистый As 2 S 3 и каркасный Ge. S 2, причем во всех случаях у неметалла КЧ 4. CS 2 As 2 S 3 N 4 Si. S 2 P 4 S 10 As 4 S 4 -Ge. S 2
26 Простые сульфиды неметаллов Если большинство сложных оксидов или оксосолей являются ионными или ионно-ковалентными соединениями, то у ближайших аналогов оксидов – сульфидов гораздо более выражен ковалентный характер связи. Наиболее ковалентны немногочисленные сульфиды неметаллов, среди которых встречаются молекулярные структуры CS 2, N 4 S 4, P 4 S 10, As 4 S 4 (реальгар), цепочечный Si. S 2, слоистый As 2 S 3 и каркасный Ge. S 2, причем во всех случаях у неметалла КЧ 4. CS 2 As 2 S 3 N 4 Si. S 2 P 4 S 10 As 4 S 4 -Ge. S 2
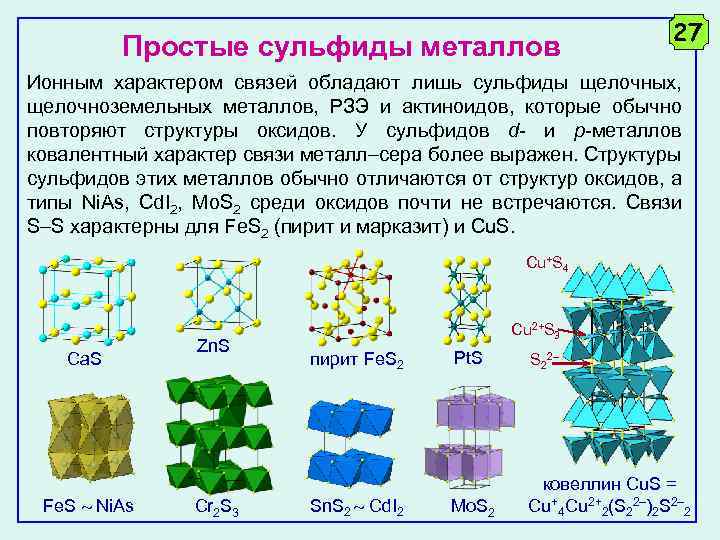 Простые сульфиды металлов 27 Ионным характером связей обладают лишь сульфиды щелочных, щелочноземельных металлов, РЗЭ и актиноидов, которые обычно повторяют структуры оксидов. У сульфидов d- и p-металлов ковалентный характер связи металл сера более выражен. Структуры сульфидов этих металлов обычно отличаются от структур оксидов, а типы Ni. As, Cd. I 2, Mo. S 2 среди оксидов почти не встречаются. Связи S S характерны для Fe. S 2 (пирит и марказит) и Cu. S. Cu+S 4 Ca. S Fe. S Ni. As Zn. S Cr 2 S 3 Cu 2+S 3 пирит Fe. S 2 Sn. S 2 Cd. I 2 Pt. S S 22 Mo. S 2 ковеллин Cu. S = Cu+4 Cu 2+2(S 22–)2 S 2– 2
Простые сульфиды металлов 27 Ионным характером связей обладают лишь сульфиды щелочных, щелочноземельных металлов, РЗЭ и актиноидов, которые обычно повторяют структуры оксидов. У сульфидов d- и p-металлов ковалентный характер связи металл сера более выражен. Структуры сульфидов этих металлов обычно отличаются от структур оксидов, а типы Ni. As, Cd. I 2, Mo. S 2 среди оксидов почти не встречаются. Связи S S характерны для Fe. S 2 (пирит и марказит) и Cu. S. Cu+S 4 Ca. S Fe. S Ni. As Zn. S Cr 2 S 3 Cu 2+S 3 пирит Fe. S 2 Sn. S 2 Cd. I 2 Pt. S S 22 Mo. S 2 ковеллин Cu. S = Cu+4 Cu 2+2(S 22–)2 S 2– 2
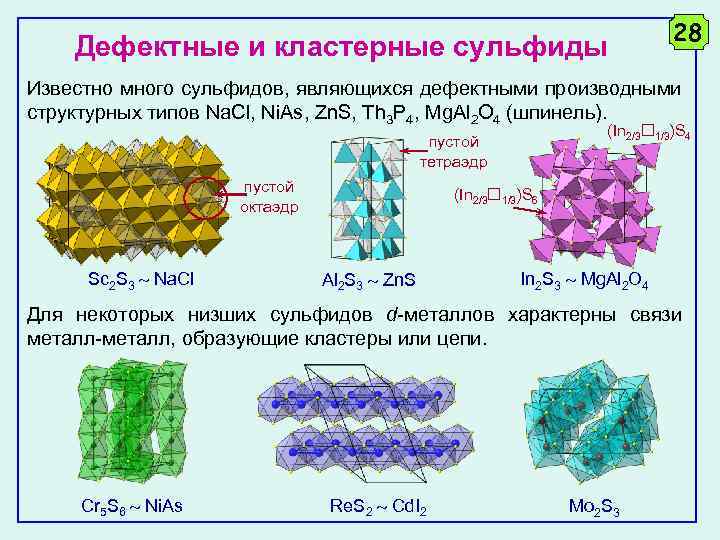 Дефектные и кластерные сульфиды 28 Известно много сульфидов, являющихся дефектными производными структурных типов Na. Cl, Ni. As, Zn. S, Th 3 P 4, Mg. Al 2 O 4 (шпинель). (In 2/3 1/3)S 4 пустой тетраэдр пустой октаэдр Sc 2 S 3 Na. Cl (In 2/3 1/3)S 6 Al 2 S 3 Zn. S In 2 S 3 Mg. Al 2 O 4 Для некоторых низших сульфидов d-металлов характерны связи металл-металл, образующие кластеры или цепи. Cr 5 S 6 Ni. As Re. S 2 Cd. I 2 Mo 2 S 3
Дефектные и кластерные сульфиды 28 Известно много сульфидов, являющихся дефектными производными структурных типов Na. Cl, Ni. As, Zn. S, Th 3 P 4, Mg. Al 2 O 4 (шпинель). (In 2/3 1/3)S 4 пустой тетраэдр пустой октаэдр Sc 2 S 3 Na. Cl (In 2/3 1/3)S 6 Al 2 S 3 Zn. S In 2 S 3 Mg. Al 2 O 4 Для некоторых низших сульфидов d-металлов характерны связи металл-металл, образующие кластеры или цепи. Cr 5 S 6 Ni. As Re. S 2 Cd. I 2 Mo 2 S 3
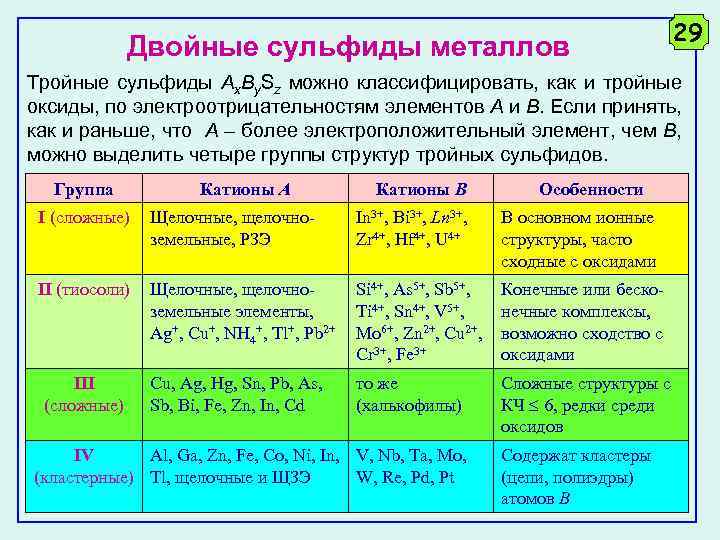 Двойные сульфиды металлов 29 Тройные сульфиды Ax. By. Sz можно классифицировать, как и тройные оксиды, по электроотрицательностям элементов А и В. Если принять, как и раньше, что А – более электроположительный элемент, чем В, можно выделить четыре группы структур тройных сульфидов. Группа Катионы А Катионы В Особенности I (сложные) Щелочные, щелочноземельные, РЗЭ In 3+, Bi 3+, Ln 3+, Zr 4+, Hf 4+, U 4+ В основном ионные структуры, часто сходные с оксидами II (тиосоли) Щелочные, щелочноземельные элементы, Ag+, Cu+, NH 4+, Tl+, Pb 2+ Si 4+, As 5+, Sb 5+, Ti 4+, Sn 4+, V 5+, Mo 6+, Zn 2+, Cu 2+, Cr 3+, Fe 3+ Конечные или бесконечные комплексы, возможно сходство с оксидами III (сложные) Cu, Ag, Hg, Sn, Pb, As, Sb, Bi, Fe, Zn, In, Cd то же (халькофилы) Сложные структуры с КЧ 6, редки среди оксидов IV Al, Ga, Zn, Fe, Co, Ni, In, V, Nb, Ta, Mo, (кластерные) Tl, щелочные и ЩЗЭ W, Re, Pd, Pt Содержат кластеры (цепи, полиэдры) атомов В
Двойные сульфиды металлов 29 Тройные сульфиды Ax. By. Sz можно классифицировать, как и тройные оксиды, по электроотрицательностям элементов А и В. Если принять, как и раньше, что А – более электроположительный элемент, чем В, можно выделить четыре группы структур тройных сульфидов. Группа Катионы А Катионы В Особенности I (сложные) Щелочные, щелочноземельные, РЗЭ In 3+, Bi 3+, Ln 3+, Zr 4+, Hf 4+, U 4+ В основном ионные структуры, часто сходные с оксидами II (тиосоли) Щелочные, щелочноземельные элементы, Ag+, Cu+, NH 4+, Tl+, Pb 2+ Si 4+, As 5+, Sb 5+, Ti 4+, Sn 4+, V 5+, Mo 6+, Zn 2+, Cu 2+, Cr 3+, Fe 3+ Конечные или бесконечные комплексы, возможно сходство с оксидами III (сложные) Cu, Ag, Hg, Sn, Pb, As, Sb, Bi, Fe, Zn, In, Cd то же (халькофилы) Сложные структуры с КЧ 6, редки среди оксидов IV Al, Ga, Zn, Fe, Co, Ni, In, V, Nb, Ta, Mo, (кластерные) Tl, щелочные и ЩЗЭ W, Re, Pd, Pt Содержат кластеры (цепи, полиэдры) атомов В
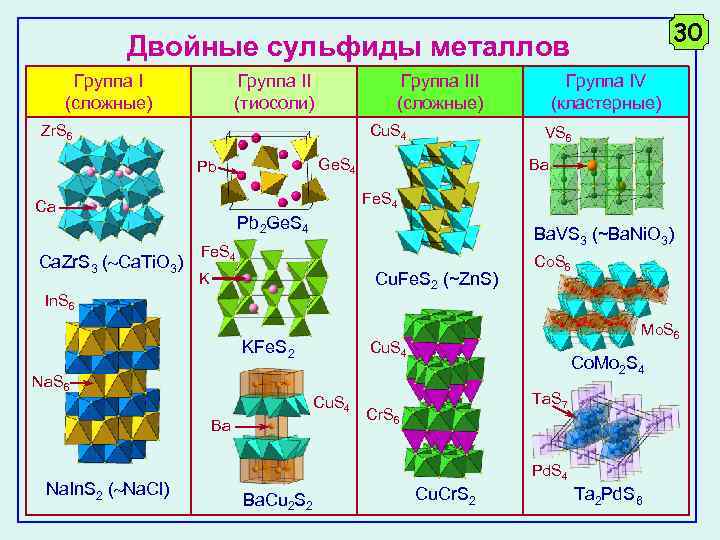 30 Двойные сульфиды металлов Группа I (сложные) Группа II (тиосоли) Группа III (сложные) Zr. S 6 Cu. S 4 Ba Fe. S 4 Ca Ca. Zr. S 3 ( Ca. Ti. O 3) VS 6 Ge. S 4 Pb Pb 2 Ge. S 4 Ba. VS 3 (~Ba. Ni. O 3) Fe. S 4 Cu. Fe. S 2 (~Zn. S) K In. S 6 KFe. S 2 Cu. S 4 Ba Co. S 6 Mo. S 6 Co. Mo 2 S 4 Na. S 6 Na. In. S 2 ( Na. Cl) Группа IV (кластерные) Ta. S 7 Cr. S 6 Pd. S 4 Ba. Cu 2 S 2 Cu. Cr. S 2 Ta 2 Pd. S 6
30 Двойные сульфиды металлов Группа I (сложные) Группа II (тиосоли) Группа III (сложные) Zr. S 6 Cu. S 4 Ba Fe. S 4 Ca Ca. Zr. S 3 ( Ca. Ti. O 3) VS 6 Ge. S 4 Pb Pb 2 Ge. S 4 Ba. VS 3 (~Ba. Ni. O 3) Fe. S 4 Cu. Fe. S 2 (~Zn. S) K In. S 6 KFe. S 2 Cu. S 4 Ba Co. S 6 Mo. S 6 Co. Mo 2 S 4 Na. S 6 Na. In. S 2 ( Na. Cl) Группа IV (кластерные) Ta. S 7 Cr. S 6 Pd. S 4 Ba. Cu 2 S 2 Cu. Cr. S 2 Ta 2 Pd. S 6
 Литература 31 1. Бокий Г. Б. Кристаллохимия. М. : Наука, 1971. 2. Современная кристаллография / Под ред. Б. К. Вайнштейна. М. : Наука, 1979. Т. 2. 3. Пенкаля Т. Очерки кристаллохимии. Л. : Химия, 1974. 4. Солодовников С. Ф. Основы кристаллохимии. Справочно-методические материалы к курсу. Новосибирск: НГУ, 2007. 5. Солодовников С. Ф. Основные термины и понятия структурной кристаллографии и кристаллохимии. Словарь-пособие. Новосибирск: ИНХ СО РАН, 2005. 6. Солодовников С. Ф. Основы кристаллохимии. Учебное пособие. Новосибирск: НГУ, 2012. Последние три пособия можно найти на сайте кафедры неорганической химии ФЕН НГУ: http: //icchair. niic. nsc. ru/ полезные файлы.
Литература 31 1. Бокий Г. Б. Кристаллохимия. М. : Наука, 1971. 2. Современная кристаллография / Под ред. Б. К. Вайнштейна. М. : Наука, 1979. Т. 2. 3. Пенкаля Т. Очерки кристаллохимии. Л. : Химия, 1974. 4. Солодовников С. Ф. Основы кристаллохимии. Справочно-методические материалы к курсу. Новосибирск: НГУ, 2007. 5. Солодовников С. Ф. Основные термины и понятия структурной кристаллографии и кристаллохимии. Словарь-пособие. Новосибирск: ИНХ СО РАН, 2005. 6. Солодовников С. Ф. Основы кристаллохимии. Учебное пособие. Новосибирск: НГУ, 2012. Последние три пособия можно найти на сайте кафедры неорганической химии ФЕН НГУ: http: //icchair. niic. nsc. ru/ полезные файлы.


