lek_1.ppt
- Количество слайдов: 28
 1 Инструментальные методы анализа Фотометрический анализ
1 Инструментальные методы анализа Фотометрический анализ
 Литература 1. Дорохова Е. Н. , Прохорова Г. В. , «Аналитическая химия. Физико-химические методы анализа» , 1991. 2. Золотов Ю. А. , «Основы аналитической химии» , Т. 2, 2004. 3. Булатов М. И. , Калинкин И. П. «Практическое руководство по фотоколориметрическим и спектрофотометрическим методам анализа» , 1972. 4. Пешкова В. М. , Громова М. И. «Методы абсорбционной спектроскопии в аналитической химии» , 1976. 2
Литература 1. Дорохова Е. Н. , Прохорова Г. В. , «Аналитическая химия. Физико-химические методы анализа» , 1991. 2. Золотов Ю. А. , «Основы аналитической химии» , Т. 2, 2004. 3. Булатов М. И. , Калинкин И. П. «Практическое руководство по фотоколориметрическим и спектрофотометрическим методам анализа» , 1972. 4. Пешкова В. М. , Громова М. И. «Методы абсорбционной спектроскопии в аналитической химии» , 1976. 2
 Оптические методы анализа Ø Ø Атомно-абсорбционный анализ – основан на поглощении световой энергии атомами анализируемых веществ. Молекулярно-абсорбционный анализ – анализ по поглощению света молекулами анализируемого вещества и сложными ионами (в БУФ, видимой, БИК). К нему относят фотоэлектроколориметрию, спектрофотометрию, ИК-спектроскопию. Анализ по поглощению и рассеиванию световой энергии взвешенными частицами анализируемого вещества, т. е. дисперсными системами (турбидиметрия, нефелометрия). Люминесцентный анализ – основан на измерении излучения, выделенного возбужденными частицами исследуемого объекта. 3
Оптические методы анализа Ø Ø Атомно-абсорбционный анализ – основан на поглощении световой энергии атомами анализируемых веществ. Молекулярно-абсорбционный анализ – анализ по поглощению света молекулами анализируемого вещества и сложными ионами (в БУФ, видимой, БИК). К нему относят фотоэлектроколориметрию, спектрофотометрию, ИК-спектроскопию. Анализ по поглощению и рассеиванию световой энергии взвешенными частицами анализируемого вещества, т. е. дисперсными системами (турбидиметрия, нефелометрия). Люминесцентный анализ – основан на измерении излучения, выделенного возбужденными частицами исследуемого объекта. 3
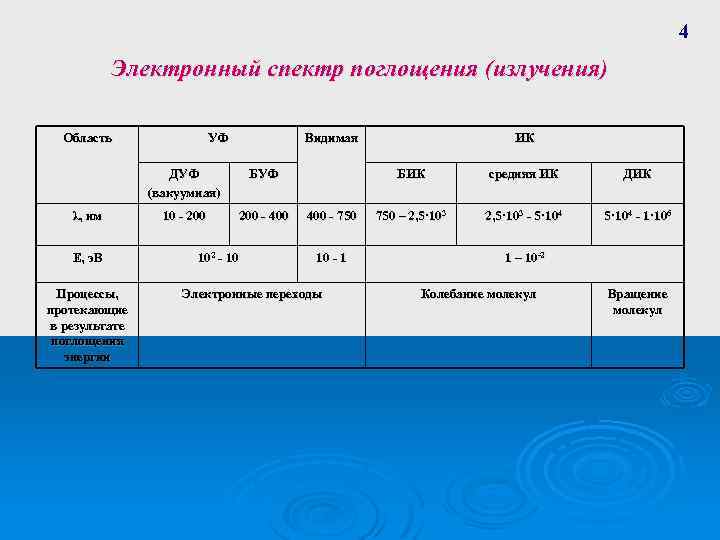 4 Электронный спектр поглощения (излучения) Область УФ Видимая ДУФ (вакуумная) λ, нм Е, э. В Процессы, протекающие в результате поглощения энергии БУФ 10 - 200 - 400 102 - 10 ИК БИК 400 - 750 10 - 1 Электронные переходы средняя ИК ДИК 750 – 2, 5· 103 - 5· 104 - 1· 106 1 – 10 -2 Колебание молекул Вращение молекул
4 Электронный спектр поглощения (излучения) Область УФ Видимая ДУФ (вакуумная) λ, нм Е, э. В Процессы, протекающие в результате поглощения энергии БУФ 10 - 200 - 400 102 - 10 ИК БИК 400 - 750 10 - 1 Электронные переходы средняя ИК ДИК 750 – 2, 5· 103 - 5· 104 - 1· 106 1 – 10 -2 Колебание молекул Вращение молекул
 5 Фотометрические методы анализа Методы, основанные на измерении избирательного поглощения светового излучения в видимой, БУФ, БИК областях спектра истинными растворами исследуемого вещества (т. е. однородными нерассеивающими системами). Io I Закон Планка ∆Е = Е* – Ео= hν =h (1) h = 6, 625· 10 -34 Дж·с Е* Екванта = Евозб. электрона = ∆Е ∆Е Ео (2)
5 Фотометрические методы анализа Методы, основанные на измерении избирательного поглощения светового излучения в видимой, БУФ, БИК областях спектра истинными растворами исследуемого вещества (т. е. однородными нерассеивающими системами). Io I Закон Планка ∆Е = Е* – Ео= hν =h (1) h = 6, 625· 10 -34 Дж·с Е* Екванта = Евозб. электрона = ∆Е ∆Е Ео (2)
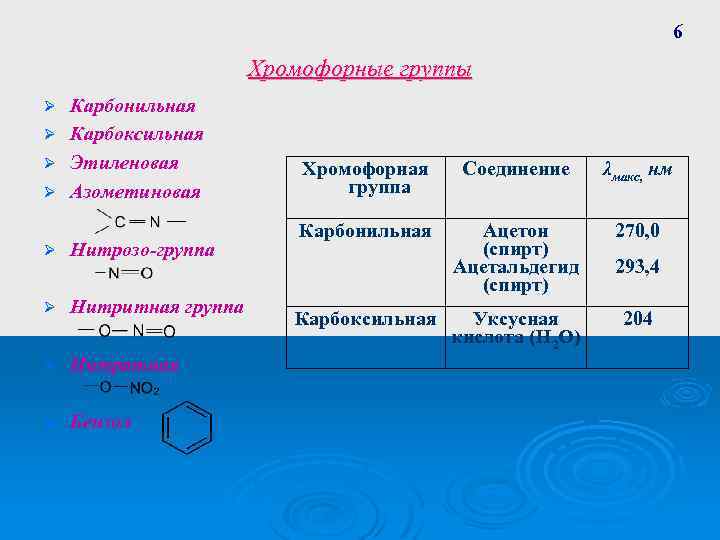 6 Хромофорные группы Карбонильная Ø Карбоксильная Ø Этиленовая Ø Азометиновая Ø Ø Нитрозо-группа Ø Нитритная группа Ø Нитратная Ø Бензол Хромофорная группа Соединение λмакс, нм Карбонильная Ацетон (спирт) Ацетальдегид (спирт) 270, 0 Уксусная кислота (H 2 O) 204 Карбоксильная 293, 4
6 Хромофорные группы Карбонильная Ø Карбоксильная Ø Этиленовая Ø Азометиновая Ø Ø Нитрозо-группа Ø Нитритная группа Ø Нитратная Ø Бензол Хромофорная группа Соединение λмакс, нм Карбонильная Ацетон (спирт) Ацетальдегид (спирт) 270, 0 Уксусная кислота (H 2 O) 204 Карбоксильная 293, 4
 7 Ауксохромные группы -OH, -NH 2, -СH 3, -N(CH 3)2, -OCH 3
7 Ауксохромные группы -OH, -NH 2, -СH 3, -N(CH 3)2, -OCH 3
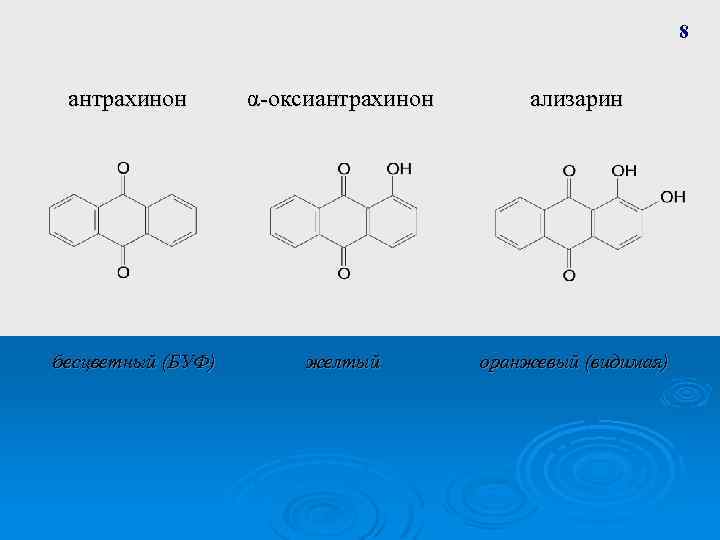 8 антрахинон бесцветный (БУФ) α-оксиантрахинон ализарин желтый оранжевый (видимая)
8 антрахинон бесцветный (БУФ) α-оксиантрахинон ализарин желтый оранжевый (видимая)
 9 Поглощающие системы в фотометрии Ø Растворы аква-комплексов (ионов), обладающие поглощением в видимой области спектра; их молярный коэффициент поглощения (ε) не выше n· 102. Органические соединения. Ø Растворы солей элементов в высших степенях окисления (Mn. O 4 -, Cr 2 O 72 - и т. д. ) Ø Растворы комплексов металлов с неорганическими (ε ~ n· 103) и органическими (ε ~ n· 104) лигандами. Ø
9 Поглощающие системы в фотометрии Ø Растворы аква-комплексов (ионов), обладающие поглощением в видимой области спектра; их молярный коэффициент поглощения (ε) не выше n· 102. Органические соединения. Ø Растворы солей элементов в высших степенях окисления (Mn. O 4 -, Cr 2 O 72 - и т. д. ) Ø Растворы комплексов металлов с неорганическими (ε ~ n· 103) и органическими (ε ~ n· 104) лигандами. Ø
 Прохождение светового потока через окрашенный раствор I 0 I Iот Iп Iот Io=I+Iп+Iот (3) 10
Прохождение светового потока через окрашенный раствор I 0 I Iот Iп Iот Io=I+Iп+Iот (3) 10
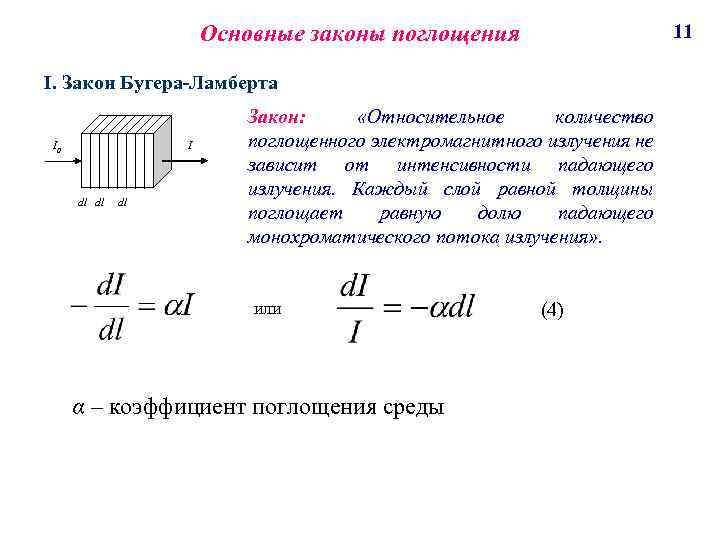 Основные законы поглощения 11 I. Закон Бугера-Ламберта I 0 I dl dl dl Закон: «Относительное количество поглощенного электромагнитного излучения не зависит от интенсивности падающего излучения. Каждый слой равной толщины поглощает равную долю падающего монохроматического потока излучения» . или α – коэффициент поглощения среды (4)
Основные законы поглощения 11 I. Закон Бугера-Ламберта I 0 I dl dl dl Закон: «Относительное количество поглощенного электромагнитного излучения не зависит от интенсивности падающего излучения. Каждый слой равной толщины поглощает равную долю падающего монохроматического потока излучения» . или α – коэффициент поглощения среды (4)
 12 Основные законы поглощения (5) (6) (8) (7) Закон Бугера-Ламберта
12 Основные законы поглощения (5) (6) (8) (7) Закон Бугера-Ламберта
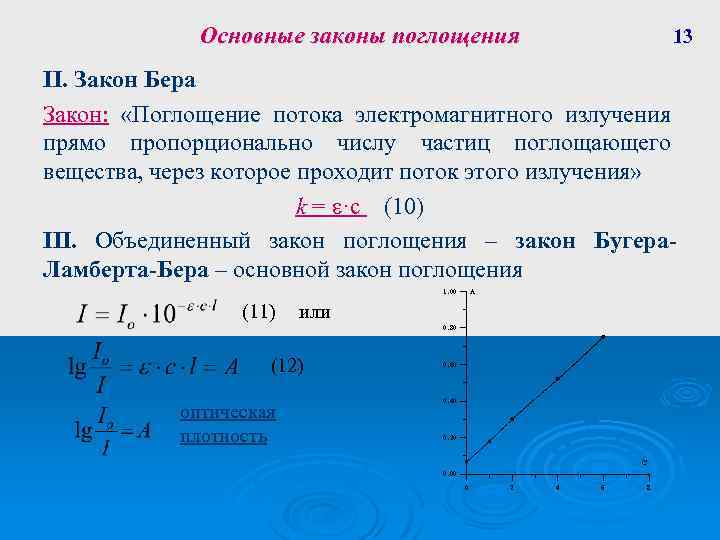 Основные законы поглощения 13 II. Закон Бера Закон: «Поглощение потока электромагнитного излучения прямо пропорционально числу частиц поглощающего вещества, через которое проходит поток этого излучения» k = ε·c (10) III. Объединенный закон поглощения – закон Бугера. Ламберта-Бера – основной закон поглощения 1. 00 (11) A или 0. 80 (12) оптическая плотность 0. 60 0. 40 0. 20 C 0. 00 0 2 4 6 8
Основные законы поглощения 13 II. Закон Бера Закон: «Поглощение потока электромагнитного излучения прямо пропорционально числу частиц поглощающего вещества, через которое проходит поток этого излучения» k = ε·c (10) III. Объединенный закон поглощения – закон Бугера. Ламберта-Бера – основной закон поглощения 1. 00 (11) A или 0. 80 (12) оптическая плотность 0. 60 0. 40 0. 20 C 0. 00 0 2 4 6 8
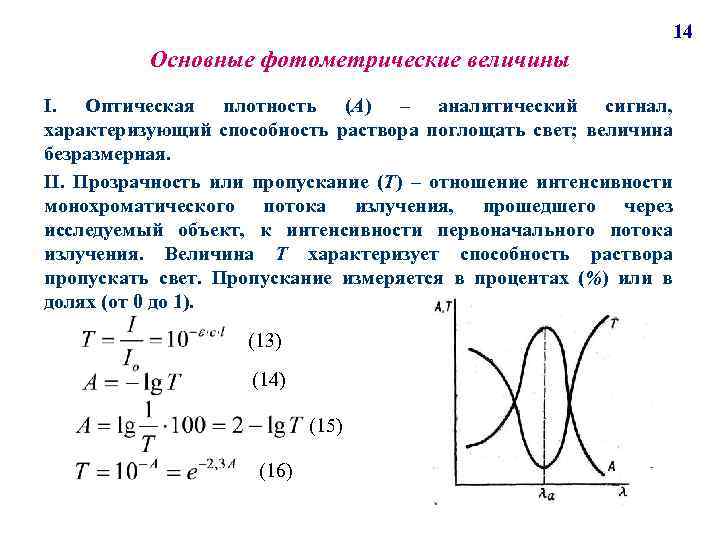 14 Основные фотометрические величины I. Оптическая плотность (А) – аналитический сигнал, характеризующий способность раствора поглощать свет; величина безразмерная. II. Прозрачность или пропускание (Т) – отношение интенсивности монохроматического потока излучения, прошедшего через исследуемый объект, к интенсивности первоначального потока излучения. Величина Т характеризует способность раствора пропускать свет. Пропускание измеряется в процентах (%) или в долях (от 0 до 1). (13) (14) (15) (16)
14 Основные фотометрические величины I. Оптическая плотность (А) – аналитический сигнал, характеризующий способность раствора поглощать свет; величина безразмерная. II. Прозрачность или пропускание (Т) – отношение интенсивности монохроматического потока излучения, прошедшего через исследуемый объект, к интенсивности первоначального потока излучения. Величина Т характеризует способность раствора пропускать свет. Пропускание измеряется в процентах (%) или в долях (от 0 до 1). (13) (14) (15) (16)
 Основные фотометрические величины III. Молярный коэффициент светопоглощения (погашения) (ε) является основной характеристикой поглощения любой системы при данной длине волны; отражает индивидуальные свойства окрашенных соединений и является их определяющей характеристикой. Физический смысл: молярный коэффициент светопоглощения представляет собой оптическую плотность раствора с концентрацией 1 моль/л, помещенного в кювету с толщиной поглощающего слоя 1 см; имеет размерность см 2/моль. Молярный коэффициент светопоглощения зависит от: Øдлины волны падающего света; Øтемпературы раствора; Øприроды растворенного вещества. Молярный коэффициент светопоглощения является мерой чувствительности данной фотометрической реакции. Молярный коэффициент светопоглощения бывает истинным и кажущимся. Значение ε характеризует два существенно важных свойства поглощающей системы: Øпостоянство значения ε говорит о соблюдении основного закона поглощения в определенном интервале концентраций; Øзначение ε удобно использовать для сравнительной оценки чувствительности фотометрической реакции. 15
Основные фотометрические величины III. Молярный коэффициент светопоглощения (погашения) (ε) является основной характеристикой поглощения любой системы при данной длине волны; отражает индивидуальные свойства окрашенных соединений и является их определяющей характеристикой. Физический смысл: молярный коэффициент светопоглощения представляет собой оптическую плотность раствора с концентрацией 1 моль/л, помещенного в кювету с толщиной поглощающего слоя 1 см; имеет размерность см 2/моль. Молярный коэффициент светопоглощения зависит от: Øдлины волны падающего света; Øтемпературы раствора; Øприроды растворенного вещества. Молярный коэффициент светопоглощения является мерой чувствительности данной фотометрической реакции. Молярный коэффициент светопоглощения бывает истинным и кажущимся. Значение ε характеризует два существенно важных свойства поглощающей системы: Øпостоянство значения ε говорит о соблюдении основного закона поглощения в определенном интервале концентраций; Øзначение ε удобно использовать для сравнительной оценки чувствительности фотометрической реакции. 15
 16 ε индивидуальных веществ (растворов солей Cu, Co, Ni) достигает всего нескольких единиц; ; Ø Ø Молярный коэффициент поглощения [Cu(NH 3)4]2+ достигает 600; ε комплексов с органическими лигандами – десятки тысяч: Ø Ø l l l ε дитизоната цинка равен 94000; ε дитизоната меди равен 45000; ε сульфосалицилата железа равен 2000.
16 ε индивидуальных веществ (растворов солей Cu, Co, Ni) достигает всего нескольких единиц; ; Ø Ø Молярный коэффициент поглощения [Cu(NH 3)4]2+ достигает 600; ε комплексов с органическими лигандами – десятки тысяч: Ø Ø l l l ε дитизоната цинка равен 94000; ε дитизоната меди равен 45000; ε сульфосалицилата железа равен 2000.
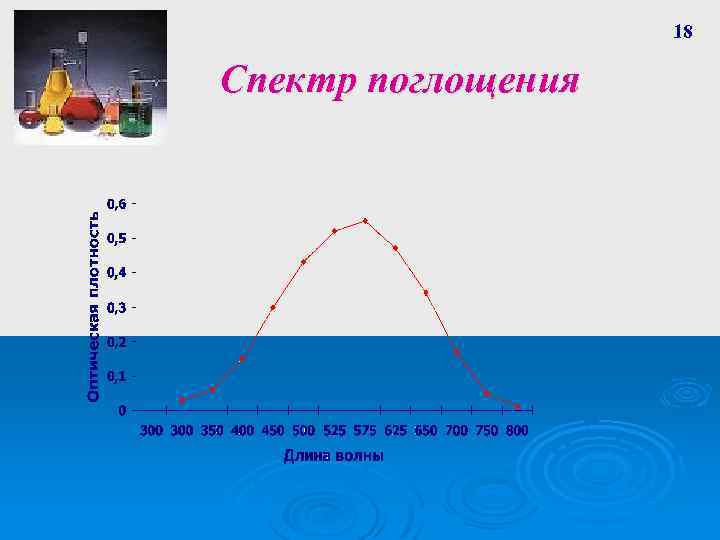 18 Спектр поглощения
18 Спектр поглощения
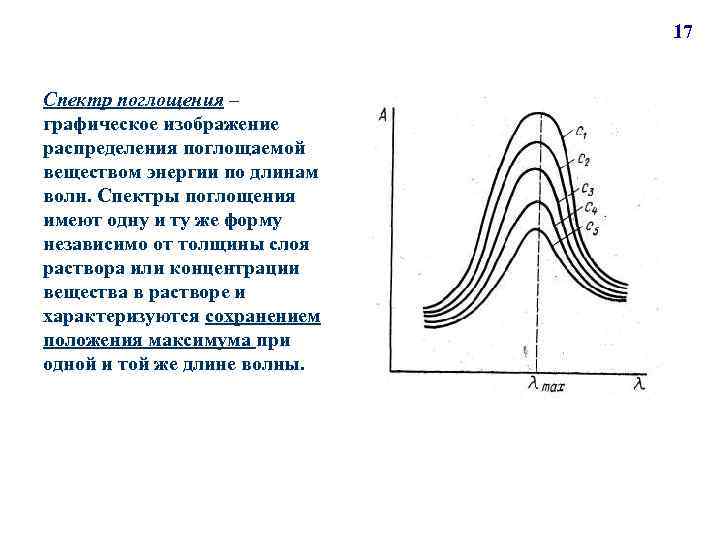 17 Спектр поглощения – графическое изображение распределения поглощаемой веществом энергии по длинам волн. Спектры поглощения имеют одну и ту же форму независимо от толщины слоя раствора или концентрации вещества в растворе и характеризуются сохранением положения максимума при одной и той же длине волны.
17 Спектр поглощения – графическое изображение распределения поглощаемой веществом энергии по длинам волн. Спектры поглощения имеют одну и ту же форму независимо от толщины слоя раствора или концентрации вещества в растворе и характеризуются сохранением положения максимума при одной и той же длине волны.
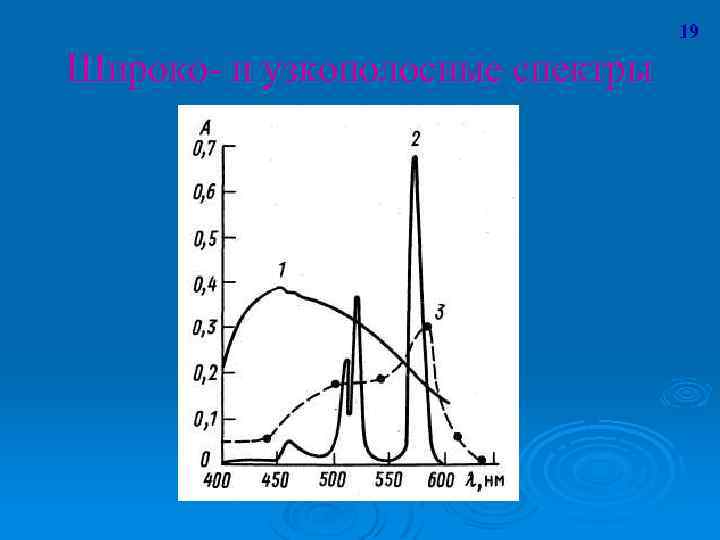 19 Широко- и узкополосные спектры
19 Широко- и узкополосные спектры
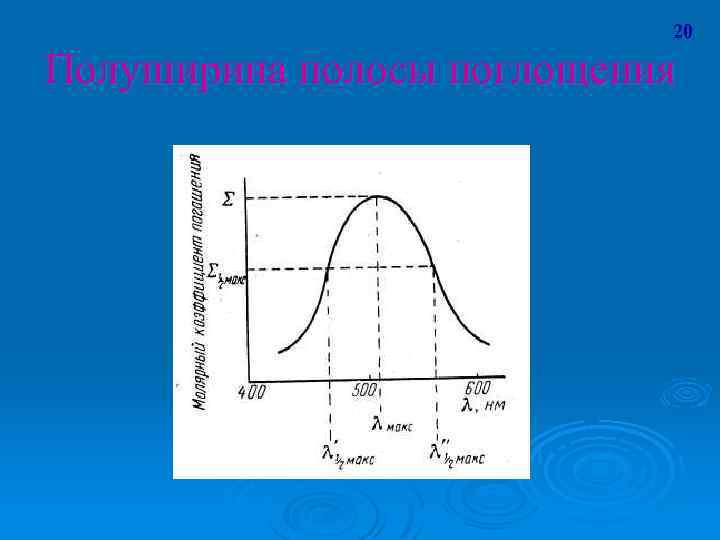 20 Полуширина полосы поглощения
20 Полуширина полосы поглощения
 21 Закон аддитивности (Фирордт, 1873 г. ) Если в растворе содержится n светопоглощающих компонентов, которые не вступают друг с другом в химическое взаимодействие, то при условии соблюдения основного закона светопоглощения оптическая плотность такого раствора будет равна сумме парциальных оптических плотностей всех содержащихся в растворе светопоглощающих компонентов. (17)
21 Закон аддитивности (Фирордт, 1873 г. ) Если в растворе содержится n светопоглощающих компонентов, которые не вступают друг с другом в химическое взаимодействие, то при условии соблюдения основного закона светопоглощения оптическая плотность такого раствора будет равна сумме парциальных оптических плотностей всех содержащихся в растворе светопоглощающих компонентов. (17)
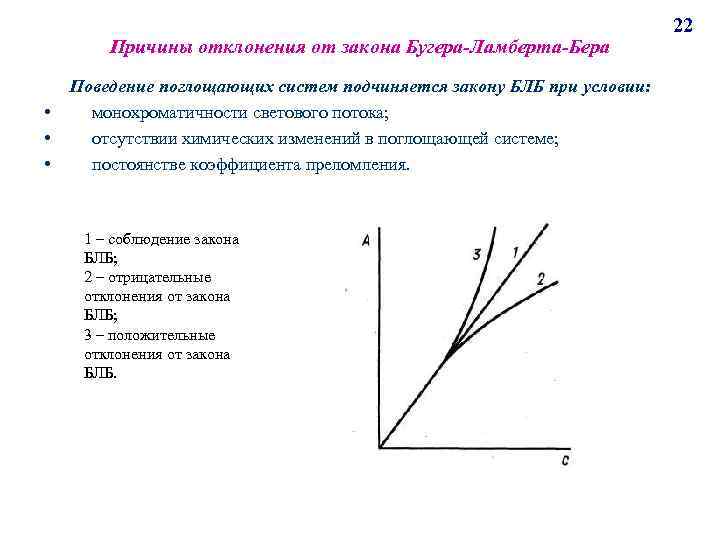 Причины отклонения от закона Бугера-Ламберта-Бера • • • Поведение поглощающих систем подчиняется закону БЛБ при условии: монохроматичности светового потока; отсутствии химических изменений в поглощающей системе; постоянстве коэффициента преломления. 1 – соблюдение закона БЛБ; 2 – отрицательные отклонения от закона БЛБ; 3 – положительные отклонения от закона БЛБ. 22
Причины отклонения от закона Бугера-Ламберта-Бера • • • Поведение поглощающих систем подчиняется закону БЛБ при условии: монохроматичности светового потока; отсутствии химических изменений в поглощающей системе; постоянстве коэффициента преломления. 1 – соблюдение закона БЛБ; 2 – отрицательные отклонения от закона БЛБ; 3 – положительные отклонения от закона БЛБ. 22
 23 Причины отклонений Кажущиеся Физические (инструментальные) Химические Истинные
23 Причины отклонений Кажущиеся Физические (инструментальные) Химические Истинные
 24 Полимеризация n. C 6 H 5 CH 2 OH ↔ (C 6 H 5 CH 2 OH)n мономер λмакс=2, 7 нм полимер λмакс=3, 0 нм
24 Полимеризация n. C 6 H 5 CH 2 OH ↔ (C 6 H 5 CH 2 OH)n мономер λмакс=2, 7 нм полимер λмакс=3, 0 нм
 25 Изобестическая точка А 1 405 нм 2 о 370 нм 450 нм λ, нм
25 Изобестическая точка А 1 405 нм 2 о 370 нм 450 нм λ, нм
 Фотометрическая реакция К фотометрическим реакциям прибегают в следующих случаях: Ø определяемый компонент не окрашен или интенсивность его светопоглощения мала; Ø полосы поглощения определяемого и посторонних компонентов перекрываются; Ø определяемый компонент присутствует в виде множества различных химических форм. 26
Фотометрическая реакция К фотометрическим реакциям прибегают в следующих случаях: Ø определяемый компонент не окрашен или интенсивность его светопоглощения мала; Ø полосы поглощения определяемого и посторонних компонентов перекрываются; Ø определяемый компонент присутствует в виде множества различных химических форм. 26
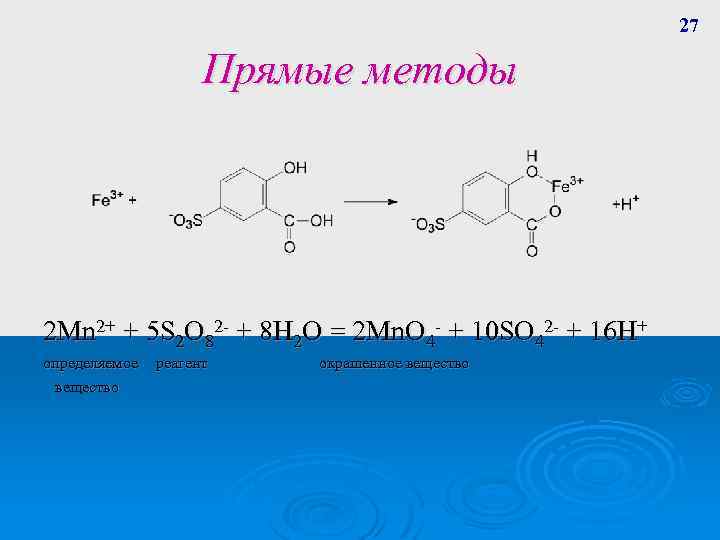 27 Прямые методы 2 Mn 2+ + 5 S 2 O 82 - + 8 H 2 O = 2 Mn. O 4 - + 10 SO 42 - + 16 H+ определяемое вещество реагент окрашенное вещество
27 Прямые методы 2 Mn 2+ + 5 S 2 O 82 - + 8 H 2 O = 2 Mn. O 4 - + 10 SO 42 - + 16 H+ определяемое вещество реагент окрашенное вещество
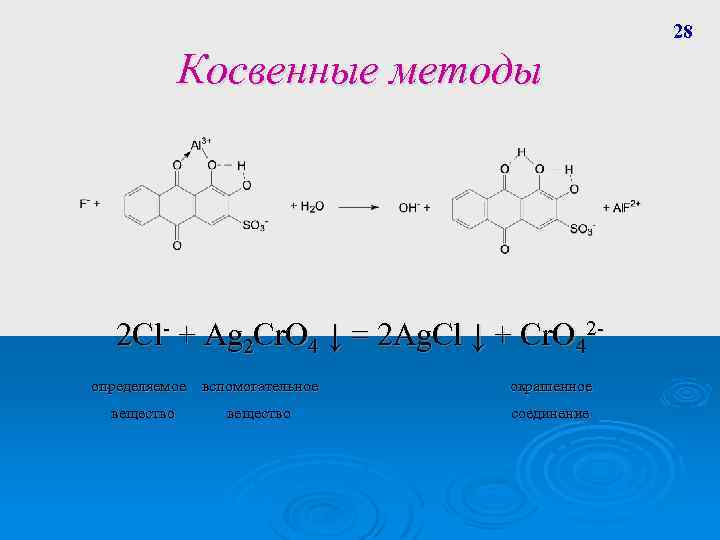 28 Косвенные методы 2 Cl- + Ag 2 Cr. O 4 ↓ = 2 Ag. Cl ↓ + Cr. O 42 определяемое вспомогательное вещество окрашенное соединение
28 Косвенные методы 2 Cl- + Ag 2 Cr. O 4 ↓ = 2 Ag. Cl ↓ + Cr. O 42 определяемое вспомогательное вещество окрашенное соединение


