ГИБРИДОМЫ Тоджаева Д 481а 2012.pptx
- Количество слайдов: 18

1 ГИБРИДОМЫ Получение моноклональных антител

Историческая справка На основании достижений клеточной биологии: • разработке метода гибридизации соматических клеток • получении линий миеломных клеток 1976 г. - Г. Келер (G. Koehler) и Ц. Мильштейн (C. Milstein) получили гибриды миеломных и нормальных АТОК, обладающих необходимыми свойствами: 1. «Бессмертие» (неограниченная пролиферация – от опухолевой клетки) 2. Способность синтезировать АТ заданной специфичности ( от нормальной АТОК) 1984 г. - Нильс Йерне, Георг Кёлер, Сезар Мильштейн получили Нобелевскую премию за учение об идиотипической сети, за создание гибридомной технологии получения моноклональных антител. 2
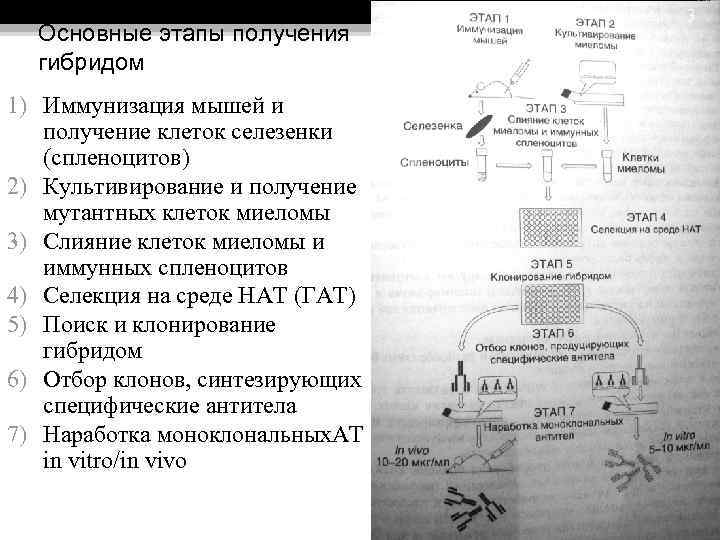
Основные этапы получения гибридом 1) Иммунизация мышей и получение клеток селезенки (спленоцитов) 2) Культивирование и получение мутантных клеток миеломы 3) Слияние клеток миеломы и иммунных спленоцитов 4) Селекция на среде НАТ (ГAT) 5) Поиск и клонирование гибридом 6) Отбор клонов, синтезирующих специфические антитела 7) Наработка моноклональных. АТ in vitro/in vivo 3

4 1. Иммунизация и получение спленоцитов Для иммунизации целевым АГ используют инбредные линии мышей, сингенные, по отношению к плазмоцитоме (чаще всего линию BALB/c). Мышей забивают цервикальной дислокацией, извлекают селезенку и готовят суспензию отдельных клеток.
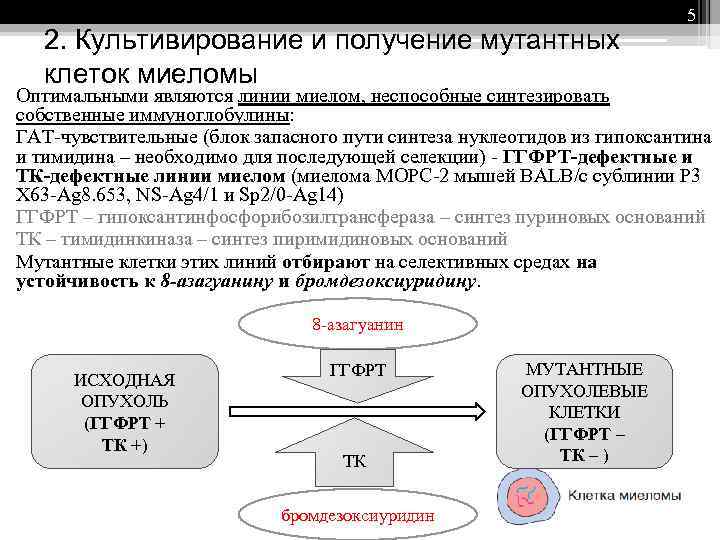
2. Культивирование и получение мутантных клеток миеломы 5 Оптимальными являются линии миелом, неспособные синтезировать собственные иммуноглобулины: ГАТ-чувствительные (блок запасного пути синтеза нуклеотидов из гипоксантина и тимидина – необходимо для последующей селекции) - ГГФРТ-дефектные и ТК-дефектные линии миелом (миелома МОРС-2 мышей BALB/c сублинии P 3 X 63 -Ag 8. 653, NS-Ag 4/1 и Sp 2/0 -Ag 14) ГГФРТ – гипоксантинфосфорибозилтрансфераза – синтез пуриновых оснований ТК – тимидинкиназа – синтез пиримидиновых оснований Мутантные клетки этих линий отбирают на селективных средах на устойчивость к 8 -азагуанину и бромдезоксиуридину. 8 -азагуанин ИСХОДНАЯ ОПУХОЛЬ (ГГФРТ + ТК +) ГГФРТ ТК бромдезоксиуридин МУТАНТНЫЕ ОПУХОЛЕВЫЕ КЛЕТКИ (ГГФРТ – ТК – )
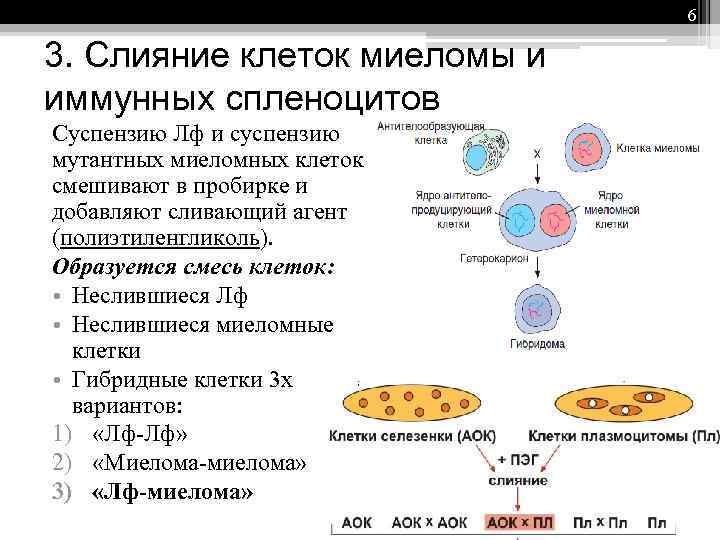
6 3. Слияние клеток миеломы и иммунных спленоцитов Суспензию Лф и суспензию мутантных миеломных клеток смешивают в пробирке и добавляют сливающий агент (полиэтиленгликоль). Образуется смесь клеток: • Неслившиеся Лф • Неслившиеся миеломные клетки • Гибридные клетки 3 х вариантов: 1) «Лф-Лф» 2) «Миелома-миелома» 3) «Лф-миелома»

7 4. Селекция на среде НАТ (ГAT) Полученную смесь клеток отмывают и разводят в объеме селективной среды НАТ (ГАТ – гипоксантин-аминоптерин тимидин). Аминоптерин — яд, подавляющий основной путь биосинтеза нуклеотидов. Гипоксантин и тимидин — субстраты для запасных путей, заблокированных у мутантных(ГГФРТ – ; ТК –) миеломных клеток (о чем свидетельствует устойчивость к 8 -азагуанину и бромдезоксиуридину) В течение 7 -10 дней культивирования, происходит: 1) Неслившиеся Лф и «Лф-Лф» погибают, поскольку не способны длительное время выживать in vitro 2) Неслившиеся клетки миеломы и «миелома-миелома» погибают, поскольку в среде HAT нет субстрата для синтеза ими нуклеотидов или этот процесс заблокирован 3) «Лф-миелома» выживают, т. к. биосинтез пуриновых оснований из гипоксантина обеспечен ГГФРТ, а биосинтез пиримидиновых оснований из тимидина – ТК.
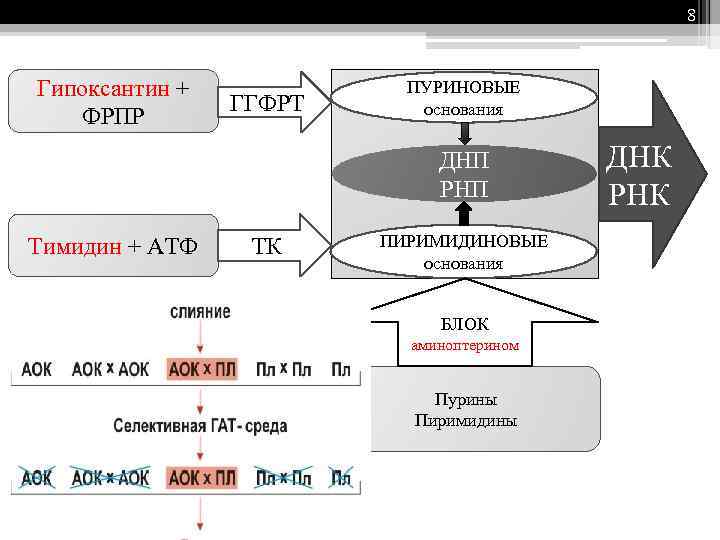
8 Гипоксантин + ФРПР ГГФРТ ПУРИНОВЫЕ основания ДНП РНП Тимидин + АТФ ТК ПИРИМИДИНОВЫЕ основания БЛОК аминоптерином Пурины Пиримидины ДНК РНК

9 5. Поиск и клонирование гибридом Выжившие клетки переводят сначала на среду НТ, а затем на обычную ростовую среду RPMI 1640. Пролиферация «non-stop» позволяет клонировать гибридные клетки: • проводят несколько пассажей клеток, постепенно увеличивая их разведение вплоть до одной клетки на лунку (для каждого пассажа берут клетки из лунок с наибольшим титром антител) • затем надо подождать, пока в условиях культивирования вырастет клон (много одинаковых клеток)

10 6. Отбор клонов, синтезирующих специфические антитела § АТ к растворимым антигенам выявляют в иммуноферментной тест-системе § АТ к мембранным — методом проточной цитометрии Поддерживают те клоны, которые обладают преимуществами перед другими: üПо специфичности антител üПродуктивности üПо скорости роста üПо изотипу (предпочтитение отдают Ig. Gантителам)
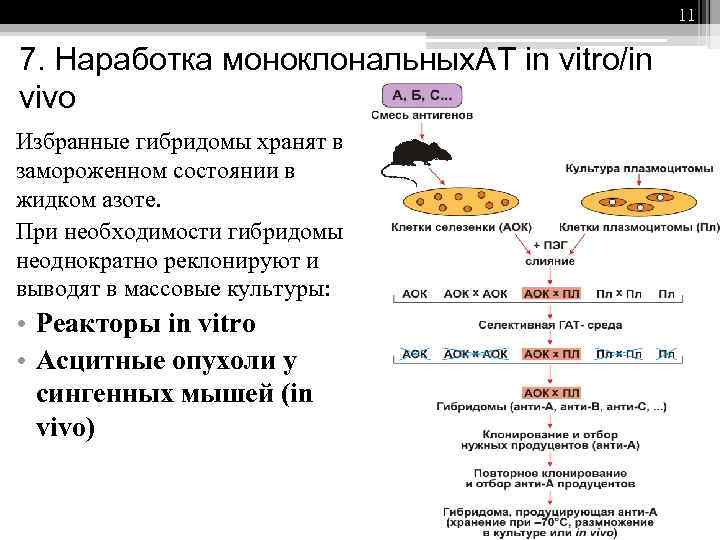
11 7. Наработка моноклональных. АТ in vitro/in vivo Избранные гибридомы хранят в замороженном состоянии в жидком азоте. При необходимости гибридомы неоднократно реклонируют и выводят в массовые культуры: • Реакторы in vitro • Асцитные опухоли у сингенных мышей (in vivo)

12 Новые задачи ØМышиные антитела плохо подходят для использования в клинической практике — они вызывают иммунный ответ в организме человека. Стремление создать полностью человеческие антитела (гуманизация мышиных АТ) ØИммунизация — необходимое условие для получения гибридомы, но не все молекулы могут легко активировать АОК. Требуется новый метод, который бы позволил получать антитела нужной аффинности и специфичности, не прибегая к иммунизации мышей.

13 «Гуманизация» мышиных АТ Химерные АТ - генетические комплексы, объединяющие: • V-ген мыши • С-ген человека «Замещенные» АТ: • Гипервариабельные CDR участки V-генов мыши • Каркасные участки V-генов человека • С-гены человека Минимальные АТ – генно-инженерные Fv- фрагменты, созданные с помощью специальной технологии фагового дисплея: Ø одноцепочечные антитела (single chain Fv-fragments), которые получают в результате экспрессии V(H) и V(L)-участков, соединенных олигонуклеотидом, кодирующим гибкий гидрофильный пептид Ø Fv-фрагменты - нековалентно ассоциированные гетеродимеры V(H) и V(L) – доменов, соединенные дисульфидными связями Ø V –домены Н-цепей - Применение основано на часто встречающемся свойстве отдельного вариабельного домена тяжелой цепи сохранять специфичность и высокое сродство (10% и выше от сродства исходного полноразмерного антитела) к антигену. Ø минимальные узнающие пептиды (minimal recognition units, m. r. u. ) - аналоги CDR-участков V-доменов.

14 Характеристика моноклональных. АТ • Высокая степень афинности, к заданной АГ-ой детерминанте • Идентичность по изотипу, аллотипу, идиотипу, аффинитету, физико-химическим свойствам Получение АТ, специфичных по отношению: ØК имуногенным АГ, определяющим гистосовместимость и дифференцировку ØОпухолевым, дифференцировочным и др. АГ клеточной поверхности ØВирусным и бактериальным АГ ØЕдиничным антигенным детерминантам разнообразных белков, НК, сахаров. Позволяет применять мон. АТ в различных отраслях наук.

15 Применение моноклональных. АТ в медицине На основе мон. АТ разработаны: • Системы диагностирования различных заболеваний (бакт-х, вирусных, онкологических) и их локализацию • Лекарственные препараты (например иммуноадгезины, рекомбинантные иммунотоксины, иммуноадгезины иммуноферменты, противоопухолевые, иммуноферменты антицитокиновые и др. ) • Способы доставки лек-х веществ • Иммуносорбция (выделение или удаление из крови пациента антигенов или клеток данной специфичности – например при аутоиммунных заболеваниях)

16 Применение в иммунологии: • Методы определения и разделения субпопуляций клеток • Методы определения отдельных стадий развития клеток ( в том числе анализ эмбрионального развития) • Методы более точного типирования тканей, идентификации микроорганизмов • Методы более надежного определения биологически важных молекул • Установление функций молекул клеточной поверхности • Анализ сложных смесей антигенов • Квадромы • Искусственные ферменты (абзимы)

17 В биологии и сельском хозяйстве гибридомную технологию применяют в целях изучения и проведения клонирования растений и животных.

18 СПАСИБО ЗА ВНИМАНИЕ
ГИБРИДОМЫ Тоджаева Д 481а 2012.pptx