5. Хромосомный уровень наследственного материала.pptx
- Количество слайдов: 69

1

ГБОУ ВПО Самарский государственный медицинский университет Кафедра медицинской биологии, генетики и экологии тема: «ХРОМОСОМНЫЙ УРОВЕНЬ 95 лет Сам. ГМУ НАСЛЕДСТВЕННОГО МАТЕРИАЛА. » Заведующая кафедрой доктор биологических наук, профессор Лидия Николаевна Самыкина лекция № 5 октябрь 2014.

Генетический материал эукариот имеет сложную надмолекулярную организацию, структурными компонентами которых являются хромосомы. Термин хромосомы был веден в 1888 году Валдейером. 3

I. Развитие представлений о хромосомах человека 70 -е годы XIX века - О. Гертвиг и В. Флемминг описали окрашиваемые нитевидные структуры в ядрах клеток эукариот 1879 г. – Дж. Арнольд (J. Arnold) – первая визуализация хромосом человека 1888 г. - В. Вальдейер (W. Waldeyer) назвал эти структуры ХРОМОСОМАМИ (chroмa –цвет; soma – тело) 1896 г. – Э. Вильсон (E. Wilson) - «Клетка, ее роль в наследственности и развитии» - заложены основы современной клеточной биологии и цитогенетики 1904 г. – В. Сеттон (W. Sutton) и Т. Бовери (Th. Boveri)– гипотеза о связи хромосом с элементами наследственности.

Определение числа хромосом у человека и детальное описание их морфологии (1956 г. ) J-H. Tjio (1919– 2001) A. Levan (1905– 1998).

• 1959 г. – Ж. Лежен (J. Lejeune) идентифицировал трисомию по хромосоме 21 при синдроме Дауна • 1960 г. – Х. Эдвардс (H. Edwards) описал синдром трисомии по хромосоме 18 ( синдром Эдвардса) • 1960 г. – К. Патау (K. Patau) описал синдром трисомии по хромосоме 13 (синдром Патау) РОЖДЕНИЕ МЕДИЦИНСКОЙ ЦИТОГЕНЕТИКИ!

Появление методов идентификации хромосом и их отдельных районов (конец 60 -х – начало 70 -х годов XX в. ) • 1968 г. – Т. Касперсон (T. Caspersson) применил для исследования метафазных хромосом метод дифференциальной Q-окраски • 1971 г. – М. Дретс (M. Drets) и М. Шау (M. Shaw) использовали GTG-метод дифференциальной окраски хромосом

Внедрение и широкое использование молекулярно-цитогенетических методов (с 1986 года) • 1986 г. - первые молекулярно-цитогенетические эксперименты на хромосомах человека – FISH- метод • 1992 г. - разработка метода сравнительной геномной гибридизации (CGH-си джи эйч) D. Pinkel A. Kallionieme

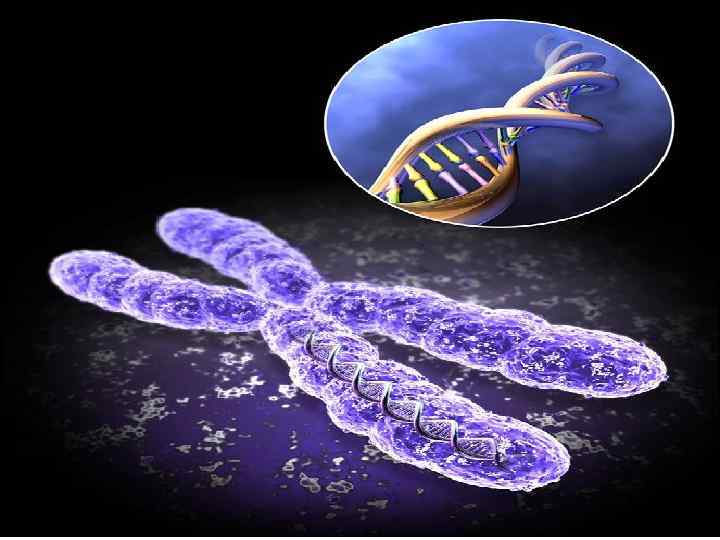
Реально хромосома представляет собой гигантскую нить с огромной функциональной поверхностью. Переход от интерфазы к метафазе характеризуется нарастающей спирализацией и упаковкой хромосом. 9
10

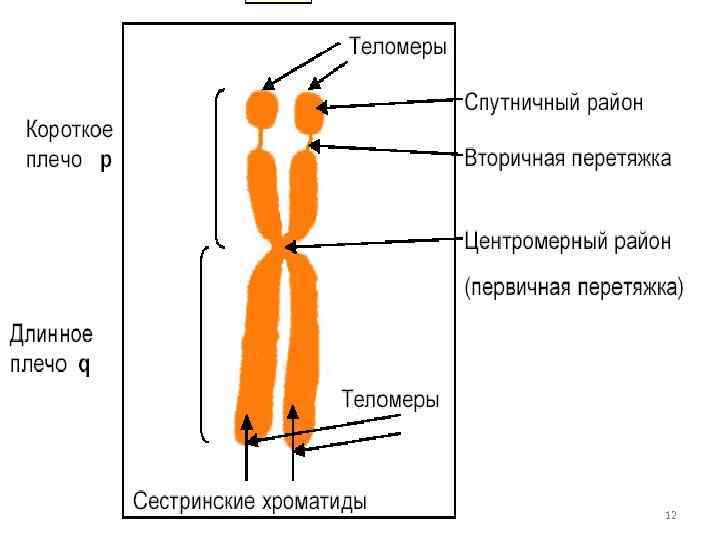
Хромосомы представляют собой удлиненные палочковидные структуры, имеющие два плеча, на конце которых располагается теломера. 11
12

СТРОЕНИЕ ТЕЛОМЕРЫ • Теломеры представляют собой в основном двунитевые некодирующие повторы (ТТАГГГ)n, заканчивающиеся 3’-однонитевым участком • Размер двунитевого участка варьируется от 3 до 20 т. п. н. , однонитевого – от 100 до 200 пар оснований «Теломеры состоят из 5 -20 kb тандемов гексануклеотидных сателлитных повторенных единиц TTAGGG и интенсивно окрашиваются методом Т-бэндинга» . (ISCN, 2009)

ФЕРМЕНТ ТЕЛОМЕРАЗА ОБЕСПЕЧИВАЕТ РЕПЛИКАЦИЮ ТЕЛОМЕРНОЙ ДНК Ø Резкое уменьшение активности теломеразы и укорочение теломер обычно сопутствует клеточной дифференцировке. Ø Часто наблюдается зависимость размера теломеры от возраста человека (возраст-зависимое прогрессивное укорочение теломер) Феномен репликативного старения клеток, вызванного концевой недорепликацией ДНК, был предсказан А. Оловниковым в 1971 г. За биохимическое доказательство его идеи Э. Блэкберн (E. Blackburn), К. Грейдер (C. Greider) и Д. Шостак (J. Szostak) были удостоены в 2009 г. Нобелевской премии по физиологии и медицине. Ø Нарушение организации теломерных районов приводит к хромосомным перестройкам.

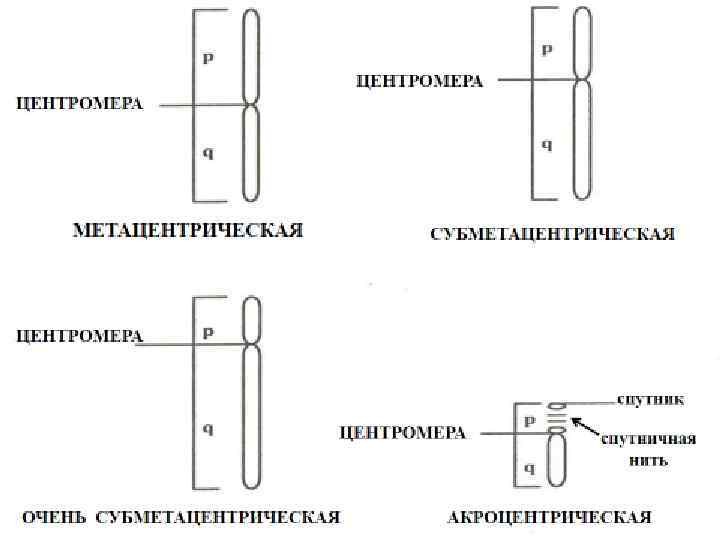
Центромера или первичная перетяжка в хромосомах с разной морфологией находится в разном положении по отношению к ее концам. 15
16

В зависимости от расположения центромеры и взаимного расположения плеч выделяют следующие типы хромосом: 1. метацентрические, имеющие примерно одинаковые плечи; 2. акроцентрические, имеющие одно очень короткое и одно очень длинное плечо; 3. субметацентрические, у которых одно длинное и одно более короткое плечо ; 4. телоцентрические, у которых одно плечо отсутствует; 5. спутничные, у которых есть не только первичная, но и вторичная перетяжка — ядрышковый организатор. 17

18

Хромосомы эукариот представляют собой нуклеопротеиды. Структурной основой служит комплекс ДНК-гистон. Николай Константинович Кольцов - основатель экспериментальной биологии в России - в 1927 году дал следующее определение: «В основе каждой хромосомы лежит тончайшая нить, которая представляет собой спиральный ряд огромных генетических молекул — генов, или является одной гигантской молекулой» . 19

Из двух компонентов хромосом - ДНК отличается стабильностью в пределах жизни клетки и генетической непрерывностью при размножении клеток. Гистоны в нуклеопротеидах постоянно обновляются. ДНК связана с гистонами ионными связями, между ДНК и гистонами 14 различных взаимодействий. 20

Преобразование интерфазной хромосомы, которое идет в течение всей профазы митоза, осуществляется при помощи сложных процессов упаковки и спирализации. В результате самая крупная хромосома в кариотипе человека оказывается равной 6 -8 мк. Таким образом, происходит уменьшение длины хромосомы в 10 000 раз. 21
• ХРОМОСОМЫ ЛОКАЛИЗОВАНЫ В ЯДРЕ КЛЕТКИ • должна быть высокая степень компактизации нити ДНК, которая обеспечивается при ее связывании с различными белками ДНК + БЕЛКИ ХРОМОСОМ = ХРОМАТИН

ЭУХРОМАТИН и ГЕТЕРОХРОМАТИН n n Эухроматин n Менее конденсированные районы хромосом n Транскрипционно активен Гетерохроматин n Плотные, компактные (конденсированные) районы хромосом интенсивно окрашиваются. n Обычно выявляются в зоне первичной перетяжки (центромера) n Транскрипционно неактивен (в целом) n Поздно реплицируется в S-фазе митоза (асинхронно с эухроматином)
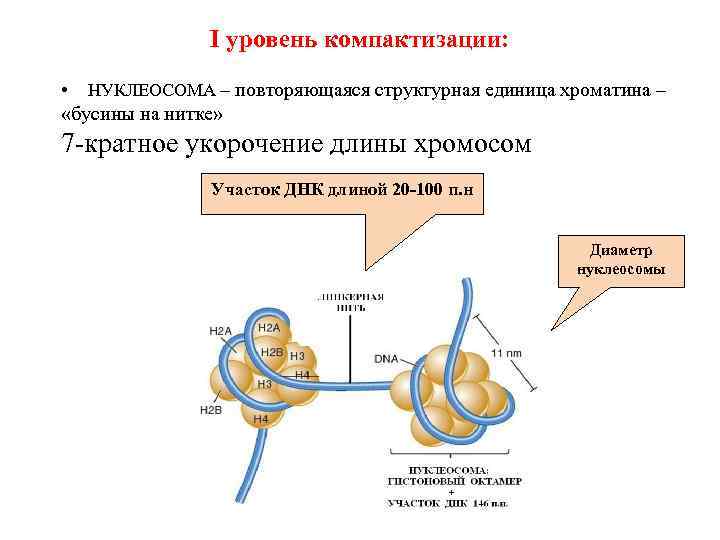
I уровень компактизации: • НУКЛЕОСОМА – повторяющаяся структурная единица хроматина – «бусины на нитке» 7 -кратное укорочение длины хромосом Участок ДНК длиной 20 -100 п. н Диаметр нуклеосомы
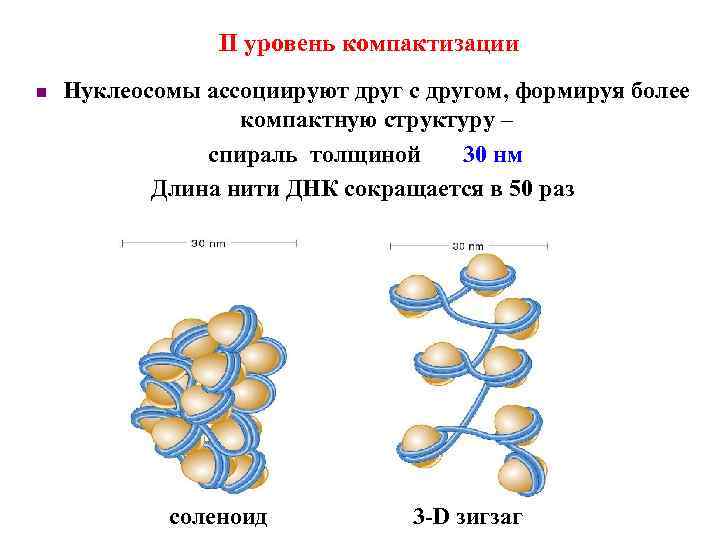
II уровень компактизации n Нуклеосомы ассоциируют друг с другом, формируя более компактную структуру – спираль толщиной 30 нм Длина нити ДНК сокращается в 50 раз соленоид 3 -D зигзаг

III уровень компактизации § Взаимодействие между 30 нм фибриллами и ядерным матриксом (негистоновые белки - ламины, Sc. II, ядерная мембрана, поровые комплексы, внутриядерная сеть) или белковым каркасом хромосом (scaffold) хроматиновые (радиальные) петли (25 000 -200 000 п. н. ) Районы прикрепления к матриксу или к scаffold

27

НОМЕНКЛАТУРА ХРОМОСОМ ЧЕЛОВЕКА • Денверская конференция (1960 г. ) – предложена система описания хромосом • Лондонская конференция (1963 г. ) – официально введено разделение хромосом на 7 морфологических групп (A – G) • V Международный конгресс по генетике человека (Мехико, 1972 г. ) – появление первой официальной номенклатуры хромосом человека «An International System for Human Cytogenetic Nomenclature» (Международная цитогенетическая номенклатура хромосом человека) (ISCN, 1978)


Недостатки Денверской классификации были впервые исправлены на международном совещании в 2009 году. Эта классификация рассматривает не группу хромосом, а каждую хромосому в отдельности. 30

В 1966 году М. Сасаки и А. Норман выделили деспирализованную интерфазную хромосому из клеточного ядра человека. Ее длина оказалась 7. 5 см. Это первая хромосома. 31

Хромосома 1— самая большая хромосома, на ее долю приходится почти 10% генома человека. Число генов - около 3000. Более 160 генов связаны с разнообразными заболеваниями: болезнь Альцгеймера, болезнь Гоше, рак протоков молочной железы, кардиомиопатия, катаракта, эктодермальная дисплазия, гипотиреоидизм, острая лимфобластная лейкемия, нейробластома, рак простаты, атеросклероз. 32

Хромосома 2 - в ней содержится меньше генов, чем в первой хромосоме. Тем не менее, число заболеваний, связанных с мутациями в генах этой хромосомы, достаточно большое: цистинурия, диабет, рак прямой кишки, фиброматозис, гипотироидизм, ожирение, болезнь Паркинсона, аутосомная рецессивная глухота-9, дистрофия мышц конечностей. 33

Хромосома 3 — гены, содержащиеся в ней, связаны более с чем 90 различными заболеваниями: кардиомиопатия, рак прямой кишки, коллоректальный рак, гемолитическая анемия, гипокальцемия, карцинома почки, шизофрения. 34

Хромосома 4 - общее число генов ниже среднего. С этой хромосомой ассоциируют заболевания: болезнь Паркинсона, фенилкетонурия, гипохондроплазия, склонность к алкоголизму. - - - - - - - - - Хромосома 5— с генами этой хромосомы связан ряд тяжелых заболеваний: мегалопластическая анемия, колоректальный рак, дистрофия роговицы, аутосомная доминантная глухота, острая лейкемия, острая дистрофия, астма и др. 35

Хромосома 6 - диабет, спиноцеребральная атрофия, гемолитическая анемия, лейкемия, тромбофлибия, болезнь Паркинсона, чувствительность к туберкулезу. ----------------------------Хромосома 7 - хронический грануломотоз, рак прямой кишки, кистозный фиброз, вялая кожа, гемолитическая анемия, карликовость, врожденная миотония, панкреатит. 36

Хромосома 8 - число генов относительно небольшое, мутации в них приводят к таким заболеваниям как: хондросаркома, эпилепсия, атеросклероз, синдром Вернера, сфероцитоз и др. -------------------------Хромосома 9 - альбинизм, галактезимия, меланома, порфирия, стомацитоз, дистония, карценома базальных клеток. 37

Хромосома 10 - кардиомиопатия, почечная гиперплазия, катаракта, лейкемия, глиобластома, эндокринная неоплазия, аденокарцинома простаты. шизэнцефалия. Хромосома 11 - альбинизм, рак груди, рак мочевого пузыря, рак простаты, глухота, эритремия, кардиомиопатия, сфероцитоз. 38

Хромосома 12 – гены распределены в ней неравномерно. Заболевания: эмфизема, энурез, задержка роста, кератодерма, липома, наследственная миопатия, фенилкетонурия, синдром слюнных желез. 39

Хромосома 13 – гены секвенированы недостаточно, относительно других хромосом обеднена генами. Выявлены: рак мочевого пузыря, глухота, недостаточность факторов свертываемости крови, мышечная дистрофия, рак поджелудочной железы, болезнь Вильсона и др. 40

Хромосома 14 – содержатся гены, важные для работы иммунной системы, с мутациями в генах этой хромосомы связан ряд тяжелых заболеваний: ранняя форма болезни Альцгеймера, кардиомиопатия, сфероцитоз, фенилкетонурия. 41

Хромосома 15 - секвенирована неполностью. Выявлен большой спектр заболеваний: альбинизм, синдром Барттера, синдром Блюма, гипомеланоз, гинекомастия, лейкемия, мышечная дистрофия, эпилепсия, шизофрения и др. 42

Хромосома 16 - рак желудка, эритроцитоз, миелоидная лейкемия, тирозинемия, поликистозная болезнь почек, карцинома яичника, мукополисахаридоз, болезнь рыбьих глаз. 43

Хромосома 17 - высокое содержание генов: спорадический рак груди, рак прямой кишки, диабет, гемолитическая анемия, рак языка, миостенический синдром, острая лейкемия, мышечная дистрофия, нейробластома, рак яичника, буллезный эпидермолиз. 44

Хромосома 18 - общее число генов , мутации в которых связанны с патологиями, невелико: амилоидоз, рак прямой кишки, рак поджелудочной железы, лимфома, буллезный эпидермолиз и др. 45

Хромосома 19 - наиболее богата ГЦ-парами нуклеотидов, имеются последовательности, гомологичные последовательностям на 16 -й и других хромосомах. С этими мутациями в этой хромосоме связывают патологии: рак прямой кишки, миотоническая дистрофия, атеросклероз коронарной артерии; гипертрофическая кардиомиопатия, миотоническая дистрофия, лимфобластная лейкемия, сахарный и идиопатический диабет и др. заболевания человека. 46

Хромосома 20 - по размеру составляет всего около 2% от генома человека. Гены этой хромосомы несут информацию о ряде заболеваний, начиная от ожирения и экземы и заканчивая слабоумием и катарактой. 47

С мутациями в генах 20 -й хромосомы связаны: болезни сердца, тяжелые нарушения иммунной системы, астма, скелетная дисплазия, диабет и многие другие. 48

Хромосома 21 - самая маленькая по размерам и информационной ёмкости хромосома (в ней обнаружено всего 200 генов). В ней есть участок из 7 млн. пар нуклеотидов (это больше всего генома бактерии E. Coli) содержащий только один ген. При наличии трех копий этой хромосомы возникает болезнь Дауна. Мутации в этой хромосоме вызывают аномалии сердца и нервной системы. 49

50

Хромосома 22 – наиболее полно описана (нерасшифровано около 3 %), секвенирована первой (1999 год). Она содержит 500 генов. Для этой хромосомы установлены функции примерно половины генов , около 160 генов показывают значительную гомологию с генами мыши. Несмотря на свои большие размеры и малое число генов, ее патология установлена при некоторых генетических и онкологических заболеваниях. 51

Х-хромосома – женская половая хромосома, наличие двух Х-хромосом определяет женский пол (ХХ-хромосома), ХY – мужской пол. Генов в Х-хромосоме немного, с ними связаны следующие заболевания: рак груди, рак простаты, кардиомиопатия, эпилепсия, гемофилия В, ихтиоз, синдром Барта, мукополисахароидоз. 52

Y-хромосома - мужская половая хромосома, в ней содержится совсем немного генов, меньше 100. Скорости мутации в этой хромосоме в 4 раза выше, чем в X-хромосоме. В ней содержится большое число палиндромов. Палиндромы – последовательность ДНК, которая одинаково читается от 5’ и 3’ – концов. 53

Основная роль тех генов, которые имеются в Y-хромосоме, заключается в контролировании дифференцировки пола, формировании яичек и процессов сперматогенеза. В частности, основной ген «самцовости» (SRY фактор), кодирует белок, который включает в работу многие гены других хромосом и тем самым вызывает каскад биохимических реакций (конечный результат - образование яичек). На сегодняшний день это самый консервативный ген внутри вида. 54

Отмечены случаи, когда в клетках имеется не одна, а две и даже три копии Y-хромосомы. При этой патологии проявляется асоциальное поведение и различные психологические нарушения у 35% больных. Совсем немного генов ассоциировано с болезнями человека. Основные из них – гонадный дисгенез и синдром клеток Сертоли. 55
МОЛЕКУЛЯРНО-ЦИТОГЕНЕТИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ Ø ФЛЮОРЕСЦЕНТНАЯ IN SITU ГИБРИДИЗАЦИЯ (FISH) Ø МЕТАФАЗНАЯ СРАВНИТЕЛЬНАЯ ГЕНОМНАЯ ГИБРИДИЗАЦИЯ (CGH) Молекулярное кариотипирование

FISH-метод: локус-специфическая флюоресцентная гибридизация in situ гибридизация • Пренатальная или предимплантационная диагностика наиболее частых анеуплоидий (интерфазная FISH – локус-специфическая флюоресцентная гибридизация) • Диагностика известных микроделеционных синдромов • Уточнение цитогенетического диагноза • Идентификация сверхчисленных маркерных хромосом • Диагностика сложных комплексных хромосомных аберраций
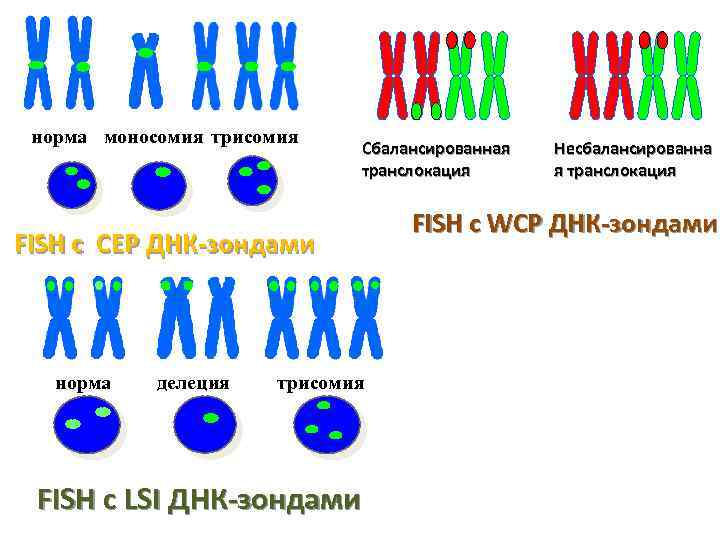
норма моносомия трисомия Сбалансированная транслокация FISH c CEP ДНК-зондами норма делеция трисомия FISH с LSI ДНК-зондами Несбалансированна я транслокация FISH c WCP ДНК-зондами

• Гибридизация нуклеиновых кислот in situ была разработана для локализации фрагментов нуклеиновых кислот в метафазных и профазных хромосомах. Это нашло широкое применение в анализе хромосомных патологий. В его основе лежит создание препаратов ДНК, содержащих последовательности нуклеотидов, отвечающих определенным требованиям. Гибридизация in situ заключается в денатурации ДНК-пробы и цитологического препарата с последующей ренатурацией, обеспечивающей формирование дуплексов меченной ДНК и ДНК-препарата. 59

МЕТАФАЗНАЯ СРАВНИТЕЛЬНАЯ ГЕНОМНАЯ ГИБРИДИЗАЦИЯ (CGH) array-CGH ( СГГ – сравнительная геномная гибридизация) Ø Возможность одновременной детекции ануплоидий, делеций, дупликаций и/или амплификации любого локуса, представленного на микрочипе 1 анализ array CGH эквивалентен 1000 FISH-анализам! Ø Мощный инструмент детекции субмикроскопических хромосомных аномалий у пациентов с идиопатической умственной отсталостью и множественными врожденными пороками развития Ø Обеспечивает более детальный, автоматизированный и менее субъективный анализ аномального количества копий ДНК по сравнению со стандартным цитогенетическим исследованием Ø Может быть использован при исследовании архивного материала и тканей с неделящимися клетками

Сравнительная геномная гибридизация – новый стандарт диагностики в репродуктивной медицине. Сравнительная геномная гибридизация имеет разрешение в 1000 и более раз выше, чем обычное кариотипирование. CGH Array является единственным методом, позволяющим диагностировать все возможные микроделецийные синдромы в пределах всего генома, что позволит своевременно провести соответствующую коррекцию ВПР и поспособствует тем самым снижению смертности, инвалидности детей и повышению уровня их здоровья. 61

• Разработанные методы анализа хромосом за короткое время позволили установить хромосомную природу многих заболеваний. • В настоящее время различают почти 1000 хромосомных синдромов, их вклад в спонтанные аборты, неонатальную смертность и заболеваемость весьма значительный. Большинство хромосомных болезней характеризуется наличием множественных врожденных пороков развития. 62
БЛАГОДАРЮ ЗА ВНИМАНИЕ! 63

ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ГЕНОМНЫЕ МУТАЦИИ ХРОМОСОМНЫЕ МУТАЦИИ Ø СТРУКТУРНЫЕ (аберрации) Ø ЧИСЛОВЫЕ • АНЕУПЛОИДИЯ • ПОЛИПЛОИДИЯ • • ДЕЛЕЦИЯ ДУПЛИКАЦИЯ ИНВЕРСИЯ ИНСЕРЦИЯ ТРАНСЛОКАЦИЯ ИЗОХРОМОСОМА КОЛЬЦЕВАЯ ХРОМОСОМА

ЧИСЛОВЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ПОЛИПЛОИДИЯ АНЕУПЛОИДИЯ • АНОМАЛИИ ХРОМОСОМ, СВЯЗАННЫЕ С НАРУШЕНИЕМ ЧИСЛА ЦЕЛЫХ ХРОМОСОМНЫХ НАБОРОВ • АНОМАЛИИ ХРОМОСОМ, СВЯЗАННЫЕ С НАРУШЕНИЕМ ЧИСЛА ОТДЕЛЬНЫХ ХРОМОСОМ

ПОЛИПЛОИДИЯ ТРИПЛОИДИЯ ТЕТРАПЛОИДИЯ • ГЕНОМНАЯ МУТАЦИЯ, ПРИ КОТОРОЙ В КАРИОТИПЕ ИМЕЕТСЯ ТРИ ГАПЛОИДНЫХ НАБОРА ХРОМОСОМ • ГЕНОМНАЯ МУТАЦИЯ, ПРИ КОТОРОЙ В КАРИОТИПЕ ИМЕЕТСЯ ЧЕТЫРЕ ГАПЛОИДНЫХ НАБОРА ХРОМОСОМ 69, XXX, 69, XXY, 69 XYY 92, XXXX, 92, XXYY

АНЕУПЛОИДИЯ- геномная мутация при которой изменяется число копий гомологичных хромосом • НУЛЛИСОМИЯ – ПОЛНОЕ ОТСУТСТВИЕ ГОМОЛОГОВ КАКОЙ-ЛИБО ПАРЫ ХРОМОСОМ • МОНОСОМИЯ - ОТСУТСТВИЕ ОДНОЙ ИЗ ГОМОЛОГИЧНЫХ ХРОМОСОМ • ТРИСОМИЯ - НАЛИЧИЕ ДОПОЛНИТЕЛЬНОЙ ГОМОЛОГИЧНОЙ ХРОМОСОМЫ (САМАЯ ЧАСТАЯ ГЕНОМНАЯ МУТАЦИЯ!) • ТЕТРАСОМИЯ И ПОЛИСОМИЯ - НАЛИЧИЕ ЧЕТЫРЕХ И БОЛЕЕ КОПИЙ ГОМОЛОГИЧНЫХ ХРОМОСОМ • ДВОЙНЫЕ И ТРОЙНЫЕ ТРИСОМИИ - НАЛИЧИЕ ДОПОЛНИТЕЛЬНЫХ КОПИЙ ДВУХ ИЛИ ТРЕХ ПАР ГОМОЛОГИЧНЫХ ХРОМОСОМ
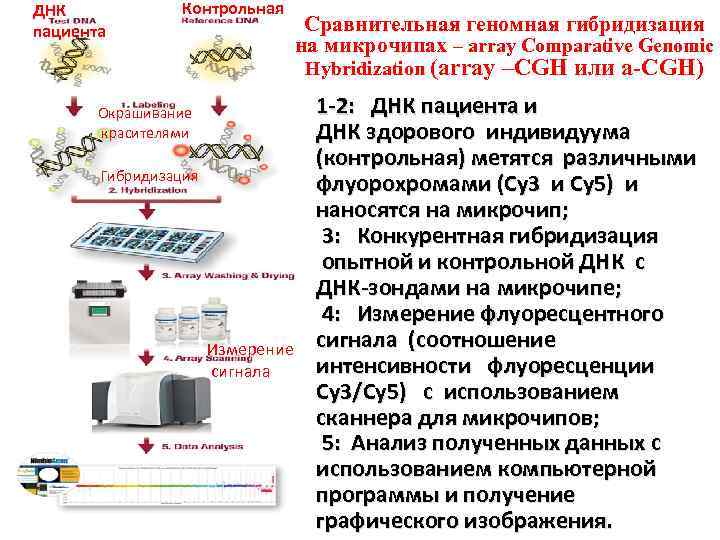
ДНК пациента Контрольная Сравнительная геномная гибридизация на микрочипах – array Comparative Genomic Hybridization (array Окрашивание красителями Гибридизация Измерение сигнала –CGH или a-CGH) 1 -2: ДНК пациента и ДНК здорового индивидуума (контрольная) метятся различными флуорохромами (Cy 3 и Cy 5) и наносятся на микрочип; 3: Конкурентная гибридизация опытной и контрольной ДНК с ДНК-зондами на микрочипе; 4: Измерение флуоресцентного сигнала (соотношение интенсивности флуоресценции Сy 3/Cy 5) с использованием сканнера для микрочипов; 5: Анализ полученных данных с использованием компьютерной программы и получение графического изображения.

Ограничения array CGH Ø Не выявляет сбалансированные хромосомные перестройки. Ø Сложности интерпретации CNVs (клинически значимые или нейтральный полиморфизм? ). Ø Не выявляет изменения количества копий в регионах генома, ДНК которых не присутствуют на микрочипе.
5. Хромосомный уровень наследственного материала.pptx