05Дыхание Bio.ppt
- Количество слайдов: 77

1. Энергетическое обеспечение ночью 2. Гетеротрофные ткани и органы (корни, эпидермис, запасающие органы и т. д. )

Углеводы Жиры Окисление органического вещества Белки 1. Запасание энергии: окислительное фосфорилирование субстратное фосфорилирование 2. Роль дыхания в пластическом обмене 3. Термогенез

Глюкоза – основной субстрат дыхания растений С 6 Н 12 О 6 + 6 О 2 6 СО 2+ 6 Н 2 О + энергия G/0= -686 ккалмоль
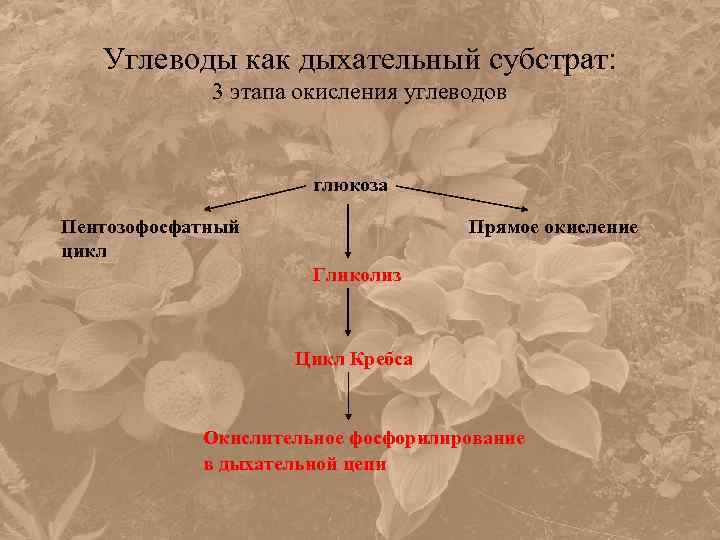
Углеводы как дыхательный субстрат: 3 этапа окисления углеводов глюкоза Пентозофосфатный цикл Прямое окисление Гликолиз Цикл Кребса Окислительное фосфорилирование в дыхательной цепи
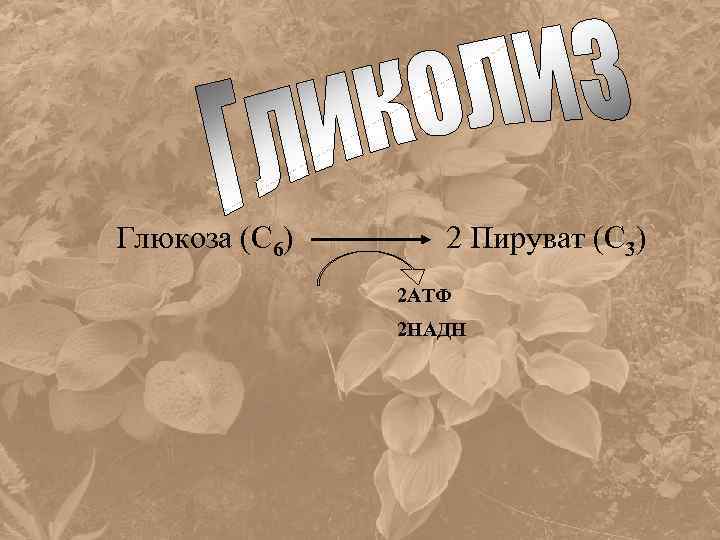
Глюкоза (С 6) 2 Пируват (С 3) 2 АТФ 2 НАДН
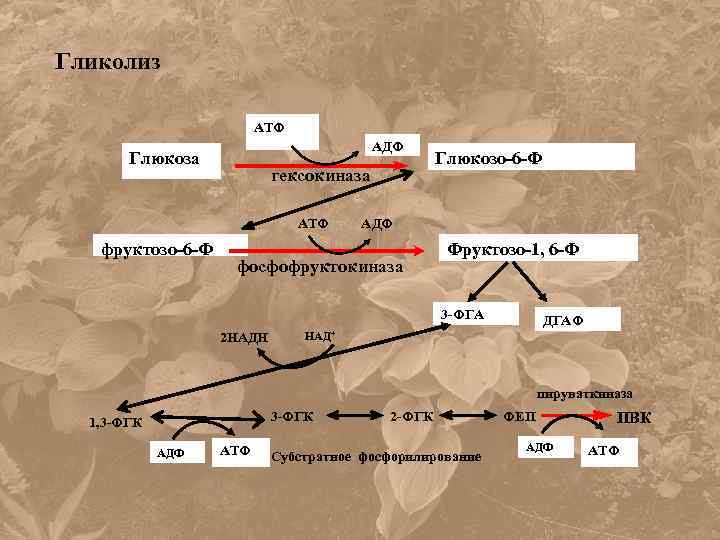
Гликолиз АТФ АДФ Глюкоза гексокиназа АТФ фруктозо-6 -Ф Глюкозо-6 -Ф АДФ фосфофруктокиназа Фруктозо-1, 6 -Ф 3 -ФГА 2 НАДН ДГАФ НАД+ пируваткиназа 3 -ФГК 1, 3 -ФГК АДФ АТФ 2 -ФГК Субстратное фосфорилирование ФЕП АДФ ПВК АТФ

Протекание гликолиза в клетках растений имеет свои особенности. Локализация: цитозоль и пластиды Обратимость гликолиза Регуляция гликолиза

Глюконеогенез Гликолиз Глюкоза Пируват Глюконеогенез (Прорастающие семена) Синтез сахаров при обращении гликолиза называется глюконеогенезом. Как растения «обходят» необратимые реакции гликолиза, катализируемые гексокиназой, фосфофруктокиназой, пируваткиназой
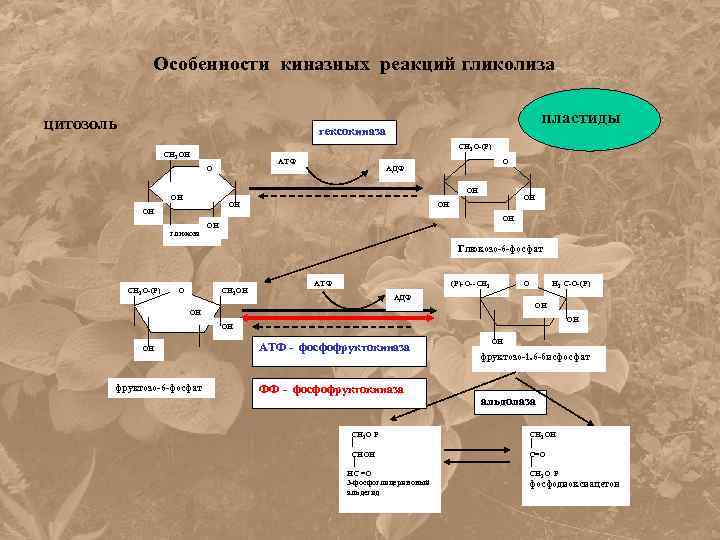
Особенности киназных реакций гликолиза цитозоль пластиды гексокиназа СН 2 О-(Р) СН 2 ОН АТФ О О АДФ ОН ОН глюкоза ОН ОН Глюкозо-6 -фосфат СН 2 О-(Р) О СН 2 ОН АТФ (Р)-О--СН 2 О АДФ Н 2 С-О-(Р) ОН ОН ОН фруктозо-6 -фосфат АТФ - фосфофруктокиназа ФФ - фосфофруктокиназа СН 2 О Р СНОН НС =О 3 -фосфоглицериновый альдегид ОН фруктозо-1. 6 -бисфосфат альдолаза СН 2 ОН С О СН 2 О Р фосфодиоксиацетон
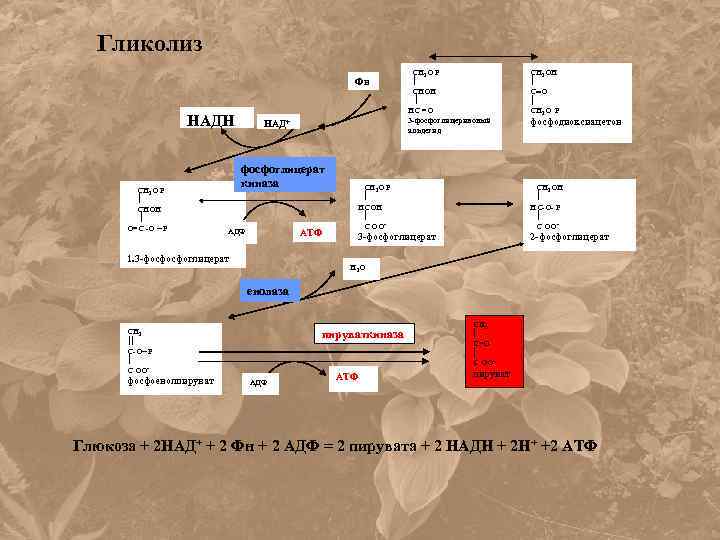
Гликолиз Фн НАДН СН 2 О Р СНОН О=С -О ~ Р НАД+ фосфоглицерат киназа АДФ АТФ 1. 3 -фосфосфоглицерат СН 2 О Р СНОН НС =О 3 -фосфоглицериновый альдегид СН 2 ОН С О СН 2 О Р фосфодиоксиацетон СН 2 О Р НСОН С ОО- СН 2 ОН НС-О- Р С ОО- 3 -фосфоглицерат 2 -фосфоглицерат Н 2 О енолаза СН 2 С-О~ Р С ОО- фосфоенолпируваткиназа АДФ АТФ СН 3 С=О С ОО- пируват Глюкоза + 2 НАД+ + 2 Фн + 2 АДФ = 2 пирувата + 2 НАДН + 2 Н+ +2 АТФ
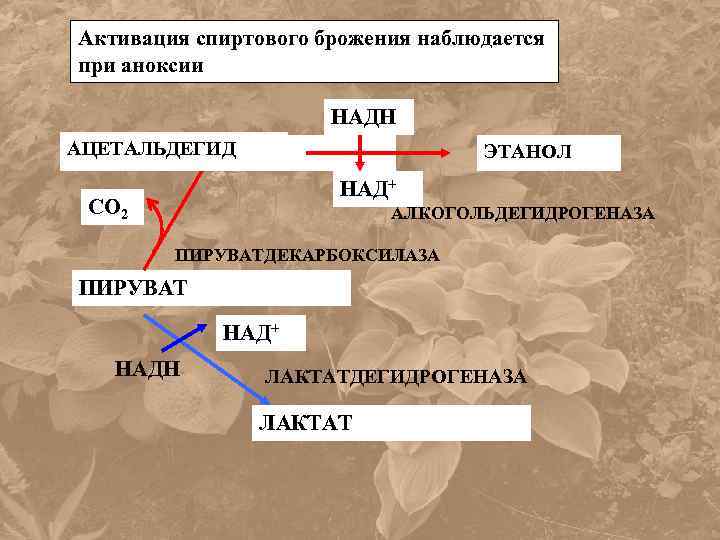
Активация спиртового брожения наблюдается при аноксии НАДН АЦЕТАЛЬДЕГИД ЭТАНОЛ НАД+ СО 2 АЛКОГОЛЬДЕГИДРОГЕНАЗА ПИРУВАТДЕКАРБОКСИЛАЗА ПИРУВАТ НАД+ НАДН ЛАКТАТДЕГИДРОГЕНАЗА ЛАКТАТ
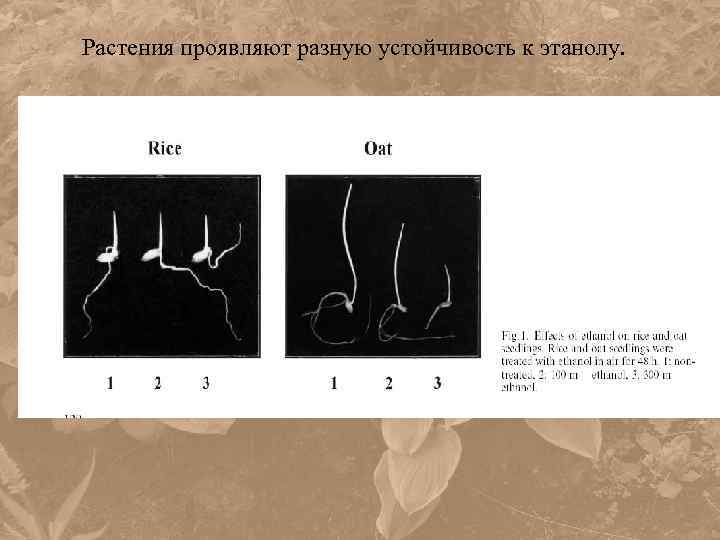
Растения проявляют разную устойчивость к этанолу.
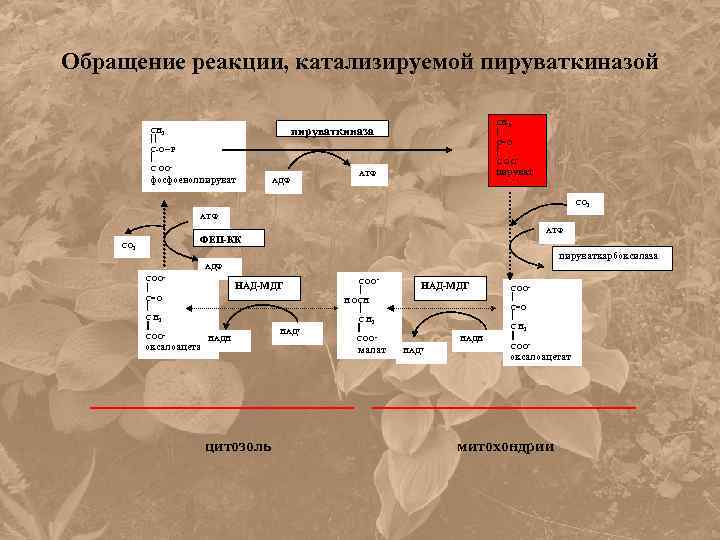
Обращение реакции, катализируемой пируваткиназой СН 3 С=О С ОО- пируваткиназа СН 2 С-О~ Р С ОО- фосфоенолпируват АДФ пируват АТФ СО 2 АТФ ФЕП-КК СО 2 пируваткарбоксилаза АДФ СОО С=О С Н 2 СОО- НАД-МДГ оксалоацетат НАДН цитозоль НАД+ СОО НОСН С Н 2 СОО- малат НАД-МДГ НАДН НАД+ СОО С=О С Н 2 СОО- оксалоацетат митохондрии
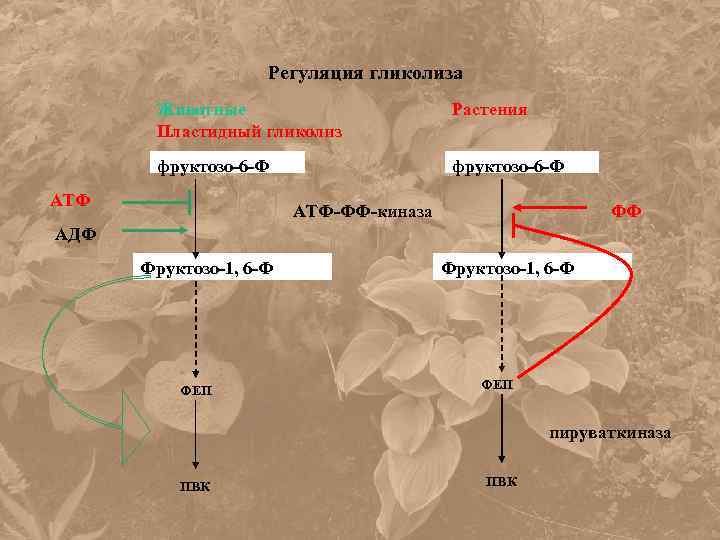
Регуляция гликолиза Животные Пластидный гликолиз Растения фруктозо-6 -Ф АТФ-ФФ-киназа ФФ АДФ Фруктозо-1, 6 -Ф ФЕП пируваткиназа ПВК
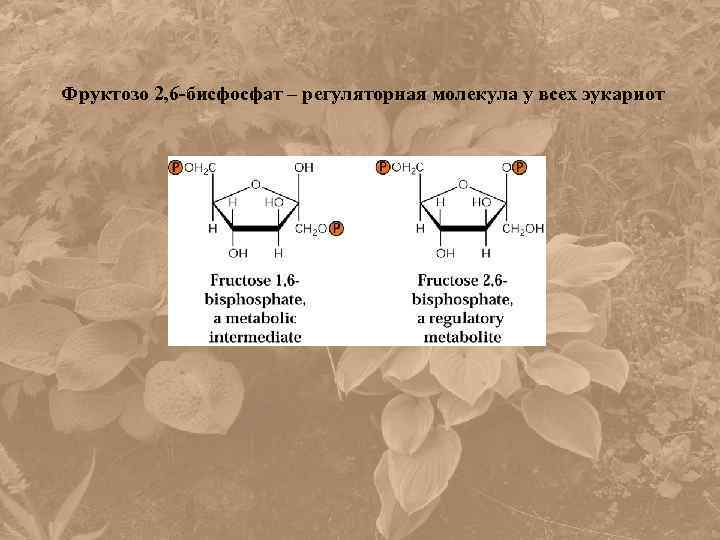
Фруктозо 2, 6 -бисфосфат – регуляторная молекула у всех эукариот
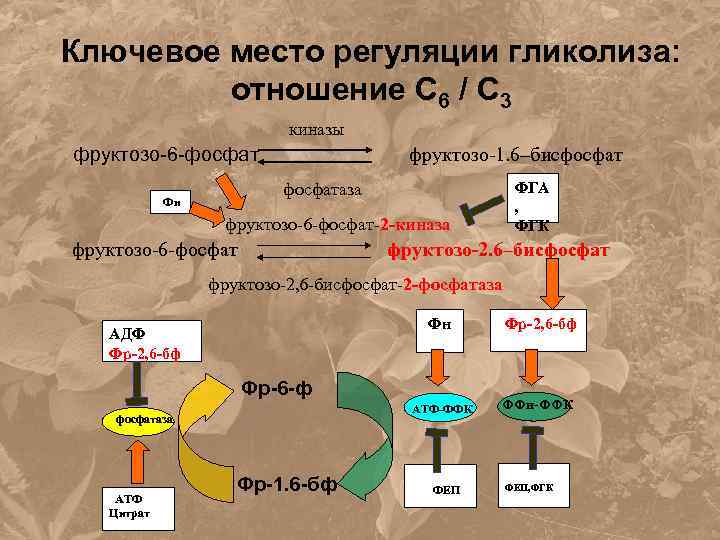
Ключевое место регуляции гликолиза: отношение С 6 / С 3 киназы фруктозо-6 -фосфат фруктозо-1. 6–бисфосфат ФГА , ФГК фосфатаза Фн фруктозо-6 -фосфат-2 -киназа фруктозо-6 -фосфат фруктозо-2. 6–бисфосфат фруктозо-2, 6 -бисфосфат-2 -фосфатаза Фн Фр-2, 6 -бф АТФ-ФФК АДФ Фр-2, 6 -бф ФФн-ФФК Фр-6 -ф фосфатаза АТФ Цитрат Фр-1. 6 -бф ФЕП, ФГК

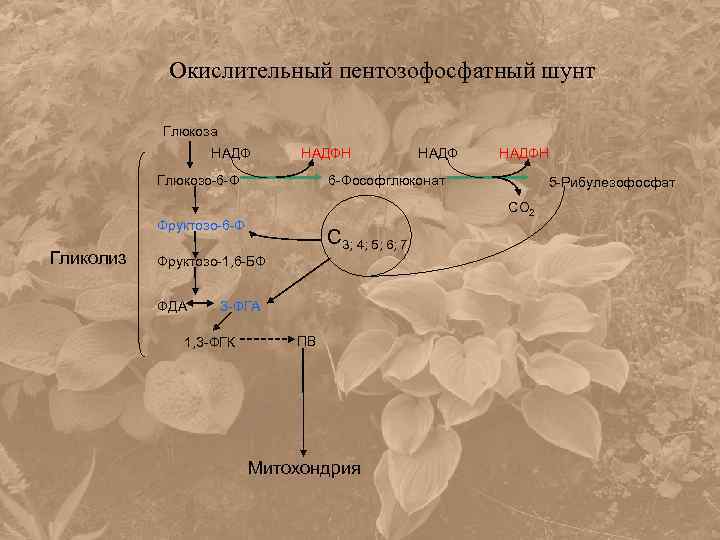
Окислительный пентозофосфатный шунт Глюкоза НАДФН Глюкозо-6 -Ф С 3; 4; 5; 6; 7 3 -ФГА 1, 3 -ФГК 5 -Рибулезофосфат СО 2 Фруктозо-1, 6 -БФ ФДА НАДФН 6 -Фософглюконат Фруктозо-6 -Ф Гликолиз НАДФ ПВ Митохондрия
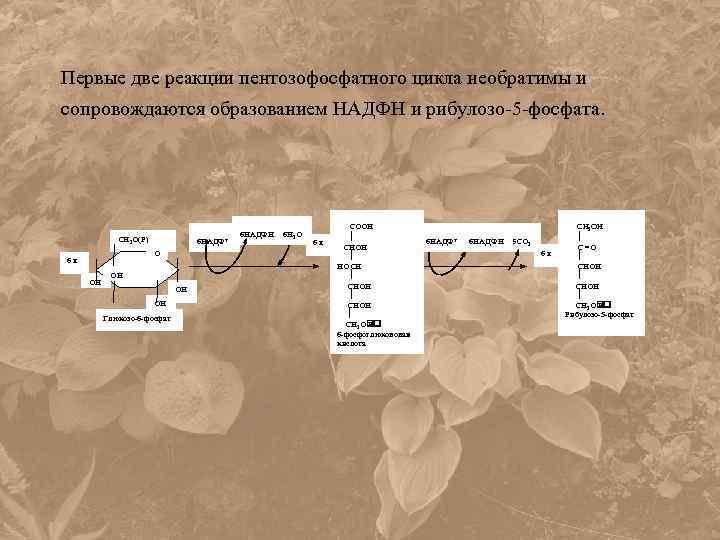
Первые две реакции пентозофосфатного цикла необратимы и сопровождаются образованием НАДФН и рибулозо-5 -фосфата. СН 2 О(Р) 6 НАДФ+ О 6 х ОН ОН Глюкозо-6 -фосфат 6 НАДФН 6 Н 2 О 6 х COOH CНOH НOCH CНOH CH 2 O P 6 -фосфоглюконовая кислота 6 НАДФ+ 6 НАДФН 6 СО 2 6 х CH 2 ОН C =O CHOH CH 2 O P Рибулозо-5 -фосфат
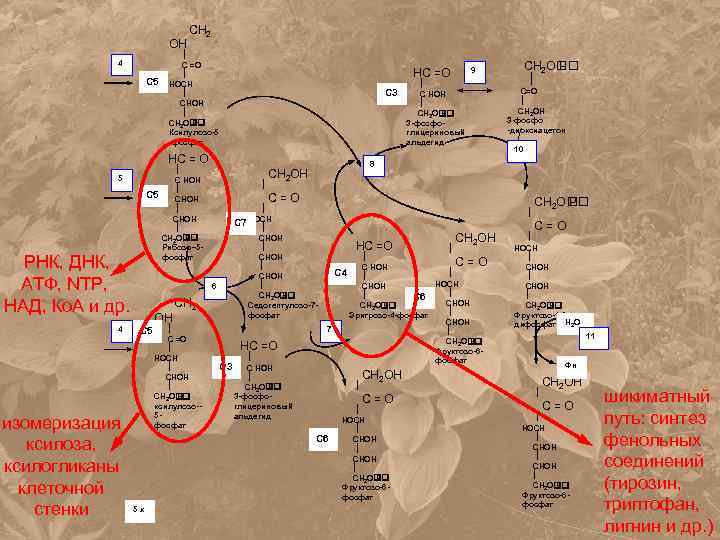
ОН 4 С 5 CH 2 C =O НОCH CHOH CH 2 O P Ксилулозо-5 -фосфат НС =О С 3 НC = О 5 С 5 РНК, ДНК, АТФ, NTP, НАД, Ко. А и др. 4 изомеризация ксилоза, ксилогликаны клеточной стенки C НOН CHOH CH 2 O P Рибозо--5 фосфат ОН СН 2 ОН 10 НС =О С 3 C НОН CH 2 O P 3 -фосфоглицериновый альдегид НС =О СН 2 ОН C=О C НОН С 4 НОCH СНОН С 6 CHOH CH 2 O P Эритрозо-4 -фосфат СНОН 7 CH 2 O P Фруктозо-6 фосфат СН 2 О Р C=О НОCH CHOH СНОН CH 2 O P Фруктозо-1. 6 дифосфат Н 2 О 11 Фн СН 2 ОН C=О С 6 5 х C=О CH 2 OН 3 -фосфо -диоксиацетон C=О СН 2 C =O НОCH CHOH CH 2 O P ксилулозо-5 фосфат C НОН CH 2 O P 3 -фосфоглицериновый альдегид 8 С 7 НОCH CHOH СНОН CH 2 O P Седогептулозо-7 фосфат 6 С 5 СН 2 О Р 9 НОCH CHOH СНОН CH 2 O P Фруктозо-6 фосфат СН 2 ОН C=О НОCH CHOH СНОН CH 2 O P Фруктозо-6 фосфат шикиматный путь: синтез фенольных соединений (тирозин, триптофан, лигнин и др. )

Растительные митохондрии имеют разнообразный размер и форму
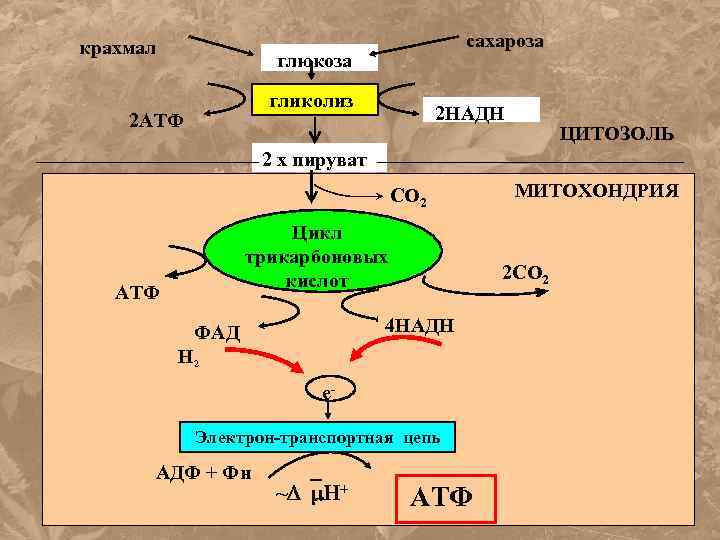
крахмал сахароза глюкоза гликолиз 2 АТФ 2 НАДН ЦИТОЗОЛЬ 2 х пируват СО 2 Цикл трикарбоновых кислот АТФ 2 СО 2 4 НАДН ФАД Н 2 e- Электрон-транспортная цепь АДФ + Фн ~ + МИТОХОНДРИЯ АТФ
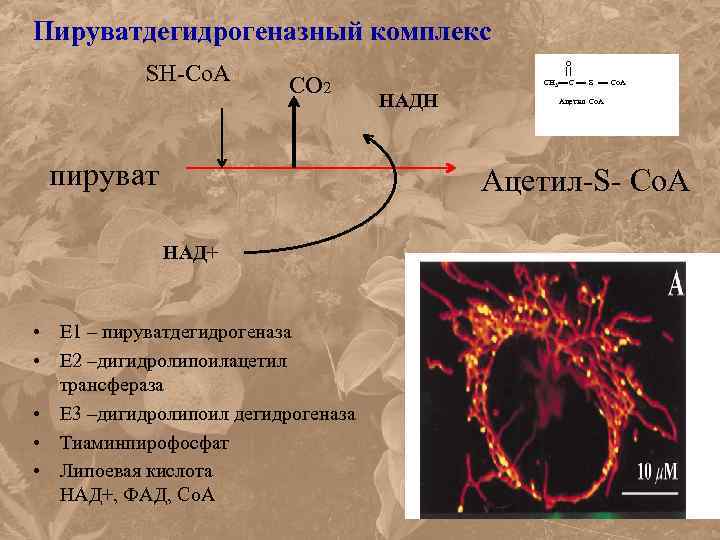
Пируватдегидрогеназный комплекс SH-Со. А СО 2 пируват О СН 3 С S Со. А НАДН Ацетил Со. А Ацетил-S- Со. А НАД+ • Е 1 – пируватдегидрогеназа • Е 2 –дигидролипоилацетил трансфераза • Е 3 –дигидролипоил дегидрогеназа • Тиаминпирофосфат • Липоевая кислота НАД+, ФАД, Со. А
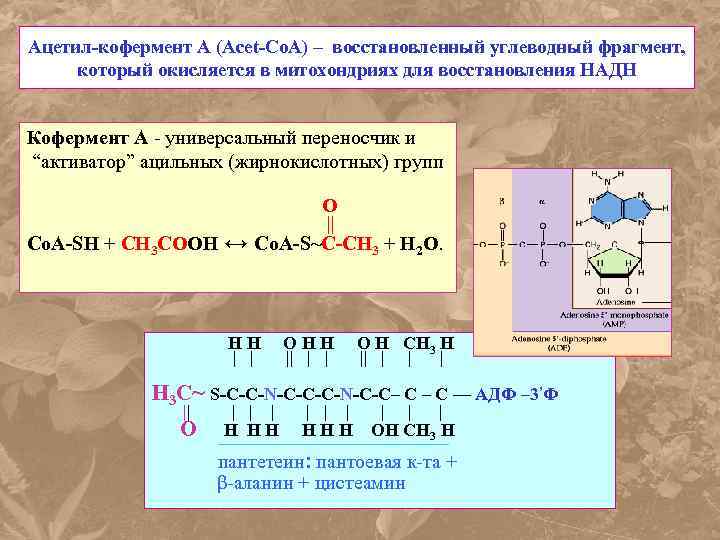
Ацетил-кофермент А (Acet-Co. A) – восстановленный углеводный фрагмент, который окисляется в митохондриях для восстановления НАДН Кофермент А - универсальный переносчик и “активатор” ацильных (жирнокислотных) групп Со. А-SH + CH 3 СOOH ↔ O || Co. A-S~C-CH 3 + Н 2 О. HH | | OHH || | | O H CH 3 H || | H 3 C~ S-C-C-N-C-C– C — АДФ – 3’Ф || O | | | H HH | | | HHH | | | OH CH 3 H ¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯ пантетеин: пантоевая к-та + β-аланин + цистеамин
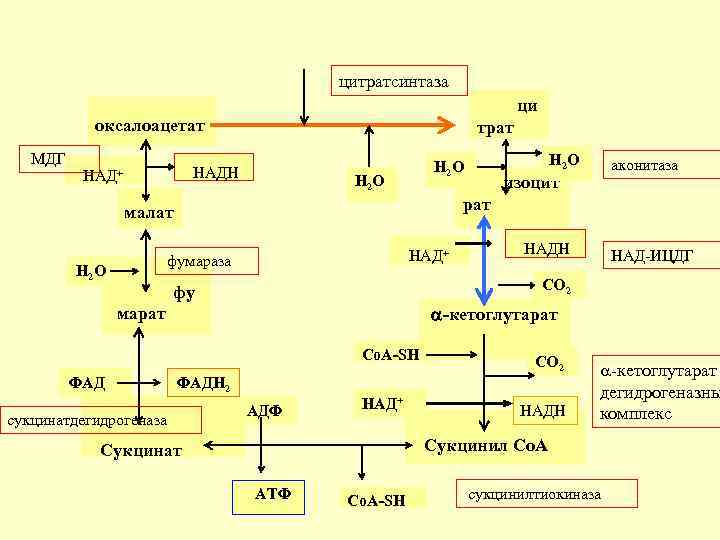
цитратсинтаза ци оксалоацетат МДГ трат НАДН НАД+ Н 2 О НАД+ фумараза изоцит НАДН -кетоглутарат Сo. A-SH СО 2 ФАДН 2 сукцинатдегидрогеназа НАД-ИЦДГ СО 2 фу фу марат ФАД аконитаза рат малат Н 2 О АДФ НАД+ НАДН -кетоглутарат дегидрогеназны комплекс Сукцинил Со. А Сукцинат АТФ Сo. A-SH сукцинилтиокиназа
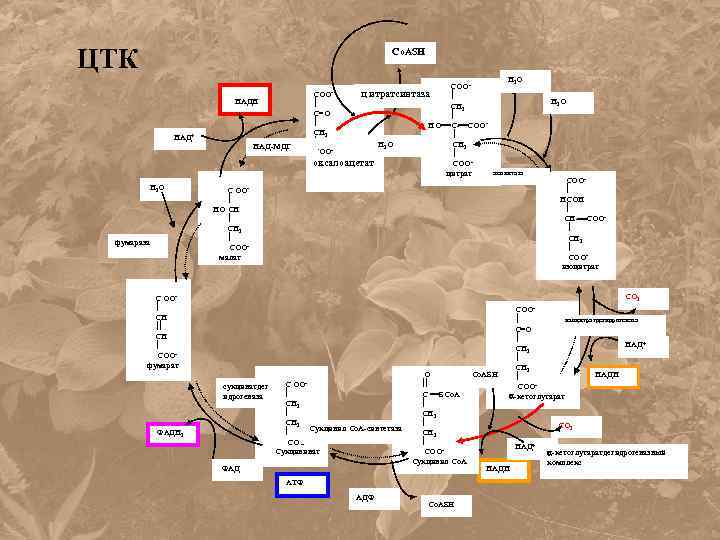
ЦТК Co. ASH НАДН НАД+ НАД-МДГ Н 2 О фумараза Н 2 О СООц итратсинтаза СН 2 С=О НО С- СООСН 2 Н 2 О СОО оксалоацетат СООаконитаза цитрат СОО- С ОО НО СН 2 СООмалат Н 2 О СОО НСОН СН- СОО СН 2 СООизоцитрат СО 2 С ОО СН СООфумарат СОО- сукцинатдег идрогеназа ФАДН 2 С ОО СН 2 Сукцинил Со. А-синтетаза СОО Сукцининат ФАД изоцитратдегидрогеназа С О НАД+ СН 2 НАДН СОО -кетоглутарат О Co. ASH С SCo. A СН 2 НАД+ СООСукцинил Со. А НАДН АТФ АДФ Co. ASH СО 2 -кетоглутаратдегидрогеназный комплекс
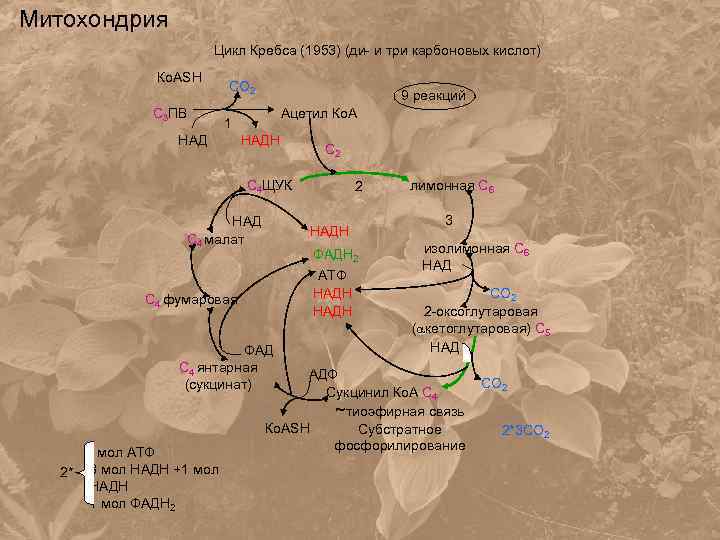
Митохондрия Цикл Кребса (1953) (ди- и три карбоновых кислот) Ко. ASH С 3 ПВ СО 2 9 реакций Ацетил Ко. А 1 НАДН С 2 С 4 ЩУК НАД С 4 малат НАДН ФАДН 2 АТФ НАДН С 4 фумаровая ФАД С 4 янтарная (сукцинат) 2* 1 мол АТФ 3 мол НАДН +1 мол НАДН 1 мол ФАДН 2 2 лимонная С 6 3 изолимонная С 6 НАД СО 2 2 -оксоглутаровая ( кетоглутаровая) С 5 НАД АДФ Сукцинил Ко. А С 4 ~тиоэфирная связь Ко. ASH Субстратное фосфорилирование СО 2 2*3 СО 2

Реакции обращения реакци ФЕП -----ПВК Особенностью растительных Мх является присутствие малик-энзима малатдегидрогеназа декарбоксилирующая НАД-зависимый малик-энзим (цитозоль, Мх) НАДФ-зависимый малик-энзим (Хл)
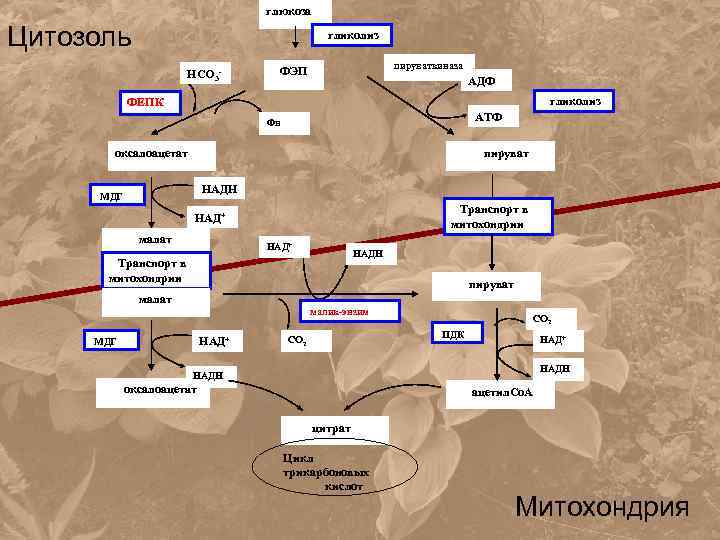
глюкоза Цитозоль гликолиз НСО 3 - пируваткиназа ФЭП АДФ гликолиз ФЕПК АТФ Фн оксалоацетат пируват НАДН МДГ Транспорт в митохондрии НАД+ малат НАД+ НАДН Транспорт в митохондрии пируват малик-энзим НАД+ МДГ СО 2 ПДК СО 2 НАД+ НАДН оксалоацетат ацетил. Со. А цитрат Цикл трикарбоновых кислот Митохондрия


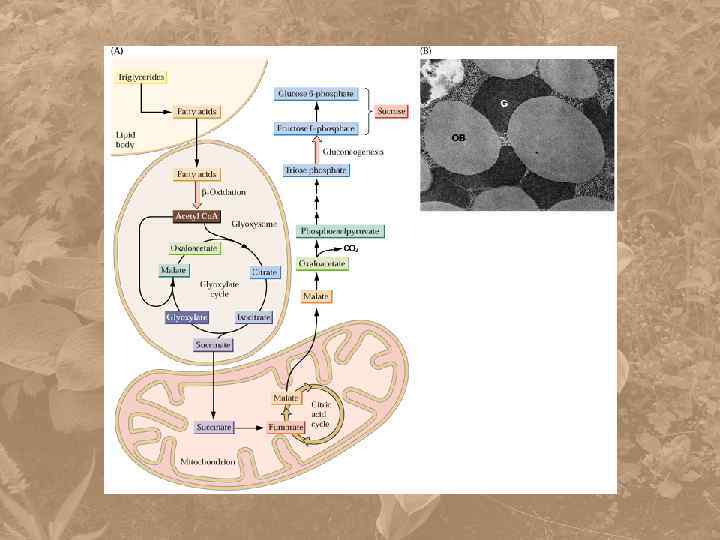
Конверсия жиров в углеводы включает три этапа: Распад жиров и -окисление жирных кислот Глиоксилатный цикл в глиоксисомах Глюконеогенез

• В клетках животных жирные кислоты подвергаются -окислению в митохондриях • В клетках растений жирные кислоты подвергаются -окислению в глиоксисомах, которые являются разновидностью пероксисом. Глиоксисомы впервые были выделены Биверсом в 1967 г. (Beevers)
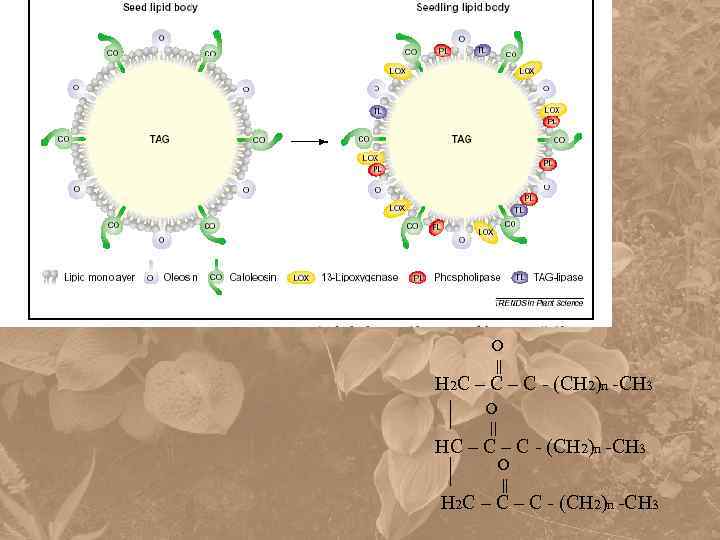
О || Н 2 С – С – С - (СН 2)n -СН 3 О || Н 2 С – С - (СН 2)n -СН 3
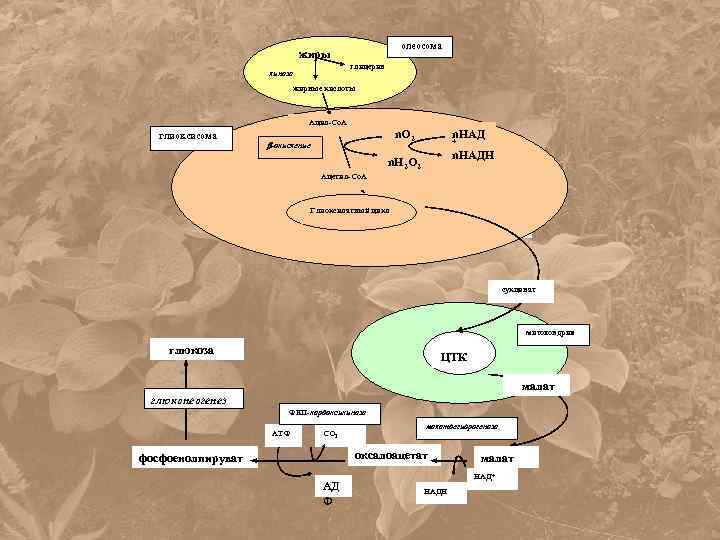
олеосома жиры глицерин липаза жирные кислоты Ацил-Со. А глиоксисома n. O 2 -окисление Ацетил-Со. А Глиоксилатный цикл n. НАД + n. НАДH n. H 2 O 2 Глиоксилатный цикл сукцинат митохондрия глюкоза ЦТК малат глюконеогенез ФЕП-карбоксикиназа АТФ СО 2 малатдегидрогеназа оксалоацетат фосфоенолпируват АД Ф малат НАД+ НАДН
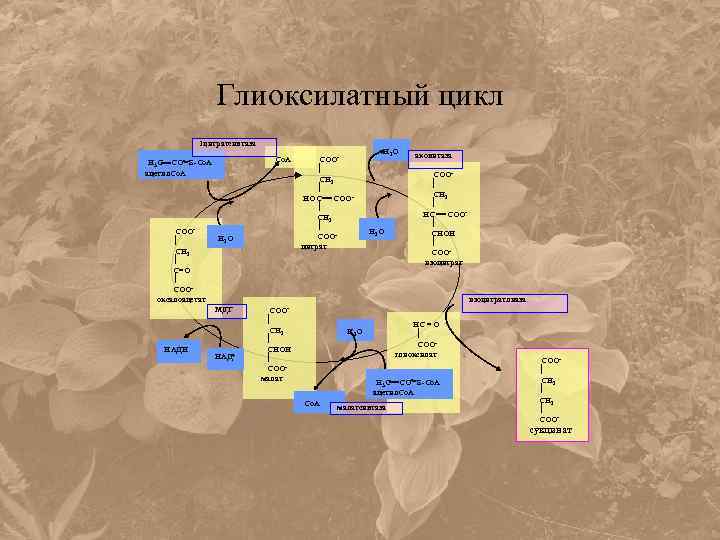
Глиоксилатный цикл 1 цитратсинтаза Н 3 С СО S-Co. A ацетил. Со. А СОО СН 2 С=О СООоксалоацетат Co. A Н 2 О аконитаза СОО СН 2 НС СОО СНОН СООизоцитратлиаза МДГ НАДН СОО СН 2 НОС СОО СН 2 СООцитрат НАД+ СОО СН 2 СНОН СООмалат НС = О СООглиоксилат Н 2 О Н 3 С СО S-Co. A ацетил. Со. А Co. A малатсинтаза СОО СН 2 СОО- сукцинат
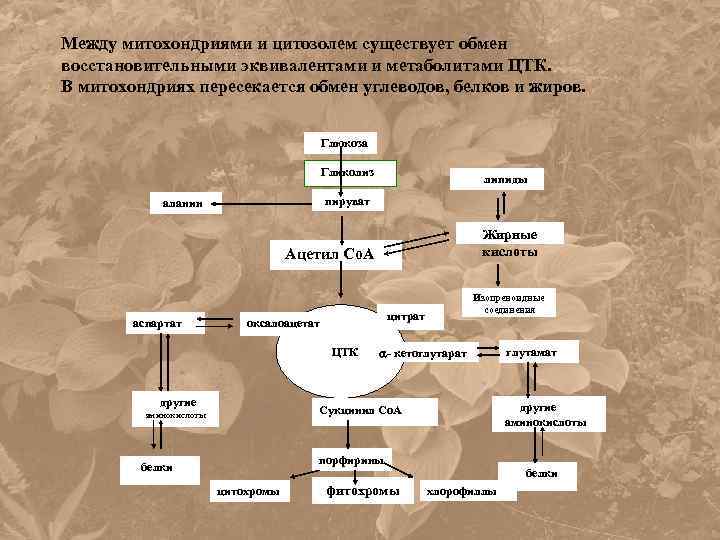
Между митохондриями и цитозолем существует обмен восстановительными эквивалентами и метаболитами ЦТК. В митохондриях пересекается обмен углеводов, белков и жиров. Глюкоза Гликолиз липиды пируват аланин Жирные кислоты Ацетил Со. А аспартат цитрат оксалоацетат ЦТК другие Изопреноидные соединения - кетоглутарат другие аминокислоты Сукцинил Со. А аминокислоты порфирины белки цитохромы фитохромы глутамат белки хлорофиллы
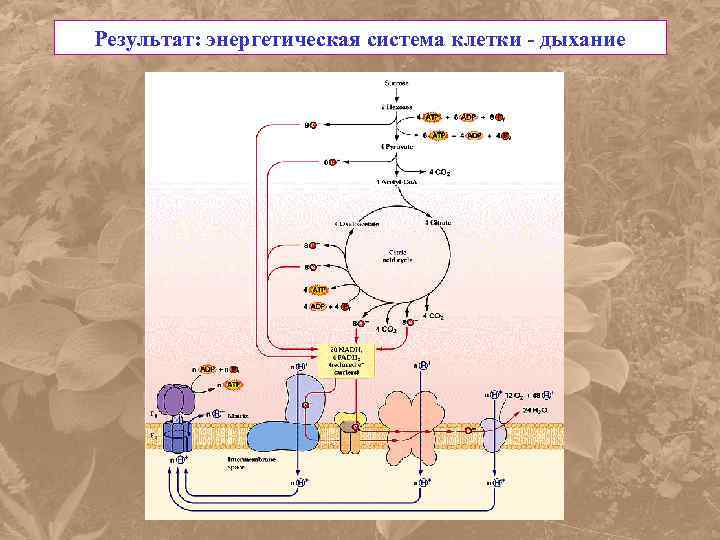
Результат: энергетическая система клетки - дыхание
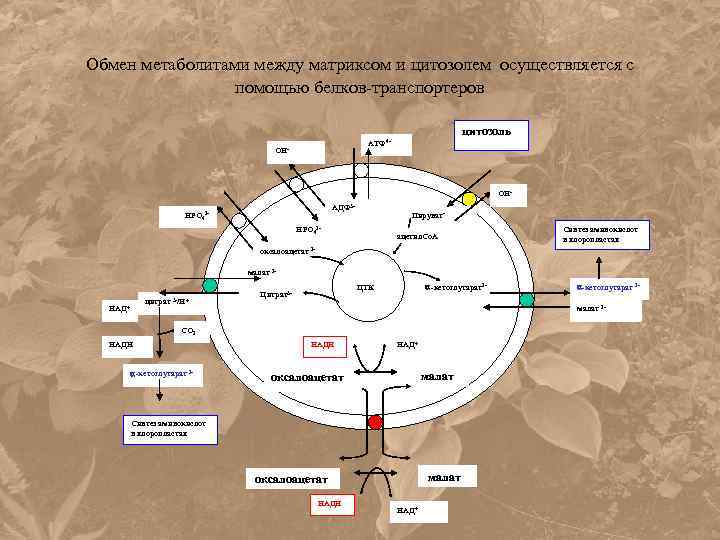
Обмен метаболитами между матриксом и цитозолем осуществляется с помощью белков-транспортеров цитозоль АТФ 4 - ОНАДФ 3 - НРО 42 - Пируват- НРО 42 - ацетил. Со. А Синтез аминокислот в хлоропластах оксалоацетат 2 малат 2 цитрат 3 -/Н+ НАД+ -кетоглутарат2 - ЦТК Цитрат3 - малат 2 - СО 2 НАДН -кетоглутарат 2 - НАДН НАД+ малат оксалоацетат Синтез аминокислот в хлоропластах малат оксалоацетат НАДН НАД+

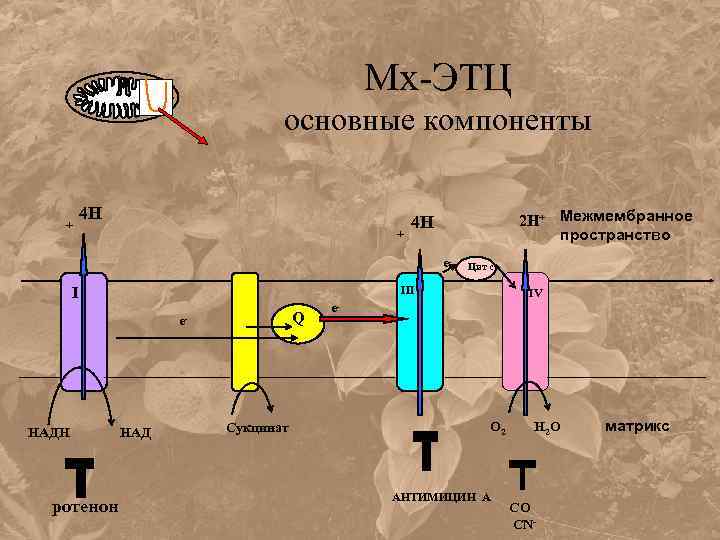
Мх-ЭТЦ основные компоненты + 4 Н + 2 Н+ Межмембранное пространство 4 Н e- III I Q e- НАДН ротенон Цит с НАД Сукцинат IV e- О 2 АНТИМИЦИН А Н 2 О СО CN- матрикс
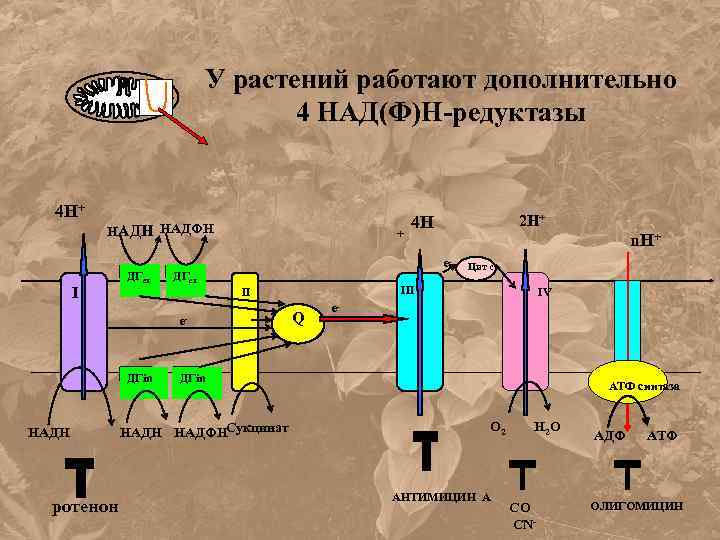
У растений работают дополнительно 4 НАД(Ф)Н-редуктазы 4 Н+ НАДН НАДФН I ДГex + ДГex e- НАДН ротенон n. Н+ e- Цит с III II ДГin 2 Н+ 4 Н Q IV e- ДГin НАДН НАДФНСукцинат АТФ синтаза О 2 АНТИМИЦИН А Н 2 О СО CN- АДФ АТФ ОЛИГОМИЦИН
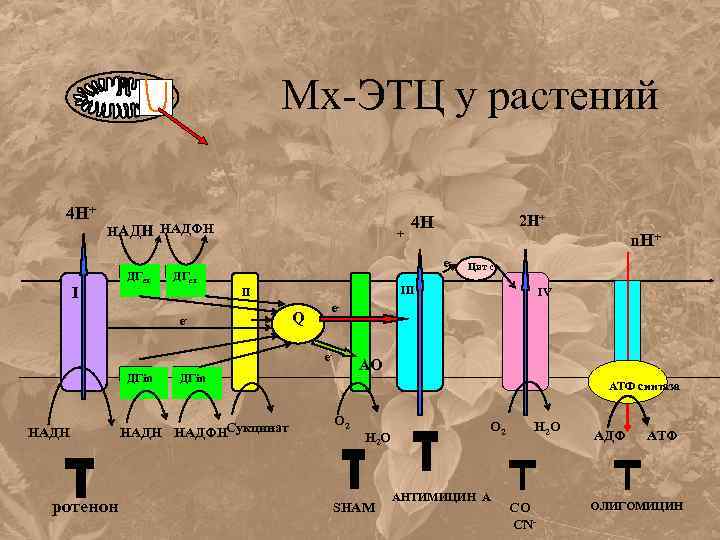
Мх-ЭТЦ у растений 4 Н+ НАДН НАДФН I ДГex + ДГex e- Q ротенон IV e- АО ДГin НАДН НАДФНСукцинат Цит с III e- НАДН n. Н+ e- II ДГin 2 Н+ 4 Н АТФ синтаза О 2 Н 2 О SHAM О 2 АНТИМИЦИН А Н 2 О СО CN- АДФ АТФ ОЛИГОМИЦИН
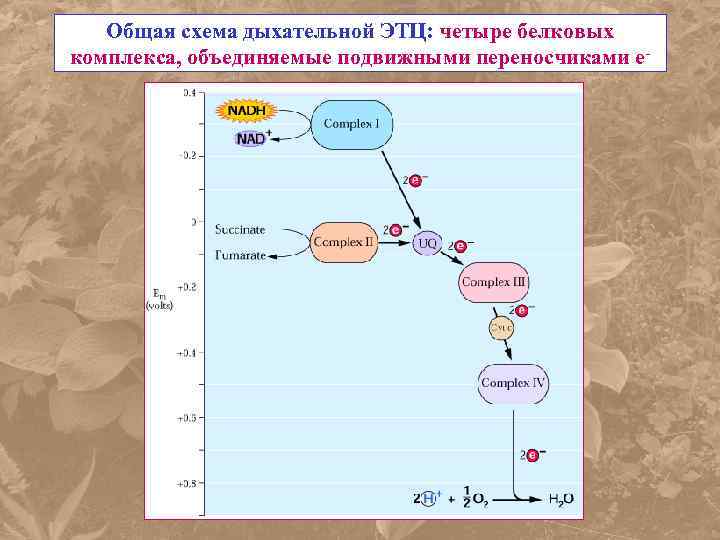
Общая схема дыхательной ЭТЦ: четыре белковых комплекса, объединяемые подвижными переносчиками е-
Комплекс I: НАДН-дегидрогеназа. Старый башмак…
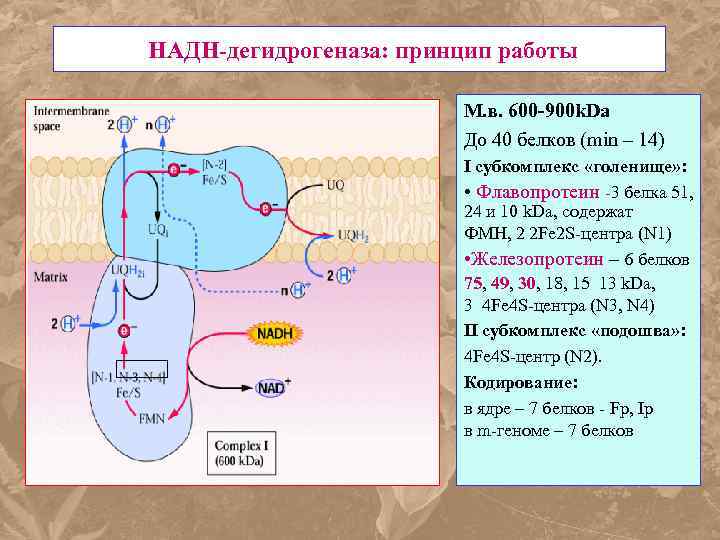
НАДН-дегидрогеназа: принцип работы М. в. 600 -900 k. Da До 40 белков (min – 14) I субкомплекс «голенище» : • Флавопротеин -3 белка 51, 24 и 10 k. Da, содержат ФМН, 2 2 Fe 2 S-центра (N 1) • Железопротеин – 6 белков 75, 49, 30, 18, 15 13 k. Da, 3 4 Fe 4 S-центра (N 3, N 4) II субкомплекс «подошва» : 4 Fe 4 S-центр (N 2). Кодирование: в ядре – 7 белков - Fp, Ip в m-геноме – 7 белков
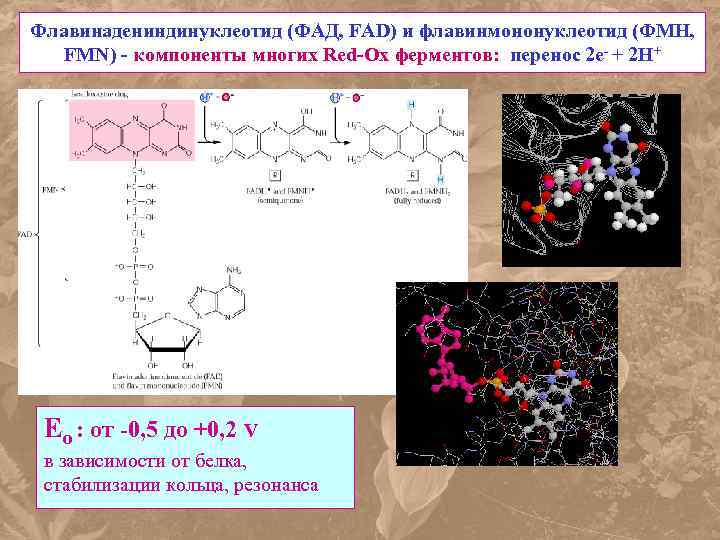
Флавинадениндинуклеотид (ФАД, FAD) и флавинмононуклеотид (ФМН, FMN) - компоненты многих Red-Ox ферментов: перенос 2 е- + 2 Н+ Eo : от -0, 5 до +0, 2 V в зависимости от белка, стабилизации кольца, резонанса
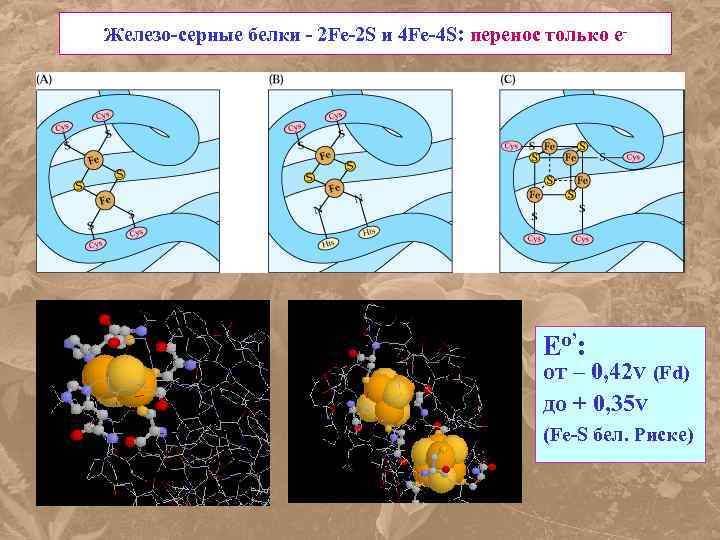
Железо-серные белки - 2 Fe-2 S и 4 Fe-4 S: перенос только е- Eо’: от – 0, 42 V (Fd) до + 0, 35 V (Fe-S бел. Риске)
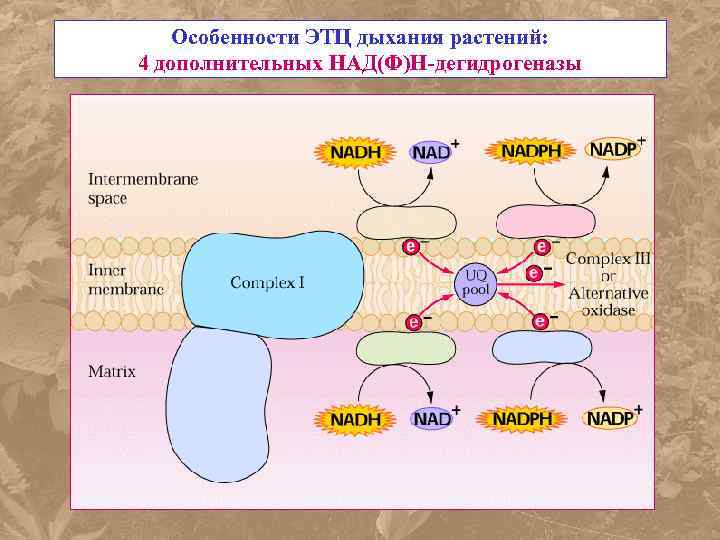
Особенности ЭТЦ дыхания растений: 4 дополнительных НАД(Ф)Н-дегидрогеназы
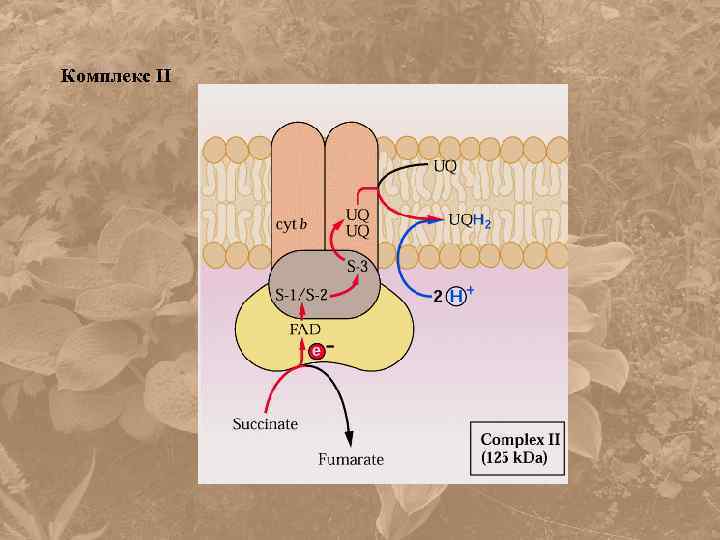
Комплекс II
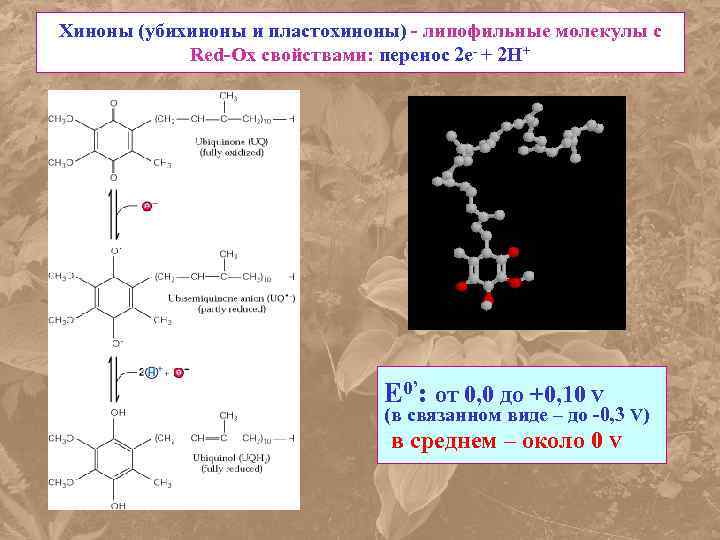
Хиноны (убихиноны и пластохиноны) - липофильные молекулы с Red-Ox свойствами: перенос 2 е- + 2 Н+ E 0’: от 0, 0 до +0, 10 V (в связанном виде – до -0, 3 V) в среднем – около 0 V
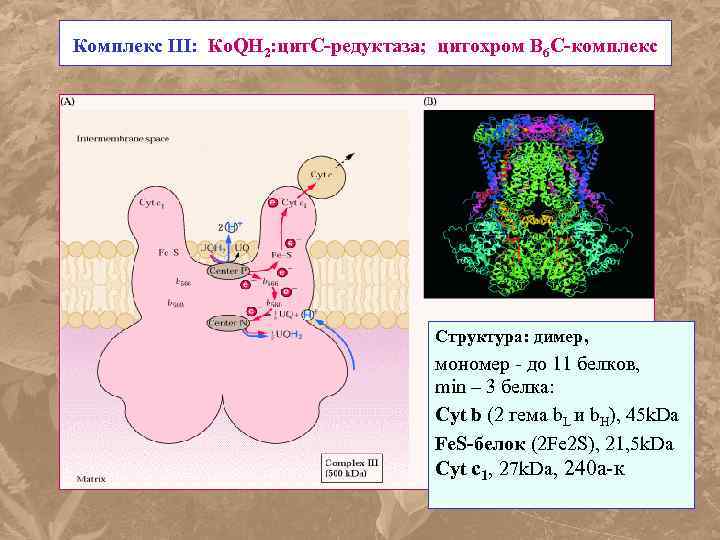
Комплекс III: Ко. QН 2: цит. С-редуктаза; цитохром В 6 С-комплекс Структура: димер, мономер - до 11 белков, min – 3 белка: Cyt b (2 гема b. L и b. H), 45 k. Da Fe. S-белок (2 Fe 2 S), 21, 5 k. Da Cyt c 1, 27 k. Da, 240 а-к
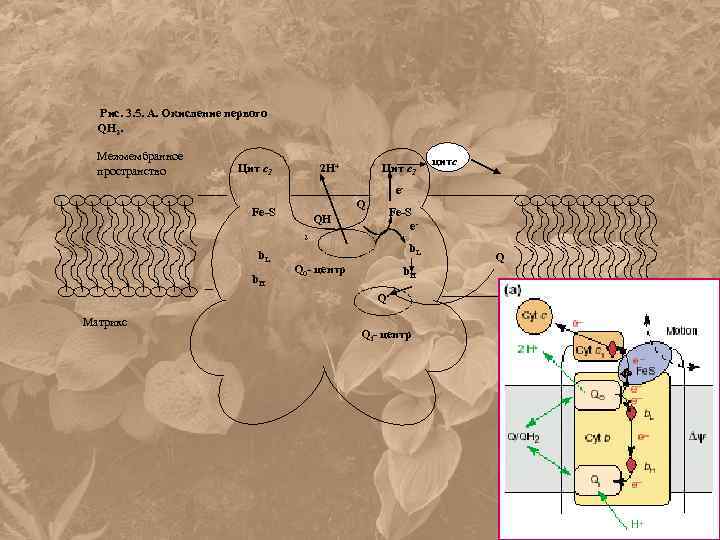
Рис. 3. 5. А. Окисление первого QH 2. Межмембранное пространство Цит с1 2 H+ Цит с1 цитс e. Q Fe-S QH Fe-S e- 2 b. L b. H b. L Q 0 - центр b. H Q. - Матрикс Qi- центр Q
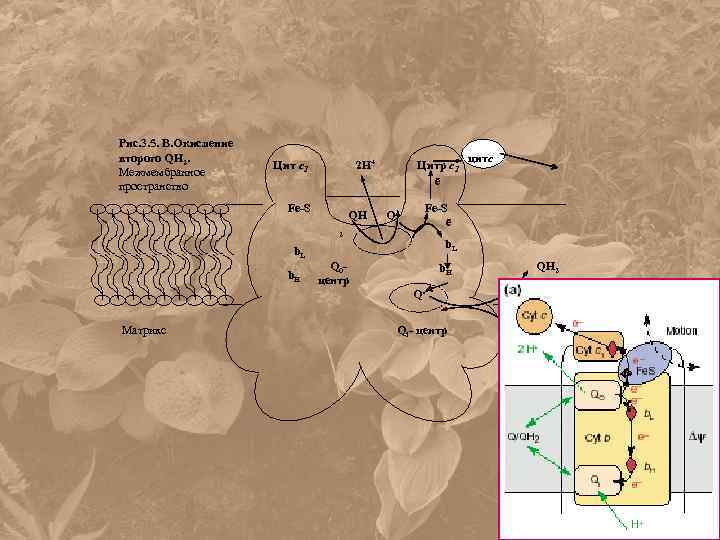
Рис. 3. 5. В. Окисление второго QH 2. Межмембранное пространство Цит с1 2 H+ Fe-S QH Цитр с1 ē Q Fe-S ē 2 b. L b. H Матрикс Q 0 центр цитс b. L b. H QH 2 Q. Qi- центр 2 Н+
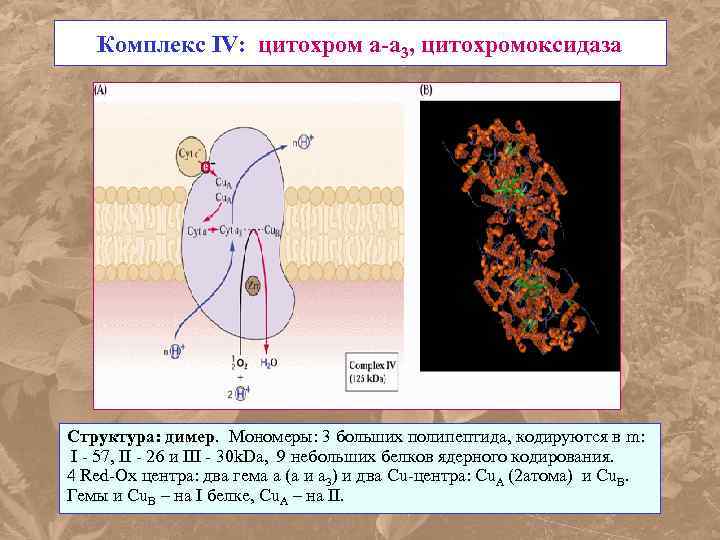
Комплекс IV: цитохром а-а 3, цитохромоксидаза Структура: димер. Мономеры: 3 больших полипептида, кодируются в m: I - 57, II - 26 и III - 30 k. Da, 9 небольших белков ядерного кодирования. 4 Red-Ox центра: два гема а (a и a 3) и два Cu-центра: Сu. А (2 атома) и Cu. В. Гемы и Cu. B – на I белке, Cu. A – на II.
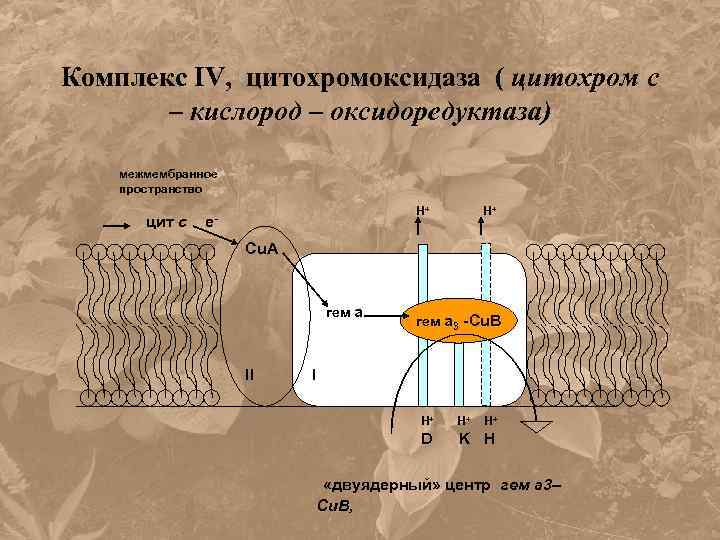
Комплекс IV, цитохромоксидаза ( цитохром с – кислород – оксидоредуктаза) межмембранное пространство цит с H+ e- H+ Cu. A гем а II гем а 3 -Сu. B I H+ H+ H+ D K H «двуядерный» центр гем а 3– Сu. В,
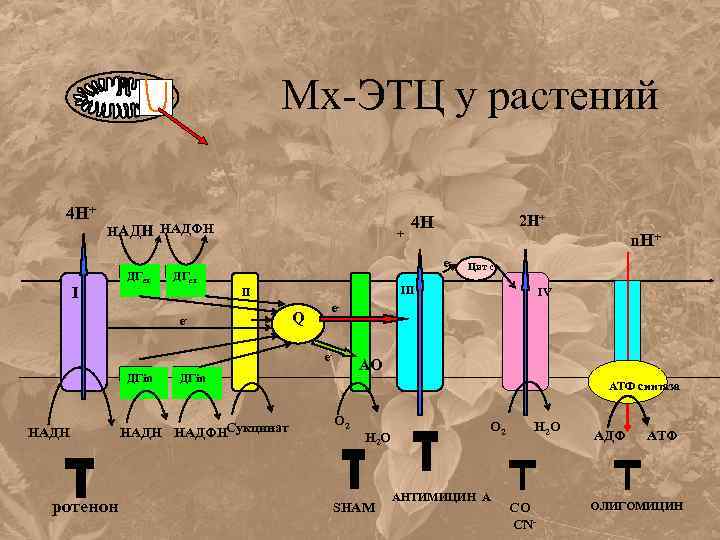
Мх-ЭТЦ у растений 4 Н+ НАДН НАДФН I ДГex + ДГex e- Q ротенон IV e- АО ДГin НАДН НАДФНСукцинат Цит с III e- НАДН n. Н+ e- II ДГin 2 Н+ 4 Н АТФ синтаза О 2 Н 2 О SHAM О 2 АНТИМИЦИН А Н 2 О СО CN- АДФ АТФ ОЛИГОМИЦИН

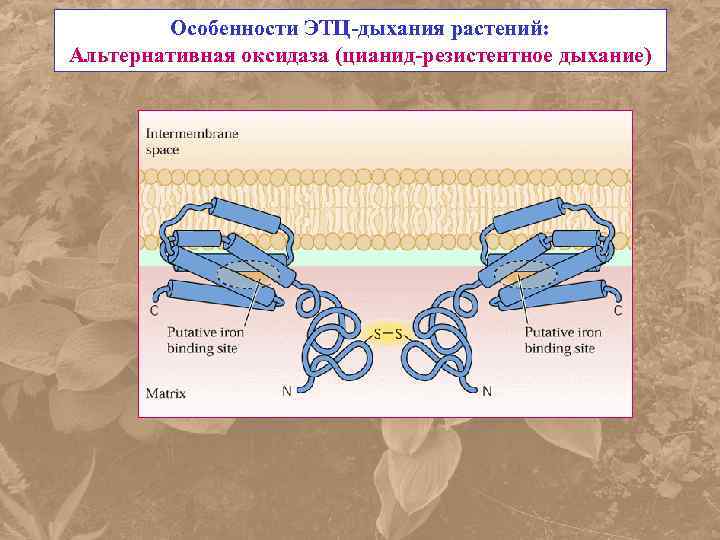
Особенности ЭТЦ-дыхания растений: Альтернативная оксидаза (цианид-резистентное дыхание)

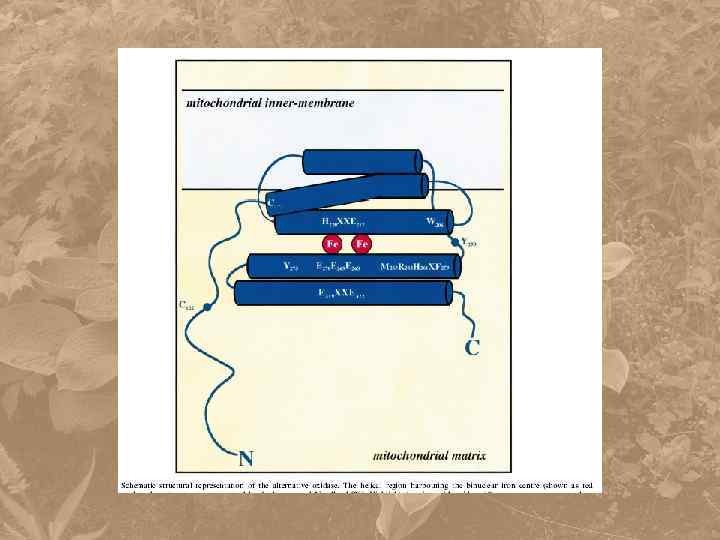
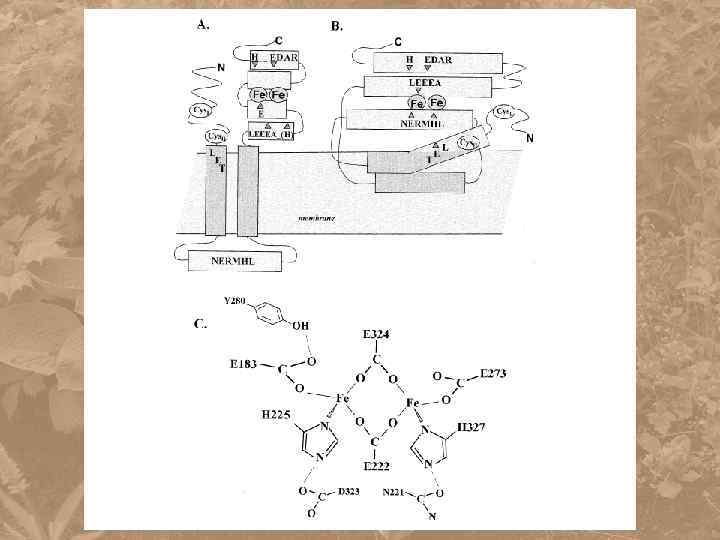
AO относится к семейству di-iron белков R-2 типа Обнаружена у E. coli, Paracoccus denitrificans, простейших Trypanosoma, водорослей и всех семенных растений. Впервые белок АО был получен из мтх Sauromatum guttatum
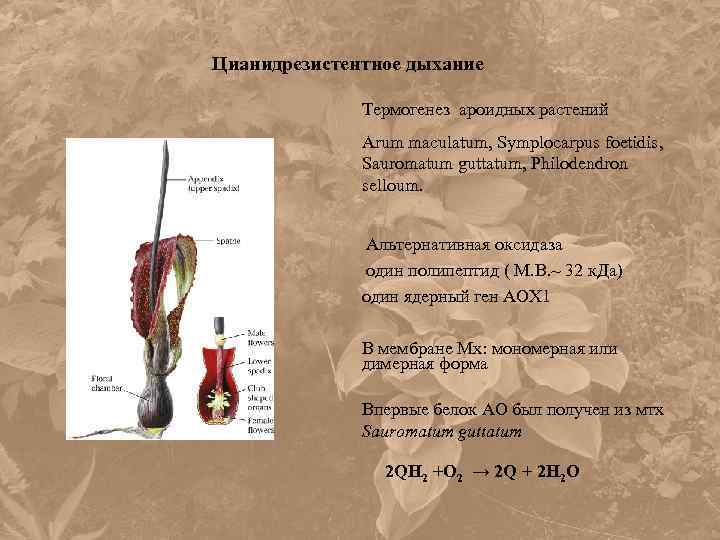
Цианидрезистентное дыхание Термогенез ароидных растений Arum maculatum, Symplocarpus foetidis, Sauromatum guttatum, Philodendron selloum. Альтернативная оксидаза один полипептид ( М. В. ~ 32 к. Да) один ядерный ген АОХ 1 В мембране Мх: мономерная или димерная форма Впервые белок АО был получен из мтх Sauromatum guttatum 2 QH 2 +O 2 → 2 Q + 2 H 2 O

• Термогенез в цветках некоторых растений связан с терморегуляцией: • При понижении температуры воздуха температура тканей цветка остается постоянной , а скорость поглощения кислорода возрастает. При повышении температуры воздуха скорость дыхания падает

• t воздуха t цветка • Symplocarpus foetidis +3 -+240 +16 -+ 260 • Philodendron selloum +4 -+390 +39 -+ 440 • Существуют точки, (switchig temperature) за пределами которых «терморегуляция» не действует

Sauromatum guttatum

Symplocarpus foetidus

Helicodeceros muscivorus
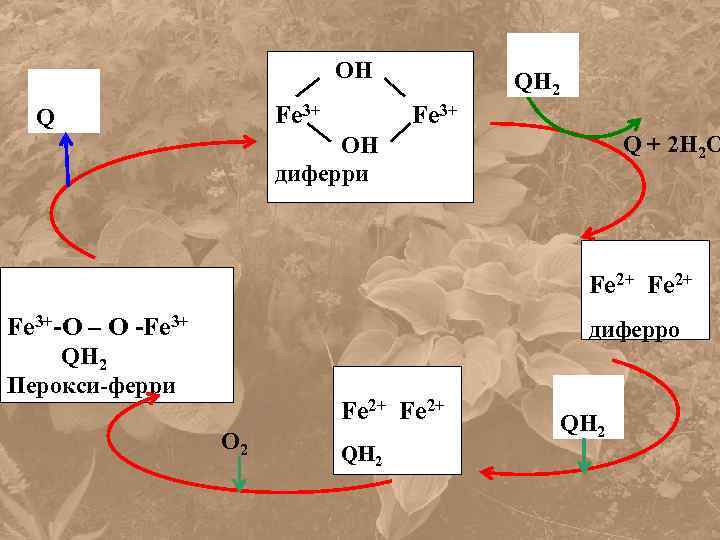
OH Fe 3+ Q QH 2 Fe 3+ Q + 2 H 2 O OH диферри Fe 2+ Fe 3+-O – O -Fe 3+ диферро QH 2 Перокси-ферри Fe 2+ O 2 QH 2
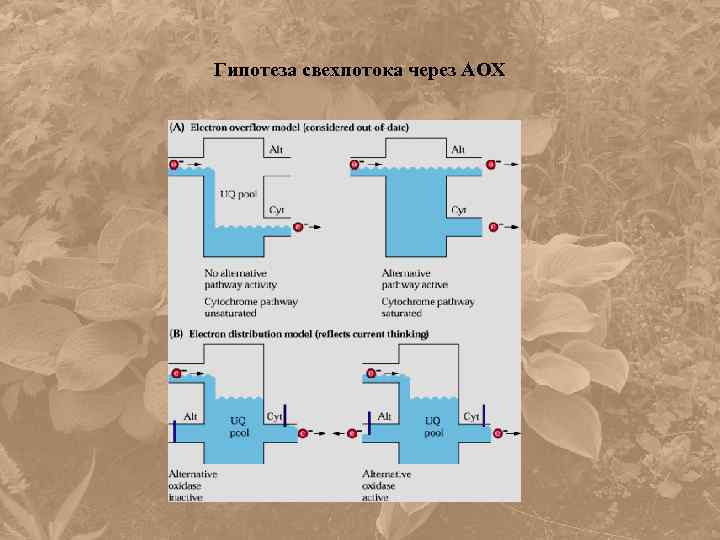
Гипотеза свехпотока через АОХ
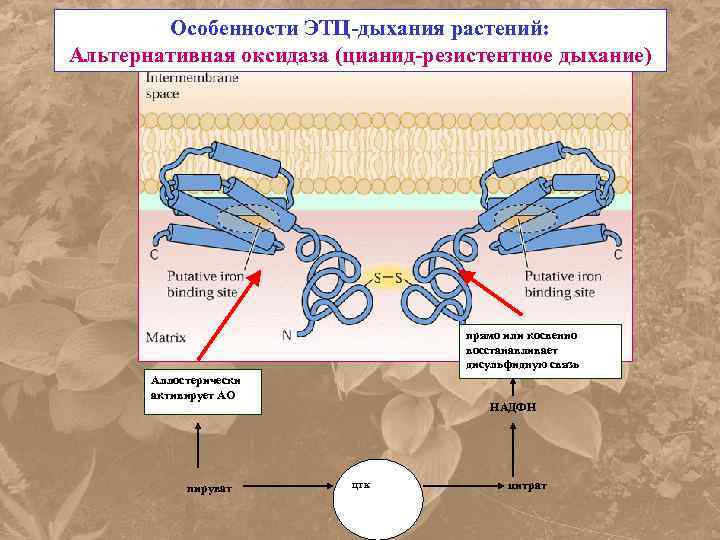
Особенности ЭТЦ-дыхания растений: Альтернативная оксидаза (цианид-резистентное дыхание) прямо или косвенно восстанавливает дисульфидную связь Аллостерически активирует АО пируват НАДФН ЦТК цитрат
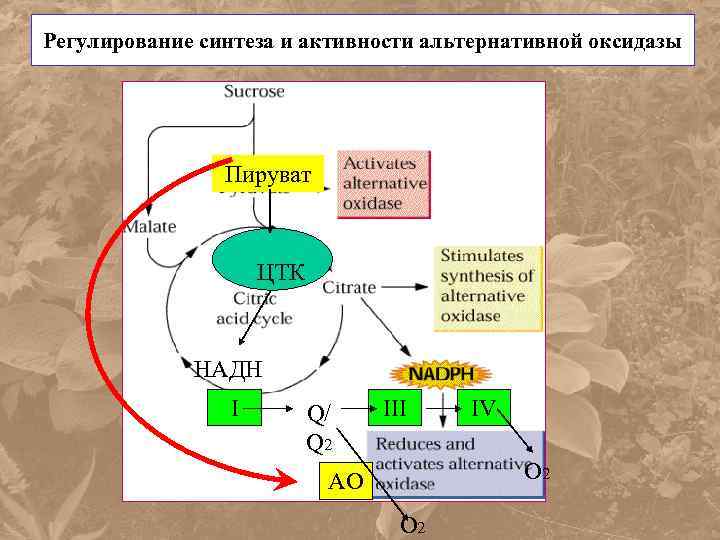
Регулирование синтеза и активности альтернативной оксидазы Пируват ЦТК НАДН I Q/ Q 2 III IV O 2 AO O 2

Регуляция активности АО • Электронные потоки в дыхательной цепи распределяются по цитохромному и альтернативному пути согласно активности двух терминальных оксидаз, которые конкурируют за электроны.
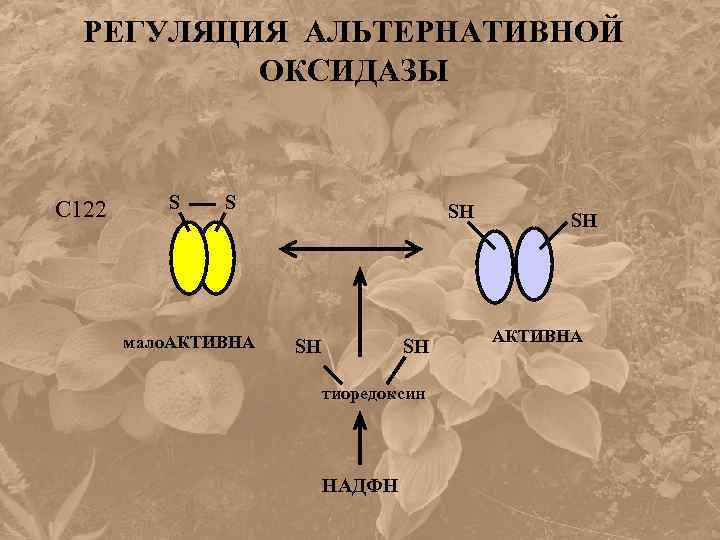
РЕГУЛЯЦИЯ АЛЬТЕРНАТИВНОЙ ОКСИДАЗЫ С 122 S S мало. АКТИВНА SH SH SH тиоредоксин НАДФН SH АКТИВНА
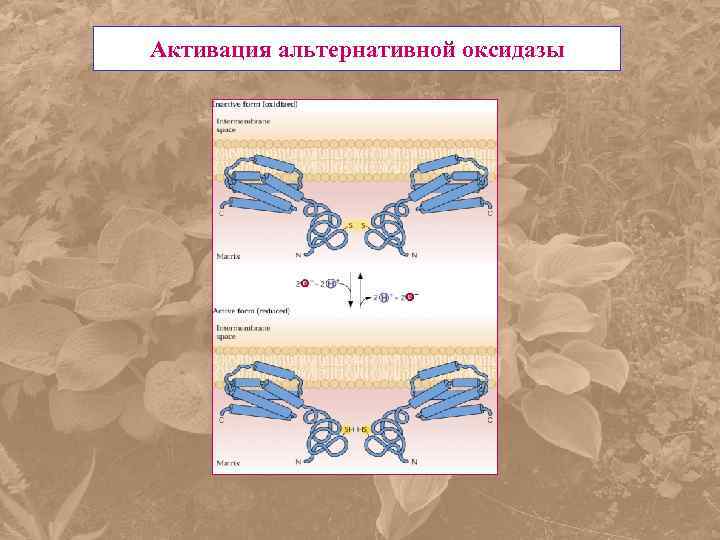
Активация альтернативной оксидазы

• В восстановленном состоянии АО аллостерически активируется пируватом и другими кетокислотами.
05Дыхание Bio.ppt