1 Цикл Карно Можно показать, что Можно построить



























38944-phys_chem_biol_3_2011.ppt
- Количество слайдов: 33
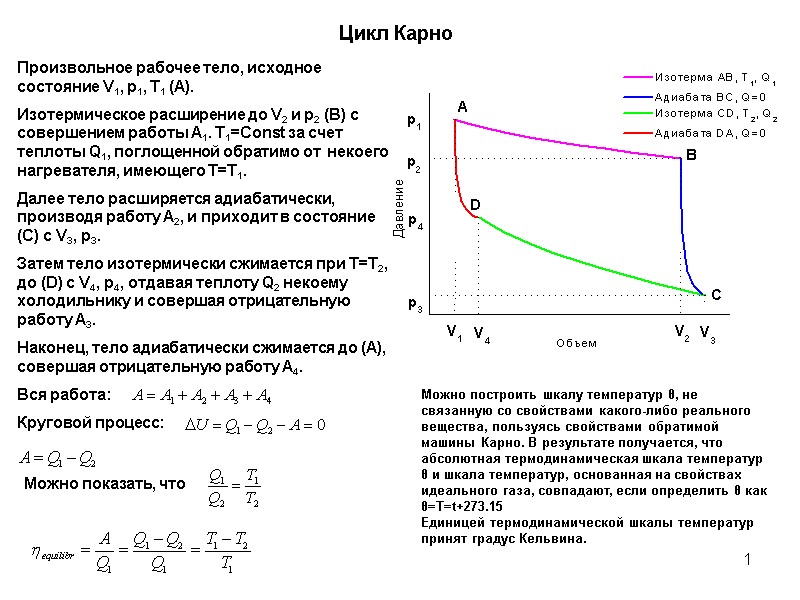
 1 Цикл Карно Можно показать, что Можно построить шкалу температур θ, не связанную со свойствами какого-либо реального вещества, пользуясь свойствами обратимой машины Карно. В результате получается, что абсолютная термодинамическая шкала температур θ и шкала температур, основанная на свойствах идеального газа, совпадают, если определить θ как θ=T=t+273.15 Единицей термодинамической шкалы температур принят градус Кельвина.
1 Цикл Карно Можно показать, что Можно построить шкалу температур θ, не связанную со свойствами какого-либо реального вещества, пользуясь свойствами обратимой машины Карно. В результате получается, что абсолютная термодинамическая шкала температур θ и шкала температур, основанная на свойствах идеального газа, совпадают, если определить θ как θ=T=t+273.15 Единицей термодинамической шкалы температур принят градус Кельвина.
 2 Количественная формулировка 2-го начала термодинамики, энтропия Для обратимой машины Карно , а для необратимой Отношение Q/T называют приведенной теплотой.
2 Количественная формулировка 2-го начала термодинамики, энтропия Для обратимой машины Карно , а для необратимой Отношение Q/T называют приведенной теплотой.
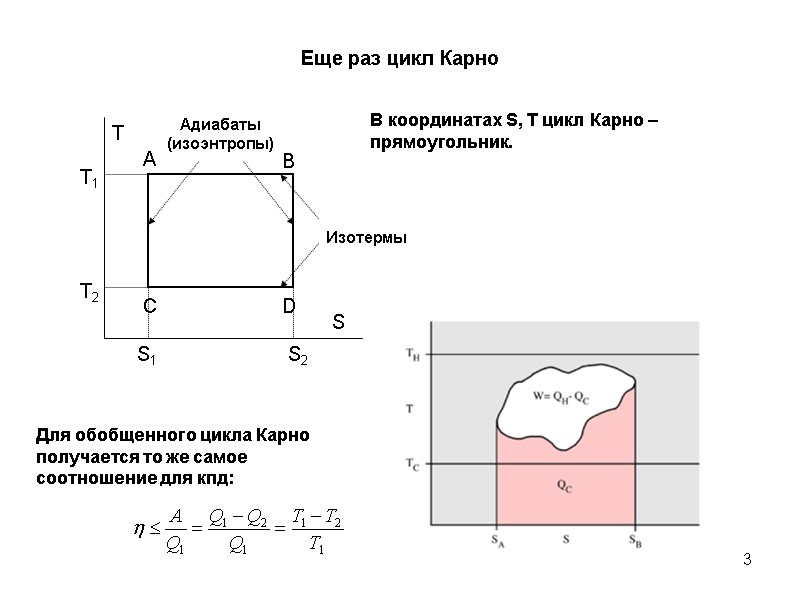
 3 Еще раз цикл Карно В координатах S, T цикл Карно – прямоугольник. Для обобщенного цикла Карно получается то же самое соотношение для кпд:
3 Еще раз цикл Карно В координатах S, T цикл Карно – прямоугольник. Для обобщенного цикла Карно получается то же самое соотношение для кпд:
 4 Энтропия и вероятность В статистической термодинамике показывается, что энтропия и вероятность состояния системы связаны уравнением вида , здесь W – вероятность состояния, A и B – некоторые константы. Почему логарифмическая связь? В принципе, это понятно т.к. энтропия системы аддитивна (складывается из энтропий ее частей), а вероятность конечного события – это произведение вероятностей отдельных событий. 2-й закон термодинамики – статистический закон, он строго соблюдается только для ансамблей из большого числа частиц (вспомним падение одиночного шарика и распределение шариков в коробке с емкостями). Пример: подбрасывание монет. 10 монет подбрасываем 500 раз. Вероятность выпасть поровну 5 орлов и 5 решек (5/5) – 24.6%, а 9 орлов и 1 решка или наоборот (9/1) – 1%. Различие между наиболее и наименее вероятными исходами всего 24.6 раза. Сделаем то же самое со 100 монетами – различие между 50/50 и 90/10 уже 1016 раз! В реальных системах число частиц порядка 1020, даже в нано-системах содержится порядка 103 частиц, поэтому 2-е начало соблюдается.
4 Энтропия и вероятность В статистической термодинамике показывается, что энтропия и вероятность состояния системы связаны уравнением вида , здесь W – вероятность состояния, A и B – некоторые константы. Почему логарифмическая связь? В принципе, это понятно т.к. энтропия системы аддитивна (складывается из энтропий ее частей), а вероятность конечного события – это произведение вероятностей отдельных событий. 2-й закон термодинамики – статистический закон, он строго соблюдается только для ансамблей из большого числа частиц (вспомним падение одиночного шарика и распределение шариков в коробке с емкостями). Пример: подбрасывание монет. 10 монет подбрасываем 500 раз. Вероятность выпасть поровну 5 орлов и 5 решек (5/5) – 24.6%, а 9 орлов и 1 решка или наоборот (9/1) – 1%. Различие между наиболее и наименее вероятными исходами всего 24.6 раза. Сделаем то же самое со 100 монетами – различие между 50/50 и 90/10 уже 1016 раз! В реальных системах число частиц порядка 1020, даже в нано-системах содержится порядка 103 частиц, поэтому 2-е начало соблюдается.
 5 Возрастание энтропии при равновесном изотермическом расширении идеального газа Феноменологический подход Работа равновесного расширения газа Теплота равна работе с обр. знаком Получаем энтропию: Сравнивая (1) и (2) получим NA=R. Если был 1 моль газа, то N – число Авогадро NA, след. постоянная A=R/NA=k – постоянная Больцмана. (1) (2)
5 Возрастание энтропии при равновесном изотермическом расширении идеального газа Феноменологический подход Работа равновесного расширения газа Теплота равна работе с обр. знаком Получаем энтропию: Сравнивая (1) и (2) получим NA=R. Если был 1 моль газа, то N – число Авогадро NA, след. постоянная A=R/NA=k – постоянная Больцмана. (1) (2)
 6 Знание о том, как меняется энтропия в том или ином процессе позволяет предвидеть, пойдет ли такой процесс самопроизвольно, или нет. Проблема в том, что надо знать общее изменение энтропии – не только рассматриваемой системы, но и окружающей ее среды. ΔSsyst+ΔSenvir=0 система находится в равновесии сама и с окружающей средой ΔSsyst+ΔSenvir>0 процесс может проходить самопроизвольно ΔSsyst+ΔSenvir<0 процесс не может проходить самопроизвольно Поэтому пользоваться энтропией как таковой неудобно. Удобнее использовать другую термодинамическую функцию – свободную энергию. Растения и животные самопроизвольно развиваются в очень сложные, высокоупорядоченные структуры. Энтропия – мера хаотичности, разупорядоченности. Находятся ли закономерности биологических систем в противоречии со 2-м началом? Считается, что противоречия нет, т.к. энтропия организма уменьшается, а энтропия окружающей среды при этом увеличивается, причем в большей степени.
6 Знание о том, как меняется энтропия в том или ином процессе позволяет предвидеть, пойдет ли такой процесс самопроизвольно, или нет. Проблема в том, что надо знать общее изменение энтропии – не только рассматриваемой системы, но и окружающей ее среды. ΔSsyst+ΔSenvir=0 система находится в равновесии сама и с окружающей средой ΔSsyst+ΔSenvir>0 процесс может проходить самопроизвольно ΔSsyst+ΔSenvir<0 процесс не может проходить самопроизвольно Поэтому пользоваться энтропией как таковой неудобно. Удобнее использовать другую термодинамическую функцию – свободную энергию. Растения и животные самопроизвольно развиваются в очень сложные, высокоупорядоченные структуры. Энтропия – мера хаотичности, разупорядоченности. Находятся ли закономерности биологических систем в противоречии со 2-м началом? Считается, что противоречия нет, т.к. энтропия организма уменьшается, а энтропия окружающей среды при этом увеличивается, причем в большей степени.
 7 Самопроизвольное возникновение упорядоченной структуры в неживом объекте
7 Самопроизвольное возникновение упорядоченной структуры в неживом объекте
 8 3-й закон термодинамики Нернст (1906 г.) экспериментально обнаружил, что при стремлении температуры к абсолютному нулю энтропия химических реакций также стремится к нулю. Планк (1912 г.) на основании данных Нернста выдвинул гипотезу (постулат): «Энтропия индивидуальных кристаллических веществ при абсолютном нуле равна нулю» Это – гипотеза, проверить ее невозможно т.к. абсолютный нуль недостижим: нет холодильника с отрицательной абсолютной температурой, которому можно было бы отдать последние остатки тепла. Если поверить в гипотезу Планка, то можно вычислить абсолютную энтропию. Например, некий кристалл плавится при 15 K. Хотим вычислить его энтропию при 273 K. Теплоемкость при сравнительно высоких температурах измеряют экспериментально, а вблизи абсолютного нуля обычно считают по теории теплоемкости Дебая.
8 3-й закон термодинамики Нернст (1906 г.) экспериментально обнаружил, что при стремлении температуры к абсолютному нулю энтропия химических реакций также стремится к нулю. Планк (1912 г.) на основании данных Нернста выдвинул гипотезу (постулат): «Энтропия индивидуальных кристаллических веществ при абсолютном нуле равна нулю» Это – гипотеза, проверить ее невозможно т.к. абсолютный нуль недостижим: нет холодильника с отрицательной абсолютной температурой, которому можно было бы отдать последние остатки тепла. Если поверить в гипотезу Планка, то можно вычислить абсолютную энтропию. Например, некий кристалл плавится при 15 K. Хотим вычислить его энтропию при 273 K. Теплоемкость при сравнительно высоких температурах измеряют экспериментально, а вблизи абсолютного нуля обычно считают по теории теплоемкости Дебая.
 9 Термодинамические потенциалы Термодинамические потенциалы – это функции состояния системы, имеющие размерность энергии. Они являются критериями направления процесса, их экстремальные значения при соответствующих условиях отвечают равновесию и являются условиями равновесия. В принципе, можно пользоваться этими потенциалами как критериями самопроизвольного протекания процесса и условиями равновесия. Но поддерживать энтропию постоянной крайне трудно. Поэтому использовать внутреннюю энергию или энтальпию в качестве потенциалов неудобно. Гораздо удобнее свободная энергия Гельмгольца, и особенно – свободная энергия Гиббса.
9 Термодинамические потенциалы Термодинамические потенциалы – это функции состояния системы, имеющие размерность энергии. Они являются критериями направления процесса, их экстремальные значения при соответствующих условиях отвечают равновесию и являются условиями равновесия. В принципе, можно пользоваться этими потенциалами как критериями самопроизвольного протекания процесса и условиями равновесия. Но поддерживать энтропию постоянной крайне трудно. Поэтому использовать внутреннюю энергию или энтальпию в качестве потенциалов неудобно. Гораздо удобнее свободная энергия Гельмгольца, и особенно – свободная энергия Гиббса.
 10 Изохорно-изотермический потенциал (V,T=Const) – свободная энергия Гельмгольца (формально – объединение 1-го и 2-го начал) В общем случае: При равновесии: Проинтегрируем от состояния 1 до состояния 2, получим: Вполне логично: максимальная работа, которую может совершить система при переходе из состояния 1 в состояние 2 равна убыли ее внутренней энергии за вычетом некой части энергии, которую превратить в работу нельзя («связанной энергии»). Величины в скобках – комбинации функций состояния, следовательно – сами по себе также функции состояния, Внутренняя энергия состоит из свободной и связанной: Связанная (TS) может переходить только в теплоту, TΔS=Q. Свободная энергия F в равновесном процессе переходит в работу, в неравновесном – частично также в теплоту. Если T≠Const, U нельзя разделить на свободную и связанную. Можно показать, что и . Это значит, что F падает с ростом объема и температуры.
10 Изохорно-изотермический потенциал (V,T=Const) – свободная энергия Гельмгольца (формально – объединение 1-го и 2-го начал) В общем случае: При равновесии: Проинтегрируем от состояния 1 до состояния 2, получим: Вполне логично: максимальная работа, которую может совершить система при переходе из состояния 1 в состояние 2 равна убыли ее внутренней энергии за вычетом некой части энергии, которую превратить в работу нельзя («связанной энергии»). Величины в скобках – комбинации функций состояния, следовательно – сами по себе также функции состояния, Внутренняя энергия состоит из свободной и связанной: Связанная (TS) может переходить только в теплоту, TΔS=Q. Свободная энергия F в равновесном процессе переходит в работу, в неравновесном – частично также в теплоту. Если T≠Const, U нельзя разделить на свободную и связанную. Можно показать, что и . Это значит, что F падает с ростом объема и температуры.
 11 Изобарно-изотермический потенциал (p,T=Const) – свободная энергия Гиббса Свободная энергия Гиббса применяется в химии чаще, чем свободная энергия Гельмгольца т.к. химические процессы обычно идут при постоянном давлении, в частности – атмосферном, но вовсе не при постоянном объеме. Среди всех возможных работ A выделим работу расширения pV. Остальные работы A’ считают «полезными»: δA=pdV+δA’. Интегрируя при p,T=Const, получим Таким образом, имеем новую функцию состояния: свободную энергию Гиббса Полезная работа, которую может совершить система В равновесном процессе: Можно показать, что и . Таким образом, G увеличивается с ростом давления и уменьшается с ростом температуры.
11 Изобарно-изотермический потенциал (p,T=Const) – свободная энергия Гиббса Свободная энергия Гиббса применяется в химии чаще, чем свободная энергия Гельмгольца т.к. химические процессы обычно идут при постоянном давлении, в частности – атмосферном, но вовсе не при постоянном объеме. Среди всех возможных работ A выделим работу расширения pV. Остальные работы A’ считают «полезными»: δA=pdV+δA’. Интегрируя при p,T=Const, получим Таким образом, имеем новую функцию состояния: свободную энергию Гиббса Полезная работа, которую может совершить система В равновесном процессе: Можно показать, что и . Таким образом, G увеличивается с ростом давления и уменьшается с ростом температуры.
 12 Характеристические функции и естественные переменные Частные производные этих функций при характерном для них наборе параметров дают величины основных параметров состояния. Таким образом, через эти функции и их производные можно выразить в явной форме любое термодинамическое свойство системы. В этом состоит характеристичность. Замена этих переменных другими (в принципе – вполне возможная) лишает их характеристичности. Поэтому такие переменные называются естественными.
12 Характеристические функции и естественные переменные Частные производные этих функций при характерном для них наборе параметров дают величины основных параметров состояния. Таким образом, через эти функции и их производные можно выразить в явной форме любое термодинамическое свойство системы. В этом состоит характеристичность. Замена этих переменных другими (в принципе – вполне возможная) лишает их характеристичности. Поэтому такие переменные называются естественными.
 13 Условия самопроизвольного протекания процессов ΔU < 0 при S,V=Const ΔH < 0 при S,p=Const ΔF < 0 при T,V=Const ΔG < 0 при p,T=Const Условия равновесия В состоянии равновесия системы ее термодинамические потенциалы имеют минимальные значения при постоянстве своих естественных переменных, а энтропия имеет максимальное значение (при своих естественных переменных – U,V или H,p). Убыль т.д. потенциалов в равновесном процессе при постоянстве естественных переменных равна максимальной работе, которую может совершить система.
13 Условия самопроизвольного протекания процессов ΔU < 0 при S,V=Const ΔH < 0 при S,p=Const ΔF < 0 при T,V=Const ΔG < 0 при p,T=Const Условия равновесия В состоянии равновесия системы ее термодинамические потенциалы имеют минимальные значения при постоянстве своих естественных переменных, а энтропия имеет максимальное значение (при своих естественных переменных – U,V или H,p). Убыль т.д. потенциалов в равновесном процессе при постоянстве естественных переменных равна максимальной работе, которую может совершить система.
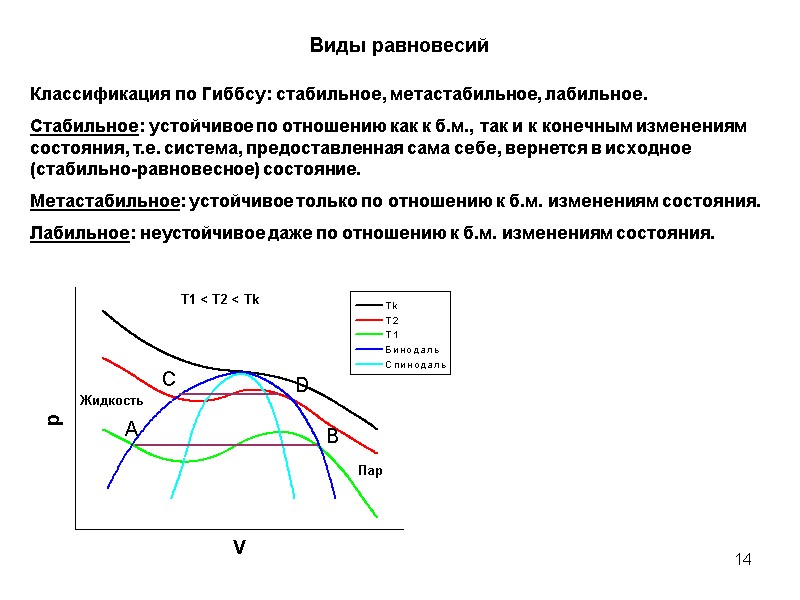
 14 Виды равновесий Классификация по Гиббсу: стабильное, метастабильное, лабильное. Стабильное: устойчивое по отношению как к б.м., так и к конечным изменениям состояния, т.е. система, предоставленная сама себе, вернется в исходное (стабильно-равновесное) состояние. Метастабильное: устойчивое только по отношению к б.м. изменениям состояния. Лабильное: неустойчивое даже по отношению к б.м. изменениям состояния. Жидкость Пар A B C D
14 Виды равновесий Классификация по Гиббсу: стабильное, метастабильное, лабильное. Стабильное: устойчивое по отношению как к б.м., так и к конечным изменениям состояния, т.е. система, предоставленная сама себе, вернется в исходное (стабильно-равновесное) состояние. Метастабильное: устойчивое только по отношению к б.м. изменениям состояния. Лабильное: неустойчивое даже по отношению к б.м. изменениям состояния. Жидкость Пар A B C D
 15 Уравнение Гиббса-Гельмгольца Гиббс и Гельмгольц независимо получили отсюда полезное выражение для энтальпии – теплового эффекта химической реакции. Поскольку , можно записать Для конечных приращений можно, соответственно, записать Зная ΔG, можно вычислить ΔH реакции, если известна температурная зависимость ΔG при постоянном давлении – надо получить зависимость ΔG/T от 1/T. ΔG= -RTlnK, K – константа равновесия химической реакции.
15 Уравнение Гиббса-Гельмгольца Гиббс и Гельмгольц независимо получили отсюда полезное выражение для энтальпии – теплового эффекта химической реакции. Поскольку , можно записать Для конечных приращений можно, соответственно, записать Зная ΔG, можно вычислить ΔH реакции, если известна температурная зависимость ΔG при постоянном давлении – надо получить зависимость ΔG/T от 1/T. ΔG= -RTlnK, K – константа равновесия химической реакции.
 16 Фазовые переходы Фазовые переходы в «чистом виде»: в системе только 1 вещество, возможно наличие нескольких фаз – различных агрегатных состояний этого вещества. 1 моль вещества переходит из состояния 1 в состояние 2. p, T=Const Работа – только расширение. Рассмотрим изменение внутренней энергии. Потенциал Гиббса для 1 моля (или 1 ед. массы) вещества в двух фазах, при равновесии один и тот же. Если фазы находятся в равновесии, то p, T не могут меняться независимо. Меняются так, что при
16 Фазовые переходы Фазовые переходы в «чистом виде»: в системе только 1 вещество, возможно наличие нескольких фаз – различных агрегатных состояний этого вещества. 1 моль вещества переходит из состояния 1 в состояние 2. p, T=Const Работа – только расширение. Рассмотрим изменение внутренней энергии. Потенциал Гиббса для 1 моля (или 1 ед. массы) вещества в двух фазах, при равновесии один и тот же. Если фазы находятся в равновесии, то p, T не могут меняться независимо. Меняются так, что при
 17 Уравнение Клаузиуса-Клапейрона λ – теплота фазового перехода Фазовые переходы 1-го рода Фазовые переходы 1-го рода: плавление, испарение, возгонка. Интенсивные параметры меняются скачкообразно, а экстенсивные – непрерывно. Откуда может взяться эта закономерность, и на что могут указывать отклонения от нее? При фазовом переходе энтальпия изменяется скачком. Это значит, что Подводимое к системе тепло затрачивается на совершение фазового перехода, а не на подъем температуры.
17 Уравнение Клаузиуса-Клапейрона λ – теплота фазового перехода Фазовые переходы 1-го рода Фазовые переходы 1-го рода: плавление, испарение, возгонка. Интенсивные параметры меняются скачкообразно, а экстенсивные – непрерывно. Откуда может взяться эта закономерность, и на что могут указывать отклонения от нее? При фазовом переходе энтальпия изменяется скачком. Это значит, что Подводимое к системе тепло затрачивается на совершение фазового перехода, а не на подъем температуры.
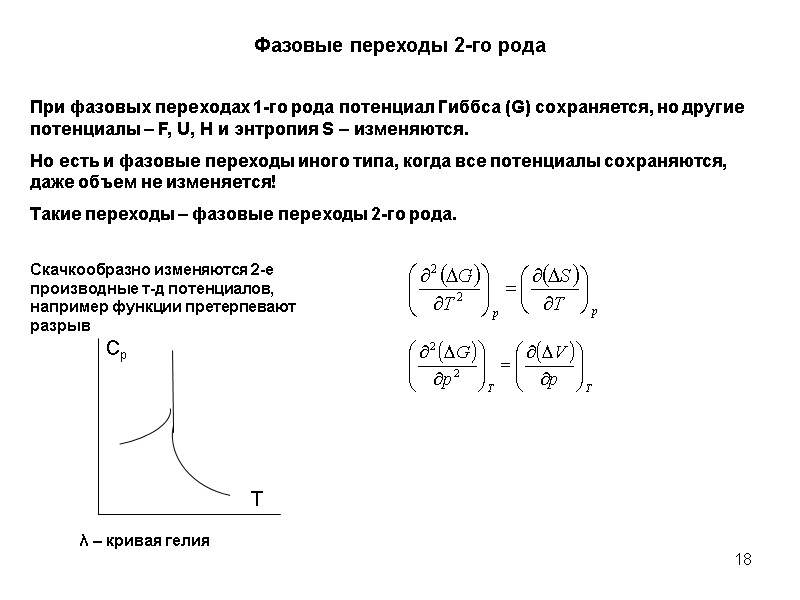
 18 Фазовые переходы 2-го рода При фазовых переходах 1-го рода потенциал Гиббса (G) сохраняется, но другие потенциалы – F, U, H и энтропия S – изменяются. Но есть и фазовые переходы иного типа, когда все потенциалы сохраняются, даже объем не изменяется! Такие переходы – фазовые переходы 2-го рода. Скачкообразно изменяются 2-е производные т-д потенциалов, например функции претерпевают разрыв λ – кривая гелия
18 Фазовые переходы 2-го рода При фазовых переходах 1-го рода потенциал Гиббса (G) сохраняется, но другие потенциалы – F, U, H и энтропия S – изменяются. Но есть и фазовые переходы иного типа, когда все потенциалы сохраняются, даже объем не изменяется! Такие переходы – фазовые переходы 2-го рода. Скачкообразно изменяются 2-е производные т-д потенциалов, например функции претерпевают разрыв λ – кривая гелия
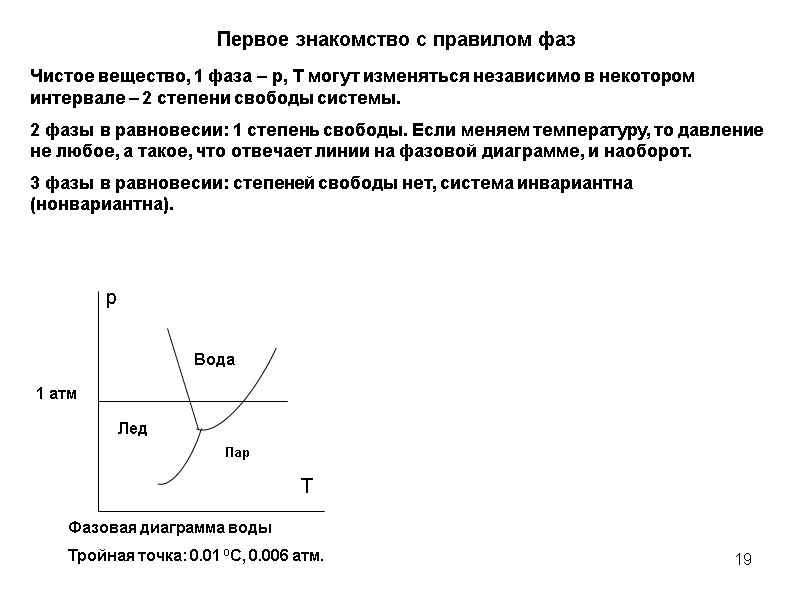
 19 Фазовая диаграмма воды Тройная точка: 0.01 0С, 0.006 атм. Чистое вещество, 1 фаза – p, T могут изменяться независимо в некотором интервале – 2 степени свободы системы. 2 фазы в равновесии: 1 степень свободы. Если меняем температуру, то давление не любое, а такое, что отвечает линии на фазовой диаграмме, и наоборот. 3 фазы в равновесии: степеней свободы нет, система инвариантна (нонвариантна). Первое знакомство с правилом фаз
19 Фазовая диаграмма воды Тройная точка: 0.01 0С, 0.006 атм. Чистое вещество, 1 фаза – p, T могут изменяться независимо в некотором интервале – 2 степени свободы системы. 2 фазы в равновесии: 1 степень свободы. Если меняем температуру, то давление не любое, а такое, что отвечает линии на фазовой диаграмме, и наоборот. 3 фазы в равновесии: степеней свободы нет, система инвариантна (нонвариантна). Первое знакомство с правилом фаз
 20 Многокомпонентные системы Система содержит k компонентов ni – число молей i-го компонента Если процесс равновесный и работа только расширения, то Химический потенциал i-го компонента Дифференциал функции Гиббса при p, T = Const
20 Многокомпонентные системы Система содержит k компонентов ni – число молей i-го компонента Если процесс равновесный и работа только расширения, то Химический потенциал i-го компонента Дифференциал функции Гиббса при p, T = Const
 21 Что произойдет если массу системы увеличить в q раз, сохраняя пропорции между ее компонентами? Все экстенсивные параметры системы – V, U, S, H, F, G также возрастут в q раз. Таким образом, эти величины, в т.ч. G – линейные однородные функции. Уравнение Гиббса-Дюгема
21 Что произойдет если массу системы увеличить в q раз, сохраняя пропорции между ее компонентами? Все экстенсивные параметры системы – V, U, S, H, F, G также возрастут в q раз. Таким образом, эти величины, в т.ч. G – линейные однородные функции. Уравнение Гиббса-Дюгема
 22 Равенство значений интенсивных параметров в сосуществующих фазах при равновесии
22 Равенство значений интенсивных параметров в сосуществующих фазах при равновесии
 23 Правило фаз Гиббса Система, находящаяся в состоянии равновесия, содержит Φ фаз и k компонентов. Сколько степеней свободы может быть у такой системы? Давление и температура во всех Φ фазах одинаковы. Химические потенциалы каждого из компонентов также одинаковы во всех фазах. Всего имеем k+2 переменных: k компонентов, их концентрации могут изменяться независимо, + давление, + температура. Уравнений связи между переменными – Φ. Следовательно, число независимых переменных (степеней свободы) равно f = k – Φ + 2 Как это согласуется со льдинами, плывущими по Неве?
23 Правило фаз Гиббса Система, находящаяся в состоянии равновесия, содержит Φ фаз и k компонентов. Сколько степеней свободы может быть у такой системы? Давление и температура во всех Φ фазах одинаковы. Химические потенциалы каждого из компонентов также одинаковы во всех фазах. Всего имеем k+2 переменных: k компонентов, их концентрации могут изменяться независимо, + давление, + температура. Уравнений связи между переменными – Φ. Следовательно, число независимых переменных (степеней свободы) равно f = k – Φ + 2 Как это согласуется со льдинами, плывущими по Неве?
 24 Идеальные газовые смеси
24 Идеальные газовые смеси
 25 Неидеальные газовые смеси, фугитивность
25 Неидеальные газовые смеси, фугитивность
 26 Растворы неэлектролитов Раствор: жидкая фаза, состав которой (в некоторых пределах) можно изменять непрерывно. Неэлектролит: вещество, которое при растворении не распадается на ионные (заряженные) составляющие, неионогенное вещество. Равновесие жидкий раствор – насыщенный пар.
26 Растворы неэлектролитов Раствор: жидкая фаза, состав которой (в некоторых пределах) можно изменять непрерывно. Неэлектролит: вещество, которое при растворении не распадается на ионные (заряженные) составляющие, неионогенное вещество. Равновесие жидкий раствор – насыщенный пар.
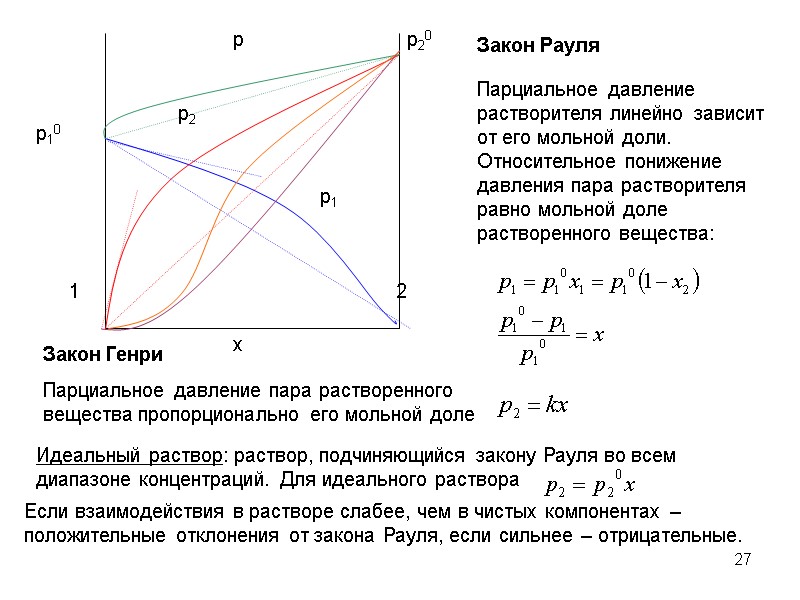
 27 Если взаимодействия в растворе слабее, чем в чистых компонентах – положительные отклонения от закона Рауля, если сильнее – отрицательные.
27 Если взаимодействия в растворе слабее, чем в чистых компонентах – положительные отклонения от закона Рауля, если сильнее – отрицательные.
 28 Активность компонента раствора Стандартное состояние растворенного вещества – такое, когда его летучесть равна коэффициенту Генри в предельно разбавленном растворе.
28 Активность компонента раствора Стандартное состояние растворенного вещества – такое, когда его летучесть равна коэффициенту Генри в предельно разбавленном растворе.
 29 Коллигативные свойства растворов Криоскопия Температура начала затвердевания раствора – Т, при которой раствор стал насыщенным по отношению к чистому растворителю. При Ткр давление пара растворителя над раствором и над твердым растворителем одинаково.
29 Коллигативные свойства растворов Криоскопия Температура начала затвердевания раствора – Т, при которой раствор стал насыщенным по отношению к чистому растворителю. При Ткр давление пара растворителя над раствором и над твердым растворителем одинаково.
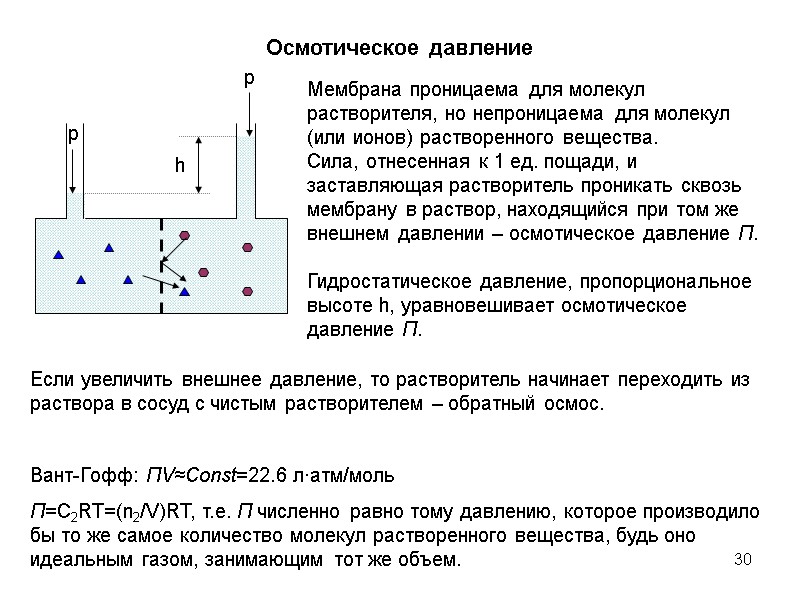
 30 Осмотическое давление Мембрана проницаема для молекул растворителя, но непроницаема для молекул (или ионов) растворенного вещества. Сила, отнесенная к 1 ед. пощади, и заставляющая растворитель проникать сквозь мембрану в раствор, находящийся при том же внешнем давлении – осмотическое давление Π. Гидростатическое давление, пропорциональное высоте h, уравновешивает осмотическое давление Π. Если увеличить внешнее давление, то растворитель начинает переходить из раствора в сосуд с чистым растворителем – обратный осмос. Вант-Гофф: ΠV≈Const=22.6 л∙атм/моль Π=С2RT=(n2/V)RT, т.е. Π численно равно тому давлению, которое производило бы то же самое количество молекул растворенного вещества, будь оно идеальным газом, занимающим тот же объем.
30 Осмотическое давление Мембрана проницаема для молекул растворителя, но непроницаема для молекул (или ионов) растворенного вещества. Сила, отнесенная к 1 ед. пощади, и заставляющая растворитель проникать сквозь мембрану в раствор, находящийся при том же внешнем давлении – осмотическое давление Π. Гидростатическое давление, пропорциональное высоте h, уравновешивает осмотическое давление Π. Если увеличить внешнее давление, то растворитель начинает переходить из раствора в сосуд с чистым растворителем – обратный осмос. Вант-Гофф: ΠV≈Const=22.6 л∙атм/моль Π=С2RT=(n2/V)RT, т.е. Π численно равно тому давлению, которое производило бы то же самое количество молекул растворенного вещества, будь оно идеальным газом, занимающим тот же объем.
 31 Термодинамика осмотического давления Осмотическая мембрана: в сущности, «продолжение» фазы растворителя. Потому фаз 2, компонентов 2, при фиксации p, T система становится нонвариантной: f=0.
31 Термодинамика осмотического давления Осмотическая мембрана: в сущности, «продолжение» фазы растворителя. Потому фаз 2, компонентов 2, при фиксации p, T система становится нонвариантной: f=0.
 32 Химическое равновесие В состоянии равновесия Равновесие химической реакции: νAA + νBB ↔ νCC + νDD
32 Химическое равновесие В состоянии равновесия Равновесие химической реакции: νAA + νBB ↔ νCC + νDD
 33 Принцип Ле-Шателье - Брауна Для экзотермических реакций, когда изменения энтальпии меньше нуля, производная константы равновесия по температуре меньше нуля, т.е. с увеличением температуры уменьшается глубина протекания процесса, идущего с выделением тепла (константа уменьшается) Для эндотермических процессов когда изменения энтальпии больше нуля, производная константы равновесия по температуре больше нуля, т.е с увеличением температуры увеличивается глубина протекания процесса, идущего с поглощением тепла (константа растет).
33 Принцип Ле-Шателье - Брауна Для экзотермических реакций, когда изменения энтальпии меньше нуля, производная константы равновесия по температуре меньше нуля, т.е. с увеличением температуры уменьшается глубина протекания процесса, идущего с выделением тепла (константа уменьшается) Для эндотермических процессов когда изменения энтальпии больше нуля, производная константы равновесия по температуре больше нуля, т.е с увеличением температуры увеличивается глубина протекания процесса, идущего с поглощением тепла (константа растет).

