 1. Что изучает химия? Химия – это наука о веществах, их свойствах и превращениях веществ.
1. Что изучает химия? Химия – это наука о веществах, их свойствах и превращениях веществ.
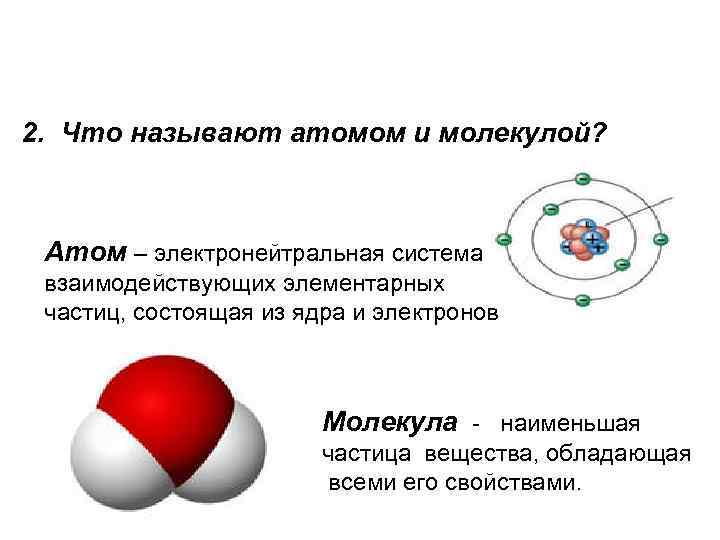 2. Что называют атомом и молекулой? Атом – электронейтральная система взаимодействующих элементарных частиц, состоящая из ядра и электронов Молекула - наименьшая частица вещества, обладающая всеми его свойствами.
2. Что называют атомом и молекулой? Атом – электронейтральная система взаимодействующих элементарных частиц, состоящая из ядра и электронов Молекула - наименьшая частица вещества, обладающая всеми его свойствами.
 • 3. Что такое абсолютная и относительная атомная и молекулярная массы?
• 3. Что такое абсолютная и относительная атомная и молекулярная массы?
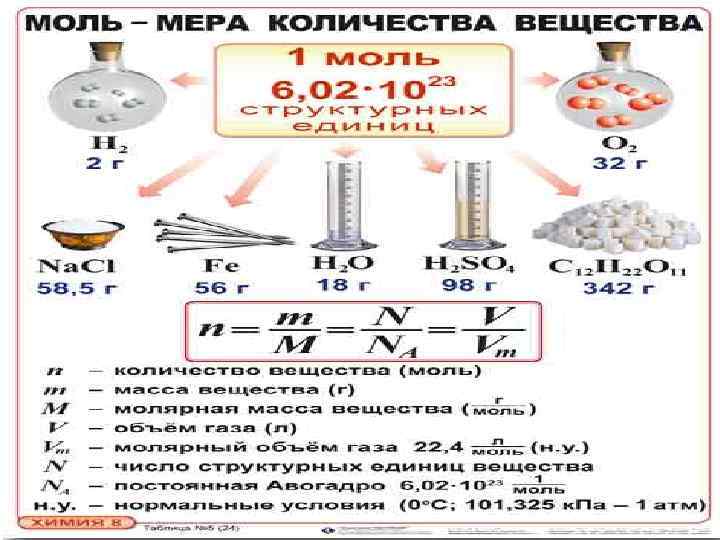
 • Относительная атомная масса (см. атомная масса химического элемента) Аr • Относительная молекулярная масса ( сумма относительных атомных масс всех атомов, образующих молекулу вещества) Mr • КОЛИЧЕСТВО ВЕЩЕСТВА – число атомов, молекул или других формульных единиц вещества (моль) Молярная масса – масса 1 моль вещества (г моль, кг моль) М • Молярный объем – объем 1 моль газа при н. у. Vm = 22, 4 л/моль
• Относительная атомная масса (см. атомная масса химического элемента) Аr • Относительная молекулярная масса ( сумма относительных атомных масс всех атомов, образующих молекулу вещества) Mr • КОЛИЧЕСТВО ВЕЩЕСТВА – число атомов, молекул или других формульных единиц вещества (моль) Молярная масса – масса 1 моль вещества (г моль, кг моль) М • Молярный объем – объем 1 моль газа при н. у. Vm = 22, 4 л/моль


 • 4. Основные положения атомно-молекулярного учения. Атомно-молекулярное теория базируется на следующих законах и утверждениях: • Все вещества состоят из атомов • Атомы одного химического вещества (химический элемент) обладают одинаковыми свойствами, но отличаются от атомов другого вещества • При взаимодействии атомов образуются молекулы (гомоядерные — простые вещества, гетероядерные — сложные вещества) • При физических явлениях молекулы не изменяются, при химических происходит изменение их состава • Химические реакции заключаются в образовании новых веществ из тех же самых атомов, из которых состояли исходные вещества
• 4. Основные положения атомно-молекулярного учения. Атомно-молекулярное теория базируется на следующих законах и утверждениях: • Все вещества состоят из атомов • Атомы одного химического вещества (химический элемент) обладают одинаковыми свойствами, но отличаются от атомов другого вещества • При взаимодействии атомов образуются молекулы (гомоядерные — простые вещества, гетероядерные — сложные вещества) • При физических явлениях молекулы не изменяются, при химических происходит изменение их состава • Химические реакции заключаются в образовании новых веществ из тех же самых атомов, из которых состояли исходные вещества
 • 5. Строение атома. -Ядро : протоны и нейтроны -Электроны
• 5. Строение атома. -Ядро : протоны и нейтроны -Электроны


 • 6. Химический элемент, изотопы. Химический элемент – совокупность атомов с одинаковым зарядом ядра ( числом протонов). Изотопы - разновидность атомов одного химического элемента с разным числом нейтронов в ядре.
• 6. Химический элемент, изотопы. Химический элемент – совокупность атомов с одинаковым зарядом ядра ( числом протонов). Изотопы - разновидность атомов одного химического элемента с разным числом нейтронов в ядре.
 7. Вещество. Это вид материи; физическая субстанция со специфическими химическими свойствами.
7. Вещество. Это вид материи; физическая субстанция со специфическими химическими свойствами.
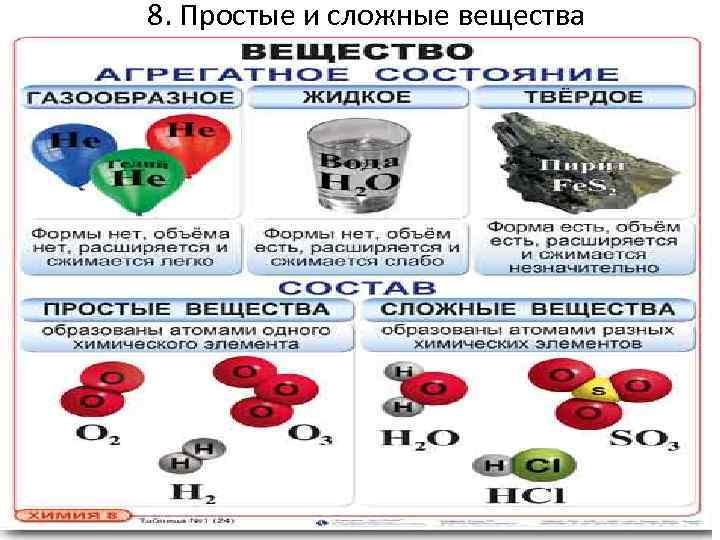 8. Простые и сложные вещества
8. Простые и сложные вещества
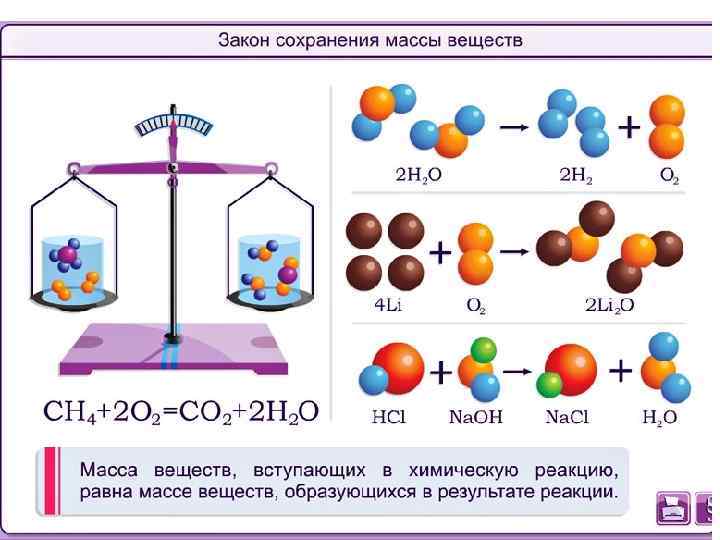 • Закон сохранения массы веществ в реакциях
• Закон сохранения массы веществ в реакциях
 • Периодический закон Свойства простых веществ, а также формы и свойства соединений элементов находятся в периодической зависимости от заряда ядра элемента. 2/17/2018 16
• Периодический закон Свойства простых веществ, а также формы и свойства соединений элементов находятся в периодической зависимости от заряда ядра элемента. 2/17/2018 16
 Основные законы химии • Закон постоянства состава Каждое вещество, каким бы способом оно ни было получено, всегда имеет один и тот же качественный и количественный состав (и свойства). • Закон эквивалентов Вещества взаимодействуют между собой в количествах, пропорциональных их эквивалентам. 2/17/2018 r 17
Основные законы химии • Закон постоянства состава Каждое вещество, каким бы способом оно ни было получено, всегда имеет один и тот же качественный и количественный состав (и свойства). • Закон эквивалентов Вещества взаимодействуют между собой в количествах, пропорциональных их эквивалентам. 2/17/2018 r 17
 Основные законы химии • Закон кратных отношений Если два элемента образуют между собой несколько соединений, то массовые доли любого из элементов в этих соединениях относятся друг к другу как небольшие целые числа. • Закон объемных отношений Объемы вступающих в реакцию газов, а также объемы газообразных продуктов 2/17/2018 18
Основные законы химии • Закон кратных отношений Если два элемента образуют между собой несколько соединений, то массовые доли любого из элементов в этих соединениях относятся друг к другу как небольшие целые числа. • Закон объемных отношений Объемы вступающих в реакцию газов, а также объемы газообразных продуктов 2/17/2018 18
 Основные законы химии • Закон Авогадро В равных объемах различных газов при одинаковых условиях (температура и давление) содержится одинаковое число молекул. • Следствия из закона Авогадро 1. При одинаковых условиях равные количества различных газов занимают равные объемы. 2. При н. у. (Т = 273, 15 К, Р = 1, 01 ∙ 105 Па или t 2/17/2018 19
Основные законы химии • Закон Авогадро В равных объемах различных газов при одинаковых условиях (температура и давление) содержится одинаковое число молекул. • Следствия из закона Авогадро 1. При одинаковых условиях равные количества различных газов занимают равные объемы. 2. При н. у. (Т = 273, 15 К, Р = 1, 01 ∙ 105 Па или t 2/17/2018 19
 Домашнее задание 1. Какое количество вещества ( моль) содержит 12, 04∙ 10²³ атомов натрия? 2. Какова масса 2 моль азота? 3. Какой объем занимают 1, 5 моль кислорода? 4. Какова масса 3 литров гелия?
Домашнее задание 1. Какое количество вещества ( моль) содержит 12, 04∙ 10²³ атомов натрия? 2. Какова масса 2 моль азота? 3. Какой объем занимают 1, 5 моль кислорода? 4. Какова масса 3 литров гелия?
 Домашнее задание Чем прославились в химии? • • • М. В. Ломоносов Дж. Дальтон ЖЛ. Пруст А. Л. Лавуазье С. Канниццаро И. Рихтер
Домашнее задание Чем прославились в химии? • • • М. В. Ломоносов Дж. Дальтон ЖЛ. Пруст А. Л. Лавуазье С. Канниццаро И. Рихтер


