Антибиотики 3.pptx
- Количество слайдов: 72

1 ЦЕФАЛОСПОРИНОВЫЕ АНТИБИОТИКИ 1

Ø Используются в клинической практике с начала 60 -х годов XX века. Ø Синтезировано более 50 ЛС этой группы. Ø Занимают ведущее место при лечении различных инфекций в стационаре. Ø В схемах начальной эмпирической терапии инфекций различной локализации в большинстве случаев отдается предпочтение ЛС цефалоспоринового ряда. 2

ü Широкий спектр антимикробной активности, ü Хорошие фармакокинетические характеристики, ü Низкая токсичность, ü Хорошая переносимость (в том числе применении в максимальных дозах), ü Хорошо сочетаются с другими антибиотиками, ü Удобны в применении и дозировании (для большинства ЛС возможно в/м или в/в болюсное введение с интервалом 8 -12 час). 3

Резистентность Применение цефалоспоринов ограничивает развитие резистентности микроорганизмов в результате продукции ими бета-лактамаз, особенно в последние годы, когда неоправданно, а часто и бесконтрольно используются цефалоспорины. 4

История открытия Ø Цефалоспорины были впервые выделены из культур Cephalosporium acremonium в 1948 году итальянским ученым Джузеппе Бротзу, который заметил, что культуры продуцировали вещества, эффективно уничтожавшие Salmonella typhi, которая имела активный фермент бета-лактамазу. Ø Исследователи из университета Оксфорда, выделили цефалоспорин C. Ø Первый антибиотик из группы цефалоспоринов - цефалотин был получен Эли Лилли в 1964 году. 5

ХИМИЧЕСКОЕ СТРОЕНИЕ ü Бициклические соединения, состоящие из беталактамного и дигидротиазинового колец. ü Оба кольца и составляют 7 аминоцефалоспорановую кислоту (7 -АЦК) общее ядро молекулы цефалоспоринов. ü Модификация химической структуры 7 -АЦК сопровождается существенными изменениями свойств (антибактериальной активности, параметров фармакокинетики и пр. ) соответствующего соединения. 6
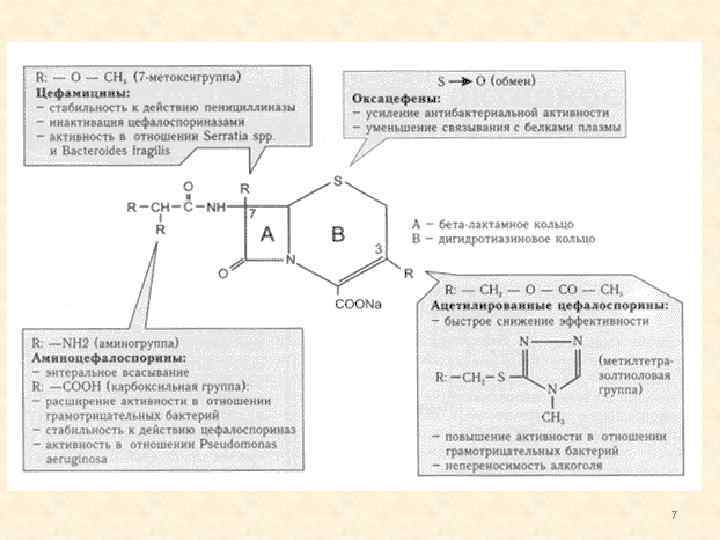
7

Механизм действия 8

Торможение синтеза пептидогликана - структурной основы микробной стенки. Пептидогликаны представляют собой длинные полисахаридные цепи со своеобразной сетчатой пространственной конформацией, в которых чередуются остатки N-ацетилглюкозамина (NAG) и Nацетилмураминовой кислоты (NAM). NAG- и NAM-пентапептидные остатки пептидогликанов синтезируются в цитоплазме микробной клетки и транспортируются через цитоплазматическую мембрану. Далее эти остатки встраиваются в существующую пептидогликанную сеть (в процессе роста и деления клетки) с участием различных энзимов транспептидаз, карбоксипептидаз, эндопептидаз. 9

В результате образования «длительной» ковалентной связи бета-лактамного антибиотика и ПСБ последние инактивируются. При этом эффект назначаемого бета-лактамного антибиотика зависит от того, какие ПСБ инактивируются и какую роль они играют в синтезе пептидогликана и выживании микробной клетки. Бактерицидный эффект цефалоспоринов реализуется только в процессе роста и размножения микроорганизмов, тогда как "покоящиеся" клетки неуязвимы для действия антибиотиков. 10

Механизмы формирования резистентности к цефалоспоринам 11
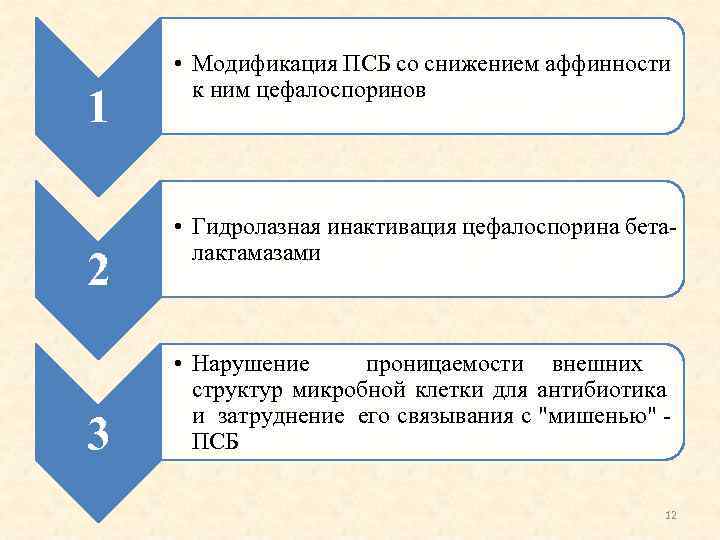
1 2 3 • Модификация ПСБ со снижением аффинности к ним цефалоспоринов • Гидролазная инактивация цефалоспорина беталактамазами • Нарушение проницаемости внешних структур микробной клетки для антибиотика и затруднение его связывания с "мишенью" ПСБ 12

Грам (+) и Грам (-) У Гр(+) микроорганизмов ЦПМ относительно порозна и непосредственно прилежит к пептидогликанному матриксу, в связи с чем цефалоспорины достаточно легко достигают ПСБ. В противоположность этому, наружная мембрана Гр(-) микроорганизмов имеет существенно более сложную "конструкцию": состоит из липидов, полисахаридов и белков, что является препятствием для проникновения цефалоспоринов в периплазматическое пространство микробной клетки. Цефалоспорины "проходят" сквозь наружную мембрану микробной клетки через так называемые пориновые каналы. В связи с этим, уменьшение проницаемости пориновых каналов может привести к формированию антибиотикорезистентности.
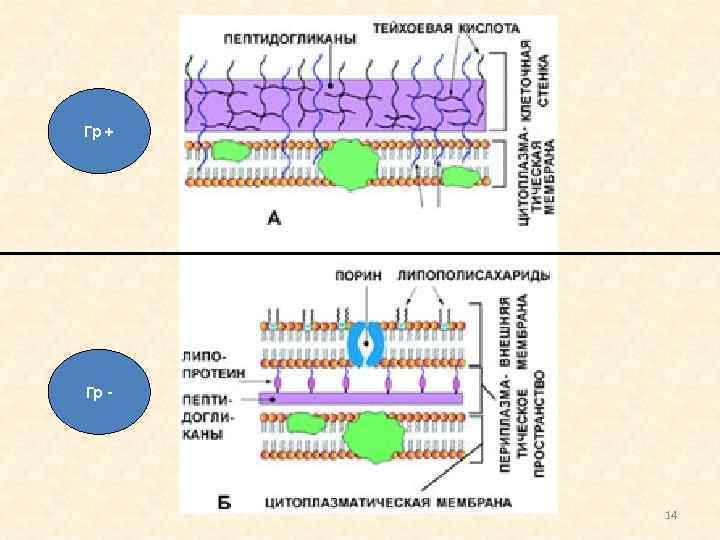
Гр + Гр - 14

Модификация ПСБ Снижение сродства ПСБ - ведущий механизм формирования резистентности Neisseria gonorrhea и Streptococcus pneumoniae к пенициллину. MRSA продуцируют ПСБ 2 (РВР 2 а), которые характеризуются значительным снижением аффинности к пенициллиназарезистентным пенициллинам и цефалоспоринам. Способность этих "новых" ПСБ 2 а к замещению эссенциальных ПСБ (с более высоким сродством к бета-лактамам), приводит к формированию устойчивости MRSA ко всем цефалоспоринам. 15

Продукция бета-лактамаз Наиболее клинически значимый механизм развития устойчивости грамотрицательных бактерий к цефалоспоринам. Бета-лактамазы кодируются хромосомами или плазмидами (плазмиды фрагменты внехромосомной ДНК, которые размножаются внутри бактерий). Бета-лактамазы широко распространены среди грамотрицательных микроорганизмов, а также продуцируются рядом грамположительных бактерий (стафилококки). Связывание бета-лактамазы с бета-лактамным антибиотиком катализирует гидролиз "критической" аминной связи лактамного кольца, что и приводит к инактивации антибиотика. 16

Бета-лактамазы ГР(+) бактерий Грамположительные микроорганизмы высвобождают бета-лактамазы непосредственно в окружающее их внеклеточное пространство. При этом большинство цефалоспоринов (за исключением цефалоридина достаточно устойчиво к гидролизующему действию стафилококковой бета-лактамазы. В связи с этим антистафилококковая активность цефалоспоринов зависит главным образом от их сродства к эссенциальным стафилококковым ПСБ. 17

Бета-лактамазы ГР(-) бактерий Бета-лактамазная резистентность грамотрицательных бактерий к цефалоспоринам носит более сложный характер. У этих микроорганизмов бета-лактамазы "заключены" в периплазматическом пространстве. Повышение продукции беталактамаз или новообразование энзимов с повышенным сродством к антибиотику является основной причиной распространения цефалоспорин-резистентных штаммов среди грамотрицательных микроорганизмов. 18

Характеристика цефалоспоринов по генерациям

Наиболее удачной является классификация цефалоспоринов, в которой учтен спектр антимикробной активности препаратов. При этом в каждом поколении цефалоспоринов выделяют препаратпрототип, свойства которого используют при создании новых соединений: 1 -е 2 -е 3 -е 4 -е поколение Цефазолин Цефуроксим Цефотаксим Цефепим

q В ряду от I к III поколению для цефалоспоринов характерна тенденция к расширению спектра действия и повышению уровня антимикробной активности в отношении грамотрицательных бактерий при некотором понижении активности в отношении грамположительных микроорганизмов. q Общим для всех цефалоспоринов является отсутствие значимой активности в отношении энтерококков, MRSA и Listeria monocytogenes. 21

ЦЕФАЛОСПОРИНЫ I ГЕНЕРАЦИИ 22

I ГЕНЕРАЦИЯ Парентеральные Цефазолин Цефалотин Ц ефапирин Цефалоридин Цефрадин Пероральные Цефалексин Цефадроксил Цефрадин 23

I ГЕНЕРАЦИЯ спектр активности ü Имеют узкий спектр антимикробной активности. ü Наибольшее клиническое значение имеет их действие на грамположительные кокки, за исключением MRSA и энтерококков. 24

I ГЕНЕРАЦИЯ спектр активности Грамположительные Грамотрицательные Стафилококки Стрептококки Пневмококки Е. Coli Klebs. Pneum. Salmonella sрр. Shigella sрр. Р. mirabilis Легко подвергаются гидролизу бета-лактамазами 25

I ГЕНЕРАЦИЯ ü Преимущественно грамположительные бактерии; ü Некоторые грамотрицательные энтеробактерии (Е. coli, Р. mirabilis) природно чувствительны к цефалоспоринам I поколения, но приобретенная устойчивость к ним высокая; ü Спектр пероральных и парентеральных цефалоспоринов одинаковый, хотя активность немного выше у парентеральных ЛС, среди которых наиболее активен цефазолин. 26

I ГЕНЕРАЦИЯ спектр активности НЕ ДЕЙСТВУЮТ Pseudomonas Enterobacter Serratia marcescens Bacteroides Индолположительный протей 27

ЦЕФАЛОСПОРИНЫ II ГЕНЕРАЦИИ 28

II ГЕНЕРАЦИЯ Парентеральные Цефуроксим Цефамандол Цефокситин Цефоницид Цефпрозил Цефметазол Цефотетан Цефоранид Пероральные Цефаклор Цефуроксимаксетил Лоракарбеф Цефпрозил 29

II ГЕНЕРАЦИЯ ЦЕФАМИЦИНЫ • Цефокситин, Цефотетан 30

II ГЕНЕРАЦИЯ спектр активности Грамположительные Грамотрицательные Стафилококки Стрептококки Пневмококки Менее активны по сравнению с I поколением Е. Coli Klebs. Pneum. Salmonella sрр. Shigella sрр. Р. Mirabilis Н. influenzae Более устойчивы к действию бета-лактамаз Enterobacter Serratia marcescens Bacteroides Индолположительный протей

II ГЕНЕРАЦИЯ спектр активности Цефамицины (цефокситин, цефотетан), активны в отношении анаэробных микроорганизмов, но по сравнению с цефуроксимом менее активны против аэробных бактерий.

II ГЕНЕРАЦИЯ спектр активности НЕ ДЕЙСТВУЮТ Pseudomonas Acinetobacter sрр. Природная устойчивость 33

ЦЕФАЛОСПОРИНЫ III ГЕНЕРАЦИИ 34

III ГЕНЕРАЦИЯ Парентеральные Цефотаксим Цефтриаксон Цефтризоксим Цефоперазон Цефтазидим Цефтизоксим Моксалактам Пероральные Цефиксим Цефподоксим проксетил Цефтибутен Цефетамет пивоксил 35

III ГЕНЕРАЦИЯ спектр активности Грамположительные Грамотрицательные Стафилококки Стрептококки Пневмококки Менее активны по сравнению с II поколением Е. Coli Klebs. Pneum. Salmonella sрр. Shigella sрр. Р. Mirabilis Н. influenzae Enterobacter Serratia marcescens Bacteroides Индолположительный протей

III ГЕНЕРАЦИЯ спектр активности АНТИПСЕВДОМОНАДНЫЕ ü Цефтазидим ü Цефоперазон Проникают через ГЭБ, кроме: ü Цефоперазон ü Цефиксим

В конце 80 -х годов были созданы цефалоспорины IV поколения, которые поколения сочетали в себе высокую активность цефалоспоринов I-II поколений в отношении стафилококков и цефалоспоринов III поколения в отношении грамотрицательных микроорганизмов. 38

ЦЕФАЛОСПОРИНЫ IV ГЕНЕРАЦИИ 39

IV ГЕНЕРАЦИЯ Парентеральные Цефепим Цефпиром 40

IV ГЕНЕРАЦИЯ спектр активности НЕ ДЕЙСТВУЮТ Bacteroides Природная устойчивость 41

IV ГЕНЕРАЦИЯ спектр активности На сегодняшний день ЛС IV поколения имеют наиболее широкий спектр антимикробной активности среди цефалоспориновых антибиотиков. Цефалоспорины IV поколения в некоторых случаях проявляют активность в отношении тех штаммов Enterobacteriaceae, которые устойчивы к ЛС III поколения. 42

ü У цефалоспоринов от I к IV поколению увеличивается активность в отношении Гр(-) бактерий и пневмококков, и немного снижается активность в отношении стафилококков от I к III поколению. ü Цефалоспорины с выраженной антианаэробной активностью (цефамицины): цефокситин, цефамицины цефотетан, цефметазол. ü Цефалоспорины с активностью в отношении Р. aeruginosa и других неферментирующих микроорганизмов: цефтазидим, цефоперазон, цефепим, цефоперазон/сульбактам. 43

Слабая активность / Не действуют ü Все цефалоспорины практически лишены активности против энтерококков, малоактивны против грамположительных анаэробов и слабоактивны против грамотрицательных анаэробов. 44
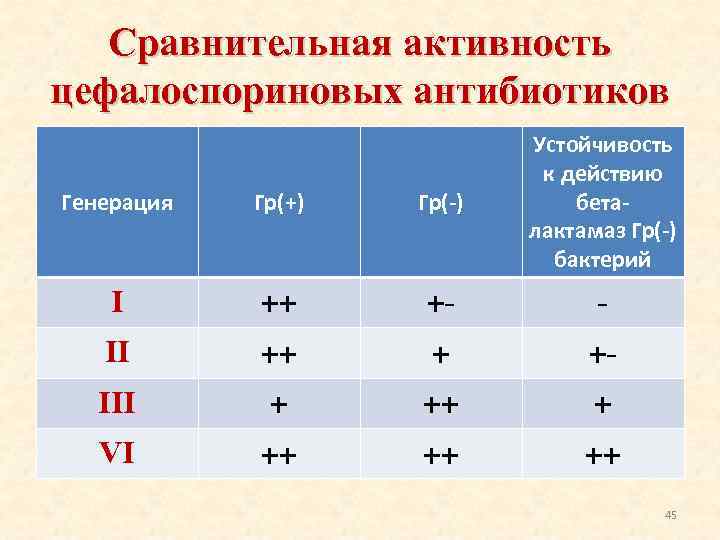
Сравнительная активность цефалоспориновых антибиотиков Генерация Гр(+) Гр(-) Устойчивость к действию беталактамаз Гр(-) бактерий I ++ ++ ++ II III VI 45

ü Цефалоспорины хорошо переносятся. ü Наиболее частые нежелательные явления при их применении: аллергические реакции (23%), хотя они возникают существенно реже по сравнению с пенициллинами. ü Примерно у 10% больных с гиперчувствительностью к пенициллину возникают перекрестные реакции на цефалоспорины. 46

ü Местная болезненность при в/м введении цефалоспоринов. Флебиты при в/в введении наблюдаются редко (менее 1%). ü Реакции ЖКТ встречаются нечасто (около 2%), обычно применении оральных ЛС. ü Парентеральные цефалоспорины, выделяющиеся с желчью (цефоперазон, цефтриаксон), чаще вызывают диарею. ü При применении цефалоспоринов, как и других антибиотиков, возможно развитие тяжелой антибиотик-ассоциированной диареи, вызванной С. difficile, и псевдомембранозного колита, хотя частота этого осложнения невысока (менее 1%).
ü При применении цефалоспоринов I поколения (цефалоридин) описаны нефротоксические эффекты, особенно при сочетании с аминогликозидами. ü Современные цефалоспорины лишены нефротоксических свойств. 48

ü Цефалоспорины, имеющие в структуре метилтиотетразольную группу в позиции 3 (цефамандол, цефметазол, цефоперазон, цефотетан), вызывают дисульфирамподобные реакции приеме алкоголя, а также геморрагический синдром в результате нарушения синтеза протромбина и всасывания витамина К в кишечнике. 49

ü Клиническое значение геморрагического синдрома, появившегося в результате применения цефалоспоринов, невелико (реже 1%), но риск возрастает у пожилых людей и больных с почечной или печеночной недостаточностью, поэтому рекомендуется контролировать протромбиновое время. 50

Цефалоспориновые антибиотики не обладают тератогенными или эмбриотоксическими свойствами и при необходимости могут применяться при лечении беременных.

2 КАРБАПЕНЕМЫ 52

Общая характеристика ü Наиболее широкий спектр антимикробной активности среди всех бета-лактамных антибиотиков. ü Оптимальны для эмпирической монотерапии тяжелых госпитальных инфекций, в том числе вызванных микроорганизмами, резистентными к цефалоспоринам и фторхинолонам. ü До настоящего времени в клинической практике применялись имипенем и меропенем, а с 2003 г. стал также доступен и эртапенем. 53

Карбапенемы ИМИПЕНЕМ МЕРОПЕНЕМ ЭРТАПЕНЕМ

Имипенем - первый карбапенемовый антибиотик, применяется с 1985 г. Он разрушается в организме почечным ферментом дегидропептидазой-1, поэтому применяется в лекарственной форме с ингибитором дегидропептидазы циластатином в соотношении 1: 1. Меропенем устойчив к почечной дегидропептидазе, поэтому применяется без ингибитора. 55
АНТИМИКРОБНАЯ АКТИВНОСТЬ ü Широкий спектр антимикробной активности; ü Включая аэробные грамположительные и грамотрицательных микроорганизмы, а также анаэробов. Широкий спектр: Грамположительные Грамотрицательные Анаэробы

МЕРОПЕНЕМ ü Активнее имипенема и эртапенема в отношении Гр(-) бактерий, в том числе штаммов, резистентных к цефалоспоринам III поколения, полусинтетическим пенициллинам и гентамицину. ü Наибольшее значение имеет более высокая активность меропенема в отношении Р. Aeruginosa. В отношении Р. aeruginosa меропенем in vitro проявляет наиболее высокую активность среди всех антибиотиков с антипсевдомонадной активностью. 57

ЭРТАПЕНЕМ ü Эртапенем не обладает активностью против Р. aeruginosa и других неферментирующих микроорганизмов (Acinetobacter sрр. , В. серасiа). ü Имипенем и эртапенем проявляют более высокую активность в отношении стафилококков, стрептококков и Е. faecalis по сравнению с меропенемом. 58

Имипенем, эртапенем и меропенем проявляют высокую активность в отношении штаммов пневмококков, резистентных к пенициллину. Оксациллинрезистентные штаммы стафилококков устойчивы к карбапенемам, как и к другим бета-лактамным антибиотикам. Карбапенемы, в отличие от цефалоспоринов, проявляют высокую активность в отношении L. monocytogenes — микроорганизма, имеющего значение в этиологии менингита у новорожденных. 59

Анаэробная активность ü Карбапенемы проявляют высокую активность в отношении анаэробов. ü Чувствительность анаэробов к карбапенемам выше, чем к другим антибиотикам с антианаэробным действием - цефокситину, линкомицину, а к карбапенемам и метронидазолу примерно одинакова, за исключением Peptostreptococcus sрр. (более активны карбапенемы). ü В отношении анаэробов имипенем, меропенем и эртапенем проявляют сходную активность. 60

РЕЗИСТЕНТНОСТЬ ü Приобретенная устойчивость к карбапенемам возникает редко. ü Результаты длительного мониторирования показали, что резистентность бактерий к имипенему и меропенему существенно не возрастала в течение нескольких лет применения этих препаратов. ü В исследованиях, проведенных в России, было показано, что грамотрицательные бактерии, выделенные в отделениях интенсивной терапии наиболее чувствительны к карбапенемам среди всех антибактериальных препаратов. 61

РЕЗИСТЕНТНОСТЬ ü Механизмы приобретенной резистентности у некоторых грамотрицательных микроорганизмов (Enterobacter, Citrobacter, Serratia, Klebsiella) включают продукцию плазмидных беталактамаз широкого и расширенного спектра. ü Они ограничивают активность не только пенициллинов, но и цефалоспоринов III поколения и частично цефалоспоринов IV поколения. Единственными бета-лактамными антибиотиками, стабильно сохраняющими активность в отношении этих возбудителей, являются карбапенемы. 62

Проблема металлобеталактамаз В отделениях интенсивной терапии на фоне применения карбапенемов в результате элиминации чувствительных микроорганизмов возможна селекция видов, продуцирующих беталактамазы класса В (металлоэнзимы) и, как следствие, проявляющих природную устойчивость к этим антибиотикам. К таким микроорганизмам относятся Stenotrophomonas maltophilia и некоторые виды Flavobacterium. 63

3 МОНОБАКТАМЫ 64

Общая характеристика ü Азтреонам. ü Проявляет активность только в отношении грамотрицательных бактерий. ü Имеет ограниченное применение. МНН АЗТРЕОНАМ Торговые Азактам

Химическое строение ü Моноциклический бета-лактамный антибиотик. ü Имеет одно (бета-лактамное) кольцо, структурно отличается от других беталактамов. ü Ядром молекулы является альфа-метил-3 амино-моно-бактамная кислота. ü Выделен из культуры Chromobacterium violaceum. 66

АЗТРЕОНАМ ü Подавляет синтез клеточной стенки. ü Действует бактерицидно. ü Устойчив к бета-лактамазам Гр(-) бактерий. Активен в отношении: Гр(-) аэробов (Salmonella spp. , Shigella spp. , Proteus spp. , Escherichia coli, Klebsiella spp. , Neisseria gonorrhoeae, Neisseria meningitidis, Haemophilus influenzae, Pseudomonas aeruginosa, Entero-Citrobacter spp. ). 67

АЗТРЕОНАМ Не действует на грамположительные микроорганизмы и анаэробы. Возможно использование при аллергии к пенициллинам, цефалоспоринам и карбапенемам. Между азтреонамом и аминогликозидами существует перекрестная резистентность. Редко вызывает дисбактериоз. 68

АЗТРЕОНАМ ПОКАЗАНИЯ Сепсис, эндокардит, менингит, перитонит, инфекции нижних дыхательных путей (пневмония, абсцесс легких, эмпиема плевры, бронхит), инфекции органов ЖКТ, инфекции желчевыводящих путей (холангит, холецистит, энтероколит), инфекции почек и мочевыводящих путей, урогенитальной сферы (гонорея, пиелонефрит, уретрит, цистит, эндометрит), инфекции костей, кожи и мягких тканей, локализованные паренхиматозные абсцессы, инфицированные ожоги и раны, инфекции или угроза инфекций у больных со сниженным иммунитетом, послеоперационные инфекции (в т. ч. профилактика). 69

АЗТРЕОНАМ ПОБОЧНЫЕ ЭФФЕКТЫ КОЖНЫЕ Аллергические реакции: кожная сыпь, зуд кожи, мультиформная экссудативная эритема, петехии, крапивница. 70

АЗТРЕОНАМ ПОБОЧНЫЕ ЭФФЕКТЫ ЛАБОРАТОРНЫЕ Эозинофилия, тромбоцитопения, увеличение протромбинового времени, анемия, нейтропения, повышение активности трансаминаз (АЛТ и АСТ) и ЩФ. 71

АЗТРЕОНАМ ПОБОЧНЫЕ ЭФФЕКТЫ ЖКТ Диарея, тошнота, рвота, стоматит, изменение вкуса, кандидамикоз. НЕРВНАЯ СИСТЕМА Судороги, диплопия, бессонница, головокружение, головные боли, спутанность сознания. 72
Антибиотики 3.pptx