Лекция 2,3. Белки, витамины, ферменты, гормоны.ppt
- Количество слайдов: 59

1. 3. Строение, свойства, биологическая роль белков 1

Белки • высокомолекулярные азотосодержащие вещества, состоящие из АМК, связанных между собой пептидными связями.

Функциональная классификация белков • • Каталитически активные белки – ферменты. Гормоны. Рецепторы. Транспортные белки. Структурные белки. Белки-ингибиторы ферментов. Сократительные белки. Защитные белки – антитела.

Строение, свойства, биологическая роль белков Общая формула аминокислот R—CH—COOН NH 2 Статическая биохимия 4

Строение, свойства, биологическая роль белков Аминокислоты по кислотно-основным свойствам подразделяются на 4 основные класса: • неполярные, или гидрофобные (аланин, валин, лейцин, изолейцин, пролин, фенилаланин, триптофан, метионин); • полярные, но незаряженные (глицин, серин, треонин, цистеин, тирозин, аспарагин, глутамин); • положительно заряженные (лизин, гистидин, аргинин); • отрицательно заряженные (аспарагиновая кислота, глутаминовая кислота). Статическая биохимия 5

Строение, свойства, биологическая роль белков По биологическому значению АМК делятся на: • Заменимые (глицин, аланин, серин, цистеин, тирозин, аспарагиновая кислота, глутаминовая кислота, аспарагин, глутамин, пролин). • Полузаменимые (аргинин, гистидин). • Незаменимые (валин, лейцин, изолейцин, треонин, лизин, метионин, фенилаланин, триптофан). Статическая биохимия
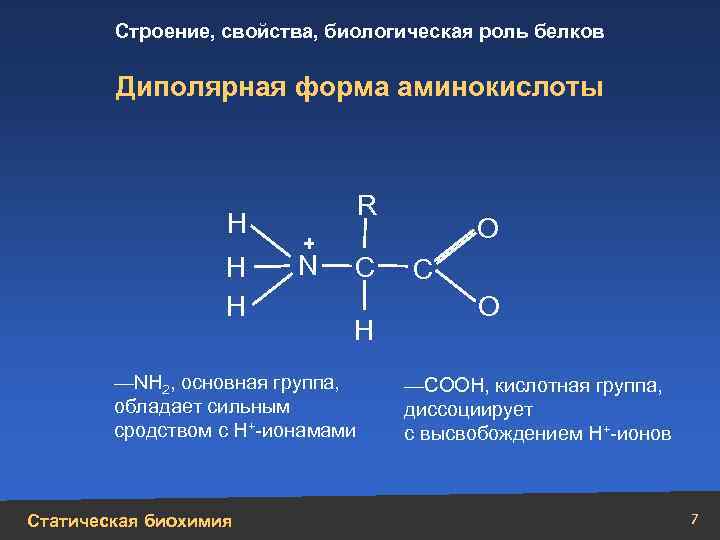
Строение, свойства, биологическая роль белков Диполярная форма аминокислоты Н Н Н R + N С Н О С О —NH 2, основная группа, —СООН, кислотная группа, обладает сильным диссоциирует +-ионамами сродством с Н с высвобождением Н+-ионов Статическая биохимия 7
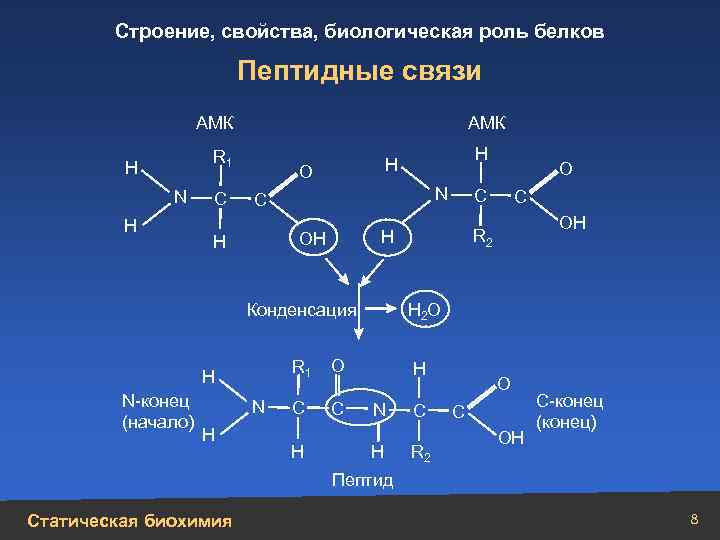
Строение, свойства, биологическая роль белков Пептидные связи АМК R 1 Н N Н С О N С ОН Н R 1 Н N Н С ОН R 2 Н 2 О О С Н Конденсация N-конец (начало) Н Н Н N Н С R 2 О С ОН С-конец (конец) Пептид Статическая биохимия 8
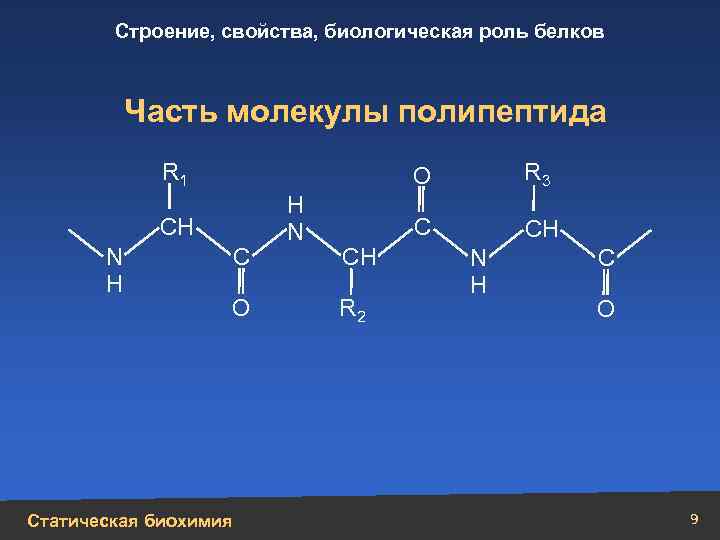
Строение, свойства, биологическая роль белков Часть молекулы полипептида R 1 О СН N Н С О Статическая биохимия Н N С СН R 2 R 3 СН N Н С О 9

Строение, свойства, биологическая роль белков Последовательность аминокислот для каждого белка уникальна и закреплена генетически Первичная структура характеризует последовательность аминокислотных остатков в полипептидной цепи, связанных ковалентными связями (миоглобин – 153 АМК остатка, инсулин – 21 АМК остаток). H O N — конец NH 2 — C — N — CH — COOH C — конец O СH 3 H (CH 2)4 NH 2 Трипептид: глициналанинлизин Статическая биохимия 10

Строение, свойства, биологическая роль белков Вторичная структура белка – это способ укладки белка в упорядоченную структуру α-спираль Стержневая форма Статическая биохимия β-складчатая структура Линейная форма 11

Строение, свойства, биологическая роль белков Третичная структура белка Доменное строение глобулярных белков (по А. А. Болдыреву) Нативная – активная структура Статическая биохимия 12

Строение, свойства, биологическая роль белков Четвертичная структура белка – структура, состоящая из определенного числа полипептидных цепей, занимающих строго фиксированное положение относительно друга. а а – гемоглобин, состоящий из четырех субъединиц (двух α-цепей и двух β-цепей), б – одна субъединица, в – простетическая группа гемоглобина б в Статическая биохимия 13

Строение, свойства, биологическая роль белков Сложные белки (металлопротеины) Цитохром с Статическая биохимия Ферритин 14

Строение, свойства, биологическая роль белков Сложные белки (нуклеопротеины) Модель вируса мозаичной болезни табака: а – спираль РНК; б – субъединицы белка Статическая биохимия 15

1. 4. Витамины, ферменты 16

Витамины, ферменты Водорастворимые витамины Витамин В 1 (тиамин) Статическая биохимия 17

Витамины, ферменты Витамин В 1 (тиамин) • Витамин устойчив в кислой среде. В щелочной среде быстро разрушается. • В отсутствие тиамина невозможен нормальный углеводный обмен и другие виды обмена. • В отсутствие витамина увеличивается количество пирувата и лактата в крови. Особенно резко нарушается углеводный обмен в мозге. • Отсутствие в пище человека тиамина приводит к заболеванию бери - бери. • Распространен в продуктах растительного происхождения (неочищенный рис, мука грубого помола, горохе и др. ). В организме животных больше всего – в печени, почках, сердечной мышце и мозге. • Потребность - 2 -3 мг Статическая биохимия

Витамины, ферменты Водорастворимые витамины СН 2 ОН (НОСН)3 СН 2 Н 3 С N N N О NН N N О Витамин В 2 (рибофлавин) Статическая биохимия 19

Витамины, ферменты Витамин В 2 (рибофлавин) • Принимает участие в окислительно - восстановительных реакциях – входит в состав простетических групп флавинзависимых дегидрогеназ (ФАД). Принимает участие в образовании гемоглобина. • Недостаток рибофлавина приводит к падению интенсивности тканевого дыхания и обмена веществ в целом. • При отсутствии рибофлавина наблюдается остановка роста, выпадение волос и заболевание глаз. Наблюдается воспалительное поражение слизистой ротовой полости и губ. В его отсутствие может возникать анемия. • В дрожжах, печени, почках, сердечной мышце, рыбе. • Ежедневная потребность человека в витамине – 2 -4 мг. Статическая биохимия

Витамины, ферменты Витамин РР (В 5). Никотинамид О N С О ОН N Никотиновая кислота Статическая биохимия N С NН 2 N Никотинамид 21

Витамины, ферменты Витамин РР (В 5). Никотинамид • Участвует в обмене веществ. • Отсутствие никотинамида в пище приводит к нарушению синтеза ферментов, катализирующих окислительно-восстановительные реакции. • При недостатке возникает заболевание пеллагра (дерматит, расстройство нервной системы, потеря памяти, галлюцинация и бред). • В рисовых отрубях, дрожжах, пшеничных отрубях, в печени. • Суточная потребность – 15 -25 мг для взрослых. Статическая биохимия

Витамины, ферменты Водорастворимые витамины СН 2 ОН НОН 2 С ОН N СН 3 Витамин В 6 (пиридоксин) Статическая биохимия 23

Витамины, ферменты Витамин В 6 (пиридоксин) • Играет важную роль в обмене аминокислот. Кофермент декарбоксилаз некоторых аминокислот. • При недостатке витамина В 6 развивается дерматит. • Распространен в продуктах животного и растительного происхождения. Особенно богаты им рисовые отруби, зародыши пшеницы, бобы, дрожжи, почки, печень, мышцы, синтезируется микрофлорой кишечника. • Потребность человека – 2 мг в день. Статическая биохимия

Витамины, ферменты Витамин В 12 (антианемический витамин, кобаламин) Статическая биохимия 25

Витамины, ферменты Витамин В 12 (кобаламин) • Оказывает антианемическое действие при злокачественном малокровии. Входит в состав кобамидных ферментов в качестве кофермента. Участвует в синтезе дезоксирибозы. • Синтезируется микробами, населяющими кишечник человека. Печень рогатого скота и цыплят обладает наибольшей концентрацией витамина. • Потребность человека – 2 – 3 мг в день. Статическая биохимия

Витамины, ферменты Витамин C (аскорбиновая кислота) Статическая биохимия 27

Витамины, ферменты C (аскорбиновая кислота) • Физиологическое значение связано с его окислительно-восстановительными свойствами. Большое значение имеет витамин для образования коллагенов и функции соединительной ткани. • При недостатке наблюдается нарушение превращения тирозина. Развивается цинга, поражение стенки кровеносных сосудов. Возникают точечные кровоизлияния. • Для человека основным источником витамины С являются растительные продукты. • Потребность человека в витамине С – 50– 100 мг. Статическая биохимия

Витамины, ферменты Пантотеновая кислота (В 3) • Имеет в своем составе аланин; входит в состав кофермента (Ко. А). • Нарушения при недостатке – дерматиты, кератиты, поражение надпочечников, депигментация волос, прекращение роста, потеря аппетита, истощение, язвы желудка и кишечника, повреждение сердца и почек, дегенеративные изменения нервной системы, параличи и невриты, подкожные кровоизлияния, понижение образования антител. • Богатый источник – дрожжи, печень, яичный желток, зеленые части растений. • Суточная потребность человека – 10 мг. Статическая биохимия

Витамины, ферменты Водорастворимые витамины О НN NН НС СН Н 2 С S С Н 2 Н 2 C С Н 2 C О ОН Витамин Н (биотин) Статическая биохимия 30

Витамины, ферменты Витамин Н (биотин) • Биотин необходим для синтеза пуринов. Участвует в реакции превращения ацетил-Ко. А. • Большим содержанием биотина отличаются печень и яичный желток. • Суточная потребность в биотине – 10 мг. Статическая биохимия

Витамины, ферменты Водорастворимые витамины ОН N N Н 2 N СН 2 NН СО NН СН СН 2 СООН N N Фолиевая кислота Статическая биохимия 32

Витамины, ферменты Фолиевая кислота • Входит в состав коферментов, участвующих в синтезе холина, урацила, тимина, пуринов, преобразовании глицина, синтезе серина. • Недостаточной фолиевой кислоты у человека может при нарушении микрофлоры кишечника в результате принятия антибиотиков. • Наиболее характерный признак авитаминоза – нарушение кроветворения, что приводит к анемиям. • Содержится в животных белках. Статическая биохимия

Витамины, ферменты Жирорастворимые витамины Н 3 С СН 3 СН 2 ОН СН 3 Витамин А (ретинол) Статическая биохимия 34

Витамины, ферменты Жирорастворимые витамины СН 3 НС СН 3 СН СН СН 2 С СН 3 НО Витамин D (кальциферол) Статическая биохимия 35

Витамины, ферменты Жирорастворимые витамины НО СН 3 ( СН 2 Н 3 С СН 3 О СН 2 СН )3 СН 3 Витамин Е (токоферол) Статическая биохимия 36

Витамины, ферменты Жирорастворимые витамины • Витамин К – антигеморрагический витамин. • Геморрагия – подкожные и внутримышечные кровоизлияния. Статическая биохимия

Витамины, ферменты Ферменты Наиболее крупный специализированный класс белковых молекул, катализирующих химические реакции, из которых слагается клеточный обмен. • Статическая биохимия 38

Витамины, ферменты Химическая кинетика В соответствии с законом действующих масс для реакции А + В С + Д скорость может выражаться уравнением v = К [A]·[B], где v – скорость реакции; К – константа скорости, отражающая влияние химической природы вещества и условий, в которых протекает реакция, на ее скорость; [A] и [B] – концентрация реагентов. Статическая биохимия 39

Витамины, ферменты Кинетика ферментативных реакций Вещества, реакцию превращения которых ускоряют ферменты (E), называются субстратами (S). В ходе ферментативной реакции образуется ферментсубстратный комплекс (ES). Фермент-субстратный комплекс становится нестабильным и затем преобразуется в комплекс «фермент – продукт» , который распадается на фермент и продукты реакции (P): S + E ES E + P. Статическая биохимия 40

Витамины, ферменты Кинетика ферментативных реакций Действие ферментов как катализаторов обладает некоторыми особенностями: • фермент не способен вызвать новую химическую реакцию, он ускоряет уже идущую; • фермент не изменяет направление реакции, определяемое концентрациями реагентов, катализирует как прямую, так и обратную реакции. Статическая биохимия 41

Витамины, ферменты Классификация активности ферментов 1. Оксидоредуктазы (окислительно-восстановительные реакции) Оксидоредуктазы осуществляют перенос атомов Н и О или электронов от одного вещества к другому. Дегидрогеназы катализируют окислительновосстановительные реакции, происходящие путем отнятия электронов и протонов от одного субстрата и переноса их на другой: АН + В А + ВН. Оксидазы катализируют перенос водорода с субстрата на кислород: АН 2 +1/2 О 2 А + Н 2 О Гидроксилазы и оксигеназы ускоряют некоторые реакции биологического окисления, протекающие с присоединением гидроксила или кислорода к окисляемому веществу. Статическая биохимия 42

Витамины, ферменты Классификация активности ферментов 2. Трансферазы (перенос функциональных групп) Ускоряют перенос определенной группы атомов от одного вещества к другому: АВ + С А + ВС Метилтрансферазы переносят метильную группу, Ацилтрансферазы – кислотный остаток (ацил), Гликозилтрансферазы – моносахаридный остаток (гликозил), Аминотрансферазы – аминную группу, Фосфотрансферазы – остаток фосфорной кислоты (фосфорил). Статическая биохимия 43

Витамины, ферменты Классификация активности ферментов 3. Гидролазы (реакции гидролиза) Ускоряют реакции гидролиза, при которых из субстрата образуются 2 продукта. К гидролазам относятся все пищеварительные ферменты: АВ + Н 2 О АОН + ВН Эстеразы ускоряют гидролиз сложных эфиров (различных липидов) на спирты и кислоты. Фосфатазы катализируют гидролитическое отщепление фосфорной кислоты от нуклеотидов и фосфорных эфиров углеводов. Глюкозидазы ускоряют гидролиз сложных углеводов. Пептидгидролазы ускоряют гидролиз пептидных связей в белках и пептидах. Статическая биохимия 44

Витамины, ферменты Классификация активности ферментов 4. Лиазы ускоряют негидролитическое присоединение к субстрату или отщепление от него группы атомов. При этом могут разрываться связи: С–С, С–N, C–O, C–S. Статическая биохимия 45

Витамины, ферменты Классификация активности ферментов 5. Изомеразы (реакции изомеризации) Внутримолекулярные перестройки: АВ ВА Статическая биохимия 46

Витамины, ферменты Классификация активности ферментов 6. Лигазы (образование связей за счет АТФ) Лигазы катализируют реакции синтеза высокомолекулярных полимеров из мономеров за счет энергии АТФ: X + Y + АТФ XY + AДФ + Фн Статическая биохимия 47

1. 5. Гормоны: биологическая роль, классификация, механизм действия 48

Гормоны: биологическая роль, классификация, механизм действия Гормоны – это биологически активные вещества, синтезируемые эндокринными железами, выделяемые ими в кровь или лимфу и регулирующие внутриклеточный метаболизм. Статическая биохимия 49

Гормоны: биологическая роль, классификация, механизм действия Гормоны гипоталамуса являются относительно простыми по структуре олигопептидами. К ним относятся: кортиколиберин, тиролиберин, люлилиберин, фоллиберин, соматостатин, пролакстатин, пролактолиберин, меланолиберин, меланостатин. Статическая биохимия 50

Гормоны: биологическая роль, классификация, механизм действия Гормоны гипофиза Гипофиз синтезирует тропные и эффекторые гормоны Тропные гормоны: • АКТГ (адренокортикотропный гормон) – пептид, регулирующий биосинтез и секрецию гормонов коры надпочечников; • ТТГ (тиреотропный гормон) – гликопротеид, регулирующий биосинтез и секрецию гормонов щитовидной железы; • ФСГ (фолликулостимулирующий гормон), ЛГ (лютеинизирующий гормон) – гликопротеиды, регулирующие биосинтез и секрецию гормонов половых желез. Статическая биохимия 51

Гормоны: биологическая роль, классификация, механизм действия Гормоны гипофиза Гипофиз синтезирует тропные и эффекторые гормоны Эффекторные гормоны • АДГ (антидиуретический гормон, вазопрессин) – простой пептид, регулирующий водный обмен, уменьшает мочеотделение. • Окситоцин – простой пептид, вызывающий сокращение матки во время родов и активное выделение молока молочными железами. • Меланостимулирующий гормон – простой пептид, регулирующий сезонное окрашивание кожи, шерсти. • Пролактин – простой пептид, регулирующий выделение молока молочными железами при кормлении. • Гормон роста (соматотропный ) – простой пептид, регулирующий рост тела в длину, усиливает процессы анаболизма. Статическая биохимия 52

Гормоны: биологическая роль, классификация, механизм действия Гормоны поджелудочной железы инсулин (белок из 51 аминокислотного остатка) и глюкагон (одноцепочечный полипептид из 29 аминокислотных остатков) не находятся под контролем гормонов гипофиза. Секреция гормонов регулируется содержанием глюкозы в крови. Статическая биохимия 53

Гормоны: биологическая роль, классификация, механизм действия Гормоны щитовидной железы Тиреоидные гормоны Тироксин и трийодтиронин являются производными аминокислотами тирозина и содержат в своем составе 4 и 3 атома йода соответственно. Тиреоидные гормоны регулируют активность ферментных систем обмена углеводов и липоидов, синтеза белка, интенсивность транспорта субстратов и кофакторов, биоэнергетические процессы. Статическая биохимия 54

Гормоны: биологическая роль, классификация, механизм действия Гормоны коры надпочечников Секреция гормонов коры надпочечников регулируется адренокортикотропным гормоном (АКТГ) гипофиза. Гормоны надпочечников подразделяются на 3 функциональные группы – глюкокортикоиды, минералокортикоиды и половые гормоны. Статическая биохимия 55

Гормоны: биологическая роль, классификация, механизм действия Гормоны мозгового вещества надпочечников Гормоны мозгового вещества надпочечников – адреналин и норадреналин (катехоламины). Статическая биохимия 56

Гормоны: биологическая роль, классификация, механизм действия Гормоны половых желез Мужские половые гормоны (андрогены) образуются в семенниках, женские половые гормоны (эстрогены, прогестины) продуцируются в яичниках. Статическая биохимия 57

Гормоны: биологическая роль, классификация, механизм действия Гормоны паращитовидной железы Паращитовидные железы секретируют 2 гормона (паратгормон и кальцитонин), которые вместе с витамином Д обеспечивают регуляцию кальциевого обмена. Статическая биохимия 58

Гормоны: биологическая роль, классификация, механизм действия Гормоны тимуса (вилочковой железы) В тимусе продуцируется 5 гормонально-активных факторов (полипептидов по природе): тимозин, гомеостатический тимусный гормон, тимопоэтины 1 и 11, тимусный гуморальный фактор. Основная функция гормонов вилочковой железы – регуляция созревания определенных популяций лимфоидных клеток, то есть участие в регуляции функционирования иммунной системы. Статическая биохимия 59
Лекция 2,3. Белки, витамины, ферменты, гормоны.ppt