Патофизиология клетки. 1 сем. 10-11.ppt
- Количество слайдов: 66
 1 1
1 1
 Из истории развития учения о клетке В 1665 году английский физик и естествоиспытатель Роберт Гук, изучая под микроскопом срезы пробкового дерева, впервые увидел клетку и ввёл этот термин в научное обращение. В 1673 году известный голландский ученый и врач Ван де Грааф направил в Королевское научное общество в Лондон письмо своего друга, привратника из города Дельфта Антония Ван Левенгука. В этом письме Левенгук, являвшийся изобретателем микроскопа, писал Ван де Граафу о том, что рассматривая под микроскопом срезы растений, он обнаружил, что растительная ткань состоит из множества ячеек. В 1680 году Левенгук первым обнаружил живые одноклеточные организмы. Однако уровень науки того времени не позволил оценить открытие этих двух учёных, и, хотя многие последователи Левенгука (в том числе такие известные ученые, как Мальпиги, Пуркинье и др. ) также видели под микроскопом клетки, эти наблюдения оставались лишь констатирующими заметками. Революция в этой области наступила лишь в 1839 году, когда немецкий ученый Теодор Шванн опубликовал книгу «Микроскопические исследования соответствия роста и строения животных и растений» , в которой он провозгласил принцип: «Все живое состоит из клеток» . Так была сформулирована клеточная теория. Вскоре клеточная теория прочно вошла в медицину благодаря классическому труду великого немецкого ученого Рудольфа Вирхова, написавшего книгу «Целлюлярная патология» . Эта книга поставила медицину на научную основу. Вирхов показал, что все патологические процессы развиваются на определенных клеточных территориях. 2
Из истории развития учения о клетке В 1665 году английский физик и естествоиспытатель Роберт Гук, изучая под микроскопом срезы пробкового дерева, впервые увидел клетку и ввёл этот термин в научное обращение. В 1673 году известный голландский ученый и врач Ван де Грааф направил в Королевское научное общество в Лондон письмо своего друга, привратника из города Дельфта Антония Ван Левенгука. В этом письме Левенгук, являвшийся изобретателем микроскопа, писал Ван де Граафу о том, что рассматривая под микроскопом срезы растений, он обнаружил, что растительная ткань состоит из множества ячеек. В 1680 году Левенгук первым обнаружил живые одноклеточные организмы. Однако уровень науки того времени не позволил оценить открытие этих двух учёных, и, хотя многие последователи Левенгука (в том числе такие известные ученые, как Мальпиги, Пуркинье и др. ) также видели под микроскопом клетки, эти наблюдения оставались лишь констатирующими заметками. Революция в этой области наступила лишь в 1839 году, когда немецкий ученый Теодор Шванн опубликовал книгу «Микроскопические исследования соответствия роста и строения животных и растений» , в которой он провозгласил принцип: «Все живое состоит из клеток» . Так была сформулирована клеточная теория. Вскоре клеточная теория прочно вошла в медицину благодаря классическому труду великого немецкого ученого Рудольфа Вирхова, написавшего книгу «Целлюлярная патология» . Эта книга поставила медицину на научную основу. Вирхов показал, что все патологические процессы развиваются на определенных клеточных территориях. 2
 Основоположники учения о клетке Роберт Гук (1635 – 1703) В 1665 году, исследуя срез пробкового дерева, впервые увидел клетку (и ввёл этот термин). Антоний ван Левенгук (1633 – 1723) В 1673 году увидел под микроскопом растительную клетку, а в 1680 году открыл живые одноклеточные организмы. Теодор Шванн (1810 – 1882) В 1839 году сформулировал основы клеточной теории, в которой провозгласил принцип: «Всё живое – из клетки» . Рудольф Вирхов (1821 – 1902) В 1858 году опубликовал труд «Целлюлярная патология» , в котором высказал принцип: «Всякая клетка – из клетки» ( «Omnis cellula e cellula» ). 3
Основоположники учения о клетке Роберт Гук (1635 – 1703) В 1665 году, исследуя срез пробкового дерева, впервые увидел клетку (и ввёл этот термин). Антоний ван Левенгук (1633 – 1723) В 1673 году увидел под микроскопом растительную клетку, а в 1680 году открыл живые одноклеточные организмы. Теодор Шванн (1810 – 1882) В 1839 году сформулировал основы клеточной теории, в которой провозгласил принцип: «Всё живое – из клетки» . Рудольф Вирхов (1821 – 1902) В 1858 году опубликовал труд «Целлюлярная патология» , в котором высказал принцип: «Всякая клетка – из клетки» ( «Omnis cellula e cellula» ). 3
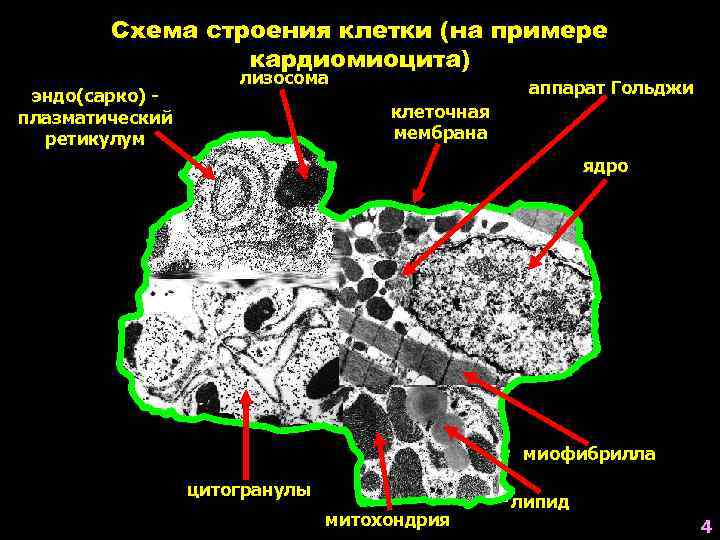 Схема строения клетки (на примере кардиомиоцита) эндо(сарко) плазматический ретикулум лизосома аппарат Гольджи клеточная мембрана ядро миофибрилла цитогранулы митохондрия липид 4
Схема строения клетки (на примере кардиомиоцита) эндо(сарко) плазматический ретикулум лизосома аппарат Гольджи клеточная мембрана ядро миофибрилла цитогранулы митохондрия липид 4
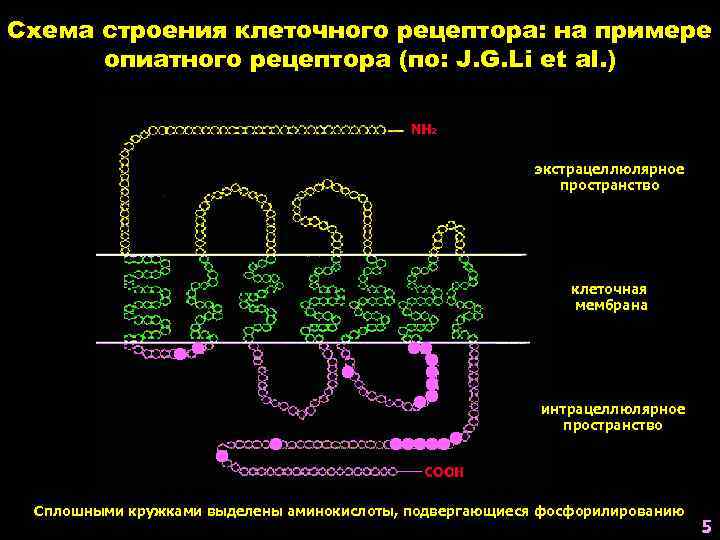 Схема строения клеточного рецептора: на примере опиатного рецептора (по: J. G. Li et al. ) экстрацеллюлярное пространство клеточная мембрана интрацеллюлярное пространство Сплошными кружками выделены аминокислоты, подвергающиеся фосфорилированию 5
Схема строения клеточного рецептора: на примере опиатного рецептора (по: J. G. Li et al. ) экстрацеллюлярное пространство клеточная мембрана интрацеллюлярное пространство Сплошными кружками выделены аминокислоты, подвергающиеся фосфорилированию 5
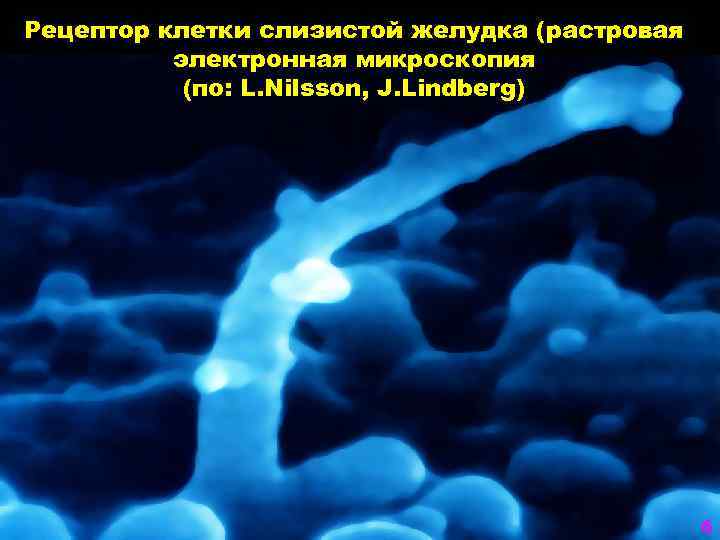 Рецептор клетки слизистой желудка (растровая электронная микроскопия (по: L. Nilsson, J. Lindberg) 6
Рецептор клетки слизистой желудка (растровая электронная микроскопия (по: L. Nilsson, J. Lindberg) 6
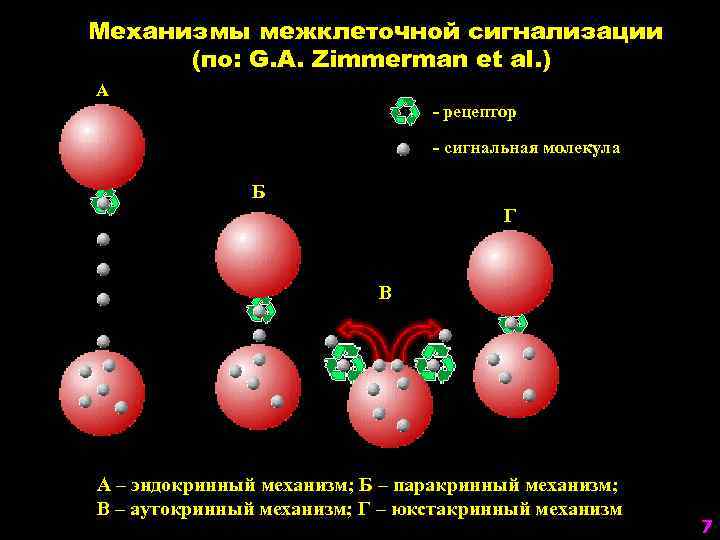 Механизмы межклеточной сигнализации (по: G. A. Zimmerman et al. ) А - рецептор - сигнальная молекула Б Г В А – эндокринный механизм; Б – паракринный механизм; В – аутокринный механизм; Г – юкстакринный механизм 7
Механизмы межклеточной сигнализации (по: G. A. Zimmerman et al. ) А - рецептор - сигнальная молекула Б Г В А – эндокринный механизм; Б – паракринный механизм; В – аутокринный механизм; Г – юкстакринный механизм 7
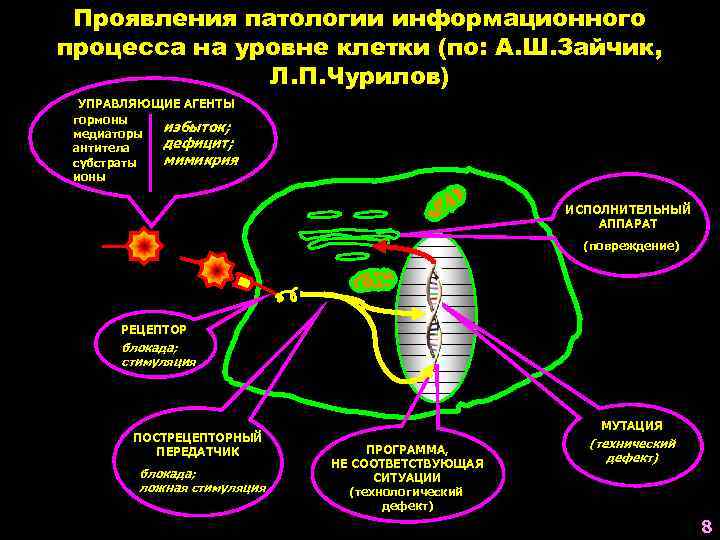 Проявления патологии информационного процесса на уровне клетки (по: А. Ш. Зайчик, Л. П. Чурилов) УПРАВЛЯЮЩИЕ АГЕНТЫ гормоны избыток; медиаторы дефицит; антитела мимикрия субстраты ионы ИСПОЛНИТЕЛЬНЫЙ АППАРАТ (повреждение) РЕЦЕПТОР блокада; стимуляция ПОСТРЕЦЕПТОРНЫЙ ПЕРЕДАТЧИК блокада; ложная стимуляция МУТАЦИЯ ПРОГРАММА, НЕ СООТВЕТСТВУЮЩАЯ СИТУАЦИИ (технологический дефект) (технический дефект) 8
Проявления патологии информационного процесса на уровне клетки (по: А. Ш. Зайчик, Л. П. Чурилов) УПРАВЛЯЮЩИЕ АГЕНТЫ гормоны избыток; медиаторы дефицит; антитела мимикрия субстраты ионы ИСПОЛНИТЕЛЬНЫЙ АППАРАТ (повреждение) РЕЦЕПТОР блокада; стимуляция ПОСТРЕЦЕПТОРНЫЙ ПЕРЕДАТЧИК блокада; ложная стимуляция МУТАЦИЯ ПРОГРАММА, НЕ СООТВЕТСТВУЮЩАЯ СИТУАЦИИ (технологический дефект) (технический дефект) 8
 Гибель клетки. Некроз и апоптоз
Гибель клетки. Некроз и апоптоз
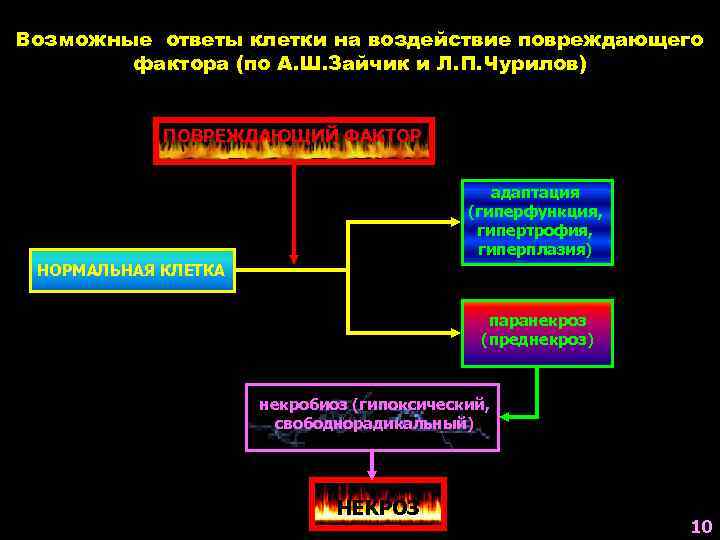 Возможные ответы клетки на воздействие повреждающего фактора (по А. Ш. Зайчик и Л. П. Чурилов) ПОВРЕЖДАЮЩИЙ ФАКТОР адаптация (гиперфункция, гипертрофия, гиперплазия) НОРМАЛЬНАЯ КЛЕТКА паранекроз (преднекроз) некробиоз (гипоксический, свободнорадикальный) НЕКРОЗ 10
Возможные ответы клетки на воздействие повреждающего фактора (по А. Ш. Зайчик и Л. П. Чурилов) ПОВРЕЖДАЮЩИЙ ФАКТОР адаптация (гиперфункция, гипертрофия, гиперплазия) НОРМАЛЬНАЯ КЛЕТКА паранекроз (преднекроз) некробиоз (гипоксический, свободнорадикальный) НЕКРОЗ 10
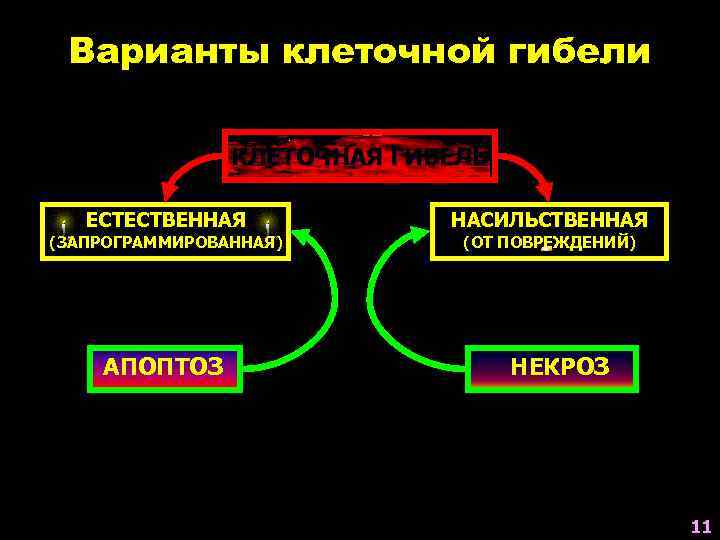 Варианты клеточной гибели КЛЕТОЧНАЯ ГИБЕЛЬ ЕСТЕСТВЕННАЯ (ЗАПРОГРАММИРОВАННАЯ) АПОПТОЗ НАСИЛЬСТВЕННАЯ (ОТ ПОВРЕЖДЕНИЙ) НЕКРОЗ 11
Варианты клеточной гибели КЛЕТОЧНАЯ ГИБЕЛЬ ЕСТЕСТВЕННАЯ (ЗАПРОГРАММИРОВАННАЯ) АПОПТОЗ НАСИЛЬСТВЕННАЯ (ОТ ПОВРЕЖДЕНИЙ) НЕКРОЗ 11
 Некроз. Определение Некроз – это деструкция и гибель клетки, возникающая в результате воздействия на нее как внешних физических и химических агентов, так и за счет прекращения снабжения клетки кислородом и питательными веществами, а также благодаря альтерации, вызванной другими эндогенными факторами, способными привести к необратимому разрушению ее метаболизма и структур.
Некроз. Определение Некроз – это деструкция и гибель клетки, возникающая в результате воздействия на нее как внешних физических и химических агентов, так и за счет прекращения снабжения клетки кислородом и питательными веществами, а также благодаря альтерации, вызванной другими эндогенными факторами, способными привести к необратимому разрушению ее метаболизма и структур.
 Апоптоз - определение понятия Апоптоз (от греческого – apo – «отделение» и ptosis – «падение» ) – запрограммированный процесс уничтожения клетки, вызванный внутренними (внутриклеточными) или внешними (внеклеточными) как физиологическими, так и патологическими факторами, активирующими генетическую программу гибели клетки и ее удаления из ткани
Апоптоз - определение понятия Апоптоз (от греческого – apo – «отделение» и ptosis – «падение» ) – запрограммированный процесс уничтожения клетки, вызванный внутренними (внутриклеточными) или внешними (внеклеточными) как физиологическими, так и патологическими факторами, активирующими генетическую программу гибели клетки и ее удаления из ткани
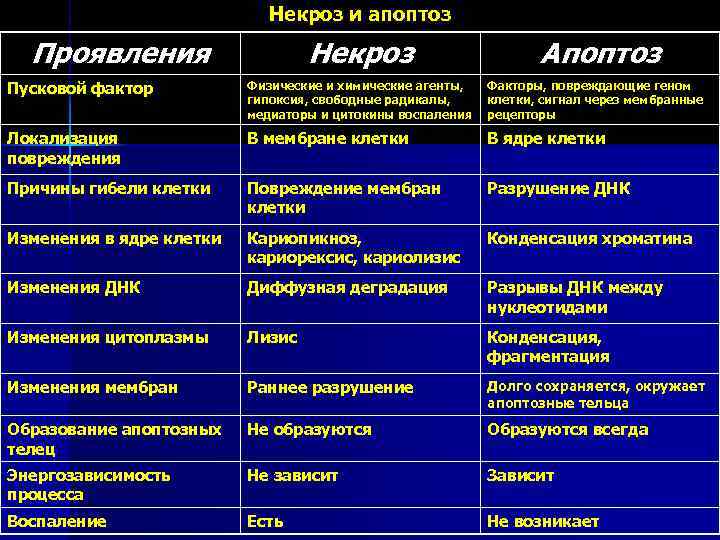 Некроз и апоптоз Проявления Некроз Апоптоз Пусковой фактор Физические и химические агенты, гипоксия, свободные радикалы, медиаторы и цитокины воспаления Факторы, повреждающие геном клетки, сигнал через мембранные рецепторы Локализация повреждения В мембране клетки В ядре клетки Причины гибели клетки Повреждение мембран клетки Разрушение ДНК Изменения в ядре клетки Кариопикноз, кариорексис, кариолизис Конденсация хроматина Изменения ДНК Диффузная деградация Разрывы ДНК между нуклеотидами Изменения цитоплазмы Лизис Конденсация, фрагментация Изменения мембран Раннее разрушение Долго сохраняется, окружает апоптозные тельца Образование апоптозных телец Не образуются Образуются всегда Энергозависимость процесса Не зависит Зависит Воспаление Есть Не возникает
Некроз и апоптоз Проявления Некроз Апоптоз Пусковой фактор Физические и химические агенты, гипоксия, свободные радикалы, медиаторы и цитокины воспаления Факторы, повреждающие геном клетки, сигнал через мембранные рецепторы Локализация повреждения В мембране клетки В ядре клетки Причины гибели клетки Повреждение мембран клетки Разрушение ДНК Изменения в ядре клетки Кариопикноз, кариорексис, кариолизис Конденсация хроматина Изменения ДНК Диффузная деградация Разрывы ДНК между нуклеотидами Изменения цитоплазмы Лизис Конденсация, фрагментация Изменения мембран Раннее разрушение Долго сохраняется, окружает апоптозные тельца Образование апоптозных телец Не образуются Образуются всегда Энергозависимость процесса Не зависит Зависит Воспаление Есть Не возникает
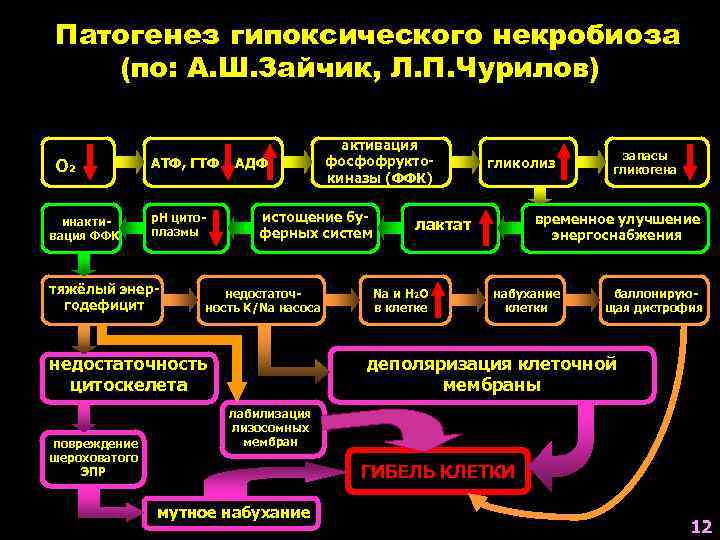 Патогенез гипоксического некробиоза (по: А. Ш. Зайчик, Л. П. Чурилов) О 2 инактивация ФФК АТФ, ГТФ р. Н цитоплазмы тяжёлый энергодефицит АДФ истощение буферных систем недостаточность K/Na насоса недостаточность цитоскелета повреждение шероховатого ЭПР активация фосфофруктокиназы (ФФК) гликолиз временное улучшение энергоснабжения лактат Na и H 2 O в клетке запасы гликогена набухание клетки баллонирующая дистрофия деполяризация клеточной мембраны лабилизация лизосомных мембран ГИБЕЛЬ КЛЕТКИ мутное набухание 12
Патогенез гипоксического некробиоза (по: А. Ш. Зайчик, Л. П. Чурилов) О 2 инактивация ФФК АТФ, ГТФ р. Н цитоплазмы тяжёлый энергодефицит АДФ истощение буферных систем недостаточность K/Na насоса недостаточность цитоскелета повреждение шероховатого ЭПР активация фосфофруктокиназы (ФФК) гликолиз временное улучшение энергоснабжения лактат Na и H 2 O в клетке запасы гликогена набухание клетки баллонирующая дистрофия деполяризация клеточной мембраны лабилизация лизосомных мембран ГИБЕЛЬ КЛЕТКИ мутное набухание 12
 Из истории изучения апоптоза (1) 1. А. Вейсман, 1864 г. , впервые описал локальную гибель клеток, которая с современной точки зрения может быть объяснена феном апоптоза. 2. В. Флеминг, 1885 г. , описал явление хроматолиза – гибель клеток, связанную с редукцией и исчезновением ядра клетки. 3. Л. Глусман, 1950 г. , описал программированную клеточную гибель (ПКГ) клеток эмбриона в процессе его развития
Из истории изучения апоптоза (1) 1. А. Вейсман, 1864 г. , впервые описал локальную гибель клеток, которая с современной точки зрения может быть объяснена феном апоптоза. 2. В. Флеминг, 1885 г. , описал явление хроматолиза – гибель клеток, связанную с редукцией и исчезновением ядра клетки. 3. Л. Глусман, 1950 г. , описал программированную клеточную гибель (ПКГ) клеток эмбриона в процессе его развития
 Из истории изучения апоптоза (2) 4. J. F. R. Kerr, A. H. Wyllie, A. R. Currie, 1972 г. , опубликовали в журнале British J. of Cancer статью о программированной гибели клеток, впервые применив для описания этого явления термин «апоптоз» . 5. Сидни Бреннер (S. Brenner), Джон Салстон (J. Sulston) – оба Великобритания, Роберт Хорвиц (R. Horvitz) - США, в 2002 г. получили нобелевскую премию по медицине за открытие и описание генетических механизмов апоптоза и его роли в физиологических и патологических процессах, протекающих в организме
Из истории изучения апоптоза (2) 4. J. F. R. Kerr, A. H. Wyllie, A. R. Currie, 1972 г. , опубликовали в журнале British J. of Cancer статью о программированной гибели клеток, впервые применив для описания этого явления термин «апоптоз» . 5. Сидни Бреннер (S. Brenner), Джон Салстон (J. Sulston) – оба Великобритания, Роберт Хорвиц (R. Horvitz) - США, в 2002 г. получили нобелевскую премию по медицине за открытие и описание генетических механизмов апоптоза и его роли в физиологических и патологических процессах, протекающих в организме
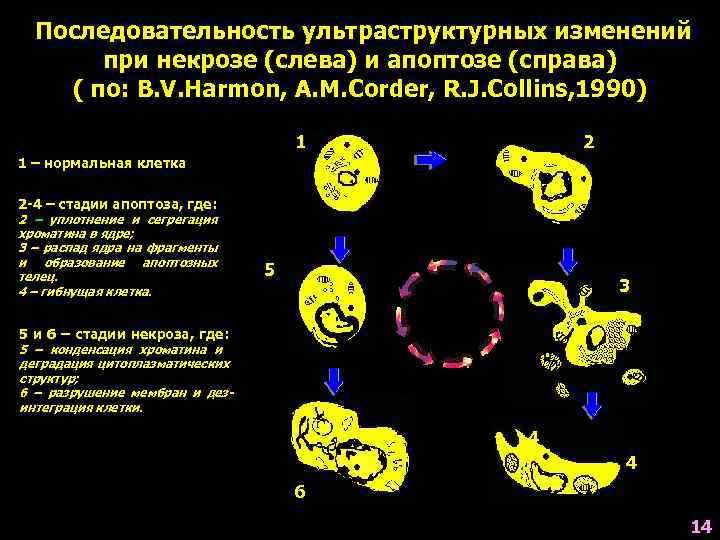 Последовательность ультраструктурных изменений при некрозе (слева) и апоптозе (справа) ( по: B. V. Harmon, A. M. Corder, R. J. Collins, 1990) 1 2 1 – нормальная клетка 2 -4 – стадии апоптоза, где: 2 – уплотнение и сегрегация хроматина в ядре; 3 – распад ядра на фрагменты и образование апоптозных телец. 4 – гибнущая клетка. 5 3 5 и 6 – стадии некроза, где: 5 – конденсация хроматина и деградация цитоплазматических структур; 6 – разрушение мембран и дезинтеграция клетки. 4 4 6 14
Последовательность ультраструктурных изменений при некрозе (слева) и апоптозе (справа) ( по: B. V. Harmon, A. M. Corder, R. J. Collins, 1990) 1 2 1 – нормальная клетка 2 -4 – стадии апоптоза, где: 2 – уплотнение и сегрегация хроматина в ядре; 3 – распад ядра на фрагменты и образование апоптозных телец. 4 – гибнущая клетка. 5 3 5 и 6 – стадии некроза, где: 5 – конденсация хроматина и деградация цитоплазматических структур; 6 – разрушение мембран и дезинтеграция клетки. 4 4 6 14
 Роль апоптоза в физиологических процессах Физиологические процессы, сопровождающиеся использованием механизмов апоптоза: - автономный апоптоз в процессе эмбриогенеза; - апоптоз в быстро и медленно пролиферирующих клеточных популяциях (гомеостаз объема ткани; клеточная дифференцировка); - апоптоз стареющих клеток
Роль апоптоза в физиологических процессах Физиологические процессы, сопровождающиеся использованием механизмов апоптоза: - автономный апоптоз в процессе эмбриогенеза; - апоптоз в быстро и медленно пролиферирующих клеточных популяциях (гомеостаз объема ткани; клеточная дифференцировка); - апоптоз стареющих клеток
 Роль апоптоза в патологии Роль апоптоза в развитии патологических процессов: - апоптоз клеток, имеющих повреждение ДНК; - апоптоз опухолевых клеток; - апоптоз клеток ишемизированных органов и тканей -апоптоз клеток, находящихся в состоянии «клеточного стресса» ; - апоптоз клеток, зараженных вирусами; - апоптоз клеток «хозяина» , индуцированный Т-лимфоцитами при трансплантации иммунокомпетентной ткани.
Роль апоптоза в патологии Роль апоптоза в развитии патологических процессов: - апоптоз клеток, имеющих повреждение ДНК; - апоптоз опухолевых клеток; - апоптоз клеток ишемизированных органов и тканей -апоптоз клеток, находящихся в состоянии «клеточного стресса» ; - апоптоз клеток, зараженных вирусами; - апоптоз клеток «хозяина» , индуцированный Т-лимфоцитами при трансплантации иммунокомпетентной ткани.
 Роль усиления или ослабления апоптоза в развитии патологии Усиление апоптоза Врожденные дефекты тканей, уродства. Панцитопении, первичные иммунодефициты. Нейродегенеративные процессы. Бактериальные и вирусные инфекции (в том числе – СПИД). Цитотоксическая терапия Ослабление апоптоза Развитие злокачественных опухолей. Аутоиммунные процессы
Роль усиления или ослабления апоптоза в развитии патологии Усиление апоптоза Врожденные дефекты тканей, уродства. Панцитопении, первичные иммунодефициты. Нейродегенеративные процессы. Бактериальные и вирусные инфекции (в том числе – СПИД). Цитотоксическая терапия Ослабление апоптоза Развитие злокачественных опухолей. Аутоиммунные процессы
 Генетические факторы способствующие или препятствующие развитию апоптоза Гены, синтезирующие белки ингибирующие авпоптоз: Bcl-2, ced-9, BHRF 1, MCL-1 Гены, синтезирующие белки, стимулирующие апотоз: р53, Bax, bcl-x. S На представленных далее слайдах для наглядности и упрощения в качестве факторов, стимулирующих апоптоз, будет указан белок р53, а в качестве фактора, ингибирующего апоптоз – белок Bcl-2
Генетические факторы способствующие или препятствующие развитию апоптоза Гены, синтезирующие белки ингибирующие авпоптоз: Bcl-2, ced-9, BHRF 1, MCL-1 Гены, синтезирующие белки, стимулирующие апотоз: р53, Bax, bcl-x. S На представленных далее слайдах для наглядности и упрощения в качестве факторов, стимулирующих апоптоз, будет указан белок р53, а в качестве фактора, ингибирующего апоптоз – белок Bcl-2
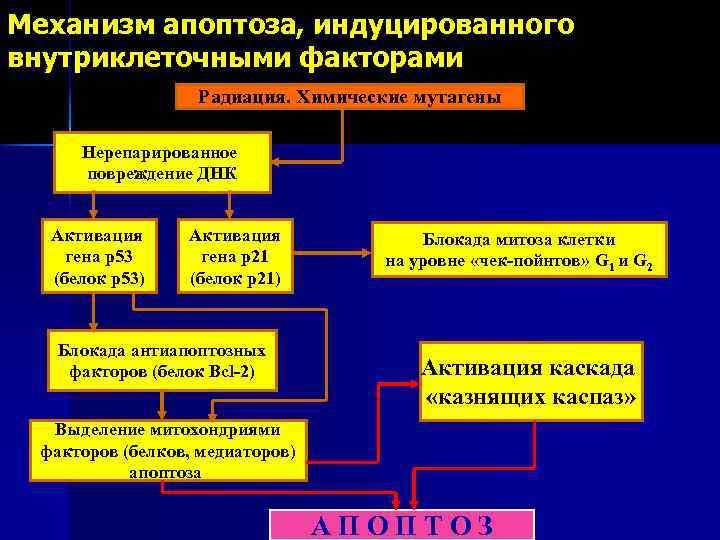 Механизм апоптоза, индуцированного внутриклеточными факторами Радиация. Химические мутагены Нерепарированное повреждение ДНК Активация гена р53 (белок р53) Активация гена р21 (белок р21) Блокада антиапоптозных факторов (белок Bcl-2) Блокада митоза клетки на уровне «чек-пойнтов» G 1 и G 2 Активация каскада «казнящих каспаз» Выделение митохондриями факторов (белков, медиаторов) апоптоза АПОПТОЗ
Механизм апоптоза, индуцированного внутриклеточными факторами Радиация. Химические мутагены Нерепарированное повреждение ДНК Активация гена р53 (белок р53) Активация гена р21 (белок р21) Блокада антиапоптозных факторов (белок Bcl-2) Блокада митоза клетки на уровне «чек-пойнтов» G 1 и G 2 Активация каскада «казнящих каспаз» Выделение митохондриями факторов (белков, медиаторов) апоптоза АПОПТОЗ
 Каспазы – специфические ферменты, относящиеся к группе цистеиновых протеаз. Название протеаз «Caspase» составлено из трех частей: «С» - отражает механизм протеолиза (в активном центре протеаз находится цистеин); «Asp» - от аспарагиновой кислоты, которую протеазы распознают как субстрат; «Ase» - окончание, свойственное названиям всех ферментов. В клетках содержится до 10 каспаз, которые взаимно активируясь образуют так называемый протеолитический «каспазный каскад» .
Каспазы – специфические ферменты, относящиеся к группе цистеиновых протеаз. Название протеаз «Caspase» составлено из трех частей: «С» - отражает механизм протеолиза (в активном центре протеаз находится цистеин); «Asp» - от аспарагиновой кислоты, которую протеазы распознают как субстрат; «Ase» - окончание, свойственное названиям всех ферментов. В клетках содержится до 10 каспаз, которые взаимно активируясь образуют так называемый протеолитический «каспазный каскад» .
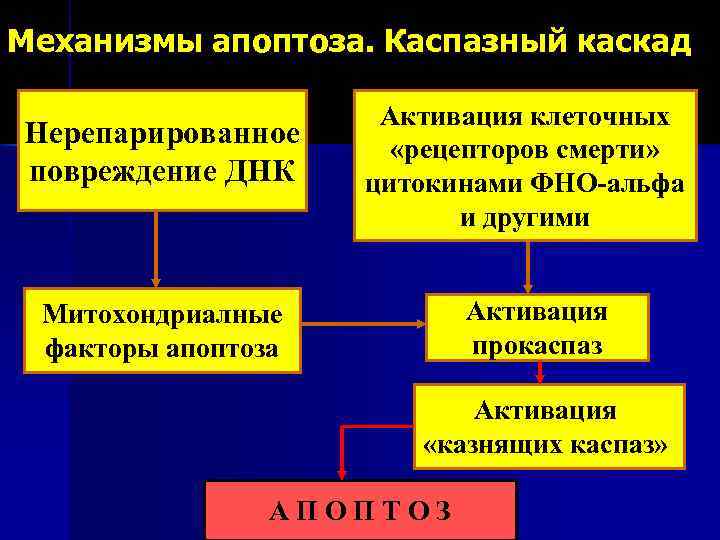 Механизмы апоптоза. Каспазный каскад Нерепарированное повреждение ДНК Активация клеточных «рецепторов смерти» цитокинами ФНО-альфа и другими Активация прокаспаз Митохондриалные факторы апоптоза Активация «казнящих каспаз» АПОПТОЗ
Механизмы апоптоза. Каспазный каскад Нерепарированное повреждение ДНК Активация клеточных «рецепторов смерти» цитокинами ФНО-альфа и другими Активация прокаспаз Митохондриалные факторы апоптоза Активация «казнящих каспаз» АПОПТОЗ
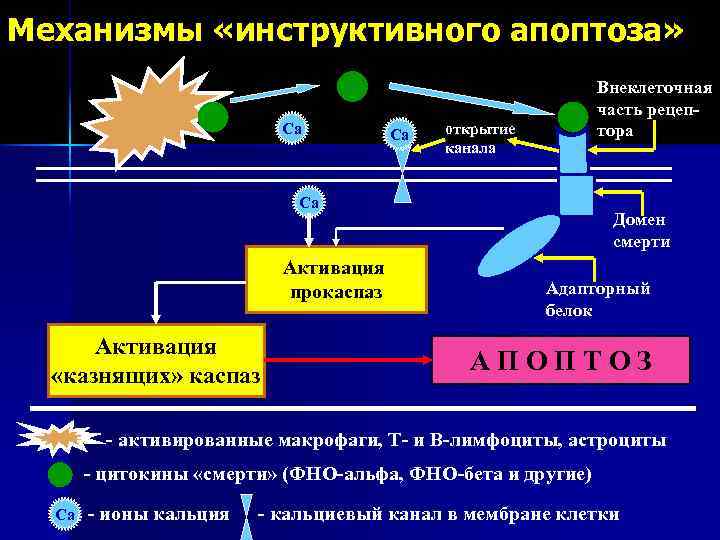 Механизмы «инструктивного апоптоза» Са Са Внеклеточная часть рецептора открытие канала Са Активация прокаспаз Активация «казнящих» каспаз Домен смерти Адапторный белок АПОПТОЗ - активированные макрофаги, Т- и В-лимфоциты, астроциты - цитокины «смерти» (ФНО-альфа, ФНО-бета и другие) Са - ионы кальция - кальциевый канал в мембране клетки
Механизмы «инструктивного апоптоза» Са Са Внеклеточная часть рецептора открытие канала Са Активация прокаспаз Активация «казнящих» каспаз Домен смерти Адапторный белок АПОПТОЗ - активированные макрофаги, Т- и В-лимфоциты, астроциты - цитокины «смерти» (ФНО-альфа, ФНО-бета и другие) Са - ионы кальция - кальциевый канал в мембране клетки
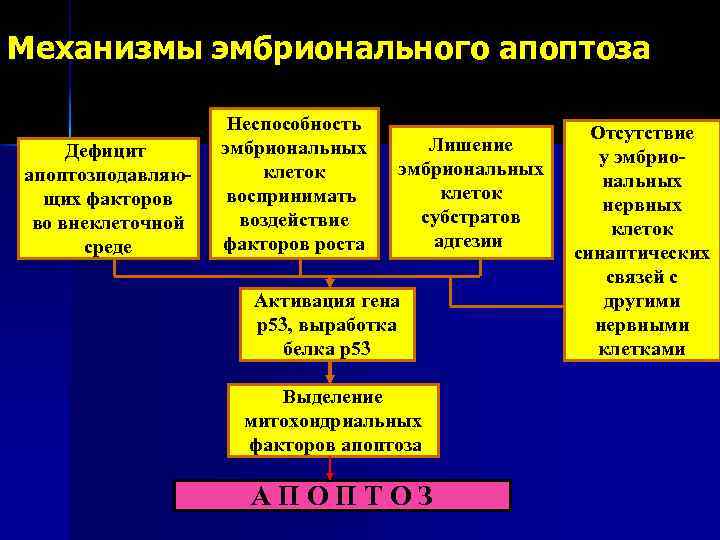 Механизмы эмбрионального апоптоза Дефицит апоптозподавляющих факторов во внеклеточной среде Неспособность эмбриональных клеток воспринимать воздействие факторов роста Лишение эмбриональных клеток субстратов адгезии Активация гена р53, выработка белка р53 Выделение митохондриальных факторов апоптоза АПОПТОЗ Отсутствие у эмбриональных нервных клеток синаптических связей с другими нервными клетками
Механизмы эмбрионального апоптоза Дефицит апоптозподавляющих факторов во внеклеточной среде Неспособность эмбриональных клеток воспринимать воздействие факторов роста Лишение эмбриональных клеток субстратов адгезии Активация гена р53, выработка белка р53 Выделение митохондриальных факторов апоптоза АПОПТОЗ Отсутствие у эмбриональных нервных клеток синаптических связей с другими нервными клетками
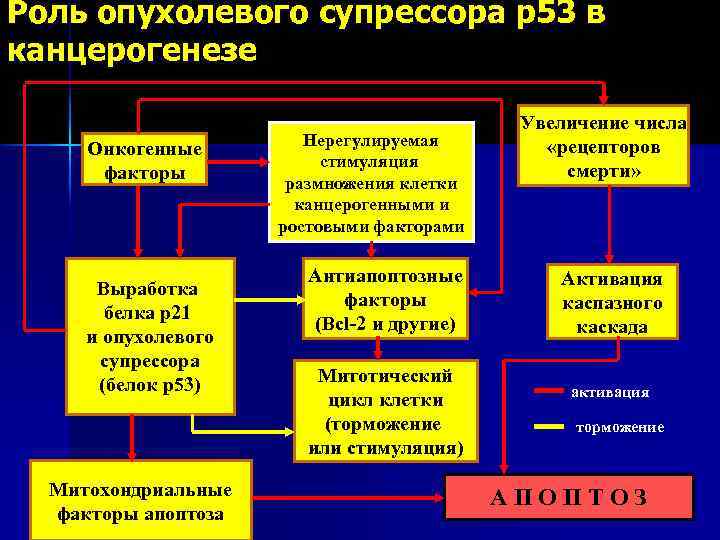 Роль опухолевого супрессора р53 в канцерогенезе Онкогенные факторы Выработка белка р21 и опухолевого супрессора (белок р53) Митохондриальные факторы апоптоза Нерегулируемая стимуляция размножения клетки канцерогенными и ростовыми факторами Антиапоптозные факторы (Bcl-2 и другие) Митотический цикл клетки (торможение или стимуляция) Увеличение числа «рецепторов смерти» Активация каспазного каскада активация торможение АПОПТОЗ
Роль опухолевого супрессора р53 в канцерогенезе Онкогенные факторы Выработка белка р21 и опухолевого супрессора (белок р53) Митохондриальные факторы апоптоза Нерегулируемая стимуляция размножения клетки канцерогенными и ростовыми факторами Антиапоптозные факторы (Bcl-2 и другие) Митотический цикл клетки (торможение или стимуляция) Увеличение числа «рецепторов смерти» Активация каспазного каскада активация торможение АПОПТОЗ
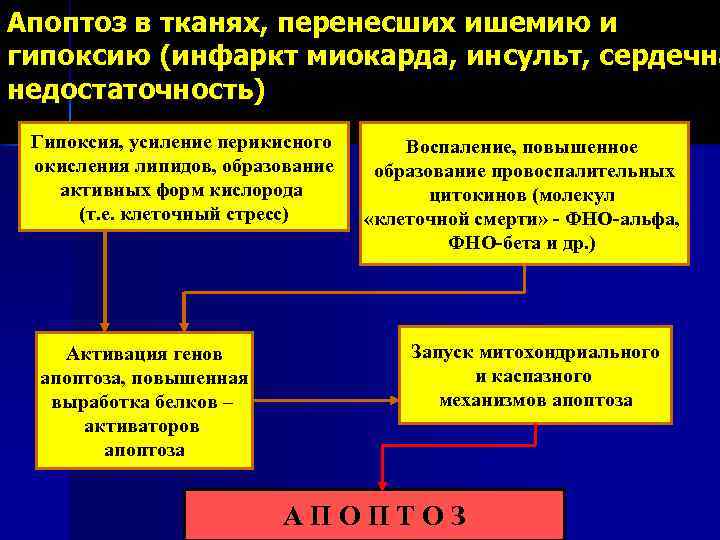 Апоптоз в тканях, перенесших ишемию и гипоксию (инфаркт миокарда, инсульт, сердечна недостаточность) Гипоксия, усиление перикисного окисления липидов, образование активных форм кислорода (т. е. клеточный стресс) Активация генов апоптоза, повышенная выработка белков – активаторов апоптоза Воспаление, повышенное образование провоспалительных цитокинов (молекул «клеточной смерти» - ФНО-альфа, ФНО-бета и др. ) Запуск митохондриального и каспазного механизмов апоптоза АПОПТОЗ
Апоптоз в тканях, перенесших ишемию и гипоксию (инфаркт миокарда, инсульт, сердечна недостаточность) Гипоксия, усиление перикисного окисления липидов, образование активных форм кислорода (т. е. клеточный стресс) Активация генов апоптоза, повышенная выработка белков – активаторов апоптоза Воспаление, повышенное образование провоспалительных цитокинов (молекул «клеточной смерти» - ФНО-альфа, ФНО-бета и др. ) Запуск митохондриального и каспазного механизмов апоптоза АПОПТОЗ

 Постулат Августа Вейсмана В 1881 году известный зоолог и теоретик эволюционного учения Август Вейсман изложил свою гипотезу о старении организма следующим образом: старение организма определяется тем обстоятельством, что у соматических клеток «способность к росту путем деления не вечна, а ограничена» . По его же мнению не старятся только половые клетки, способность к делению которых не ограничена.
Постулат Августа Вейсмана В 1881 году известный зоолог и теоретик эволюционного учения Август Вейсман изложил свою гипотезу о старении организма следующим образом: старение организма определяется тем обстоятельством, что у соматических клеток «способность к росту путем деления не вечна, а ограничена» . По его же мнению не старятся только половые клетки, способность к делению которых не ограничена.
 Лимит Хейфлика В 1961 году американский цитолог, работавший в Вистаровском институте, Леонард Хейфлик совместно с П. Мурхедом, экспериментируя с культурой фибробластов человеческого эмбриона, показали, что при многочисленных пересевах культуры клеток размножение их останавливается после того, как клетки совершали 50 - 60 делений. Тем самым Л. Хейфлик полностью подтвердил постулат А. Вейсмана о «смертности» соматических клеток человека. В дальнейшем многочисленные эксперименты с культурой соматических клеток других позвоночных показали такие же результаты, с той поправкой, что для различных животных «лимит Хейфлика» оказался различным.
Лимит Хейфлика В 1961 году американский цитолог, работавший в Вистаровском институте, Леонард Хейфлик совместно с П. Мурхедом, экспериментируя с культурой фибробластов человеческого эмбриона, показали, что при многочисленных пересевах культуры клеток размножение их останавливается после того, как клетки совершали 50 - 60 делений. Тем самым Л. Хейфлик полностью подтвердил постулат А. Вейсмана о «смертности» соматических клеток человека. В дальнейшем многочисленные эксперименты с культурой соматических клеток других позвоночных показали такие же результаты, с той поправкой, что для различных животных «лимит Хейфлика» оказался различным.
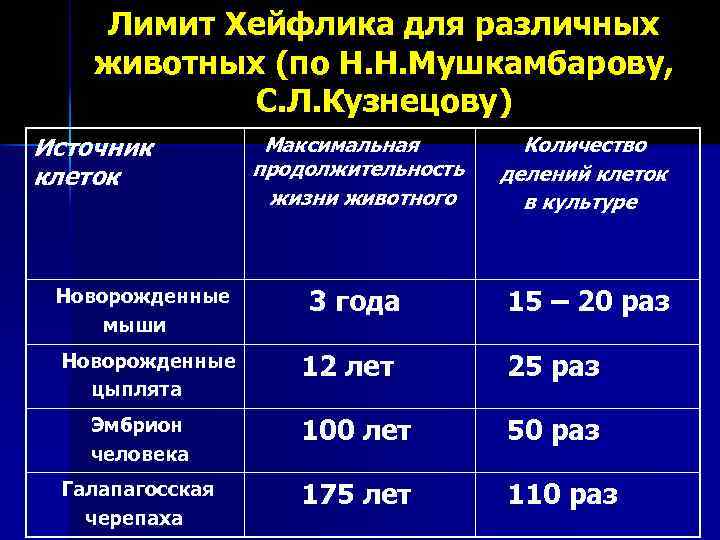 Лимит Хейфлика для различных животных (по Н. Н. Мушкамбарову, С. Л. Кузнецову) Источник клеток Максимальная продолжительность жизни животного Количество делений клеток в культуре 3 года 15 – 20 раз 12 лет 25 раз Эмбрион человека 100 лет 50 раз Галапагосская черепаха 175 лет 110 раз Новорожденные мыши Новорожденные цыплята
Лимит Хейфлика для различных животных (по Н. Н. Мушкамбарову, С. Л. Кузнецову) Источник клеток Максимальная продолжительность жизни животного Количество делений клеток в культуре 3 года 15 – 20 раз 12 лет 25 раз Эмбрион человека 100 лет 50 раз Галапагосская черепаха 175 лет 110 раз Новорожденные мыши Новорожденные цыплята
 Теломеразная теория старения клетки В 1971 году русский ученый А. М. Оловников, обобщив свои наблюдения и эксперименты, пришел к выводу, что при репликации хромосом их концевые участки (теломеры) с каждым делением клетки укорачиваются и при достижении определенного предела репликация хромосом в соматических клетках прекращается, клетки перестают делиться и начинается процесс их старения, заканчивающийся гибелью клетки. В 1985 году Грейдер и Блэкборн обнаружили и описали клеточный фермент – теломеразу. Механизм действия теломеразы – это повторяющееся кодирование с помощью РНКматрицы, входящей в состав теломеразы, новых нуклеотидных последовательностей теломеры и, таким образом, восстановление ее исходной длины.
Теломеразная теория старения клетки В 1971 году русский ученый А. М. Оловников, обобщив свои наблюдения и эксперименты, пришел к выводу, что при репликации хромосом их концевые участки (теломеры) с каждым делением клетки укорачиваются и при достижении определенного предела репликация хромосом в соматических клетках прекращается, клетки перестают делиться и начинается процесс их старения, заканчивающийся гибелью клетки. В 1985 году Грейдер и Блэкборн обнаружили и описали клеточный фермент – теломеразу. Механизм действия теломеразы – это повторяющееся кодирование с помощью РНКматрицы, входящей в состав теломеразы, новых нуклеотидных последовательностей теломеры и, таким образом, восстановление ее исходной длины.
 Теломера – это нуклеопротеидный комплекс (одноцепочечная ДНК), локализованный на конце линейной хромосомы. Линейные хромосомы имеют по две теломеры. Теломера содержит специальные последовательности ДНК (нуклеотидные последовательности), обеспечивающие точную репликацию хромосом. У человека нуклеотидные последовательности теломеры можно обозначить как TTAGGG (Т – тимин; А – аденин; G – гуанин). При каждом делении клетки длина теломеры укорачивается на определенное число нуклеотидных последовательностей. При достижении некоего предела укорочения теломеры репликация хромосом прекращается и клетка перестает делиться.
Теломера – это нуклеопротеидный комплекс (одноцепочечная ДНК), локализованный на конце линейной хромосомы. Линейные хромосомы имеют по две теломеры. Теломера содержит специальные последовательности ДНК (нуклеотидные последовательности), обеспечивающие точную репликацию хромосом. У человека нуклеотидные последовательности теломеры можно обозначить как TTAGGG (Т – тимин; А – аденин; G – гуанин). При каждом делении клетки длина теломеры укорачивается на определенное число нуклеотидных последовательностей. При достижении некоего предела укорочения теломеры репликация хромосом прекращается и клетка перестает делиться.
 Теломераза – фермент (белок), основная функция которого достраивать новые нуклеотидные последовательности в теломерных участках хромосом. Теломераза несет собственную РНК-матрицу, и поэтому относится к классу обратных транскриптаз. В соматических клетках ген теломеразы на протяжении всей жизни клеток остается не активным. Он активен только в половых клетках, в стволовых клетках, а также в соматических клетках, подвергнувшихся малегнизации. Именно поэтому эти клетки носят название «иммортальные» , то есть – бессмертные.
Теломераза – фермент (белок), основная функция которого достраивать новые нуклеотидные последовательности в теломерных участках хромосом. Теломераза несет собственную РНК-матрицу, и поэтому относится к классу обратных транскриптаз. В соматических клетках ген теломеразы на протяжении всей жизни клеток остается не активным. Он активен только в половых клетках, в стволовых клетках, а также в соматических клетках, подвергнувшихся малегнизации. Именно поэтому эти клетки носят название «иммортальные» , то есть – бессмертные.
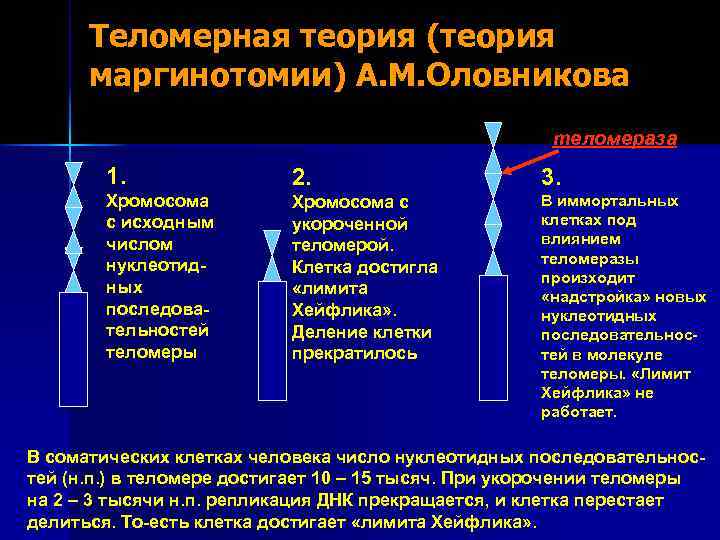 Теломерная теория (теория маргинотомии) А. М. Оловникова теломераза 1. 2. 3. Хромосома с исходным числом нуклеотидных последовательностей теломеры Хромосома с укороченной теломерой. Клетка достигла «лимита Хейфлика» . Деление клетки прекратилось В иммортальных клетках под влиянием теломеразы произходит «надстройка» новых нуклеотидных последовательностей в молекуле теломеры. «Лимит Хейфлика» не работает. В соматических клетках человека число нуклеотидных последовательностей (н. п. ) в теломере достигает 10 – 15 тысяч. При укорочении теломеры на 2 – 3 тысячи н. п. репликация ДНК прекращается, и клетка перестает делиться. То-есть клетка достигает «лимита Хейфлика» .
Теломерная теория (теория маргинотомии) А. М. Оловникова теломераза 1. 2. 3. Хромосома с исходным числом нуклеотидных последовательностей теломеры Хромосома с укороченной теломерой. Клетка достигла «лимита Хейфлика» . Деление клетки прекратилось В иммортальных клетках под влиянием теломеразы произходит «надстройка» новых нуклеотидных последовательностей в молекуле теломеры. «Лимит Хейфлика» не работает. В соматических клетках человека число нуклеотидных последовательностей (н. п. ) в теломере достигает 10 – 15 тысяч. При укорочении теломеры на 2 – 3 тысячи н. п. репликация ДНК прекращается, и клетка перестает делиться. То-есть клетка достигает «лимита Хейфлика» .
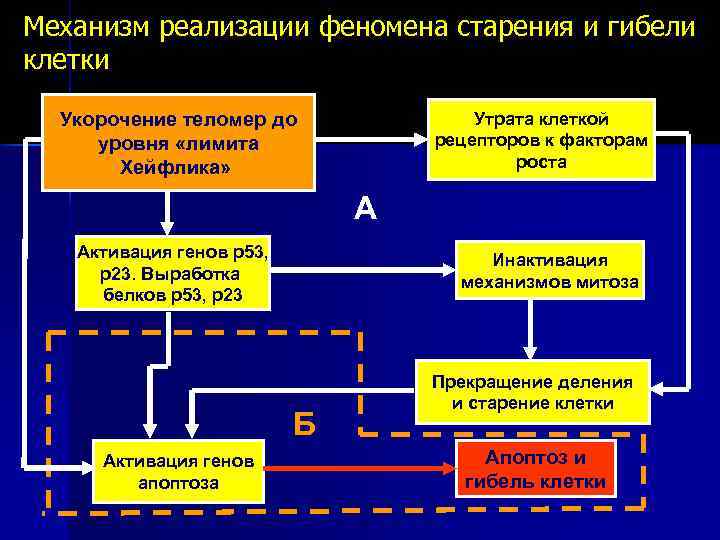 Механизм реализации феномена старения и гибели клетки Укорочение теломер до уровня «лимита Хейфлика» Утрата клеткой рецепторов к факторам роста А Активация генов р53, р23. Выработка белков р53, р23 Инактивация механизмов митоза Б Активация генов апоптоза Прекращение деления и старение клетки Апоптоз и гибель клетки
Механизм реализации феномена старения и гибели клетки Укорочение теломер до уровня «лимита Хейфлика» Утрата клеткой рецепторов к факторам роста А Активация генов р53, р23. Выработка белков р53, р23 Инактивация механизмов митоза Б Активация генов апоптоза Прекращение деления и старение клетки Апоптоз и гибель клетки
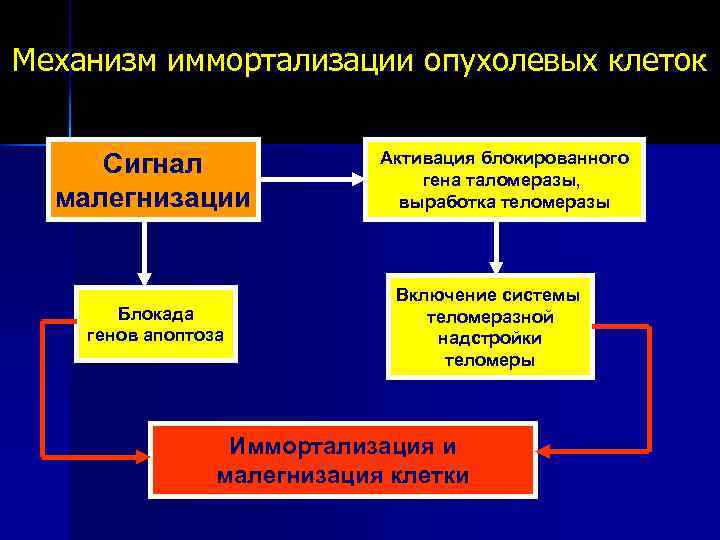 Механизм иммортализации опухолевых клеток Сигнал малегнизации Блокада генов апоптоза Активация блокированного гена таломеразы, выработка теломеразы Включение системы теломеразной надстройки теломеры Иммортализация и малегнизация клетки
Механизм иммортализации опухолевых клеток Сигнал малегнизации Блокада генов апоптоза Активация блокированного гена таломеразы, выработка теломеразы Включение системы теломеразной надстройки теломеры Иммортализация и малегнизация клетки
 Факты, подтверждающие теломеразную теорию старения клетки (1) 1. Фибробласты эмбриона человека, прошедшие в культуре ткани определенное число делений (например, 30) и замороженные на длительное время, после размораживание делятся не более 20 раз и, достигнув лимита Хейфлика, прекращают деление и погибают. 2. Соматические клетки, взятых у животных одного вида, но разного возраста, достигают лимита Хейфлика в разное время. Чем старше животное, тем меньшее количество делений совершают клетки. 3. Теломеры соматических клеток больных синдромами наследственной прогерии (синдром Хатчинсона-Гилфорда и синдром Вернера) при каждом делении укорачиваются на большее число н. п. , чем клетки здорового организма
Факты, подтверждающие теломеразную теорию старения клетки (1) 1. Фибробласты эмбриона человека, прошедшие в культуре ткани определенное число делений (например, 30) и замороженные на длительное время, после размораживание делятся не более 20 раз и, достигнув лимита Хейфлика, прекращают деление и погибают. 2. Соматические клетки, взятых у животных одного вида, но разного возраста, достигают лимита Хейфлика в разное время. Чем старше животное, тем меньшее количество делений совершают клетки. 3. Теломеры соматических клеток больных синдромами наследственной прогерии (синдром Хатчинсона-Гилфорда и синдром Вернера) при каждом делении укорачиваются на большее число н. п. , чем клетки здорового организма
 Факты, подтверждающие теломеразную теорию старения клетки (2) 4. Ген теломеразы, введенный в культуру соматических клеток, увеличивает лимит Хейфлика на 20 – 30 делений. 5. Теломеры половых клеток при их делении не укорачиваются, но даже могут удлиняться. В половых клетках ген теломеразы активен и в них идет постоянное образование теломеразы. 6. Ген теломеразы активен и в опухолевых клетках. Теломераза является маркером опухолевого процесса. 7. Введение в культуру опухолевых клеток веществ, блокирующих или разрушающих теломеразу, приводит к остановке безудержного размножения этих клеток.
Факты, подтверждающие теломеразную теорию старения клетки (2) 4. Ген теломеразы, введенный в культуру соматических клеток, увеличивает лимит Хейфлика на 20 – 30 делений. 5. Теломеры половых клеток при их делении не укорачиваются, но даже могут удлиняться. В половых клетках ген теломеразы активен и в них идет постоянное образование теломеразы. 6. Ген теломеразы активен и в опухолевых клетках. Теломераза является маркером опухолевого процесса. 7. Введение в культуру опухолевых клеток веществ, блокирующих или разрушающих теломеразу, приводит к остановке безудержного размножения этих клеток.
 Факты, не подтверждающие теломеразную теорию старения клетки 1. В организме человека и животных имеются неделящиеся клетки, срок жизни которых сравним со сроком жизни макроорганизма (например, нейроны головного мозга). Их гибель не обусловлена достижением «лимита Хейфлика» 2. Заражение клеток вирусом SV 40 приводит к тому, что они способны совершать по 20 – 40 делений сверх «лимита Хейфлика» . Однако, в этих клетках отсутствует теломераза и в них продолжается укорочение теломер. 3. Помимо укорочения теломер в соматических клетках наблюдается и много других изменений ДНК. Например, увеличение числа разрывов в цепях ДНК, усиление прочности связывания белков с ДНК, снижение активности ферментов репарации ДНК и др.
Факты, не подтверждающие теломеразную теорию старения клетки 1. В организме человека и животных имеются неделящиеся клетки, срок жизни которых сравним со сроком жизни макроорганизма (например, нейроны головного мозга). Их гибель не обусловлена достижением «лимита Хейфлика» 2. Заражение клеток вирусом SV 40 приводит к тому, что они способны совершать по 20 – 40 делений сверх «лимита Хейфлика» . Однако, в этих клетках отсутствует теломераза и в них продолжается укорочение теломер. 3. Помимо укорочения теломер в соматических клетках наблюдается и много других изменений ДНК. Например, увеличение числа разрывов в цепях ДНК, усиление прочности связывания белков с ДНК, снижение активности ферментов репарации ДНК и др.
 17
17
 О типовых реакциях поврежденной клетки На организм в течение всей его жизни воздействует поистине бесчисленное количество самых различных раздражителей. Вряд ли было бы правильным предполагать, что в процессе эволюции сформировались и закрепились «на всякий случай» специфические реакции на каждый из этих раздражителей. По-видимому, вернее считать, что в организме имеется ограниченное количество более или менее простых неспецифических (то есть не зависящих от качественных особенностей раздражителя) механизмов, направленных на поддержание нормального функционирования таких процессов, как энергообеспечение клетки, ее воспроизводство и реакция на раздражение. Соответственно, и характер патологического процесса будет зависеть от нарушения каким-либо внешним воздействием этих простейших неспецифических механизмов. Специфика же как защитно-приспособительных, так и патологических реакций будет определяться количеством, временем и порядком включения в процесс этих неспецифических компонентов. Отсюда вытекает, что ключ к пониманию механизмов как защиты, так и патологии, следует искать на пути изучения простейших составляющих физиологической или патологической реакции.
О типовых реакциях поврежденной клетки На организм в течение всей его жизни воздействует поистине бесчисленное количество самых различных раздражителей. Вряд ли было бы правильным предполагать, что в процессе эволюции сформировались и закрепились «на всякий случай» специфические реакции на каждый из этих раздражителей. По-видимому, вернее считать, что в организме имеется ограниченное количество более или менее простых неспецифических (то есть не зависящих от качественных особенностей раздражителя) механизмов, направленных на поддержание нормального функционирования таких процессов, как энергообеспечение клетки, ее воспроизводство и реакция на раздражение. Соответственно, и характер патологического процесса будет зависеть от нарушения каким-либо внешним воздействием этих простейших неспецифических механизмов. Специфика же как защитно-приспособительных, так и патологических реакций будет определяться количеством, временем и порядком включения в процесс этих неспецифических компонентов. Отсюда вытекает, что ключ к пониманию механизмов как защиты, так и патологии, следует искать на пути изучения простейших составляющих физиологической или патологической реакции.
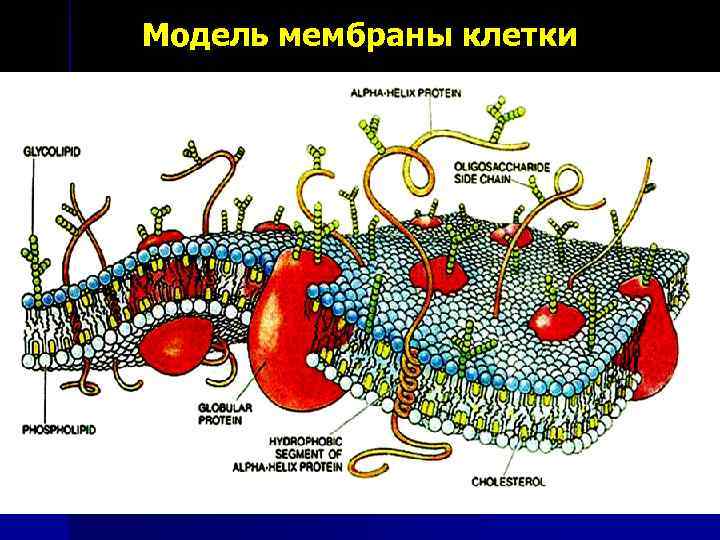 Модель мембраны клетки
Модель мембраны клетки
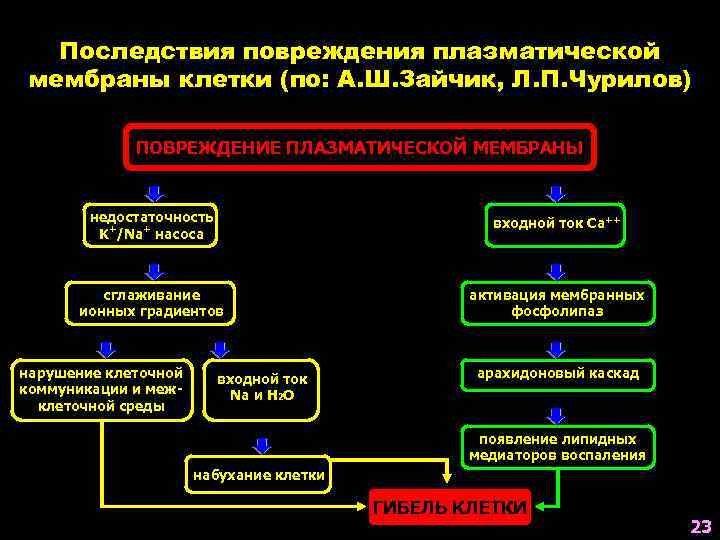 Последствия повреждения плазматической мембраны клетки (по: А. Ш. Зайчик, Л. П. Чурилов) ПОВРЕЖДЕНИЕ ПЛАЗМАТИЧЕСКОЙ МЕМБРАНЫ недостаточность K+/Na+ насоса входной ток Ca++ сглаживание ионных градиентов активация мембранных фосфолипаз нарушение клеточной коммуникации и межклеточной среды входной ток Na и H 2 O арахидоновый каскад появление липидных медиаторов воспаления набухание клетки ГИБЕЛЬ КЛЕТКИ 23
Последствия повреждения плазматической мембраны клетки (по: А. Ш. Зайчик, Л. П. Чурилов) ПОВРЕЖДЕНИЕ ПЛАЗМАТИЧЕСКОЙ МЕМБРАНЫ недостаточность K+/Na+ насоса входной ток Ca++ сглаживание ионных градиентов активация мембранных фосфолипаз нарушение клеточной коммуникации и межклеточной среды входной ток Na и H 2 O арахидоновый каскад появление липидных медиаторов воспаления набухание клетки ГИБЕЛЬ КЛЕТКИ 23
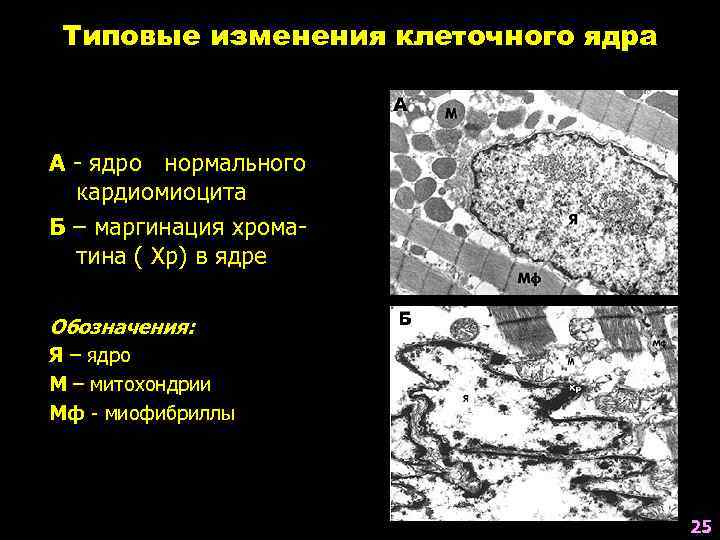 Типовые изменения клеточного ядра А - ядро нормального кардиомиоцита Б – маргинация хроматина ( Хр) в ядре Обозначения: Я – ядро М – митохондрии Мф - миофибриллы 25
Типовые изменения клеточного ядра А - ядро нормального кардиомиоцита Б – маргинация хроматина ( Хр) в ядре Обозначения: Я – ядро М – митохондрии Мф - миофибриллы 25
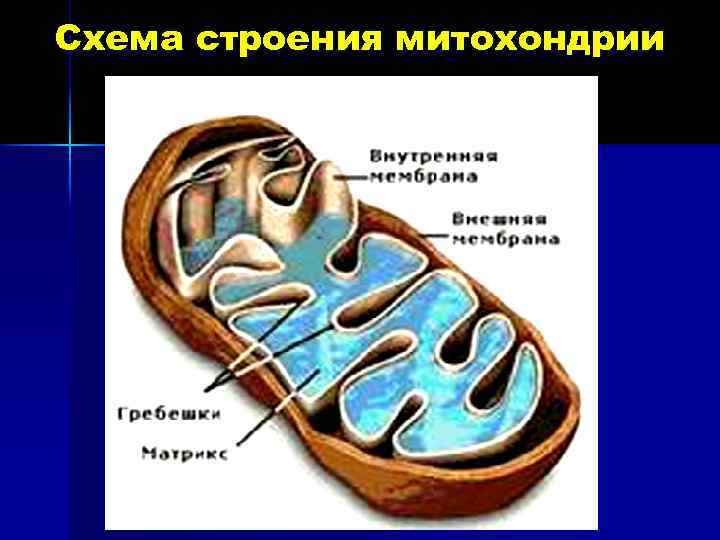 Схема строения митохондрии
Схема строения митохондрии
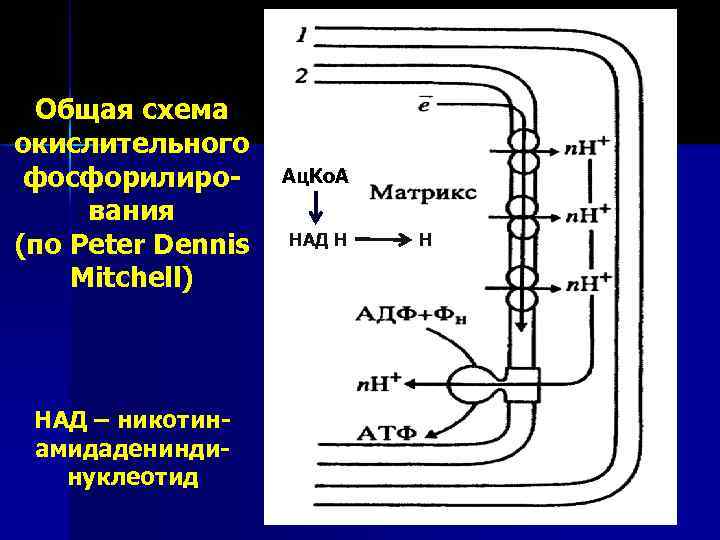 Общая схема окислительного фосфорилирования (по Peter Dennis Mitchell) НАД – никотинамидадениндинуклеотид Ац. Ко. А НАД Н Н
Общая схема окислительного фосфорилирования (по Peter Dennis Mitchell) НАД – никотинамидадениндинуклеотид Ац. Ко. А НАД Н Н
 Типовые изменения митохондрий (трансмиссионная электронная микроскопия) А – митохондрии нормального кардиомиоцита Б – набухание митохондрий В – гомогенизация митохондрий Г – деструкция митохондрий Обозначения: М – митохондрии Мф – миофибриллы
Типовые изменения митохондрий (трансмиссионная электронная микроскопия) А – митохондрии нормального кардиомиоцита Б – набухание митохондрий В – гомогенизация митохондрий Г – деструкция митохондрий Обозначения: М – митохондрии Мф – миофибриллы
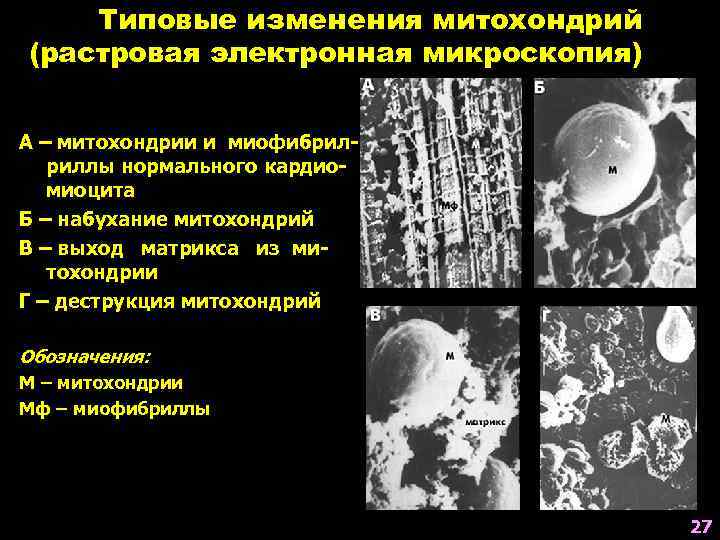 Типовые изменения митохондрий (растровая электронная микроскопия) А – митохондрии и миофибрилриллы нормального кардиомиоцита Б – набухание митохондрий В – выход матрикса из митохондрии Г – деструкция митохондрий Обозначения: М – митохондрии Мф – миофибриллы 27
Типовые изменения митохондрий (растровая электронная микроскопия) А – митохондрии и миофибрилриллы нормального кардиомиоцита Б – набухание митохондрий В – выход матрикса из митохондрии Г – деструкция митохондрий Обозначения: М – митохондрии Мф – миофибриллы 27
 Типовые изменения миофибрилл (1) А – миофибриллы нормального кардиомиоцита Б – гипертрофия миофибрилл В – пересокращение миофибрилл, их отёк и разволокнение Г – гомогенизация миофибрилл Обозначения: М – митохондрии Мф – миофибриллы 28
Типовые изменения миофибрилл (1) А – миофибриллы нормального кардиомиоцита Б – гипертрофия миофибрилл В – пересокращение миофибрилл, их отёк и разволокнение Г – гомогенизация миофибрилл Обозначения: М – митохондрии Мф – миофибриллы 28
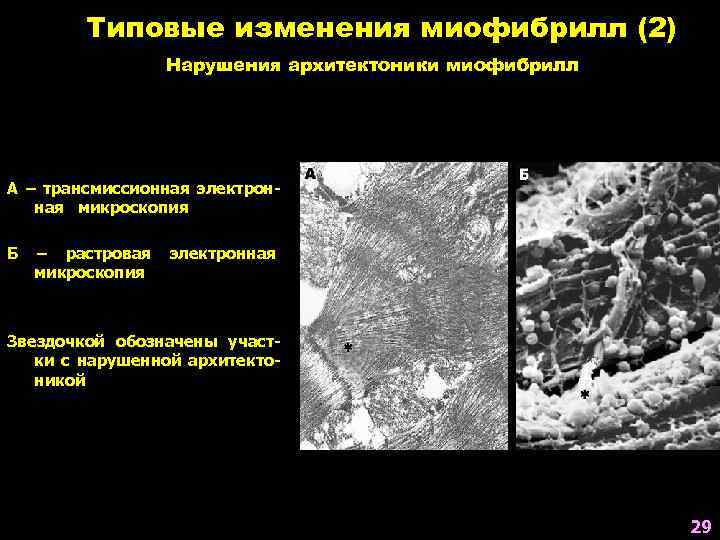 Типовые изменения миофибрилл (2) Нарушения архитектоники миофибрилл А – трансмиссионная электронная микроскопия Б – растровая микроскопия электронная Звездочкой обозначены участки с нарушенной архитектоникой 29
Типовые изменения миофибрилл (2) Нарушения архитектоники миофибрилл А – трансмиссионная электронная микроскопия Б – растровая микроскопия электронная Звездочкой обозначены участки с нарушенной архитектоникой 29
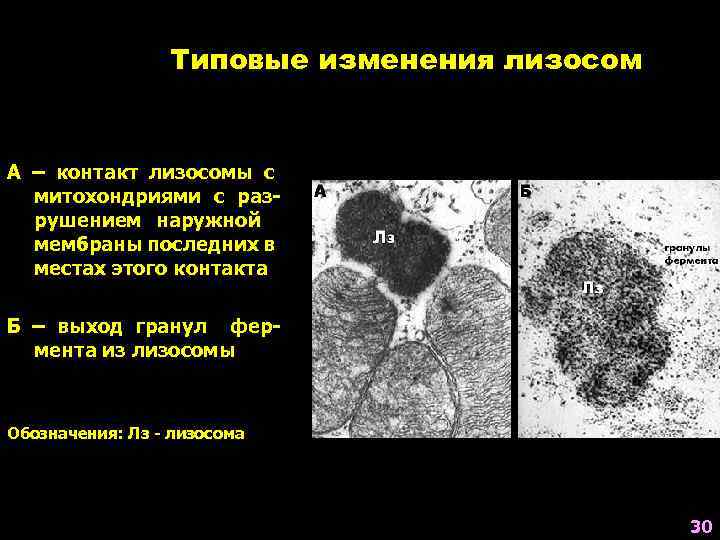 Типовые изменения лизосом А – контакт лизосомы с митохондриями с разрушением наружной мембраны последних в местах этого контакта Б – выход гранул фермента из лизосомы Обозначения: Лз - лизосома 30
Типовые изменения лизосом А – контакт лизосомы с митохондриями с разрушением наружной мембраны последних в местах этого контакта Б – выход гранул фермента из лизосомы Обозначения: Лз - лизосома 30
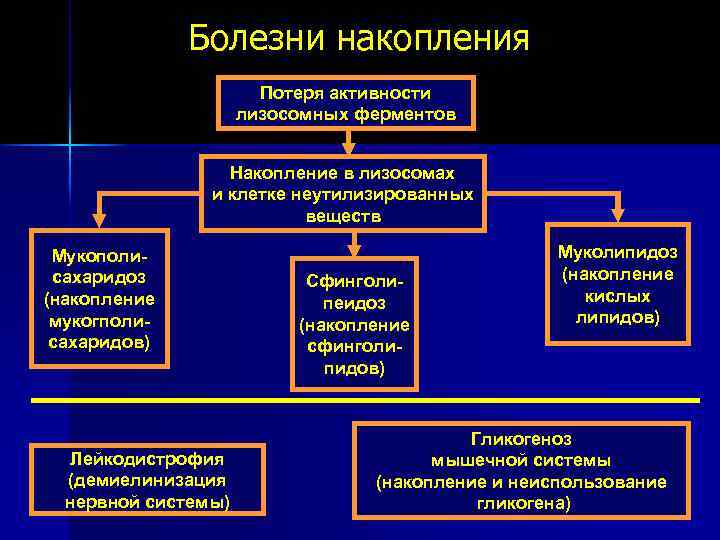 Болезни накопления Потеря активности лизосомных ферментов Накопление в лизосомах и клетке неутилизированных веществ Мукополисахаридоз (накопление мукогполисахаридов) Лейкодистрофия (демиелинизация нервной системы) Сфинголипеидоз (накопление сфинголипидов) Муколипидоз (накопление кислых липидов) Гликогеноз мышечной системы (накопление и неиспользование гликогена)
Болезни накопления Потеря активности лизосомных ферментов Накопление в лизосомах и клетке неутилизированных веществ Мукополисахаридоз (накопление мукогполисахаридов) Лейкодистрофия (демиелинизация нервной системы) Сфинголипеидоз (накопление сфинголипидов) Муколипидоз (накопление кислых липидов) Гликогеноз мышечной системы (накопление и неиспользование гликогена)
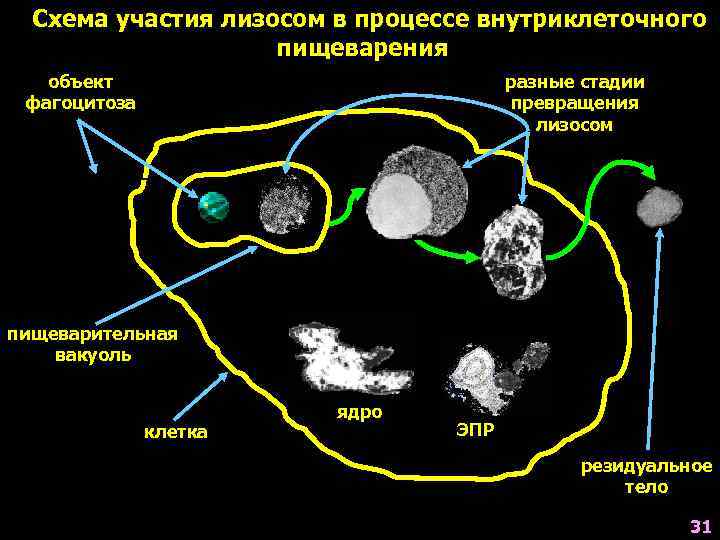 Схема участия лизосом в процессе внутриклеточного пищеварения объект фагоцитоза разные стадии превращения лизосом пищеварительная вакуоль клетка ядро ЭПР резидуальное тело 31
Схема участия лизосом в процессе внутриклеточного пищеварения объект фагоцитоза разные стадии превращения лизосом пищеварительная вакуоль клетка ядро ЭПР резидуальное тело 31
 Схема развития «болезней накопления» ГЕНЕТИЧЕСКИ ОБУСЛОВЛЕННОЕ ГИБЕЛЬ КЛЕТКИ НАРУШЕНИЕ СИНТЕЗА СООТВЕТСТВУЮЩЕГО ФЕРМЕНТА ЛИЗОСОМ 32
Схема развития «болезней накопления» ГЕНЕТИЧЕСКИ ОБУСЛОВЛЕННОЕ ГИБЕЛЬ КЛЕТКИ НАРУШЕНИЕ СИНТЕЗА СООТВЕТСТВУЮЩЕГО ФЕРМЕНТА ЛИЗОСОМ 32
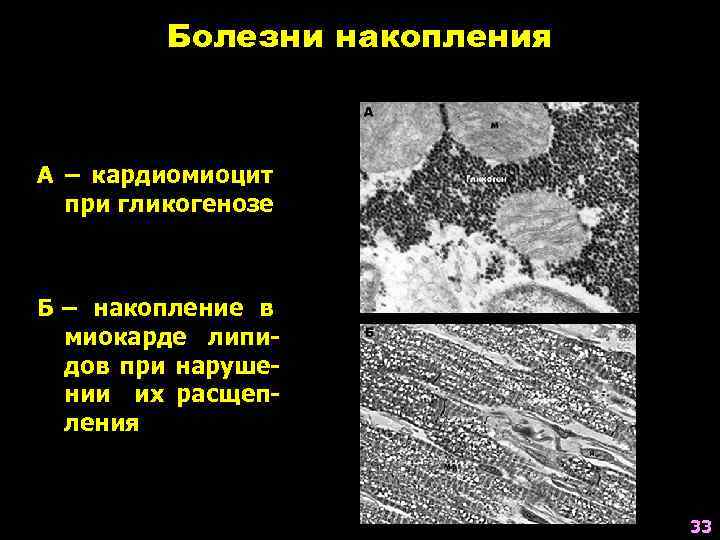 Болезни накопления А – кардиомиоцит при гликогенозе Б – накопление в миокарде липидов при нарушении их расщепления 33
Болезни накопления А – кардиомиоцит при гликогенозе Б – накопление в миокарде липидов при нарушении их расщепления 33
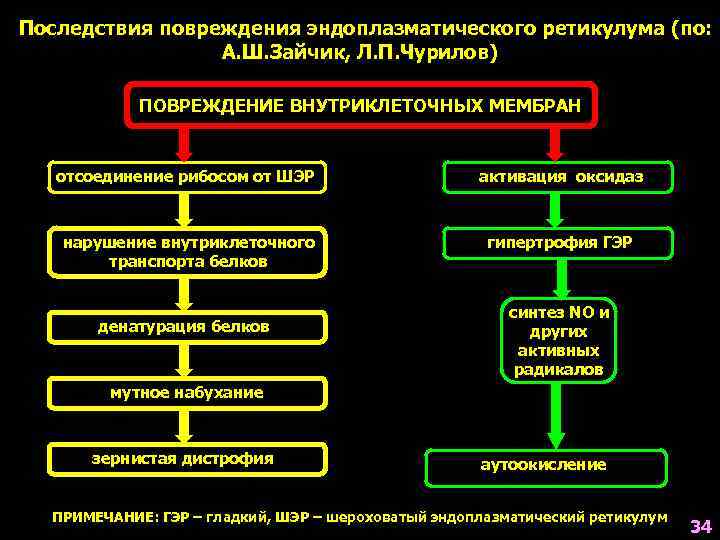 Последствия повреждения эндоплазматического ретикулума (по: А. Ш. Зайчик, Л. П. Чурилов) ПОВРЕЖДЕНИЕ ВНУТРИКЛЕТОЧНЫХ МЕМБРАН отсоединение рибосом от ШЭР активация оксидаз нарушение внутриклеточного транспорта белков гипертрофия ГЭР денатурация белков синтез NO и других активных радикалов мутное набухание зернистая дистрофия аутоокисление ПРИМЕЧАНИЕ: ГЭР – гладкий, ШЭР – шероховатый эндоплазматический ретикулум 34
Последствия повреждения эндоплазматического ретикулума (по: А. Ш. Зайчик, Л. П. Чурилов) ПОВРЕЖДЕНИЕ ВНУТРИКЛЕТОЧНЫХ МЕМБРАН отсоединение рибосом от ШЭР активация оксидаз нарушение внутриклеточного транспорта белков гипертрофия ГЭР денатурация белков синтез NO и других активных радикалов мутное набухание зернистая дистрофия аутоокисление ПРИМЕЧАНИЕ: ГЭР – гладкий, ШЭР – шероховатый эндоплазматический ретикулум 34
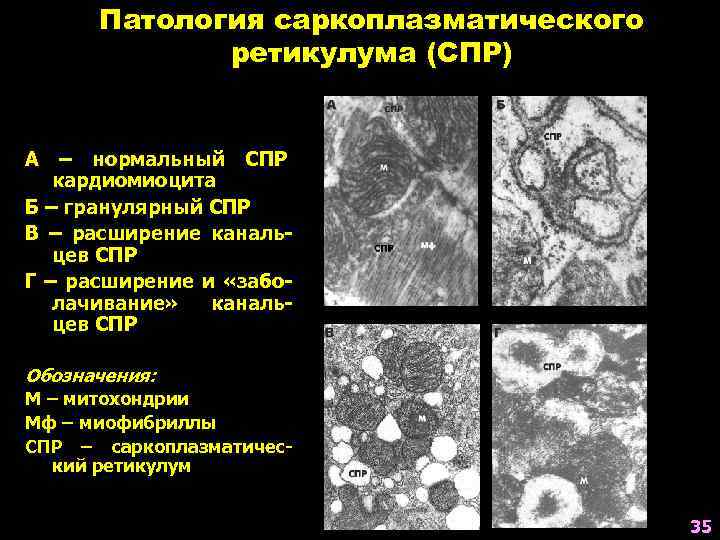 Патология саркоплазматического ретикулума (СПР) А – нормальный СПР кардиомиоцита Б – гранулярный СПР В – расширение канальцев СПР Г – расширение и «заболачивание» канальцев СПР Обозначения: М – митохондрии Мф – миофибриллы СПР – саркоплазматический ретикулум 35
Патология саркоплазматического ретикулума (СПР) А – нормальный СПР кардиомиоцита Б – гранулярный СПР В – расширение канальцев СПР Г – расширение и «заболачивание» канальцев СПР Обозначения: М – митохондрии Мф – миофибриллы СПР – саркоплазматический ретикулум 35
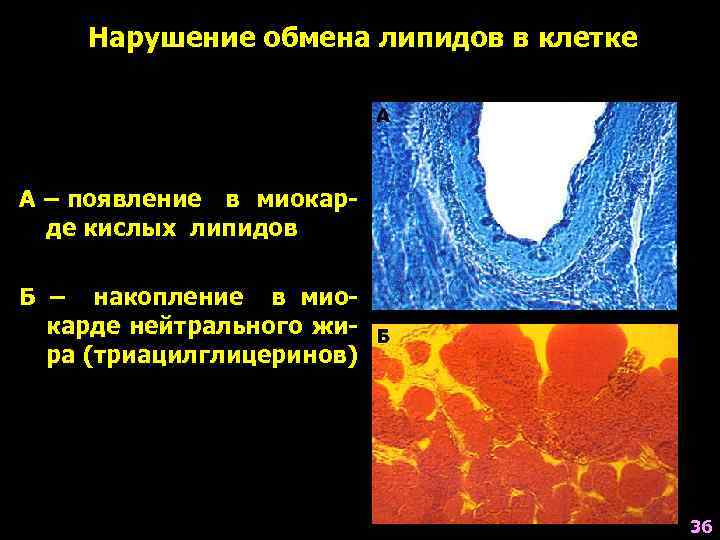 Нарушение обмена липидов в клетке А – появление в миокарде кислых липидов Б – накопление в миокарде нейтрального жира (триацилглицеринов) 36
Нарушение обмена липидов в клетке А – появление в миокарде кислых липидов Б – накопление в миокарде нейтрального жира (триацилглицеринов) 36
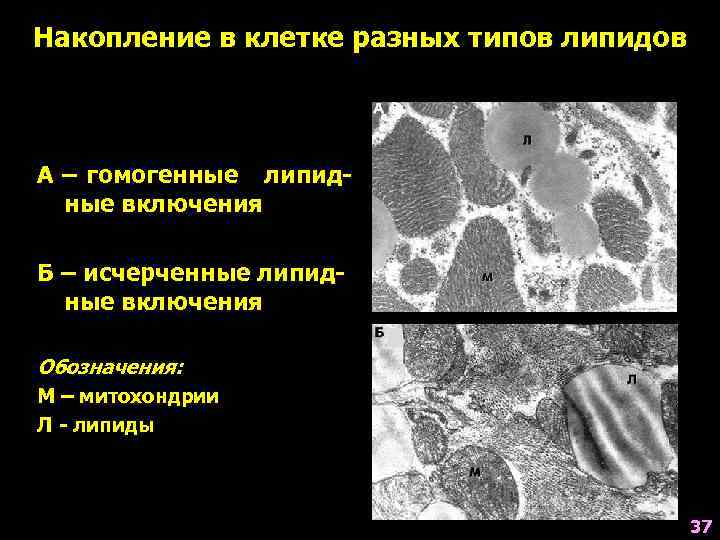 Накопление в клетке разных типов липидов А – гомогенные липидные включения Б – исчерченные липидные включения Обозначения: М – митохондрии Л - липиды 37
Накопление в клетке разных типов липидов А – гомогенные липидные включения Б – исчерченные липидные включения Обозначения: М – митохондрии Л - липиды 37
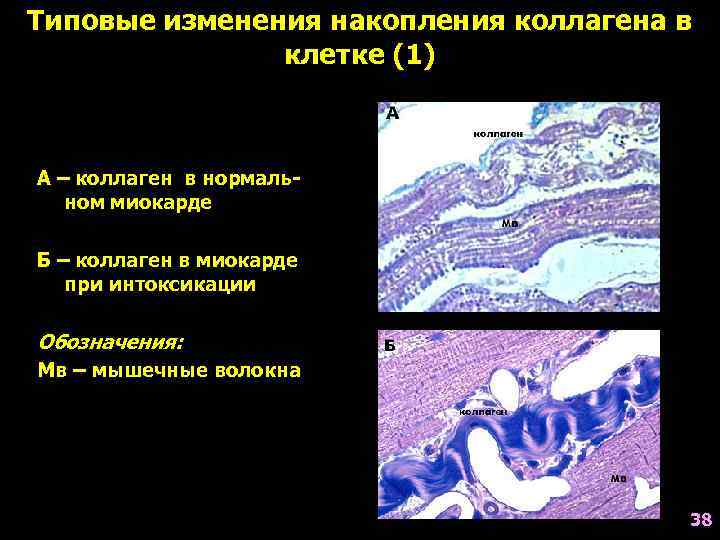 Типовые изменения накопления коллагена в клетке (1) А – коллаген в нормальном миокарде Б – коллаген в миокарде при интоксикации Обозначения: Мв – мышечные волокна 38
Типовые изменения накопления коллагена в клетке (1) А – коллаген в нормальном миокарде Б – коллаген в миокарде при интоксикации Обозначения: Мв – мышечные волокна 38
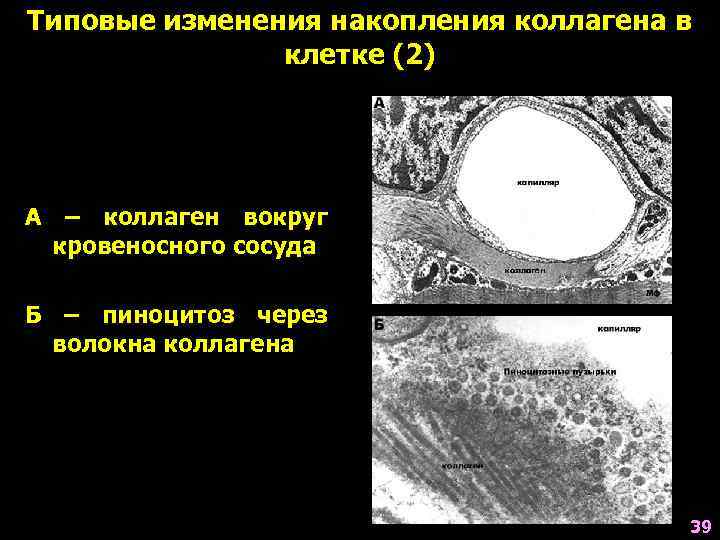 Типовые изменения накопления коллагена в клетке (2) А – коллаген вокруг кровеносного сосуда Б – пиноцитоз через волокна коллагена 39
Типовые изменения накопления коллагена в клетке (2) А – коллаген вокруг кровеносного сосуда Б – пиноцитоз через волокна коллагена 39
 Отек как типовая реакция клетки на повреждение А – внутриклеточный отек Б – внеклеточный отек 40
Отек как типовая реакция клетки на повреждение А – внутриклеточный отек Б – внеклеточный отек 40
 Все живое из клетки Теодор Шванн Omnis cellula e cellula Рудольф Вирхов 41
Все живое из клетки Теодор Шванн Omnis cellula e cellula Рудольф Вирхов 41


