2._Фураны_+_Тиофены.ppt
- Количество слайдов: 37
 02. 06. 10 Гетероциклические лекарственные средства Лекарственные средства, производные фурана доцент КФТХ к. х. н. Успенская Елена Валерьевна
02. 06. 10 Гетероциклические лекарственные средства Лекарственные средства, производные фурана доцент КФТХ к. х. н. Успенская Елена Валерьевна
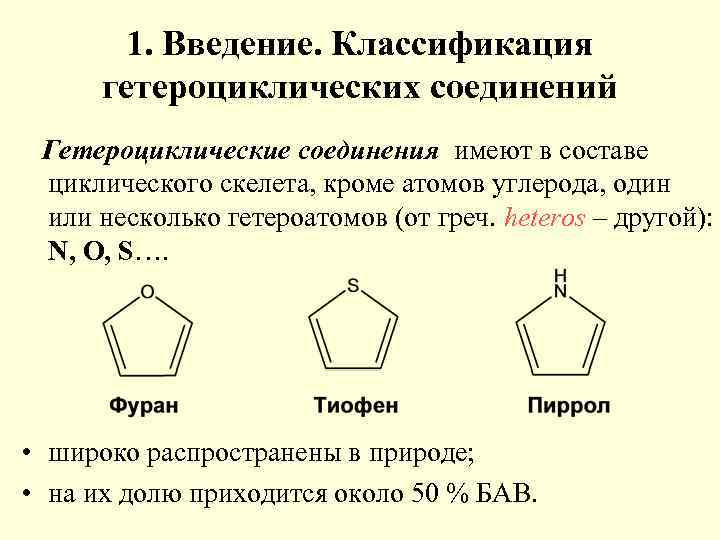 1. Введение. Классификация гетероциклических соединений Гетероциклические соединения имеют в составе циклического скелета, кроме атомов углерода, один или несколько гетероатомов (от греч. heteros – другой): N, O, S…. • широко распространены в природе; • на их долю приходится около 50 % БАВ.
1. Введение. Классификация гетероциклических соединений Гетероциклические соединения имеют в составе циклического скелета, кроме атомов углерода, один или несколько гетероатомов (от греч. heteros – другой): N, O, S…. • широко распространены в природе; • на их долю приходится около 50 % БАВ.
 2. Лекарственные средства, производные фурана 2. 1. Перечень программных ЛС: • Амиодарон; • Гризеофульвин. • ЛС нитрофуранового ряда: нитрофурал (фурацилин), фуразолидон, нитрофурантоин (фурадонин), фурагин. ! Синтезированы в Институте органической химии АН Латвии)
2. Лекарственные средства, производные фурана 2. 1. Перечень программных ЛС: • Амиодарон; • Гризеофульвин. • ЛС нитрофуранового ряда: нитрофурал (фурацилин), фуразолидон, нитрофурантоин (фурадонин), фурагин. ! Синтезированы в Институте органической химии АН Латвии)
 2. 2. Применение в медицине • Амиодарон (Кардиодарон. R)– анитиаритмическое ЛС – блокатор калиевых и кальциевых (в меньшей степени) каналов мембран кардиомиоцитов; обладает свойством вазодилататора (снижает сопротивление коронарных сосудов) • Гризеофульвин – антибиотическое ЛС- нарушает формирование и деление грибковой клетки. • Нитрофурал (фурацилин), фуразолидон, нитрофурантоин (фурадонин), фурагин – антибактериальные ЛС, молекулярные механизмы действия – нарушение синтеза ДНК и белка микробных клеток;
2. 2. Применение в медицине • Амиодарон (Кардиодарон. R)– анитиаритмическое ЛС – блокатор калиевых и кальциевых (в меньшей степени) каналов мембран кардиомиоцитов; обладает свойством вазодилататора (снижает сопротивление коронарных сосудов) • Гризеофульвин – антибиотическое ЛС- нарушает формирование и деление грибковой клетки. • Нитрофурал (фурацилин), фуразолидон, нитрофурантоин (фурадонин), фурагин – антибактериальные ЛС, молекулярные механизмы действия – нарушение синтеза ДНК и белка микробных клеток;
 2. 3. Химическое строение В основе химической структуры лежит пятичленный кислородсодержащий гетероцикл: ! • • • фуран Критерии ароматичности: Плоский циклический σ-скелет; Сопряженная замкнутая π-электронная система, охватывающая все атомы цикла; Число π электронов: 4 n+2π (правила Хюккеля). Фуран является ароматическим гетероциклическим соединением
2. 3. Химическое строение В основе химической структуры лежит пятичленный кислородсодержащий гетероцикл: ! • • • фуран Критерии ароматичности: Плоский циклический σ-скелет; Сопряженная замкнутая π-электронная система, охватывающая все атомы цикла; Число π электронов: 4 n+2π (правила Хюккеля). Фуран является ароматическим гетероциклическим соединением
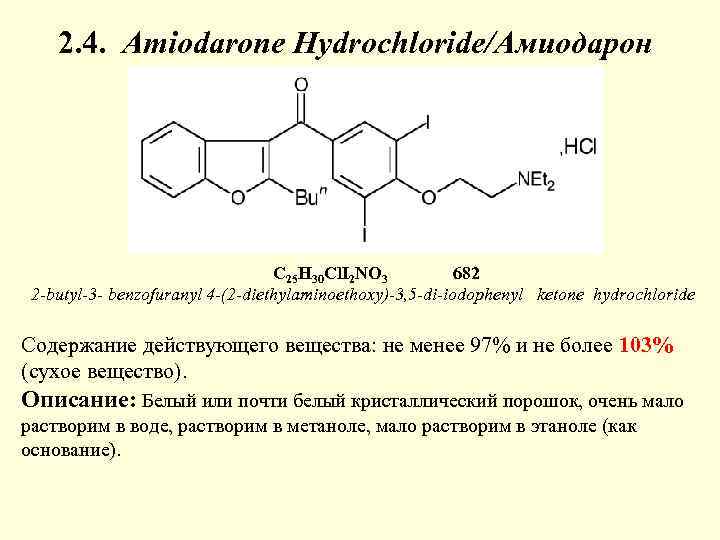 2. 4. Amiodarone Hydrochloride/Амиодарон C 25 H 30 Cl. I 2 NO 3 682 2 -butyl-3 - benzofuranyl 4 -(2 -diethylaminoethoxy)-3, 5 -di-iodophenyl ketone hydrochloride Содержание действующего вещества: не менее 97% и не более 103% (сухое вещество). Описание: Белый или почти белый кристаллический порошок, очень мало растворим в воде, растворим в метаноле, мало растворим в этаноле (как основание).
2. 4. Amiodarone Hydrochloride/Амиодарон C 25 H 30 Cl. I 2 NO 3 682 2 -butyl-3 - benzofuranyl 4 -(2 -diethylaminoethoxy)-3, 5 -di-iodophenyl ketone hydrochloride Содержание действующего вещества: не менее 97% и не более 103% (сухое вещество). Описание: Белый или почти белый кристаллический порошок, очень мало растворим в воде, растворим в метаноле, мало растворим в этаноле (как основание).
 2. 4. 1. Связь между структурой ЛВ и его свойствами. • Третичная алифатическая аминогруппа в боковой цепи придает молекуле основные свойства, следовательно, способность солеобразования и растворимость в воде. • Молекула амиодарона не является по структуре имином (щиффовым основанием), следовательно не имеет окраску. • Присутствие в молекуле эпокси- и простой эфирной- групп обусловливает значительную лабильность вещества Условия хранения: в хорошо укупоренных контейнерах, в защищенном от света месте, при температуре, не превышающей 30 0 С.
2. 4. 1. Связь между структурой ЛВ и его свойствами. • Третичная алифатическая аминогруппа в боковой цепи придает молекуле основные свойства, следовательно, способность солеобразования и растворимость в воде. • Молекула амиодарона не является по структуре имином (щиффовым основанием), следовательно не имеет окраску. • Присутствие в молекуле эпокси- и простой эфирной- групп обусловливает значительную лабильность вещества Условия хранения: в хорошо укупоренных контейнерах, в защищенном от света месте, при температуре, не превышающей 30 0 С.
 2. 4. 2. Подлинность (EPh) First identification (первостепенные способы): A, B, D. Second identification (второстепенные способы): A, C, D. A. Точка плавления: от 159°C дo 163°C. С. Метод ТСХ – Основное пятно на хроматограмме испытуемого раствора должно быть схожим по положению и размеру пятна, обнаруживаемого для раствора сравнения. Детектор – УФ-облучатель при 254 нм. D. ЛВ дает реакцию на хлориды. (It gives reaction (b) of chlorides).
2. 4. 2. Подлинность (EPh) First identification (первостепенные способы): A, B, D. Second identification (второстепенные способы): A, C, D. A. Точка плавления: от 159°C дo 163°C. С. Метод ТСХ – Основное пятно на хроматограмме испытуемого раствора должно быть схожим по положению и размеру пятна, обнаруживаемого для раствора сравнения. Детектор – УФ-облучатель при 254 нм. D. ЛВ дает реакцию на хлориды. (It gives reaction (b) of chlorides).
 ИК – спектрофотомерия (участок электромагнитного спектра в интервале от 0, 76 до ~ 1000 мкм). ! Инфракрасные спектры характеризуются сериями полос поглощения, определяемые волновым числом и интенсивностью. На оси абсцисс откладывается в линейной шкале значение волнового числа (см -1), на оси ординат - величина светопропускания Т (%). (А=lg 1/T) Диски с KBr: навеску твердого вещества (1 -3 мг) тщательно смешивают в вибромельнице или в ступке со спектроскопически чистым калия бромидом (150 -200 мг) и смесь прессуют. Спектр полученного образца получают относительно воздуха или относительно диска, приготовленного из чистого КВr, помещенного во второй канал прибора.
ИК – спектрофотомерия (участок электромагнитного спектра в интервале от 0, 76 до ~ 1000 мкм). ! Инфракрасные спектры характеризуются сериями полос поглощения, определяемые волновым числом и интенсивностью. На оси абсцисс откладывается в линейной шкале значение волнового числа (см -1), на оси ординат - величина светопропускания Т (%). (А=lg 1/T) Диски с KBr: навеску твердого вещества (1 -3 мг) тщательно смешивают в вибромельнице или в ступке со спектроскопически чистым калия бромидом (150 -200 мг) и смесь прессуют. Спектр полученного образца получают относительно воздуха или относительно диска, приготовленного из чистого КВr, помещенного во второй канал прибора.
 B. ИК-абсорбционный спектр амиодарона 15 % раствора в дихлорметане (диск с KBr) В ИК- спектре амиодарона появляются полосы поглощения, обусловленные: • валентными колебаниями (ν) сопряженных связей С=С в интервале частот 1585 -1620 см-1 ; • деформационными колебаниями (δ) связей С-Н в интервале частот 1430 -1470 см-1 ; • валентными колебаниями связей С-О (простые эфиры) в интервале частот 1050 -1280 см-1.
B. ИК-абсорбционный спектр амиодарона 15 % раствора в дихлорметане (диск с KBr) В ИК- спектре амиодарона появляются полосы поглощения, обусловленные: • валентными колебаниями (ν) сопряженных связей С=С в интервале частот 1585 -1620 см-1 ; • деформационными колебаниями (δ) связей С-Н в интервале частот 1430 -1470 см-1 ; • валентными колебаниями связей С-О (простые эфиры) в интервале частот 1050 -1280 см-1.
 2. 4. 3. Чистота ЛВ • Прозрачность раствора: раствор ЛВ в метаноле должен быть прозрачным и по цветности не превышать эталон. • p. H водного раствора от 3. 2 до 3. 8. • Related substances (родственные примеси): Метод ТСХ ( thin-layer chromatography), используя silica gel (силикагель) GF 254 в качестве неподвижной фазы.
2. 4. 3. Чистота ЛВ • Прозрачность раствора: раствор ЛВ в метаноле должен быть прозрачным и по цветности не превышать эталон. • p. H водного раствора от 3. 2 до 3. 8. • Related substances (родственные примеси): Метод ТСХ ( thin-layer chromatography), используя silica gel (силикагель) GF 254 в качестве неподвижной фазы.
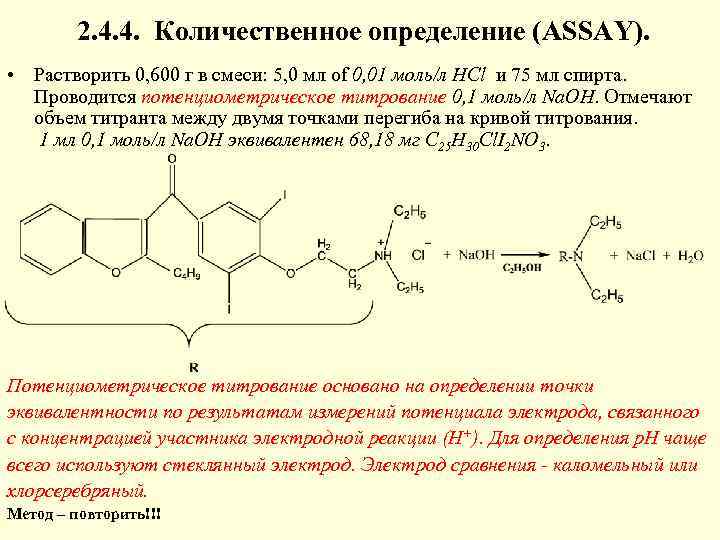 2. 4. 4. Количественное определение (ASSAY). • Растворить 0, 600 г в смеси: 5, 0 мл of 0, 01 моль/л HCl и 75 мл спирта. Проводится потенциометрическое титрование 0, 1 моль/л Na. OH. Отмечают объем титранта между двумя точками перегиба на кривой титрования. 1 мл 0, 1 моль/л Na. OH эквивалентен 68, 18 мг C 25 H 30 Cl. I 2 NO 3. Потенциометрическое титрование основано на определении точки эквивалентности по результатам измерений потенциала электрода, связанного с концентрацией участника электродной реакции (Н+). Для определения р. Н чаще всего используют стеклянный электрод. Электрод сравнения - каломельный или хлорсеребряный. Метод – повторить!!!
2. 4. 4. Количественное определение (ASSAY). • Растворить 0, 600 г в смеси: 5, 0 мл of 0, 01 моль/л HCl и 75 мл спирта. Проводится потенциометрическое титрование 0, 1 моль/л Na. OH. Отмечают объем титранта между двумя точками перегиба на кривой титрования. 1 мл 0, 1 моль/л Na. OH эквивалентен 68, 18 мг C 25 H 30 Cl. I 2 NO 3. Потенциометрическое титрование основано на определении точки эквивалентности по результатам измерений потенциала электрода, связанного с концентрацией участника электродной реакции (Н+). Для определения р. Н чаще всего используют стеклянный электрод. Электрод сравнения - каломельный или хлорсеребряный. Метод – повторить!!!
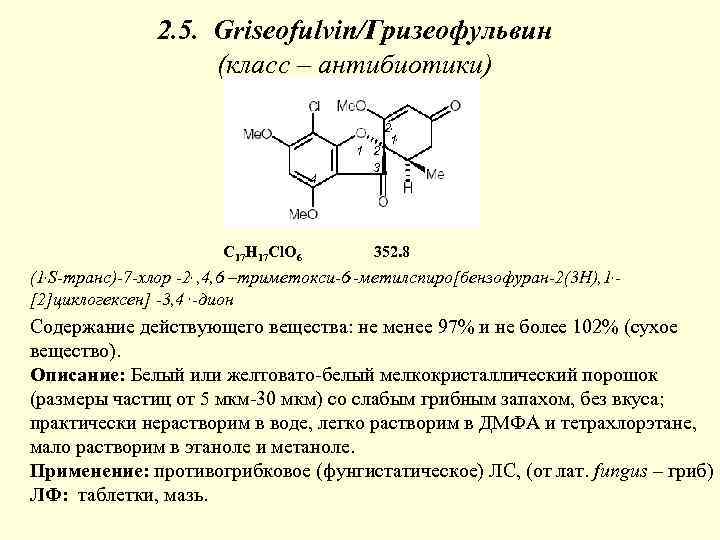 2. 5. Griseofulvin/Гризеофульвин (класс – антибиотики) 4 C 17 H 17 Cl. O 6 1 2 3 2, 1, 352. 8 (1, S-транс)-7 -хлор -2, , 4, 6 –триметокси-6, -метилспиро[бензофуран-2(3 Н), 1, [2]циклогексен] -3, 4 , -дион Содержание действующего вещества: не менее 97% и не более 102% (сухое вещество). Описание: Белый или желтовато-белый мелкокристаллический порошок (размеры частиц от 5 мкм-30 мкм) со слабым грибным запахом, без вкуса; практически нерастворим в воде, легко растворим в ДМФА и тетрахлорэтане, мало растворим в этаноле и метаноле. Применение: противогрибковое (фунгистатическое) ЛС, (от лат. fungus – гриб) ЛФ: таблетки, мазь.
2. 5. Griseofulvin/Гризеофульвин (класс – антибиотики) 4 C 17 H 17 Cl. O 6 1 2 3 2, 1, 352. 8 (1, S-транс)-7 -хлор -2, , 4, 6 –триметокси-6, -метилспиро[бензофуран-2(3 Н), 1, [2]циклогексен] -3, 4 , -дион Содержание действующего вещества: не менее 97% и не более 102% (сухое вещество). Описание: Белый или желтовато-белый мелкокристаллический порошок (размеры частиц от 5 мкм-30 мкм) со слабым грибным запахом, без вкуса; практически нерастворим в воде, легко растворим в ДМФА и тетрахлорэтане, мало растворим в этаноле и метаноле. Применение: противогрибковое (фунгистатическое) ЛС, (от лат. fungus – гриб) ЛФ: таблетки, мазь.
 2. 5. 1. Связь между структурой ЛВ и его свойствами. Молекулы существуют и вступают в химические превращения в трехмерном пространстве как стериоизомеры (изомеры, отличающиеся расположением атомов в пространстве). R, S-система для обозначения конфигурации ассиметрических атомов углерода (1951). От лат rectus – правый, sinister-левый. • Присутствие в молекуле метокси-, кето-, эпокси-групп и Hal обусловливает лабильность лекарственного вещества (способность к Ox/Red реакциям).
2. 5. 1. Связь между структурой ЛВ и его свойствами. Молекулы существуют и вступают в химические превращения в трехмерном пространстве как стериоизомеры (изомеры, отличающиеся расположением атомов в пространстве). R, S-система для обозначения конфигурации ассиметрических атомов углерода (1951). От лат rectus – правый, sinister-левый. • Присутствие в молекуле метокси-, кето-, эпокси-групп и Hal обусловливает лабильность лекарственного вещества (способность к Ox/Red реакциям).
 2. 5. 4. Количественное определение УФ-спеткрометрия при аналитической длине волны 291 нм. Удельное поглощение (Е 1%1 см = 686). 1% A=E C х- ? 1 см · Cх · l
2. 5. 4. Количественное определение УФ-спеткрометрия при аналитической длине волны 291 нм. Удельное поглощение (Е 1%1 см = 686). 1% A=E C х- ? 1 см · Cх · l
 2. 6. Общая формула ЛС анибактериального действия, производных фурана - NO 2 - нитро-группа; - CH=N- иминная группа; - О - эпокси-группа.
2. 6. Общая формула ЛС анибактериального действия, производных фурана - NO 2 - нитро-группа; - CH=N- иминная группа; - О - эпокси-группа.
 Где: -R= - фурацилин семикарбазид -R= - фуразолидон 3 -аминооксазолидон-2 -R= 1 -аминогидантоин - фурадонин
Где: -R= - фурацилин семикарбазид -R= - фуразолидон 3 -аминооксазолидон-2 -R= 1 -аминогидантоин - фурадонин
 2. 6. 2. Описание ЛВ нитрофуранового ряда • желтые (оранжево-желтые) кристаллические порошки. • Имины – мало устойчивые, быстро разлагающиеся соединения, но ароматические производные более устойчивы). • Хранение ЛС: в хорошо укупоренной таре, защищающей от действия света.
2. 6. 2. Описание ЛВ нитрофуранового ряда • желтые (оранжево-желтые) кристаллические порошки. • Имины – мало устойчивые, быстро разлагающиеся соединения, но ароматические производные более устойчивы). • Хранение ЛС: в хорошо укупоренной таре, защищающей от действия света.
 2. 7. Nitrofurazone/Nitrofural/Фурацилин C 6 H 6 N 4 O 4 198. 1 5 -nitro-2 -furaldehyde semicarbazone Содержание действующего вещества: не менее 97% и не более 103%. Описание (EPh 2006): желтый или коричнево-желтый кристаллический порошок, очень мало растворим в воде (1 г субстанции растворяется в объеме растворителя от 100 мл до 1000 мл); мало растворим в спирте; практически не растворим в эфире. Применение: антибактериальное, противопротозойное ЛС
2. 7. Nitrofurazone/Nitrofural/Фурацилин C 6 H 6 N 4 O 4 198. 1 5 -nitro-2 -furaldehyde semicarbazone Содержание действующего вещества: не менее 97% и не более 103%. Описание (EPh 2006): желтый или коричнево-желтый кристаллический порошок, очень мало растворим в воде (1 г субстанции растворяется в объеме растворителя от 100 мл до 1000 мл); мало растворим в спирте; практически не растворим в эфире. Применение: антибактериальное, противопротозойное ЛС
 2. 7. 1. Кислотно-основные свойства фурацилина Порядок возрастания кислотности по Брёнстеду: CH-кислота
2. 7. 1. Кислотно-основные свойства фурацилина Порядок возрастания кислотности по Брёнстеду: CH-кислота
 • Группа -NO 2 проявляет – М эффект, понижает электронную плотность в сопряженной системе и определяет способность ЛВ растворяться в растворах щелочей с образованием нитронатов. нитронат натрия • -N иминной группы придает основный характер. фурацилин является амфолитом
• Группа -NO 2 проявляет – М эффект, понижает электронную плотность в сопряженной системе и определяет способность ЛВ растворяться в растворах щелочей с образованием нитронатов. нитронат натрия • -N иминной группы придает основный характер. фурацилин является амфолитом
 2. 7. 2. Идентификация Eph: First identification (первостепенный способ): B- ИК – спектрофотомерия. Second identification (второстепенные способы): A, С, D.
2. 7. 2. Идентификация Eph: First identification (первостепенный способ): B- ИК – спектрофотомерия. Second identification (второстепенные способы): A, С, D.
 Способ А: УФ- спектрофотометрия В основе спектрофотометрических измерений и расчетов лежит закон, характеризующий зависимость поглощения монохроматического излучения от толщины поглощающего слоя и от концентрации анализируемого раствора (закон Бугера-Ламберта-Бера), который можно представить в логарифмической форме: A=εlc, Где А - абсорбция (экстинкция, поглощение) ε=k/2, 3 - молярный коэффициент экстинкции (л·моль-1·см-1). (Численно молярный коэффициент экстинкции равен абсорбции при концентрации анализируемого раствора с = 1 моль/л и толщине поглощающего слоя l= 1 см).
Способ А: УФ- спектрофотометрия В основе спектрофотометрических измерений и расчетов лежит закон, характеризующий зависимость поглощения монохроматического излучения от толщины поглощающего слоя и от концентрации анализируемого раствора (закон Бугера-Ламберта-Бера), который можно представить в логарифмической форме: A=εlc, Где А - абсорбция (экстинкция, поглощение) ε=k/2, 3 - молярный коэффициент экстинкции (л·моль-1·см-1). (Численно молярный коэффициент экстинкции равен абсорбции при концентрации анализируемого раствора с = 1 моль/л и толщине поглощающего слоя l= 1 см).
 Eph: • Абсорбция раствора имеет два максимума: при 260 нм и 375 нм. • Отношение абсорбции, измеренной при 375 нм к абсорбции, измеренной при 260 nm, составляет от 1, 15 до 1, 30. ! (Идентификация ЛС по определению отношения величин поглощения при двух максимумах (λ мах) «уменьшает влияние переменных характеристик прибора на испытание и исключает использование стандартного образца» ).
Eph: • Абсорбция раствора имеет два максимума: при 260 нм и 375 нм. • Отношение абсорбции, измеренной при 375 нм к абсорбции, измеренной при 260 nm, составляет от 1, 15 до 1, 30. ! (Идентификация ЛС по определению отношения величин поглощения при двух максимумах (λ мах) «уменьшает влияние переменных характеристик прибора на испытание и исключает использование стандартного образца» ).
 Способ С: метод ТСХ (хроматография в тонком слое сорбента) с использованием силикагеля в качестве неподвижной фазы. Способ D: «Dissolve about 1 mg in 1 ml of dimethylformamide R and add 0. 1 ml of alcoholic potassium hydroxide solution R. A violet-red colour is produced. » фурацилин нитронат натрия (фиолетово-красный) (оранжево-красный) в случае Na. OH
Способ С: метод ТСХ (хроматография в тонком слое сорбента) с использованием силикагеля в качестве неподвижной фазы. Способ D: «Dissolve about 1 mg in 1 ml of dimethylformamide R and add 0. 1 ml of alcoholic potassium hydroxide solution R. A violet-red colour is produced. » фурацилин нитронат натрия (фиолетово-красный) (оранжево-красный) в случае Na. OH
 Взаимодействие ЛВ, производных фурана, с концентрированным щелочами приводит к разрыву фуранового цикла и боковой цепи с образованием различных продуктов разложения: Гидролитическое расщепление ЛВ в щелочной среде:
Взаимодействие ЛВ, производных фурана, с концентрированным щелочами приводит к разрыву фуранового цикла и боковой цепи с образованием различных продуктов разложения: Гидролитическое расщепление ЛВ в щелочной среде:
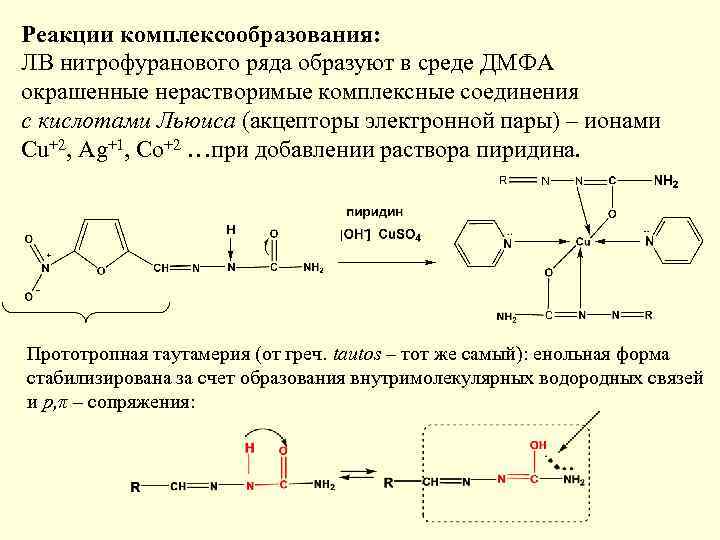 Реакции комплексообразования: ЛВ нитрофуранового ряда образуют в среде ДМФА окрашенные нерастворимые комплексные соединения с кислотами Льюиса (акцепторы электронной пары) – ионами Cu+2, Ag+1, Co+2 …при добавлении раствора пиридина. Прототропная таутамерия (от греч. tautos – тот же самый): енольная форма стабилизирована за счет образования внутримолекулярных водородных связей и p, π – сопряжения:
Реакции комплексообразования: ЛВ нитрофуранового ряда образуют в среде ДМФА окрашенные нерастворимые комплексные соединения с кислотами Льюиса (акцепторы электронной пары) – ионами Cu+2, Ag+1, Co+2 …при добавлении раствора пиридина. Прототропная таутамерия (от греч. tautos – тот же самый): енольная форма стабилизирована за счет образования внутримолекулярных водородных связей и p, π – сопряжения:
 2. 7. 3. Испытания на чистоту: • p. H: To 1. 0 g add 100 ml of carbon dioxide-free water R. Shake and filter. The p. H of the filtrate is 5. 0 to 7. 0. • Related substances (родственные вещества) - Examine by liquid chromatography. A. 5 -nitro-2 -furaldehyde azine B. (5 -nitro-2 -furyl)methylene diacetate • Sulphated ash Not more than 0. 1 per cent, determined on 1. 0 g.
2. 7. 3. Испытания на чистоту: • p. H: To 1. 0 g add 100 ml of carbon dioxide-free water R. Shake and filter. The p. H of the filtrate is 5. 0 to 7. 0. • Related substances (родственные вещества) - Examine by liquid chromatography. A. 5 -nitro-2 -furaldehyde azine B. (5 -nitro-2 -furyl)methylene diacetate • Sulphated ash Not more than 0. 1 per cent, determined on 1. 0 g.
 2. 7. 4. Количественное определение: Физико-химические методы: УФ спектрофотометрия (Eph). Метод «одного стандарта» , λmax = 375 нм. Принцип: • Испытуемый раствор (test solution) и раствор сравнения (reference solution) готовят одинаковым способом. • Испытания проводятся в одних условиях. • Количественный расчет осуществляется по закону Бугера. Ламберта-Бера для обоих растворов: Ast=εlcst Ax=εlcx !!! Вывести формулу для расчета cx
2. 7. 4. Количественное определение: Физико-химические методы: УФ спектрофотометрия (Eph). Метод «одного стандарта» , λmax = 375 нм. Принцип: • Испытуемый раствор (test solution) и раствор сравнения (reference solution) готовят одинаковым способом. • Испытания проводятся в одних условиях. • Количественный расчет осуществляется по закону Бугера. Ламберта-Бера для обоих растворов: Ast=εlcst Ax=εlcx !!! Вывести формулу для расчета cx
 1. Производные тиофена. 1. 1. Строение. • Тиофен - бесцветная жидкость с запахом бензина; • Обладает выраженными ароматическими свойствами; • Гетероатом в положении « 1» повышает электронную плотность в сопряженной системе (+М) за счет ρ, π-сопряжения; • Облегчаются реакции SE (по сравнению с бензолом) в положениях α и α’.
1. Производные тиофена. 1. 1. Строение. • Тиофен - бесцветная жидкость с запахом бензина; • Обладает выраженными ароматическими свойствами; • Гетероатом в положении « 1» повышает электронную плотность в сопряженной системе (+М) за счет ρ, π-сопряжения; • Облегчаются реакции SE (по сравнению с бензолом) в положениях α и α’.
![1. 2. Ticlopidine Hydrochloride/Тиклопидина г/хл Торговые названия: Тиклид, Тикло 5 -[2 -Хлорфенил)метил]-4, 5, 6, 1. 2. Ticlopidine Hydrochloride/Тиклопидина г/хл Торговые названия: Тиклид, Тикло 5 -[2 -Хлорфенил)метил]-4, 5, 6,](https://present5.com/presentation/-46003468_138688762/image-31.jpg) 1. 2. Ticlopidine Hydrochloride/Тиклопидина г/хл Торговые названия: Тиклид, Тикло 5 -[2 -Хлорфенил)метил]-4, 5, 6, 7 -тетрагидротиено[3, 2 -c]пиридина гидрохлорид • Содержание действующего вещества: не менее 99, 0% и не более 101, 0%. • Описание: белый или почти белый кристаллический порошок, легко растворим в воде, метаноле, умеренно растворим в метиленхлориде и этаноле, трудно растворим в ацетоне. • Применение: антитромботическое, антиагрегационное ЛС
1. 2. Ticlopidine Hydrochloride/Тиклопидина г/хл Торговые названия: Тиклид, Тикло 5 -[2 -Хлорфенил)метил]-4, 5, 6, 7 -тетрагидротиено[3, 2 -c]пиридина гидрохлорид • Содержание действующего вещества: не менее 99, 0% и не более 101, 0%. • Описание: белый или почти белый кристаллический порошок, легко растворим в воде, метаноле, умеренно растворим в метиленхлориде и этаноле, трудно растворим в ацетоне. • Применение: антитромботическое, антиагрегационное ЛС
 1. 3. Связь между структурой ЛВ и его свойствами. • Атом N в положении « 5» бицикла – тиенотетрагидропиридина- обусловливает основные свойства молекулы тиклопидина способность образовывать растворимые в воде соли; • Атом S в положении « 1» облегчает реакции SE в положении «α» ; • Присутствие в структуре молекулы атомов Hal и гетероатомов обусловливает идентификацию после минерализации ЛВ.
1. 3. Связь между структурой ЛВ и его свойствами. • Атом N в положении « 5» бицикла – тиенотетрагидропиридина- обусловливает основные свойства молекулы тиклопидина способность образовывать растворимые в воде соли; • Атом S в положении « 1» облегчает реакции SE в положении «α» ; • Присутствие в структуре молекулы атомов Hal и гетероатомов обусловливает идентификацию после минерализации ЛВ.
 1. 4. Идентификация ЛВ А. ИК-спектрофотометрия; В. Определение ионов Cl- JP XIV, First identification Eph Second identification Eph: А. УФ-спектрофотометрия: 0, 04% водный раствор характеризуется λ 1 max=268 нм и λ 2 max=375 нм. Отношение абсорбции, измеренной при 268 нм к абсорбции, измеренной при 375 нм, составляет от 1, 1 до 1, 2.
1. 4. Идентификация ЛВ А. ИК-спектрофотометрия; В. Определение ионов Cl- JP XIV, First identification Eph Second identification Eph: А. УФ-спектрофотометрия: 0, 04% водный раствор характеризуется λ 1 max=268 нм и λ 2 max=375 нм. Отношение абсорбции, измеренной при 268 нм к абсорбции, измеренной при 375 нм, составляет от 1, 1 до 1, 2.
 • С. Химический метод: нагревание при 80 0 С на водяной бане смеси, состоящей из 6 мг лимонной кислоты, 0, 3 мл уксусного ангидрида и 5 мг субстанции ЛВ, приводит к появлению красного окрашивания.
• С. Химический метод: нагревание при 80 0 С на водяной бане смеси, состоящей из 6 мг лимонной кислоты, 0, 3 мл уксусного ангидрида и 5 мг субстанции ЛВ, приводит к появлению красного окрашивания.
 1. 5. Чистота ЛС При проведении фармацевтического анализа контролируют: • Прозрачность и цветность (раствор ЛВ в 1% НСl должен быть прозрачным и б/цв); • Кислотность: р. Н раствора - от 3, 5 до 4. 0; • Родственные примеси (ТСХ); • Потеря при высушивании; • Сульфатная зола; • Тяжелые металлы.
1. 5. Чистота ЛС При проведении фармацевтического анализа контролируют: • Прозрачность и цветность (раствор ЛВ в 1% НСl должен быть прозрачным и б/цв); • Кислотность: р. Н раствора - от 3, 5 до 4. 0; • Родственные примеси (ТСХ); • Потеря при высушивании; • Сульфатная зола; • Тяжелые металлы.
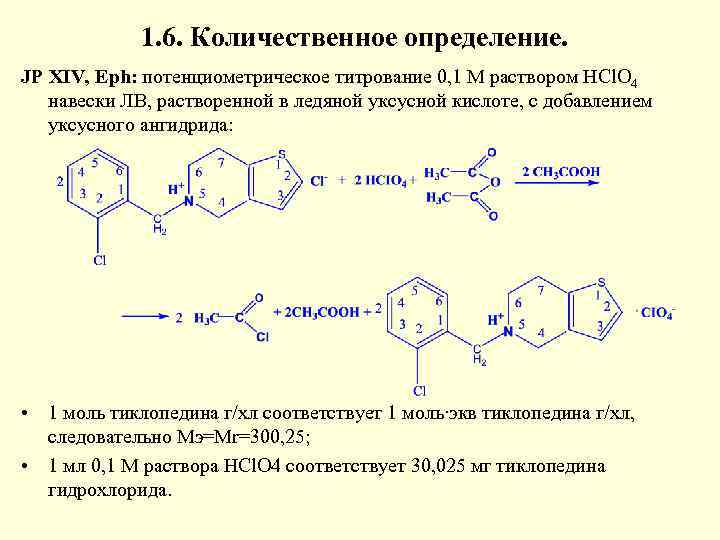 1. 6. Количественное определение. JP XIV, Eph: потенциометрическое титрование 0, 1 М раствором HCl. O 4 навески ЛВ, растворенной в ледяной уксусной кислоте, с добавлением уксусного ангидрида: • 1 моль тиклопедина г/хл соответствует 1 моль∙экв тиклопедина г/хл, следовательно Мэ=Мr=300, 25; • 1 мл 0, 1 М раствора HCl. O 4 соответствует 30, 025 мг тиклопедина гидрохлорида.
1. 6. Количественное определение. JP XIV, Eph: потенциометрическое титрование 0, 1 М раствором HCl. O 4 навески ЛВ, растворенной в ледяной уксусной кислоте, с добавлением уксусного ангидрида: • 1 моль тиклопедина г/хл соответствует 1 моль∙экв тиклопедина г/хл, следовательно Мэ=Мr=300, 25; • 1 мл 0, 1 М раствора HCl. O 4 соответствует 30, 025 мг тиклопедина гидрохлорида.
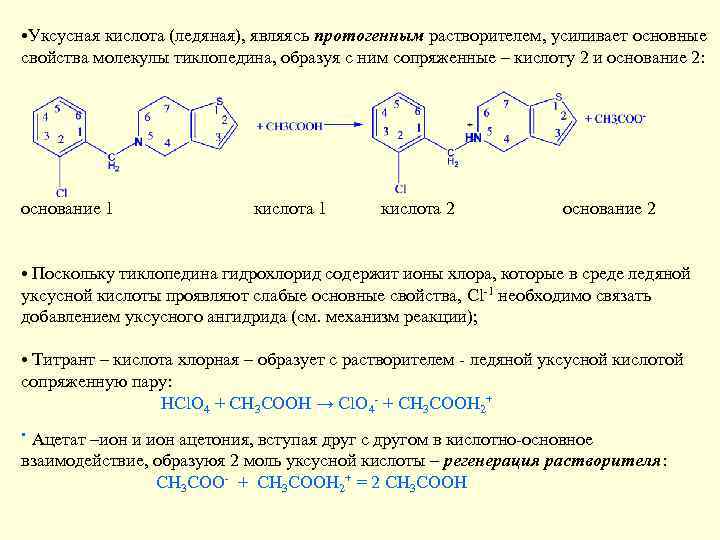 • Уксусная кислота (ледяная), являясь протогенным растворителем, усиливает основные свойства молекулы тиклопедина, образуя с ним сопряженные – кислоту 2 и основание 2: основание 1 кислота 2 основание 2 • Поскольку тиклопедина гидрохлорид содержит ионы хлора, которые в среде ледяной уксусной кислоты проявляют слабые основные свойства, Cl-1 необходимо связать добавлением уксусного ангидрида (см. механизм реакции); • Титрант – кислота хлорная – образует с растворителем - ледяной уксусной кислотой сопряженную пару: HCl. O 4 + CH 3 COOH → Cl. O 4 - + CH 3 COOH 2+ • Ацетат –ион и ион ацетония, вступая друг с другом в кислотно-основное взаимодействие, образуюя 2 моль уксусной кислоты – регенерация растворителя: CH 3 COO- + CH 3 COOH 2+ = 2 CH 3 COOH
• Уксусная кислота (ледяная), являясь протогенным растворителем, усиливает основные свойства молекулы тиклопедина, образуя с ним сопряженные – кислоту 2 и основание 2: основание 1 кислота 2 основание 2 • Поскольку тиклопедина гидрохлорид содержит ионы хлора, которые в среде ледяной уксусной кислоты проявляют слабые основные свойства, Cl-1 необходимо связать добавлением уксусного ангидрида (см. механизм реакции); • Титрант – кислота хлорная – образует с растворителем - ледяной уксусной кислотой сопряженную пару: HCl. O 4 + CH 3 COOH → Cl. O 4 - + CH 3 COOH 2+ • Ацетат –ион и ион ацетония, вступая друг с другом в кислотно-основное взаимодействие, образуюя 2 моль уксусной кислоты – регенерация растворителя: CH 3 COO- + CH 3 COOH 2+ = 2 CH 3 COOH


