5e59d3a38ec0db1d0e2c363697ef7b90.ppt
- Количество слайдов: 30

제네릭 의약품의 개발전략 - Hatch-Waxman 소송 사례 분석 - 특허청 약품화학심사팀장 윤경애

목 차 1 2 제네릭 의약품의 개발 과정 3 2007 윤경애 특허제도 및 Hatch-Waxman 법 Hatch-Waxman 소송 사례 분석 2

특허제도의 기본원리 특허법 제 1조 (목적 ) 이 법은 발명을 보호·장려하고 그 이용을 도모함으로써 기술의 발전을 촉진하여 산업발전에 이바지함을 목적으로 한다. 私 益 특허발명에 대하여 독점 배타적 특허권 부여 2007 윤경애 公益 공개된 특허정보를 이용한 신기술 개발 촉진 3
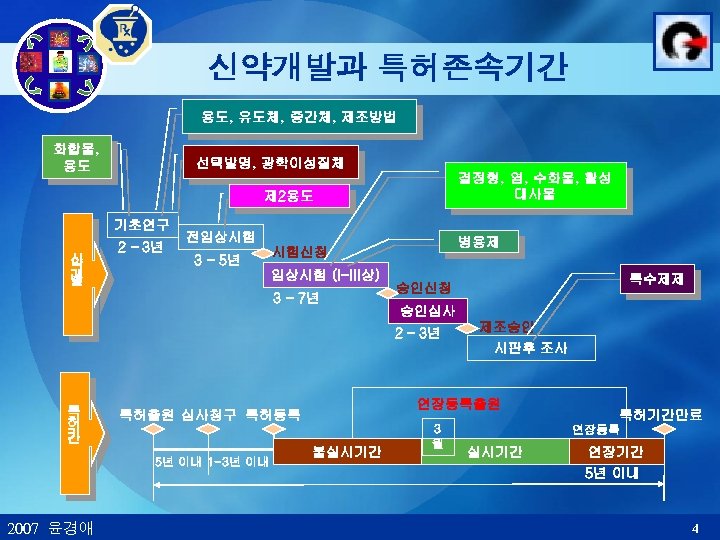
신약개발과 특허존속기간 용도, 유도체, 중간체, 제조방법 화합물, 용도 선택발명, 광학이성질체 결정형, 염, 수화물, 활성 대사물 제 2용도 기초연구 신 약 개 발 2 – 3년 전임상시험 3 – 5년 병용제 시험신청 임상시험 (I-III상) 3 – 7년 특수제제 승인신청 승인심사 2 – 3년 제조승인 시판후 조사 특 허 기 간 5년 이내 1 -3년 이내 2007 윤경애 연장등록출원 특허출원 심사청구 특허등록 불실시기간 3 월 특허기간만료 연장등록 실시기간 연장기간 5년 이내 4
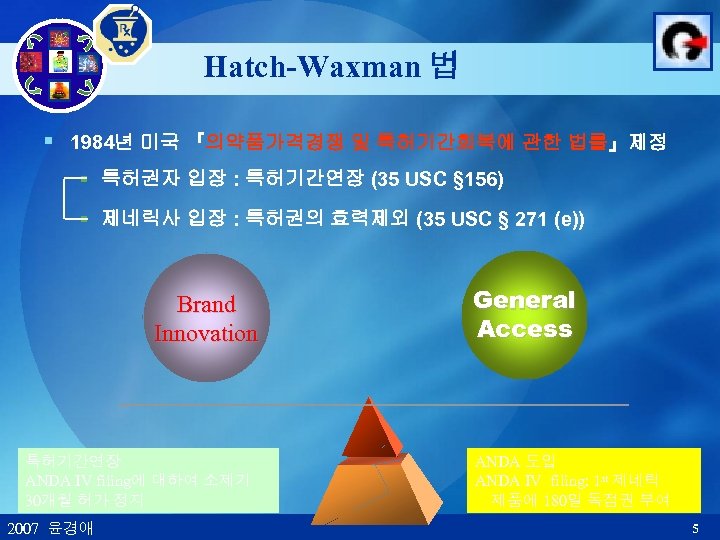
Hatch-Waxman 법 § 1984년 미국 『의약품가격경쟁 및 특허기간회복에 관한 법률』제정 § 특허권자 입장 : 특허기간연장 (35 USC § 156) § 제네릭사 입장 : 특허권의 효력제외 (35 USC § 271 (e)) Brand Innovation 특허기간연장 ANDA IV filing에 대하여 소제기 30개월 허가 정지 2007 윤경애 General Access ANDA 도입 ANDA IV filing: 1 st 제네릭 제품에 180일 독점권 부여 5
제네릭 의약품 시장 § 제네릭 의약품의 가격은 브랜드와 비교하여 평균 30~80% 저렴 § 미국 처방전에서 제네릭 의약품의 시장점유율 § 1984년 19% § 2002년 47% § 2005년 56% § 1998년 미국 : 제네릭 의약품으로 매년 $8 -10 billion 절약 특허만료 예정 브랜드 의약품의 가격 2007년 : $27 billion 2008년 : $29 billion 2007 윤경애 6

제네릭 의약품 개발과 개량신약 § 제네릭 의약품의 개발은 활성약물의 제조방법, 제형 등의 개발 유도 § 제네릭사는 활성약물의 새로운 결정 등의 개량기술관련 특허획득 및 Sup 2007 윤경애 7

제네릭 의약품의 개발 과정 초기 개발 단계부터 시장진입까지 소요되는 평균 기간 : Patent Search & Analysis 5 - 7 years • Type of IP : multiple databases 제네릭 의약품의 개발 단계 1 - 특허맵 분석(기술동향, • Time (until expiry) 기업분석, 존속기간), - 시장규모 파악 • Territory 2 타겟 제품 선정 및 API 공급사 파악 • Terminated 3 • Technical scope of the monopoly 4 • True monopoly (validity) Testing for Pharmaceutical Equivalence & 5 Formulation Experimentation Bio Equivalence Submission - include historical IP rights To find all relevant patents, an 특허관련 대응책 특허exact(특허 침해성 및 무효성 검색) 평가 disclosure or a general sample within the subject - 침해를 회피할 수 있는 API/제조방법 개발 matter scope - 특허 무효 전략 - 침해를 회피할 수 있는 제형/제조방법 개발 - 특허 무효 전략 6 Preparation of certification - 침해를 회피할 수 있는 용도특허 개발 - 특허무효 전략 Address all listed patents 7 Litigation 신규 특허 모니터링 검색 - State of the Art 2007 윤경애 8

Drug lifecycle Management • Branding : 브랜드의 가치 • Product Support • Trade relationship • Manufacturing cost advantage • Product improvements Patent • Product line extensions 2007 윤경애 9
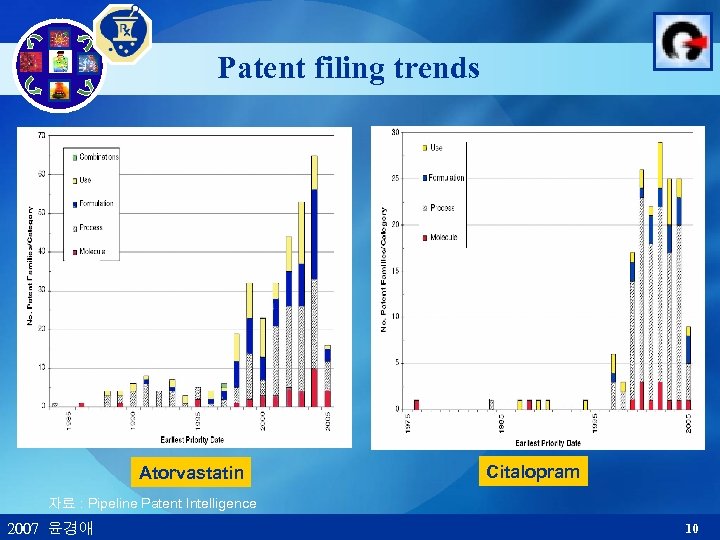
Patent filing trends Atorvastatin Citalopram 자료 : Pipeline Patent Intelligence 2007 윤경애 10
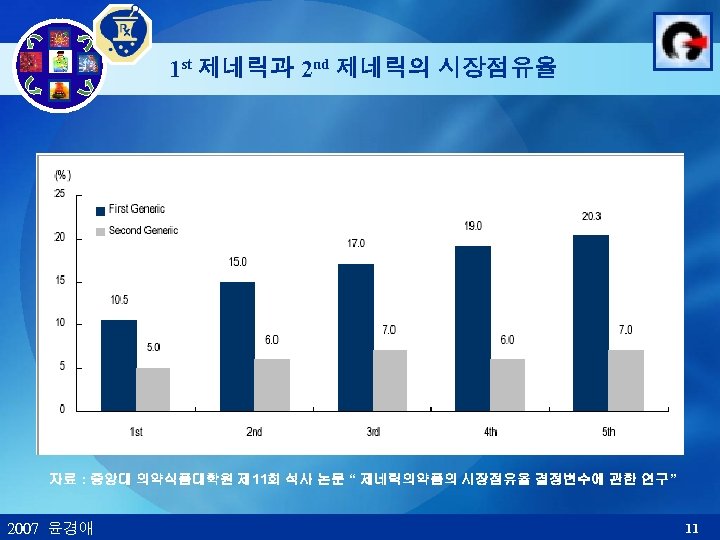
1 st 제네릭과 2 nd 제네릭의 시장점유율 자료 : 중앙대 의약식품대학원 제 11회 석사 논문 “ 제네릭의약품의 시장점유율 결정변수에 관한 연구” 2007 윤경애 11
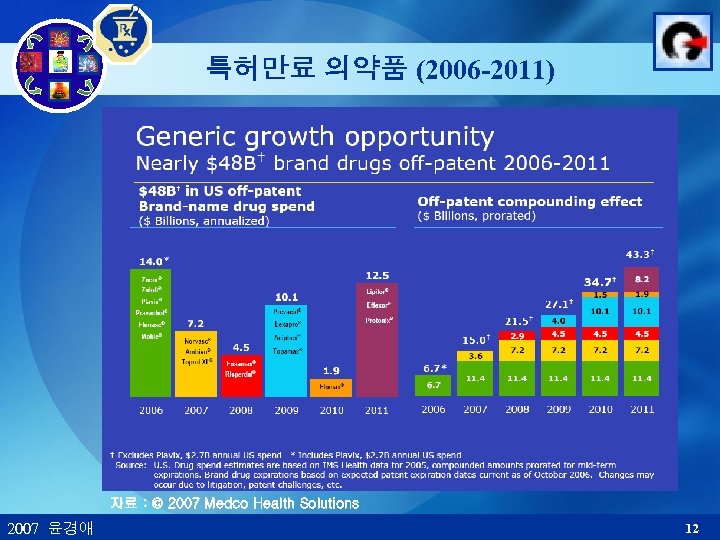
특허만료 의약품 (2006 -2011) 자료 : © 2007 Medco Health Solutions 2007 윤경애 12

1 st 제네릭 의약품 : 180일 독점권 1 st 제네릭사 브랜드사 Litigation - 신약개발에 장기간, 고비용 투자 - 특허권 획득 - 에버그린 전략 - 제품 개발 비용 - 소송 비용 - Challenge patent validity - ‘design around’ patent - 180일 독점권 후발 제네릭사 FTC (Federal Trade Commission) “The 180 -day marketing exclusivity provision was intended to increase the economic incentives for a generic company to be the first to file an ANDA containing a paragraph IV certification and get to market. ” 2007 윤경애 - 1 st 제네릭사의 노력에 편승하여 쉽게 시장 진입 13
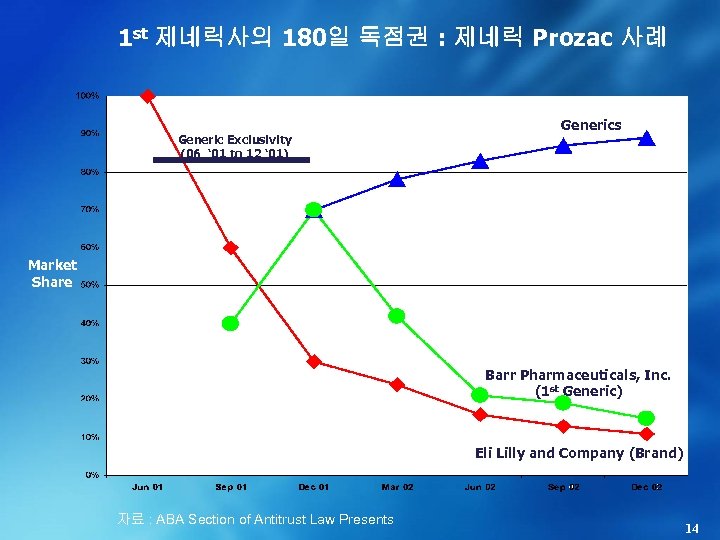
1 st 제네릭사의 180일 독점권 : 제네릭 Prozac 사례 Generic Exclusivity (06 ‘ 01 to 12 ‘ 01) Generics Market Share Barr Pharmaceuticals, Inc. (1 st Generic) Eli Lilly and Company (Brand) 자료 : ABA Section of Antitrust Law Presents 14
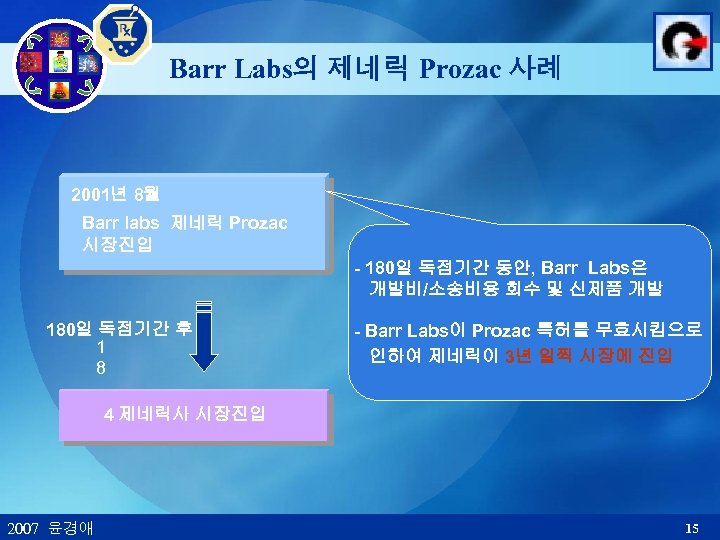
Barr Labs의 제네릭 Prozac 사례 2001년 8월 Barr labs 제네릭 Prozac 시장진입 - 180일 독점기간 동안, Barr Labs은 개발비/소송비용 회수 및 신제품 개발 180일 독점기간 후 1 8 - Barr Labs이 Prozac 특허를 무효시킴으로 인하여 제네릭이 3년 일찍 시장에 진입 4 제네릭사 시장진입 2007 윤경애 15
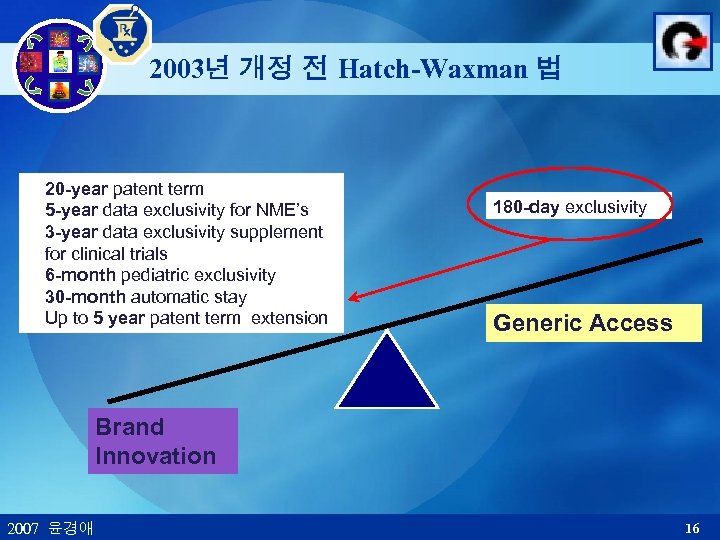
2003년 개정 전 Hatch-Waxman 법 20 -year patent term 5 -year data exclusivity for NME’s 3 -year data exclusivity supplement for clinical trials 6 -month pediatric exclusivity 30 -month automatic stay Up to 5 year patent term extension 180 -day exclusivity Generic Access Brand Innovation 2007 윤경애 16

2003년 개정 Hatch-Waxman 법 § 1. Orange Book 특허 등재 § - 등재 대상 특허에 대한 범위 및 성 격 명료화 § 2. 30일 허가정지 기간을 1회 적 용 § - ANDA 신청 이전까지 등록된 특허 에 대해서만 증명 § 2007 윤경애 - ANDA 신청 등록 후 20일 이내 공지 § - ANDA 신청자의 특허확인 판결 소 17
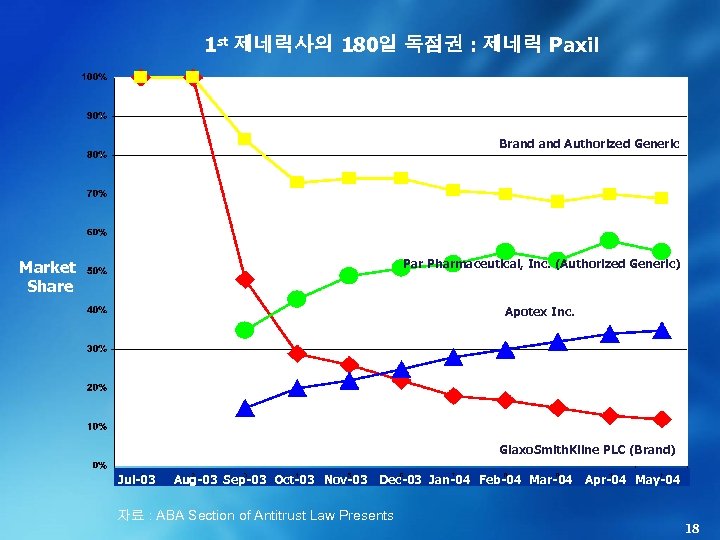
1 st 제네릭사의 180일 독점권 : 제네릭 Paxil Brand Authorized Generic Par Pharmaceutical, Inc. (Authorized Generic) Market Share Apotex Inc. Glaxo. Smith. Kline PLC (Brand) Jul-03 Aug-03 Sep-03 Oct-03 Nov-03 Dec-03 Jan-04 Feb-04 Mar-04 자료 : ABA Section of Antitrust Law Presents Apr-04 May-04 18

Pfizer v. Dr. Reddy’s Lab Federal Circuit, 2004. 2. 27. § Orange book 등재 특허 : US 4, 572, 909 - claim : dihydropyridines and their acid addition salts - 특허존속기간 : 2003. 2. 25. ★ Norvasc(amlodipine besylate)에 의한 존속기간 연장 : 2006. 7. 31. § Dr. Reddy가 amlodipine maleate에 대한 ANDA IV 신청 (2001. 12. ) § Pfizer 소 제기 - District court : no infringement and dismisses case - Federal Circuit : reverses (☞ Active ingredient : amlodipine) 2007 윤경애 20

University of Rochester v. G. D. Searle Federal Circuit, 2004. 2. 13. § 35 USC § 112 : Written description and enablement § 치료방법 청구항 : - treatment by selective inhibition of COX-2 § Rochester 특허 : 청구항에 기재된 치료방법에서 사용될 수 있는 화합물을 구체적으로 기재하지 않았음 ☞ 35 USC § 112 first paragraph 위배 2007 윤경애 21

Schering Corp. v. Geneva Pharma. Federal Circuit, 2004. 8. TM § Loratadine (CLARITIN )관련 특허만료 후 제네릭사 시 장진입 모색 § Schering : metabolite of loratadine 특허 오렌지북 등재 (descarboethoxyloratadine) ☞ Inherent anticipation does not require recognition or actual creation or reduction to practice 2007 윤경애 22

Recent Hatch-Waxman Litigation LIPITOR (특허권자 : 화이자) Orange Book 등재 특허 ANDA IV 신청 CAFC (Aug. 2006) - US 4, 681, 893 : NCE (master patent), Mar. 2010 - US 5, 273, 995 : R-enantiomer, Hemicalcium salt, Jun. 2011 - US 5, 969, 156 : Polymorph - US 5, 686, 104 : Formulation - US 6, 126, 971 - Ranbaxy filed ANDA IV ‘ 893 patent covers only racemate, improper patent term extension ‘ 995 patent is invalid, unenforceable - claim 1 of '893 patent was infringed - claim 6 of '995 patent in invalid (선행문헌 : ‘ 893) ☞ Ranbaxy : 2010. 3. 이후 180일 독점권 가능 2007 윤경애 23
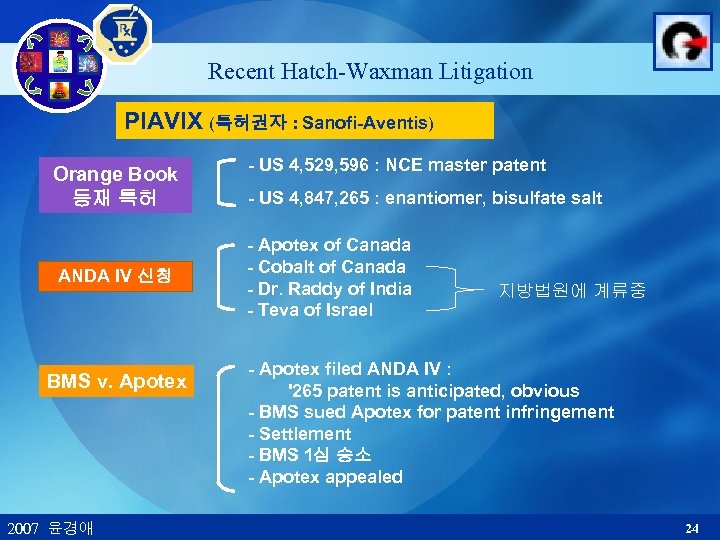
Recent Hatch-Waxman Litigation Pl. AVIX (특허권자 : Sanofi-Aventis) Orange Book 등재 특허 ANDA IV 신청 BMS v. Apotex 2007 윤경애 - US 4, 529, 596 : NCE master patent - US 4, 847, 265 : enantiomer, bisulfate salt - Apotex of Canada - Cobalt of Canada - Dr. Raddy of India - Teva of Israel 지방법원에 계류중 - Apotex filed ANDA IV : '265 patent is anticipated, obvious - BMS sued Apotex for patent infringement - Settlement - BMS 1심 승소 - Apotex appealed 24

Hatch-Waxman Litigation Pending Cases § Clarinex : Sepracor v. Glenmark Pharms § Effexor XR : Wyeth v. Mylan § Eloxatin : Sanofi-Aventis v. Abraxis, (Actavis, Ebewe Pharma(NJ), Ebewe Pharma(SC), Mayne Pharma, Par Pharma, Pharmachemie, Sun(NJ), Sun(MI), Mayne Pharma § § § § Floxin Otic : Daiichi Sankyo v. Apotex Lotrel : Novartis v. Dr. Reddy's Prilosec OTC : Astra. Zeneca v. Dr. Reddy's Rilutec : Impax v. Aventis Toprol-XL : In re Metoprolol Succinate Patent Litigation Ultracet : Ortho-Mc. Neil v. Apotex, (Par Pharma) Valtrex : Glaxo. Smith. Kline v. Ranbaxy 2007 윤경애 25

Recent Hatch-Waxman Litigation § Apotex v. FDA (C. A. D. C. June 6, 2006) § In re Tamoxifen Citrate Antitrust Litigation (2 d Cir. 2005) § Teva Pharmaceutical Ind v. Crawford (D. C. Cir. 2005) 2007 윤경애 26
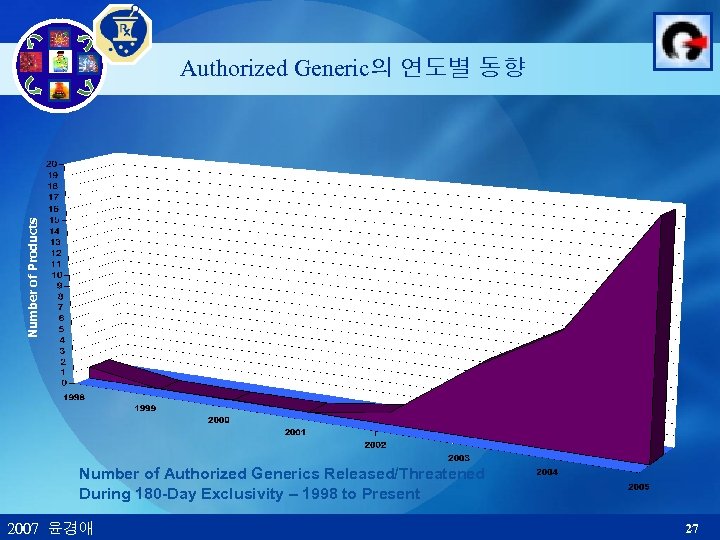
Number of Products Authorized Generic의 연도별 동향 Number of Authorized Generics Released/Threatened During 180 -Day Exclusivity – 1998 to Present 2007 윤경애 27

Authorized Generics의 파급효과 § 제네릭 약가 § 1 st 제네릭사의 incentive 감소 - 브랜드의 무효특허가 지속되는 효과 - ‘design around’ patent 개발의욕 감소 - 제네릭 의약품의 진입이 늦어짐 - 제네릭 의약품 진입 지연 = 소비자 손해 2007 윤경애 28

Hatch-Waxman 법의 개정안 (1) Elimination of Authorized Generics (2) – Rockefeller, Leahy, Schumer bill (3)(2) Creation of an Effective Declaratory Judgment (4) Provision (5) – Remove potential for patent settlements to bottleneck (6)trigger market entry by allowing subsequent filers to (7) exclusivity period (8)(3) Possible Limitation on Reverse Payments in Patent (9) Settlements (10) 2007 윤경애 – Kohl bill 29
Hatch-Waxman 법: 브랜드와 제네릭의 균형 회복 Brand Innovation 2007 윤경애 General Access 30

kay 21@kipo. go. kr kaykipo@hanmail. net
5e59d3a38ec0db1d0e2c363697ef7b90.ppt