c7706dd17244772061191ffe4cb4b7b5.ppt
- Количество слайдов: 50

임상시험의 개요 임상시험 특강 (동아대학교) 2010년 10월 15일 김성제(LSK Global PS) www. lskglobal. com

목차 1. 임상시험 및 신약개발 과정 2. 임상시험의 유형 3. 임상시험의 기본원칙 4. 임상시험 담당자들의 역할

1. 임상시험 및 신약개발 과정

임상시험의 시초 영국 해군 군의관 Lind에 의한 괴혈병 치료비교(1747년) 기존식단 + (① 사과즙, ② 식초, ③ 바닷물, ④ 묽은 황산, ⑤ 향식료 혼합물, ⑥ 오렌지와 레몬) 무작위배정(Randomization) 1926년 R. A. Fisher에 의해 소개되고 농업연구에 이용 임상연구에는 1931년 24명의 폐결핵환자에게 이용 맹검(Blindness) Sanocrysin vs. distilled water Cold vaccine vs. saline (as a placebo) 1938년

미국, 유럽의 관련법규의 제정 - 1938년 미국 소아용 실파 시럽제사고(Elixir of Sulfanilamide, 109명 사망, 항균제, 쓴맛을 없 애기 위해 용매로 사용한 디에틀렌 글라이콜 사용, 시판 승인 시 인체에서의 안전성자료요 구) - 1960년 유럽 thalidomide (10, 000명의 기형아) - 1962년 The Kefauver-Harris Amendments (안전성뿐만 아니라 효과 입증 시 판매허가, 임상 시험 참여자 동의서, GMP 확립 및 FDA의 생산기록과 현장실사 권한) - 1963년 IND(조건부 임상시험 허가)/NDA(신약허가심사) - 1964년 Helsinki 선언을 토대로 피험자 권익보호차원에서 윤리적 발전과 과학화 추진

미국, 유럽의 관련법규의 제정 1977. 9 임상연구자의 의무 1977. 9 개발기업과 모니터의 의무 1978. 8 임상시험심사위원회(IRB)의 역할과 의무 1979. 8 피험자 동의서 취득 Þ 1981년 임상시험관리기준(GCPs) 의무화 1992년 International Conference on Harmonization (www. ich. org)

국내 임상시험 환경 변화 - 1980년대 중반 G 7 프로젝트에 따른 신약개발 시작 - 1987년 KGCP(안) 공고 (동의취득의 어려움과 여건 미성숙) - 1989~1992 외국에서 개발된 신약에 대한 임상시험 - 1992 보건복지부/식약청에 의한 IND용 임상시험 실시 - 1992년 임상시험 실시기관 지정(141개 병원, 2010. 5. 31 현재) - 1995. 10 KGCP 제정 - 1999. 12 ICH-E 5 (Ethnic Factors in the Acceptability of Foreign Clinical Data)채택, 다국가 임상시험 활성화 - 2001. 1 ICH-GCP에 상응하는 개정 KGCP
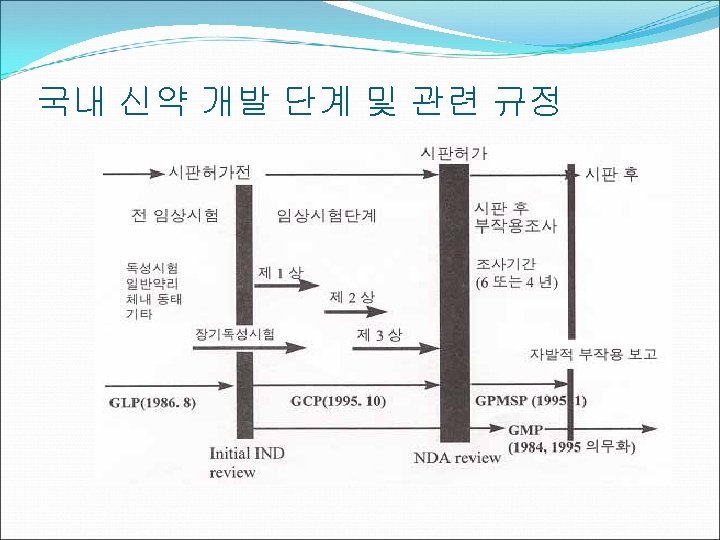
국내 신약 개발 단계 및 관련 규정

임상시험의 정의 임상에 사용되는 의약품의 안전성과 유효성을 증명할 목적으로 해당 약물의 약동, 약력, 약리 , 임상적 효과를 확인하고 이상반응을 조사하 기 위하여 사람을 대상으로 실시하는 시험 또 는 연구

임상시험(제 1상) 진입을 위한 선행조건 제제학적 시험 : 안정성, 흡수성, 용해도, 제제의 형태 독성시험 : 혈중농도와 독성의 관련성(급성독성, 아급성 독성, 만성독성, 생식독성, 의존성, 항원성 변이원 성, 발암성, 국소 자극성, 독성약동학자료) 약력학적 시험 : 주요 약리작용의 profile 일반약리 시험 : 여러 장기의 기능에 미치는 효과에 대한 profile 약동학적 시험 : 흡수, 분포, 대사, 배설

임상시험의 단계 Phase I : Safety, MTD study (안전용량), PK/PD - 건강한 지원자 대상 - 주로 안전성 검토 Phase II : Safety, Promising activity, 유효용량 - 단기 안전성/유효성 검토 Phase III : Safety, Efficacy - 충분한 환자에게 장기 투여시 안전성 확립/유효성 재확인 Phase IV : Post Marketing Surveillance - 시판후 부작용조사 및 추가임상시험 - 장기 투여시 희귀부작용 검토 - 새로운 적응증 탐색
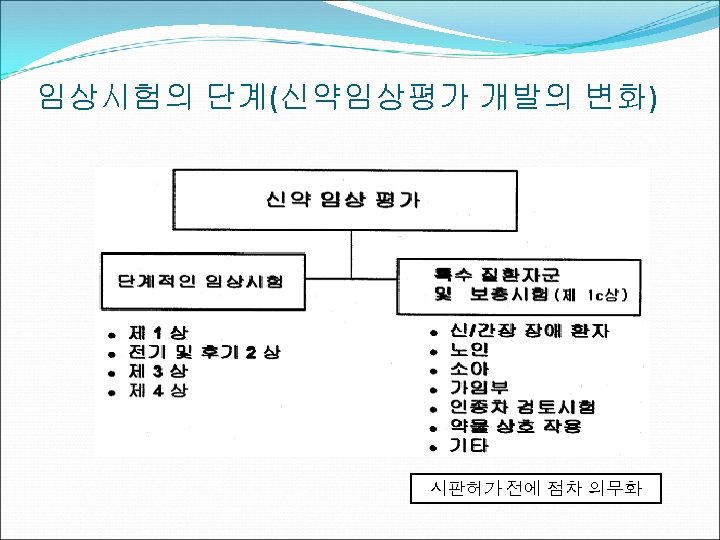
임상시험의 단계(신약임상평가 개발의 변화) 시판허가 전에 점차 의무화
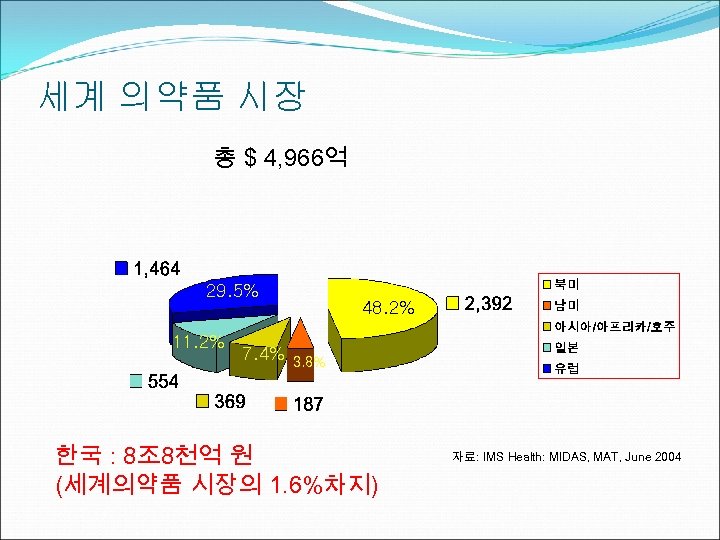
세계 의약품 시장 총 $ 4, 966억 29. 5% 11. 2% 7. 4% 48. 2% 3. 8% 한국 : 8조 8천억 원 (세계의약품 시장의 1. 6%차지) 자료: IMS Health: MIDAS, MAT, June 2004
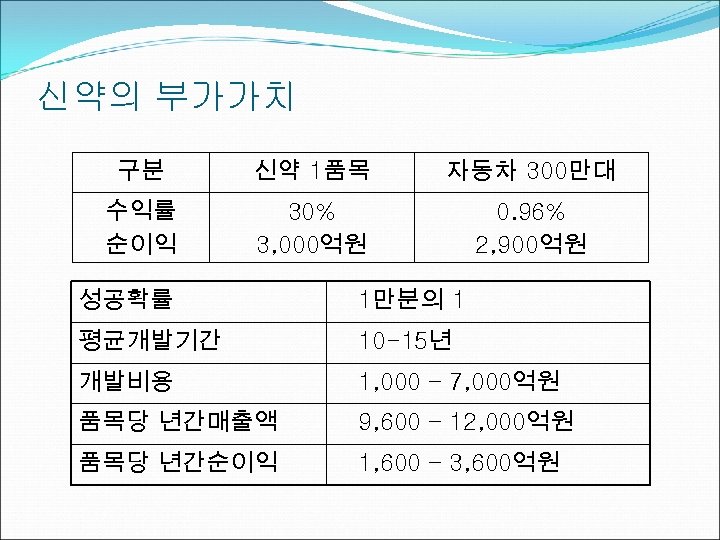
신약의 부가가치 구분 신약 1품목 자동차 300만대 수익률 순이익 30% 3, 000억원 0. 96% 2, 900억원 성공확률 1만분의 1 평균개발기간 10 -15년 개발비용 1, 000 – 7, 000억원 품목당 년간매출액 9, 600 – 12, 000억원 품목당 년간순이익 1, 600 – 3, 600억원
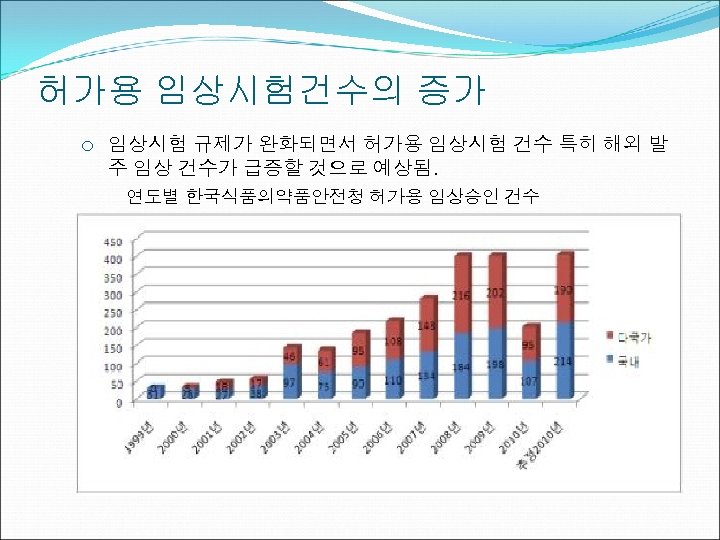
허가용 임상시험건수의 증가 ¡ 임상시험 규제가 완화되면서 허가용 임상시험 건수 특히 해외 발 주 임상 건수가 급증할 것으로 예상됨. 연도별 한국식품의약품안전청 허가용 임상승인 건수

2. 임상시험의 유형

임상시험의 유형(설계방법에 따른 분류) Evidence Based Medicine 1. 2. 3. 4. 5. 6. 7. 8. Anecdotal case study Case series with control Database (Retrospective analysis) Case-control study (Retrospective), Cohort study (Prospective) Historical study Randomized controlled trial (RCT) Confirmed RCT

임상시험의 유형(설계방법에 따른 분류) 관측연구(Observational study) 한 집단 또는 여러 집단의 환자들의 상태와 특성을 단순히 관찰, 분석 Case-control, cohort, cross-sectional study 실험연구(Experimental study) 피험자에게 특정한 처리(treatment: intervention)를 한 후에 효과 를 관찰하여 처리와 반응과의 인과관계를 규명 결과에 영향을 미칠 수 있는 여러 요인들을 직접 통제, 관리 Concurrent, non-concurrent Ref: 이재원(2005 생명과학연구를 위한 통계적 방법), De. Mets (1998 Fundamentals of Clinical Trials)

임상시험의 유형(설계방법에 따른 분류) 관측연구 1. Case-control study (retrospective) - 결과에 따라 사례군(case)과 대조군(control)으로 구분하고 각 집단에 대하여 과거의 위험인자(risk factor)를 가지고 있 었는지 조사하는 방법(과거에 무슨 일이 있었는가? ) - 심장발작을 일으킨 군과 일으키지 않은 군을 대상으로 그 들이 양물남용의 경험이 있는지를 조사하여 심장발작과 약물남용간의 인과관계를 확인 - 희귀질환이나 경과기간이 긴 연구에서 효율적

임상시험의 유형(설계방법에 따른 분류) 관측연구 2. Cohort study (prospective) - 연구 대상이 되는 집단을 일정기간 추적 조사(앞으로 어떤 일이 있을 것인가? ) - 비흡연 집단과 흡연자 집단을 각각 20년간 추적하여 폐암발 생여부를 조사하여 흡연이 폐암에 영향을 미치는지 알아보 는 연구 - 연구 관리의 문제점 (탈락, 비용, 기간)

임상시험의 유형(설계방법에 따른 분류) 관측연구 3. Cross-sectional study (현황조사) - 어느 특정 시점에서 대상자들을 조사(survey)하여 모은 자료를 분석(무슨 일이 일어나고 있는가? ) - 단기간, 비용 저렴 - 시점에 따라 영향을 받는 연구의 경우 왜곡될 가능성이 존재(예: 계절적 요인, …)

임상시험의 유형(설계방법에 따른 분류) 실험연구(Intervention/Treatment: 치료, 예방, 진단, 치료계획, 치 료절차 등) Concurrent control Randomized Blinded (single, double, triple) Unblinded Non randomized Cross over Factorial Non-concurrent control No control (single arm): bias Historical control: 같은 의사, 비슷한 환자, … Literature control: publish bias Database control

임상시험의 유형(설계방법에 따른 분류) Randomized design 환자들을 각 처리집단으로 할당할 때 발생할 수 있는 편향(bias)를 감소시켜 처리효과에 대한 보다 신뢰성 있는 결론을 내림 Fixed Allocation Randomization Simple (Complete) Randomization Blocked Randomization Stratified Randomization Adaptive Randomization Procedures Baseline Adaptive Randomization Procedures Response Adaptive Randomization
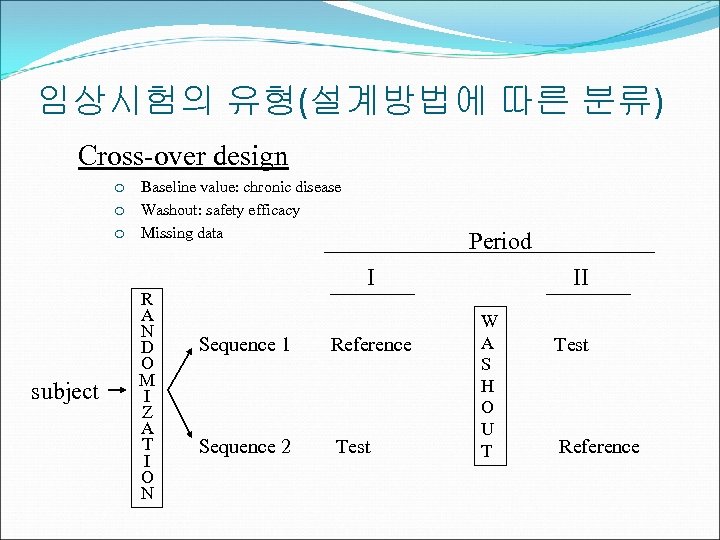
임상시험의 유형(설계방법에 따른 분류) Cross-over design ¡ ¡ ¡ subject Baseline value: chronic disease Washout: safety efficacy Missing data R A N D O M I Z A T I O N Period I Sequence 1 Reference Sequence 2 Test II W A S H O U T Test Reference

Study population (임상 모집단) 임상효과의 발견 가능성 극대화(초기단계) 좁은 범위의 세부 집단(초기단계) 동질성 유지(확증시험) 선정/제외 기준을 적절히 완화(유용성 증가) 전체 환자 집단을 완전히 대표하는 집단을 찾기는 힘듬 거주지역, 진행시간, 시험 담당자, 실시기관
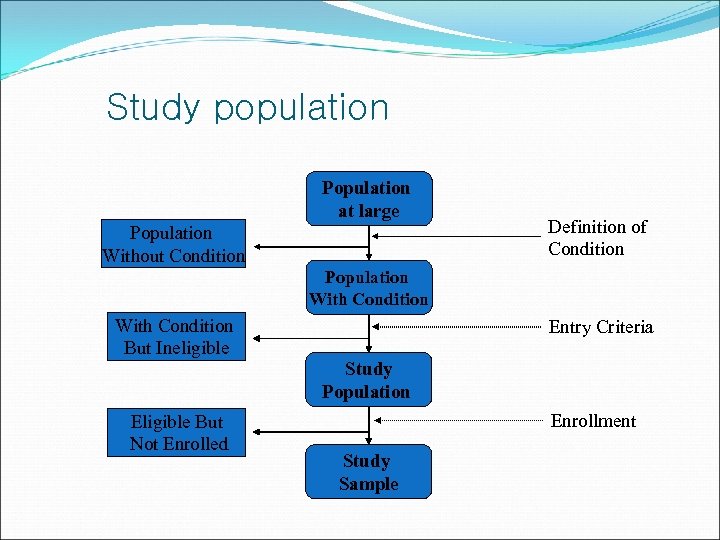
Study population Population at large Population Without Condition Definition of Condition Population With Condition But Ineligible Eligible But Not Enrolled Entry Criteria Study Population Enrollment Study Sample

Study population Eligibility criteria considerations ① 임상시험의 혜택 가능성 ② 원하는 효과를 볼 수 있는 가능성 ③ Adverse effects; Pregnant women ④ Competing risk problem; long term study, 생존기간 예측, 다른 심각한 질환 여부 ⑤ Compliance (순응도): Run-in period, Social Economic Index

3. 임상시험의 기본원칙

Principles of Clinical Trials How not to bias? 임상시작전 How to avoid unintended error? Be transparency
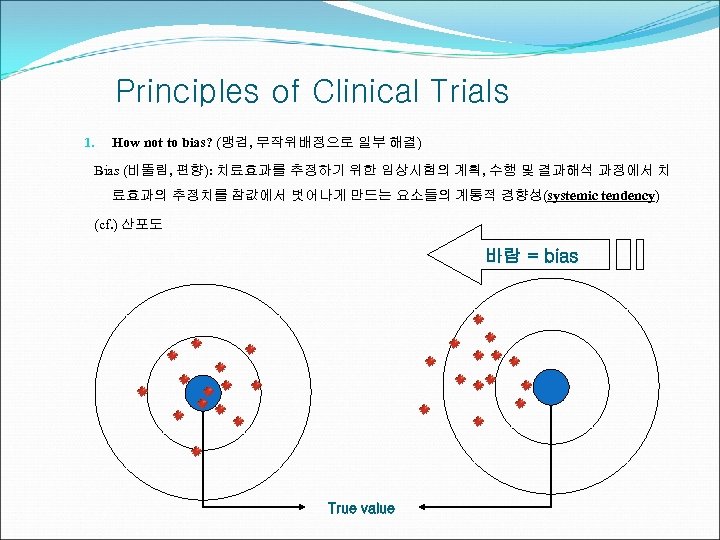
Principles of Clinical Trials 1. How not to bias? (맹검, 무작위배정으로 일부 해결) Bias (비뚤림, 편향): 치료효과를 추정하기 위한 임상시험의 계획, 수행 및 결과해석 과정에서 치 료효과의 추정치를 참값에서 벗어나게 만드는 요소들의 계통적 경향성(systemic tendency) (cf. ) 산포도 바람 = bias True value

Principles of Clinical Trials 1. How not to bias? (계속) 비교 가능하게 Group assign이 필요(나이, 성별, 인종 등) Ex. ) GroupⅠ vs. Group Ⅱ 노인 70% 노인 30% Biased (age) cf. ) GroupⅠ vs. Group Ⅱ 건강 80% Comparable but difficult to see efficacy Baseline : Comparable PP Analysis : Can non-comparable

Principles of Clinical Trials 2. How to avoid unintended error? - Sample size, Type I, II error 실제 현상 H 0 사실 H 0: µ 1=µ 2 HA: µ 1≠µ 2 H 0 채택 옳은 결정 제 2종 오류 (Type II error: β) HA 채택 검정결과 HA 사실 제 1종 오류 (Type I error: α) 옳은 결정 (Power)

Principles of Clinical Trials 2. How to avoid unintended error? (계속) Type I (0. 05) Type II (0. 1) 효과가 있을 확률 0. 1(100) 90개 승인 효과가 없을 확률 0. 9(900) 45개 승인 135개 승인 중 45개 (45/135=33%) false 3. Be transparency - Reproducible (GCP) - CR, DM - 예)생동성 임상 조작(2008년)

Principles of Clinical Trials Clinical Trial Failure Sample size (time/money) Outcome variable (research 부족) Patient population (모집용이 -> 효과확인 힘든 피험자) Drug itself Design/Planning problem

임상시험과 도덕적 규제 기본원리 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 사전에 반드시 동물에 대한 실험/관찰을 통해 과학적 근거 계획과 과정의 구체적인 명시, 중립적인 심사위원회 평가 임상의사의 지도/감독하에 진행, 해당분야 전문가 참여, 피험자가 지 원했다 하여도 책임은 지도/감독자가 짐 예상되는 위험에 비해 이익이 월등하게 크다는 판정 약의 효과/부작용에 대한 문헌조사 및 동물자료필요, 피험자의 문제 가 과학이나 사회의 관심사보다 소중함 개인의 비밀보장과 피험자의 안전 인체에 불리한 반응발생시 건강에 피해를 준다고 판정시 즉시 중단 피험자에게 시험의 목적, 방법, 기대효과, 예상되는 부작용 설명, 사전 승인 필요, 언제든 승인취소하고 시험거부 가능 피험자 승인시 진료와 직접관계가 되는 의사가 진행 대화능력이나 합리적인 판단이 안될 경우 법적 대리인의 승인 정확한 내용의 시험발표, 위의 내용이 맞지 않을 경우 발표 금지 Ref: 고응린 외 (신약평가를 위한 임상시험과 자료분석)

임상시험과 도덕적 규제 특수대상의 승낙 취약한 피험자 연구 참여와 연관된 이익에 대한 기대 또는 참여를 거부하는 경우 조직 위계의 상급자로부터 받게 될 불이익을 우려하여 자발적인 참 여 결정에 영향을 받을 가능성이 있는 피험자(예: 의과대학/약학대 학/치과대학/간호대학의 학생, 병원 또는 연구소 근무자, 제약회사 직원, 군인, 수감자) 불치병에 걸린 사람 시행규칙에서 정한 집단시설에 수용 중인 자, 실업자, 빈곤자, 응급 상황에 처한 환자, 소수 인종, 부랑자, 난민, 미성년자 등 자유로운 선택을 하기 어려운 상황에 처해있는 피험자 어린이 임산부 정신병 및 정신장애자(법적 보호자의 승인) 지역사회 주민대상의 경우(적극적인 홍보, 의견수렴)

4. 임상시험 담당자들의 역할
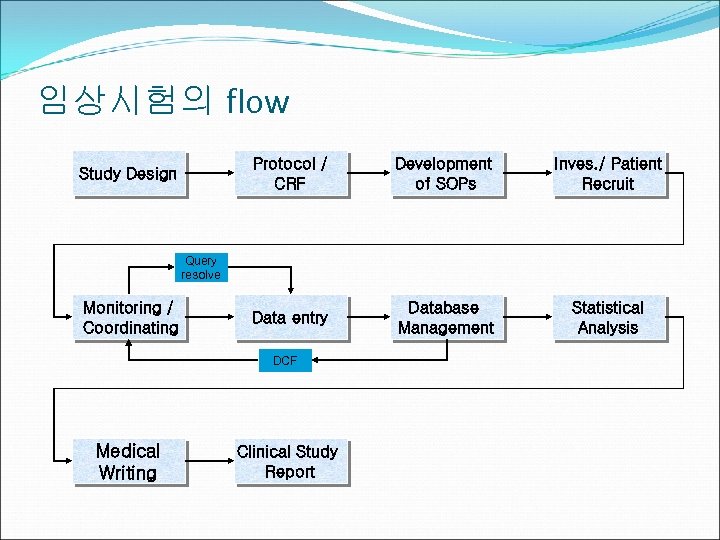
임상시험의 flow Protocol / CRF Study Design Development of SOPs Inves. / Patient Recruit Data entry Database Management Statistical Analysis Query resolve Monitoring / Coordinating DCF Medical Writing Clinical Study Report

임상시험 대행기관 Contract Research Organization (CRO) 임상시험과 관련된 의뢰자의 임무나 역할의 일부 또는 전 부를 대행하기 위하여 의뢰자로부터 계약에 의해 위임 받 은 개인이나 기관 즉, 신약후보물질의 안전성과 효능을 과학적으로 잘 디자인된 임상 시험을 통해서 완벽하게 입증해 내고 관계 허가기관(예: FDA, KFDA) 의 판매허가를 Sponsor를 대신해서 취득하는 사업을 말합니다
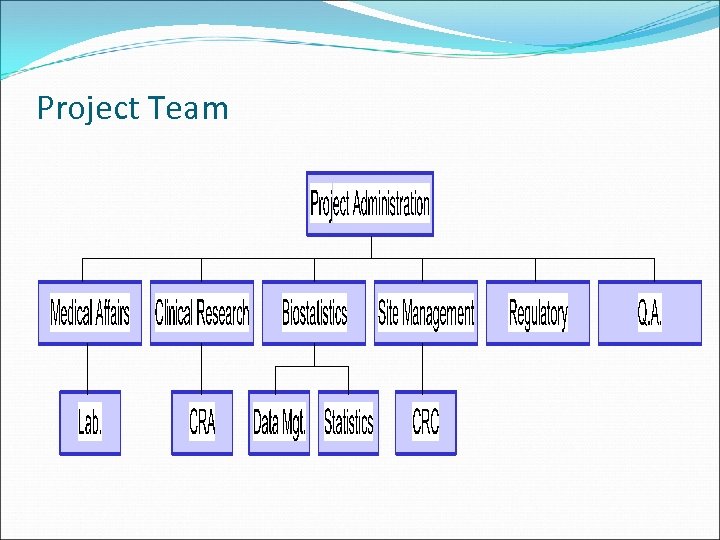
Project Team

Project Administration ¡ Project 전체 기술적 지원 ¡ FDA규정과 GCP에 맞는 법적문서의 확인, FDA 제출 ¡ 의뢰자, 시험기관, Project팀간의 연결

Medical Affairs ¡ Study Development Plan ¡ Protocol & CRF ¡ Monitor Adverse Experiences ¡ Medical Interpretation ¡ Medical Quality of Clinical Databases (Pharmacovigilance)

Clinical Research Associate ¡ Clinical Monitoring Process 관리, 수행 ¡ GCP, SOP와의 조화 (안전성, 유효성) ¡ Protocol, 규정준수여부 확인 (임상시험센터 방문) ¡ 시험약물관리 확인 ¡ Lab quality 여부 확인 (Certificate) ¡ 필요한 문서 작성

Site Management Clinical Research Coordinator (CRC) l Patient education l Management of patients schedule l Management of study procedure l Audit/Inspection preparation l Archive study-related documents

Biostatistics & DM Biostatistics l Reference review l Study Design l Sample Size 결정 (Type I & II errors) l Randomization l 데이터베이스 Cleanup l 통계분석 (Table, Figure, Listing) l 통계보고서

Biostatistics & DM Protocol & CRF Design/Review Development Stage Data Processing Stage Closing Stage DQM Plan Pre-entry review DCF Issue & Resolution Data dictionary Double data entry DB Audit Data validation program Unmatched check Medical coding Data entry application Logical check DB Lock Transformation to SAS data Validation of SAS data set

Regulatory ¡ 약 개발을 위한 국내, 국제적 전략 조언 ¡ 의뢰자와 규제기관과의 중재 ¡ 상품출원의 준비, 등록, 관리 ¡ 관련자료조사 ¡ 경쟁사소식 갱신

Quality Assurance ¡ On-site investigator 감사 ¡ 결과보고서 감사 ¡ IRB 감사 ¡ 임상시험 진행에서 관련법규, ICH Guideline, 회사 SOP 준수 확인 ¡ 의뢰자와의 계약준수여부 확인 및 평가

임상시험(State-of-the-art) Team Work 의학, 한의학, 약학, 간호학, 수의학, 생물학, 임상병리, 보건학, 식품영양학, 보건행정학, 통계, 전산, IT, 마케팅, 회계, 총무, 인사, 법학, 국문학, 영문학

감사합니다. 김성제 LSK Global PS
c7706dd17244772061191ffe4cb4b7b5.ppt