af7eaf5264579288d05d04c86316e361.ppt
- Количество слайдов: 152

싱글PPM 품질혁신을 통한 국제제품인증 획득요령 2006~2007

v목차 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 품질, 시스템 및 제품인증 그리고 싱글PPM CE 마킹의 적용과 의미 New and Global Approach 적합성 평가 모듈 비조화 영역 제품인증 전기제품 CE 인증 개인용 보호장구 CE 인증 체외진단용 의료기기 CE 인증 의료기기의 CE 인증 ISO 13485: 2003 의료기 품질경영 시스템 기술 문서 FDA NRTL CCC 중국 강제인증 SFDA 제조물책임법 대응 필수요구사항 (Essential Requirement) 자주묻는 질문들


v 품질이란? Ø 원시적 의미의 품질 어떤 물질을 구성하고 있는 기본적 내용 속성 ·종류 정도 등을 의미하는, 즉 물 품자체가 지니는 고유의 성질·특성·개성 Ø 생산자 관점에서의 품질 - 요건에 대한 일치성(conformance to requirements) - 시방과의 일치성(conformance with specification) Ø 소비자 관점에서의 품질 - 용도에 대한 적합성 (Fitness for use) - 고객 만족 (Quality is Customer Satisfaction)
v 품질이란? Ø 시스템 (ISO) 에서의 품질 품질은 실체가 지니고 있는 명시적 내지 묵시적 요구를 만족시키는 능력에 관 계되는 특성의 전체 종합적 의미의 품질 강제적 품질(법률적, 사회적) 고객 요구 품질 자발적 품질
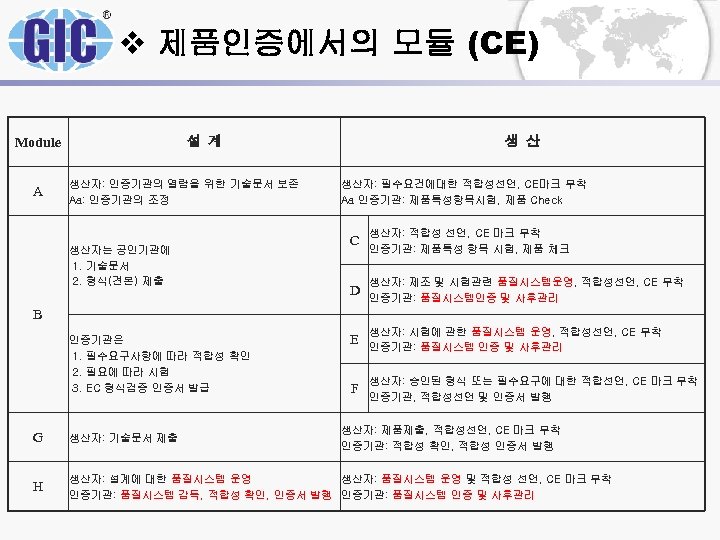
v 제품인증에서의 모듈 (CE) Module A 설 계 생산자: 인증기관의 열람을 위한 기술문서 보존 Aa: 인증기관의 조정 생산자는 공인기관에 1. 기술문서 2. 형식(견본) 제출 생 산 생산자: 필수요건에대한 적합성선언, CE마크 부착 Aa 인증기관: 제품특성항목시험, 제품 Check C 생산자: 적합성 선언, CE 마크 부착 인증기관: 제품특성 항목 시험, 제품 체크 D 생산자: 제조 및 시험관련 품질시스템운영, 적합성선언, CE 부착 인증기관: 품질시스템인증 및 사후관리 E 생산자: 시험에 관한 품질시스템 운영, 적합성선언, CE 부착 인증기관: 품질시스템 인증 및 사후관리 F 생산자: 승인된 형식 또는 필수요구에 대한 적합선언, CE 마크 부착 인증기관, 적합성선언 및 인증서 발행 B 인증기관은 1. 필수요구사항에 따라 적합성 확인 2. 필요에 따라 시험 3. EC 형식검증 인증서 발급 생산자: 제품제출, 적합성선언, CE 마크 부착 인증기관: 적합성 확인, 적합성 인증서 발행 G 생산자: 기술문서 제출 H 생산자: 설계에 대한 품질시스템 운영 생산자: 품질시스템 운영 및 적합성 선언, CE 마크 부착 인증기관: 품질시스템 감독, 적합성 확인, 인증서 발행 인증기관: 품질시스템 인증 및 사후관리

v 제품인증에서의 모듈 (CE) Ø 제품인증에서 제품의 위험도 및 인증기관의 관여가 많을 수록 시스템의 검증을 요구한다. Ø 검증된 시료 제품이 지속적으로 반복성과 재현성을 가지 고 균일한 품질을 보장할 수 있는 부분은 시스템 뿐. Ø 시스템의 검증은 일회가 아닌 주기적인 관리를 통한 제 품품질 및 공정품질을 검증함.

v System Ø ‘ISO 9001’ 등과 ‘싱글PPM’의 상관관계 • 불량률 싱글PPM 수준을 달성하기 위해서는 품질경영시스템을 갖추고 있어야 함 • 품질경영시스템의 예 - ISO 9001 - ISO/TS 16949 등

v System간의 포함관계 Ø ‘ISO’와 ‘싱글PPM’ 시스템과의 관계 싱글PPM ISO 9001 ISO 13485. .

v 제품 인증의 의미 Ø 제품인증을 획득하고 마킹을 했다는 의미는? 의료용 진단 PC 1023
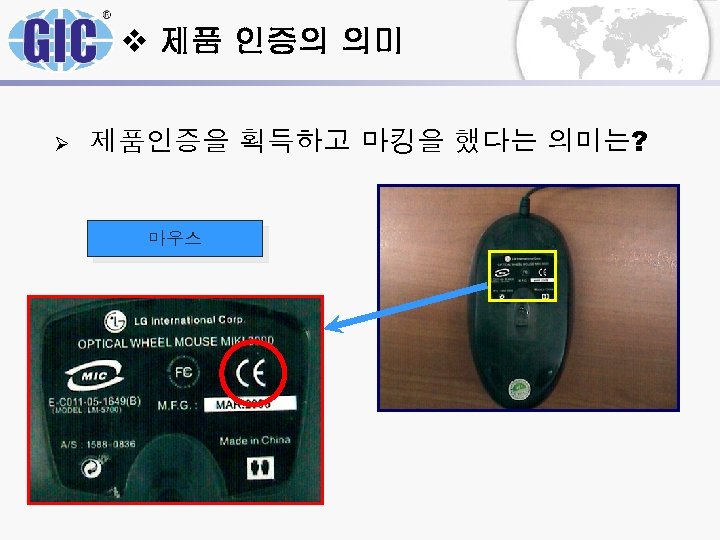
v 제품 인증의 의미 Ø 제품인증을 획득하고 마킹을 했다는 의미는? 마우스

v 제품 인증의 의미 Ø 제품인증을 획득하고 마킹을 했다는 의미는? 1. 제품에 대한 성능 합격? 2. 제품의 품질이 법규 요구 사항에 충족하다는 의미? 예) 제품품질이 싱글PPM 수준임 3. 제품이 사용상 안전하며 앞으로 생산되는 제품 또한 균 일한 품질로서 믿을 만 함?

v 제품 인증의 의미 Ø 제품에 대한 지속적 품질관리를 위해서 1. ISO 9001 시스템 유지를 요구 - 일반 전기전자 및 CPD, PPE 등 생산 기업 경우 2. ISO 13485 에 대한 시스템 유지를 요구 - 의료기기 생산 업체의 경우
v 싱글PPM의 특징 Ø 중소기업의 품질수준을 높이는데 가장 이상적 Ø 모기업과 연계하여 서로 만족할 수 있는 수준의 품질을 달성 Ø 현재 출하 및 납품불량률을 중심으로 심사하고있 음 - 추후 공정불량률도 심사기준에 포함될 예정

v 총체적 품질관리의 필요 Ø ISO 9001: 2000 시스템을 통한 품질관리 Ø ISO 13485: 2003 을 통한 품질관리 Ø 제품인증을 통한 품질관리 - 제품과 시스템을 동시에 관리

v CE(CPD) 인증을 통한 부품사의 품질관리 사례 Ø Initial type testing (ITT) - To determine the performance of the product type Ø Factory production control (FPC) - The permanent internal control of production exercised by the Certification Body to assure that all products conform to ITT
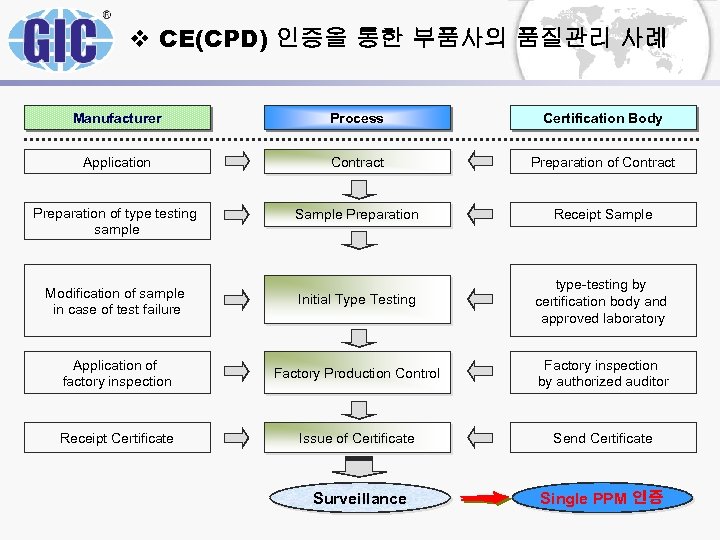
v CE(CPD) 인증을 통한 부품사의 품질관리 사례 Manufacturer Process Certification Body Application Contract Preparation of type testing sample Sample Preparation Receipt Sample Modification of sample in case of test failure Initial Type Testing type-testing by certification body and approved laboratory Application of factory inspection Factory Production Control Factory inspection by authorized auditor Receipt Certificate Issue of Certificate Send Certificate Surveillance Single PPM 인증

2. CE 마킹의 적용과 의미

v CE 마킹 - 개요 CE 는 “European Conformity” 의 프랑스어인 “Conformité Européene” 의 약자이다. ± ± 최초 사용 명칭은 “EC Mark” 였으나 1993년 93/68/EEC 지침에 의하여 "CE Marking" 으로 공 식 변경됨. "CE Marking" 은 현재 모든 유럽연합 공식 문서에 쓰이고 있다.

v CE 인증의 카테고리 (Directive 별) ± ± 기계류 (98/37/EC) 완구류 (88/378/EEC) 건축자재 (89/106/EEC) 전기전자 (EMC - 89/336/EEC, LVD - 73/23/EEC, 96/57/EC, 92/75/EEC) ± ± ± 개인용 보호장구 (89/686/EEC) 의료기기 (93/42/EEC) 능동이식형 의료기기 (90/385/EEC) 체외진단의료기기 (98/79/EC) 압력용기 (97/23/EC)

v CE 인증의 카테고리 (Directive 별) v 통신장비 (R&TTE) (1999/5/EC) v 단순압력용기 (87/404/EEC) v 가스기기 (90/396/EEC) v 승강기 (95/16/EC) v Recreational craft (94/25/EC) v Equipment and protective systems for use in explosive atmospheres (94/9/EC) v Non-automatic weighing instruments (90/384/EEC) v Cableways (2000/9/EC) v Explosives for civil use (93/15/EEC) v Hot water boilers (92/42/EEC)

v. CE 에 제외되는 제품류 For examples: v Chemicals (화학제품) v Pharmaceuticals (약품) v Cosmetics (화장품) v Foodstuffs (식품)

v. CE 마킹의 의미 ± 제품의 CE 마킹은 제조자 또는 유럽연합 내 대리인의 선언으로써 제품이 유럽연합의 건강, 안전 그리고 환 경 보호 관련 법률의 필수 요구사항을 따르고 있다는 의미이다. ± 제품이 각각 CE 마킹이 가능한 여러 지침에 동시에 해 당되는 경우 해당 제품의 CE 마킹은 모든 지침과의 적 합성을 가정한다는 표시이다.

v CE 마킹의 의미 ± 정부관계자들에게 자국시장 내에서 제품이 판매될 수 있음을 표시 ± 유럽자유무역연합과 유럽연합 28개국의 단일시장 내에서 제품의 자유 이동을 보장 ± 감시기관이 부적합 제품을 시장에서 회수할 수 있는 권한이 있음을 의미한다.

v CE 마킹 신청상의 기본 규칙 ± The CE marking is mandatory and must be affixed on any selected product before its placing on the single EU market ± The CE marking must take the form according to picture below. If the CE marking is reduced or enlarged the proportions must be respected.

v CE 마킹 신청상의 기본 규칙 ± The CE marking must be affixed visibly, legibly and indelibly to the product or to its data label. A minimum height of the CE marking is required 5 mm. ± If according to the applicable directives is involved Notified Body participation in the production control phase, must affix its identification number near CE marking.

v 유럽연합시장의 조사 ± The main goal of the New Approach directives is to assure that products which freely circulate in the EU market have a proper level of safety. ± Principle responsibility of manufacturers in the field conformance with requirements of applied directives. ± Market surveillance is a necessary element to correctly implement the above mentioned principles. ± Rules of the market surveillance are particular in individual EU member states.

v 유럽연합시장의 조사 ± The member state must provide by means of National authorities the necessary legal and administrative implement to assure the compliance of the products on the market with the directives. ± National authorities are responsible for ensuring the implementation of a proper market surveillance mechanism. ± For communication between National authorities has been installed database RAPEX - a rapid exchange of information about dangers consumer products.
v 시장조사의 주체

v 시장조사의 주체 Actors for checking of product compliance with the New Approach directives: ± ± The manufacturer checks product before its launching (placing) on the market The customs official checks products at the origin import from outside the EU The market surveillance authority checks products during its live in the market The court, checks products when an incident occurs

v CE 마킹과 품질인증의 차이점 CE marking ± CE marking is NOT quality mark! Its principles and obligations for manufacturers arises from New Approach directives. ± CE marking bears only on the European health, safety and environmental protection legislation

v CE 마킹과 품질인증의 차이점 Quality marks ± For quality marks the important rule is valid – system is voluntary and is not dependent on EU legislative. Details are very good inscribed in standard ISO/IEC 17030 ± Quality marks system according to ISO/IEC 17030 has included beyond fulfilling of the legislation safety requirements also fulfilling of quality requirements. ± Certification body makes periodic supervision of quality control system of the manufacturer production

3. New and Global Approach to technical harmonization The main objects and bodies involved into products’ conformity assessment in EU
v EU – market 2005

v Harmonised sphere ± Products that are harmonised at Community level (30 % goods in EU): a) there are common EU technical rules (Old and New Approach Directives) b) selected products must have the CE mark affixed

v Old and New Approach Both are ways to harmonize the national requirements on products with aim to support free trade of goods ± ± the Old Approach has been left the New Approach is possible solution at present, the discussions about amendment of it are going (“New Approach”) differences of New and Old Approach: Old approach - to estimate parameters, limits, methods in law ® New Approach - to estimate basic essential requirements only ®
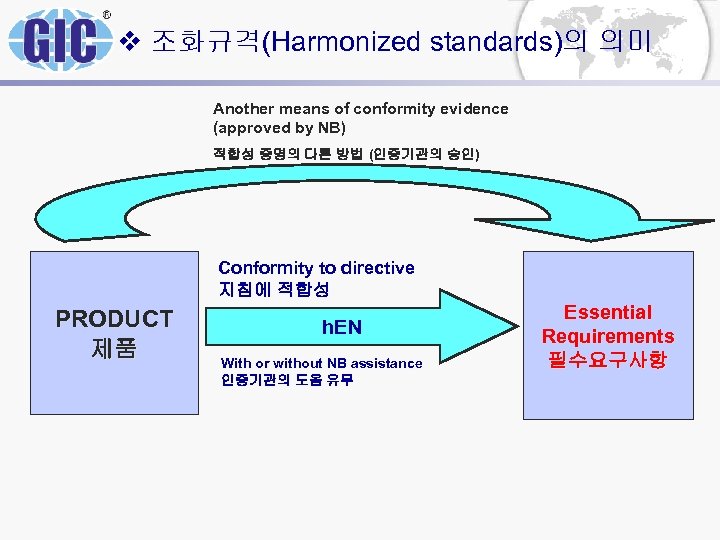
v 조화규격(Harmonized standards)의 의미 Another means of conformity evidence (approved by NB) 적합성 증명의 다른 방법 (인증기관의 승인) Conformity to directive 지침에 적합성 PRODUCT 제품 h. EN With or without NB assistance 인증기관의 도움 유무 Essential Requirements 필수요구사항

v Global Approach ± New Approach 는 제품의 공통적인 기술요구사항을 확립하 여 자유무역의 기술적 장벽을 제거하는데 목적이 있다. ± Global Approach 는 다양한 적합성평가 절차에서 비롯되는 두 번째 기술적 장벽을 제거하는 도구이다. ± Significance of the Global Approach is in establishing of uniform testing of products and other procedures for CE marked products Global Approach 는 CE 마킹을 위한 단일한 제품 테스트 및 기타 절차들의 확립에 그 중요성이 있다. ±
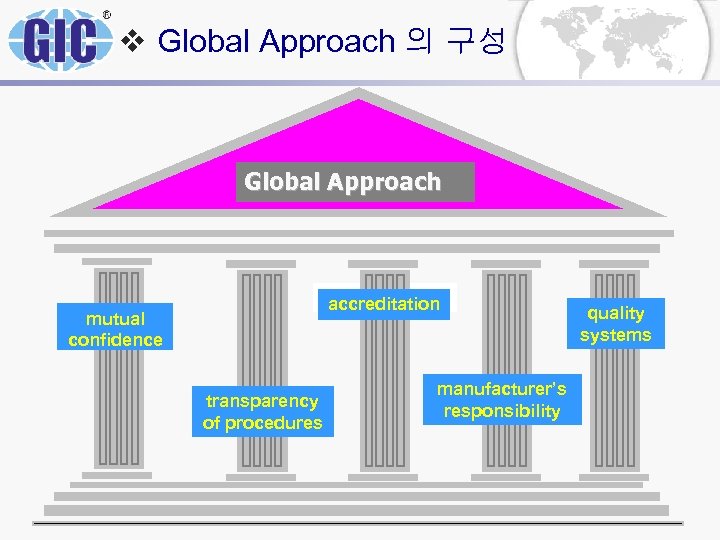
v Global Approach 의 구성 GLOBÁLNÍ PŘÍSTUP Global Approach accreditation mutual confidence transparency of procedures manufacturer’s responsibility quality systems

v 제조자 책임 ± Exclusive responsibility for product safety (even in case NB activity) ± Most of the products assessed in module based on sole manufacturers responsibility (Module A) ± Quality system and Factory production control are cornerstones of all procedures ± Only manufacturer has the right to choice the proper procedure, if the alternatives are given by directive ± Manufacturer signs EC Conformity Declaration ± Manufacturer affixes the CE mark

v 품질 시스템 ± Quality system is key aspect of manufacture ± All Modules are based on the establishing and maintaining of quality system in production ± In the product with higher risks, the Modules with higher demand on quality system and its surveillance apply ± In many directives the Full Quality Assurance is applicable as alternative to other Modules ± Main tasks of Notified Bodies in highly hazardous product is production surveillance

v 비조화 영역 Non - harmonized sphere ± 유럽 공동체 레벨에서 조화되지 않은 영역의 제품이 유럽연 합 내에서 70%에 달함

4. 적합성 평가모듈 Variety of conformity assessment procedures

v 모듈 시스템의 개요 n modules for the various phases of the conformity assessment procedures which are intended to be used in the technical harmonization directives • Council Decision 90/683/EEC: n the rules for the affixing and use of the CE conformity marking

v 모듈 시스템의 기본원칙 ± Modular system is based on two principles of Conformity assessments ® on the intervention of a first party (manufacturer) OR ® on the intervention of a neutral (third) party (notified body)

v 관련 적합성평가 부분 the product design phase OR ± the product manufacturing phase OR ± both above mentioned phases at the same time ± Every module specifies the obligations of the manufacturer and, if applicable, of the notified body. An overview of the modules shows the necessary complimentarity between the two phases of conformity assessment in the design phase and in the manufacturing phase of the product.

v Modules (A to H) ± ± ± ± Module A Internal production control Module B EC type examination Module C Conformity to type (supplement to B) Module D Production quality assurance (suppl. to B) Module E Product quality assurance (suppl. to B) Module F Product verification (supplement to B) Module G Unit verification Module H Full quality assurance

v Modules description (A, B) ± Module A - Internal production control provides for an internal design and production control. This module does not require any involvement of a notified body. ± Module B - EC Type Examination is applied to the product design phase and must be complemented by a module that provides for an assessment of the production phase. The EC type examination certificate is issued by a notified body.

v Modules description (C) ± Module C - Conformity to Type is applied to the production phase and follows upon Module B. It ensures that the product corresponds to the type, as it is described in the EC type examination certificate, issued in accordance with Module B. There is no need to involve a notified body for this module.

v Modules description (D) ± Module D - Production Quality Assurance is applied during the production phase and follows upon Module B. It is based on the quality assurance standard ISO 9001 (but it is not identical) and involves intervention by a notified body that is responsible for approving and monitoring the quality assurance system established by the manufacturer, applicable to production, final acceptance and testing.

v Modules description (E, F) ± Module E - Product Quality Assurance Is applied during the production phase and follows upon Module B. It is based on quality assurance standard EN ISO 9001 and involves intervention by a notified body that is responsible for approving and monitoring the quality assurance system established by the manufacturer, applicable to final acceptance and testing. ± Module F - Product Verification Is applied during the production phase and follows upon Module B. A notified body checks the conformity to type, as it is described in the EC type examination certificate, issued in accordance with Module B, and issues a certificate of conformity.

v Modules description (G, H) ± Module G - Unit Verification Is applied during the design and production phase. Every product is examined by a notified body, which issues a certificate of conformity. ± Module H - Full Quality Assurance Is applied during the design and production phase. It is based on quality assurance standard EN ISO 9001 and involves a notified body that is responsible for approving and monitoring the quality assurance system established by the manufacturer, applicable to design, production, final acceptance and testing. Note: The ISO 9001 Certificate is not satisfactory document for modules D, E, G, H.

5. 비조화 영역 제품인증

v Introduction ± ± Non harmonized sphere creates approximately 70 % goods in EU. Non – harmonized sphere is very interesting area for development of different procedures with participation of the third - party Voluntary procedures in the EU states – inspection, certification, granting of the mark Mark affixed on the product gives to consumers information about added value of goods and focuses attention to its differences.

v Important and famous EU marks EU eco-labelling the 'Flower' mark

v EU eco-labelling 'Flower' mark ± Aim - to award a Community Eco-label to products and services with reduced environmental impacts. ± The scheme is VOLUNTARY. ± Criteria are established for individual product groups, (the total number of product categories covered by the scheme was in year 2004 about 30 )

v Certification Body’s Marks “ITC certified quality “ mark “Safe toys” mark

v “Certification Body own quality” Mark ± ITC certified quality mark is applicable to affixing on product, documents and publication where indicates conformity with specific requirements. ± Rules are in the accordance with ISO/IEC 17030 (Conformity assessment – General requirements for third-party marks of conformity)

6. 전기제품 CE 마킹

v Scope of LVD directive 73/23/EEC ± As regard to LVD directive, it relates to all electrical equipment designed for use with a voltage rating between 50 V and 1000 V of the alternating current (AC) or between 75 V and 1500 V of the direct current (DC). Therefore the battery operated electrical instruments are not covered by this directive in majority of cases. In addition, the following equipments are excluded from the force of LVD (as they are covered by other more specific directives taking also into account the electrical safety): ± ± ± ± for use in the explosive atmosphere for medical use for lifts electricity meters plugs and socket outlets for domestic use electric fences specialized equipment used in ships, aircrafts and railways (as they are subject of specific legislation) radio-electrical interference.

v 기타 CE 마킹 대상 제품들 ± Examples are the radio and TV sets powered from electricity distribution network, electromotors and any instruments driven by electromotors, transformers, electrical fuses, capacitors, resistors and another electrical parts, switches, dimmers, power supplies, battery chargers, household home appliances (like vacuum cleaners, washing machines, steam irons, dryers, hair dryers, electric cookers), lights, electrical hobby tools, industrial equipment powered by electricity and their driving and controlling units, computers, printers, measuring instruments, etc. For the LVD is typical, that obligation of conformity assessment relates both to parts (as semiconductor parts or capacitors) and to complete assembled product (as a TV set). It is necessary to prevent confusion by CE marking of parts and products.

v 전자파 지침의 범위 ± EMC directive relates to any electrical and electronic equipment (including electronic components), liable to cause electromagnetic disturbances (sources of disturbance) or performance of which is liable to be affected by such disturbance (products sensitive to disturbance or electromagnetic interference). As no voltage limit is applied; the battery operated equipments are also objects of the EMC directive. Excluded is military equipment. Practically each common electric and/or electronic appliance (including individual electronic components) shall be evaluated from viewpoint of EMC. In addition to this, the products powered by voltage higher than 50 V (AC) / 75 V (DC) shall be assessed for compliance to LVD (electrical safety).

7. 개인용 보호장구의 CE 마킹

v 개인용 보호장구지침의 적합성 평가 ± PPE is defined as ‘‘any device or appliance designed to be worn or held for protection against one or more safety and health hazards’’. ± Directive does not differentiate between PPE used for work activities and for leisure. All protective equipment is required to comply, whether it is intended for use at work or in the home, even at sporting activities. ± Responsibility for deciding if a product is PPE or not rests with the manufacturer (or his authorized representative).

v Simple PPE – Category I Article 8. 3 of the Directive defines the ‘PPE of simple design‘ exclusively as the PPE intended to protect the wearer against: ± mechanical action whose effects are superficial (gardening gloves, thimbles etc. ); cleaning materials of weak action and easily reversible effects (gloves affording protection against diluted detergents, aprons etc. ); ± risks encountered in the handling of hot components which do not expose the user to a temperature exceeding 50 degrees C, or to dangerous impacts (gloves, aprons for professional use etc. ); ± atmospheric agents of a neither exceptional nor extreme nature (headgear, seasonal clothing, footwear etc. ); ± ± minor impacts and vibrations etc. which do not affect vital areas of the body and whose effects cannot cause irreversible lesions (light anti-scalping helmets, gloves, light footwear etc. ); sunlight (sunglasses).

v PPE, neither simple nor complex Category II ± ± ± The equipment in categories I and III are listed in the Directive. These lists are comprehensive and items which do not clearly fall within the descriptions of one list or the other must be either Category II PPE, or not PPE at all. Similar and exchangeable equipment not included in the scope of the PPE Directive: protective equipment for military use; protective equipment for self-defense; protective equipment for use by consumers to protect against: moisture, heat, certain weather conditions protective equipment intended for rescue activities on board ship or aircraft

v Complex PPE - Category III ± ± ± ± Article 8. 4(a) of the Directive defines the ‘PPE of complex design‘ as the PPE’s intended to protect against mortal danger, or against dangers that may seriously and irreversibly harm the health of an individual, the immediate effects of which cannot be identified in sufficient time. This category III covers exclusively: filtering respiratory devices for protection against solid and liquid aerosols or irritant, dangerous, toxic or radio-toxic gases; respiratory protection devices providing full insulation from the atmosphere, including those for use in diving; PPE providing only limited protection against chemical attack or against ionizing radiation; emergency equipment for use in high-temperature environments, the effects of which are comparable to those of an air temperature of 100 degrees C or more and which may or may not be characterized by the presence of infra-red radiation, flames or the projection of large amounts of molten material; emergency equipment for use in low-temperature environments the effects of which are comparable to those of an air temperature of -50 degrees C or less; PPE to protect against falls from a height; PPE to protect against electrical risks and dangerous voltages or that used as insulation in high-tension work.

8. 체외진단용 의료기기 CE 인증

v Scope of the In-Vitro Diagnostics Directive ± ± IVD relates to medical devices for in vitro diagnostics and their accessories. Each medical appliance that is: Reagent/reactive product/calibration material/control material/kit/instrument device/or a system ± In vitro investigation of specimens originating from the human body (saliva, perspiration, excrements, blood, tissue samples) with the aim to provide information: concerning a physiological or pathological state concerning a congenital (inherited) abnormality to determine the safety and compatibility with potential recipients to monitor therapeutic processes. In addition, specimen receptacles (containers for in-vitro tested samples) are IVD. ± Excluded from the scope of IVD are: ± products for general laboratory use, provided that the manufacturer did not appointed those products as specialised for In-vitro testing invasive sampling devices for collecting samples for In-vitro diagnostic IVD devices produced and used in the same institution, without any transport or sale to other bodies ± ± ±

v Classification of IVD ± ± The Directive recognises 4 categories of IVDs. The level of regulatory control applied to an IVD is proportional to the degree of risk connected with the IVD application. In following indents, the categories of IVD are ordered according to increasing risk level: ® General IVDs ® IVDs for self testing, i. e. test kits used in a home environment (excluding self test devices covered by Annex II) ® IVDs in Annex II, List B of the Directive, e. g. test kits for rubella, Chlamydia, CMV, PSA, or the major tissue typing groups ® IVDs in Annex II List A of the Directive, e. g. test kits for HIV, hepatitis B, C, or D, HTLV and the major blood groups.

v IVD List A & B ± Lists A and B in the Annex II are in detail described in following articles List A ± ± reagents, related calibrators and control materials, for determining the following blood groups: ® ABO system / rhesus (C, c, D, E, e) / anti-Kell, reagents, related calibrators and control materials, for the detection, confirmation and quantification in human specimens of markers of ® HIV infection (HIV 1 and 2) ® HTLV I and II ® and hepatitis B, C and D. List B ± ± ± ± ± IVD IVD IVD for for for determining the following blood groups: anti-Duffy and anti-Kidd determining irregular anti-erythrocytic antibodies the detection of the congenital infections: rubella, toxoplasmosis diagnosing of phenylketonuria determining infections by cytomegalovirus Chlamydia determining the HLA tissue groups: DR, A, B detection tumoral marker PSA evaluating the risk of trisomy 21 self-diagnosis of blood sugar content

v Conformity assessment of IVD General ± ± IVD that are not covered by Annex II and that are not the IVD devices for self testing nor performance evaluation: the manufacturer follows the procedure of Annex III (excluding point 6) draws up the EC declaration of conformity and affix the CE marking before placing the IVD on the market
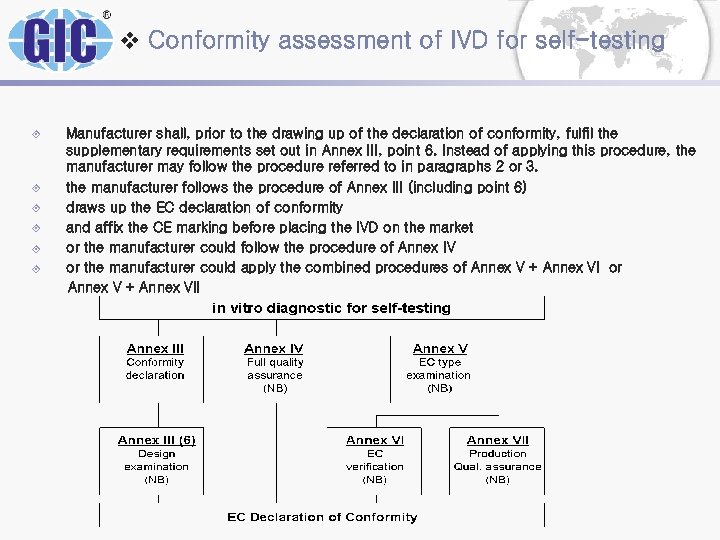
v Conformity assessment of IVD for self-testing ± ± ± Manufacturer shall, prior to the drawing up of the declaration of conformity, fulfil the supplementary requirements set out in Annex III, point 6. Instead of applying this procedure, the manufacturer may follow the procedure referred to in paragraphs 2 or 3. the manufacturer follows the procedure of Annex III (including point 6) draws up the EC declaration of conformity and affix the CE marking before placing the IVD on the market or the manufacturer could follow the procedure of Annex IV or the manufacturer could apply the combined procedures of Annex V + Annex VI or Annex V + Annex VII


v 필수 요구사항 의료기기 지침 93/42/EEC 제 3조 의료기기는 부속서 I에 나타난 필수요구사항을 만족시켜야 한다. 이 요건은 의료기기의 의도된 목적을 고려하여 적용된다. 부속서 I I. 일반 요구사항 Clause 1 ~ 6 II. 설계 및 구조에 관한 요구사항 7. 화학적, 물리적 및 생물학적 특성 8. 감염 및 세균오염 9. 구조 및 환경의 특성 10. 측정 기능을 가진 의료기기 11. 방사선에 대한 방어 12. 에너지원에 접속되는 의료기기 또는 에너지원을 갖는 의료기기에 대한 요구사항 13. 제조자에 의해 제공되어야 하는 정보 14. 기본요건에의 적합성이 (6)항에서처럼 임상데이터에 기초할 필요가 있는 경우, 그러한 데이터는 부속서 X (Annex X)에 따라 확립되어야 한다.

v 의료기기의 등급 분류 의료기기 지침 93/42/EEC 제 9조 1. 의료기기는 Class I, IIa, IIb 및 III으로 각각 분류된다. 등급분류는 부속서 IX (Annex IX)의 분류 규정에 따라야 한다. 2. 제조자와 인증기관과의 사이에 분류 규정을 적용한 결과 논쟁이 된 경우, 그 문제는 인증기관을 관할하는 행정당국으로 되돌린다. 3. 부속서 IX에 나타난 분류 규정은 제 7조 (2)에 나타난 절차에 따라 개정할 수 있다. 그때 기술진보를 고려하여, 제 10조에서 말하는 정보제도에 의해 입수 할 수 있는 정보를 고려한다.

v 의료기기의 등급 분류 부속서 IX (Annex IX) 1. 용어의 정의 1) 접촉시간 (Contact duration) 일시적(60분 미만), 단기간(60분 이상 30일 이하), 장기간(30일 초과) 2) 능동의료기기(Active medical device) 3) 삽입의료기기(Invasive medical device) 2. 분 류 1) 인체 비삽입 의료기기 : Rule 1 ~ 4 2) 인체 삽입 의료기기 : Rule 5 ~ 8 3) 능동 의료기기를 위한 추가 적용 규칙 : Rule 9 ~12 4) 특별 규칙 : Rule 13 ~ 18

v 의료기기의 등급 분류 규칙 등급 규칙 1 I IIa 규칙 2 I 비삽입 의료기기 다음 규칙에 적용되지 않는 모든 비삽입 의료기기 예) 인공항문 파우치, 소변 수집백, 병원용 침대, 수동 휠체어 채내에 주입, 주사할 목적으로 혈액, 체액, 조직, 액체, 가스의 통로가 되거나 저장하는 비삽입 의료기기 -능동형 의료기기에 연결되어 사용하는 경우 -체액, 혈액의 통로, 저장 또는 장기 및 인체조직을 저장하는 경우 예) 인슐린 펌프용 주사기 및 튜브, 정액 보관용기 등 - 그 외의 모든 경우 예) 의약품 계량용 컵 및 스푼 등 IIb 체내주입을 목적으로 혈액, 체액, 기타 액체를 생물학적, 화학적으로 변형시키는 비삽입 의료기기 예) 혈액 투석시스템 등 IIa - 여과, 원심분리, 가스 또는 열교환 방식을 사용하는 경우 예) 혈액 원심분리기, 의약품 정온기, 혈액 냉장/냉동고 등 I 손상된 피부에 접촉하는 비삽입 의료기기 - 기계적 보호막으로서 압박, 분비물 흡수에 사용하는 경우 예)거즈, 압박용 붕대, 면봉 등 규칙 3 규칙 4 IIa - 창상의 미생물 환경관리에 사용하는 것을 포함한 모든 경우 예) 국부마취용 접착제 IIb - 진피가 파열된 창상을 이차적 의도로 치료하는 데 사용하는 경우 예) 화상환자의 감염방지용 거즈(약품 포함)
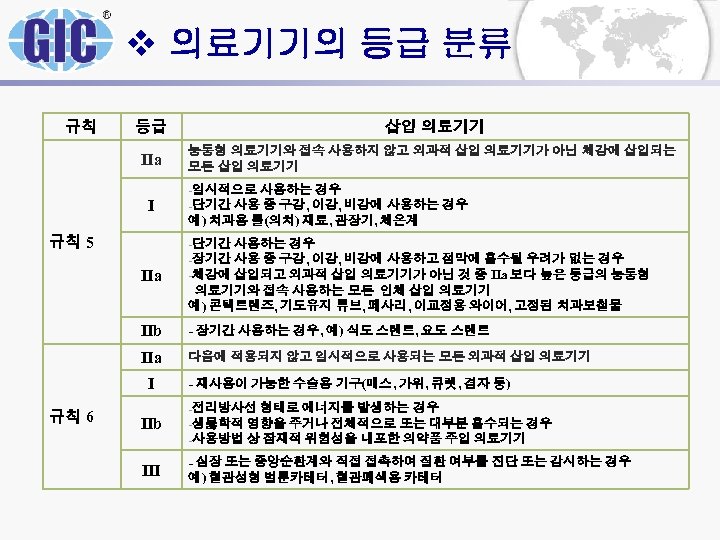
v 의료기기의 등급 분류 규칙 등급 삽입 의료기기 IIa 능동형 의료기기와 접속 사용하지 않고 외과적 삽입 의료기기가 아닌 체강에 삽입되는 모든 삽입 의료기기 -일시적으로 I 규칙 5 사용하는 경우 -단기간 사용 중 구강, 이강, 비강에 사용하는 경우 예) 치과용 틀(의치) 재료, 관장기, 체온계 -단기간 IIa 사용하는 경우 사용 중 구강, 이강, 비강에 사용하고 점막에 흡수될 우려가 없는 경우 -체강에 삽입되고 외과적 삽입 의료기기가 아닌 것 중 IIa 보다 높은 등급의 능동형 의료기기와 접속 사용하는 모든 인체 삽입 의료기기 예) 콘택트렌즈, 기도유지 튜브, 페사리, 이교정용 와이어, 고정된 치과보철물 IIb - 장기간 사용하는 경우, 예) 식도 스텐트, 요도 스텐트 IIa 다음에 적용되지 않고 일시적으로 사용되는 모든 외과적 삽입 의료기기 -장기간 I 규칙 6 - 재사용이 가능한 수술용 기구(매스, 가위, 큐렛, 겸자 등) -전리방사선 IIb 형태로 에너지를 발생하는 경우 -생뭃학적 영향을 주거나 전체적으로 또는 대부분 흡수되는 경우 -사용방법 상 잠재적 위험성을 내포한 의약품 주입 의료기기 III - 심장 또는 중앙순환계와 직접 접촉하여 질환 여부를 진단 또는 감시하는 경우 예) 혈관성형 벌룬카테터, 혈관폐색용 카테터

v 의료기기의 등급 분류 규칙 등급 IIa 삽입 의료기기 다음을 제외하고 단기간 사용하는 모든 외과적 삽입 의료기기 예) 클램프, 주입용 카뉼라, 임시충전재료 -전리방사선 규칙 7 IIb 형태로 에너지를 발생하는 경우 -의약품 주입 및 치아에 사용하는 것을 제외하고 체내에서 화학적 변화를 하는 경우 예) 비흡수성 합성폴리머재료, 비흡수성 생체조직용 접착제 -직접 III 접촉하여 심장, 중앙순환계의 결함을 진단, 감시하는 경우 직접 접촉 사용되는 경우 -생물학적 영향을 주거나 전체적으로 또는 대부분 흡수되는 경우 예) 심혈관 카테터, 흉부 카테터, 흡수성 봉합사, 생체조직용 접착제 -중추신경계에 IIb 규칙 8 다음을 제외한 모든 임플란트 및 장기간 사용되는 외과적 삽입 의료기기 예) 비혈관 스텐트, 비흡수성 봉합사, 골고정재, 골시멘트, 연속착용렌즈 IIa - 치아에 사용하는 경우 예) 치과용 합금, 세라믹 및 폴리머, 브리지 -심장, III 중앙순환계, 중추신경계에 직접 접촉되는 경우 -생물학적 영향을 주거나 전체적으로 또는 대부분 흡수되는 경우 -의약품주입 및 치아에 사용하는 것을 제외하고 체내에서 화학적 변화를 하는 경우 예) 혈관스텐트, 심혈관용 봉합사, 흡수성 봉합사, 약물방출 보철물

v 의료기기의 등급 분류 규칙 등급 IIa 능동형 의료기기 다음을 제외한 주사 또는 에너지 교환을 목적으로 하는 모든 치료용 능동기기 예) TENS, 열교환기, 전동드릴, 보청기 -의료기기의 IIb 특성, 강도, 에너지 전달 위치 등을 고려할 때 잠재적으로 위험한 방법 으로 주사 또는 에너지 교환을 화는 경우 -치료용 능동의료기기의 성능을 제어, 감시하거나 성능에 직접 영향을 주는 경우 예) 인공호흡장치, 인큐베이터, 고주파 전기수술기, 레이저수술기, X-선 치료기 IIa 진단용 능동기기 -환자조명기기를 제외하고 인체에 에너지가 흡수되는 경우 -방사선 물질로 영향을 취득하는 경우 예) MRI장비, 펄스테스터, 초음파진단기, 감마카메라, 전동 혈압계 규칙 9 규칙 10 -심장기능, IIb 호흡수 등 중요한 생리학적 지표를 감시하는 경우 전리방사선을 이용하여 진단, 치료하는 능동기기 예) 환자감시장치, X-선 진단장치 IIa 다음을 제외하고 의약품, 체액, 기타물질을 체내에 주입 또는 제거하는데 사용하는 모든 능동기기 (흡입장치, 급식펌프, 의료용 분무기) IIb - 관련물질의 특성, 신체의 부분, 적용방법이 잠재적 위험성이 내포된 경우 예) 약품주입펌프, 인공호흡장치, 마취기, 혈액펌프, 고압챔버, 의료용 가스혼합기 규칙 11 규칙 12 I 모든 다른 능동기기 예) 의료용 조명장치, 광중합기, 환자견인기
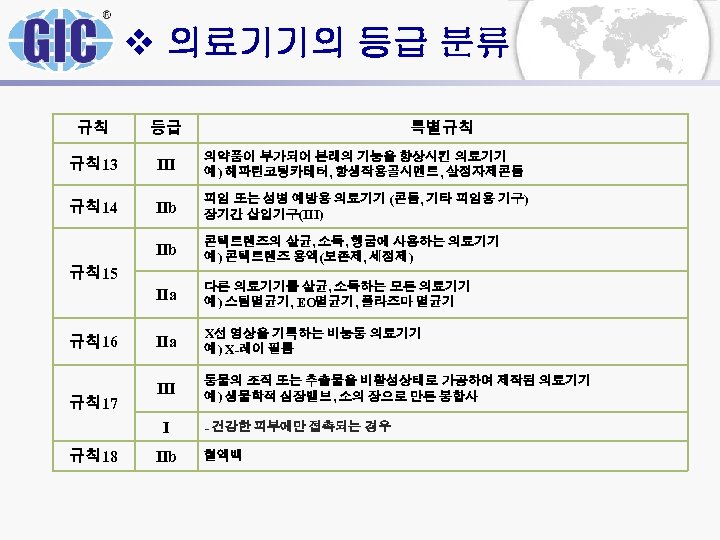
v 의료기기의 등급 분류 규칙 등급 규칙 13 III 의약품이 부가되어 본래의 기능을 향상시킨 의료기기 예) 헤파린코팅카테터, 항생작용골시멘트, 살정자제콘돔 규칙 14 IIb 피임 또는 성병 예방용 의료기기 (콘돔, 기타 피임용 기구) 장기간 삽입기구(III) IIb 콘택트렌즈의 살균, 소독, 헹굼에 사용하는 의료기기 예) 콘택트렌즈 용액(보존제, 세정제) IIa 다른 의료기기를 살균, 소독하는 모든 의료기기 예) 스팀멸균기, EO멸균기, 플라즈마 멸균기 IIa X선 영상을 기록하는 비능동 의료기기 예) X-레이 필름 III 동물의 조직 또는 추출물을 비활성상태로 가공하여 제작된 의료기기 예) 생물학적 심장밸브, 소의 장으로 만든 봉합사 규칙 15 규칙 16 규칙 17 I 규칙 18 IIb 특별규칙 - 건강한 피부에만 접촉되는 경우 혈액백
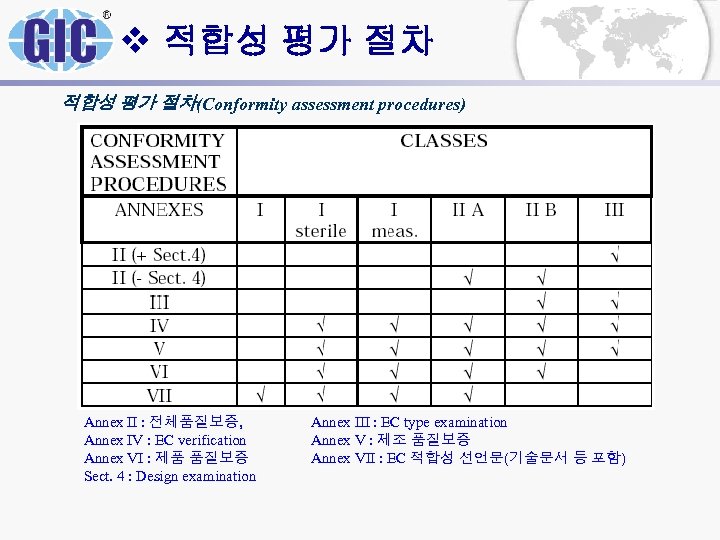
v 적합성 평가 절차(Conformity assessment procedures) Annex II : 전체품질보증, Annex IV : EC verification Annex VI : 제품 품질보증 Sect. 4 : Design examination Annex III : EC type examination Annex V : 제조 품질보증 Annex VII : EC 적합성 선언문(기술문서 등 포함)
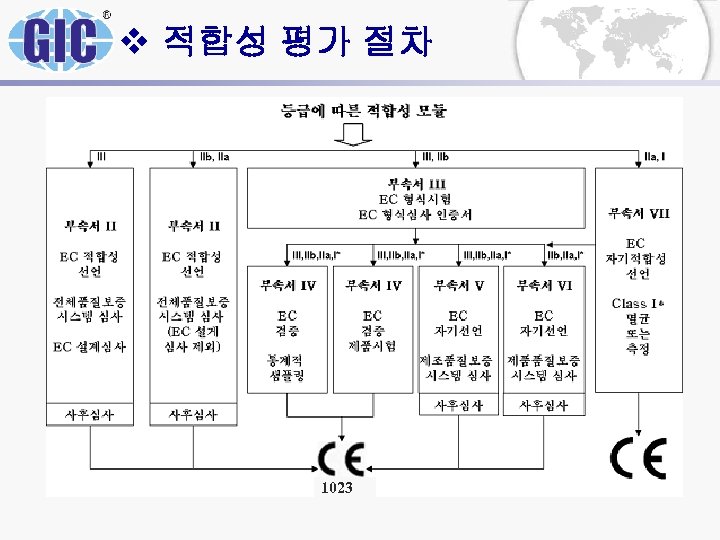
v 적합성 평가 절차 1023

v 적합성 평가 절차 인증서의 타입 지침에 의해 발행될 수 있는 EC certificate는 다음과 같다. - EC Design-Examination Certificate (Annex II section 4 MDD; Annex 2 section 4 AIMD) - EC Type Examination Certificate (Annex III MDD; Annex 3 AIMD) - Full Quality Assurance System Approval Certificate (Annex II section 3 MDD; Annex 2 section 3 AIMD) - EC Verification Certificate (Annex IV MDD; Annex 4 AIMD) - Production Quality Assurance System Approval Certificate (Annex V MDD; Annex 5 AIMD) - Product Quality Assurance System Approval Certificate (Annex VI MDD)

v CE 마킹 의료기기 지침 93/42/EEC 제 17조 1. 제 3조에서 말하는 기본 요구사항에 합치한다고 생각되는 의료기기는 시장 출하 시 적합한 CE marking을 부착하여야 한다. 단, 주문형 의료기기 또는 임상 시험용 의료기기는 제외한다. 2. CE marking은 부속서 XII에 나타내듯이, 보기 쉽고, 읽기 쉽고, 지우기 어려운 방법으로 의료기기에 붙인다. 또는, 멸균 팩이 실제적으로 적당하면 멸균 팩에 붙인다. 어느 경우나 취급설명서에 표시한다. 가능하면, CE marking은 판매용 포장에도 표시한다. CE marking에는, 부속서 II, IV, V, VI의 순서의 실시에 책임을 가진 인증기관의 식별번호를 부착하여야 한다. 3. 제삼자가 볼 때, 의미 및 도형이 CE marking과 혼동하기 쉬운 마크 및 명판은 붙여서는 안 된다. 다른 마크를 의료기기, 포장 및 의료기기에 첨부하는 취급 설명서에 부착해도 좋지만, 그에 따라 CE marking의 보기 쉽거나, 읽기 쉬움을 감소시켜서는 안 된다.

v CE 마킹 부속서 XII CE marking은 다음의 형태로 된 “CE” 글자로서 구성되어야 한다. XXXX - 만약 이 마크를 축소하거나 확대할 경우에는 위의 도면을 반드시 고려하여야 한다. - CE marking의 여러 부분은 반드시 동일한 수직제원을 충분히 갖추어야 하며, 5 mm 이상 크기여야 한다. 최소한의 제원은 작은 의료기기에 적용되지 않을 수 있다.

v 임상 시험 의료기기 지침 93/42/EEC 제 15조 2. Class III의 의료기기 및 임플란트 및 외과적 장기 삽입의료기기로 Class IIa 또는 IIb의 의료기기의 경우, 제조자는 신고 후 60일 뒤에 임상시험을 개시할 수 있다. 단 행정당국이 이 기간 내에 공중의 건강 또는 공공정책에 대하여 고려한 결과, 시험을 허가하지 않는 뜻을 제조자에게 통보한 경우는 제외 한다. 그러나 윤리위원회가 그 시험프로그램에 찬성의견을 표명한 경우, 가맹국은 제조자에 대하여 상기 60일 간의 기한만료 이전이라도 제조자에 대하여 임상 시험 개시를 허가할 수 있다. 5. 임상시험은 부속서 X (Annex X) 조항에 따라 실시되어야 한다. 부속서 X의 조항 은 제 7조 (2)에 정하는 절차에 의해 조정될 수 있다.

v 감시 시스템 (Vigilance system) 시장 출하 후에 일어나는 사고에 관한 정보 의료기기 지침 93/42/EEC 제 10조 1. 가맹국 각 국은 필요한 수단을 강구해 다음 사실을 보증한다. 이 지침의 규정에 따라 각 국이 알아낸 정보로, 이하의 사고와 관련해, 의료기기가 관여하고 있는 정보의 기록 및 평가는 모두 중앙에 집약해 행하여야 한다. 2. a) 의료기기의 특성 및 성능의 이상 또는 노화를 초래하거나 라벨링이나 취 급 설명서가 적절하지 않음으로 인한, 환자 또는 사용자가 사망 또는 건강 상태가 매우 악화될 우려가 있거나 우려가 있었던 사고 3. b) a)에서 말하는 의료기기의 특성 및 성능에 관해, 제조자가 동종 타입의 의료기기를 리콜하는 기술적 이유 또는 의학적 이유 2. 가맹국이 의료종사자 또는 의료기관에 대하여 1항에서 말하는 사고를 전부 행정 당국에 보고하도록 요청한 경우, 가맹국은 필요한 수단을 강구하여, 당해 의료기 기의 제조자 또는 EC지역 내의 대리인이 사고정보를 입수할 수 있도록 보증하여 야 한다.

v 감시 시스템 (Vigilance system) 시장 출하 후에 일어나는 사고에 관한 정보 의료기기 지침 93/42/EEC 제 10조 3. 가맹국은 가능하면 제조자와 공동으로 평가를 실시한 후, 제 8조(안전보호규정) 에 구애되지 않고, EC위원회 및 다른 가맹국에 1항에서 말하는 사고를 즉시 보고 한다. 여기에는 어떠한 수단을 강구한 사고, 혹은 수단을 검토 중인 사고를 포함 한다.


v 개요 1. 일반 ü ISO 9001 과 ISO 13485 를 통한 의료기기 제조업체의 품질경영시 스템 인증은 업체에게 많은 이점을 가져다 주며 많은 경우 의료기기 수출업체들에게 강제사항이기도 하다. ü 유럽연합 내에서 능동형 의료기기지침, 의료기기 지침, 체외진단의 료기 지침 등의 EU 지침의 이행은 의료기기의 유럽연합 내 자유이 동을 보장한다. EU 지침 요구사항과의 적합성증명에 있어 상당 부 분은 품질시스템의 수립과 이의 객관적 평가가 차지한다. ü 현행 유럽 의료기기 품질시스템 규격은 2003년 7월 24일 공표된 EN ISO 13485: 2003 이다. 이 규격은 이전 조화규격 EN SIO 13485: 2000 과 EN ISO 13488: 2000 을 대체하며 유예기간은 2006 년 7월 말까지였다.

v 개요 2. ISO 13485 – 인증 해당 업체 ü 자체브랜드로 의료기기를 제조하는 회사로서 향후 유럽연합시장 에서 자사브랜드로 제품을 팔고자 하는 회사. ü 의료기기나 체외진단 의료기를 설계, 제조 및 조립하는 회사, 또는 의료기기 부품 제조업체 ü 체외진단의료기 제조업체 중 마케팅에 경쟁력을 제고하고자 하는 업체나 미래에 유럽시장에 진입계획을 가지고 유럽의 강제적 체외 진단의료기 관련 법규에 대비하고자 하는 업체.


v CE 인증을 위하여 요구되는 문서 리스트 1. Device Master File 2. Design File 3. QM documents 4. QM records 5. EC Declaration of conformance 6. Checklist of the Essential requirements 7. Reference to specific documents 8. Description of the device 9. Copy of issued Certificate by Notified Body 10. Labels and instructions for use


v FDA 개요 • 미국 식품의약품안전청 FDA는 식품 의약품 법에 의하여 불순물의 혼합, 허위 표시된 식품, 의약품, 화장품 및 의료 기기 등에 의한 잠재적인 건강상의 위해로부터 미국 내 소 비자들의 보호를 위해 설립된 국가 기관 • 승인을 위한 조사, 분석, 연구 및 규정 준수 여부 감시는 국립의료 기기 및 방사능 보호센터, 생물학 및 연구소, 의 약품 평가 및 연구소, 식품안전 및 영양센터, 수의약품센 터 등에서 관할

v FDA 의료기기 등급 분류 의료용구를 안전성, 유효성에 따라 3등급으로 분류하여 등급 에 따라 판매 전 허가절차를 달리하고 있으며, 1등급 경우 신고의 절차를 밟고 2등급 이상은 허가 절차를 밟게 됨. • Class 1: 일반규제요건 준수의무 • Class 2: 일반규제요건, 시판전신고 (510(k)), GMP 준수의무 • Class 3: 일반규제요건, 시판전승인 (PMA), GMP 준수의무

v FDA 의료기기 등급 분류_Class I • 반창고, 붕대, 장갑 등과 같이 위험도가 낮은 제품 • GMP (Good Manufacturing Practice) 심사 면제 • Class I의 일반 규제 요건 1. 제조자, 배급업자, 포장과 재 표시업자등 CFR 807. 2 조항에 해당되는 회사의 등록 (Registration) 2. 제품의 등록 (Device Listing) 3. 의료용구의 금지 FDA 에서 인체에 위해를 중 우려가 있는 의료용구는 연방관보에 발표 후, 청문회를 개최하며, 건강에 심각한 위해가 있을 경우 즉각 금지 4. 통보 및 수리, 교환과 환불 제조자는 불량 의료용구 발견 즉시 사용자에게 통보하거나 수리, 교환, 환불할 의무가 있음. 5. 기록과 보고 제조자는 의료용구의 품질을 보증하기 위한 시험검사기록 등을 유지하여야 하며, 필요한 경우 이를 보 고할 의무가 있음 6. 의료용구의 제한 의료용구의 안전성, 유효성의 합리적 보증이 불가능할 경우 FDA는 그 의료용구의 판매, 유통, 사용을 제한할 수 있음 7. 1과 2의 시설 및 제품등록 은 매년 FDA에 보고되어야 함

v FDA 의료기기 등급 분류_Class II • 일반규제만으로 그 안전성 및 효과 성을 확인하기 힘든 경우이며, 일 반 규제요건 외에 510(k)가 이루어져야 함 • 510(k) Submission은 일반적으로 2등급 의료용구의 판매승인을 위한 내용 시판전 신고 510(k)의 개요 • 시판 전 신고 510(k)는 시판 예정인 의료기기와 미국 시장에서 과거 또는 현재 판매 되고 있는 의료기기의 본질적 동등성 을 검증하기 위 함 (SE: Substantially Equivalent)을 검증하기 위함

v 본질적 동등성_Class II • 조건 1: Predicate Device와 동일한 용도로 사용되며 그 기술적 특 성이 같음 • 조건 2: Predicate Device와 동일한 용도로 사용되며 그 기술적 특 성은 다르나 안전성 및 효능이 문제 없고 Predicate Device 와 동일한 안전성 및 효능이 인정 됨 • 조건 1과 조건 2 모두를 만족 시킨다면 시판된 의료기기와 본질적으로 동등하다고 간주 • 동등성이 판명되면 시판승인서 (SE Letter)발송 후 판매 및 유통 • 동등하지 않은 경우 510(k)를 다시 하거나 PMA절차를 따름

v 510(K) 주요 제출 내용_Class II • 신청자의 현황 – 신청자명, 주소 등 • 제품의 설명 – 제품명, 해당 등급, 형상 및 구조, 사용목적 및 기타 필요한 제품정보 • 표시사항, 멸균에 관한 자료 • 성능기준 (Perfomance Standard): 제품에 적용되는 성능 기준을 기술 • 본질적 동등성 입증자료 • 시험검사성적서 자료: 성능 및 생체적합성에 관한 시험검 사결과 자료

v Class III • Class III 의료기기는 가장 엄격한 규제 범위이며, Class III 기기는 일반 규제범위 또는 510(k) 만으로는 그 안전성과 효능을 확인하기에 불충분한 정보들이 존재 • Class III에 속하는 기기는 인간의 생명을 유지시키는 기구들로, 인간 건강의 손상을 예방할 때 다른 질병이나 부상의 잠재적인 위험을 제공 할 수 있음

v Class III PMA 신청서는 해당 기기의 안전성 및 효능의 설득력 있는 정보 요구 • 의료기기가 자체의 사용용도에 대해 안전하고 효과적이라는 것을 증명 할 과학적 자료 • 대부분의 경우 규정에 의한 임상연구에 대한 자료를 요구 • PMA 신청을 지원하기 위한 임상연구는 임상시험 의료기기 적용면제 규정에 따름

v Class III PMA 심사진행은 행정, 신청심사, 과학 미 규정심사, 자문위원회 심사, 추천, 그리고 최종 허가의 문서화와 통지 등으로 이루어짐 • 상업적으로 배급되는 1%의 의료기기는 PMA과정을 경험 • 510(k)과정을 통해 시판된 3등급 의료기기는 FDA가 아 직도 시판 전 허가신청서를 요청하지 않은 개정 전기기 (Preamendment Device)임

v Class III 510(k) 시판전 승인 내용 PMA는 510(k)의 일반사항 이외에 안전성, 유효성심사를 위한 다음의 추 가자료를 요구 하며, 최종승인을 위하여 GMP 현장심사가 추가 • 전임상시험자료 (Preclinical Laboratory Testing Data) - 기기 및 재료의 물리적, 화학적, 기계적 특성에 관한 시험 - 재료에 대한 독성시험등 생체적합성 시험 • 동물시험 자료 (Animal Testing Data) - 새로운 재료 또는 변형재료, 임플란트, 인공심장박동기 등에 적용 • 임상시험성적자료 (Human Clinical Testing Data)


v NRTL 이란? NRTL 인증은 ? 미국 노동부(Department of Labor) 산하의 직업안전보건청(OSHA; Occupational Safety & Health Administration)에서 작업자의 안전을 위하여 산업현장(workplace)에 서 사용되는 모든 산업용품에 대하여 공인된 시험소를 통하여 그 제품의 안전성을 인증 받도록 하는 인증제도임 국내에서 생산된 제품이 미국으로 수출되어 유통되기 위해서는 NRTL 인증을 획득 할 수 있으며, 이렇게 안전성 인증을 받아야 하는 산업용품은 OSHA에서 직접 지정․ 고시함 현재 OSHA에서 지정한 산업용품군은 엘리베이터, 케이블, 모니터, 컴퓨터 및 AV 기기 등을 비롯한 37개의 품목 군이 해당 되며 600여개 품목에 달하고 있음(거의 모 든 제품이 해당된다고 볼 수 있음)

v UL? & NRTL? • 지금까지 많은 제조자들은 미국 수출을 위해 UL을 고집 (Underwriters Laboratory) • UL은 미국 강제인증제도? -> UL은 강제 인증이 아님. • 미국의 인증제도는 UL이 전부인가? -> UL과 동일한 효력의 인증이 존재. (NRTL) • UL도 NRTL 중 하나에 불가
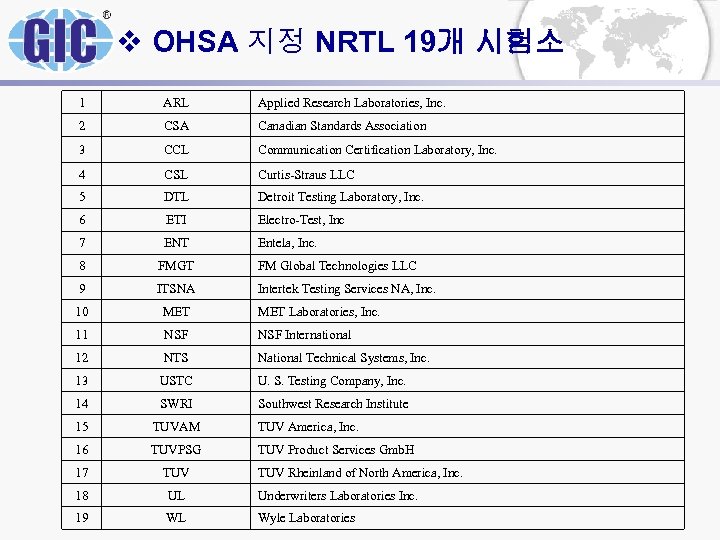
v OHSA 지정 NRTL 19개 시험소 1 ARL Applied Research Laboratories, Inc. 2 CSA Canadian Standards Association 3 CCL Communication Certification Laboratory, Inc. 4 CSL Curtis-Straus LLC 5 DTL Detroit Testing Laboratory, Inc. 6 ETI Electro-Test, Inc 7 ENT Entela, Inc. 8 FMGT FM Global Technologies LLC 9 ITSNA Intertek Testing Services NA, Inc. 10 MET Laboratories, Inc. 11 NSF International 12 NTS National Technical Systems, Inc. 13 USTC U. S. Testing Company, Inc. 14 SWRI Southwest Research Institute 15 TUVAM TUV America, Inc. 16 TUVPSG TUV Product Services Gmb. H 17 TUV 18 UL Underwriters Laboratories Inc. 19 WL Wyle Laboratories TUV Rheinland of North America, Inc.


v CCC 중국 강제인증 개요 중국의 품질 및 안전관련 인증제도는 국내산품과 수입 품에 대해 별도의 인증을 적용 하는 등 이원적으로 운영 되었는데, 이는 WTO기본이념인 "내국민대우의 원칙"에 위배. WTO 가입을 계기로 인증제도의 개선을 위해 2002. 5. 1일 부터 이를 하나의 인증제도로 통합하여 CCC(China Compulsory Certification, 중국강제 인증) 마크제도를 시 행.

v CCC 개요 • CCC는 China Compulsory Certification 의 약어 로, 통상 “중국강제인증” 으로 지칭. • 중국 내 유통되는 모든 제품을 대상으로 IEC(국제전기 표준 협회) 및 중국 국가 표준에 의한 안전 및 품질 인증 을 의무화한 제도. • CCC 인증을 취득하지 못할 경우, 중국 국내산 제품의 생산 및 수출, 외국산 제품의 중국 내 수입이 일체 금지 된다.
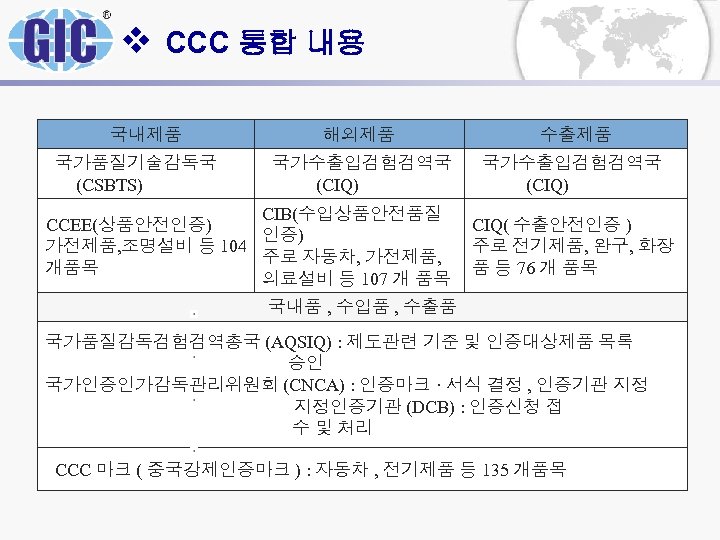
v CCC 통합 내용 국내제품 해외제품 국가품질기술감독국 (CSBTS) 수출제품 국가수출입검험검역국 (CIQ) CIB(수입상품안전품질 CCEE(상품안전인증) 가전제품, 조명설비 등 104 주로 자동차, 가전제품, 개품목 의료설비 등 107 개 품목 CIQ( 수출안전인증 ) 주로 전기제품, 완구, 화장 품 등 76 개 품목 국내품 , 수입품 , 수출품 국가품질감독검험검역총국 (AQSIQ) : 제도관련 기준 및 인증대상제품 목록 승인 국가인증인가감독관리위원회 (CNCA) : 인증마크 · 서식 결정 , 인증기관 지정 지정인증기관 (DCB) : 인증신청 접 수 및 처리 CCC 마크 ( 중국강제인증마크 ) : 자동차 , 전기제품 등 135 개품목
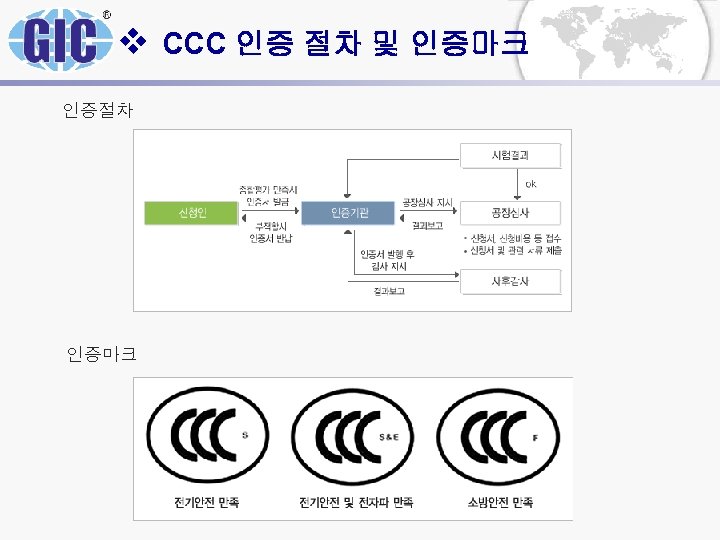
v CCC 인증 절차 및 인증마크 인증절차 인증마크

v WTO 가입 이후 중국의 변화 • 가입전 : 내국에서 생산되는 제품, 수출되는 제품, 수입되는 제품별로 서 로 다른 인증제도를 적용. • 가입후 : WTO의 기본정신인 "내국민 대우의 원칙"에 따라 중국 내 에 서 유통되는 모든 제품에 대해 • 동일한 인증제도를 적용하고 강제성 강화함. • 중국내 인증관리 체계 및 적용 요건의 국제 표준화. • 수입품 및 국내 생산품 승인관련 기구를 통일함. • 기술규범 및 기술수준의 국제 규격화.


v SFDA 의료기기 정의 중국의료기기 감독 및 관리규정 제 3조 의료기기란 적절하게 적용하기 위하여 필요한 소프웨어를 포함하여, 단독 또는 조합되는 임의의 장비, 기구, 장치, 재료 또는 기타 물품을 말한다. 그것 은 약학적, 면역학적 또는 신진대사에 따라 인체에서 또는 인체내에서 주요 한 활동을 이루는 것이 아니고 이러한 방법에 의하여 그 기능을 보조할 수 있 는 것이다. 의료기기의 사용목적 -질병의 진단, 예방, 감시, 치료 -상해 또는 장애상태의 진단, 감시, 치료, 완화 경감 또는 보충 -해부학 또는 생리학에 대한 연구, 대체 또는 수정 -임신 조절 의료기기의 관리감독 국무원 산하 국가약품감독관리국(State Food Drug Administration , 이하 "SFDA"라 함)에서 전국의 의료기기에 대한 관리 및 감독의 책임이 있다. - 수 입의료기기에 대해서는 전부 SFDA의 승인을 득 하여야 한다. - 중국내 제조 되는 의료기기에 대해서는 군급 이상의 행정기관의 약품감독기관이 각 관할 지 역내의 의료기기에 대한 관리 감독의 책임이 있다.

v SFDA 의료기기 등급 분류 등급분류 정 의 등록 및 관리감독 중국내제조 수입 1등급 일반적 관리로 안전성 및 유 효성을 보장할 수 있는 의료 기기이다. 2등급 안전성 및 유효성을 보장하기 성, 자치구, 직할시 정부 약품감독 위하여 추가적인 관리가 요구 관리부문심사 및 등록증 발급 되는 의료기기이다. SFDA 심사 생 산 등록증 발 급 3등급 생명 보조 또는 유지에 사용 되거나 인체에 삽입되거나 또 는 인체에 대한 잠재적 위험 SFDA(국무원 약품감독관리부문) 성을 가지고 있어 안전성 및 심사 및 생산등록증 발급 유효성의 관점에서 엄격하게 관리되어야 하는 의료기기이 다. SFDA 심사 생 산 등록증 발 급 설립지역의 시급 약품감독관리부 문심사 및 등록증 발급 SFDA(등록)
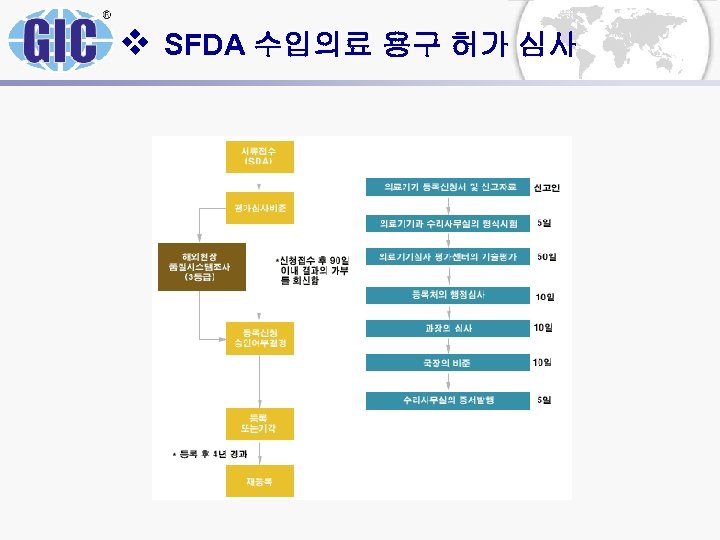
v SFDA 수입의료 용구 허가 심사

v SFDA 의료기기 판매회사 의료기기판매회사의 구비조건 1. 판매되는 의료기기에 필요한 적절한 시설 및 환경의 보유. 2. 판매되는 의료기기에 필요한 적절한 품질검사직원의 보유 3. 판매되는 의료기기에 필요한 기술교육, 보수 및 A/S를 제공 할 수 있는 적 절한 능력의 보 유 의료기기 판매회사의 판매업 유효기간 : 5년 의료기기 판매업 허가 신청 1. 중앙정부 직속의 성, 자치구, 직할시의 약품감독기관이 승인 2, 감독기관은 신청서 접수 후 1개월 이내에 허가여부 결정 통보 의료기기 광고 1. 성급 이상의 약품감독기관의 검토 및 승인을 받아야 출판, 방송, 유포 및 게시 할 수 있음. 2. 광고 내용은 감독기관으로부터 승인 받은 사용설명서에 근거하여야 함.

v SFDA 신청서류 심사검사 1. 중국은 외국과 상호 인가 협의 가 되어 있지 않아 자국의 법률에 의거 심사와 감독관리를 진행 2. 심사의 내용: 기술성 심사가 핵심내용이며, 제조국에서의 심사 및 신청 자료도 중시함. 3. 심사 신청시의 자료: 제조국의 자료에 근거하여 판단하고 추가로 동일 하지 않은 것에 대해서 필요자료를 요구함. 제조국 자료가 없을 시는 중 국의 기준에 따라 준비 제출되어야 함. 4. 수입제품의 임상 요구: 2, 3등급 의료기기의 임상 시험 성적 자료 요구. 1) 제조국에서 허가 받지 않은 제품은 중국에서 임사을 거쳐야 함. 2) 제조국 허가 제품은 중국의 심사 기준에 의거 기존 임상자료 확인. 3) 면제대상: 비교적 위험성이 작고, 중국 내 출시가 오래 되었으며, 제 품 품질의 불평이 없는 경우에 한하여 임상의 감면이 가능.

v SFDA 신청서류 심사검사 5. 제품의 시험 검사 1) 검사의 기준: 국가기준, 업종기준, 강제기준 등을 적용 안전기준, ISO 60601 -1 계역기준, ISO 10993 계열기준 및 중국의 안전기준 2) 등록전 검사: 일반적인 의료기기 3) 등록후 검사: 설치장소를 요하는 대형 설비 제품이 대상. SFDA 인 가 기구에서 시험검사 실시 4) 검사의 감면대상: 이미 중국 시장에 출시되어 사용자의 불만이 없 는 경우의 제품에서 가능 5) 성능시험: 주요 성능 요구사항과 설명서 등에서 언급된 성능 등에 대해서 기준상에 구체화 하고 시험방법의 제시가 있어야 함

v SFDA 의료기기 허가 신청 서류 1. 2. 3. 4. 5. 6. 등록 신청서 – 중, 영문 대조 의료기기 제조업체(생산자)의 자격증명서 신청인의 자격 증명서 제품의 기술보고서 (Product Technical File) 제품의 모든 성능 및 기능에 대한 자체 시험성적서 SFDA에서 인정한 시험기관에서 시험생산 등록 신청전 1년내에 발행한 형식시험성적서 7. 최소 임상시험 2개소에서의 임상시험 보고서 8. 제품사용설명서 9. 품질보증서 10. A/S 위탁서 및 A/S 업체의 승낙서 11. A/S 업체의 자격증명 12. 제출한 서류의 진실성을 보장하는 각서 13. 기 타

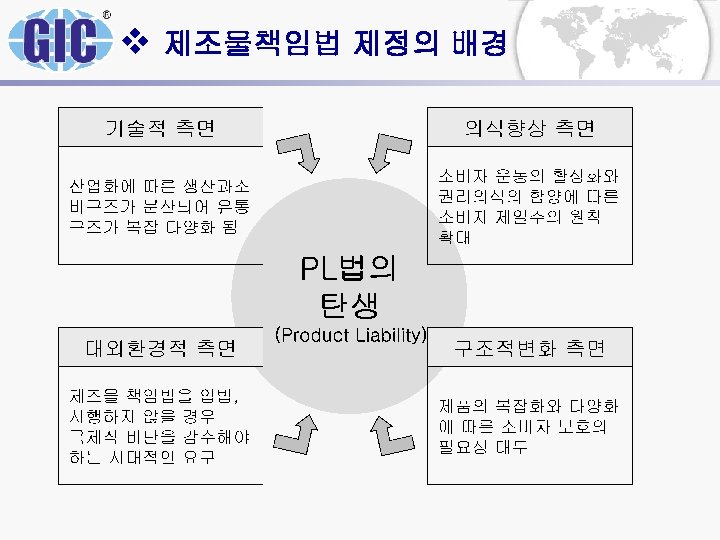
v 제조물책임법 제정의 배경
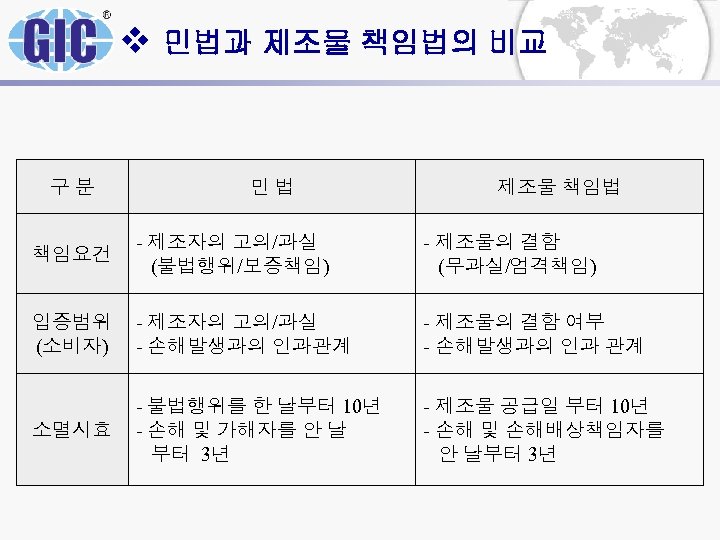
v 민법과 제조물 책임법의 비교 구 분 민 법 제조물 책임법 책임요건 - 제조자의 고의/과실 (불법행위/보증책임) - 제조물의 결함 (무과실/엄격책임) 입증범위 (소비자) - 제조자의 고의/과실 - 손해발생과의 인과관계 - 제조물의 결함 여부 - 손해발생과의 인과 관계 소멸시효 - 불법행위를 한 날부터 10년 - 손해 및 가해자를 안 날 부터 3년 - 제조물 공급일 부터 10년 - 손해 및 손해배상책임자를 안 날부터 3년
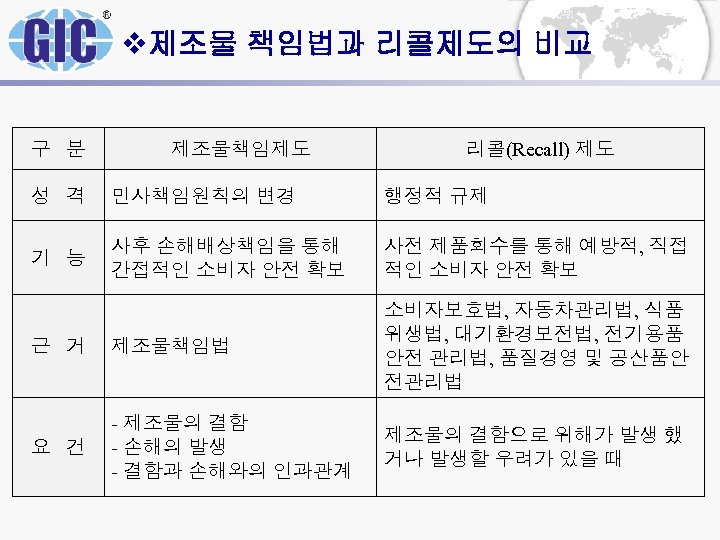
v제조물 책임법과 리콜제도의 비교 구 분 제조물책임제도 리콜(Recall) 제도 성 격 민사책임원칙의 변경 행정적 규제 기 능 사후 손해배상책임을 통해 간접적인 소비자 안전 확보 사전 제품회수를 통해 예방적, 직접 적인 소비자 안전 확보 근 거 제조물책임법 소비자보호법, 자동차관리법, 식품 위생법, 대기환경보전법, 전기용품 안전 관리법, 품질경영 및 공산품안 전관리법 요 건 - 제조물의 결함 - 손해의 발생 - 결함과 손해와의 인과관계 제조물의 결함으로 위해가 발생 했 거나 발생할 우려가 있을 때
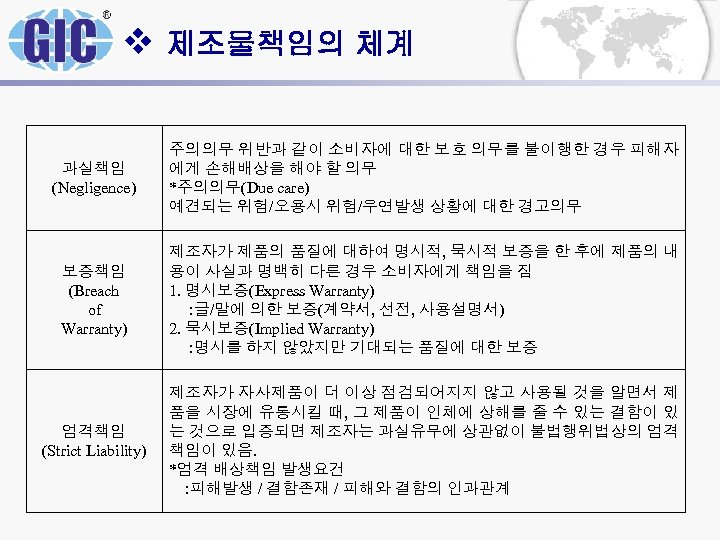
v 제조물책임의 체계 과실책임 (Negligence) 주의의무 위반과 같이 소비자에 대한 보호 의무를 불이행한 경우 피해자 에게 손해배상을 해야 할 의무 *주의의무(Due care) 예견되는 위험/오용시 위험/우연발생 상황에 대한 경고의무 보증책임 (Breach of Warranty) 제조자가 제품의 품질에 대하여 명시적, 묵시적 보증을 한 후에 제품의 내 용이 사실과 명백히 다른 경우 소비자에게 책임을 짐 1. 명시보증(Express Warranty) : 글/말에 의한 보증(계약서, 선전, 사용설명서) 2. 묵시보증(Implied Warranty) : 명시를 하지 않았지만 기대되는 품질에 대한 보증 엄격책임 (Strict Liability) 제조자가 자사제품이 더 이상 점검되어지지 않고 사용될 것을 알면서 제 품을 시장에 유통시킬 때, 그 제품이 인체에 상해를 줄 수 있는 결함이 있 는 것으로 입증되면 제조자는 과실유무에 상관없이 불법행위법상의 엄격 책임이 있음. *엄격 배상책임 발생요건 : 피해발생 / 결함존재 / 피해와 결함의 인과관계
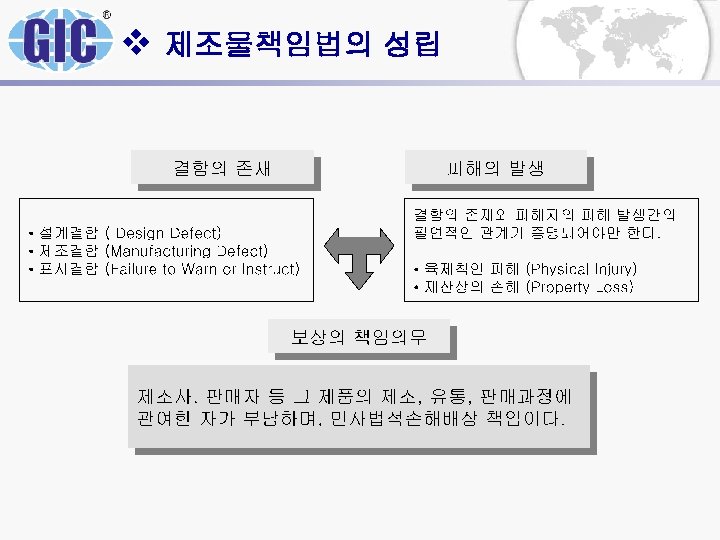
v 제조물책임법의 성립

v 결함의 종류 • 제조상의 결함: 설계도면대로 제품이 생산되지 아니한 경우 • 설계상의 결함: 설계자체가 안전설계가 되지 아니한 경우 • 표시상의 결함: 제품을 올바로 사용할 수 있도록 설명·지시 또 는 위험성에 대한 경고를 하지 않은 경우 • 기타 통상적으로 기대할 수 있는 안전성이 결여된 경우

v 제조물 책임의 예방책 (PLP) 시스템 수립에 의한 예방 (ISO 9001 등) 1) 고객만족 2) 업무효율성 및 생산성 증대 3) 이미지 제고 및 신규 시장 개척 4) 경쟁력 강화에 따른 이익 증대 5) 국제적인 변화에 대응

v 제조물 책임의 예방책 (PLP) 제품인증에 의한 예방책 제품 안전의 확신의 수단으로 제품 안전 인증을 획득 하는 것도 좋은 방법이다. 이를 통하여 국내의 시장에서의 신뢰 성 및 인지도를 높여 매출 증대의 효과도 부수적으로 얻을 수 있다. 1) CE (유럽) 2) NRTL (미국) 3) FDA (미국) 4) CCC, SFDA, AQSIQ (중국)

v 제조물 책임법의 기대 효과 • 제조물의 안전성 강화 • 고객만족경영의 실현 (소비자 보호) • 기업 경쟁력 강화 • 기업의 책임 분산 • 사고재발의 방지

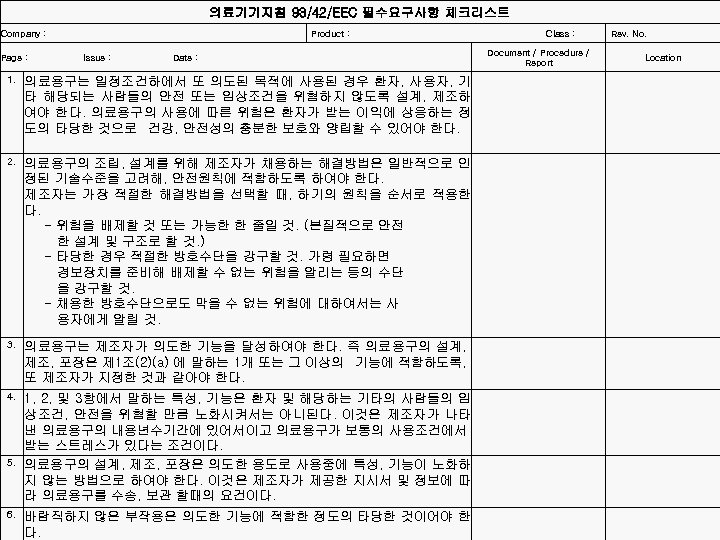
의료기기지침 93/42/EEC 필수요구사항 체크리스트 Company : Product : Class : Document / Procedure / Report Page : Issue : Date : 1. 2. 의료용구는 일정조건하에서 또 의도된 목적에 사용된 경우 환자, 사용자, 기 타 해당되는 사람들의 안전 또는 임상조건을 위협하지 않도록 설계, 제조하 여야 한다. 의료용구의 사용에 따른 위험은 환자가 받는 이익에 상응하는 정 도의 타당한 것으로 건강, 안전성의 충분한 보호와 양립할 수 있어야 한다. 의료용구의 조립, 설계를 위해 제조자가 채용하는 해결방법은 일반적으로 인 정된 기술수준을 고려해, 안전원칙에 적합하도록 하여야 한다. 제조자는 가장 적절한 해결방법을 선택할 때, 하기의 원칙을 순서로 적용한 다. - 위험을 배제할 것 또는 가능한 한 줄일 것. (본질적으로 안전 한 설계 및 구조로 할 것. ) - 타당한 경우 적절한 방호수단을 강구할 것. 가령 필요하면 경보장치를 준비해 배제할 수 없는 위험을 알리는 등의 수단 을 강구할 것. - 채용한 방호수단으로도 막을 수 없는 위험에 대하여서는 사 용자에게 알릴 것. 3. 의료용구는 제조자가 의도한 기능을 달성하여야 한다. 즉 의료용구의 설계, 제조, 포장은 제 1조(2)(a) 에 말하는 1개 또는 그 이상의 기능에 적합하도록, 또 제조자가 지정한 것과 같아야 한다. 4. 1, 2, 및 3항에서 말하는 특성, 기능은 환자 및 해당하는 기타의 사람들의 임 상조건, 안전을 위협할 만큼 노화시켜서는 아니된다. 이것은 제조자가 나타 낸 의료용구의 내용년수기간에 있어서이고 의료용구가 보통의 사용조건에서 받는 스트레스가 있다는 조건이다. 의료용구의 설계, 제조, 포장은 의도한 용도로 사용중에 특성, 기능이 노화하 지 않는 방법으로 하여야 한다. 이것은 제조자가 제공한 지시서 및 정보에 따 라 의료용구를 수송, 보관 할때의 요건이다. 5. 6. Rev. No. 바람직하지 않은 부작용은 의도한 기능에 적합한 정도의 타당한 것이어야 한 다. Location
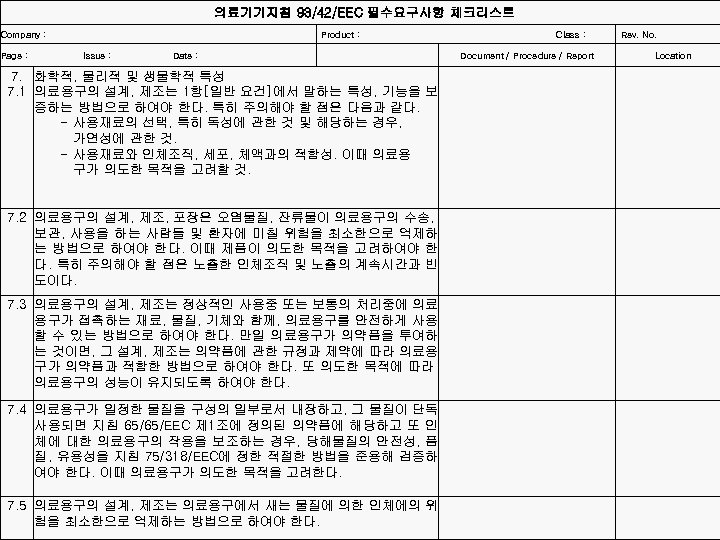
의료기기지침 93/42/EEC 필수요구사항 체크리스트 Company : Product : Class : Page : Issue : Date : 7. 7. 1 7. 2 화학적, 물리적 및 생물학적 특성 의료용구의 설계, 제조는 1항[일반 요건]에서 말하는 특성, 기능을 보 증하는 방법으로 하여야 한다. 특히 주의해야 할 점은 다음과 같다. - 사용재료의 선택, 특히 독성에 관한 것 및 해당하는 경우, 가연성에 관한 것. - 사용재료와 인체조직, 세포, 체액과의 적합성. 이때 의료용 구가 의도한 목적을 고려할 것. 의료용구의 설계, 제조, 포장은 오염물질, 잔류물이 의료용구의 수송, 보관, 사용을 하는 사람들 및 환자에 미칠 위험을 최소한으로 억제하 는 방법으로 하여야 한다. 이때 제품이 의도한 목적을 고려하여야 한 다. 특히 주의해야 할 점은 노출한 인체조직 및 노출의 계속시간과 빈 도이다. 7. 3 의료용구의 설계, 제조는 정상적인 사용중 또는 보통의 처리중에 의료 용구가 접촉하는 재료, 물질, 기체와 함께, 의료용구를 안전하게 사용 할 수 있는 방법으로 하여야 한다. 만일 의료용구가 의약품을 투여하 는 것이면, 그 설계, 제조는 의약품에 관한 규정과 제약에 따라 의료용 구가 의약품과 적합한 방법으로 하여야 한다. 또 의도한 목적에 따라 의료용구의 성능이 유지되도록 하여야 한다. 7. 4 의료용구가 일정한 물질을 구성의 일부로서 내장하고, 그 물질이 단독 사용되면 지침 65/65/EEC 제 1조에 정의된 의약품에 해당하고 또 인 체에 대한 의료용구의 작용을 보조하는 경우, 당해물질의 안전성, 품 질, 유용성을 지침 75/318/EEC에 정한 적절한 방법을 준용해 검증하 여야 한다. 이때 의료용구가 의도한 목적을 고려한다. 7. 5 의료용구의 설계, 제조는 의료용구에서 새는 물질에 의한 인체에의 위 험을 최소한으로 억제하는 방법으로 하여야 한다. Rev. No. Document / Procedure / Report Location
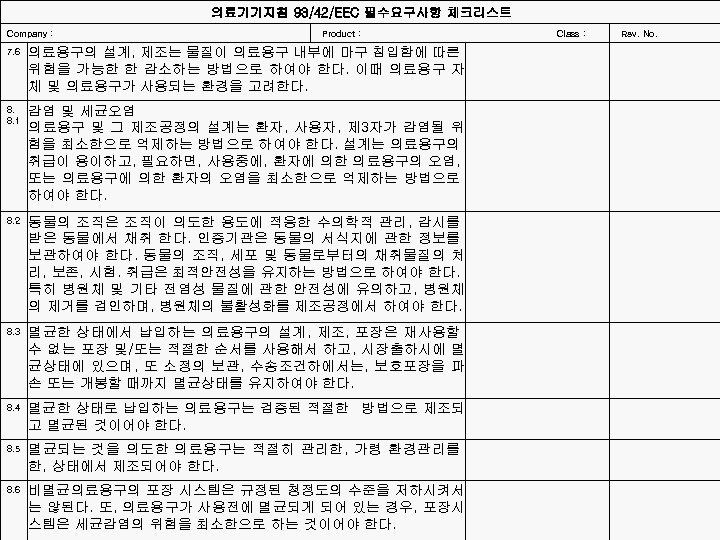
의료기기지침 93/42/EEC 필수요구사항 체크리스트 Company : 7. 6 8. 8. 1 8. 2 8. 3 8. 4 8. 5 8. 6 Product : Class : Rev. No. 의료용구의 설계, 제조는 물질이 의료용구 내부에 마구 침입함에 따른 위험을 가능한 한 감소하는 방법으로 하여야 한다. 이때 의료용구 자 체 및 의료용구가 사용되는 환경을 고려한다. 감염 및 세균오염 의료용구 및 그 제조공정의 설계는 환자, 사용자, 제 3자가 감염될 위 험을 최소한으로 억제하는 방법으로 하여야 한다. 설계는 의료용구의 취급이 용이하고, 필요하면, 사용중에, 환자에 의한 의료용구의 오염, 또는 의료용구에 의한 환자의 오염을 최소한으로 억제하는 방법으로 하여야 한다. 동물의 조직은 조직이 의도한 용도에 적응한 수의학적 관리, 감시를 받은 동물에서 채취 한다. 인증기관은 동물의 서식지에 관한 정보를 보관하여야 한다. 동물의 조직, 세포 및 동물로부터의 채취물질의 처 리, 보존, 시험. 취급은 최적안전성을 유지하는 방법으로 하여야 한다. 특히 병원체 및 기타 전염성 물질에 관한 안전성에 유의하고, 병원체 의 제거를 검인하며, 병원체의 불활성화를 제조공정에서 하여야 한다. 멸균한 상태에서 납입하는 의료용구의 설계, 제조, 포장은 재사용할 수 없는 포장 및/또는 적절한 순서를 사용해서 하고, 시장출하시에 멸 균상태에 있으며, 또 소정의 보관, 수송조건하에서는, 보호포장을 파 손 또는 개봉할 때까지 멸균상태를 유지하여야 한다. 멸균한 상태로 납입하는 의료용구는 검증된 적절한 방법으로 제조되 고 멸균된 것이어야 한다. 멸균되는 것을 의도한 의료용구는 적절히 관리한, 가령 환경관리를 한, 상태에서 제조되어야 한다. 비멸균의료용구의 포장 시스템은 규정된 청정도의 수준을 저하시켜서 는 않된다. 또, 의료용구가 사용전에 멸균되게 되어 있는 경우, 포장시 스템은 세균감염의 위험을 최소한으로 하는 것이어야 한다.
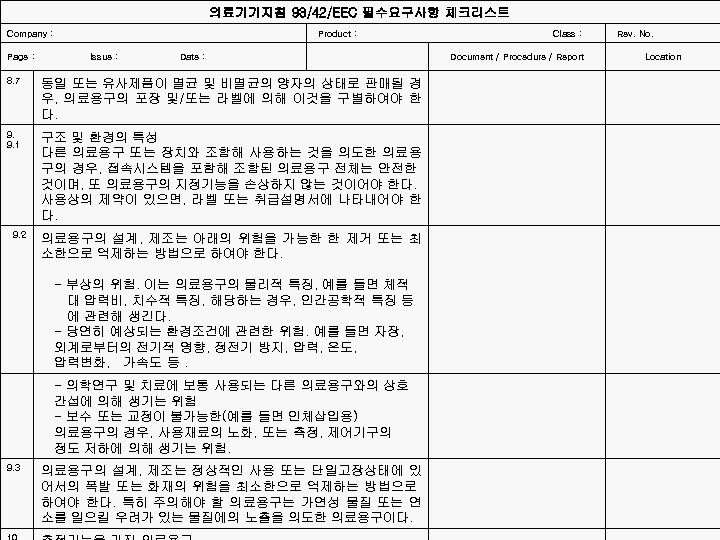
의료기기지침 93/42/EEC 필수요구사항 체크리스트 Company : Product : Class : Page : Issue : Date : 8. 7 Document / Procedure / Report Location 동일 또는 유사제품이 멸균 및 비멸균의 양자의 상태로 판매될 경 우, 의료용구의 포장 및/또는 라벨에 의해 이것을 구별하여야 한 다. 9. 2 구조 및 환경의 특성 다른 의료용구 또는 장치와 조합해 사용하는 것을 의도한 의료용 구의 경우, 접속시스템을 포함해 조합된 의료용구 전체는 안전한 것이며, 또 의료용구의 지정기능을 손상하지 않는 것이어야 한다. 사용상의 제약이 있으면, 라벨 또는 취급설명서에 나타내어야 한 다. 9. 9. 1 9. 3 Rev. No. 의료용구의 설계, 제조는 아래의 위험을 가능한 한 제거 또는 최 소한으로 억제하는 방법으로 하여야 한다. - 부상의 위험. 이는 의료용구의 물리적 특징, 예를 들면 체적 대 압력비, 치수적 특징, 해당하는 경우, 인간공학적 특징 등 에 관련해 생긴다. - 당연히 예상되는 환경조건에 관련한 위험. 예를 들면 자장, 외계로부터의 전기적 영향, 정전기 방지, 압력, 온도, 압력변화, 가속도 등. - 의학연구 및 치료에 보통 사용되는 다른 의료용구와의 상호 간섭에 의해 생기는 위험 - 보수 또는 교정이 불가능한(예를 들면 인체삽입용) 의료용구의 경우, 사용재료의 노화, 또는 측정, 제어기구의 정도 저하에 의해 생기는 위험. 의료용구의 설계, 제조는 정상적인 사용 또는 단일고장상태에 있 어서의 폭발 또는 화재의 위험을 최소한으로 억제하는 방법으로 하여야 한다. 특히 주의해야 할 의료용구는 가연성 물질 또는 연 소를 일으킬 우려가 있는 물질에의 노출을 의도한 의료용구이다.
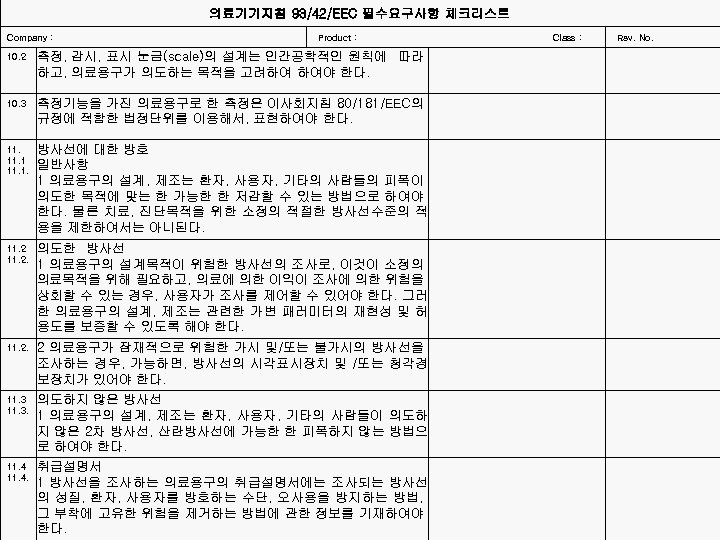
의료기기지침 93/42/EEC 필수요구사항 체크리스트 Company : 10. 2 10. 3 11. 1. 11. 2. 11. 3. 11. 4. Product : Class : Rev. No. 측정, 감시, 표시 눈금(scale)의 설계는 인간공학적인 원칙에 따라 하고, 의료용구가 의도하는 목적을 고려하여 하여야 한다. 측정기능을 가진 의료용구로 한 측정은 이사회지침 80/181/EEC의 규정에 적합한 법정단위를 이용해서, 표현하여야 한다. 방사선에 대한 방호 일반사항 1 의료용구의 설계, 제조는 환자, 사용자, 기타의 사람들의 피폭이 의도한 목적에 맞는 한 가능한 한 저감할 수 있는 방법으로 하여야 한다. 물론 치료, 진단목적을 위한 소정의 적절한 방사선수준의 적 용을 제한하여서는 아니된다. 의도한 방사선 1 의료용구의 설계목적이 위험한 방사선의 조사로, 이것이 소정의 의료목적을 위해 필요하고, 의료에 의한 이익이 조사에 의한 위험을 상회할 수 있는 경우, 사용자가 조사를 제어할 수 있어야 한다. 그러 한 의료용구의 설계, 제조는 관련한 가변 패러미터의 재현성 및 허 용도를 보증할 수 있도록 해야 한다. 2 의료용구가 잠재적으로 위험한 가시 및/또는 불가시의 방사선을 조사하는 경우, 가능하면, 방사선의 시각표시장치 및 /또는 청각경 보장치가 있어야 한다. 의도하지 않은 방사선 1 의료용구의 설계, 제조는 환자, 사용자, 기타의 사람들이 의도하 지 않은 2차 방사선, 산란방사선에 가능한 한 피폭하지 않는 방법으 로 하여야 한다. 취급설명서 1 방사선을 조사하는 의료용구의 취급설명서에는 조사되는 방사선 의 성질, 환자, 사용자를 방호하는 수단, 오사용을 방지하는 방법, 그 부착에 고유한 위험을 제거하는 방법에 관한 정보를 기재하여야 한다.
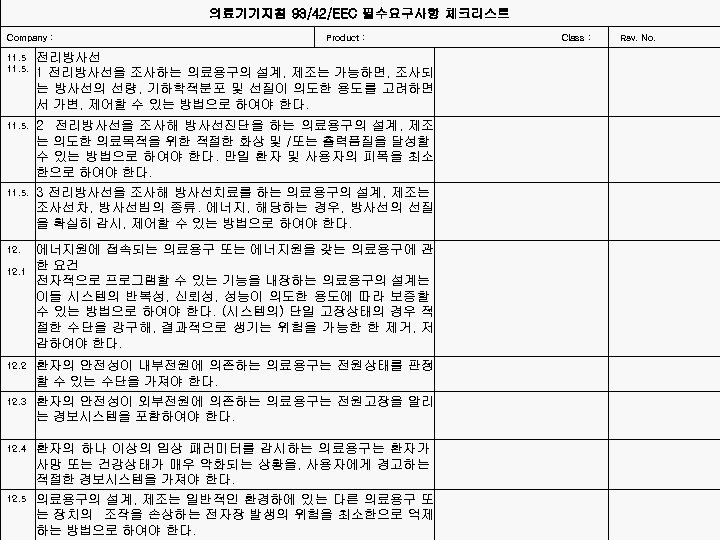
의료기기지침 93/42/EEC 필수요구사항 체크리스트 Company : Product : Class : Rev. No. 전리방사선 1 전리방사선을 조사하는 의료용구의 설계, 제조는 가능하면, 조사되 는 방사선의 선량, 기하학적분포 및 선질이 의도한 용도를 고려하면 서 가변, 제어할 수 있는 방법으로 하여야 한다. 2 전리방사선을 조사해 방사선진단을 하는 의료용구의 설계, 제조 는 의도한 의료목적을 위한 적절한 화상 및 /또는 출력품질을 달성할 수 있는 방법으로 하여야 한다. 만일 환자 및 사용자의 피폭을 최소 한으로 하여야 한다. 3 전리방사선을 조사해 방사선치료를 하는 의료용구의 설계, 제조는 조사선차, 방사선빔의 종류. 에너지, 해당하는 경우, 방사선의 선질 을 확실히 감시, 제어할 수 있는 방법으로 하여야 한다. 에너지원에 접속되는 의료용구 또는 에너지원을 갖는 의료용구에 관 한 요건 전자적으로 프로그램할 수 있는 기능을 내장하는 의료용구의 설계는 이들 시스템의 반복성, 신뢰성, 성능이 의도한 용도에 따라 보증할 수 있는 방법으로 하여야 한다. (시스템의) 단일 고장상태의 경우 적 절한 수단을 강구해, 결과적으로 생기는 위험을 가능한 한 제거, 저 감하여야 한다. 12. 2 환자의 안전성이 내부전원에 의존하는 의료용구는 전원상태를 판정 할 수 있는 수단을 가져야 한다. 12. 3 환자의 안전성이 외부전원에 의존하는 의료용구는 전원고장을 알리 는 경보시스템을 포함하여야 한다. 11. 5. 12. 1 12. 4 12. 5 환자의 하나 이상의 임상 패러미터를 감시하는 의료용구는 환자가 사망 또는 건강상태가 매우 악화되는 상황을, 사용자에게 경고하는 적절한 경보시스템을 가져야 한다. 의료용구의 설계, 제조는 일반적인 환경하에 있는 다른 의료용구 또 는 장치의 조작을 손상하는 전자장 발생의 위험을 최소한으로 억제 하는 방법으로 하여야 한다.
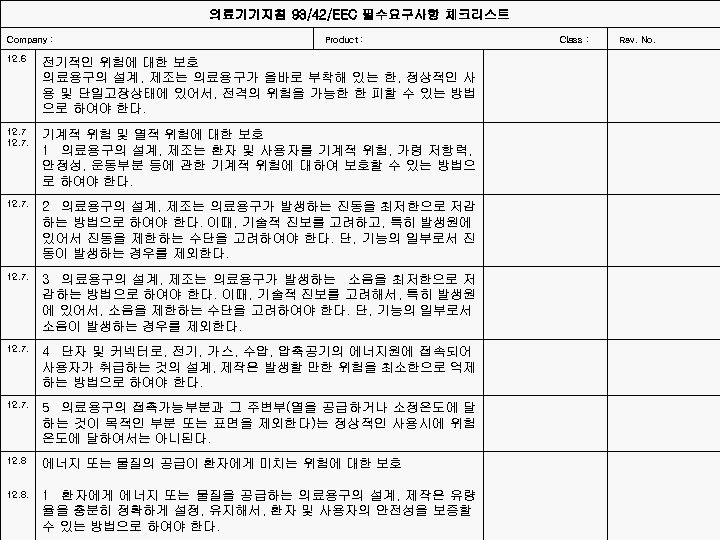
의료기기지침 93/42/EEC 필수요구사항 체크리스트 Company : 12. 6 12. 7. 12. 8. Product : Class : Rev. No. 전기적인 위험에 대한 보호 의료용구의 설계, 제조는 의료용구가 올바로 부착해 있는 한, 정상적인 사 용 및 단일고장상태에 있어서, 전격의 위험을 가능한 한 피할 수 있는 방법 으로 하여야 한다. 기계적 위험 및 열적 위험에 대한 보호 1 의료용구의 설계, 제조는 환자 및 사용자를 기계적 위험, 가령 저항력, 안정성, 운동부분 등에 관한 기계적 위험에 대하여 보호할 수 있는 방법으 로 하여야 한다. 2 의료용구의 설계, 제조는 의료용구가 발생하는 진동을 최저한으로 저감 하는 방법으로 하여야 한다. 이때, 기술적 진보를 고려하고, 특히 발생원에 있어서 진동을 제한하는 수단을 고려하여야 한다. 단, 기능의 일부로서 진 동이 발생하는 경우를 제외한다. 3 의료용구의 설계, 제조는 의료용구가 발생하는 소음을 최저한으로 저 감하는 방법으로 하여야 한다. 이때, 기술적 진보를 고려해서, 특히 발생원 에 있어서, 소음을 제한하는 수단을 고려하여야 한다. 단, 기능의 일부로서 소음이 발생하는 경우를 제외한다. 4 단자 및 커넥터로, 전기, 가스, 수압, 압축공기의 에너지원에 접속되어 사용자가 취급하는 것의 설계, 제작은 발생할 만한 위험을 최소한으로 억제 하는 방법으로 하여야 한다. 5 의료용구의 접촉가능부분과 그 주변부(열을 공급하거나 소정온도에 달 하는 것이 목적인 부분 또는 표면을 제외한다)는 정상적인 사용시에 위험 온도에 달하여서는 아니된다. 에너지 또는 물질의 공급이 환자에게 미치는 위험에 대한 보호 1 환자에게 에너지 또는 물질을 공급하는 의료용구의 설계, 제작은 유량 율을 충분히 정확하게 설정, 유지해서, 환자 및 사용자의 안전성을 보증할 수 있는 방법으로 하여야 한다.
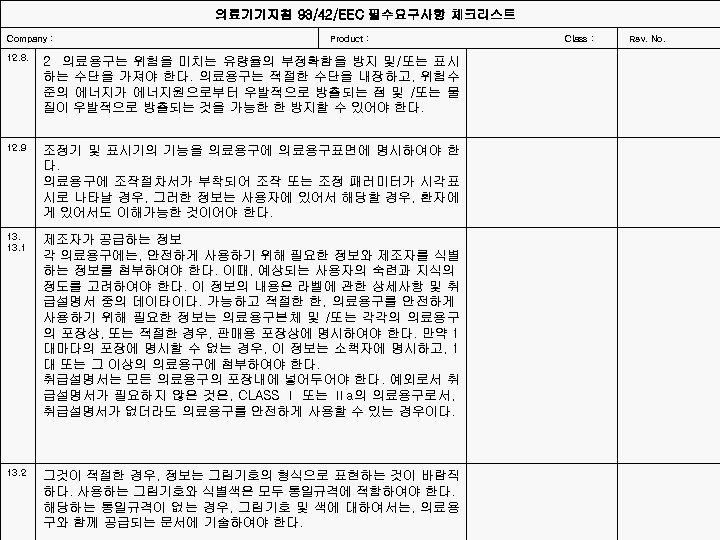
의료기기지침 93/42/EEC 필수요구사항 체크리스트 Company : 12. 8. 12. 9 13. 1 13. 2 Product : Class : 2 의료용구는 위험을 미치는 유량율의 부정확함을 방지 및/또는 표시 하는 수단을 가져야 한다. 의료용구는 적절한 수단을 내장하고, 위험수 준의 에너지가 에너지원으로부터 우발적으로 방출되는 점 및 /또는 물 질이 우발적으로 방출되는 것을 가능한 한 방지할 수 있어야 한다. 조정기 및 표시기의 기능을 의료용구에 의료용구표면에 명시하여야 한 다. 의료용구에 조작절차서가 부착되어 조작 또는 조정 패러미터가 시각표 시로 나타날 경우, 그러한 정보는 사용자에 있어서 해당할 경우, 환자에 게 있어서도 이해가능한 것이어야 한다. 제조자가 공급하는 정보 각 의료용구에는, 안전하게 사용하기 위해 필요한 정보와 제조자를 식별 하는 정보를 첨부하여야 한다. 이때, 예상되는 사용자의 숙련과 지식의 정도를 고려하여야 한다. 이 정보의 내용은 라벨에 관한 상세사항 및 취 급설명서 중의 데이타이다. 가능하고 적절한 한, 의료용구를 안전하게 사용하기 위해 필요한 정보는 의료용구본체 및 /또는 각각의 의료용구 의 포장상, 또는 적절한 경우, 판매용 포장상에 명시하여야 한다. 만약 1 대마다의 포장에 명시할 수 없는 경우, 이 정보는 소책자에 명시하고, 1 대 또는 그 이상의 의료용구에 첨부하여야 한다. 취급설명서는 모든 의료용구의 포장내에 넣어두어야 한다. 예외로서 취 급설명서가 필요하지 않은 것은, CLASS Ⅰ 또는 Ⅱa의 의료용구로서, 취급설명서가 없더라도 의료용구를 안전하게 사용할 수 있는 경우이다. 그것이 적절한 경우, 정보는 그림기호의 형식으로 표현하는 것이 바람직 하다. 사용하는 그림기호와 식별색은 모두 통일규격에 적합하여야 한다. 해당하는 통일규격이 없는 경우, 그림기호 및 색에 대하여서는, 의료용 구와 함께 공급되는 문서에 기술하여야 한다. Rev. No.
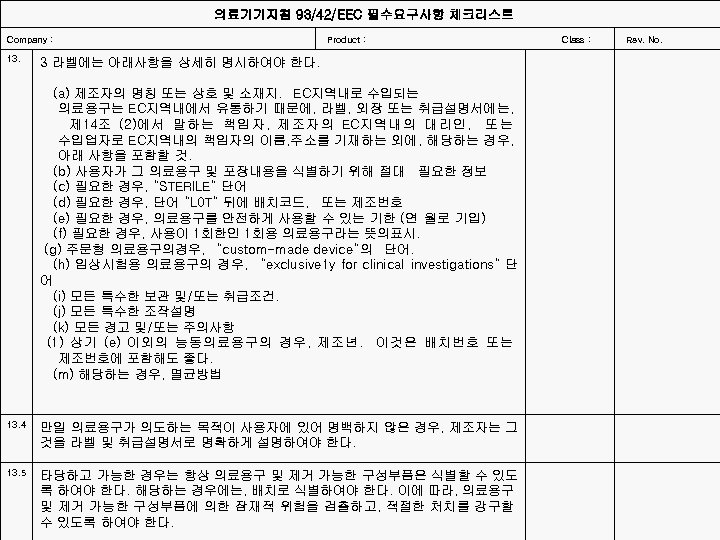
의료기기지침 93/42/EEC 필수요구사항 체크리스트 Company : 13. 4 13. 5 Product : Class : 3 라벨에는 아래사항을 상세히 명시하여야 한다. (a) 제조자의 명칭 또는 상호 및 소재지. EC지역내로 수입되는 의료용구는 EC지역내에서 유통하기 때문에, 라벨, 외장 또는 취급설명서에는, 제 14조 (2)에 서 말 하 는 책 임 자 , 제 조 자 의 EC지 역 내 의 대 리 인 , 또 는 수입업자로 EC지역내의 책임자의 이름, 주소를 기재하는 외에, 해당하는 경우, 아래 사항을 포함할 것. (b) 사용자가 그 의료용구 및 포장내용을 식별하기 위해 절대 필요한 정보 (c) 필요한 경우, “STERl. LE“ 단어 (d) 필요한 경우, 단어 “L 0 T“ 뒤에 배치코드, 또는 제조번호 (e) 필요한 경우, 의료용구를 안전하게 사용할 수 있는 기한 (연 월로 기입) (f) 필요한 경우, 사용이 1회한인 1회용 의료용구라는 뜻의표시. (g) 주문형 의료용구의경우, “custom-made device“의 단어. (h) 임상시험용 의료용구의 경우, “exclusive 1 y for clinical investigations“ 단 어 (i) 모든 특수한 보관 및/또는 취급조건. (j) 모든 특수한 조작설명 (k) 모든 경고 및/또는 주의사항 (1) 상기 (e) 이외의 능동의료용구의 경우, 제조년. 이것은 배치번호 또는 제조번호에 포함해도 좋다. (m) 해당하는 경우, 멸균방법 만일 의료용구가 의도하는 목적이 사용자에 있어 명백하지 않은 경우, 제조자는 그 것을 라벨 및 취급설명서로 명확하게 설명하여야 한다. 타당하고 가능한 경우는 항상 의료용구 및 제거 가능한 구성부품은 식별할 수 있도 록 하여야 한다. 해당하는 경우에는, 배치로 식별하여야 한다. 이에 따라, 의료용구 및 제거 가능한 구성부품에 의한 잠재적 위험을 검출하고, 적절한 처치를 강구할 수 있도록 하여야 한다. Rev. No.
의료기기지침 93/42/EEC 필수요구사항 체크리스트 Company : 13. 6 Product : Class : 필요한 경우, 취급설명서에는 아래사항을 상세히 기재하여야 한다. (a) 13. 3항에서 서술한 내용. 단 항목 (d)및 (e)를 제외. (b) 3항에서 서술한 기능 및 모든 바람직하지 않은 부작 용 (c) 의도한 목적대로 조작시키기 위하여서는, 다른 의료용구 또는 장치와 조합해 부착, 접속을 하여야 하는 의료용구가 있다. 이 경우, 안전한 조합이 가능하도록 올바른 상대의 의료용구 또는 장치를 식별하기 위한 특성을 상세하게 설명한다. (d) 의료용구가 적절히 부착되어 정확, 안전하게 작동함을 검증하기 위해 필요한 모든 정보 및 의료용구가 적절 안전하게 항상 작동하는 것을 확인하기 위해 필요한 보수, 교정의 내용, 빈도에 관한 상세한 정보. (e) 필요한 경우, 의료용구의 삽입에 관련해 있을 수 있는 위험 을 회피하기 위한 정보 (f) 특정 연구나 치료시 의료용구의 존재에 의해 생기는 상호간섭의 위험에 관한 정보 (g) 멸균팩이 파손한 경우에 필요한 지시사항. 필요한 경 우, 재 멸균방법의 상세 (h) 재사용 가능한 의료용구의 경우, 재사용을 가능하게 하기 위한 적절한 처치방법. 가령 청정, 소독, 포장 및, 필요한 경우, 재멸균되는 의료용구의 멸균방법, 재사용의 최대횟수 등. 사용전에 멸균되어야 할 의료용구의 경우, 청정, 멸균의 지시서에 의해, 만약 그 대로 정확하게 실시하면 1항에서 말하는 요구사항에 여전히 적합하도록 지시할 것. (i) 의료용구의 사용전에 필요한 모든 추가처리 또는 취급 방법 (예를 들면 멸균, 최종조립 등 ) Rev. No.
의료기기지침 93/42/EEC 필수요구사항 체크리스트 Company : 14. Product : Class : Rev. No. (j) 의료목적의 방사선을 조사하는 의료용구의 경우, 방사선의 성질, 종 류, 강도, 분포에 관한 상세한 사항. 취급설명서에는 모든 금기나 사전 주의에 대하여 의료진이 환자에게 요점을 설명할 수 있도록 상세한 정 보를 넣어두어야 한다. 여기에는 특히 아래의 상세한 사항을 포함하여 야 한다. (k) 의료용구의 성능이 변할 때의 사전 주의사항 (1) 당연히 예상되는 환경조건에 있어서, 다음의 영향을 받는 경우의 사전 주의사항. 가령 자장, 외부에서의 전기의 영향, 정전기, 압력변화, 가속도, 열적발화원 등. (m) 당해 의료용구가 의약품의 투여를 목적으로 하는 것인 경우, 그 의약품에 관한 충분한 정보. 예를 들면 투여할 수 있는 의약품을 선택할 때의 제약 등. (n) 의료용구의 폐기에 관해 생기는 특별한 이상한 위험에 대한 사전 주의사항 (o) 7. 4항에 따라 의료용구가 구성의 일부로서 내장하는 의약 물질 (p) 측정기능을 갖는 의료용구에 요구되는 정도 기본요건에의 적합성이 (6)항에서처럼 임상데이타에 기초할 필요가 있는 경우, 그러한 데이타는 부속서 X에 따라 확립되어야 한다. Signed by : ___________ (name) ___________ (function) On behalf of : ___________ (company) ___________ (signature) ___________ (date)


v 자주 묻는 질문 • 국내에서 받은 13485인증을 유럽에서 인정합니까? CE인증을 진행하려면 다시 ISO 13485인증을 받아야 합니까? • ISO 13485인증 진행 시 기업에서 어떤 자료를 제공하고 어떤 일들을 해야 합니까? • 금방 설립된 3 -4명인 기업은 ISO 13485인증을 받을 수 있습니까? ISO 13485인증 적용범위? 외국에서 인정해줍니까? • 1등급 의료기기를 생산하는 기업입니다. 만약 우리가 지금 ISO 13485시스템 인증 을 진행하면 후에 2등급 의료기기 제품을 생산하면 지금 받은 ISO 13485인증이 효 력이 있습니까?

v 자주 묻는 질문 • 어떻게 ISO 17025인증을 받은 실험실을 찾을 수 있습니까? • 우리회사의 제품은 스위스로 수출하고 있고 스위스에 공장을 설립하려고 하는데 국 내에서 받은 CE인증과 스위스에서 받은 CE인증은 같습니까? • 제품 테스트 진행 시 기업은 어떤 일들을 해야 합니까? • 만약 회사에서 새로 연구개발한 제품일 때 CE인증을 받으려면 임상보고서는 어떻 게 작성해야 합니까? 얼마간의 임상시간이 필요합니까? • 만약 회사가 무역회사일 때 기업자체가 이미 CE인증을 받은 경우에 무역회사의 이 름으로 다시 CE인증을 받을 수 있습니까? 테스트 진행할 때 CE인증을 받으려는 제 품만 제공하면 되는 겁니까?

v 자주 묻는 질문 • 우리회사는 명성이 있는 인증기관을 찾으려고 합니다. 작은 나라의 인증기관은 인 정되지 않기 때문입니다. • 만약 CE인증 동시에 ISO 13485인증도 진행하면 비용은 각각 지불해야 합니까? • 수술확대경을 생산하는 기업인데 확대경 모델이 배수가 다름에 따라 여러 가지 모 델이 있습니다. CE인증이 가능합니까? 모델이 60~70개 전후인데 한 개 시리즈로 인증이 가능 합니까? 인증서는 하나로 발행이 가능합니까? • 회사가 수술칼을 생산하는 회사고 재질은 스테인리스 강일 때 CE인증에 스테인리 스 강 재질 제품에 특수한 요구가 있습니까? • COC와DOC구별?

v 자주 묻는 질문 • 전해질 분석기제품 견적서에 일반전기제품과 IVD로 두 가지 CE인증비용을 제안 받 았는데 이 두 가지 인증은 어떤 차이점이 있습니까? • 만약 기계제품을 테스트하려면 기계를 시험소에 직접 가져가야 합니까? • 지금<콘텍트렌즈안약>제품을 공인 시험소에서 테스트하고 있는데, CE인증시 제출 해야할 테스트report와 같습니까? • 구급상자를 생산하는 기업입니다. 빈 구급상자만 CE인증 가능합니까? • 원심분리기를 생산하는 기업입니다. 모델이 아주 많은데 매 모델마다 각각 테스트 를 진행해야 합니까?

v 자주 묻는 질문 • CE인증은 모두 사후관리 심사가 있습니까? • FDA와 인증의 관계는 무엇입니까? • 우리회사는 치실 생산하는 회사인데 FDA인증을 받으려면 어떻게 하면 됩니까? • FDA는 어떤 기관입니까? 어떤 방법으로 인증을 합니까? FDA인증 시 기업은 어떤 일들을 해야 합니까? 인증 과정은? • 지금까지 한국에 FDA 대리기관이 없다고 들었습니다. 맞습니까? • 욕창방지 에어 쿠션을 생산하여 러시아로 수출하는데 인증을 받아야 합니까? 받아 야 한다면 어떤 인증을 받아야 합니까?
af7eaf5264579288d05d04c86316e361.ppt