01ffe12bc539aea60d5283a97d91f501.ppt
- Количество слайдов: 85

疾病的细胞机制 (Cellular Mechanism of Diseases) 浙江大学医学院 陈莹莹 病理生理学 1

细胞增殖 细胞分化 生 死 细胞凋亡 增 殖 通过有丝分裂,达到细胞数量增加、组织 和器官增大及个体生长 分 化 通过细胞形态、结构和功能的特化,实现 表型差异、组织和器官的功能及个体成熟 凋 亡 体内外生理或病理因素激活细胞内死亡程 序,导致细胞主动死亡 2

• 疾病的细胞机制:细胞“生”的过程和/或“死”的过 程的失控 – 细胞增殖异常与疾病 – 细胞分化异常与疾病 – 细胞凋亡异常与疾病 – 细胞自噬异常与疾病(自学) 3
第一节 细胞增殖异常与疾病 (Abnormal Cell Proliferation and Diseases) • 细胞增殖:细胞分裂和再生的过程 – 细胞生长→DNA复制→细胞分裂 细胞周期 4
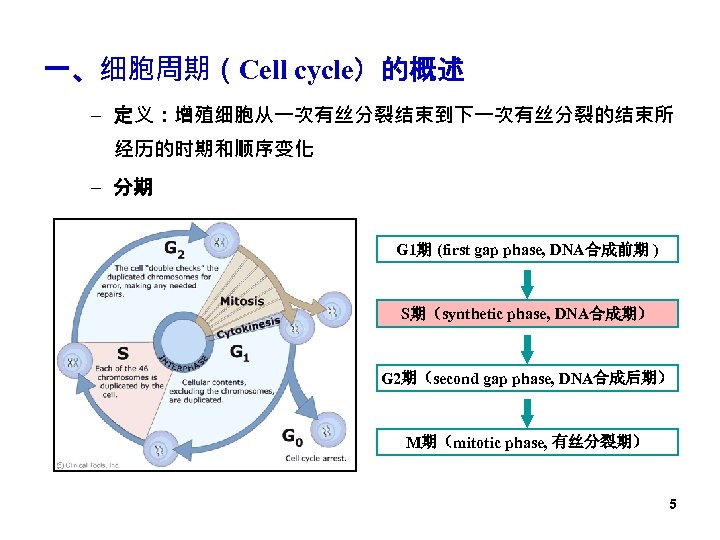
一、细胞周期(Cell cycle)的概述 – 定义:增殖细胞从一次有丝分裂结束到下一次有丝分裂的结束所 经历的时期和顺序变化 – 分期 G 1期 (first gap phase, DNA合成前期 ) S期(synthetic phase, DNA合成期) G 2期(second gap phase, DNA合成后期) M期(mitotic phase, 有丝分裂期) 5
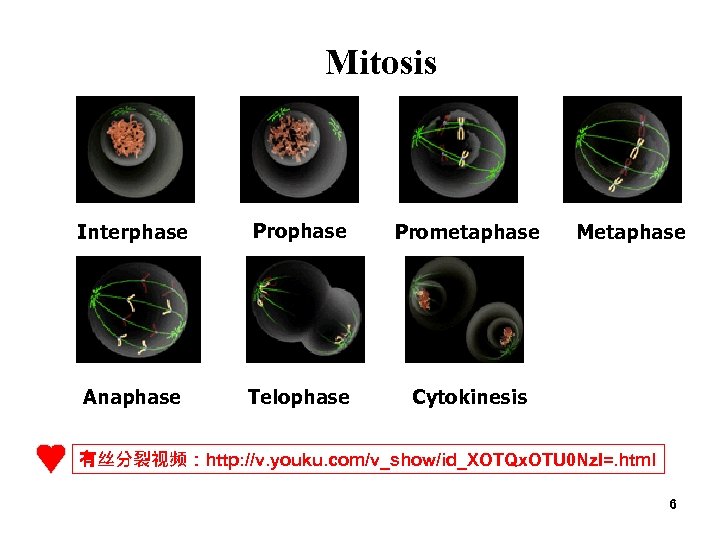
Mitosis Interphase Prometaphase Anaphase Telophase Cytokinesis Metaphase 有丝分裂视频:http: //v. youku. com/v_show/id_XOTQx. OTU 0 Nz. I=. html 6
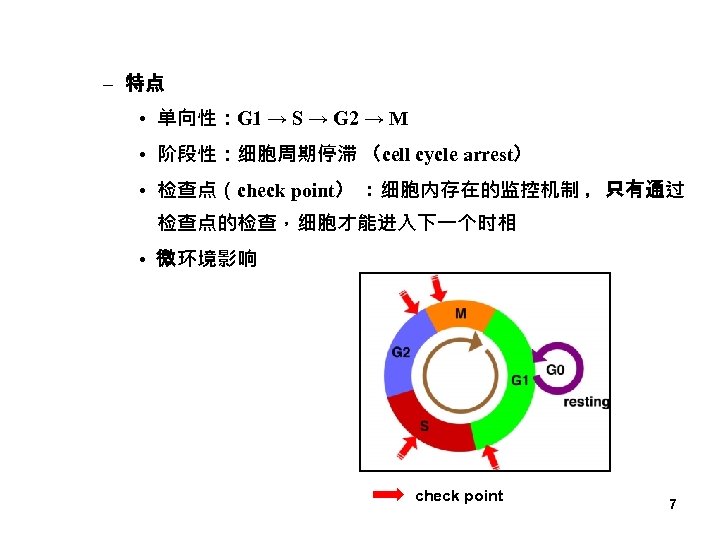
– 特点 • 单向性:G 1 → S → G 2 → M • 阶段性:细胞周期停滞 (cell cycle arrest) • 检查点(check point) :细胞内存在的监控机制 ,只有通过 检查点的检查,细胞才能进入下一个时相 • 微环境影响 check point 7
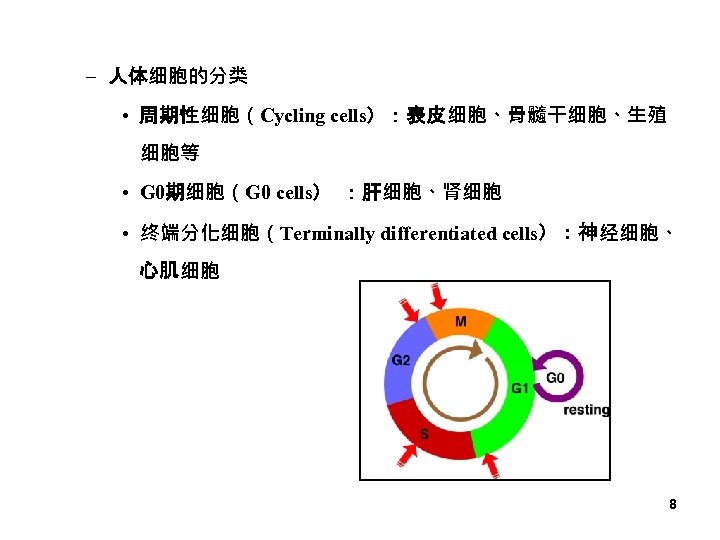
– 人体细胞的分类 • 周期性细胞(Cycling cells):表皮细胞、骨髓干细胞、生殖 细胞等 • G 0期细胞(G 0 cells) :肝细胞、肾细胞 • 终端分化细胞(Terminally differentiated cells):神经细胞、 心肌细胞 8

二、细胞周期的调控(Regulation of Cell Cycle) • 自身调控(Self-control) – 周期蛋白(Cyclin)和周期素依赖性蛋白激酶(Cyclin dependent kinase, CDK ) – 检查点(check point) • 细胞外信号( Extracellular signals )的调控 9
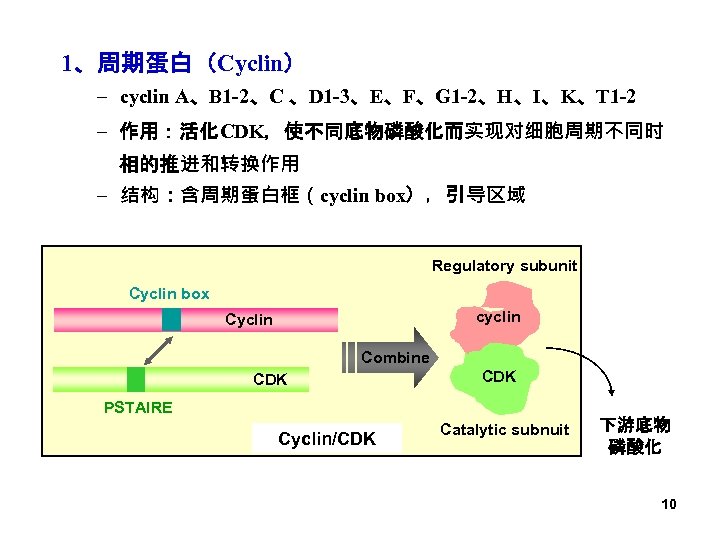
1、周期蛋白(Cyclin) – cyclin A、B 1 -2、C 、D 1 -3、E、F、G 1 -2、H、I、K、T 1 -2 – 作用:活化CDK,使不同底物磷酸化而实现对细胞周期不同时 相的推进和转换作用 – 结构:含周期蛋白框(cyclin box),引导区域 Regulatory subunit Cyclin box cyclin Combine CDK PSTAIRE Cyclin/CDK Catalytic subnuit 下游底物 磷酸化 10
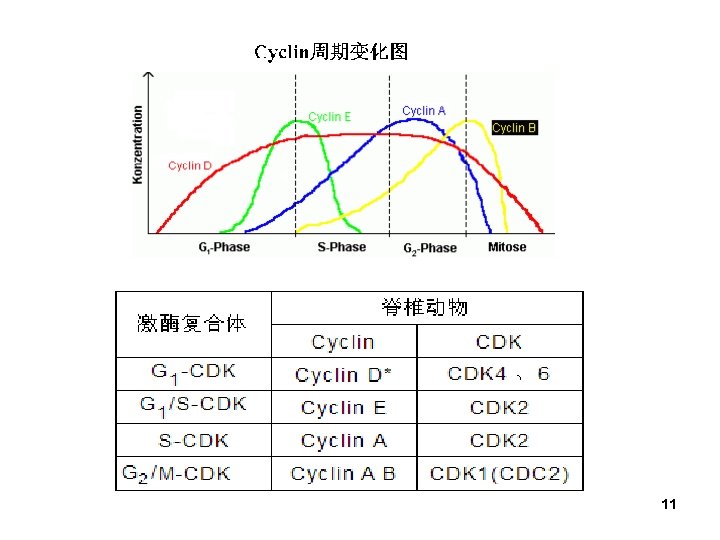
11
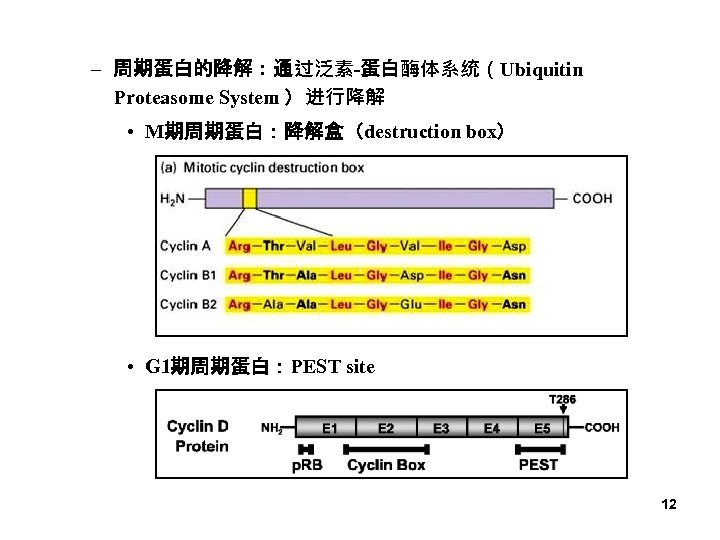
– 周期蛋白的降解:通过泛素-蛋白酶体系统(Ubiquitin Proteasome System )进行降解 • M期周期蛋白:降解盒(destruction box) • G 1期周期蛋白:PEST site 12
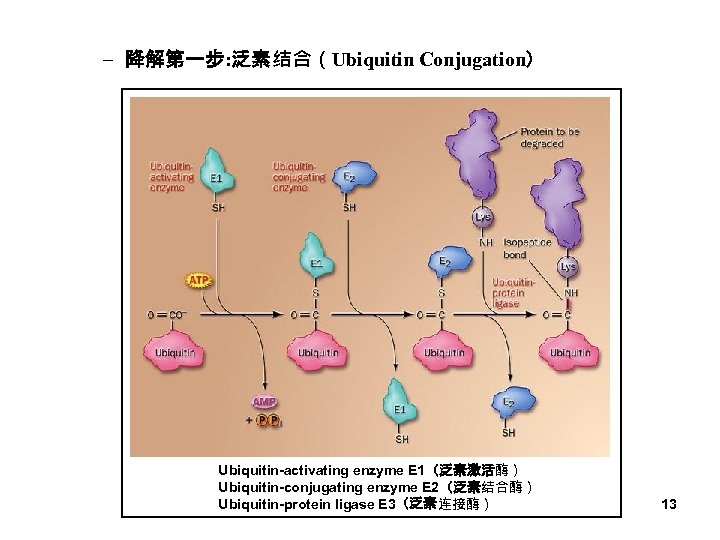
– 降解第一步: 泛素结合(Ubiquitin Conjugation) Ubiquitin-activating enzyme E 1(泛素激活酶) Ubiquitin-conjugating enzyme E 2(泛素结合酶) Ubiquitin-protein ligase E 3(泛素连接酶) 13
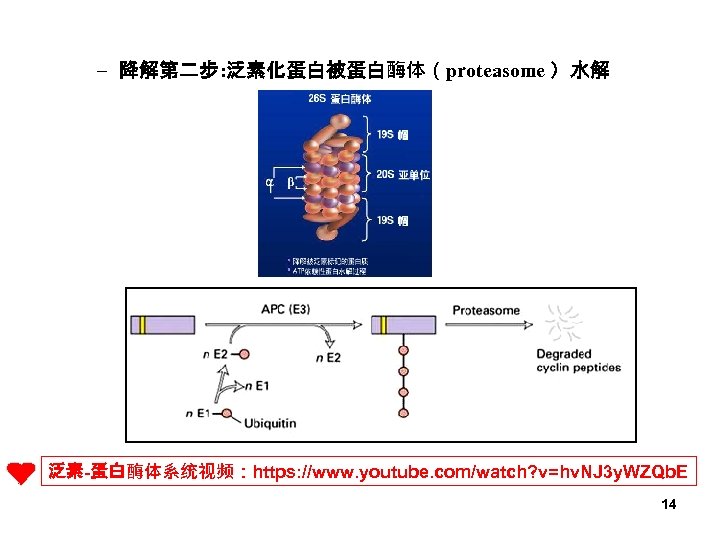
– 降解第二步: 泛素化蛋白被蛋白酶体(proteasome )水解 泛素-蛋白酶体系统视频:https: //www. youtube. com/watch? v=hv. NJ 3 y. WZQb. E 14
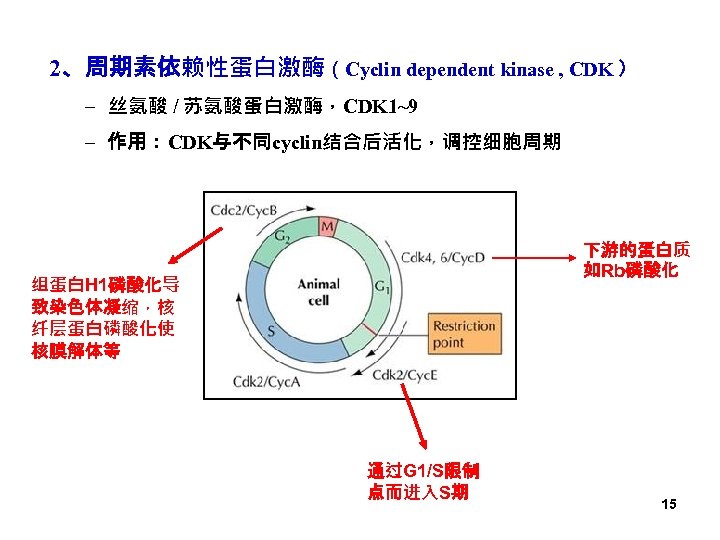
2、周期素依赖性蛋白激酶(Cyclin dependent kinase , CDK ) – 丝氨酸 / 苏氨酸蛋白激酶,CDK 1~9 – 作用:CDK与不同cyclin结合后活化,调控细胞周期 下游的蛋白质 如Rb磷酸化 组蛋白H 1磷酸化导 致染色体凝缩,核 纤层蛋白磷酸化使 核膜解体等 通过G 1/S限制 点而进入S期 15
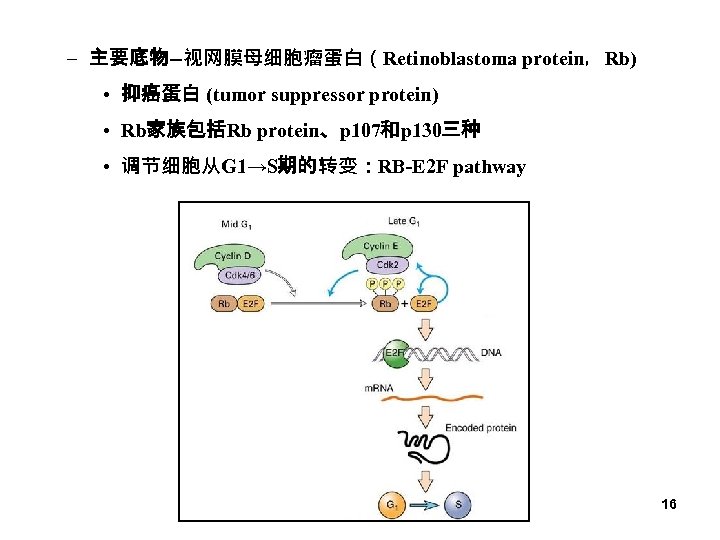
– 主要底物--视网膜母细胞瘤蛋白(Retinoblastoma protein,Rb) • 抑癌蛋白 (tumor suppressor protein) • Rb家族包括Rb protein、p 107和p 130三种 • 调节细胞从G 1→S期的转变:RB-E 2 F pathway 16
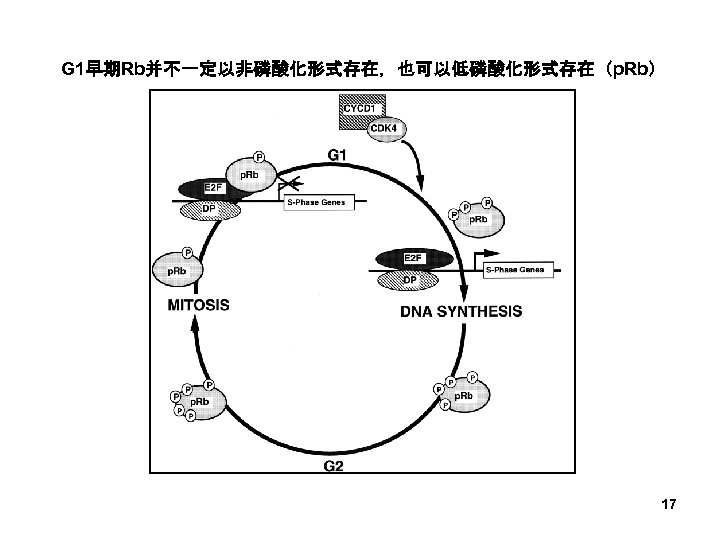
G 1早期Rb并不一定以非磷酸化形式存在,也可以低磷酸化形式存在(p. Rb) 17
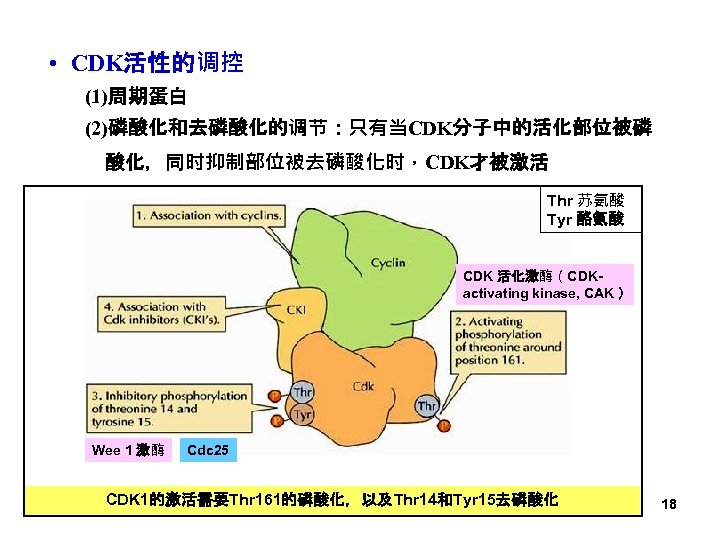
• CDK活性的调控 (1)周期蛋白 (2)磷酸化和去磷酸化的调节:只有当CDK分子中的活化部位被磷 酸化,同时抑制部位被去磷酸化时,CDK才被激活 Thr 苏氨酸 Tyr 酪氨酸 CDK 活化激酶(CDKactivating kinase, CAK ) Wee 1 激酶 Cdc 25 CDK 1的激活需要Thr 161的磷酸化,以及Thr 14和Tyr 15去磷酸化 18
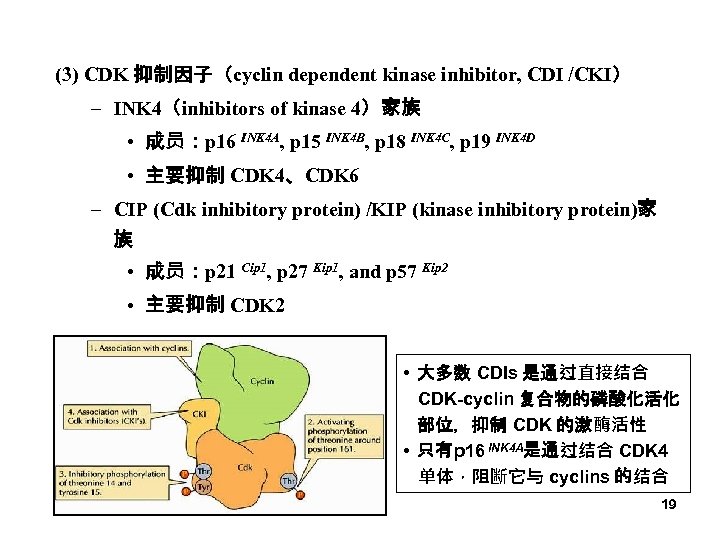
(3) CDK 抑制因子(cyclin dependent kinase inhibitor, CDI /CKI) – INK 4(inhibitors of kinase 4)家族 • 成员:p 16 INK 4 A, p 15 INK 4 B, p 18 INK 4 C, p 19 INK 4 D • 主要抑制 CDK 4、CDK 6 – CIP (Cdk inhibitory protein) /KIP (kinase inhibitory protein)家 族 • 成员:p 21 Cip 1, p 27 Kip 1, and p 57 Kip 2 • 主要抑制 CDK 2 • 大多数 CDIs 是通过直接结合 CDK-cyclin 复合物的磷酸化活化 部位,抑制 CDK 的激酶活性 • 只有p 16 INK 4 A是通过结合 CDK 4 单体,阻断它与 cyclins 的结合 19
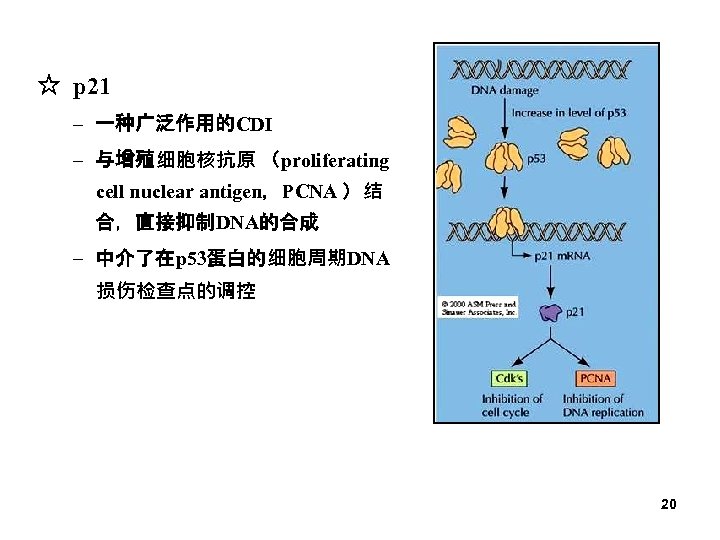
☆ p 21 – 一种广泛作用的CDI – 与增殖细胞核抗原 (proliferating cell nuclear antigen,PCNA )结 合,直接抑制DNA的合成 – 中介了在p 53蛋白的细胞周期DNA 损伤检查点的调控 20
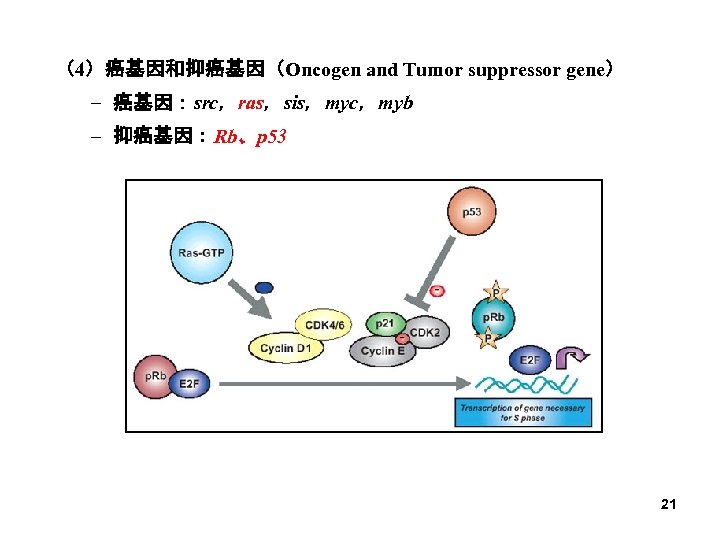
(4)癌基因和抑癌基因(Oncogen and Tumor suppressor gene) – 癌基因:src,ras,sis,myc,myb – 抑癌基因:Rb、p 53 21
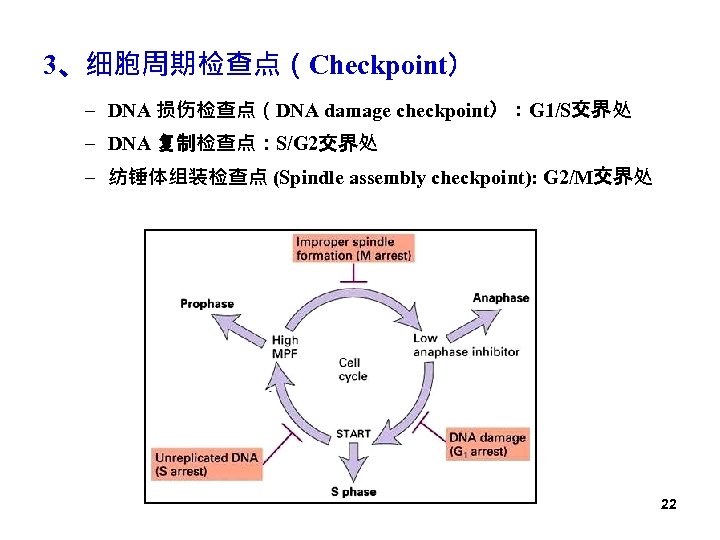
3、细胞周期检查点(Checkpoint) – DNA 损伤检查点(DNA damage checkpoint):G 1/S交界处 – DNA 复制检查点:S/G 2交界处 – 纺锤体组装检查点 (Spindle assembly checkpoint): G 2/M交界处 22
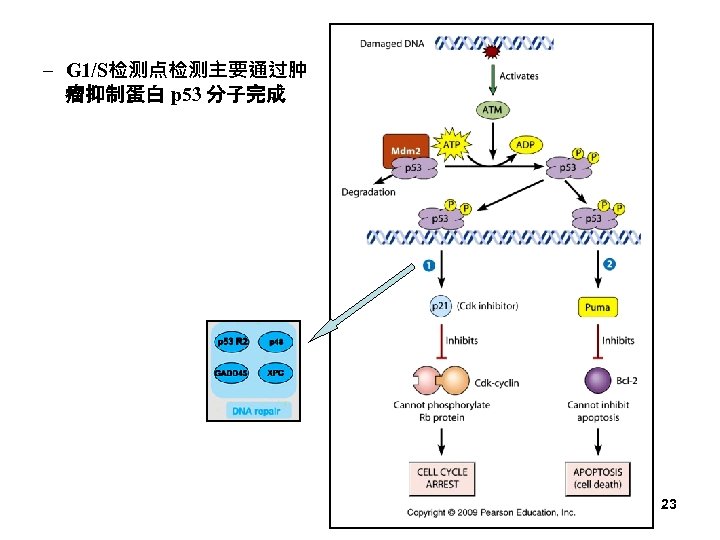
– G 1/S检测点检测主要通过肿 瘤抑制蛋白 p 53 分子完成 23
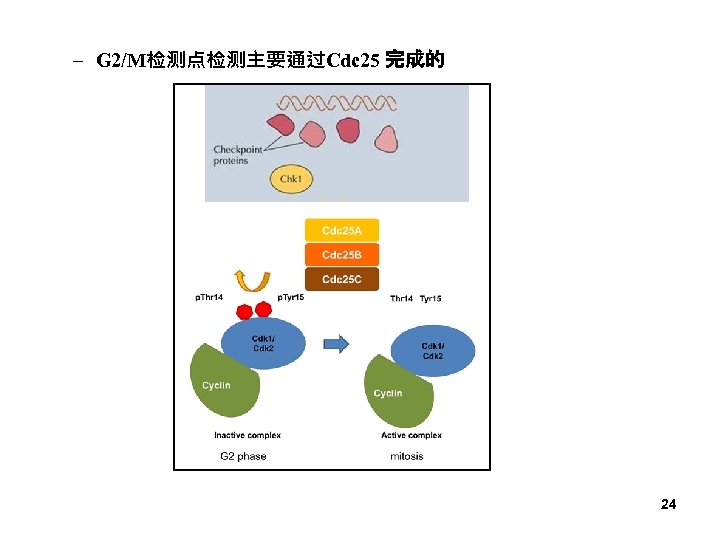
– G 2/M检测点检测主要通过Cdc 25 完成的 24
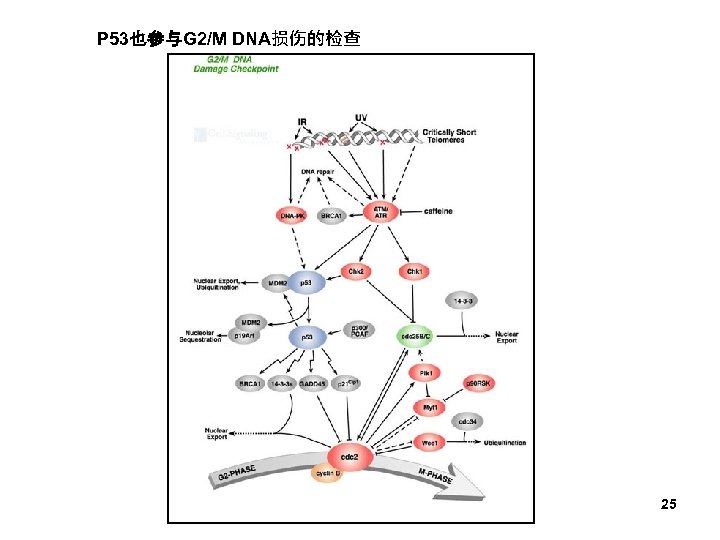
P 53也参与G 2/M DNA损伤的检查 25
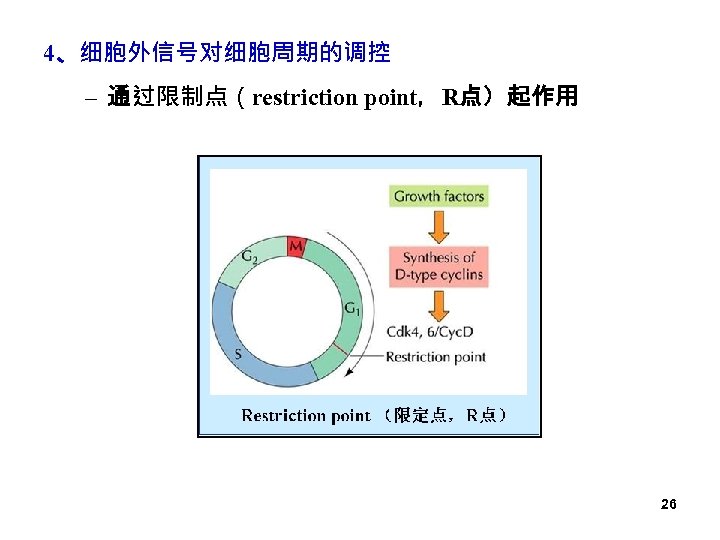
4、细胞外信号对细胞周期的调控 – 通过限制点(restriction point,R点)起作用 26
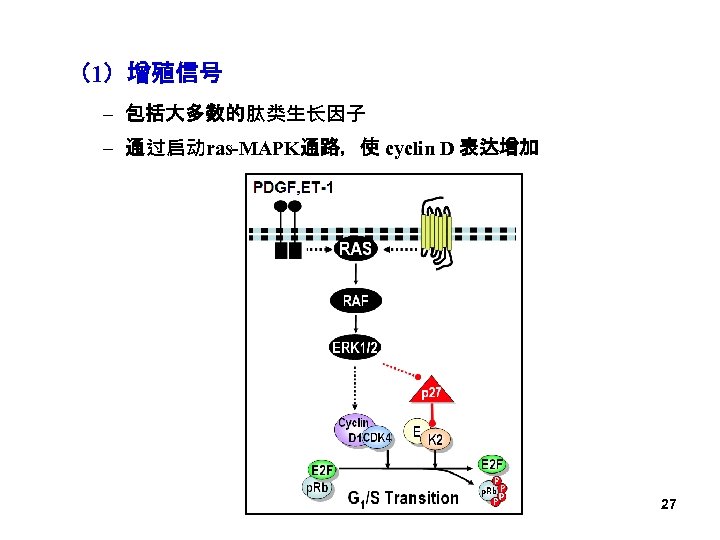
(1)增殖信号 – 包括大多数的肽类生长因子 – 通过启动ras-MAPK通路,使 cyclin D 表达增加 27
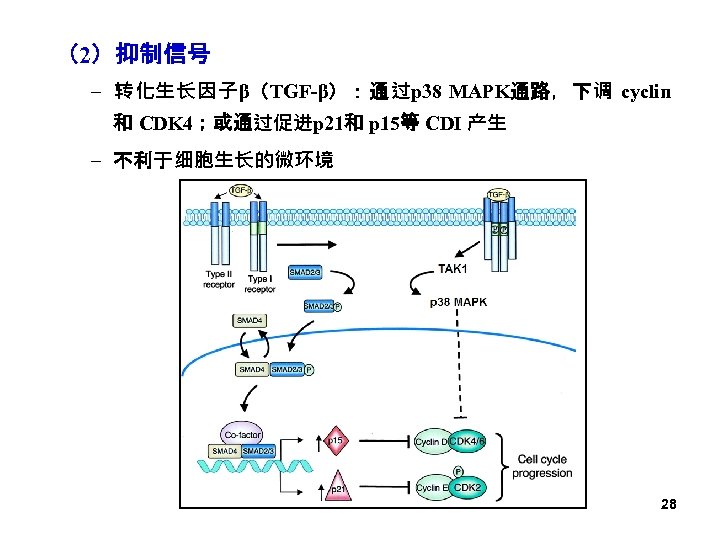
(2)抑制信号 – 转化生长因子β(TGF-β):通过p 38 MAPK通路,下调 cyclin 和 CDK 4;或通过促进p 21和 p 15等 CDI 产生 – 不利于细胞生长的微环境 28

三、细胞周期调控异常(Dysregulation of cell cycle) – 细胞周期的驱动失控(Cyclin、CDK和CDI表达异常) – 监控(检查)机制受损 细胞增殖异常与相关疾病 增殖过度 增殖分化异常 恶性肿瘤、前列腺肥大 糖尿病肾病 银屑病、原发性血小板增多症 神经退行性疾病 家族性红细胞增多症、类风湿关节炎再生障碍性贫血 肝肺肾纤维化、肾小管间质性病变 动脉粥样硬化 29
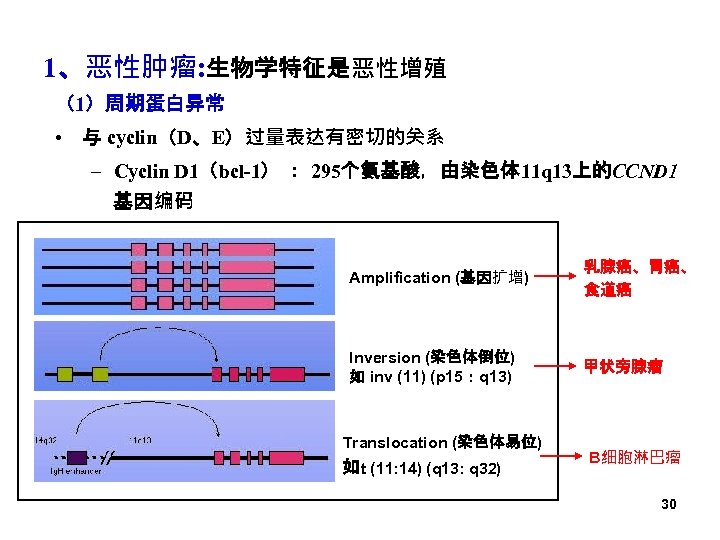
1、恶性肿瘤: 生物学特征是恶性增殖 (1)周期蛋白异常 • 与 cyclin(D、E)过量表达有密切的关系 – Cyclin D 1(bcl-1) : 295个氨基酸,由染色体 11 q 13上的CCND 1 基因编码 Amplification (基因扩增) 乳腺癌、胃癌、 食道癌 Inversion (染色体倒位) 如 inv (11) (p 15:q 13) 甲状旁腺瘤 Translocation (染色体易位) 如t (11: 14) (q 13: q 32) B细胞淋巴瘤 30
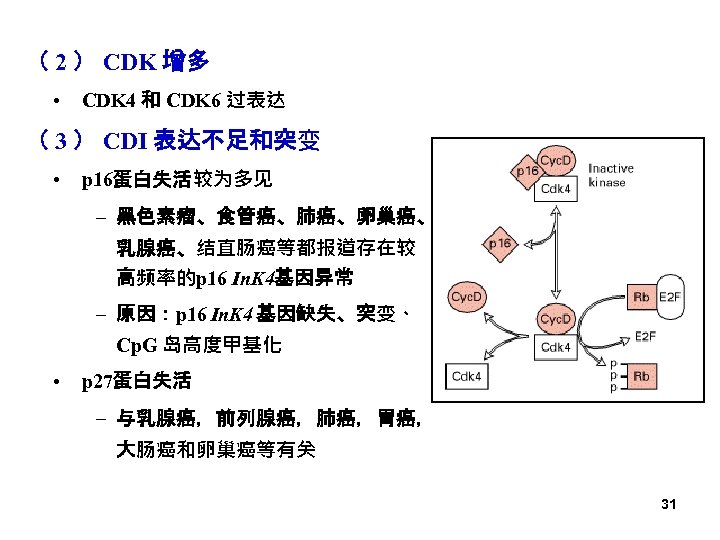
( 2 ) CDK 增多 • CDK 4 和 CDK 6 过表达 ( 3 ) CDI 表达不足和突变 • p 16蛋白失活较为多见 – 黑色素瘤、食管癌、肺癌、卵巢癌、 乳腺癌、结直肠癌等都报道存在较 高频率的p 16 In. K 4基因异常 – 原因:p 16 In. K 4 基因缺失、突变、 Cp. G 岛高度甲基化 • p 27蛋白失活 – 与乳腺癌,前列腺癌,肺癌,胃癌, 大肠癌和卵巢癌等有关 31
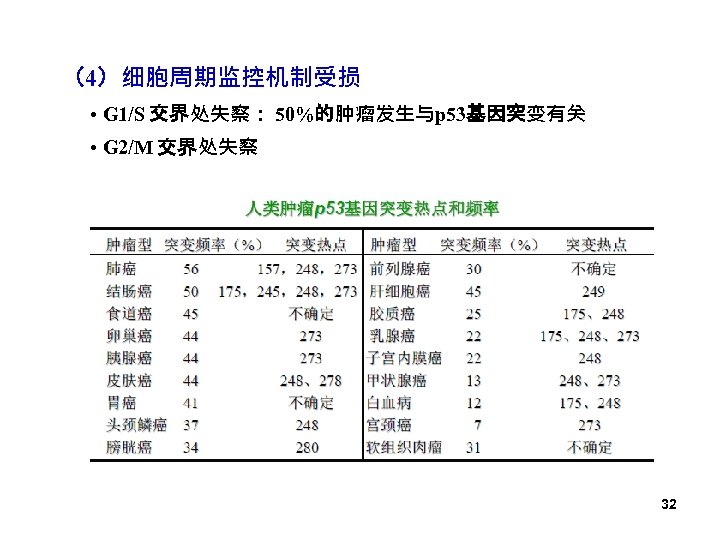
(4)细胞周期监控机制受损 • G 1/S 交界处失察: 50%的肿瘤发生与p 53基因突变有关 • G 2/M 交界处失察 32
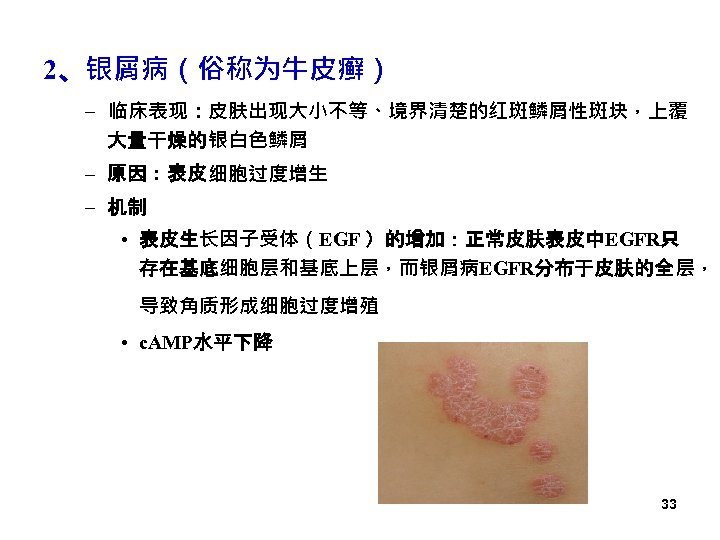
2、银屑病(俗称为牛皮癣) – 临床表现:皮肤出现大小不等、境界清楚的红斑鳞屑性斑块,上覆 大量干燥的银白色鳞屑 – 原因:表皮细胞过度增生 – 机制 • 表皮生长因子受体(EGF )的增加:正常皮肤表皮中EGFR只 存在基底细胞层和基底上层,而银屑病EGFR分布于皮肤的全层, 导致角质形成细胞过度增殖 • c. AMP水平下降 33
3、原发性血小板增多症( primary throbocythemia) – 临床特征:出血倾向及血栓形成 – 机制:骨髓巨核细胞过度增殖,外周血血小板持续明显增多(为 正常的2 -12倍),功能也不正常 – 病因:与X染色体遗传有关,血小板生成抑制因子TGF- 1减少、 血液微环境中辅助细胞的缺乏等 34
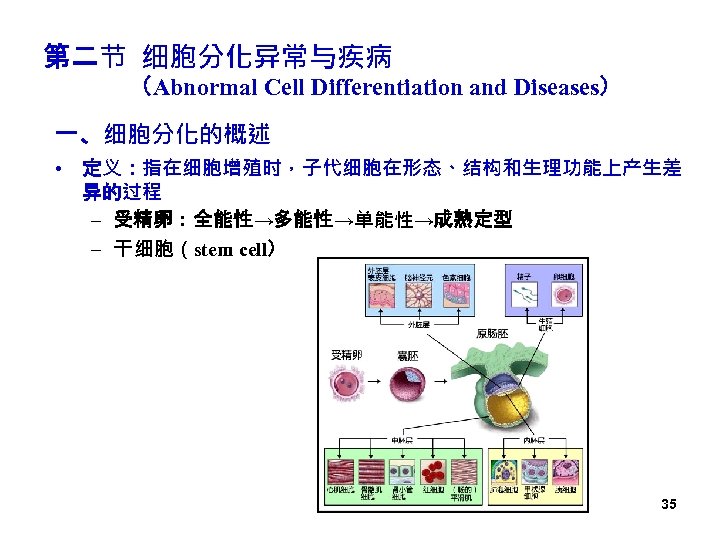
第二节 细胞分化异常与疾病 (Abnormal Cell Differentiation and Diseases) 一、细胞分化的概述 • 定义:指在细胞增殖时,子代细胞在形态、结构和生理功能上产生差 异的过程 – 受精卵:全能性→多能性→单能性→成熟定型 – 干细胞(stem cell) 35
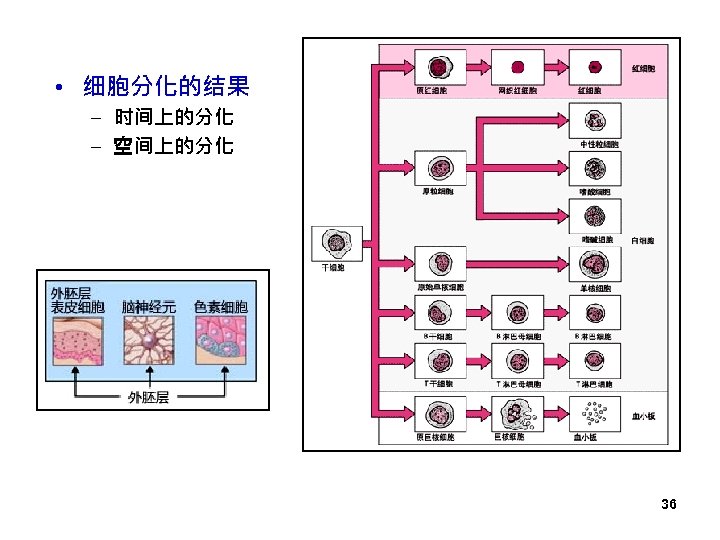
• 细胞分化的结果 – 时间上的分化 – 空间上的分化 36
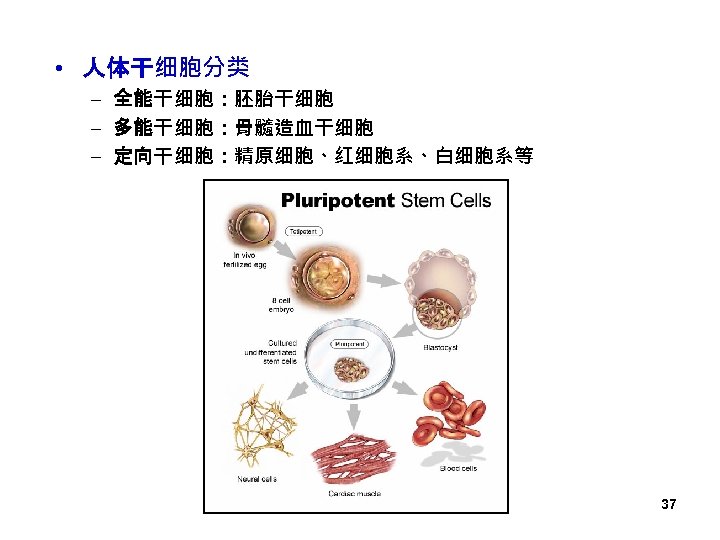
• 人体干细胞分类 – 全能干细胞:胚胎干细胞 – 多能干细胞:骨髓造血干细胞 – 定向干细胞:精原细胞、红细胞系、白细胞系等 37
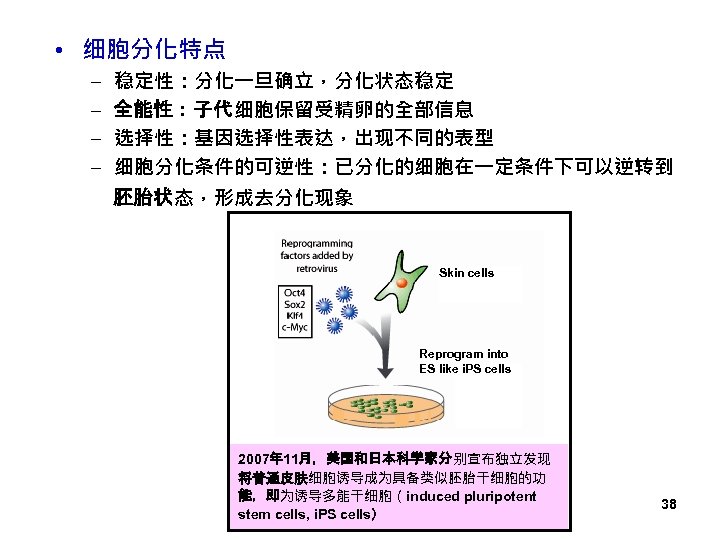
• 细胞分化特点 – – 稳定性:分化一旦确立,分化状态稳定 全能性:子代细胞保留受精卵的全部信息 选择性:基因选择性表达,出现不同的表型 细胞分化条件的可逆性:已分化的细胞在一定条件下可以逆转到 胚胎状态,形成去分化现象 Skin cells Reprogram into ES like i. PS cells 2007年 11月,美国和日本科学家分别宣布独立发现 将普通皮肤细胞诱导成为具备类似胚胎干细胞的功 能,即为诱导多能干细胞(induced pluripotent stem cells, i. PS cells) 38

二、细胞分化的机制及其调控 1、细胞分化的机制 – “决定”先于分化:细胞决定( determination )是指细胞内某 些基因永久地关闭,而另一些基因顺序表达,具备向某一特定方 向分化的能力 – 细胞质在决定细胞差别中作用 – 细胞间相互作用 – 微环境:壁龛(niche )结构包括壁龛细胞、细胞外基质( extracellular matrix,ECM)和来源于壁龛细胞的可溶性因子 39

2、细胞分化的调控 – 基因水平的调控 • 奢侈基因(luxury gene):编码细胞中特异性蛋白的基因, 对细胞分化起重要作用 • 管家基因( house keeping genes ):对细胞分化只起协作作用 – 转录和转录后水平调控 • 转录水平调控:调节蛋白(转录因子)对专一基因的启动子和增强 子进行调控 • 转录后水平调控:对 m. RNA 前体的处理和加 – 翻译与翻译后水平调控 – 细胞外因素调控:激素、细胞因子、黏附分子、药物等 40

三、细胞分化异常(Abnormal Cell Differentiation ) 1、肿瘤 • 肿瘤细胞的共同特征:细胞分化不足,而只是保持持续增殖 • 确定肿瘤细胞的分化程度对于肿瘤病情的判断具有重要意义 – 恶性肿瘤细胞异常分化的表现为:低分化;去分化(dedifferentiation) 或反分化(retrodifferentiation);趋异性分化(divergent differentiation) 即肿瘤细胞分化程度和分化方向的差异性 41

• 恶性肿瘤细胞异常分化的机制 – 细胞的增殖和分化脱耦联:在体外培养的癌细胞表现为失去密度 依赖性抑制,无限传代成为“永生的”细胞系 – 基因表达时空上失调 • 特异性基因表达受到抑制:如肝癌细胞不合成白蛋白;结肠肿 瘤不合成粘蛋白 • 胚胎性基因重现表达:如肝癌细胞过多合成甲胎蛋白和胎儿型 醛缩酶 A 等 – 癌基因和抑癌基因的协同失衡 42

• 细胞分化理论可用以指导临床肿瘤治疗 – 采取适当的方法诱导其发生终末分化,肿瘤的增殖能力就可能会 被抑制 – 能诱导肿瘤细胞发生分化的物质称为分化诱导剂 • 对正常细胞的非特异性毒副作用小,有非常好的应用前景 • 作用机理:诱导癌细胞向终未阶段分化的同时,启动了细胞 死亡程序 • 代表----维甲类(Retinoids):如全反式维甲酸已用于早幼粒 细胞白血病的临床治疗,视黄醇与干扰素a 合用治疗皮肤鳞癌 或宫颈鳞癌 43
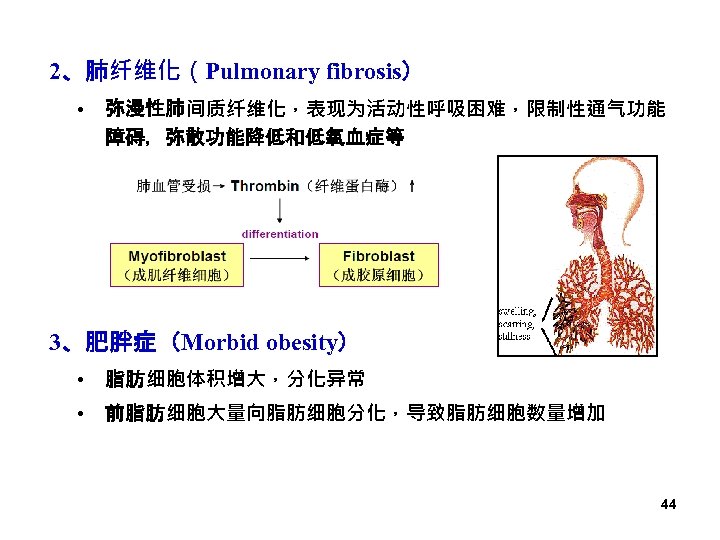
2、肺纤维化(Pulmonary fibrosis) • 弥漫性肺间质纤维化,表现为活动性呼吸困难,限制性通气功能 障碍,弥散功能降低和低氧血症等 3、肥胖症(Morbid obesity) • 脂肪细胞体积增大,分化异常 • 前脂肪细胞大量向脂肪细胞分化,导致脂肪细胞数量增加 44

4、畸胎瘤(teratoma) • 在胚胎不同时期,某些多能细胞脱落下来,分化发生异常 • 具有内胚层、中胚层和外胚层三个胚层的异常分化组织 45
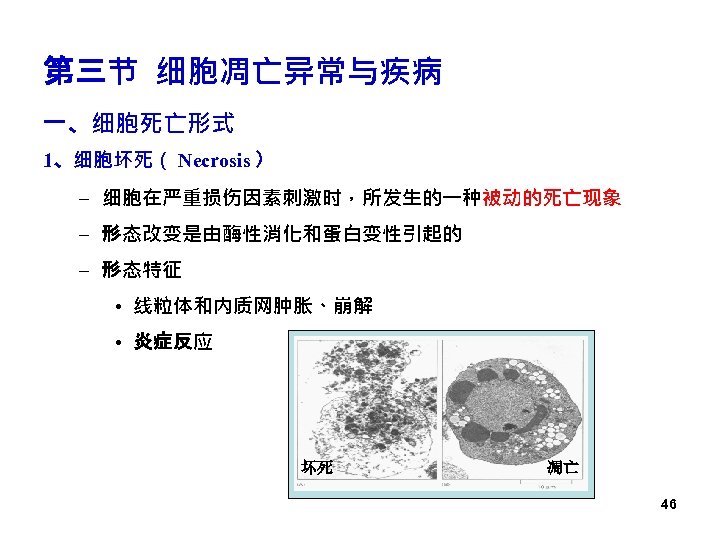
第三节 细胞凋亡异常与疾病 一、细胞死亡形式 1、细胞坏死( Necrosis ) – 细胞在严重损伤因素刺激时,所发生的一种被动的死亡现象 – 形态改变是由酶性消化和蛋白变性引起的 – 形态特征 • 线粒体和内质网肿胀、崩解 • 炎症反应 坏死 凋亡 46
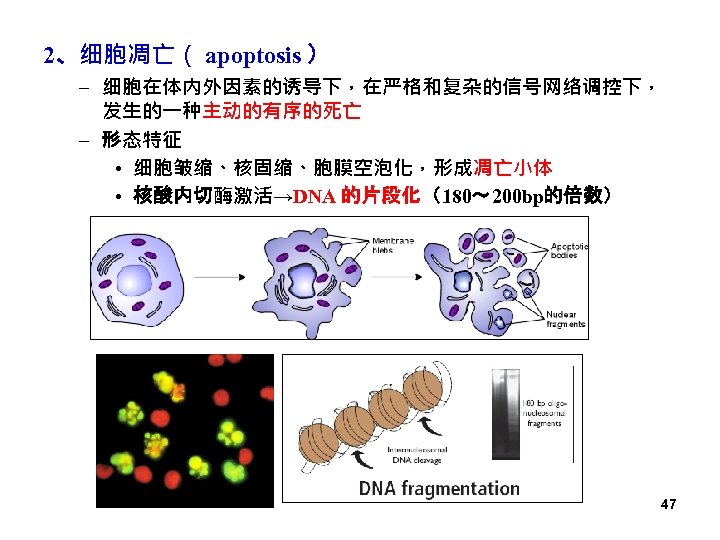
2、细胞凋亡( apoptosis ) – 细胞在体内外因素的诱导下,在严格和复杂的信号网络调控下, 发生的一种主动的有序的死亡 – 形态特征 • 细胞皱缩、核固缩、胞膜空泡化,形成凋亡小体 • 核酸内切酶激活→DNA 的片段化(180~ 200 bp的倍数) 47

– 细胞凋亡的生理学意义 • 清除多余的和失去功能的细胞,确保组织器官正常发育、生长 • 清除受损、突变或者衰老的细胞,维持内环境稳定 • 发挥积极的防御功能:当细胞受到病毒感染时,受感染的细胞 可以通过凋亡来阻止病毒的增殖,或通过 DNA 的降解,把病 毒的 DNA 进行分解 48

细胞凋亡与细胞坏死的比较 坏 死 凋 亡 1. 性 质 病理性,非特异性 生理性/病理性,特异性 2. 诱 因 强烈刺激,随机发生 较弱刺激,非随机发生 3. 基因调控 4. 生化特点 无 被动过程, 无新蛋白合成, 不耗能 5. 形态改变 细胞肿胀 结构溶解,破坏 6. 凋亡小体 无 7. DNA变化 弥散性降解 电泳呈均一片状 8. 溶酶体改变 破裂 9. 炎症反应 局部炎症反应 有 主动过程, 有新蛋白合成, 耗能 细胞皱缩,核固缩 胞膜/细胞器相对完整 有 片段化(180 -200 bp) 电泳呈“梯”状条带 相对完整 局部无炎症反应 49
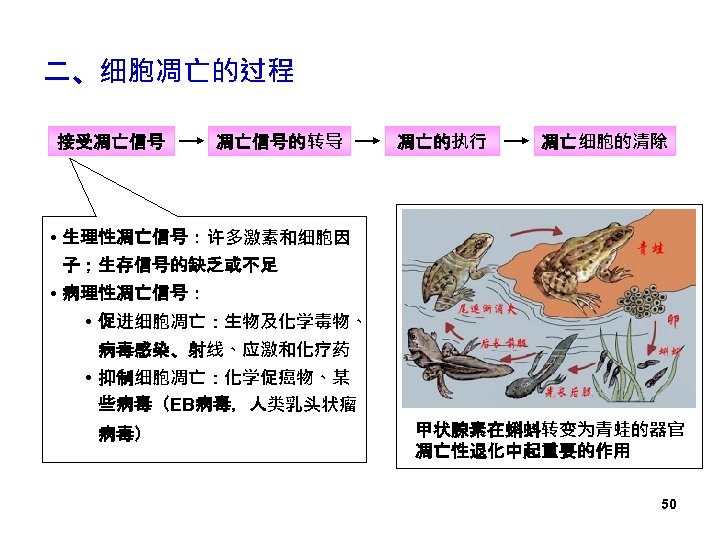
二、细胞凋亡的过程 接受凋亡信号的转导 凋亡的执行 凋亡细胞的清除 • 生理性凋亡信号:许多激素和细胞因 子;生存信号的缺乏或不足 • 病理性凋亡信号: • 促进细胞凋亡:生物及化学毒物、 病毒感染、射线、应激和化疗药 • 抑制细胞凋亡:化学促癌物、某 些病毒(EB病毒,人类乳头状瘤 病毒) 甲状腺素在蝌蚪转变为青蛙的器官 凋亡性退化中起重要的作用 50
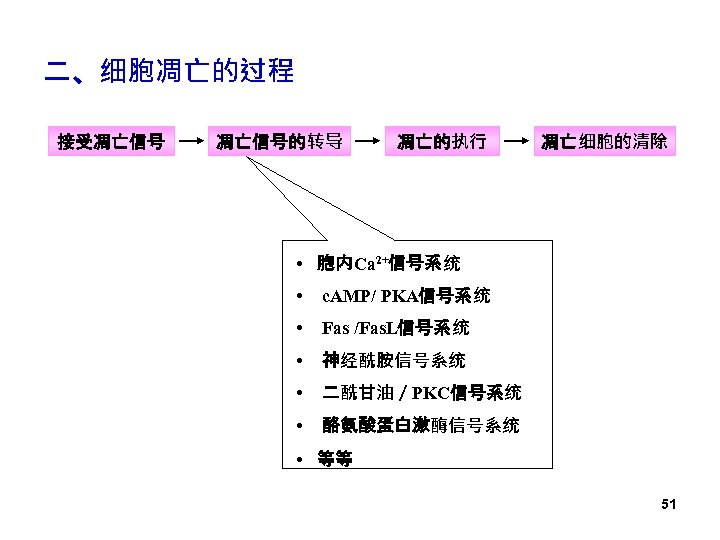
二、细胞凋亡的过程 接受凋亡信号的转导 凋亡的执行 凋亡细胞的清除 • 胞内Ca 2+信号系统 • c. AMP/ PKA信号系统 • Fas /Fas. L信号系统 • 神经酰胺信号系统 • 二酰甘油/PKC信号系统 • 酪氨酸蛋白激酶信号系统 • 等等 51

• 这个系统的特点 – 多样性:不同种类的细胞有不同的信号转导系统 – 耦联性:死亡信号的转导系统与细胞增殖、分化过程中的信号转 导系统在某些环节上有交叉、耦联 – 同一性:不同的凋亡诱导因素可以通过同一信号转导系统触发细 胞凋亡 – 多途性:同一凋亡诱导因素可经过多条信号转导途径触发凋亡 52
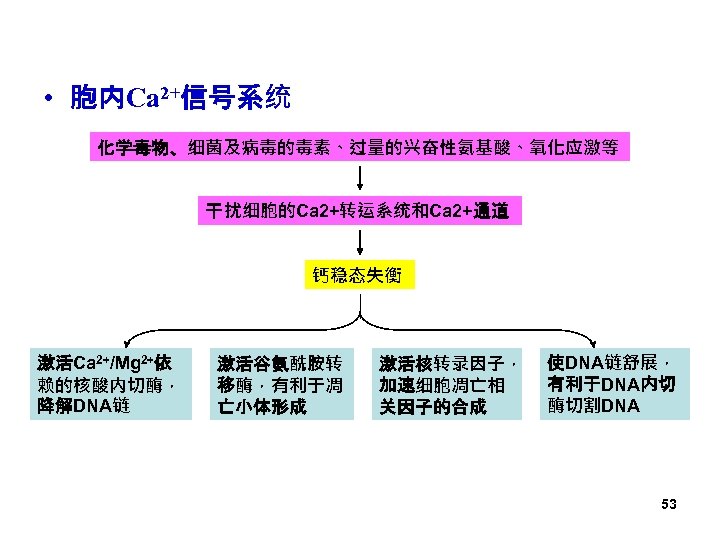
• 胞内Ca 2+信号系统 化学毒物、细菌及病毒的毒素、过量的兴奋性氨基酸、氧化应激等 干扰细胞的Ca 2+转运系统和Ca 2+通道 钙稳态失衡 激活Ca 2+/Mg 2+依 赖的核酸内切酶, 降解DNA链 激活谷氨酰胺转 移酶,有利于凋 亡小体形成 激活核转录因子, 加速细胞凋亡相 关因子的合成 使DNA链舒展, 有利于DNA内切 酶切割DNA 53
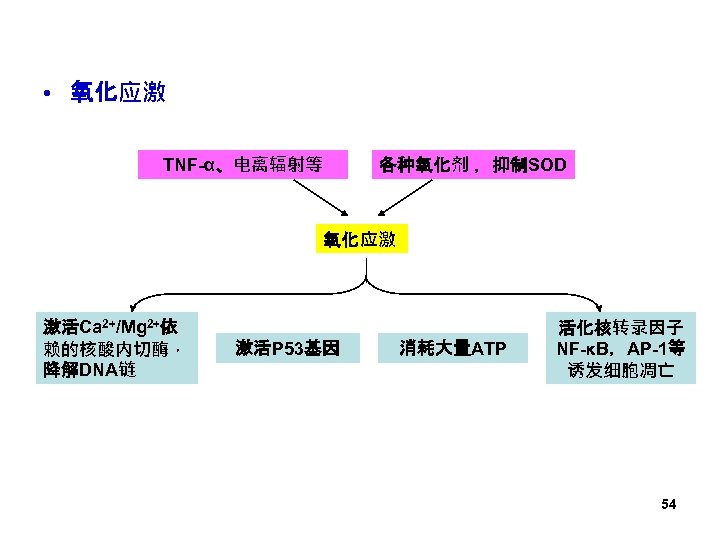
• 氧化应激 TNF-α、电离辐射等 各种氧化剂 ,抑制SOD 氧化应激 激活Ca 2+/Mg 2+依 赖的核酸内切酶, 降解DNA链 激活P 53基因 消耗大量ATP 活化核转录因子 NF-κB,AP-1等 诱发细胞凋亡 54
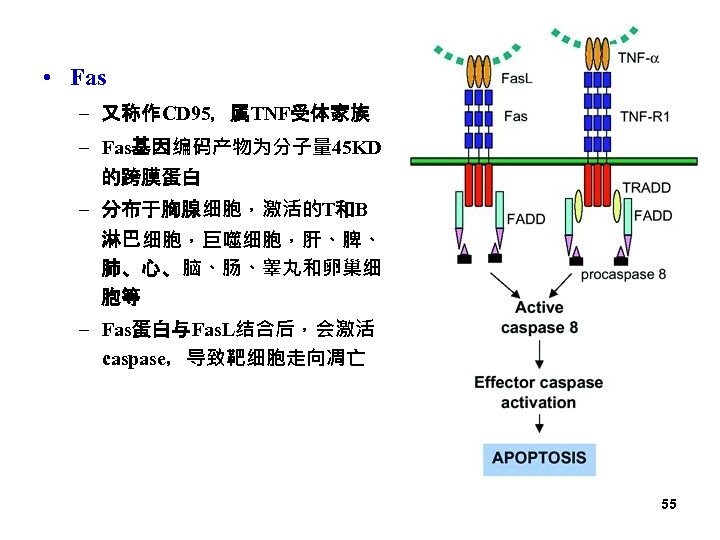
• Fas – 又称作CD 95,属TNF受体家族 – Fas基因编码产物为分子量 45 KD 的跨膜蛋白 – 分布于胸腺细胞,激活的T和B 淋巴细胞,巨噬细胞,肝、脾、 肺、心、脑、肠、睾丸和卵巢细 胞等 – Fas蛋白与Fas. L结合后,会激活 caspase,导致靶细胞走向凋亡 55

– Fas所介导的细胞凋亡的信号转导机制 • Fas. L或抗Fas抗体与Fas蛋白结合,引起神经鞘磷脂酶的活性 迅速上升,使神经鞘磷脂分解产生神经酰胺,神经酰胺作为第 二信使激活相应的蛋白激酶,从而诱导细胞凋亡 • 抗Fas抗体或TNF与Fas蛋白结合后可激活ICE样的caspase, 后者可降解H 1组蛋白,使染色体松弛,DNA链舒展而暴露出 核酸内切酶的酶切位点,使DNA链更容易被切割 • Fas蛋白被激活后也可以通过Ca 2+信号系统传递死亡信息而导 致细胞凋亡 56

• 神经酰胺信号系统 – 神经酰胺(ceramide)是神经鞘磷脂(sphingomyelin, SM)在SM 酶的作用下产生的一类新型第二信使 – 生物学效应包括:诱导凋亡;抑制细胞生长;引起细胞周期阻滞, 细胞周期通常被阻滞于G 0/G 1期 – 电离辐射、TNF-a、Fas、糖皮质激素均可通过神经酰胺信号系统 诱导细胞凋亡 57

• 线粒体损伤 – 凋亡的早期就会出现线粒体内膜通透性增大,线粒体跨膜电位( △ψm)明显下降 – 线粒体损伤引起细胞凋亡的可能机制是:线粒体内、外膜之间的 PTP具有调节线粒体膜通透性的作用,使细胞凋亡的启动因子如 细胞色素C(Cyt. C)、凋亡蛋白酶激活因子(Apaf)和凋亡诱导因 子(AIF)等从线粒体内释放出来 58
二、细胞凋亡的过程 接受凋亡信号的转导 凋亡的执行 凋亡细胞的清除 • Caspases • 内源性核酸内切酶(如Endo. G) • 作用:切割染色质DNA • 特点:这些酶多数为Ca 2+/Mg 2+依赖的, 但Zn 2+可抑制其活性 59
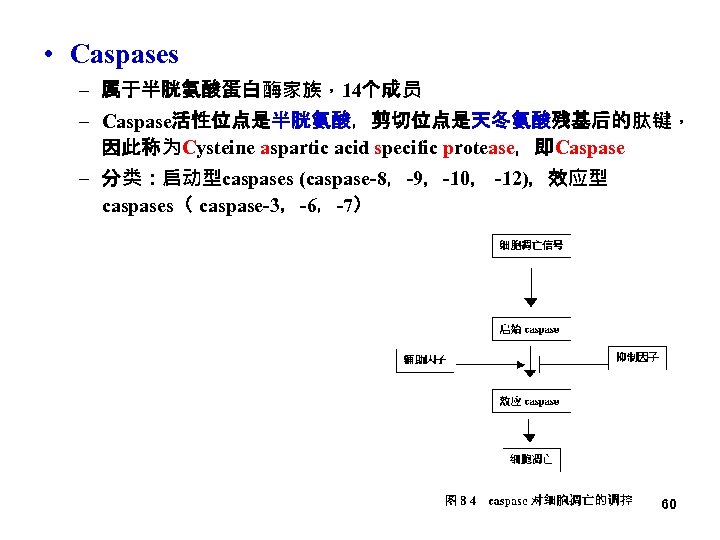
• Caspases – 属于半胱氨酸蛋白酶家族,14个成员 – Caspase活性位点是半胱氨酸,剪切位点是天冬氨酸残基后的肽键, 因此称为Cysteine aspartic acid specific protease,即Caspase – 分类:启动型caspases (caspase-8,-9,-10, -12),效应型 caspases( caspase-3,-6,-7) 60
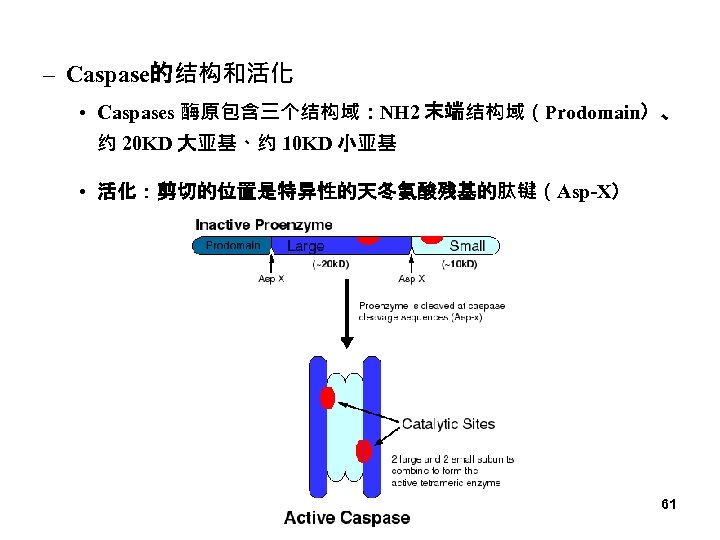
– Caspase的结构和活化 • Caspases 酶原包含三个结构域:NH 2 末端结构域(Prodomain)、 约 20 KD 大亚基、约 10 KD 小亚基 • 活化:剪切的位置是特异性的天冬氨酸残基的肽键(Asp-X) 61
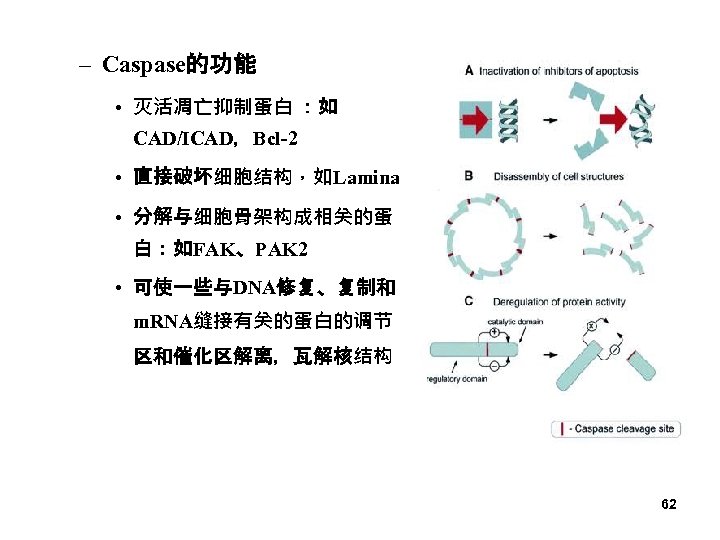
– Caspase的功能 • 灭活凋亡抑制蛋白 :如 CAD/ICAD,Bcl-2 • 直接破坏细胞结构,如Lamina • 分解与细胞骨架构成相关的蛋 白:如FAK、PAK 2 • 可使一些与DNA修复、复制和 m. RNA缝接有关的蛋白的调节 区和催化区解离,瓦解核结构 62

– 按照启动型caspase的不同,凋亡信号转导途径分为 • 外在途径(extrinsic pathway)或死亡受体途径:由细 胞表面的死亡受体如Fas和肿瘤坏死因子受体家族 (tumour necrosis factor receptor,TNF-R)引发,导 致caspase-8或 10的活化 • 内在途径(intrinsic pathway)或线粒体途径 (mitochondrial pathway):由许多应激条件、化学治 疗试剂和药物所起始,导致caspase-9的活化 • 内质网应激途径:各凋亡信号导致的caspase-12的活 化,从而导致凋亡 63
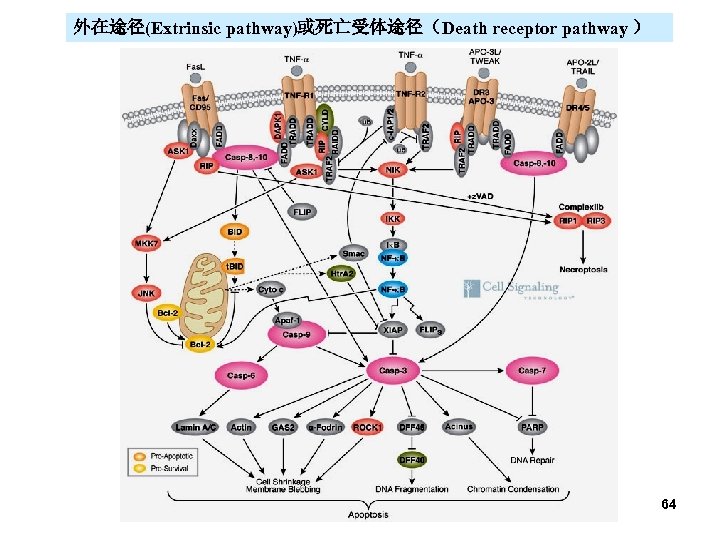
外在途径(Extrinsic pathway)或死亡受体途径(Death receptor pathway ) 64
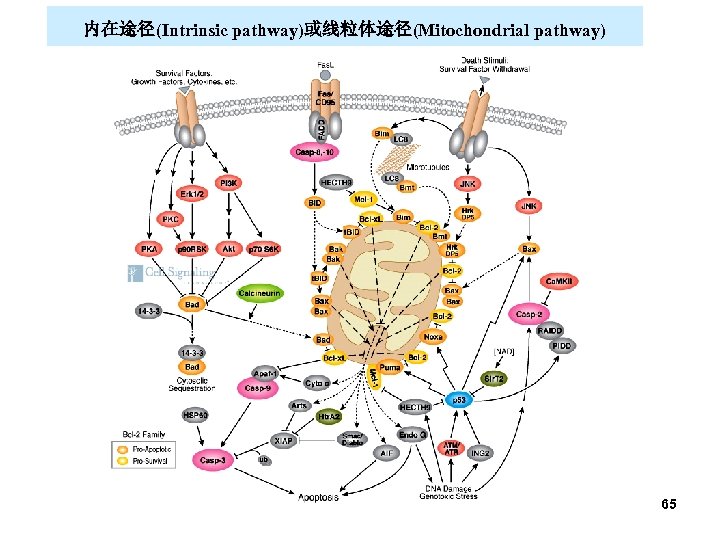
内在途径(Intrinsic pathway)或线粒体途径(Mitochondrial pathway) 65
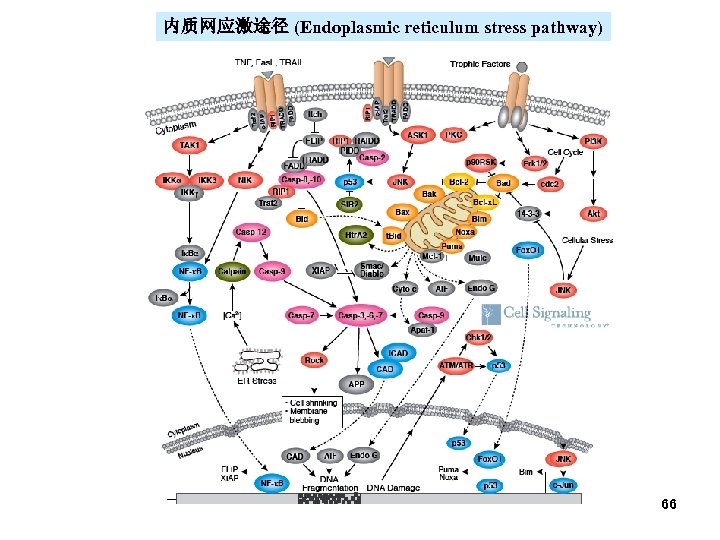
内质网应激途径 (Endoplasmic reticulum stress pathway) 66
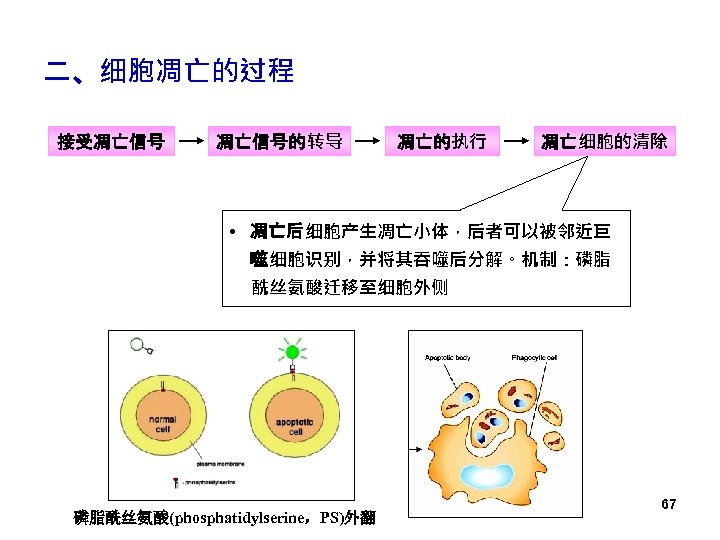
二、细胞凋亡的过程 接受凋亡信号的转导 凋亡的执行 凋亡细胞的清除 • 凋亡后细胞产生凋亡小体,后者可以被邻近巨 噬细胞识别,并将其吞噬后分解。机制:磷脂 酰丝氨酸迁移至细胞外侧 磷脂酰丝氨酸(phosphatidylserine,PS)外翻 67

三、细胞凋亡的调控机制 功能 抑制凋亡基因 基因 Bcl-2、Bcl-XL、A 1/Bfl-1、Bcl-w、Bcl-G和Mcl-1等 促凋亡基因 P 53、Bax、Bad、Bak、Bid、Bim、Bik、Bok、 Bcl-B、 Bcl-Xs、Krk、Mtd、Nip 3、Nix、Noxa等 双向调控基因 c-myc、Bel-x 68
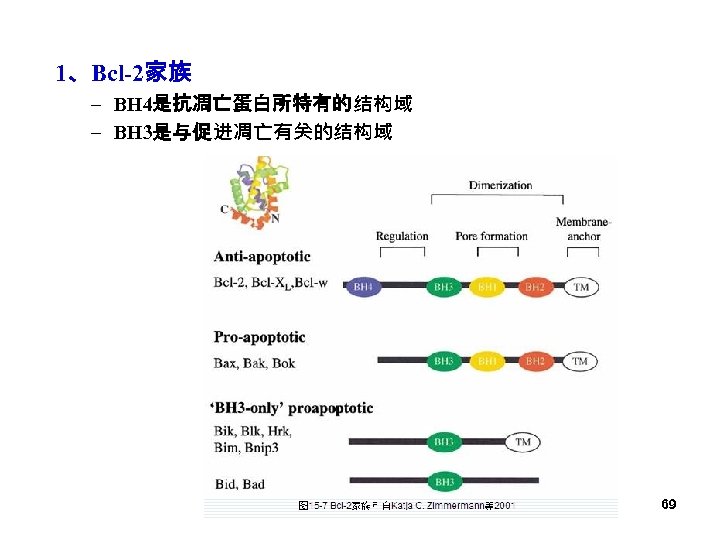
1、Bcl-2家族 – BH 4是抗凋亡蛋白所特有的结构域 – BH 3是与促进凋亡有关的结构域 69

– Bcl-2等抗凋亡蛋白 • 存在于线粒体膜、内质网膜以及外核膜上,但主要定位于线粒 体外膜 • 抗凋亡的机制 – 直接抗氧化 – 抑制线粒体释放促凋亡的蛋白质 – 抑制促凋亡调节蛋白Bax、Bak的细胞毒作用 – 抑制凋亡蛋白酶的激活 – 维持细胞钙稳态 70

– 促凋亡蛋白 • 主要定位于细胞质 • 受到凋亡因子的诱导而激活后,向线粒体转位,通过寡聚化在线 粒体外膜形成跨膜通道,或者开启线粒体的PT孔,从而导致线 粒体中的凋亡因子释放,激活caspase,导致细胞凋亡 • 激活方式: – 去磷酸化,如Bad – 被caspase加 为活性分子,如Bid – 从结合蛋白上释放出来,如Bim是与微管蛋白结合在一起的 71

2、p 53: “ 分子警察”(molecular policeman) – 促凋亡机制 • P 53通过与Bcl-2基因相互作用,下调Bcl-2的表达 • P 53诱导细胞凋亡的靶蛋白表达(线粒体和死亡受体介导) • P 53诱导线粒体内凋亡的相关蛋白(Bax、NOXA、 PUMA) 表达,并触发细胞色素C释放和caspase活化 • P 53诱导死亡受体Fas表达 • P 53能使死亡受体再定位于细胞膜上 72

四、细胞凋亡异常与疾病 73
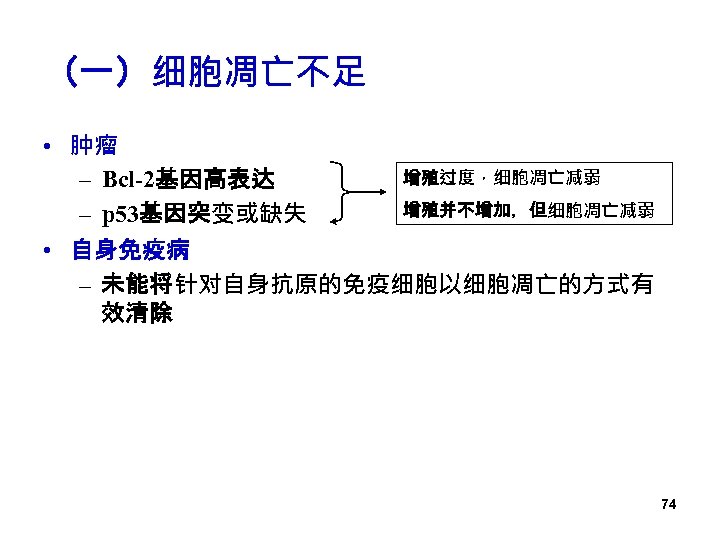
(一)细胞凋亡不足 • 肿瘤 增殖过度,细胞凋亡减弱 – Bcl-2基因高表达 增殖并不增加,但细胞凋亡减弱 – p 53基因突变或缺失 • 自身免疫病 – 未能将针对自身抗原的免疫细胞以细胞凋亡的方式有 效清除 74

(二)细胞凋亡过度 • 心肌缺血与缺血-再灌注损伤 – 缺血早期以凋亡为主,晚期以细胞的坏死为主 – 在梗死灶的中心以坏死为主,梗死灶周边以凋亡为主 – 轻度缺血以凋亡为主,重度缺血以坏死为主 – 缺血-再灌注损伤时发生的细胞凋亡单纯缺血更严重 – 急性、严重的心肌缺血以心肌坏死为主,而慢性、轻 度的心肌缺血则发生细胞凋亡 • 心力衰竭 – 氧化应激/压力、容量负荷↑/神经-内分泌失调/TNF/缺血 /缺氧→心肌细胞凋亡 75
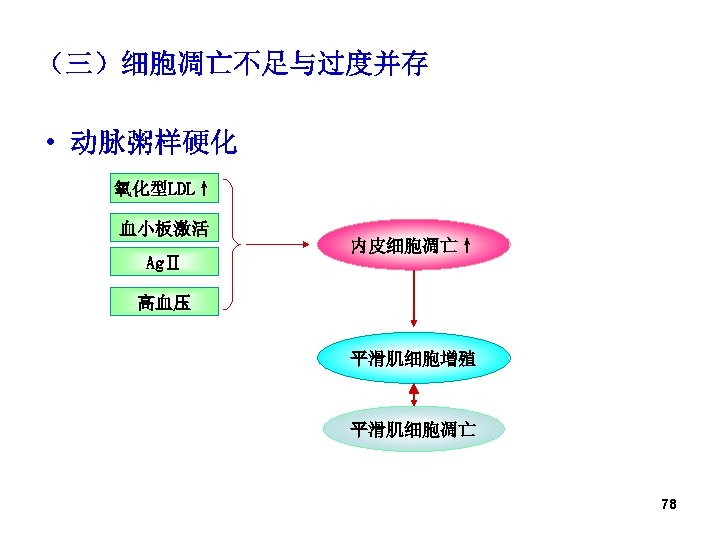
(三)细胞凋亡不足与过度并存 • 动脉粥样硬化 氧化型LDL↑ 血小板激活 AgⅡ 内皮细胞凋亡↑ 高血压 平滑肌细胞增殖 平滑肌细胞凋亡 78

五、细胞凋亡与疾病防治 1、合理利用凋亡因素 – 低剂量照射→急性T细胞性白血病 – TNF-α→白血病细胞株U 937 – 高温(43℃)→肿瘤 – NGF→老年性痴呆 – 撤除雄激素→前列腺癌 79

2、干预凋亡信号转导 – 阿霉素→Fas/Fas. L表达↑→肿瘤细胞凋亡 – 环孢霉素A →调节和抑制线粒体介导的凋亡 3、调节凋亡相关基因 – 基因转移 wt. P 53→P 53基因突变肿瘤细胞 – 基因封闭 反义寡核苷酸→bcl-2表达 80

4、控制凋亡相关酶的活性 – 核酸内切酶和caspases – Ca 2+载体/阻断剂→核酸内切酶活性↑/↓ – Zn 2+↑→caspases活性↓ 81

第四节 细胞自噬异常与疾病 一、自噬(Autophagy)的定义 – 11962年Ashford等在胰高血糖素处理的小鼠肝细胞中 观察到autophagy – 1963年, De Duve首次提出细胞自噬的生物学概念: 细 胞在缺乏营养和能量供应时,部分细胞质与细胞器被包 裹进一种特异性的双层膜或者多层膜结构的自噬体 (autophagosome)中,形成的自噬体再与溶酶体 (Lysosome)融合形成自噬溶酶体(autolysosome),胞质 和细胞器成分在这里被降解为核苷酸、氨基酸、游离脂 肪酸等小分子物质,这些小分子物质可以被重新利用合 成大分子或者合成ATP。 82 82

二、细胞自噬过程 – 自噬体膜的来源: • 粗面内质网的非核糖体区域 • 高尔基体 • 一种新合成的结构 – 被降解物: • 部分胞浆 • 细胞内需降解的细胞器(线粒体) • 细胞内需降解的蛋白质 83

1. 饥饿、氧化应激损伤→自噬体膜脱落,形成 环状分隔膜,包绕在被降解物周围 2. 分隔膜逐渐延伸,将要被降解的胞浆成分完 全包绕形成自噬体(autophagosome) 3. 自噬体通过细胞骨架微管系统运输至溶酶体, 与之融合形成自噬溶酶体(autolysosome), 并降 解其内成分,自噬体膜脱落再循环利用 84
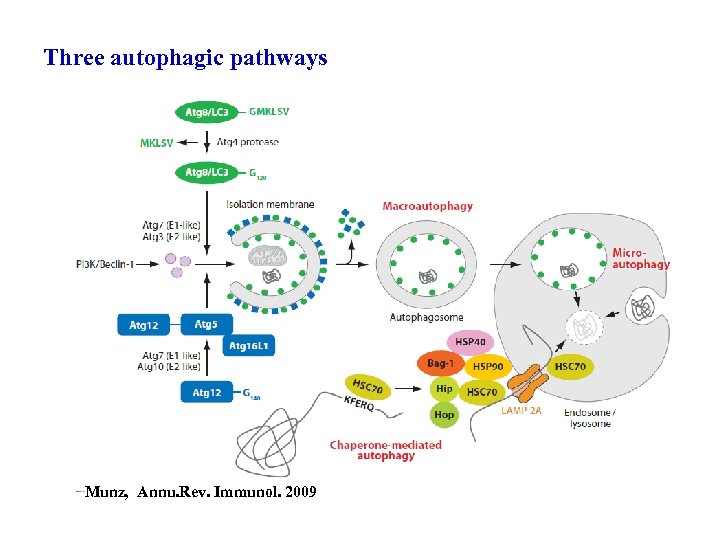
Three autophagic pathways Munz, Annu. Rev. Immunol. 2009
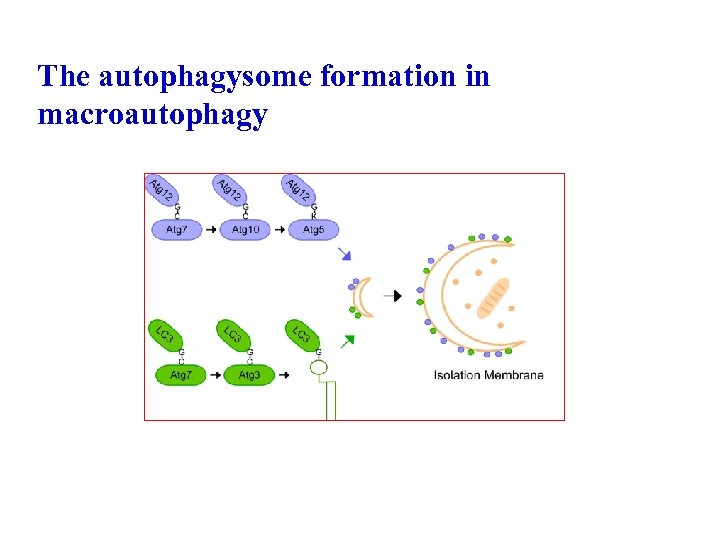
The autophagysome formation in macroautophagy

三、自噬的功能 – 对外源性刺激(包括营养缺乏、细胞密度负荷、低氧、 氧化应激、感染等)的适应性反应:降解产物氨基酸、 核苷酸、游离脂肪酸等可供物质能量循环 – 细胞保持稳定状态的管家机制:调控长寿命蛋白、过 氧化物体、线粒体和内质网的更新 – 参与一定的组织特异性融合 – 一种防御机制: 清除胞质内受损的细胞器、代谢产物, 进 行亚细胞水平上的重构, 保护受损的细胞;作为一种细 胞死亡程序诱导细胞主动性死亡 87
01ffe12bc539aea60d5283a97d91f501.ppt