f3484d193f882a63c88d77d1b27e5a73.ppt
- Количество слайдов: 163

提升認可傳染病檢驗機構及小中型實驗室品管 主講:盧世乾 理事長 現職:中華民國醫事檢驗師公會全國聯合會 主辦單位:秀傳醫療財團法人彰濱秀傳紀念醫院、 彰化縣醫事檢驗師公會 、彰化縣衛生局 地 點:秀傳醫療財團法人彰濱秀傳紀念醫院 1樓人文藝術館 時 間: 101年 09月 15日 10: 20 -11: 10

認可傳染病檢驗品質 政策說明 2
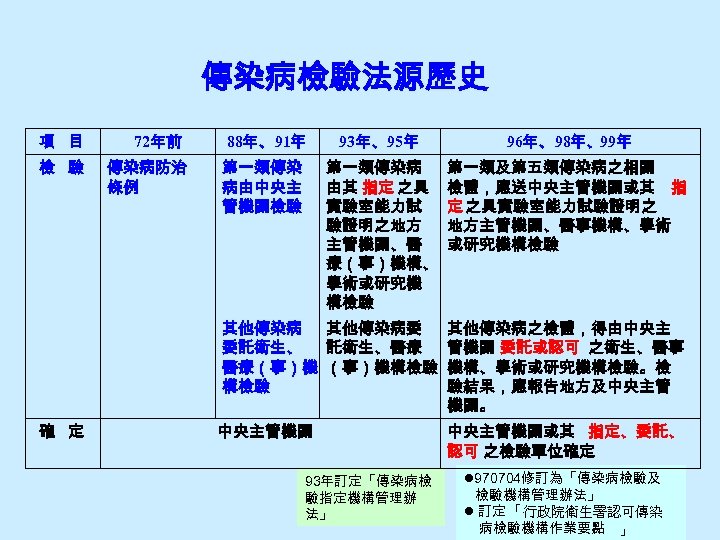
傳染病檢驗法源歷史 項 目 檢 驗 確 定 72年前 88年、91年 93年、95年 96年、98年、99年 傳染病防治 條例 第一類傳染 病由中央主 管機關檢驗 第一類傳染病 由其 指定 之具 實驗室能力試 驗證明之地方 主管機關、醫 療(事)機構、 學術或研究機 構檢驗 第一類及第五類傳染病之相關 檢體,應送中央主管機關或其 指 定 之具實驗室能力試驗證明之 地方主管機關、醫事機構、學術 或研究機構檢驗 其他傳染病委 委託衛生、醫療 醫療(事)機構檢驗 其他傳染病之檢體,得由中央主 管機關 委託或認可 之衛生、醫事 機構、學術或研究機構檢驗。檢 驗結果,應報告地方及中央主管 機關。 中央主管機關 93年訂定「傳染病檢 驗指定機構管理辦 法」 中央主管機關或其 指定、委託、 認可 之檢驗單位確定 l 970704修訂為「傳染病檢驗及 檢驗機構管理辦法」 l 訂定 「行政院衛生署認可傳染 病檢驗機構作業要點 」

緣起與紀事 • 目的 • • 建構傳染病檢驗網 提供即時且正確之檢驗服務 有效之疫病監測及通報 品質提 升 97. 04 辦法修訂公 告 98. 01授證開 始 加強宣導 99起實地訪查 100~101 啟動輔導計 畫 4

法源依據 -1 ◎ 「傳染病防治法」第 46條 ◎ 「傳染病檢驗及檢驗機構管理辦法 」 檢驗指定、委託、認可機構之資格、期限、申請、審核 之程序、檢體及其檢出病原體之保存及其他應遵 行事項之辦法。 5

傳染病檢驗機構申請資格 種 類 辦理方式 傳染病類 別 指 定 經本局指 定 第一類及 第五類 1. 具 BSL-3或 BSL-4實驗室 2. 人員經生物安全訓練合 格 3. 具實驗室生物安全管理 措 施及文件 本局酌 予部分 或全額 補助 委 託 經本局公 告甄選程 序 第二類 第三類 第四類 1. 使用中央主管機關規定 之 標準方法 2. 經實驗室能力試驗合格 3. 通過相當等級實驗室生 物 安全檢測 4. 備有生物安全管理手冊 或 規定 依簽定 之合約 訂定補 助標準 資 格 費用支 付 管理機制 1. 書面審 查 (4年效 期) 2. 每 2年能 力試驗 書面審 查 3. 實地訪 查至少 1 次 4. 檢驗結 果線上 通報 5. 檢驗結 果異常 3 日內傳 6 真通報
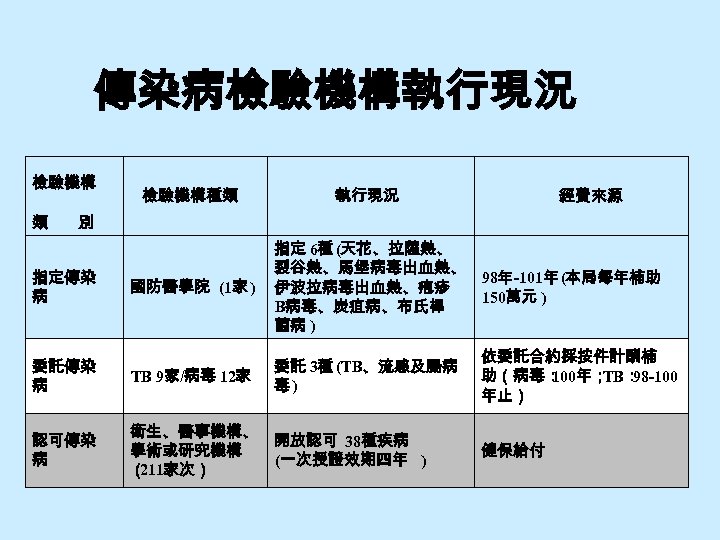
傳染病檢驗機構執行現況 檢驗機構 類 檢驗機構種類 執行現況 經費來源 別 國防醫學院 (1家 ) 指定 6種 (天花、拉薩熱、 裂谷熱、馬堡病毒出血熱、 98年-101年 (本局每年補助 伊波拉病毒出血熱、疱疹 150萬元 ) B病毒、炭疽病、布氏桿 菌病 ) 委託傳染 病 TB 9家/病毒 12家 委託 3種 (TB、流感及腸病 毒) 認可傳染 病 衛生、醫事機構、 開放認可 38種疾病 學術或研究機構 (一次授證效期四年 ) ( 211家次) 指定傳染 病 依委託合約採按件計酬補 助(病毒: 100年; TB: 98 -100 年止) 健保給付
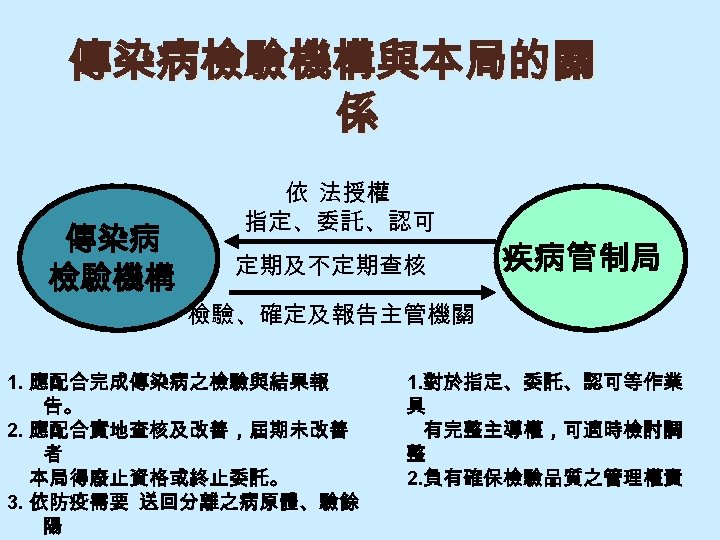
傳染病檢驗機構與本局的關 係 傳染病 檢驗機構 依 法授權 指定、委託、認可 定期及不定期查核 疾病管制局 檢驗、確定及報告主管機關 1. 應配合完成傳染病之檢驗與結果報 告。 2. 應配合實地查核及改善,屆期未改善 者 本局得廢止資格或終止委託。 3. 依防疫需要 送回分離之病原體、驗餘 陽 1. 對於指定、委託、認可等作業 具 有完整主導權,可適時檢討調 整 2. 負有確保檢驗品質之管理權責
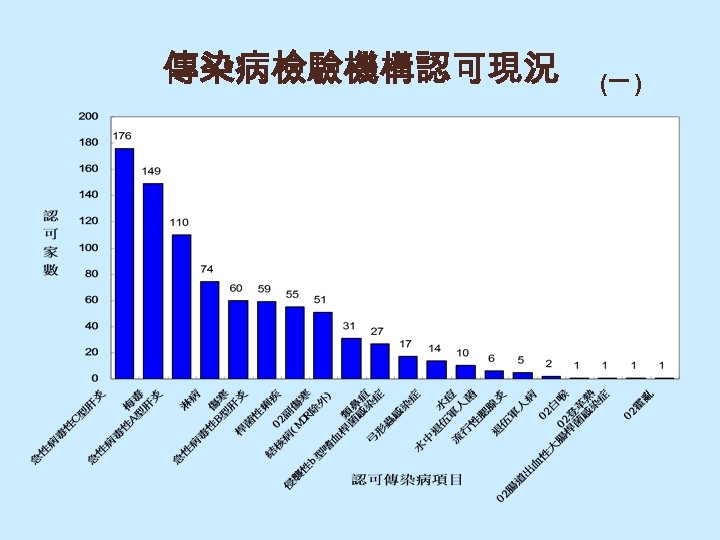
傳染病檢驗機構認可現況 (一 )

傳染病檢驗認可制度 認可證書效期 -四 年

法源依據 -2 ◎ 「傳染病防治法」第 46條第 1項之第 2款及第 3款 第四十六條 傳染病病人之體液、分泌物、排泄物與其他可能具傳染性物品之採檢、檢驗 與報告、確定及消毒,應採行下列方式: 一、採檢: ……………………………………………. 二、檢驗與報告:第一類及第五類傳染病之相關檢體,應送中央主管機關或其 指定 之具 實驗室能力試驗證明之地方主管機關、醫事機構、學術或研究機構檢驗;其他傳染 病之檢體,得由中央主管機關 委託 或 認可 之 衛生、醫事機構、學術或研究 機構檢驗。 檢驗結果,應報告地方及中央主管機關。 三、確定 :傳染病檢驗結果,由中央主管機關或其指定、委託、認可之檢驗單位確定之。 四、消毒:…………………………………………… 前項第一款病人檢體之採檢項目、採檢時間、送驗方式及第二款檢驗指定、委託、認可 機構之資格、期限、申請、審核之程序、檢體及其檢出病原體之保存及其他應遵行事項 之辦法,由中央主管機關定之。 11

法源依據 -3 ◎ 「傳染病防治法」第 67條 違反第 46條第一項規定,檢驗機構未配合檢驗、報告、確 定者,除逕行強制處分外並得處新台幣六萬元以上三十萬元 以下罰款。 ◎ 「傳染病防治法」第 69條 違反第 46條第一項第二款規定,未配合檢驗、報告者,處新 台幣一萬元以上十五萬元以下罰款。必要時, 並得限期令其改 善,屆期未改善者,按次處罰之。 ◎ 「傳染病防治法」第 70條 違反第 46條第二項檢體及其檢出病原體之保存規定者,處 新台幣三千元以上一萬伍千元以下罰款。必要時, 並得限期令 其改善,屆期未改善者,按次處罰之。 12
行政規範 機構資格、期限、 申請、審核之程序 行政院衛生署認 可傳染病檢驗機 構作業要點 採檢項目、 採檢時間、 送驗方式 、 檢驗時效 。 防疫檢體 採檢手冊 傳染病標準 檢驗方法手 冊 檢驗方法 13

傳染病檢驗認可現況 類別 (計 40項 ) 通過認可 (計 20項 ) 申請未通過 (計 8項 ) 第二類 (共 16項 ) 白喉、 傷寒、 登革熱、 副傷寒、 桿 菌 性 痢 疾 、急 性 病 毒 性 A 型肝炎、 道出血性大腸桿 腸 菌感染症、霍亂 (8項 ) 阿米巴性痢疾、 瘧疾、麻疹、德國 麻疹 (4項 ) 第三類 (共 12項 ) 結核病( 多重抗藥性結核 除 病 外 ) 除 A型 外 之 急 性 病 毒 、 性 肝 炎 (B型 及 C型 ) 、 行 性 流 腮 腺 炎 、 伍 軍 人 病 (水 中 退 退 伍 軍 人 菌 )、 襲 性 b 嗜 血 侵 型 桿菌感染症、梅毒、淋病 (9項 ) 先天性德國麻疹 症候群 (1項 ) 申請後 終止 (計 1 漢他病毒症候群、 屈公病、西尼羅熱、 流行性斑疹傷寒 (4 項) 百日咳、日本腦炎 (2項 ) 第四類 類鼻疽、水痘、弓形 (共 12項 ) 蟲感染症 (3項 ) 肉毒桿菌中毒、侵 襲性肺炎鏈球菌感 染症、貓抓病 (3項 ) 未提出申請 (計 11項 ) 項) 鉤端螺旋體病、 Q熱、 恙蟲病 地方性斑疹傷寒、 萊姆病、兔熱病 (5項 ) 14
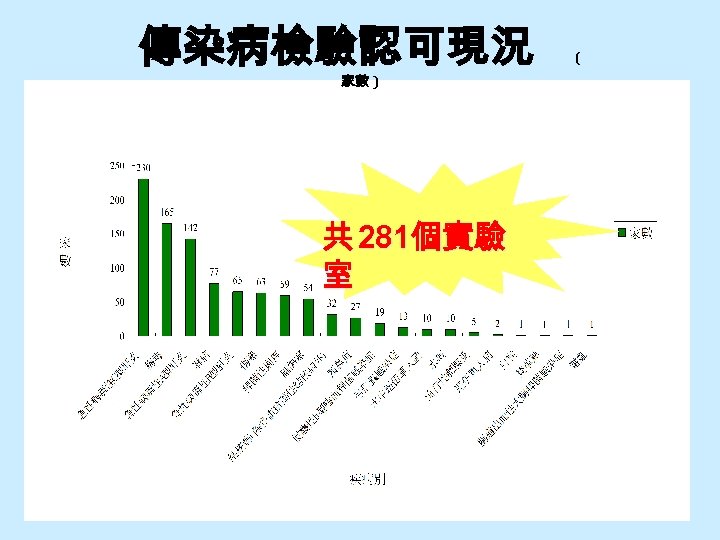
傳染病檢驗認可現況 ( 家數 ) 共 281個實驗 室 15

未來修訂方向 一、除特殊病原外,以 全面開放 為原則 二、審查作業 納入生物安全考量 三、分項 認可:單一確認檢驗方法 四、分段 認可:篩檢、確認 五、新增辦理 變更、廢止 之相關規定 16

共 55項法定傳染病 類 別 第二類至第四類認可傳染 病 傳染病名稱 第二類 白喉、 傷寒、 登革熱、 流行性腦脊髓膜炎、 副傷寒、 小兒麻痺症、 (共 19項 桿菌性痢疾、 阿米巴性痢疾、 瘧疾、 麻疹、 急性病毒性A 型肝炎、 ) 腸道出血性大腸桿菌感染症、 他病毒症候群、 亂、 國麻 漢 霍 德 疹、多重抗藥性結核病 、屈公病、西尼羅熱、流行性斑疹傷寒 第三類 百 日 咳 、 傷 風 、 本 腦 炎 、 核 病 ( 多 重 抗 藥 性 結 核 病 外 ) 破 日 結 除 、 (共 19項 先 天 性 德 國 麻 疹 症 候 群 、 性 病 毒 性 B型 肝 炎 、 性 病 毒 性 C型 急 急 ) 肝 炎 、 性 病 毒 性 D型 肝 炎 、 性 病 毒 性 E型 肝 炎 、 行 性 腮 腺 急 急 流 炎、 退伍軍人病、 水中退伍軍人菌、 侵襲性b 型嗜血桿菌感染症、 梅毒、 病、 生兒破傷風、 病毒感染併發重症、 類免疫缺 淋 新 腸 人 乏病毒感染 、 漢生病 鉤 類 肉 侵 第四類 疱 疹 B病 毒 感 染 症 、 端 螺 旋 體 病 、 鼻 疽 、 毒 桿 菌 中 毒 、 (共 17項 襲 性 肺 炎 鏈 球 菌 感 染 症 、 Q熱 、 方 性 斑 疹 傷 寒 、 姆 病 、 熱 地 萊 兔 ) 病、 氏桿菌症、 蟲病、 痘、 抓病、 形蟲感染症、 感 布 恙 水 貓 弓 流 併發重症、 NDM-1腸道菌感染症 、 庫賈氏病 藍字為新增開放項目 ; 紅字維持不開放項 17
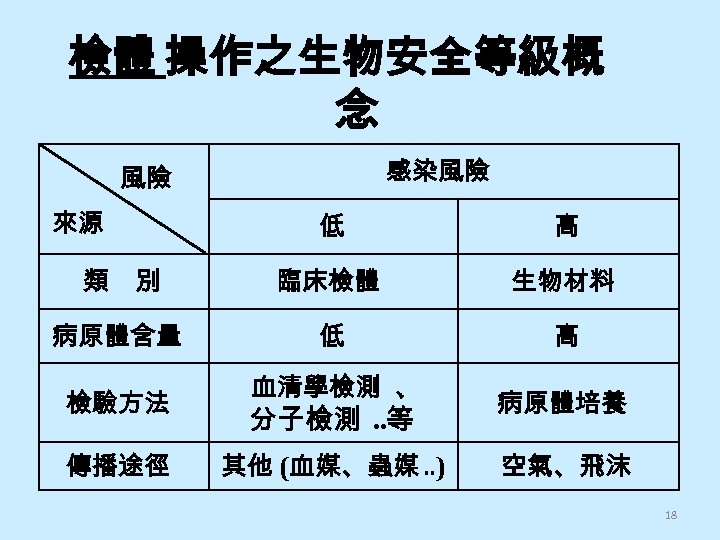
檢體 操作之生物安全等級概 念 來源 風險 感染風險 低 高 類 別 臨床檢體 生物材料 病原體含量 低 高 檢驗方法 傳播途徑 血清學檢測 、 分子檢測. . 等 其他 (血媒、蟲媒. . ) 病原體培養 空氣、飛沫 18

傳染病檢驗及檢驗機構管理辦法 認可檢驗機構 申請應檢具文件 : 現行版 一、申請書。 二、資格證明文件。 三、標準檢驗方法。 修訂草案 一、申請書。 二、資格證明文件。 三、標準檢驗方法。 四、備有與操作檢體 相 當等級之生物安 全 新增 管理手冊或規定。 19
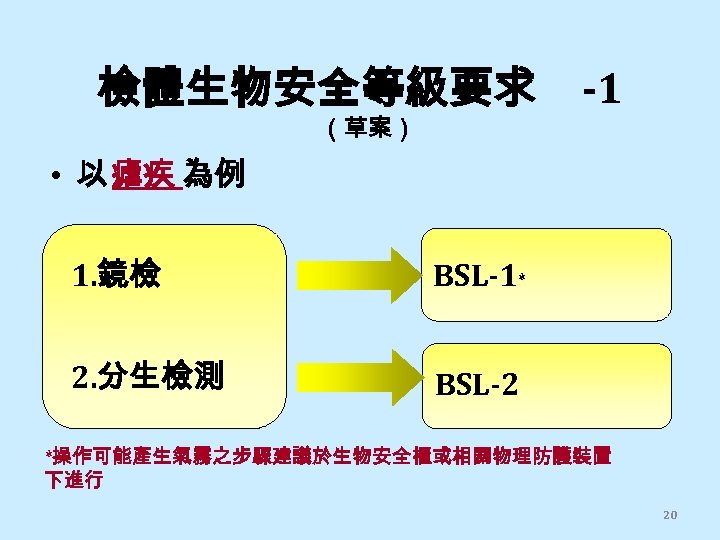
檢體生物安全等級要求 (草案) -1 • 以 瘧疾 為例 1. 鏡檢 BSL-1* 2. 分生檢測 BSL-2 *操作可能產生氣霧之步驟建議於生物安全櫃或相關物理防護裝置 下進行 20
檢體生物安全等級要求 (草案) -2 • 以 梅毒 為例 RPR 或 VDRL BSL-1* TPHA 或 TPPA BSL-1* * 操作可能產生氣霧之步驟建議於生物安全櫃或相關物理防護裝置 下進行 21
檢體生物安全等級要求 -3 (草案) • 以 急性病毒性肝炎 及 人類免疫缺乏病毒 感染 為例 抗體檢測 BSL-1* * 操作可能產生氣霧之步驟建議於生物安全櫃或相關物理防護裝置 下進行 22
檢體生物安全等級要求 -4 (草案) • 以 傷寒 、 副傷寒 及 桿菌性痢疾 為例 1. 病原體分離鑑 定 2. 血清型別鑑定 BSL-2 23
檢體生物安全等級要求 • 以 結核病 為 例 1. 抗酸菌抹片 2. 病原體培養鑑 定 3. 藥物感受性試 驗 4. 病原體分生檢 -5 (草案) BSL-2(負壓) BSL-2 24
檢體生物安全等級要求 -7 (草案) • 以 布氏桿菌病 為例 病原體分離鑑定 BSL-3 病原體分生檢測 BSL-2 25
分 項 認可 -1 • 以 瘧疾 為例 現行版 1. 鏡檢 測 2. 分生檢 修訂版 鏡檢 分生檢測 26
分 項 認可 -2 • 以 百日咳 為 例 現行版 修訂版 1. 病原體分離 病原體鑑定 2. 抗體檢測 (Ig. A或 Ig. M) 分生檢測 27
分 段 認可 -1 • 以 梅毒 為例 現行版 修訂版 1. RPR 或 VDRL 2. TPHA 或 TPPA 28
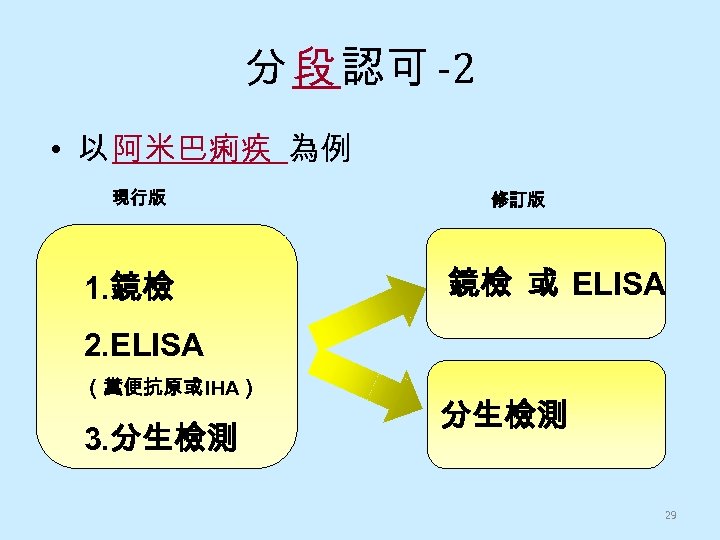
分 段 認可 -2 • 以 阿米巴痢疾 為例 現行版 1. 鏡檢 修訂版 鏡檢 或 ELISA 2. ELISA (糞便抗原或IHA) 3. 分生檢測 29
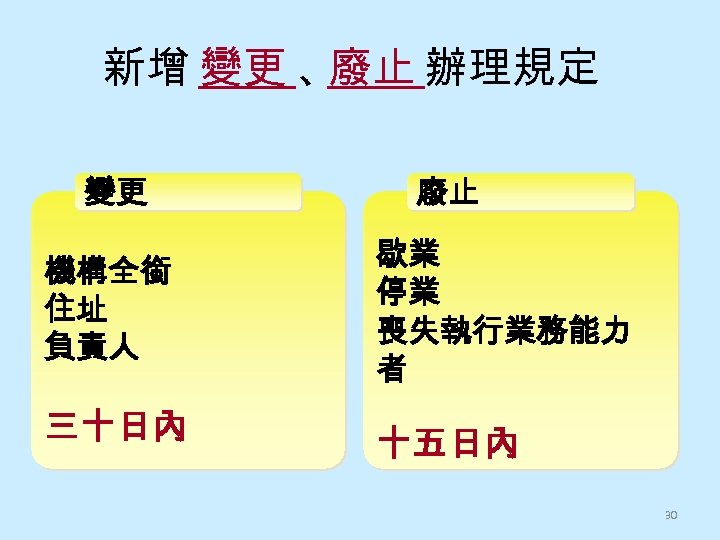
新增 變更 、 廢止 辦理規定 變更 機構全銜 住址 負責人 三十日內 廢止 歇業 停業 喪失執行業務能力 者 十五日內 30

認可傳染病檢驗機構 檢驗結果線上通報 31

法源依據及管理辦法 • 傳染病防治法第 46條第一項第二、三款 – 檢驗與報告 檢驗結果應報告地方及中央主管機 關。 – 確定 中央主管機關或其指定、委託、認可檢驗單 位。 • 傳染病防治法第 40條第一項 – 報告 醫事人員執行業務,發現傳染病或疑似傳 染病病人或其屍體,應即報告醫師或地方主管機 關。 • 傳染病防治法施行細則第 4條 – 檢驗 化驗、鑑定或其他必要之檢查等行為。 • 傳染病檢驗及檢驗機構管理辦法第 8條 – 應依 防疫檢體採檢手冊 所訂之 時限 完成檢驗及報 32

傳染病通報及檢驗作業流程 • 通報 採檢送驗 檢驗 檢驗報告 登錄作業 • 採檢送驗 檢驗 陽性結果通報 (急性病毒性 A 、B 、C肝炎、梅毒、淋病、 結核病 ) 33

陽性結果通報 • 系統通報作業之附加資訊功能 急性病毒性 A、 C型肝炎、梅毒、淋病 ─可利用 B、 現行系統 ─通報作業 ─附加資訊 功能輸入檢驗結 果 (陽性通報 →即登錄檢驗結果 ) • 結核病代檢網 結核病檢驗結果上傳 結核病代檢網 • 無法透過醫療院所通報時,檢驗結果 傳真當地衛生局所 34

傳染病檢驗結果網路通報作業說 明 • 固定式 IP連線 認可傳染病檢驗機構系統網路服務申請表 • 帳號控管 疾病管制局全球資訊網專業版 →通報與檢驗類 →傳染病 通報系統 → 1. 法定傳染病監視通報系統 →衛生局所版 /帳 號申請 /認可傳染病檢驗機構帳號申請 /線上申請並列印 帳號申請表 /申請者親筆簽名 /實驗室主管核定 傳真 (02)26519632至疾病管制局研究檢驗中心第二科 35

現況分析與未來規劃 • 以往作業方式 -系統一個帳號僅有一種 權限 通報 →通報 / 檢驗結果登錄 →檢驗結果登錄 • 目前及未來規劃 →法定傳染病 檢驗結果須登錄系統。 →系統檢核機制:僅有認可傳染病檢驗機構 檢驗結果始予認可。 → 6月 18日起新版系統上線後,有通報及檢驗結 果登錄兩種權限 (已完成) ,並結核病代檢網認 可檢驗機構上傳檢驗結果 (目前測試中) 。 36

101年認可傳染病 檢驗機構品質提升計畫 之訪查方式及查檢表填寫說明 中華民國醫事檢驗師公會全國聯合會 計畫研究團隊 北區 : 廖皓宏主任 /行政院衛生署樂生療養院檢驗科 中區 : 吳明訓主任 /敏盛綜合醫院檢驗科 南區 : 何文育主任 /中國醫藥大學北港附設醫院檢驗科 撰稿 : 廖皓宏主任 37

訪查目的 • 持續推動認可檢驗制度,透過與業界互動 收集意見,作為認可政策後續規劃參考。 • 了解認可實驗室其未取得認證資格者其傳 染病檢驗現況及品質,以針對個別需要提 供實驗室技術性建議。 • 系統性檢驗作業及優質檢驗品質之文化導 入各傳染病認可檢驗機構,導入實驗室自 主管理模式,全面提升認可傳染病檢驗機 構檢驗品質。 38

101年度實驗室訪查問題 Q&A 1. 認可傳染病檢驗機構接受實地訪查之法源依據為 何? Ø 依據傳染病檢驗及檢驗機構管理辦法第六條規定: 「中央主管機關對傳染病檢驗機構得予查核,傳 染病檢驗機構應配合,並不得拒絕、規避或妨礙。 前項查核,得以 書面審查 、 能力試驗 或 實地訪查 為之。第一項查核,發現有缺失時,傳染病檢驗機 構應於中央主管機關指定之期限內完成改善;屆 期未改善者,中央主管機關得廢止其指定、認可 或終止委託。」 39

101年度實驗室訪查問題 Q&A 2. 認可傳染病檢驗機構可否拒絕實地訪查 ? Ø 實地訪查活動為法令規定,認可傳染病 檢驗機構有義務接受訪查,若拒絕訪查 可能會被主管機關取消認可資格。 3. 101年度實地訪查的查核對象為何? Ø 於 100~ 101年提出認可申請傳染病檢驗 項目屬不具認證資格之認可傳染病檢驗 機構。+ 100年複查機構 40
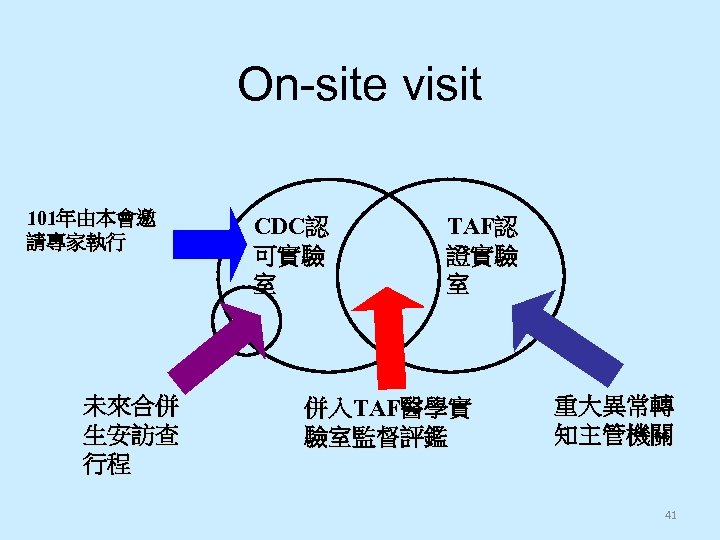
On-site visit 101年由本會邀 請專家執行 未來合併 生安訪查 行程 CDC認 可實驗 室 TAF認 證實驗 室 併入TAF醫學實 驗室監督評鑑 重大異常轉 知主管機關 41
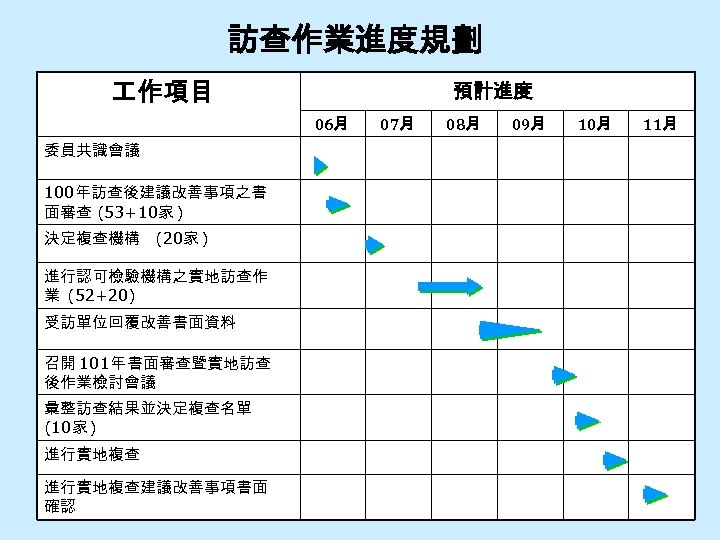
訪查作業進度規劃 作項目 預計進度 06月 07月 08月 09月 10月 11月 委員共識會議 100年訪查後建議改善事項之書 面審查 (53+10家 ) 決定複查機構 (20家 ) 進行認可檢驗機構之實地訪查作 業 (52+20) 受訪單位回覆改善書面資料 召開 101年 書面審查暨實地訪查 後作業檢討會議 彙整訪查結果並決定複查名單 (10家 ) 進行實地複查建議改善事項書面 確認 42
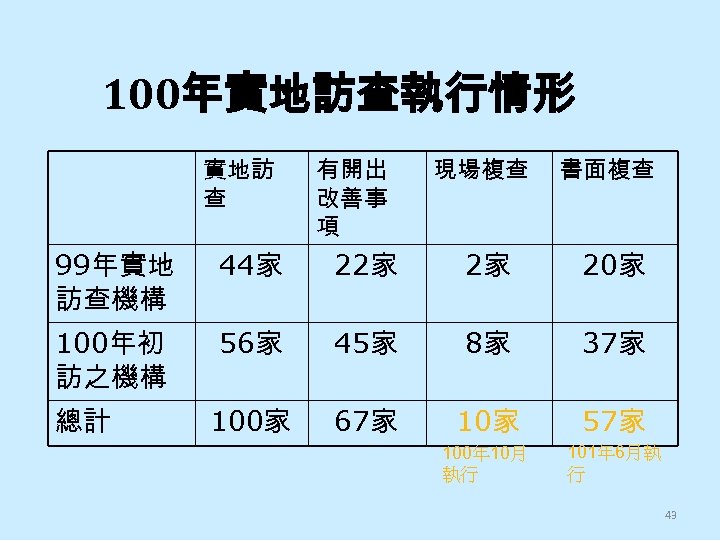
100年實地訪查執行情形 實地訪 查 有開出 改善事 項 現場複查 書面複查 99年實地 訪查機構 44家 22家 2家 20家 100年初 訪之機構 56家 45家 8家 37家 100家 67家 10家 57家 100年 10月 執行 101年 6月執 行 總計 43

101年度實驗室訪查問題 Q&A 4. 檢驗機構於 99或 100年已接受實地訪查,為何 101年 還被安排實地訪查?為何每年都要接受訪查? Ø 法令並未規定實地訪查的次數。主管機關會參考前 一年度實地訪查檢驗機構品保的執行情形、現階段 認可制度推動成果及輔導計畫執行內容,決定年度 訪查安排方式。 Ø 100年辦理之實地訪查發現,仍有相當高比例之中、 小型規模實驗室管理現況僅 ”部分符合 ”「傳染病檢驗 機構品保查核表」之要求;因此,針對 100年已接受 實地訪查之檢驗機構,決定挑選約 20家機構進行複 查 (重大缺失尚未完成改善者進行 ) 。 44
45

100年實地訪查 改善事項 執行情 形 • 於 100年 10月執行 10家現場複查,仍有 4家未 完全改善,有 6家持續開出改善事項 • 57家書面複查,其中有 3家已申請終止, 1家未 回饋改善措施,實際書面審查共 53家。 • 於 101年 6月執行 53家書面審查,仍有 12家 不 符合 改善確認, 8家 建議補充 資料 • 53家書面審查 +10家現場複查中,於 101年 7月 「認可機構訪查小組」 作會議決定 20家執行 現場複查 46
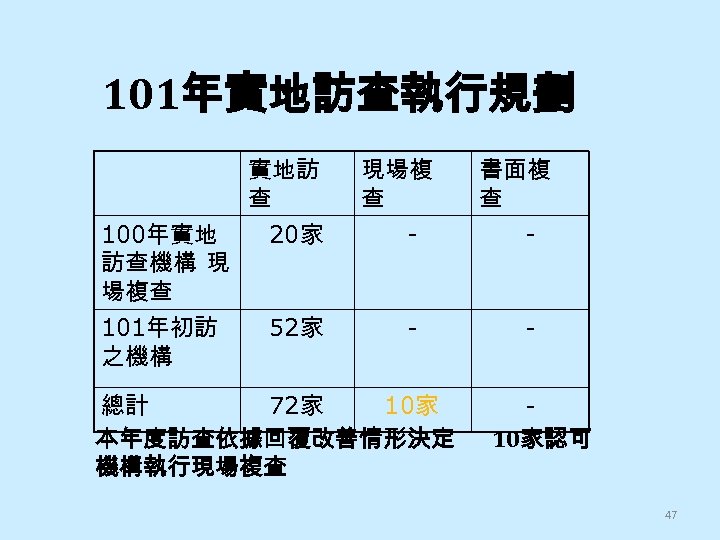
101年實地訪查執行規劃 實地訪 查 現場複 查 書面複 查 100年實地 訪查機構 現 場複查 20家 - - 101年初訪 之機構 52家 - - 總計 72家 10家 本年度訪查依據回覆改善情形決定 機構執行現場複查 10家認可 47

101年實地訪查執行方式 • • 實地訪查期間: 7/23 -8/24 實地訪查家數: 72家 訪查委員一名 委員訪查原則上安排一天兩家,實地訪查時間為 早上 9點到 12點,下午2點到 5點。 訪查委員安排認可傳染病檢驗機構時以同區 (北中 南 )跨縣市為優先考量。 已請各位委員確認與受訪之檢驗機構間無任何利 害衝突關係 由計畫研究助理 鄭美湖 醫檢師協調安排各受訪機 構及委員訪查日期時間 48
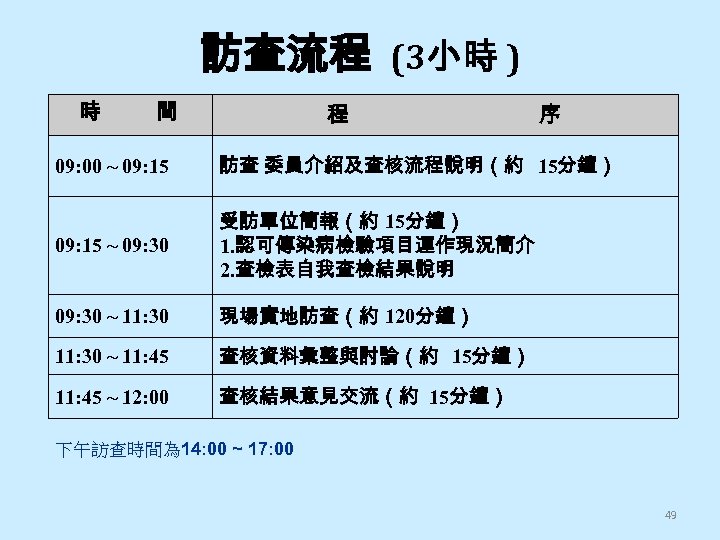
訪查流程 (3小時 ) 時 間 程 序 09: 00 ~ 09: 15 訪查 委員介紹及查核流程說明(約 15分鐘) 09: 15 ~ 09: 30 受訪單位簡報(約 15分鐘) 1. 認可傳染病檢驗項目運作現況簡介 2. 查檢表自我查檢結果說明 09: 30 ~ 11: 30 現場實地訪查(約 120分鐘) 11: 30 ~ 11: 45 查核資料彙整與討論(約 15分鐘) 11: 45 ~ 12: 00 查核結果意見交流(約 15分鐘) 下午訪查時間為 14: 00 ~ 17: 00 49

訪查時進行事項 訪查 委員 介紹及查核流程說明 受訪單位簡報 -型式不拘 100年實地訪查現場複查機構,查核改善狀況 訪查委員填寫「傳染病檢驗機構品保查檢表」 ( 書面或電子檔 ) • 訪查委員發現缺失於「 傳染病檢驗機構品 保查檢表 」對應項目勾選「 」 否 (有星號*之查 檢項目不符合列為 改善事項 ,無星號*之查 檢項目不符合或缺失列為 建議事項 ) • • 50

改善事項及建議事項 • • 「改善事項」性質為受訪單位於一個月內 (從 受訪日期起算 )完成改善並回覆 「建議事項」性質為提供受訪單位參考,不必 提出書面回覆資料 本次訪查是依 2版查檢表草案的精神,主要 查核必要的星號部份,查檢表有星號部份勾 「否」開立「改善事項」,無星號部份勾「否」的 開立為「建議事項」。 查檢表若勾「是」但有部分缺失,將依缺失嚴 重情形採行口頭建議或開立「建議事項」。 51

訪查時需進行事項 • 改善及建議事項填寫於「 101年認可傳染 病檢驗機構實地訪查紀錄」 (如無改善及 建議事項填「無」 ) • 查核資料彙整與討論 • 查核結果意見交流 • 「傳染病檢驗機構品保查檢表」及「101年 認可傳染病檢驗機構實地訪查紀錄」經 委員及 受訪機構簽名後需留存一份於受 訪機構 ,正本由委員帶回 52

101年度實驗室訪查問題 Q&A 5. 101年度實地訪查的查核範圍 (檢驗項目 )? Ø 查核範圍為是檢驗機構是 取得認可之法定傳 染病檢驗項目 。 6. 委員執行實地訪查時,發現有缺失時是如何處 理? Ø 於實地訪查總結會議時,由訪查委員說明訪查 改善事項,經 雙方溝通同意後 由委員填寫於「 認可傳染病檢驗機構實地訪查紀錄」。 53

101年度實驗室訪查問題 Q&A 7. 經雙方溝通後,若檢驗機構不同意訪查 委員開立之改善或建議事項如何處理? Ø 於實地訪查總結會議時提出,檢驗機構 向訪查委員說明不同意的事項及理由, 並記錄於「認可傳染病檢驗機構實地訪 查紀錄」,後續將由主管機關及訪查 作 小組會議裁定。檢驗機構不同意改善事 項須於實地訪查總結會議時提出, 實地 訪查結束後不接受「不同意改善事項」之 申訴 。 54

受訪單位回覆改善書面資料 • 101年度實地訪查完成後,若受訪單位 有改善事項或建議事項, 計畫研究助理 會 寄給各受訪檢驗機構「認可傳染病檢驗 機構實地訪查改善事項改善紀錄」填寫 改善狀況。 • 受訪單位若僅被開立建議事項,不需回 覆改善狀況。 • 改善事項要求於一個月內 (從受訪日期 起算 )完成改善回覆。 55

101年實地訪查後改善狀況書面審 查 • • • 審查時間:預定於 9月底 -10月初 進行實地訪查改善事項書面確認 建議複查機構名單 (10家 ) 傳染病認可檢驗機構常見問題檢討 建議訪查結果良好機構名單,邀請機構參與 成果發表 56

符合、不符合、建議補充的書審標準 • 符合:能針對缺失問題擬定相對改善措施執行, 改善狀況自述說明填寫清楚並適當檢附相關 改善資料。如有必要但未檢附相關改善資料, 不得列為「符合」。 • 不符合:改善狀況自述說明未填寫且未檢附相 關改善資料。改善事項內容與缺失問題無關。 • 建議補充:未檢附相關改善資料 …。 57
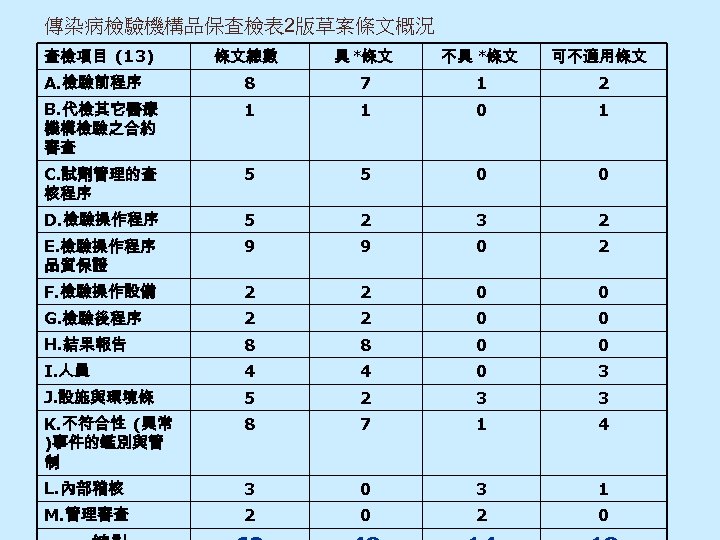
傳染病檢驗機構品保查檢表 2版草案條文概況 查檢項目 (13) 條文總數 具 *條文 不具 *條文 可不適用條文 A. 檢驗前程序 8 7 1 2 B. 代檢其它醫療 機構檢驗之合約 審查 1 1 0 1 C. 試劑管理的查 核程序 5 5 0 0 D. 檢驗操作程序 5 2 3 2 E. 檢驗操作程序 品質保證 9 9 0 2 F. 檢驗操作設備 2 2 0 0 G. 檢驗後程序 2 2 0 0 H. 結果報告 8 8 0 0 I. 人員 4 4 0 3 J. 設施與環境條 5 2 3 3 K. 不符合性 (異常 )事件的鑑別與管 制 8 7 1 4 L. 內部稽核 3 0 3 1 M. 管理審查 2 0
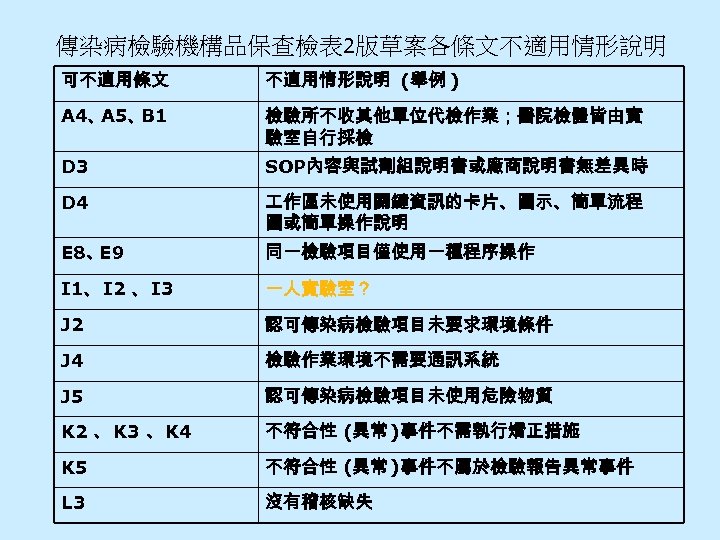
傳染病檢驗機構品保查檢表 2版草案各條文不適用情形說明 可不適用條文 不適用情形說明 (舉例 ) A 4、 A 5、 B 1 檢驗所不收其他單位代檢作業;醫院檢體皆由實 驗室自行採檢 D 3 SOP內容與試劑組說明書或廠商說明書無差異時 D 4 作區未使用關鍵資訊的卡片、圖示、簡單流程 圖或簡單操作說明 E 8、 E 9 同一檢驗項目僅使用一種程序操作 I 1、 I 2 、 I 3 一人實驗室? J 2 認可傳染病檢驗項目未要求環境條件 J 4 檢驗作業環境不需要通訊系統 J 5 認可傳染病檢驗項目未使用危險物質 K 2 、 K 3 、 K 4 不符合性 (異常 )事件不需執行矯正措施 K 5 不符合性 (異常 )事件不屬於檢驗報告異常事件 L 3 沒有稽核缺失

傳染病檢驗機構品保作業要求 2. 0草案 • 傳染病項目檢驗應制定標準操作程序書 • 訂定品保 /品管相關作業程序 Ø 管理要求 -至少應包含 文件管制 、試劑管理、不符合事項 之鑑別與管制、矯正 /預防 /持續改善措施 等。 Ø 技術要求 -至少應包含 人員訓練、檢體處理程序、實驗室 設備管理、檢驗程序品質管制、傳染病陽性結果通報程 序 等。 • 不符合事項處理 • 檢驗報告錯誤事件之處理及通報作業 60
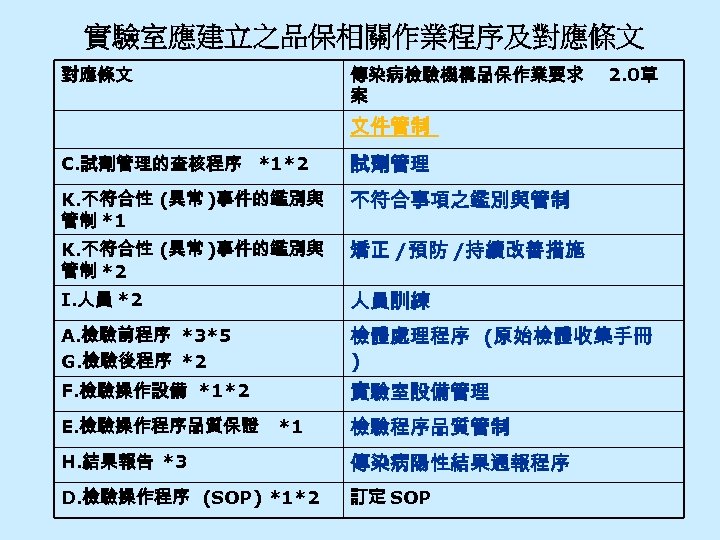
實驗室應建立之品保相關作業程序及對應條文 傳染病檢驗機構品保作業要求 案 2. 0草 文件管制 C. 試劑管理的查核程序 *1*2 試劑管理 K. 不符合性 (異常 )事件的鑑別與 管制 *1 不符合事項之鑑別與管制 K. 不符合性 (異常 )事件的鑑別與 管制 *2 矯正 /預防 /持續改善措施 I. 人員 *2 人員訓練 A. 檢驗前程序 *3*5 G. 檢驗後程序 *2 檢體處理程序 (原始檢體收集手冊 ) F. 檢驗操作設備 *1*2 實驗室設備管理 E. 檢驗操作程序品質保證 *1 檢驗程序品質管制 H. 結果報告 *3 傳染病陽性結果通報程序 D. 檢驗操作程序 (SOP) *1*2 訂定 SOP
品保相關文件範例(全聯會官網) 須會員登入後才可下載品 保相關文件範例 62
點選網頁左下角「傳染 病檢驗機構品質提升計 畫專區」 63
點選文件下載區 64

A. 檢驗前程序 • *1. 請確認現有使用之書面或電子檢驗申請單是否 包括以下內容 Ø a). 受檢者之 唯一識別 及資訊,如姓名、性別、出生 日期或年齡等; Ø b). 申請檢驗者之唯一的識別,如醫師或其它可要 求檢驗的單位名稱或受檢者自行要求; Ø c). 檢體的種類; Ø d). 檢驗項目; Ø e). 採檢日期與 時間 ; Ø f). 實驗室接受檢體的日期與 時間 65

A. 檢驗前程序 • *2. 確認接受之原始檢體是否可追溯至 可識別之個人,且分裝的檢體能識別追 溯至原始檢體。 • *3. 是否已建立「原始檢體收集手冊」 • 4. 承上題,請確認是否有提供給實驗室 外人員使用 (可不適用 ) • *5. 請確認是否有監控檢體運送至實驗室 的作業程序文件 (可不適用 ) 66

防疫檢體採檢手冊 5. 0 Ø 防疫檢體採檢手冊 1. 3. 採檢容器通則:裝檢體之第 一層容器為無菌、不滲漏容器,容器外壁上註明個 案資料,例如姓名、採檢日期、檢體種類及條碼( bar -code)。 Ø 防疫檢體採檢手冊 2. 8. 7 : 低溫運送泛指 2 -8 ℃ ,常 溫運送泛指 22 -35 ℃ 。 。 Ø 防疫檢體採檢手冊 1. 5 檢體運送時效及包裝通則: 一般臨床檢體運送規定自採檢次日起至實驗室收件 日不得超過 3 日,菌株不得超過 10 日,結核菌臨床 檢體( 24小時內)及菌株均應儘速送達實驗室。 67
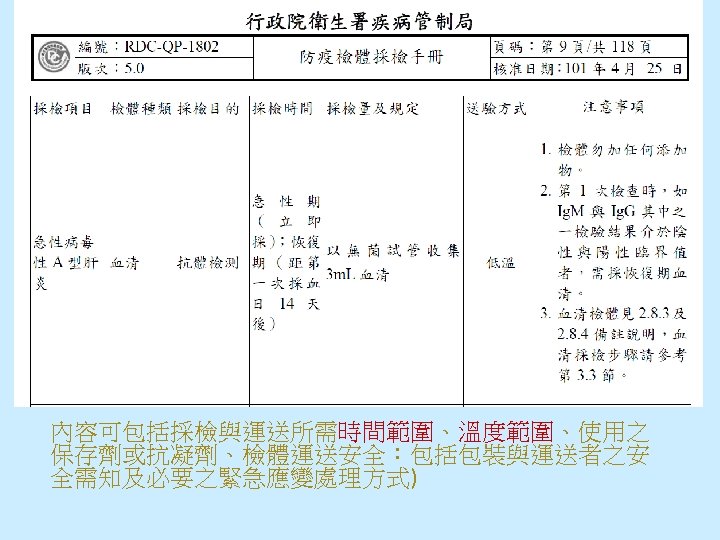
內容可包括採檢與運送所需時間範圍、溫度範圍、使用之 保存劑或抗凝劑、檢體運送安全:包括包裝與運送者之安 全需知及必要之緊急應變處理方式)

防疫檢體採檢手冊 5. 0 Ø 防疫檢體採檢手冊 1. 3. 採檢容器通則:裝檢體 之第一層容器為無菌、不滲漏容器,容器外壁 上註明個案資料,例如姓名、採檢日期、檢體 種類及條碼(bar-code)。 Ø 防疫檢體採檢手冊 2. 8. 7 : 低溫運送泛指 2 -8 ℃ ,常溫運送泛指 22 -35 ℃ 。 69

A. 檢驗前程序 • *6. 請確認是否已明訂原始檢體接收或拒 收之準則,並維持對應執行紀錄 • *7. 承上題,請確認原始檢體的接收紀錄 內容,是否包括檢體接收的日期與時間 及接收人員之識別: • *8. 承上題,請確認是否訂定檢體可複驗 或加驗的條件。 70
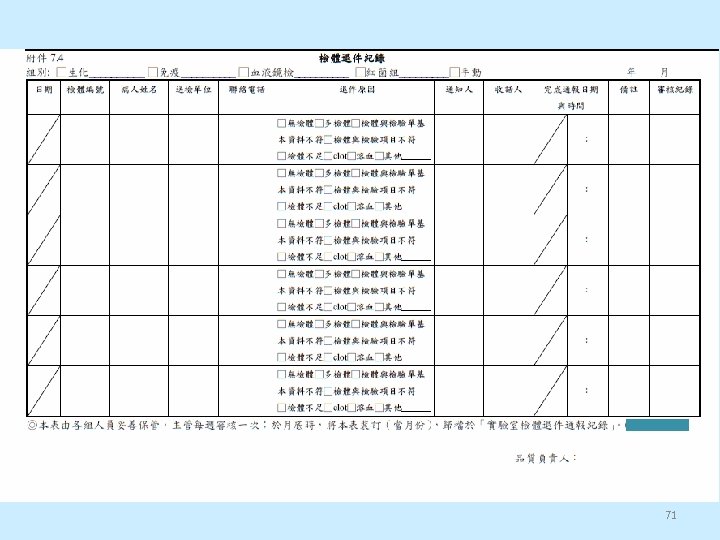
71

B. 代檢其它醫療機構檢驗之合 約審查 • *1. 請確認是否有代檢其它醫療機構檢驗 之合約審查程序並留有審查紀錄。 (可不適 用) 72

C. 試劑管理的查核程序 • *1. 請確認是否已建立試劑管理的作業程 序。 • *2. 承上題,請確認是否訂定各檢驗試劑 的驗收、允收 /退貨和貯存之程序和標準。 • *3. 承上題,請確認是否有對應執行紀錄。 • *4. 請確認庫存紀錄內容是否包括以下內 容 (進貨日期、批號、使用日期、原始效 期 ),且紀錄定期接受內部審查。 73

C. 試劑管理的查核程序 • *5. 承上題,啟用之試劑應有適當的標示, 包括開封日期、開封後末效。 74

D. 檢驗操作程序 (SOP) • *1. 請確認是否依據現在使用之試劑組說 明書或廠商說明書定訂 SOP,如果自行研 發的檢驗經適當驗證符合預期用途。 • *2. SOP內容至少包含 (CDC提供 ) • 3. 承上題,如對使用之 SOP與試劑組說明 書或廠商說明書有差異時,如 Cut off values之變更而影響陽性或陰性結果之 判讀,是否有執行對應差異評估與記錄, 以證明符合預期用途。 (可不適用 ) 75

D. 檢驗操作程序 (SOP) • 4. 請確認實驗室 作區,若有使用某些 關鍵資訊的卡片、圖示、簡單流程圖或 簡單操作說明提醒 作人員或操作,該 表單或紀錄有列入對應操作 SOP內以為 連接。 (可不適用 ) • 5. 請確認更改檢驗方法、程序或系統時, 有建立對應處理措施包括對實驗室服務 使用者解釋影響層面評估、檢驗結果間 評估、採檢手冊內容評估等。 76

E. 檢驗操作程序品質保證 • *1. 請確認是否針對現有檢驗項目皆設計有內部品 質管制措施 (如使用陽性、陰性、對照組或標準菌 株執行 )。 • *2. 請確認是否有檢驗試劑管理,不同批號不能混 用 (包括倒在一起 )使用。 • *3. 承上題,請確認是否現有檢驗項目設計一套品 質保證措施 (得包括定量檢驗利用品管圖監控、定 性報告確認機制、人 查核或確認機制、品管指 標監控、設備溫度監控等。 77

E. 檢驗操作程序品質保證 • *4. 請確認是否建立現有使用之檢驗系統之校正與 量測追溯查證方案。 • *5. 承上題,請確認是否維持校正與量測追溯查證 方案執行紀錄如外校報告或比對紀錄、追溯一覽 表。 • *6. 請確認是否定期參加外部品管計劃 (經過主管 機關委託或通過認證之能力試驗提供者或國際能 力試驗機構舉辦之能力試驗 ),若申請項目無對應 能力試驗提供者則採實驗室間比對。 78

E. 檢驗操作程序品質保證 • *7. 承上題,請確認是否有相關對應程序 提及如何參與外部能力試驗活動或實驗 室間比對如參與時機,檢體處理方式、後 續處理方式 (能力試驗結果審查機制 )與 結果落於接受範圍外處理措施等。 • *8. 請確認當對於使用不同程序 (同一檢 驗項目不同 SOP)、設備或於不同地點或 包括上述三者所執行的檢驗時,是否有 管理機制,以查證臨床結果範圍內之可 比較性。 (可不適用 ) 79

E. 檢驗操作程序品質保證 • *9. 承上題,請確認如果比對結果有差異, 是否利用矯正系統,採取適當行動並保 有紀錄。(可不適用 ) 80

F. 檢驗操作設備 • *1. 請確認針對影響報告品質之重要設備 是否有一套針對設備運作使用之管理文 件 (可能包括整體設備管理要求與對應 各設備之操作 SOP),該文件包括說明現 有使用那些設備、針對設備如何校正 /查 核 /維修保養等機制,執行時機、誰去執 行、執行後如何證明設備處之功能正常、 判定準則、對於不符準則之後續管理模 式。 81

F. 檢驗操作設備 • *2. 請確認設備於使用過程發現有缺點 ( 品管異常、校正異常 )、或是正在維修保 養,是否有對應管理機制與後續處理程 序。 82

G. 檢驗後程序 • *1. 請確認是否授權適當人員審查檢驗結 果,以評估受檢者與釋出的結果是否符 合臨床訊息。 • *2. 請確認是否有作業程序明訂對原始檢 體與其它實驗室檢體儲存方式、期限及 廢棄物管理。 83

防疫檢體採檢手冊 5. 0版 1. 4 檢體保存通則 • 1. 4. 1 檢體採檢後,全血血瓶放置於常溫,抗凝固全血、 血清、組織等應立即放入低溫 2 -8 ℃保存。檢驗後,應 保存至少三日,但經確認內含病原體或其抗體之血清 或血漿檢體,應保存至少一個月。分離培養之結核菌 菌株保存 2 年,其他病原培養物視個別需要訂定 。 • 1. 4. 2 經培養確認內含病原體檢體,如需繼續保存逾一 個月者,應置專責管理人員、保存之冷藏設備,應上鎖 或設有門禁管制,並有足供警示之文字、並製作保存 清單。另菌株或病毒株等病原培養物之保存、使用或 異動者,應經單位生物安全委員會(或專責人員)同意, 始可為之。若前項病原體屬第三級感染性生物材料( Risk Group 3)以上者,應事先向疾病管制局辦理異動 核備作業。 84

H. 結果報告 • *1. 請確認是否建立適當結果報告之格式 內容 • *2. 承上題,請確認當接收原始檢體品質 無法適用於檢驗或可能影響結果時,實 驗室報告中可以指出說明。 • *3. 請確認,當結果如為法定傳染病通報 時,於您實驗室是否有通報處理程序 (包 括誰被授權通報、如何通報、接受對象 等 )。 85

H. 結果報告 • *4. 請確認於針對傳染病通報是否維持執 行紀錄 (該紀錄包括日期、時間、負責的 實驗室 作成員、被通知的人及檢驗結 果 )等,並於相關稽核期間進行審查。 • *5. 請確認是否明訂原始檢驗結果之保存 方式與時間包括原始檢驗結果應可追溯 至實際操作醫檢師。 86

H. 結果報告 • *6. 請確認是否依照主管機關要求,明訂每項傳染 病檢驗之報告完成所需時間與監控審查報告完成 所需時間之管理。 • *7. 承上題,請確認當檢驗報告延遲時,是否有相 關對應程序。 • *8. 請確認是否訂有文件化之政策及程序以處理報 告 (包括電子報告 )之修訂。對於紙本原始報告經 修訂後,可清楚顯示修訂時間、日期、修訂者的姓 名以及修正之處或對於電子報告修訂後,原始電 子修訂紀錄可被保留且顯示修正處。 87
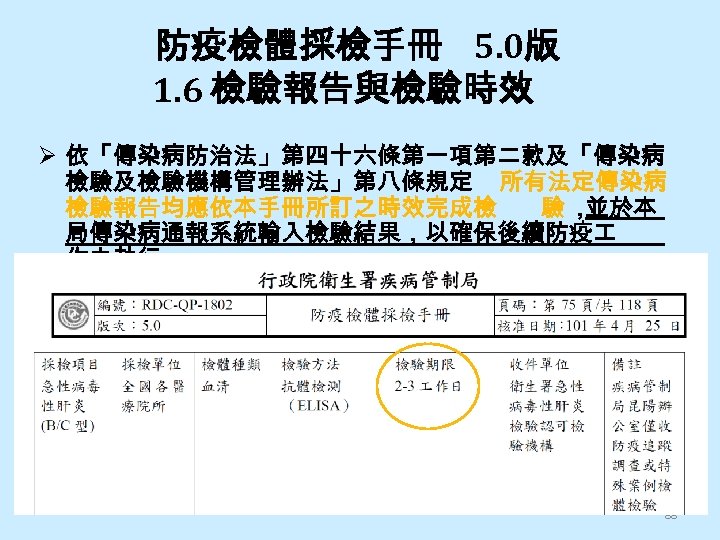
防疫檢體採檢手冊 5. 0版 1. 6 檢驗報告與檢驗時效 Ø 依「傳染病防治法」第四十六條第一項第二款及「傳染病 檢驗及檢驗機構管理辦法」第八條規定 所有法定傳染病 檢驗報告均應依本手冊所訂之時效完成檢 驗, 並於本 局傳染病通報系統輸入檢驗結果,以確保後續防疫 作之執行。 88

I. 人員 • *1. 請確認是否有明訂對應實驗室管理權 責人員且各職稱 作人員已建立代理人 制度。(可不適用 ) • *2. 請確認是否建立書面化的人員管理程 序,內容包括新進與在職人員訓練要求 ( 品質管理、實驗室安全、資訊系統操作、 檢驗技術操作、 作輪換職務、檢驗數據 保密、實驗室使用文件閱讀等 )、訓練考 核流程與要求及考核管理授權。 (可不適用 ) 89

I. 人員 • *3承上題,請確認實驗室人員是否有定 期接受內部訓練 (訓練內容需與 作職務 所需符合,並接受能力評估 (能力是指檢 驗技術與職務要求之能力 )。 (可不適用 ) • *4. 請確認是否有規定對於檢驗機密資料 之保護措施於對應文件且有告知對應人 員瞭解。 90

J. 設施與環境條件 • 1. 請確認於您現有實驗室空間使用,是 否能滿足目前之 作品質、 作人員安 全以及受檢者照護服務或曾發生相互污 染情況影響檢驗結果。 • 2. 承上題,請確認申請認可傳染病檢驗 項目之環境條件管理是否已明訂於對應 程序並有監控 ? (可不適用 ) • *3. 請確認是否有管制措施以防止檢體被 未經授權者取得如進出與使用管制措施。 91

J. 設施與環境條件 • 4. 請確認通訊系統功能是否有效且定期 檢查,以避免發生緊急事件無法通知現 場 作人員。 (可不適用 ) • *5. 請確認危險物質之儲存與丟棄是否已 依據相關特定的法規處理。 (可不適用 ) 92

K. 不符合性 (異常 )事件的鑑別 與管制 • *1. 請確認是否有針對檢驗過程發生問題 (可能包括與檢驗 SOP不一致、與實驗室 各程序不一致時等),建立內部不符合性 ( 異常 )事件之管理程序 (程序內容應思考 包括處理流程、如何評估、如有必要暫停 檢驗 作是否應通知那些重要人士,如 醫師、是否需判定為重新檢驗與召回過 往報告、針對問題改善後之確認及後續 監控措施 )。 93

K. 不符合性 (異常 )事件的鑑別 與管制 • *2. 承上題,請確認如有不符合性 (異常 ) 事件之發生,該事件內容是否涉及導入 矯正措施活動。 (矯正措施程序是為實驗 室針對所發生問題以調查步驟尋找問題 的根本原因並予解決之手段。所以矯正 措施之執行可能會因為問題之大小與可 能遭遇風險,處理方式有所不同 )。(可不適 用) • *3. 承上題,請確認所發生之不符合性 (異 常 )事件之矯正措施是否有監控改善成 效。 (可不適用 ) 94

K. 不符合性 (異常 )事件的鑑別 與管制 • *4. 承上題,請確認不符合性 (異常 )事件 之矯正措施,所造成作業程序之修訂 /調 整,實驗室是否已書面化與實施。 (可不適 用) • *5. 承上題,請確認不符合性 (異常 )事件 紀錄是否屬於檢驗報告異常,且該事項 已有回溯檢查此項發生之事件,對先前 檢驗結果之審查影響評估與紀錄。 (可不適 用) 95

K. 不符合性 (異常 )事件的鑑別 與管制 • *6. 承上題,針對上述檢驗報告錯誤,已 涉及傳染病檢驗機構品保作業要求之定 義時,您實驗室所有相關人員是否確實 知悉上述事件發生,應於規定時效內填 寫傳染病檢驗報告錯誤通報單進行通報 作業。 • *7. 承上題,請確認是否已建立對應檢驗 報告錯誤通報處理與回饋疾病管制局之 作業程序。 96

K. 不符合性 (異常 )事件的鑑別 與管制 • 8. 請確認針對當可能發生群聚感染、天 災及人為等因素影響檢驗服務流程時, 是否有對應之緊急應變程序或委託檢驗 服務措施。 97

L. 內部稽核 • 1. 請確認於是否建立書面化之內部稽核 程序。 • 2. 承上題,請確認內部稽核程序內容是 否有包括如何訂定稽核計劃、如何組織 稽核小組、如何執行、稽核形式、稽核頻 率、稽核方法、稽核所需要對應文件、稽 核後續處理與確認事宜之機制。 • 3. 承上題,請確認內部稽核內容是否有 稽核缺失且依據程序完成矯正並且確認 改善。(可不適用 ) 98

M. 管理審查 • 1. 請確認是否建立文件化之管理審查程 序。 • 2. 請確認是否曾執行管理審查並保有紀 錄,且後續引發之程序變更或改善措施, 已讓實驗室相關同仁知道與執行。 99

傳染病檢驗機構品保作業要 求 至少應針對下列要求訂定品保 /品管相關作業 程序 第一版 管理要求 -至少應包含外部服務與供應、不符合事項之管制與鑑別、 矯正 /預防 /持續改善措施. . 等。 技術要求 -至少應包含人員訓練、實驗室設備、檢驗程序品質保證 … 等。 第二版 (草案 ) 管理要求 -至少應包含 文件管制 、試劑管理、不符合事項之鑑別與管 制、矯正/預防 /持續改善措施等。 5. 1. 2 技術要求 -至少應包含人員訓練、 檢體處理程序 、實驗室設備管 理、檢驗程序品質 管制 、 傳染病陽性結果通報程序 等。

基層檢驗所常見缺失 (建議事 項) • 應依「傳染病檢驗機構作業要求」訂定相關作業程序,包括試劑 管理、不符合事項之鑑別與管制、矯正 /預防 /持續改善措施、 人員訓練、檢體處理程序、實驗室設備管理、檢驗程序品質管 制、傳染病陽性結果通報程序等。 • C型肝炎檢驗 SOP應訂定陽性重測及 gray zone之處理方式。 • 應訂定 C型肝炎檢驗相關品管作業規範。 • 檢驗所使用簡單流程圖或簡單操作說明提醒 作人員或操作, 該表單或紀錄應列入對應操作 SOP內以為連接。 • 應建立代檢其它醫療機構檢驗之合約審查程序並留有審查紀錄。 • 當結果如為法定傳染病通報時,檢驗所應建立通報處理程序 ( 包括誰被授權通報、如何通報、接受對象等 ),相關通報權責應 與使用之醫師協調後決定。 • ……

檢驗標準作業程序文件撰寫說 明
品質 (Quality) ?規範 (Rule)?法律 (Law)? Question 1. 你要你的 檢驗結果正確嗎 ?你會 希 望你的 檢驗報告品質 是實驗室 穩 定 的產品嗎?幫我完成檢驗的醫檢 師 是 菜鳥嗎 ?他 (她 )專心嗎 ?為什 麼? 2. 為什麼談品質 (認可、認證 )就一定 要 有 SOP? 真的沒有就不能做事嗎

SOP = Consensus + Promise • 不需要有一致性的承諾,或是保證有一 致 性的作法,且當有問題時可追溯到一致 性 的證據,則可以不需要有 SOP • 所以 SOP就是藉由「定於一」,來對流程 的穩定做要求,對產品的品質做保障 • Standard Operating Program

SOP = 定於一 • • • 選「定」方法 確「定」效能 訂「定」步驟 明「定」限制 傳「定」訊息 符合所約「定」的承諾
建立品質文件時的基本原則 做 一致 說 寫
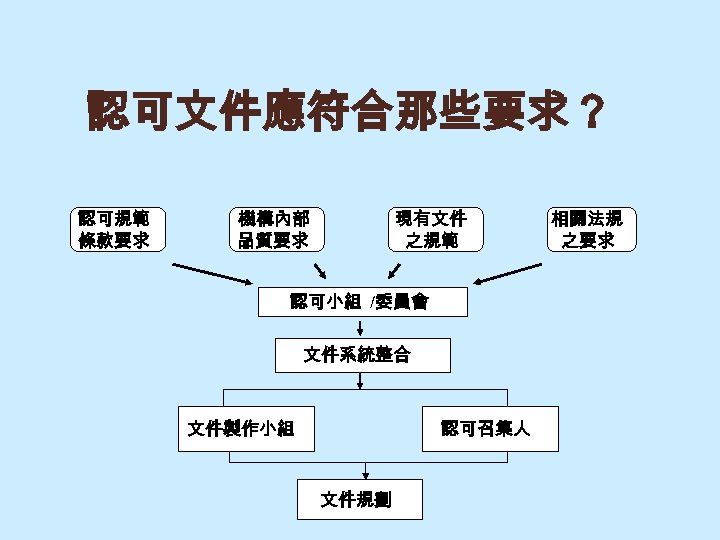
認可文件應符合那些要求? 認可規範 條款要求 機構內部 品質要求 現有文件 之規範 認可小組 /委員會 文件系統整合 文件製作小組 認可召集人 文件規劃 相關法規 之要求

認可文件應符合那些要求? 認可組織要求 醫院 (機構 )行政規定要求 自訂要求 國家行政命令法規- – 中央法規 /行政規則 /銓敘法規 /法務法規 – 環保法規、政法採購法 – 衛生署相關醫療法規; • 衛生褔利法規 • 醫師法、醫療法、醫檢師法實施細 則、醫檢師執業登記及繼續教育辦法、醫療 機構設置標準、 ………. • 當地醫療法規-縣市衛生局醫療法規 • •
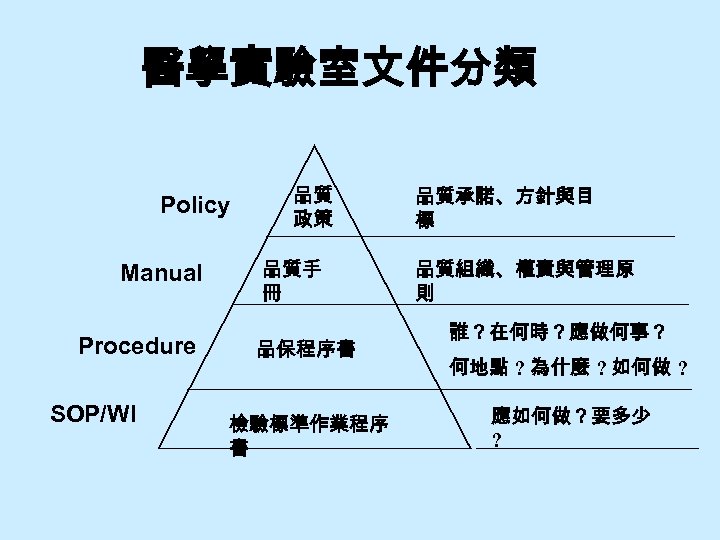
醫學實驗室文件分類 Policy Manual Procedure SOP/WI 品質 政策 品質手 冊 品保程序書 檢驗標準作業程序 書 品質承諾、方針與目 標 品質組織、權責與管理原 則 誰?在何時?應做何事? 何地點 ? 為什麼 ? 如何做 ? 應如何做?要多少 ?

醫學實驗室文件分階 文件一定要分四階嗎? 一階:就全部叫 SOP → OK 二階:分為管理 (QP / SOP)、 SOP兩類 → OK 三階:表單系統獨立;分為管理 (QP / SOP)、 SOP、 Records三類 → OK • 四階:將品質政策 (Policy)寫成文件,作為組織 整 體品質管理之最高指導書 (原則 ) → OK • 五階?也可以 → OK • •

品質手冊(第一階) • 原則性之作法敘述,不提及詳細作法,保留彈性。 • 以相關索引方式,將第二階文件串聯。 • 明定權責人員或執行人員。

品保程序書(第二階) 非原則性作法之敘述,而是實務上作法之說明。 說寫做一致。 界定該程序之範圍,以銜接之方或予以串聯。 若機構已經通過 ISO 9001驗證,可以參考現有品 質制度之做成相對應品質文件,避免兩制。 • 品保程序宜以簡單彈性為原則。 • 品保程序書應融合實驗室的管理風格及機構文 化。 • •

檢驗標準作業程序書(第三階 ) – 第三階文件應以實用為原則,減少人為操作之彈性差異。 – 如有更細部需要可另訂 作指導書。 – 應採用符合申請檢驗者需要,且適合檢驗之檢驗方法程序。 – 應使用確認過的程序以證實這些程序適合使用。 – 方法確認應足夠廣泛以符合應用範疇之要求。實驗室應記錄 所獲得的結果與方法確認之程序。 – 如可行時,文件的內容應包括 ISO 15189 § 5. 5. 3 之 17要項要求。 – 應製作現有的檢驗程序之清單,包括原始檢體的要求與檢驗 性能之規格。 – 儀器標準操作程序書應以方便指引操作實務為原則。

檢驗標準作業程序書(第三階 ) • • SOP (Standard Operating Program) SIP (Standard Investigating Program) SCP (Standard Calibrating Program) SVP (Standard Verifying Program) SSP (Standard Sampling Program) ………………. . 都可稱之檢驗標準作業程序書 (SOP)

檢驗標準作業程序書 • 所有程序應文件化 • 作場所供相關人員方便取用 • 使用實驗室人員了解語言編寫 • 正式使用前及每年定期審查程序適用性 (備註 ) • 只要有完整的手冊可供參考,摘錄關鍵資訊的卡片檔 案或類似系統可在 作台使用。這些卡片檔案或類似 系統應與手冊的內容一致,這種 摘錄式的程序 應成為 文件管制的一部份。 • 如果 廠商的使用說明書 所描述的程序與實驗室所實施 的程序相同,且以實驗室人員所普遍了解的語言編寫, 並遵照要求,則該使用說明書 (例如包裝內之說明書 ) 可用來做為程序之一部份。
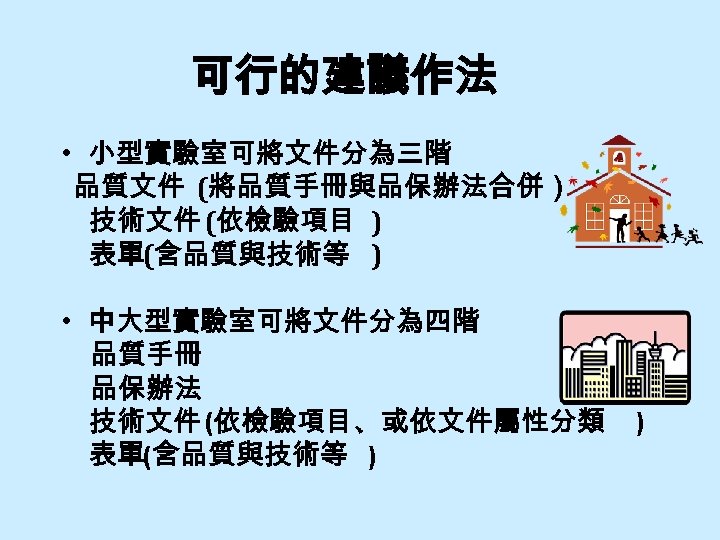
可行的建議作法 • 小型實驗室可將文件分為三階 品質文件 (將品質手冊與品保辦法合併) 技術文件 (依檢驗項目 ) 表單(含品質與技術等 ) • 中大型實驗室可將文件分為四階 品質手冊 品保辦法 技術文件 (依檢驗項目、或依文件屬性分類 表單(含品質與技術等 ) )

文件建立與管制的作法 • 建立文件及資料管制作業程序 • 文件之建立 (分類、裝訂順序、內容、字型及大小、編號、 審核與簽署、發行、修訂、改版及作廢 ) • 文件制訂依序由上至下,並列出 【 總目錄表 】 ,才不致重複而紊亂。 • 成立文件管制中心的權責人員。 • 作分配。

格式標準化 • 將品質文件之格式予以明定:格式化的 內容可包括封面格式、內頁格式、文件 內容格式、章節條款目格式、文件編號 原則、字型及其大小規定等資訊。

文件之核准與發行 • 審查、核准。審查核准之權責應予以界定 • 文件之總覽表與最新版次狀態、分發之記錄應 予 以建立。 • 在實驗室運作之重要場地,實驗室人員執行業 務 時應有經核准之最新版次文件供人員使用、參考。 • 文件應定期審查,以確認品質系統之適切性。 • 無效或過期之文件意指舊版次或已作廢之文件 , 應回收以防止誤用。 • 品質系統文件,應有唯一之識別編號。

文件修改 • 只要是適切性不良、流程改變、標準再版 …等因素均可予以修訂。 • 除非另有指派,否則修訂文件時應由原 審查、核准之功能單位執行審查、核准事 宜。

如何撰寫儀器操作程序書之格式,以下格式僅供參 考: ※摘錄原廠所提供之操作手冊為最佳參考 ※ 1. 目的 2. 量測方法及適用範圍 3. 名詞解釋及原理概述 4. 權責 5. 參考資料 6. 人員資格 7. 作標準

作標準 (續前投影片第 7 項 ) 本節中可更清楚地說明 7. 1 功能及規格 7. 2 面板及結構 7. 3 附件及消耗品規格 7. 4 環境需求 7. 5 操作方法 7. 6 精度及校驗 7. 7 保養方法 7. 8 維修及校正 7. 9 品質管制 7. 10 異常處理

如何撰寫檢體採集手冊 原始 檢體 收集手冊應包括下列: (引用 ISO 15189 5. 4. 3) a). 下列文件的副本或出處: 1). 實驗室所提供可利用之檢驗項目清單; 2). 同意書 (當可行時 ); 3). 提供病人收集檢體前的本身相關準備資料與說明書; 4). 提供實驗室服務使用者有關臨床適應症與適當選擇可利用的檢驗 程序的說明資料; b). 下列作業程序: 1). 病人的準備 (例如給護士與抽血人員的說明書 ); 2). 原始檢體的識別; 3). 原 始 檢 體 的 收 集 (例 如 抽 血 、 膚 穿 刺 、 液 與 其 他 的 體 液 皮 血 尿 等 )原

如何撰寫檢體採集手冊 (續 ) c)下列各事項的說明: 1). 如何完成檢驗單或電子申請單; 2). 原始檢體收集的種類與數量; 3). 如果要求的話,特殊的收集時間; 4). 收 集 時 間 與 實 驗 室 收 到 時 間 之 間 的 任 何 特 殊 處 理 (例 如 運送 要求、冷凍、保溫、立即傳送等 ); 5). 原始檢體的標示; 6). 臨床資訊 (例如服用藥物的病史 ); 7). 採檢時,確認病人身份之詳細方法; 8). 原始檢體收集人員的識別記錄; 9). 用於檢體採集物質之安全棄置;

如何撰寫檢體採集手冊 (續 ) d). 下列各事項的說明: 1). 檢驗檢體之儲存; 2). 申請附加檢驗項目的時間需求; 3). 附加檢驗項目; 4). 由於分析失敗而重複檢驗或是同一原始檢體再進一步的 檢驗;

如何撰寫標準作業程序書 (SOP) ※引用 ISO 15189 5. 5. 3說明對醫學實驗室 SOP 內容的要求 ※此內容的要求為撰寫各類專業醫學實驗室 SOP 的極大化 (最大聯集 ),部份下述條款可能不 適 用於醫學實驗室範疇下所有對應學科

醫學實驗室認證規範 ISO 15189: 2007 § 5. 5. 3 ( 1)檢驗目的( Purpose of the examination) ( 2)檢驗程序之原理(principle of the procedure used for examinations) ( 3)檢驗性能之規格(performance specifications) ( 4)原始檢體種類( primary sample system、type of container and additive ) ( 5)容器與添加物的種類 (type of container and additive) ( 6)所需的設備與試劑(required equipment and reagents) ( 7)校正程序( calibration procedures) ( 8)程序步驟( procedural steps) ( 9)品質管制程序( quality control procedures)

醫學實驗室認證規範 ISO 15189: 2007 § 5. 5. 3 ( 10)干擾( interferences and cross reactions) ( 11)計算結果程序的原理(principle of procedure for calculating results, including measurement uncertainty) ( 12)生物參考區間( biological reference intervals) ( 13)病人檢驗結果的可報告範圍 (reportable interval of patient examination results) ( 14)警告 /危險臨界值(alert/critical values, where appropriates ) ( 15)實驗室的解釋( laboratory interpretation) ( 16)安全防護( safety precautions) ( 17)潛在變異來源( potential sources of variability)

(1) 檢驗目的 Purpose of the examination • 應包括醫學上做此測試之原 因與包括之檢體種類 • 明確敘述此項檢驗項目的目 的

(2)檢驗程序之原理 Principle of the procedure used for examinations • 需說明該項檢驗方法或實驗反應所依據之理 論 • 自動化項目:應包含機台原理 • 手 操作項目:應包含測試原理

(3)檢驗性能之規格 Performance specification • Linearity • Precision • Accuracy expressed as uncertainty of measurement • Detection limit • Trueness of measurement • Sensitivity and specificity

(3)檢驗性能之規格 (一 ) Performance specification • 線性 Linearity – 線性範圍 待測物使用某一方法,利用某一儀器檢驗 時,反應變化可達到線性相關之最大範圍。 • 精密度 Precision – Within-run : = over 20, = ×× ﹪ no. CV – Between-run : = over 20, = ×× ﹪ no. CV – Total precision: CVt=√CVa 2+CVb 2+…

(3)檢驗性能之規格 (二 ) Performance specification • 準確度 Accuracy – Accuracy expressed as uncertainty of measurement – Combined standard uncertainty (Uc ); Coverage factor (k) equal to 2( 95%CI) – Uncertainty( U); Uc x k U= – 總誤差值 (Total error):(TE= BIAS + 2 SD) • 偵測極限 Detection limit – 待測物使用某一方法,利用某一儀器檢驗時, 實際可檢測之最高或最低偵測濃度 。

(3)檢驗性能之規格 (三 ) Performance specification • Trueness of measurement – 參與 EQA之 peer group mean評估實驗室 BIAS值 – BIAS = peer group mean - lab data • Sensitivity and specificity( clinical studies) – Sensitivity: true-positive rate in disease state : TP/( TP+FN) – Specificity: true-negative rate in non-disease : TN/( TN+FP)

Linearity tests • Mini-pool two conc. Sample-low conc. Sample as low as possible, high conc. near to verify point. • Make equal dilution as following table tube 1 2 3 4 5 6 7 Low pool 0 1 2 3 4 5 6 High pool 6 5 4 3 2 1 0 • The dilution No. should be more than 6(6 or 7) • Each test should be triplicates • Check outlier

關於量測不確定度之要求 (1)精密度 (precision):實驗室應提供申請之測 試項目所計算出之 CV值。 (2)真度 (正確性 )(trueness):實驗室應根據其參 與 EQA之 peer group mean評估計算 BIAS 值,或由與其他醫院所做之比對結果計算。 (3)總 誤 差 值 (Total error): 驗 室 由 自 行 所 作 實 數 據統計之 (TE= BIAS + 2 SD)。 (4)定 量 檢 驗 項 目 CV值 一 定 要 呈 現 , 於 總 誤 至 差 值 (Total error),目前可暫不顯示。

方法查證之時機 • • • 開設新檢驗項目 更換步驟或試劑 更換方法 更換檢驗儀器 更換試劑廠牌

(4) 原始檢體種類 (一 ) Primary sample system • 病人準備 – 病人在採檢之前需要進行哪些動作 – 病人需禁食 8 -10小時方可採檢 – 或依指定時間採檢 • 可接受之檢體種類 – 適用於此檢驗項目之檢體種類 – 全血、血漿、血清、24小時尿液、 Throat swap

(4) 原始檢體種類 (二 ) Primary sample system • 採檢時間限制 – 需採取清晨第一口痰 – 給藥後一小時 – 需在輸血後 1小時後採檢 – 兩次採檢時間需間隔 30分鐘

(5) 容器與添加物的種類 Type of container and additive • 可接受之抗凝劑種類 – 指檢體所使用抗凝劑的種類 – 使用哪一種採血管 • 檢體保存與運送方式 – 檢體檢驗前及檢驗後需保存在室溫還 是在 4℃冰箱,甚至是 -70 ℃冷凍櫃 – 從護理站送檢體到檢驗科櫃檯時需要 用冰寶或是冰塊及保溫箱運送

(6)所需的設備、試劑 Required equipment and reagents • 設備 – 離心機、微量吸管、自動化儀器 – 採檢之設備 • 試劑 – 包含廠牌、品名、內含物、試劑配製與 保存方式 – 包裝量標示

(7)校正程序 (一 ) Calibration procedures • 標準品 (Standard或 Calibrator) – 來源、配製方式、保存方式 – 追溯至國際單位制 (SI) • 校正步驟 – 如何做校正的動作 – 自動化儀器應包括簡易儀器操作步驟

(7)校正程序 (二 ) Calibration procedures • 校正點數與頻率 – 參與校正之各種濃度支數 – 多久校正一次 – 或每天早上開機時先用 Standard (or Calibrator)作校正 • 校正結果可接受的標準

(8)步驟 Procedural steps • 手 操作詳細步驟 • 自動化儀器應包括簡易儀器 操作步 驟 • 儀器內之自動添加之反應步驟不必 說明 • 可行時應加註 『 檢驗參數 』

(9)品質管制程序 (一 ) Quality control procedures • 品管液 (Control) – 來源、配製方式、保存方式 – 如做為比對之用之參考物質應有追溯文件 – 血庫 A cell, cell的泡製 B – 標準菌株之來源文件、鑑定、配製及保存方 式 • 品管步驟 – 繪製每日 QC chart(定量) – 若為自動化儀器應包括簡易儀器操作步驟

(9)品質管制程序 (二 ) Quality control procedures • 品管頻率 – 每 40檢體加作一支 QC – 三班輪值時,每班均至少一次品管 • 品管判讀與異常如何處理 – 定性品管應完全符合 – 依 2 SD Rule或 Westergard rule判讀品管結果 – 當 Coombs control Cell反應如為 2+以下時,需重新 泡製 – 判定為異常之品管時應停止檢驗並依異常處理 程序處理。
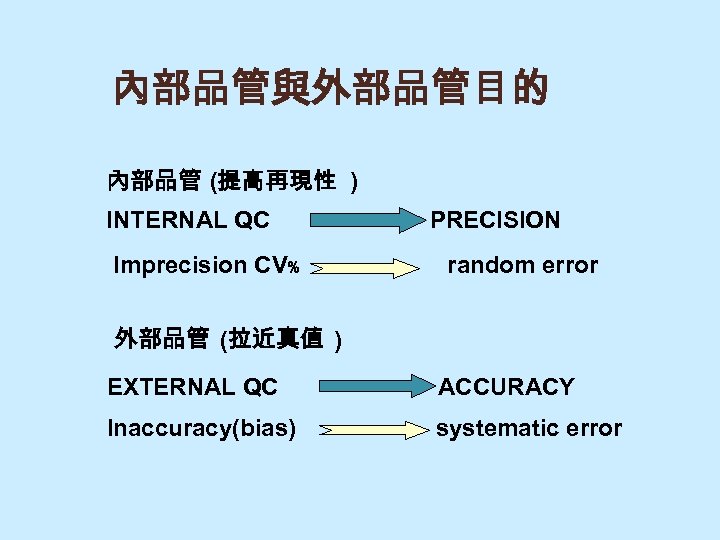
內部品管與外部品管目的 內部品管 (提高再現性 ) INTERNAL QC Imprecision CV﹪ PRECISION random error 外部品管 (拉近真值 ) EXTERNAL QC ACCURACY Inaccuracy(bias) systematic error

(10)干擾 Interferences and cross reactions • 指檢體本身造成的干擾,如:脂血、溶血、 黃疸 – 溶血檢體的檢驗值會偏高 – 脂血檢體會影響到比色值,導致結果 無法判讀 • 檢體與試劑可能造成之生物偽陽或偽 陰之交叉反應。

(11)計算結果的原理 (Principle of procedure for calculating results,including measurement uncertainty) • 結果如何運算或判讀 • 說明量測不確定度之計算原理

(12)生物參考區間 Biological reference intervals • 生物參考區間通常為生物參考值常態分布中間 的百分之九十五信賴區間 (95% Confidence Interval) – 參考值 – 參考範圍 (區間 );某些具體情況下,對參考區 間重新賦予分類或不均勻性 (不對稱性 )的取 值可能更為合適。 – 它不可與正常值範圍「 normal range」來誤用 • 實驗室應建立自己實驗室的參考區間

(13)病人檢驗結果的可報告範圍 Reportable interval of patient examination results • 何種情況下病人結果可作報告 –Calibrator或 Standard curve皆符合設定 標準 –Control皆符合設定標準 –已了解結果小於 Detection limit如何處 理 –已了解結果大於線性範圍如何處理 –已了解結果落於 Border line如何處理 –已了解結果出現干擾性反應如何處理 • AMR & CRR的差異探討

(14)警告 /危險臨界值 Alert/critical values,where appropriates – 實驗室應與臨床醫師討論需通報 之臨界值 – 高值、低值界限 – 危險臨界值通報程序與記錄

(15)實驗室的解釋 Laboratory interpretation – 臨床意義 – 實驗室對檢體檢驗後臨床檢驗人 員或報告簽署人對檢驗結果的說 明。

(16)安全防護 Safety precautions • 指在檢驗過程中操作人員會受到的 生物危害、化學危害及必要防護措施 手套、實驗衣、防護鏡、生物安全操 作箱等 • 對被檢驗之病患可能在檢驗過程中 產生之病患安全之預防與防護。

(17)潛在變異來源 Potential sources of variability • 檢體可能因不當收集或處置造成。 • 會造成檢驗結果偽陽性或偽陰性之影響因素 – 當病人在採檢前有食用含有豬血、鴨血、雞 血之類的食物時,會造成糞便潛血反應為 陽性 – 當病人接收高劑量抗生素治療時,會造成 DAT陽性

注意事項 參考資料 • 實驗操作標準檢驗作業程序時,可能產 生之錯誤或疏失 • 或異常事件之累積 • 前車之鑑 • 溫度 • 材料的替代性 • 方法確認之紀錄資料 • 量測追溯之證明文件

撰寫標準作業程序書差異性探討 討論 (撰寫 SOP時之差異性探討比較 表 )因為: 此內容的要求為撰寫各類專業醫學 實驗室 SOP的極大化 (最大聯集 ),部 份下述條款可能不適用於醫學實驗 室範疇下所有對應學科

檢驗標準操作程序依照 TAF標準撰寫 SOP時之一致性比較表 (請根據您個人專業及實務經驗加以評估 ) 組 別 項 目 檢 驗 目 的 檢 驗 方 法 原 理 檢 驗 效 能 生化 細菌 / 病毒 血庫 血清免 疫 血液 鏡檢 ○: 均可行 X : 均不可行 △: 依方法差異部份可行 R :此項可獨立成立一份 SOP 專業組別: 學員姓名: 原 始 樣 本 種 類 容 器 及 添 加 物 種 類 設 備 與 試 劑 校 正 程 序 步 驟 品 質 管 制 程 序 干 擾 及 交 叉 反 應 計 算 結 果 的 原 理 生 圍病 物 人 參 檢 考 驗 區 結 間 果 可 報 告 範 警 告 或 臨 界 值 實 驗 室 的 解 釋 安 全 防 護 潛 在 變 異 來 源

參考附錄 • 檢驗作業程序 (SIP)撰寫項目內容應包含,但不限於: • (1)檢驗目的:敘述檢驗項目之目的及醫學上做此測試之原因。 • (2)檢驗程序的原理:依據參與能力試驗方法分類寫出方法名稱,並 說明檢驗項目所依據之理論或反應式。 • (3)檢驗效能之規格:定性以真假陽性比例,敏感度,特異性表示;定 量則包括分析的範圍性 (線性)、精密度、準確度的表現如量測不確定 度、偵測極限、量測區間以及量測真值 …等來表現。 • (4)原始檢體種類:適用該檢驗項目之檢體種類,例如血漿、血清、全 血、尿液、脊髓液。 • (5)容器與添加物的種類:包含可使用之採檢容器、檢體量、採檢方 式、採檢人員、可接受抗凝劑種類、檢體的運送要求、檢體的保存條 件及檢體處理注意事項等。 • (6)所需的設備與試劑:列出操作此檢驗項目之主要檢驗儀器及輔助 設備 (例如溫箱、離心機、微量吸管等 );試劑部分註明試劑名稱、廠 牌品名、包裝規格、試劑的儲存與穩定、試劑配製步驟、開封後使用 效期或特殊保存,特別狀況。 • (7)校正程序 (量測追溯 ):校正物質來源、配置方法、保存方式、校正 點數、校正頻率、校正程序步驟、校正結果允收標準、量測追溯聲明。 • (8)程序步驟:手 操作撰寫詳細步驟;自動化儀器操作步驟,可撰寫 簡易操作步驟或指出遵照的相關程序 (如儀器操作程序 )。

參考附錄 • (9)品質管制程序:內部品管物質來源、點數、配置方法、保存方式、 步驟、頻率、判讀標準及異常品管如何處理;替代性品管操作方法。 • (10)干擾:檢體其它內含物質造成的干擾,例如脂血、溶血、黃疸或 藥物;添加物造成的干擾,例如抗擬劑肝磷脂、檸檬酸鹽、草酸酯、 EDTA以及鈉氟化物;檢體與試劑可能造成生物偽陽或偽陰之交互反 應 (定性項目 )。 • (11)計算結果的原理 (定量 )或結果判讀 (定性 ):定量項目說明計算結 果的公式及如何計算;定性項目說明如何計算 Cut-off值、價數判讀標 準、陰性陽性判讀標準、細胞形態學如何判讀。 • (12)生物參考區間 (定量 ):敘述該檢驗項目各檢體類別之生物參考區 間,並考慮性別、年齡及族群等條件,是否有不同生物參考區間。 • (13)病人檢驗結果的可報告範圍 (定量 )或報告格式 (定性 ):定量項目 參考線性規格訂定,並說明超出可報告範圍如何處理及出具報告, 例如可稀釋或濃縮的項目,其可報告範圍應乘以稀釋倍數或除以濃 縮倍數,才是可報告範圍;定性項目敘述該檢驗項目陰性及陽性結 果之報告格式,例如 XXXX was found/Not found、 Positive/negative、 reactive/Non-reactive、 1: 160(+)/<1: 80(-)。 • (14)警告 /危險值:註明危險值之數據,說明高值、低值界限,並考慮 性別及年齡等條件,是否有不同警告 /危險值設定。

參考附錄 • (15)實驗室的解釋:敘述該檢驗結果之臨床意義,比較檢驗結果落於 參考區間內外 (定量 )或陰性陽性結果 (定性 )與臨床診斷發現,來說明 檢驗結果是正常、不正常或不確定的,當不確定時後續處理追蹤之 建議等。 • (16)安全防護:敘述在檢驗過程中操作人員會受到的生物、化學危害 及必要防護措施及操作此項檢驗所需之防護裝備;除參照科內安全 衛生作業程序之要求,針對各檢驗項目特殊狀況必須加以說明,包 括廢棄物之處理,實驗操作的注意事項等。 • (17)潛在的變異來源:敘述影響該項檢驗結果常見之潛在的因素,包 括未依照 SOP執行,如使用儀器不當、採量、檢體稀釋、計時錯誤等; 校正結果偏移;儀器輸入量誤差;試劑成份穩定性、泡製、儲存等; 適用的儀器設備,如電力穩定性、水質、校正、維護保養時間、使用 率等;作業環境,如空調、溫度、濕度、照明、振動等。檢體保存的條 件,如保存容器、時間、溫度、檢體解凍等。 • 當程序有合適之資訊時,文件化的內容可包含,但不限於: • (18)注意事項 • (19)參考文獻 • (20)有關聯的文件 • (21)附件 (表單、標籤、卡片、張貼文件 )

參考附錄 • 針對部分細菌檢驗項目,檢驗報告是綜合多項檢驗結果而成的,檢 驗作業程序 (SIP)會涉及流程面之內容,其可另訂撰寫格式,不需依 上述規定之格式撰寫。 • 針對部分血庫檢驗項目,檢驗報告是綜合多項檢驗結果而成的,檢 驗作業程序 (SIP)會涉及流程面之內容,其可另訂撰寫格式,不需依 上述規定之格式撰寫。 • 針對部分形態學檢驗項目,檢驗報告是綜合多項檢驗結果而成的, 檢驗作業程序 (SIP)會涉及流程面之內容,其可另訂撰寫格式,不需 依上述規定之格式撰寫。

Thanks for your Attention 163
f3484d193f882a63c88d77d1b27e5a73.ppt