ee248dc1b3afb326ffe1d6b54ec45b9b.ppt
- Количество слайдов: 85

井冈山大学化学化 学院 胡 荣 华 1 3 9 7 0 6 5 6 0 2 8
第九章 卤代烃 Alkyl Halides 第一节 分类、命名和同分异构现象 第二节 一卤代烷 * 第三节 亲核取代反应历程* 第四节 一卤代烯烃和一卤代芳烃 第五节 卤代烃的制法 第六节 重要的卤代烃 第七节 有机氟代物

第一节 卤代烃的分类、命名和同分异构现象 Classification, Nomenclature & Isomerism 一、Classification of Alkyl halides 烃中氢原子被卤原子取代后生成的产物,称为卤代 烃。卤原子是其官能团,通常是氯、溴、碘。氟的 性质极活泼,用常规方法不能制得,故不在本章重 点讨论之列。卤代烃的性质较为活泼,可转化成多 种有机化合物,在 业、农业和医药方面都有广泛 的用途。 卤代烃的种类很多,分类的依据不同,类名也不相同。

第一节 卤代烃的分类、命名和同分异构现象 Classification, Nomenclature & Isomerism 一、Classification of Alkyl halides 1 2 3 4 根据卤素的种类分类: 氟代烃,氯代烃,溴代烃和碘代烃四大类。 根据卤素的数目分类: 一卤代烃,二卤代烃,多卤代烃等。 根据烃基的类别分类: 饱和卤代烃,不饱和卤代烃,卤代芳烃等。 根据与卤素相连的碳的级别分类: 一级卤代烃(伯),二级卤代烃(仲)和三级卤代烃(叔)
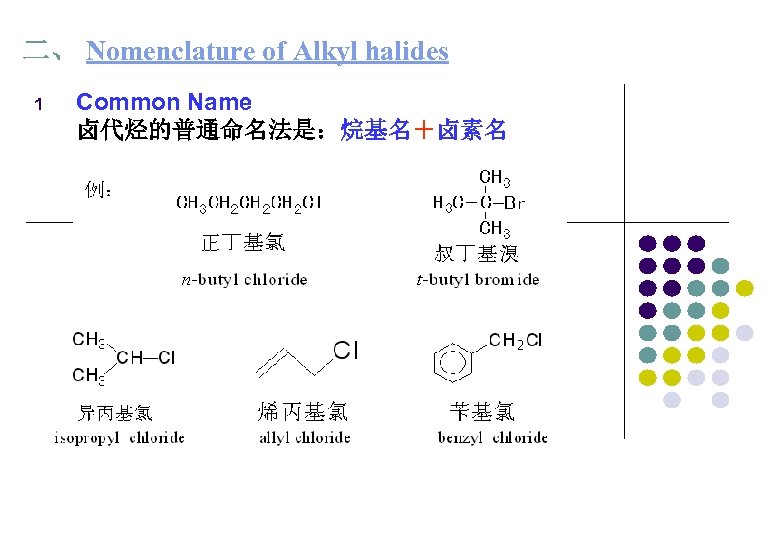
二、 Nomenclature of Alkyl halides 1 Common Name 卤代烃的普通命名法是:烷基名+卤素名
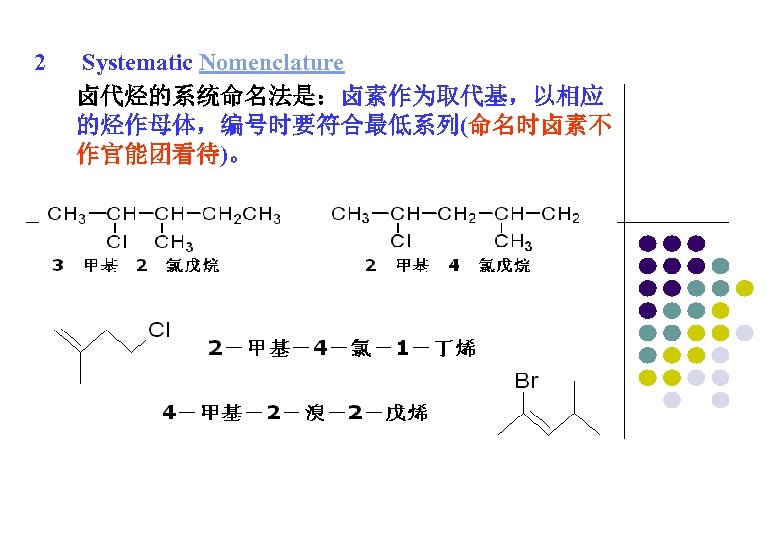
2 Systematic Nomenclature 卤代烃的系统命名法是:卤素作为取代基,以相应 的烃作母体,编号时要符合最低系列(命名时卤素不 作官能团看待)。
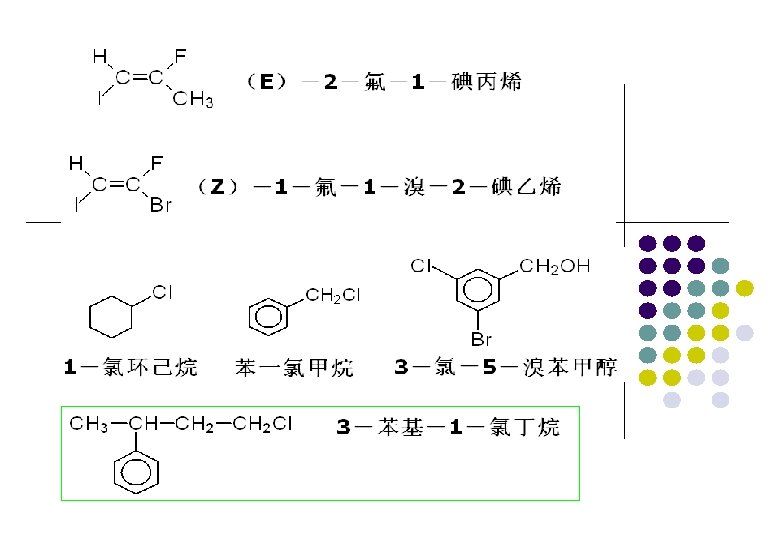
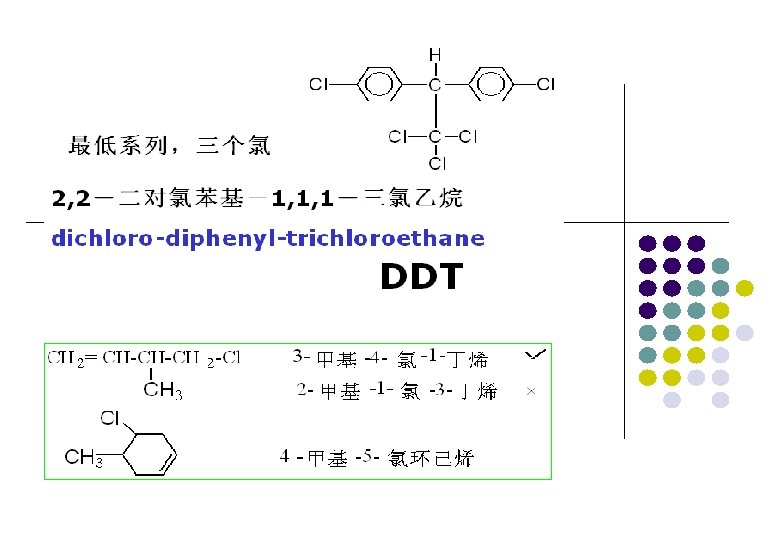
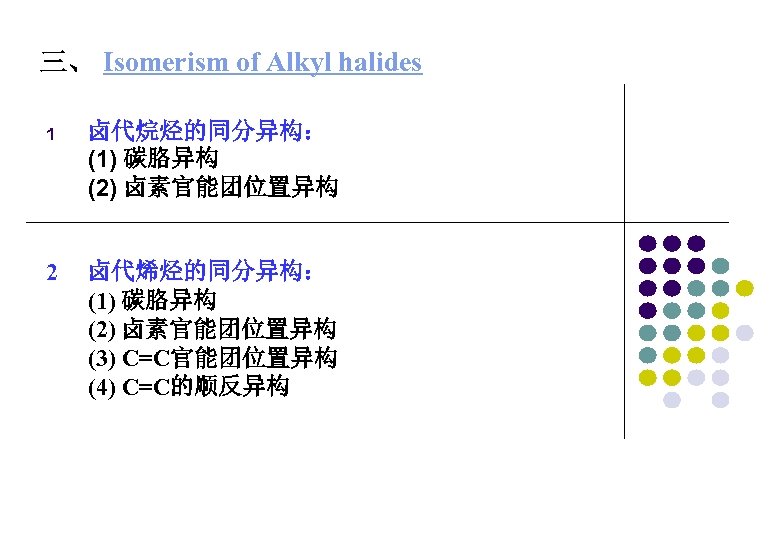
三、 Isomerism of Alkyl halides 1 卤代烷烃的同分异构: (1) 碳胳异构 (2) 卤素官能团位置异构 2 卤代烯烃的同分异构: (1) 碳胳异构 (2) 卤素官能团位置异构 (3) C=C官能团位置异构 (4) C=C的顺反异构

第二节 一卤代烷(Alkyl Monohalides) 一、 Physical Properties of Alkyl Monohalides 1 2 3 4 5 6 一般卤代烷为不溶于水的液体; 一般卤代烷是无色的,但碘代烷久置后因分出解碘而带棕 红色; 卤代烷的蒸气有一定的毒性,使用时要加以注意; Beilstein Test: 卤代烷在铜丝上燃烧时能产生绿色火焰(挥 发性的卤化铜) 卤代烃具有一定的极性,沸点比相同碳原子的烷、烯、炔等烃 类高; 烃基相同时,以碘代烷的沸点最高;卤素相同时,分支越多沸 点越低。
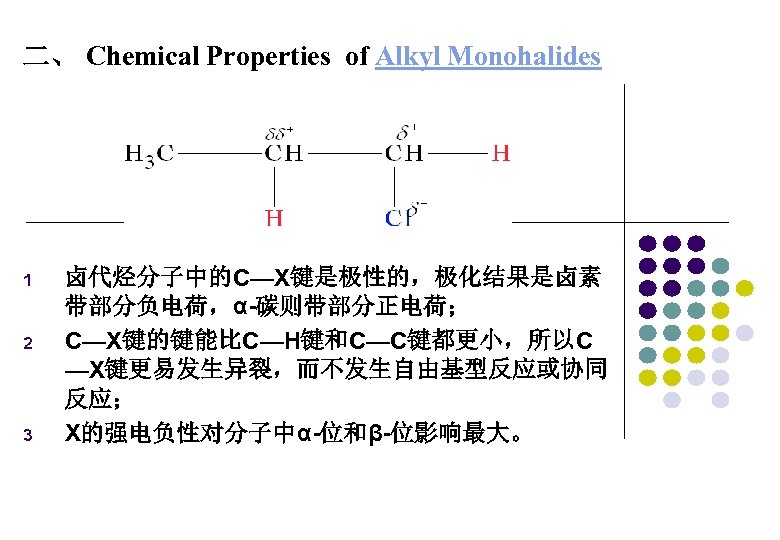
二、 Chemical Properties of Alkyl Monohalides 1 2 3 卤代烃分子中的C—X键是极性的,极化结果是卤素 带部分负电荷,α-碳则带部分正电荷; C—X键的键能比C—H键和C—C键都更小,所以C —X键更易发生异裂,而不发生自由基型反应或协同 反应; X的强电负性对分子中α-位和β-位影响最大。
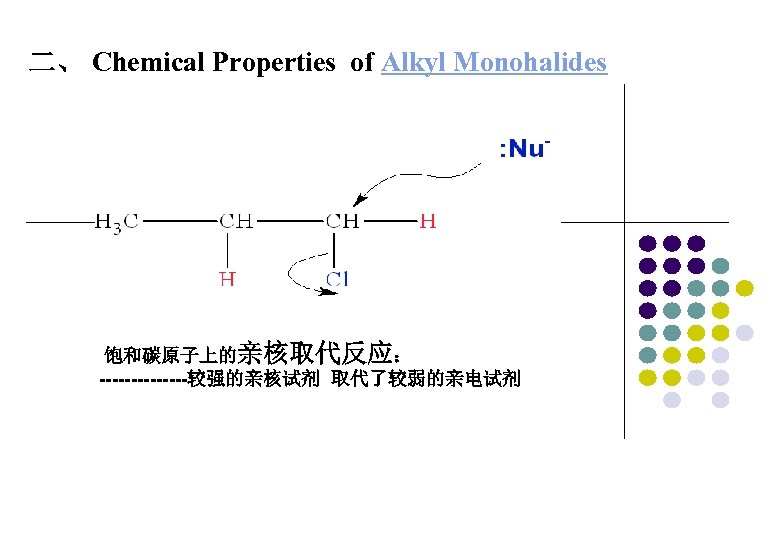
二、 Chemical Properties of Alkyl Monohalides 饱和碳原子上的亲核取代反应: -------较强的亲核试剂 取代了较弱的亲电试剂
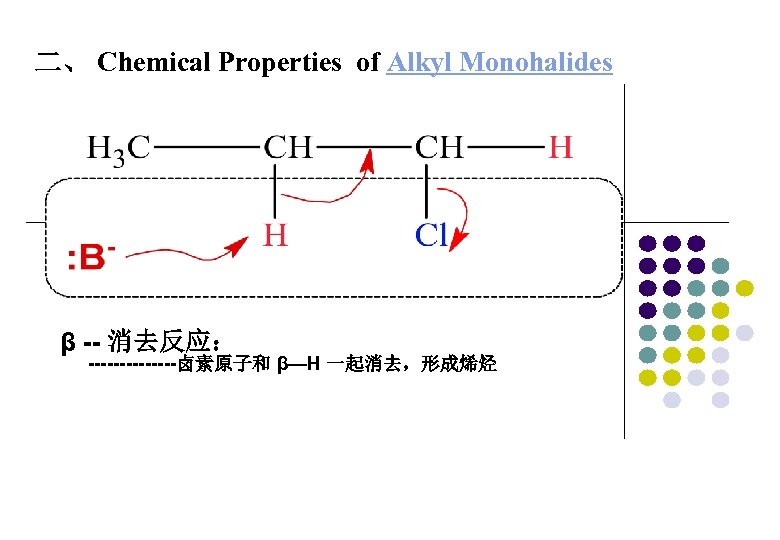
二、 Chemical Properties of Alkyl Monohalides β -- 消去反应: -------卤素原子和 β—H 一起消去,形成烯烃
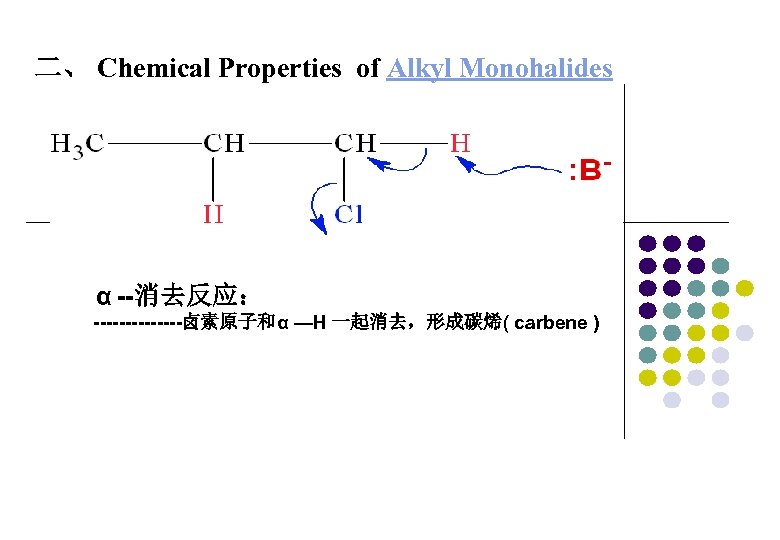
二、 Chemical Properties of Alkyl Monohalides α --消去反应: -------卤素原子和α —H 一起消去,形成碳烯( carbene )
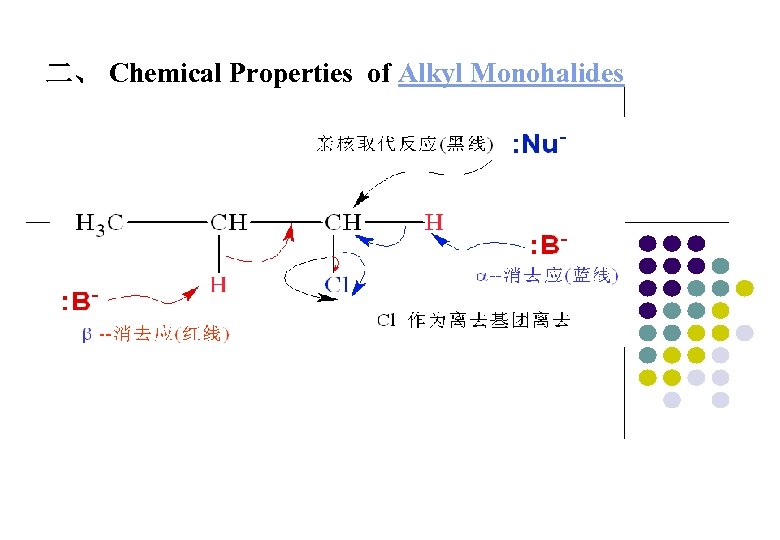
二、 Chemical Properties of Alkyl Monohalides

1. 取代反应 (Nucleophilic Substitution) 亲核试剂——带有孤对电子或负电荷,对原子核或正电荷有 亲和力的试剂,用Nu:或Nu-表示。 常见的亲核试剂有:OR-、OH-、CN-、NH 3、H 2 O等。 (1) 水解 (2) 与醇钠作用 (3) 与氰化钠作用 (4) 与氨作用 (5) 卤离子交换反应 (6) 与硝酸银作用
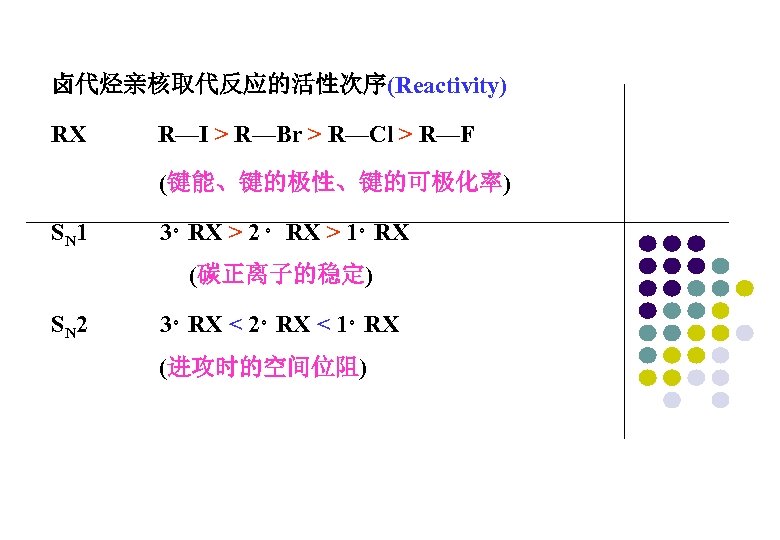
卤代烃亲核取代反应的活性次序(Reactivity) RX R—I > R—Br > R—Cl > R—F (键能、键的极性、键的可极化率) SN 1 3。RX > 2 。 RX > 1。RX (碳正离子的稳定) SN 2 3。RX < 2。RX < 1。RX (进攻时的空间位阻)
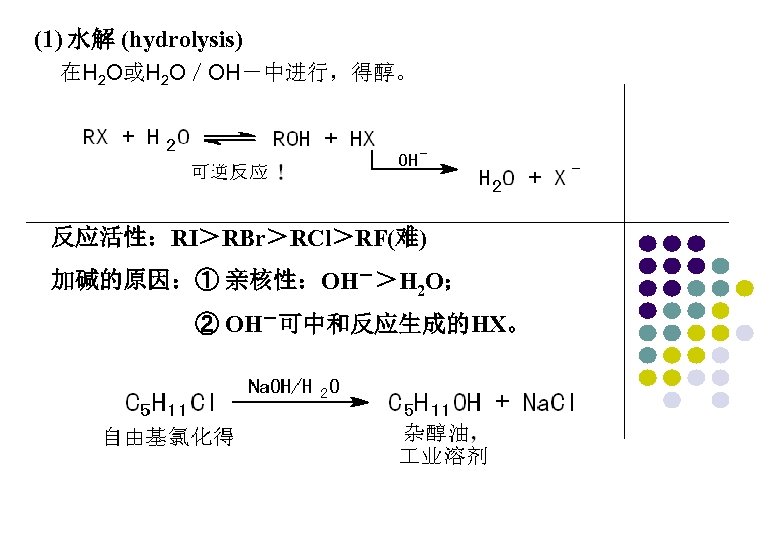
(1) 水解 (hydrolysis) 在H 2 O或H 2 O/OH-中进行,得醇。 反应活性:RI>RBr>RCl>RF(难) 加碱的原因:① 亲核性:OH->H 2 O; ② OH-可中和反应生成的HX。
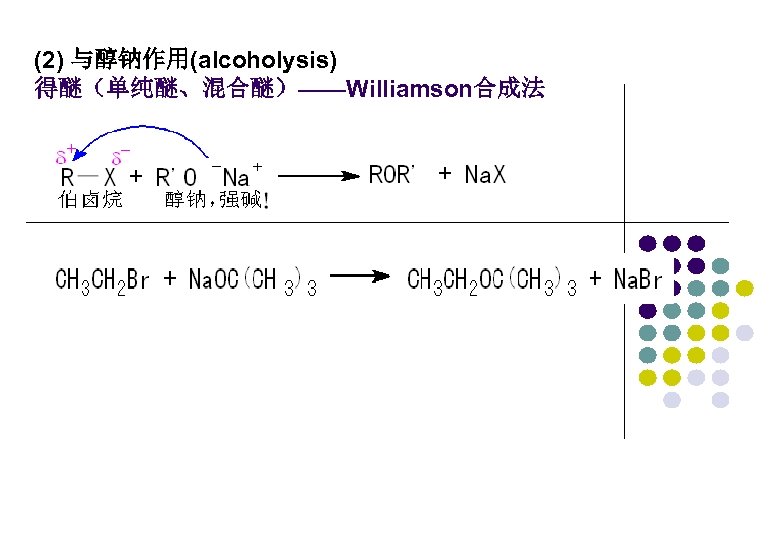
(2) 与醇钠作用(alcoholysis) 得醚(单纯醚、混合醚)——Williamson合成法
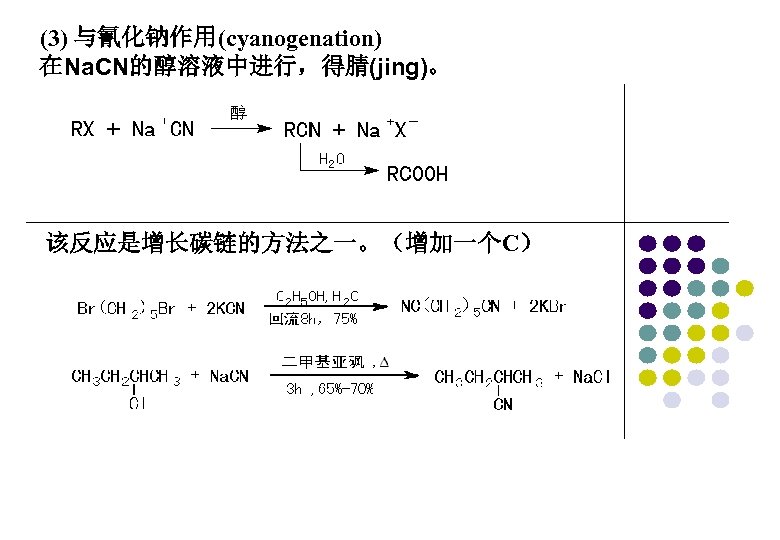
(3) 与氰化钠作用(cyanogenation) 在Na. CN的醇溶液中进行,得腈(jing)。 该反应是增长碳链的方法之一。(增加一个C)
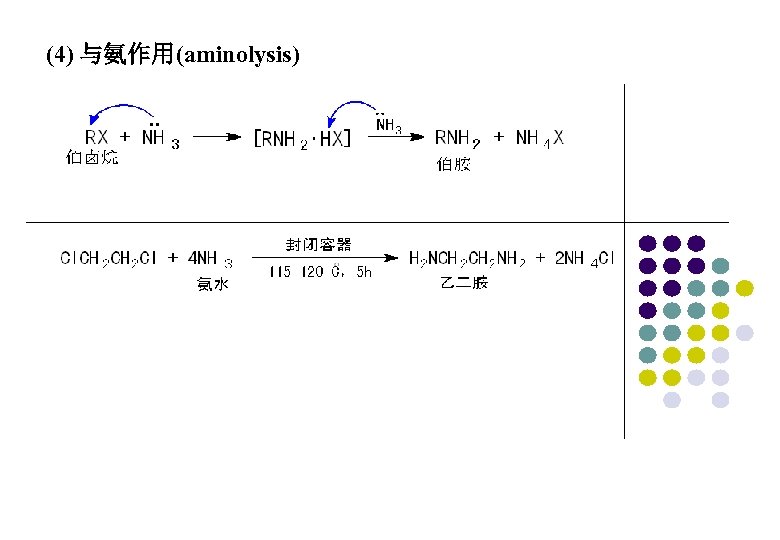
(4) 与氨作用(aminolysis)

(5) 卤离子交换反应(halogenation) 反应活性:伯卤烷>仲卤烷>叔卤烷。(参见SN 2) 生成的Na. Cl或Na. Br不溶于丙酮而形成沉淀,此反应可 用于检验氯代烷和溴代烷。
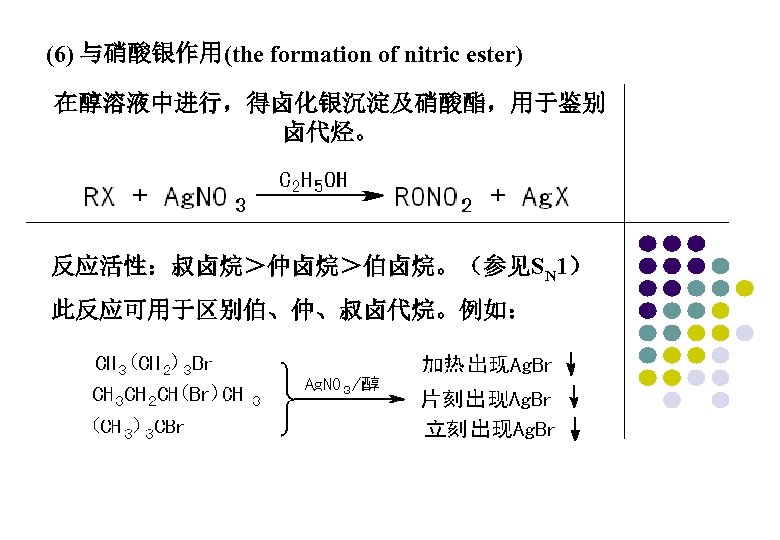
(6) 与硝酸银作用(the formation of nitric ester) 在醇溶液中进行,得卤化银沉淀及硝酸酯,用于鉴别 卤代烃。 反应活性:叔卤烷>仲卤烷>伯卤烷。(参见SN 1) 此反应可用于区别伯、仲、叔卤代烷。例如:
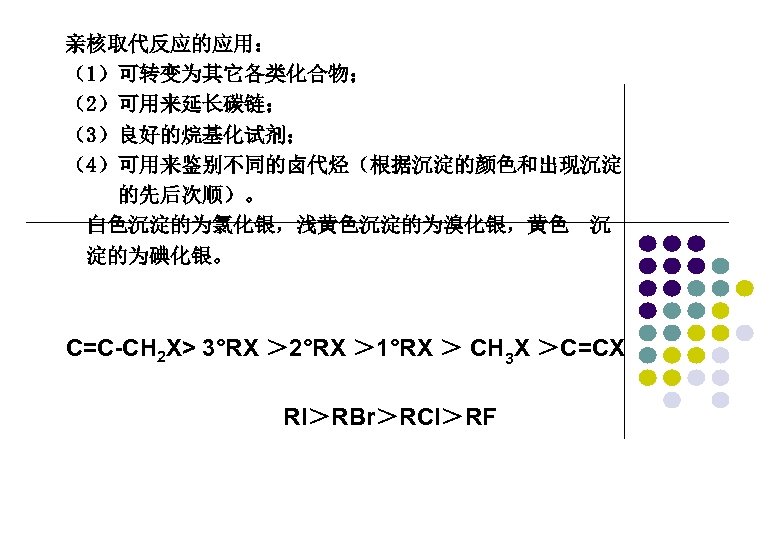
亲核取代反应的应用: (1)可转变为其它各类化合物; (2)可用来延长碳链; (3)良好的烷基化试剂; (4)可用来鉴别不同的卤代烃(根据沉淀的颜色和出现沉淀 的先后次顺)。 白色沉淀的为氯化银,浅黄色沉淀的为溴化银,黄色 沉 淀的为碘化银。 C=C-CH 2 X> 3°RX > 2°RX > 1°RX > CH 3 X >C=CX RI>RBr>RCl>RF

2. 消去反应 (Elimination Reaction) 消除反应——反应中失去一个小分子(如H 2 O、NH 3、 HX等)的反应叫消除反应,用E(Elimination)表示。 (1) 脱卤化氢(dehydrohalogenation) 由于-X的-I效应,R-X的β-H有微弱酸性, 在Na. OH/醇中可消去HX,得烯烃或炔烃: 反应活性:叔卤烷>仲卤烷>伯卤烷。
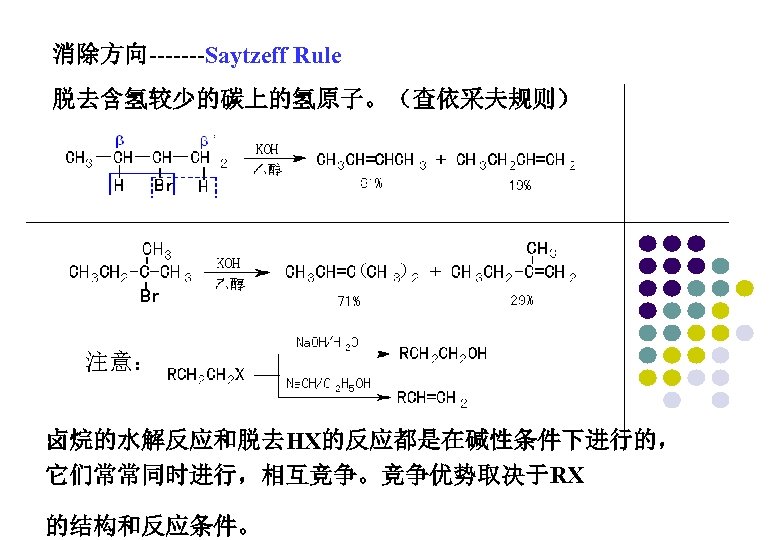
消除方向-------Saytzeff Rule 脱去含氢较少的碳上的氢原子。(查依采夫规则) 注意: 卤烷的水解反应和脱去HX的反应都是在碱性条件下进行的, 它们常常同时进行,相互竞争。竞争优势取决于RX 的结构和反应条件。
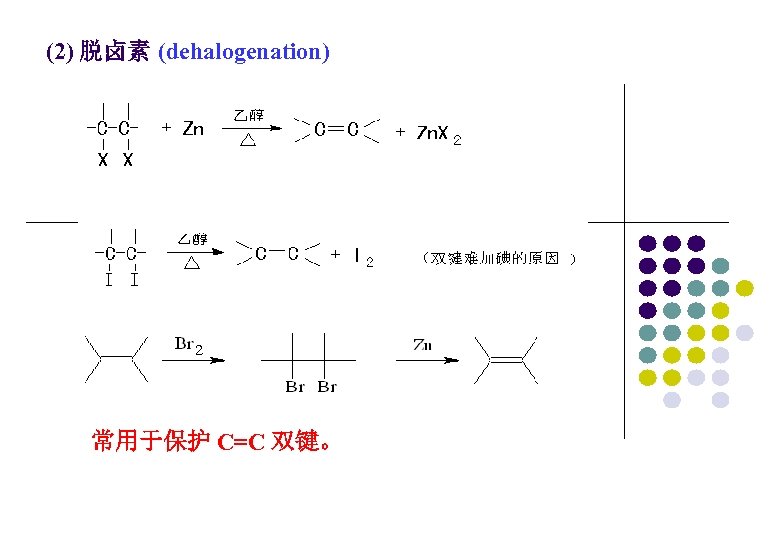
(2) 脱卤素 (dehalogenation) 常用于保护 C=C 双键。

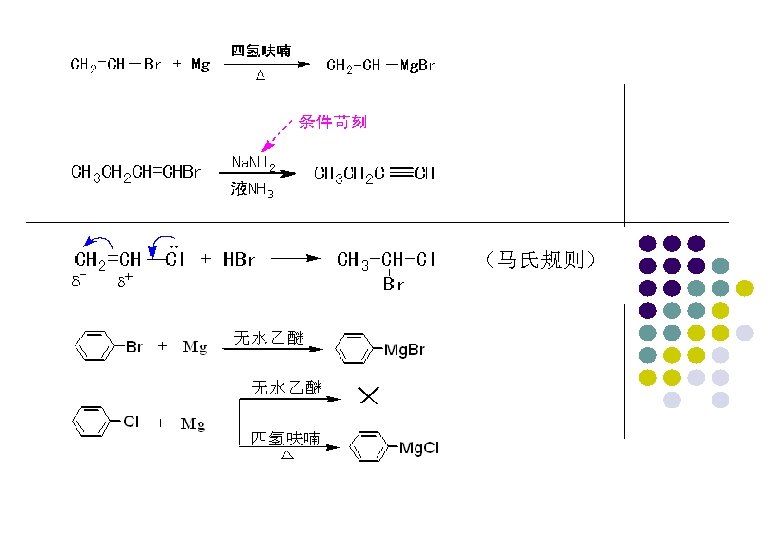
3. 与金属反应 (Reaction with Metals) 卤代烃能与某些金属发生反应,生成有机金属化合物 ——金属原子直接与碳原子相连接的化合物。 (1) 与金属镁的反应 绝对乙醚——无水、无乙醇的乙醚。 格氏试剂的结构目前还不十分清楚,一般认为它是溶剂化的:

用四氢呋喃(THF,b. p 66℃)代替乙醚(b. p 34℃ ),可使许多不 活泼的乙烯型卤代烃制成格氏试剂:
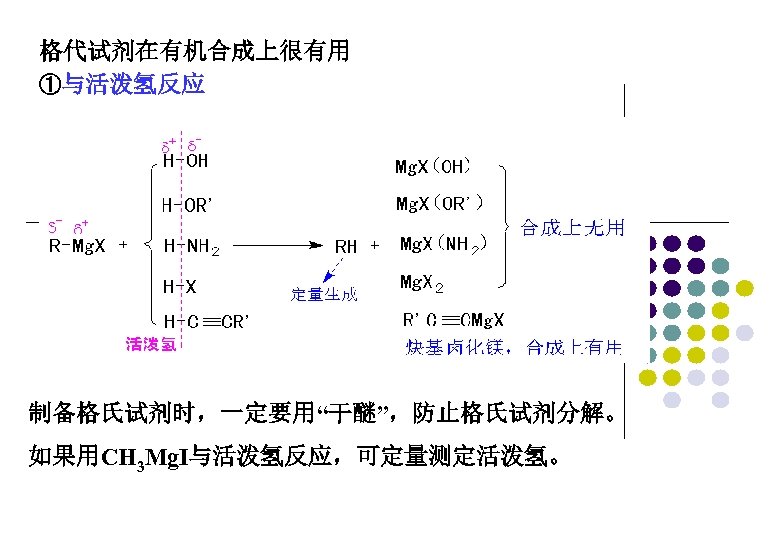
格代试剂在有机合成上很有用 ①与活泼氢反应 制备格氏试剂时,一定要用“干醚”,防止格氏试剂分解。 如果用CH 3 Mg. I与活泼氢反应,可定量测定活泼氢。
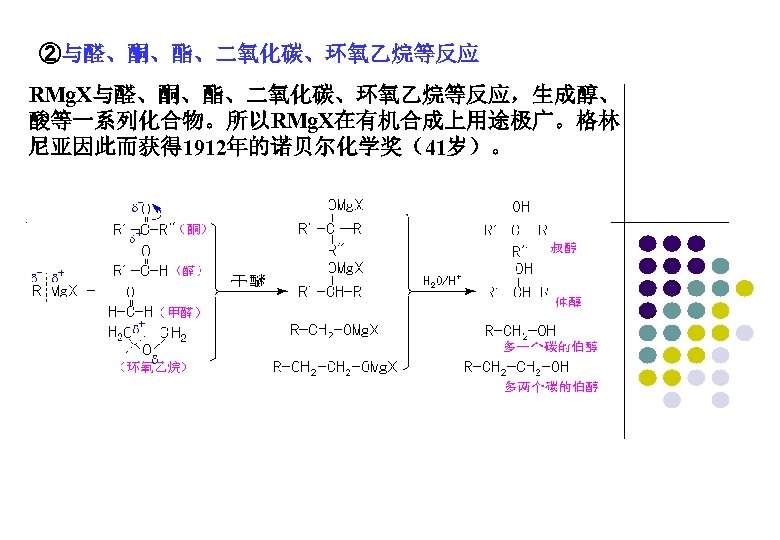
②与醛、酮、酯、二氧化碳、环氧乙烷等反应 RMg. X与醛、酮、酯、二氧化碳、环氧乙烷等反应,生成醇、 酸等一系列化合物。所以RMg. X在有机合成上用途极广。格林 尼亚因此而获得 1912年的诺贝尔化学奖(41岁)。
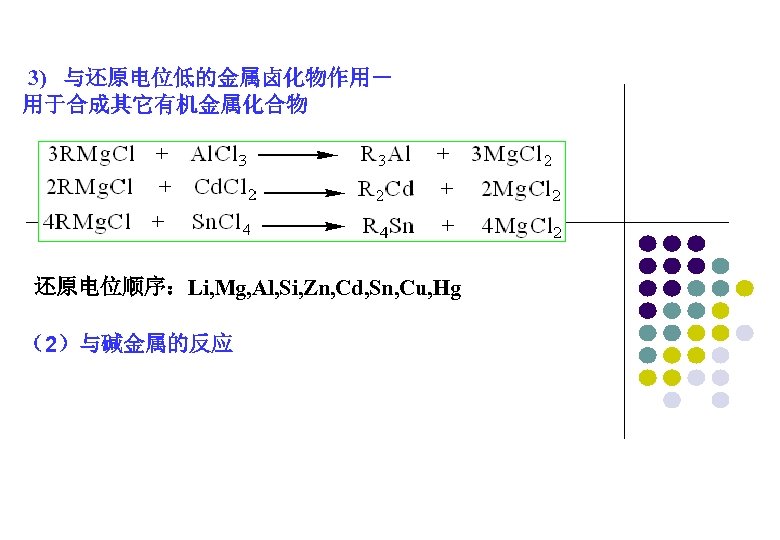
3) 与还原电位低的金属卤化物作用- 用于合成其它有机金属化合物 还原电位顺序:Li, Mg, Al, Si, Zn, Cd, Sn, Cu, Hg (2)与碱金属的反应

1) 2) 3) 4) 与金属钠的反应(Wurtz Reaction) 2 R—X + 2 Na → R—R + 2 Na 此反应可用来从卤代烷制备含偶数碳原子,结构对称的 烷烃(只适用于伯卤代烷,不同烷基无实用价值)。 2) 与金属锂反应 卤代烷与金属锂在非极性溶剂(无水乙醚、石油醚、苯) 中作用生成有机锂化合物: 反应活性:RI>RBr>RCl>RF
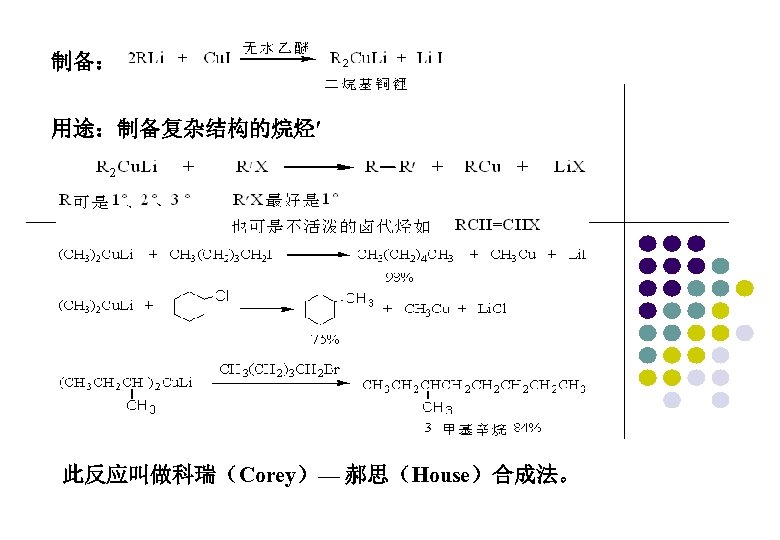
制备: 用途:制备复杂结构的烷烃′ 此反应叫做科瑞(Corey)— 郝思(House)合成法。
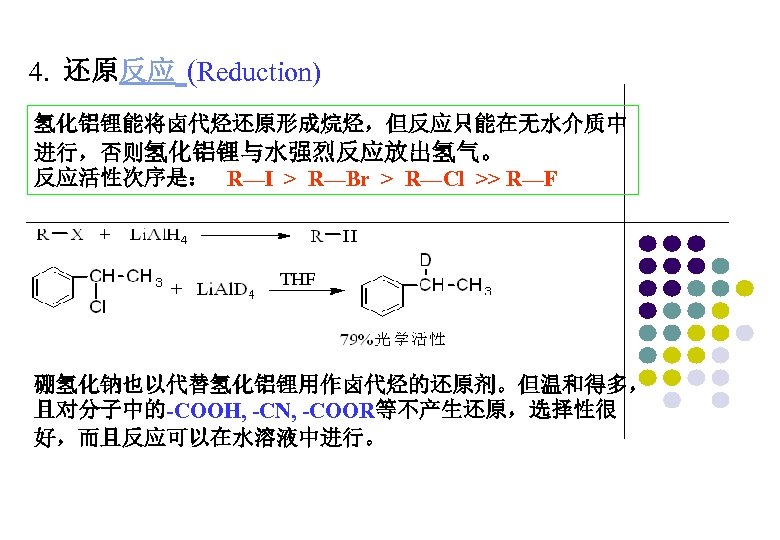
4. 还原反应 (Reduction) 氢化铝锂能将卤代烃还原形成烷烃,但反应只能在无水介质中 进行,否则氢化铝锂与水强烈反应放出氢气。 反应活性次序是: R—I > R—Br > R—Cl >> R—F 硼氢化钠也以代替氢化铝锂用作卤代烃的还原剂。但温和得多, 且对分子中的-COOH, -CN, -COOR等不产生还原,选择性很 好,而且反应可以在水溶液中进行。

第三节 亲核取代反应历程 ( Mechanism of Nucleophilic Substitution) 卤代烃的亲核取代反应(简写为SN)是饱和碳上取代反应的 最典型代表。已知卤代烷RX在合适的条件下能发生水解、氰 解、氨解、醇解等一系列亲核取代反应。反应通式为: 这类反应的历程研究较为深入,C. K. Ingold和E. D. Hughes在 1927年到 1935年间对饱和碳原子上的亲核取代 反应进行了广泛和深入地研究,并提出了SN 1历程和SN 2 历程两种基本的反应历程。到了1950年以后,S. Winstein提出了他的溶剂解离子对历程,继承和发展了 Ingold-Hughes的SN 1 -SN 2历程。
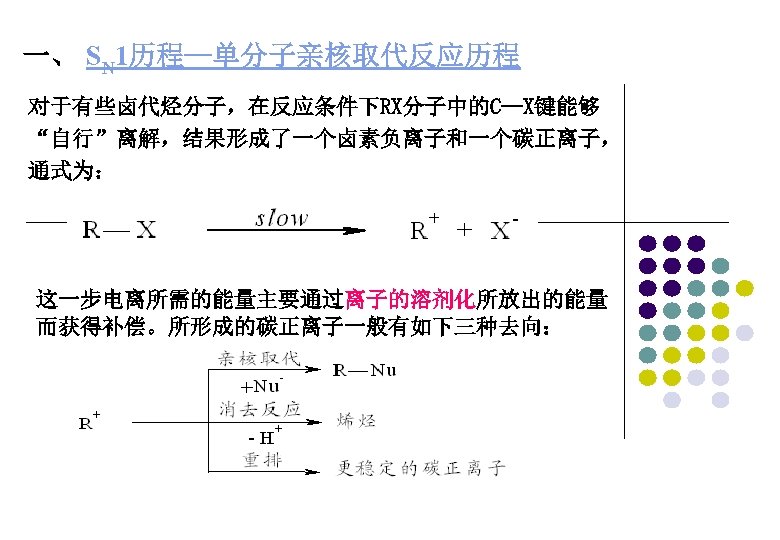
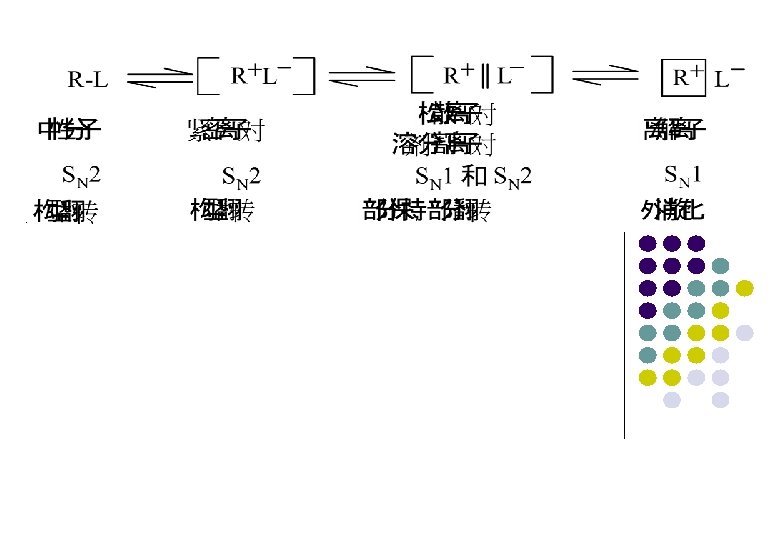
一、 SN 1历程—单分子亲核取代反应历程 对于有些卤代烃分子,在反应条件下RX分子中的C—X键能够 “自行”离解,结果形成了一个卤素负离子和一个碳正离子, 通式为: 这一步电离所需的能量主要通过离子的溶剂化所放出的能量 而获得补偿。所形成的碳正离子一般有如下三种去向:
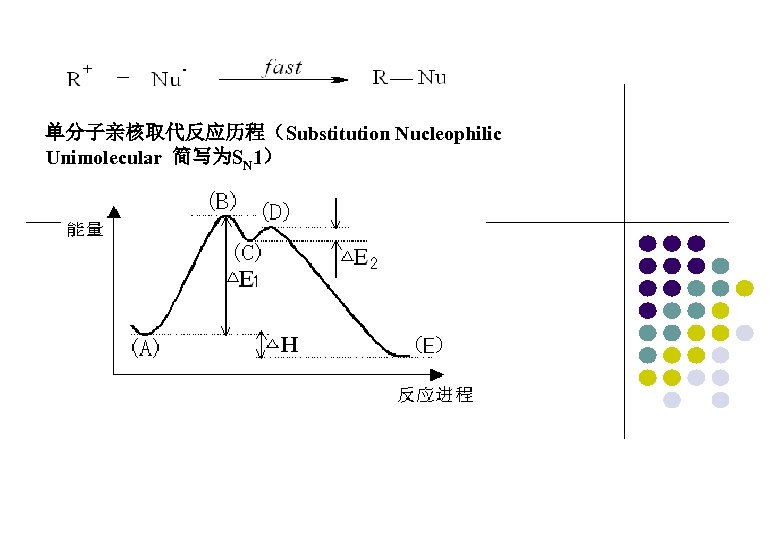
单分子亲核取代反应历程(Substitution Nucleophilic Unimolecular 简写为SN 1)

2 单分子亲核取代反应的特征 : (1) SN 1反应的动力学特征 反应速率只与卤代烃的浓度有关,与亲核试剂的浓度无关。反 应动力学对RX为一级反应,总反应也为一级反应。如:
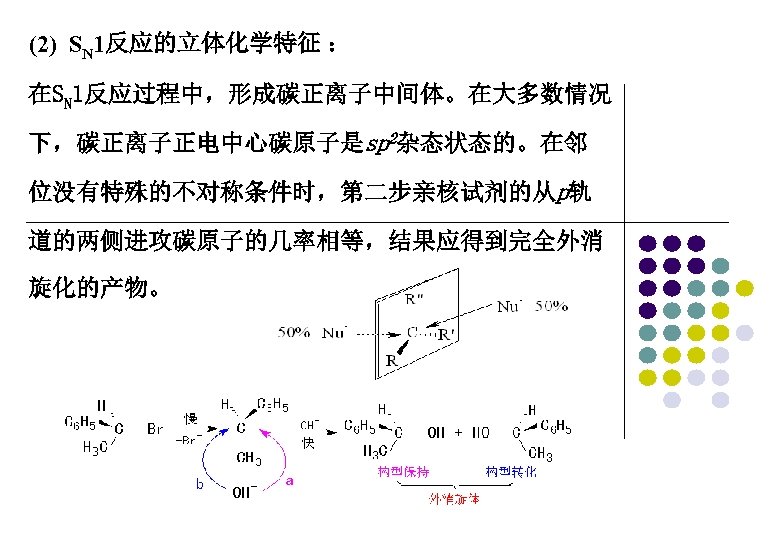
(2) SN 1反应的立体化学特征 : 在SN 1反应过程中,形成碳正离子中间体。在大多数情况 下,碳正离子正电中心碳原子是sp 2杂态状态的。在邻 位没有特殊的不对称条件时,第二步亲核试剂的从p轨 道的两侧进攻碳原子的几率相等,结果应得到完全外消 旋化的产物。
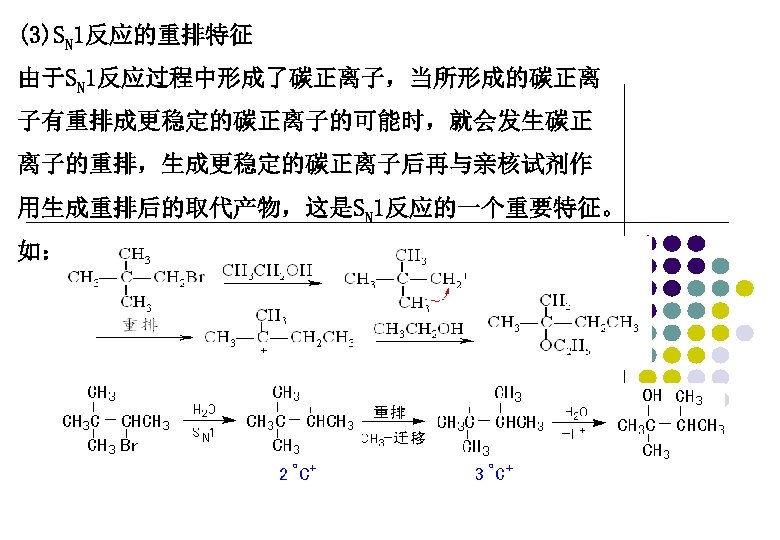
(3)SN 1反应的重排特征 由于SN 1反应过程中形成了碳正离子,当所形成的碳正离 子有重排成更稳定的碳正离子的可能时,就会发生碳正 离子的重排,生成更稳定的碳正离子后再与亲核试剂作 用生成重排后的取代产物,这是SN 1反应的一个重要特征。 如:
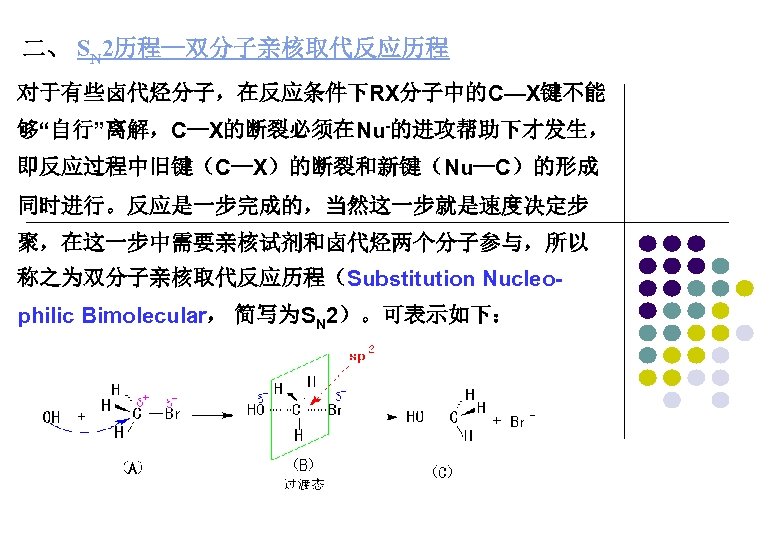
二、 SN 2历程—双分子亲核取代反应历程 对于有些卤代烃分子,在反应条件下RX分子中的C—X键不能 够“自行”离解,C—X的断裂必须在Nu-的进攻帮助下才发生, 即反应过程中旧键(C—X)的断裂和新键(Nu—C)的形成 同时进行。反应是一步完成的,当然这一步就是速度决定步 聚,在这一步中需要亲核试剂和卤代烃两个分子参与,所以 称之为双分子亲核取代反应历程(Substitution Nucleophilic Bimolecular, 简写为SN 2)。可表示如下:
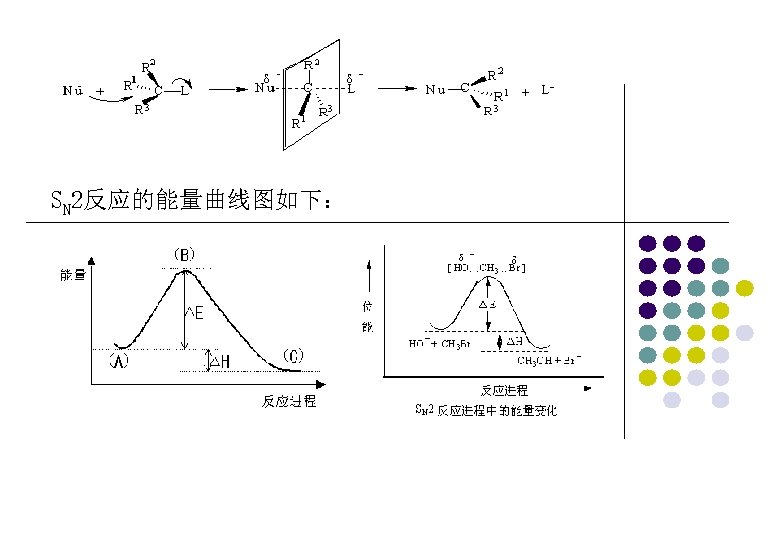
SN 2反应的能量曲线图如下:

双分子亲核取代反应的特征 : (1) SN 2反应的动力学特征 反应速度不仅与作用底物(卤代烃)的浓度有关,还与亲核 试剂的浓度有关,多数反应动力学对RX为一级反应,对Nu也是一级的,总反应为二级反应。例如:
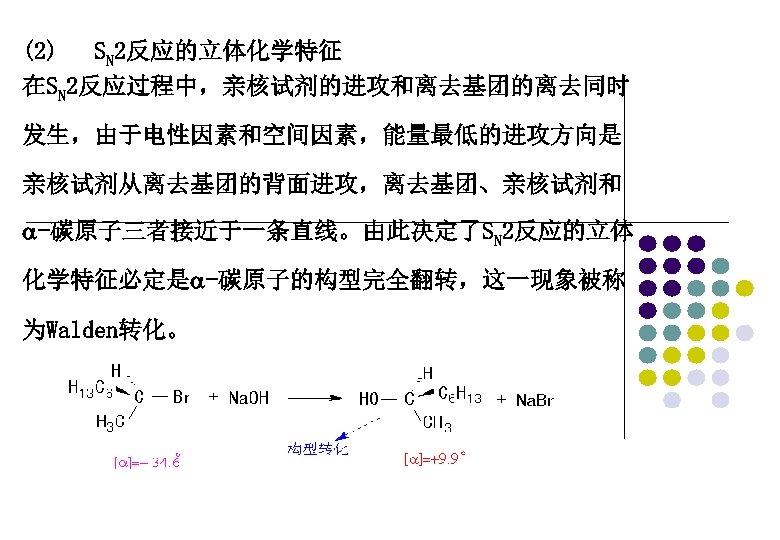
(2) SN 2反应的立体化学特征 在SN 2反应过程中,亲核试剂的进攻和离去基团的离去同时 发生,由于电性因素和空间因素,能量最低的进攻方向是 亲核试剂从离去基团的背面进攻,离去基团、亲核试剂和 -碳原子三者接近于一条直线。由此决定了SN 2反应的立体 化学特征必定是 -碳原子的构型完全翻转,这一现象被称 为Walden转化。
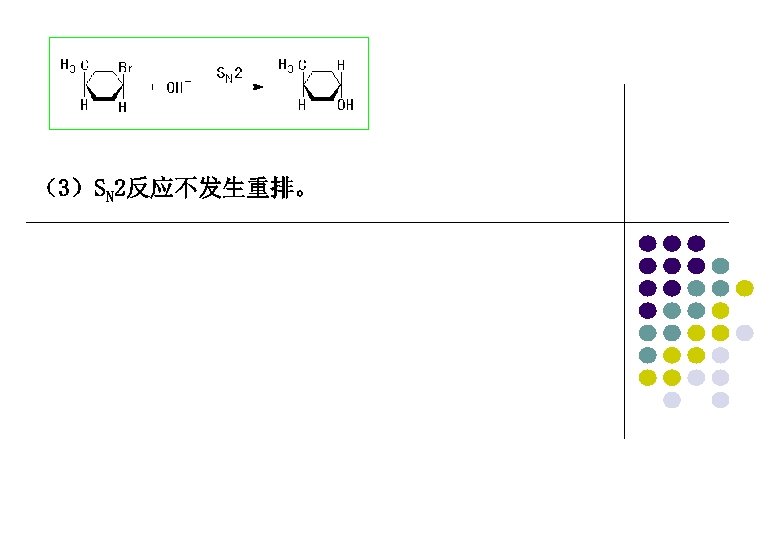
(3)SN 2反应不发生重排。
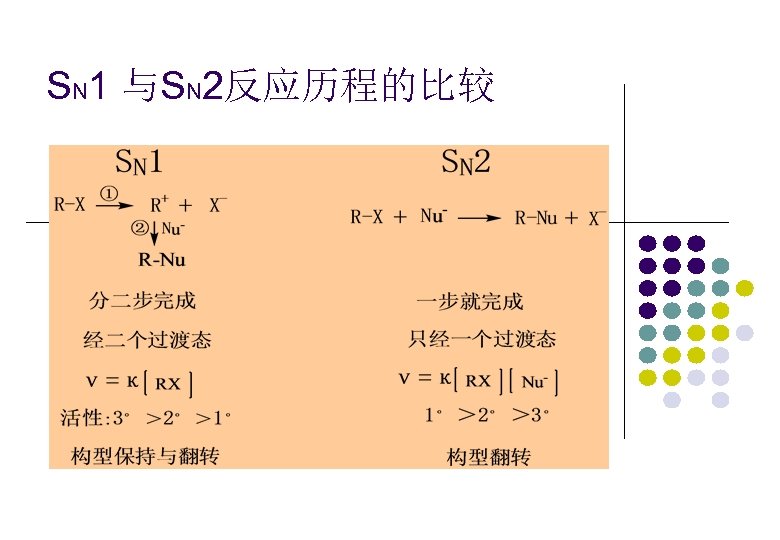
SN 1 与SN 2反应历程的比较
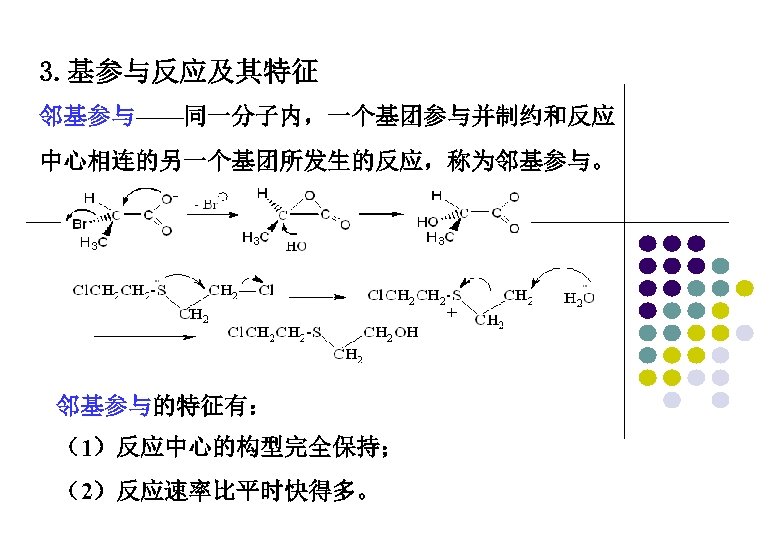
3. 基参与反应及其特征 邻基参与——同一分子内,一个基团参与并制约和反应 中心相连的另一个基团所发生的反应,称为邻基参与。 邻基参与的特征有: (1)反应中心的构型完全保持; (2)反应速率比平时快得多。
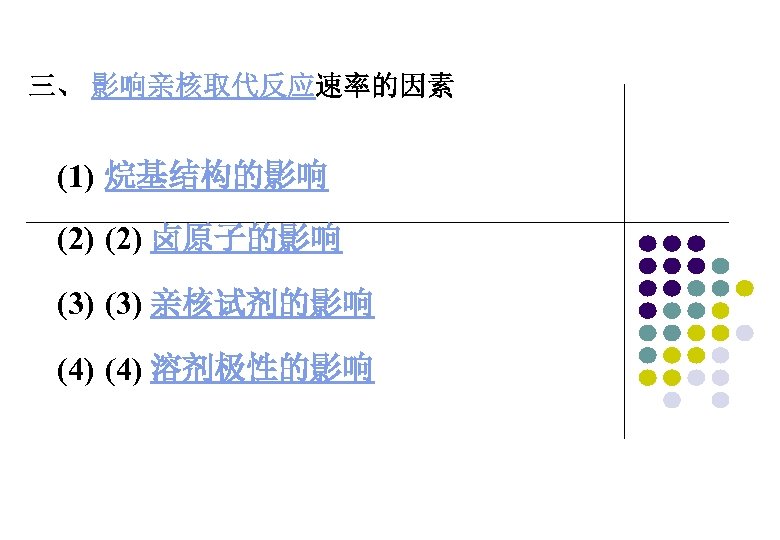
三、 影响亲核取代反应速率的因素 (1) 烷基结构的影响 (2) 卤原子的影响 (3) 亲核试剂的影响 (4) 溶剂极性的影响

1. 烷基结构的影响 (1) 烷基结构对SN 2反应的影响 决定SN 2反应速度的是过渡态的稳定性。过渡态越稳定, 反应所需的活化能越低,反应速度越快。 影响SN 2过渡态稳定性的因素关键是: 电子效应:α-C上所连的烃基越多,则α-C 上的电 子云密度越大,这样就越不利于亲核试剂的进攻。 空间效应: α-C上所连的烃基越多,则空间位 阻越大,亲核试剂越难靠近α-C ∴SN 2反应活性:CH 3 X> 1°RX> 2°RX> 3°RX

两组实验数据: ①在C 2 H 5 OH中,C 2 H 5 ONa与不同RBr于55℃发生SN 2反 应的 相对速率: 可见,α-C上取代基越大,空间障碍越大,SN 2速率越小。 ②在C 2 H 5 OH中,C 2 H 5 ONa与不同RBr于25℃发生SN 2反应 的相对速率: 可见,正构伯卤代烷进行SN 2反应时,碳链的增长对反应 速率的影响不大(即 碳以后的空间效应减弱)。
(2) 烷基结构对SN 1反应的影响 决定SN 1反应速度的是C+稳定性。越是稳定的C+,越容 易生成。 电子效应:α-C上所连的烃基越多,所形成的碳正离子越 稳定。 空间效应: 三级卤代烷中心碳连有三个烃基较拥挤,而 形成碳正离子后呈平面三角形,烃基间的距离增大,有利 于碳正离子的形成。 ∵C+稳定性:Ar. CH 2+>C=C-CH 2+>3°> 2°> 1°>CH 3+ ∴SN 1反应活性: Ar. CH 2+>C=C-CH 2+> 3°RX > 2°RX > 1°RX > CH 3 X
例如,在甲酸水溶液中,RBr的水解相对速度为: (CH 3)3 CBr>(CH 3)2 CHBr>CH 3 CH 2 Br>CH 3 Br 问题:(CH 3)3 CCH 2 Br(A)或(CH 3)3 CBr(B)在水-甲酸溶 液中何者水解速度快? (考虑C+稳定性) 答案:反应速度:B>A

(3)如被取代的基团连接在桥环化合物的桥头碳上, 则进行亲核取代反应时,不论是SN 1还是SN 2都难以进行。 综上所述: 即: 3°RX主要进行SN 1反应; 1°RX主要进行SN 2反应; 2°RX随条件不同而定。或SN 1 ,或SN 2 ,或两者均 有,但SN 1和SN 2速度都很慢。

2 卤原子(离去基团)的影响 SN 2和SN 1反应的慢步骤都包括C-X的断裂,因此离去基团X的性质对SN 2和SN 1反应将产生相似的影响。即: SN 1和SN 2反应活性:R-I>R-Br>R-Cl>R-F 由于SN 2反应中,参与形成过渡态的因素除了离去基团外,还有亲核试剂。 所以,离去基团的离去能力大小对SN 1反应的影响更为突出。 静态时,看R-L共价键的强弱;离去后,看L负离子的稳定性, 即离去基团的碱性(或共轭酸的酸性)、亲核性。 共轭酸酸性越大,离去能力越强!

离去能力:I->Br->Cl-;(酸性:HI>HBr>HCl) 好的离去基团:I-、p-CH 3 C 6 H 4 SO 3-; (HI、p-CH 3 C 6 H 4 SO 3 H均为强酸) 差的离去基团:OH-、RO-、NH 2-(H 2 O、ROH、NH 3 均为弱酸或碱) 碱性很强的基团不能作为离去基团。 (3) 亲核试剂的影响 亲核性——试剂亲碳原子核的能力;
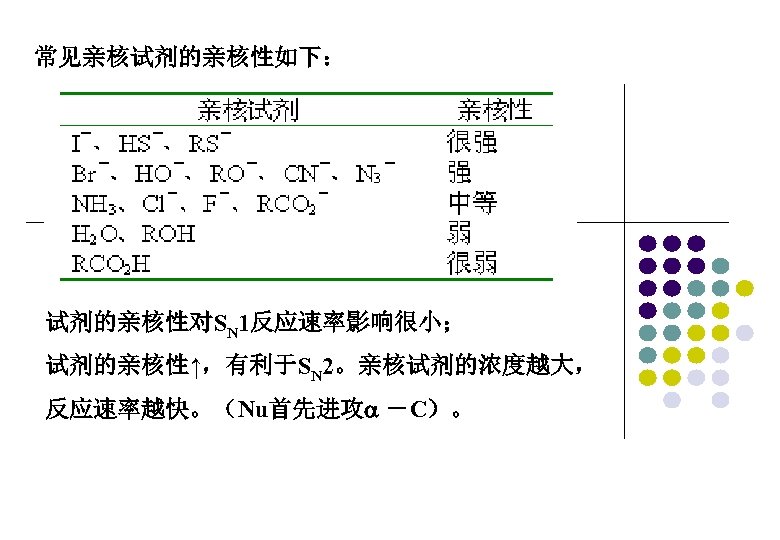
常见亲核试剂的亲核性如下: 试剂的亲核性对SN 1反应速率影响很小; 试剂的亲核性↑,有利于SN 2。亲核试剂的浓度越大, 反应速率越快。(Nu首先进攻 -C)。
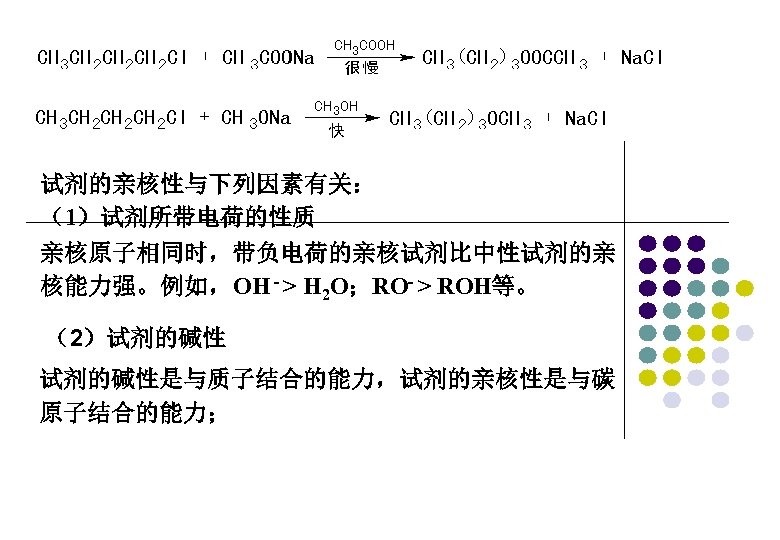
试剂的亲核性与下列因素有关: (1)试剂所带电荷的性质 亲核原子相同时,带负电荷的亲核试剂比中性试剂的亲 核能力强。例如,OH - > H 2 O;RO- > ROH等。 (2)试剂的碱性是与质子结合的能力,试剂的亲核性是与碳 原子结合的能力;
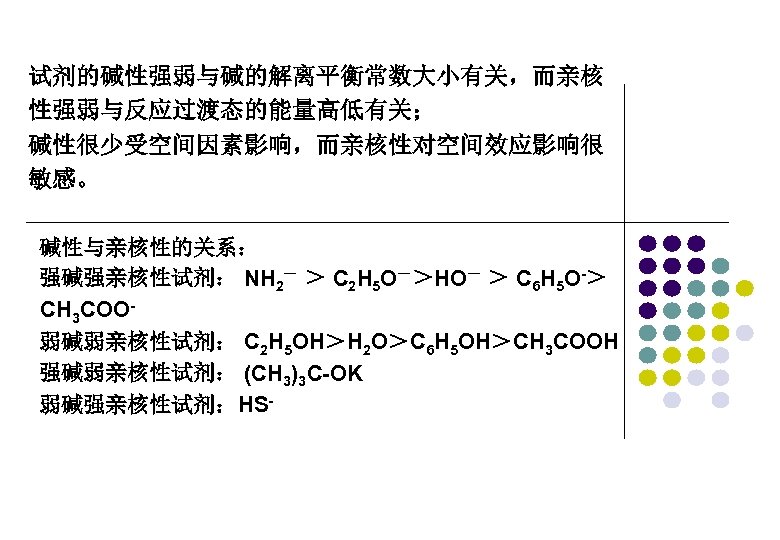
试剂的碱性强弱与碱的解离平衡常数大小有关,而亲核 性强弱与反应过渡态的能量高低有关; 碱性很少受空间因素影响,而亲核性对空间效应影响很 敏感。 碱性与亲核性的关系: 强碱强亲核性试剂: NH 2- > C 2 H 5 O->HO- > C 6 H 5 O-> CH 3 COO弱碱弱亲核性试剂: C 2 H 5 OH>H 2 O>C 6 H 5 OH>CH 3 COOH 强碱弱亲核性试剂: (CH 3)3 C-OK 弱碱强亲核性试剂:HS-

(3)溶剂对亲核性的影响 质子溶剂中,亲核试剂可与溶剂形成氢键,即发生溶剂 化作用,这样,削弱了亲核试剂与中心碳原子间的作用, 使其亲核性减弱: NH 2- >HO- >F - (同周期) RS - > RO - I - > Br - > Cl - > F - (同主族) 碱性相近的亲核试剂,其可极化性愈大,则亲核能力愈强。 试剂的亲核性主要由两个因素决定:碱性和极化度。这两 个因素对试剂亲核性的影响有时是一致的,有时不一致。 同一周期的原子作为亲核中心时,试剂的亲核性与碱性有 相同的强弱次序。
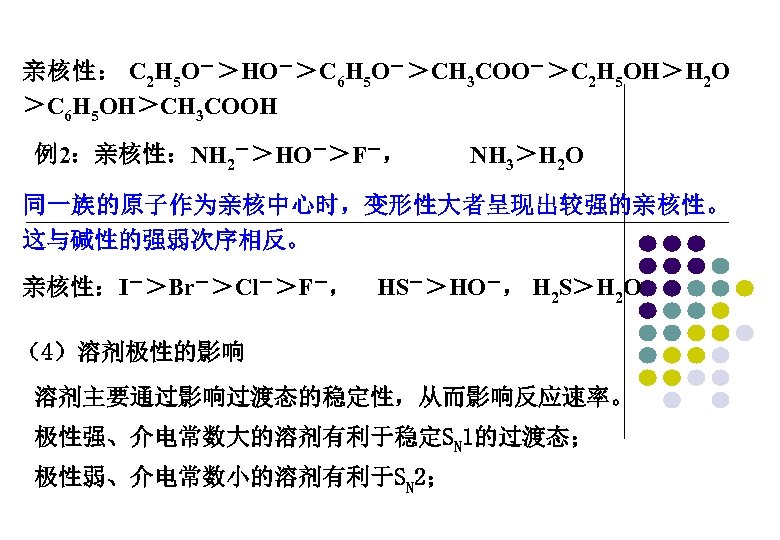
亲核性: C 2 H 5 O->HO->C 6 H 5 O->CH 3 COO->C 2 H 5 OH>H 2 O >C 6 H 5 OH>CH 3 COOH 例2:亲核性:NH 2->HO->F-, NH 3>H 2 O 同一族的原子作为亲核中心时,变形性大者呈现出较强的亲核性。 这与碱性的强弱次序相反。 亲核性:I->Br->Cl->F-, HS->HO-, H 2 S>H 2 O (4)溶剂极性的影响 溶剂主要通过影响过渡态的稳定性,从而影响反应速率。 极性强、介电常数大的溶剂有利于稳定SN 1的过渡态; 极性弱、介电常数小的溶剂有利于SN 2;
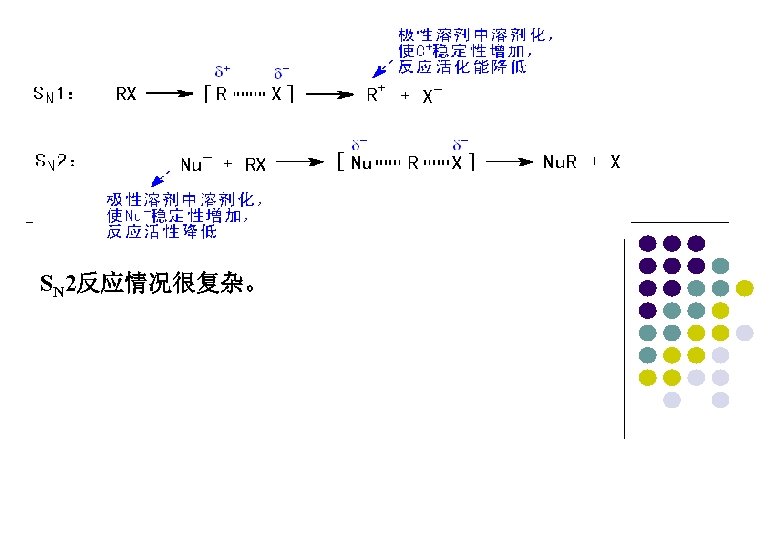
SN 2反应情况很复杂。
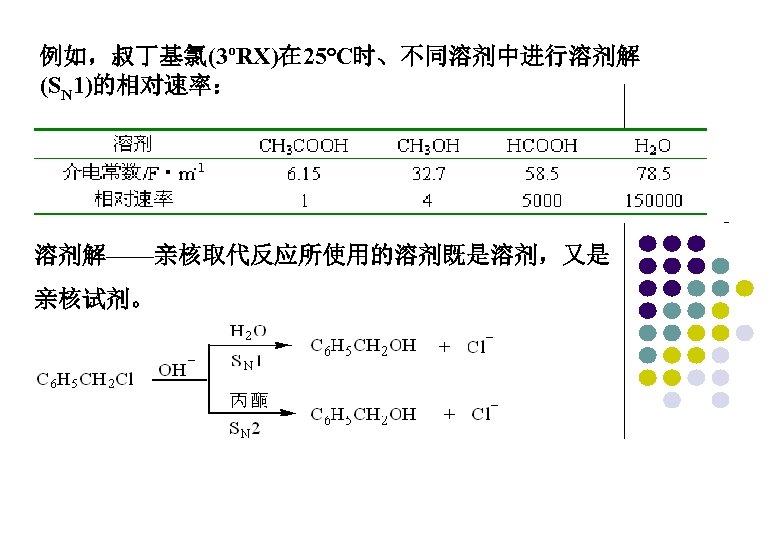
例如,叔丁基氯(3ºRX)在 25℃时、不同溶剂中进行溶剂解 (SN 1)的相对速率: 溶剂解——亲核取代反应所使用的溶剂既是溶剂,又是 亲核试剂。

四、 紧密离子对历程 1965年温斯顿 (S. Winstein)认为作用底物RL在溶液中 的离解是一个连续的过程。该过程可以分为尚未分离的 紧密离子对(Intimate ion-pair),此时发生的取代反应 与SN 2历程相当;溶剂分隔离子对(Solvent-separate ionpair),此时发生的取代反应则介于SN 1和SN 2之间;相对 自由的溶剂化正、负离子(Solvated ion),此时发生的 取代反应则与SN 1反应历程相当,实际上很多反应都是按 溶剂分隔离子对历程进行的介于SN 1和SN 2之间的反应。
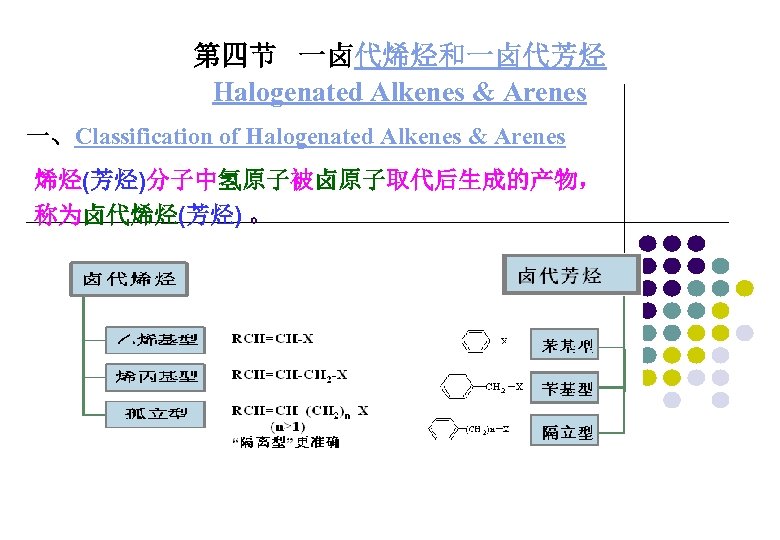
第四节 一卤代烯烃和一卤代芳烃 Halogenated Alkenes & Arenes 一、Classification of Halogenated Alkenes & Arenes 烯烃(芳烃)分子中氢原子被卤原子取代后生成的产物, 称为卤代烯烃(芳烃) 。
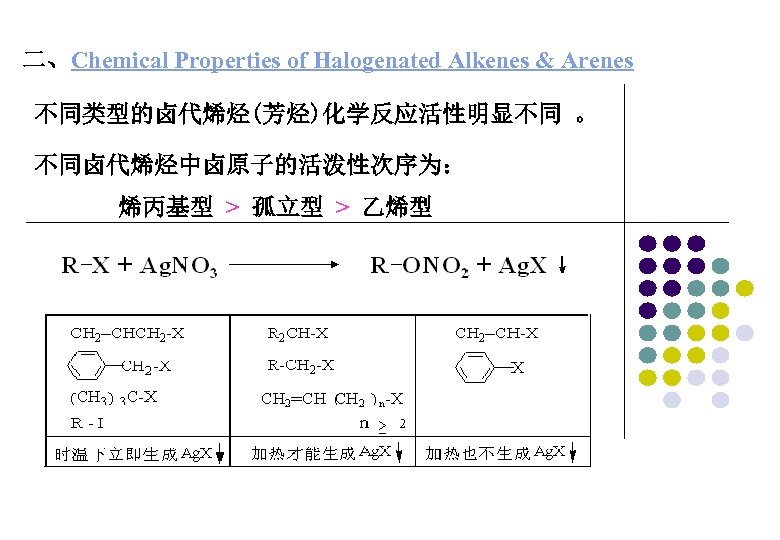
二、Chemical Properties of Halogenated Alkenes & Arenes 不同类型的卤代烯烃(芳烃)化学反应活性明显不同 。 不同卤代烯烃中卤原子的活泼性次序为: 烯丙基型 > 孤立型 > 乙烯型
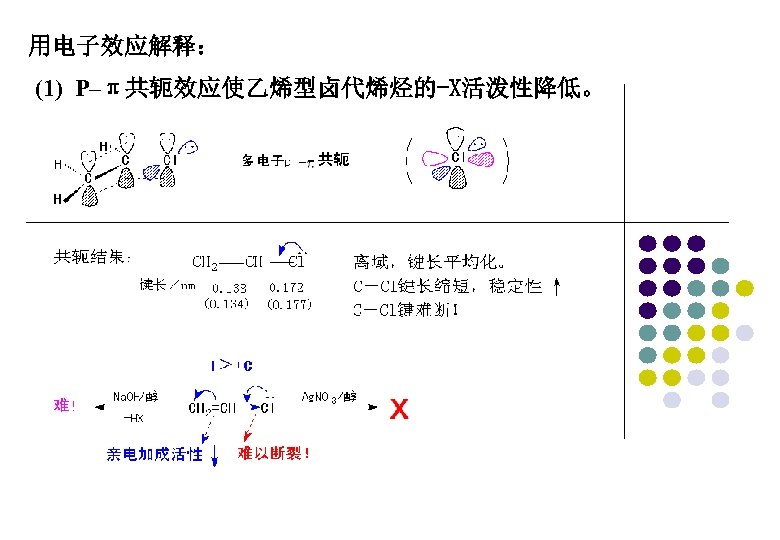
用电子效应解释: (1) P–π共轭效应使乙烯型卤代烯烃的-X活泼性降低。
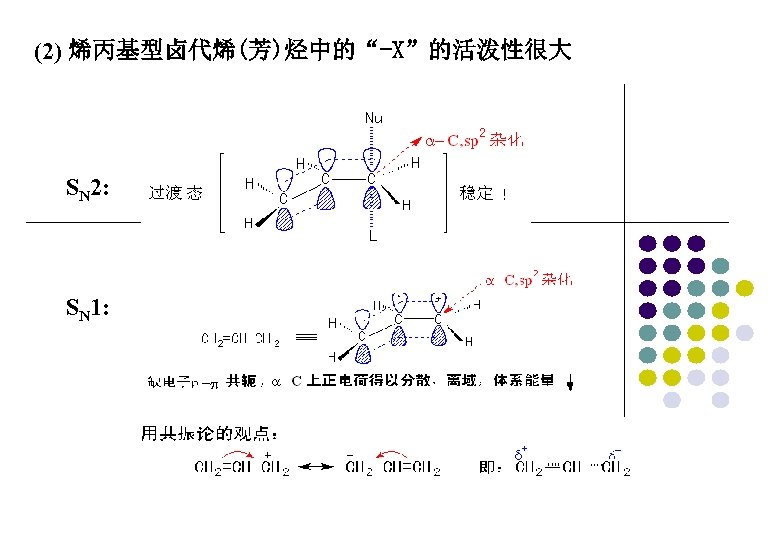
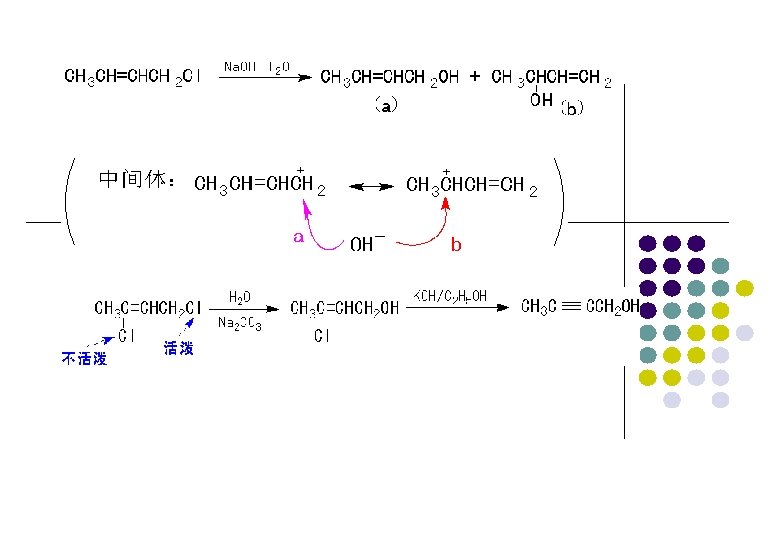
(2) 烯丙基型卤代烯(芳)烃中的“-X”的活泼性很大 SN 2: SN 1:
第五节 卤代烃的制法 Preparation of Alkyl Halides 卤代烃是烃及其衍生物之间的桥梁,在有机合成中占 有重要的地位。 一 、 由烃制备 二 、 从醇制备 三 、 卤原子交换
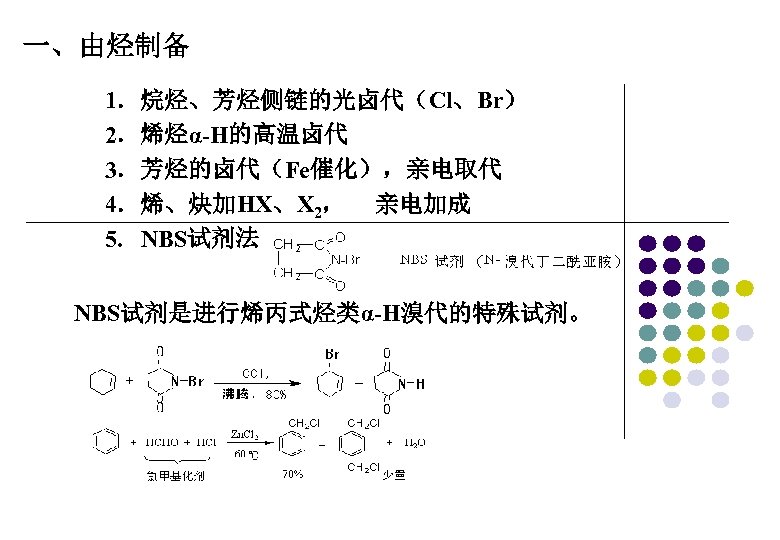
一、由烃制备 1.烷烃、芳烃侧链的光卤代(Cl、Br) 2.烯烃α-H的高温卤代 3.芳烃的卤代(Fe催化),亲电取代 4.烯、炔加HX、X 2, 亲电加成 5. NBS试剂法 NBS试剂是进行烯丙式烃类α-H溴代的特殊试剂。
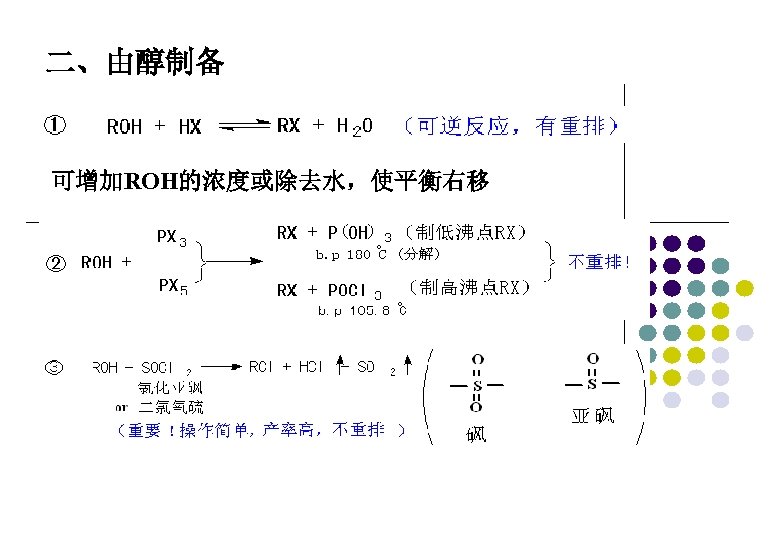
二、由醇制备 可增加ROH的浓度或除去水,使平衡右移
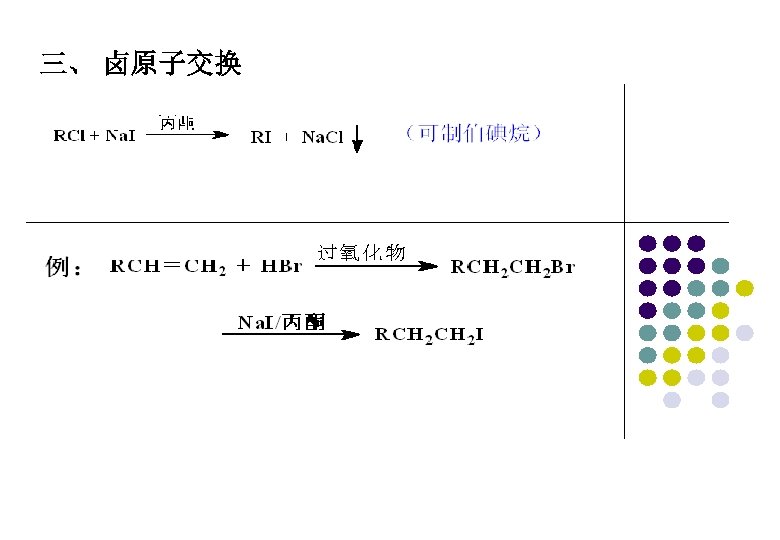
三、 卤原子交换

第六节 重要的卤代烃(自学) 第七节 有机氟化物 Organoflurorine Compounds 一、有机氟化合物具有特殊性质 1 氟原子的半径最小(H除外); 2 氟原子的电负性最大。 二、一氟代烷很不稳定,但不与Na、Mg等金属反应 容易自身分解失去HF,生成烯烃。

三、多氟代烷具有特殊的稳定性 当同一个碳上连有二个或二个以上的氟原子时,化 合物 稳定性很好,一般不容易发生各种化学反应,如:CF 4 CH 3 CHF 2 CH 3 CF 2 CH 3 等。 (1) 全氟代烷则特别稳定,因而有特殊用途。 (2) 全氟代烷特别稳定的原因: A. 因C—F键的键能很高,强度很大,而且C—F键 越多, 键的强度也越大。如: CH 3 F 447. 7 k. J/mol, CF 4 485. 3 k. J/mol B. B. 氟原子的半径小,在碳链外围正好形成了紧密的氟保 护套层,对内层碳起到了良好的屏蔽作用。
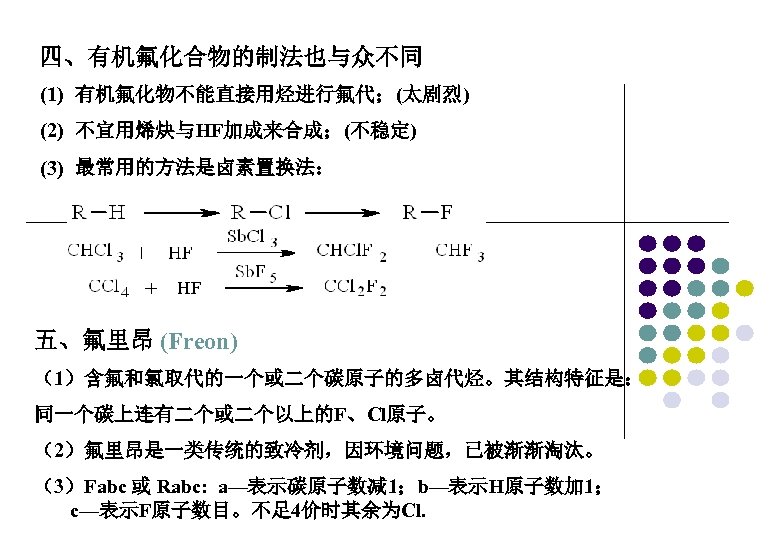
四、有机氟化合物的制法也与众不同 (1) 有机氟化物不能直接用烃进行氟代;(太剧烈) (2) 不宜用烯炔与HF加成来合成;(不稳定) (3) 最常用的方法是卤素置换法: 五、氟里昂 (Freon) (1)含氟和氯取代的一个或二个碳原子的多卤代烃。其结构特征是: 同一个碳上连有二个或二个以上的F、Cl原子。 (2)氟里昂是一类传统的致冷剂,因环境问题,已被渐渐淘汰。 (3)Fabc 或 Rabc: a—表示碳原子数减 1;b—表示H原子数加 1; c—表示F原子数目。不足 4价时其余为Cl.
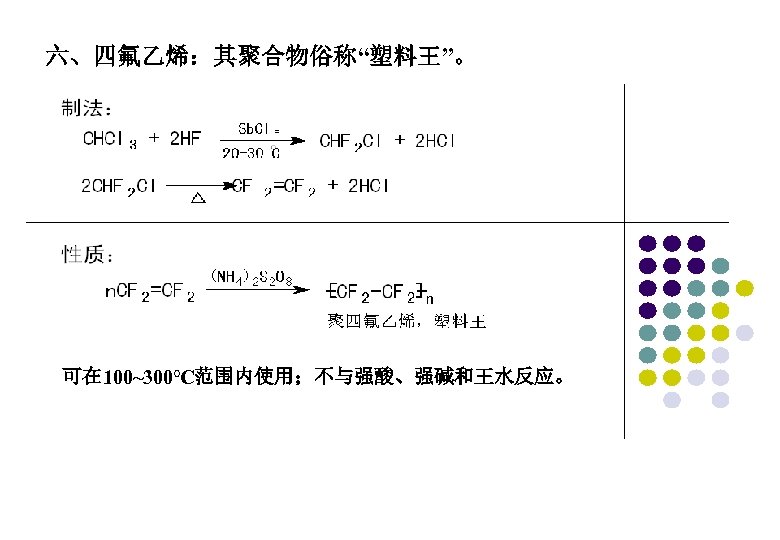
六、四氟乙烯:其聚合物俗称“塑料王”。 可在 100~300℃范围内使用;不与强酸、强碱和王水反应。
本章习题 P. 254 -258 第一次: 1. (3)(5)(6)(7) 5. 双 6. (2)(3) 17 26. (3) 本章内容学习完成 下一章:第十章 醇、酚、醚

ee248dc1b3afb326ffe1d6b54ec45b9b.ppt