• Ядерная ламина (30 -100 нм)



структра оболочки клеточного ядра и ядрышка.ppt
- Количество слайдов: 6
 • Ядерная ламина (30 -100 нм) представляет собой слой белков под внутренней ядерной мембраной и состоит из белков ламинов А-и В-типа и ряда интегральных белков внутренней ядерной мембраны, таких как рецептор ламина B (LBR), эмерин, а также различных изоформ ламин-связанных полипептидов 1 (LAP 1) и других белков • Молекулярная масса ламина A 74 к. Да, ламина В 67 к. Да, ламина C - в 65 к. Да. • Функция ламинов нарушена при ряде наследственных заболваний, например, мутации и вариации гена LMNA ассоциированы с мышечной дистрофией Эмери -Дрейфуса, связанной с потерей функции emerin-lamin A/C комплекса, семейной частичной липодистрофией, конечностно-поясной мышечной дистрофией, дилатационной кардиомиопатией, болезнью Шарко-Мари-Тута и синдромом прогерии Хатчинсона-Гилфорда. Синдром прогерии, исключительно редкое расстройство, вызывается синтезом ламина A неправильной формы, называемой прогерином. • It has been shown that lamin polypeptides have an affinity for binding chromatin through their α-helical (rod like) domains at specific DNA sequences called matrix attachment regions (MAR). A MAR has a length of approximately 300– 1000 bp and has a high A/T content. Lamin A and B can also bind core histones through a sequence element in their tail domain. • This nuclear breakdown is necessary to allow the mitotic spindle to interact with the (condensed) chromosomes and to bind them at their kinetochores. • These different disassembly events are initiated by the cyclin B/Cdk 1 protein kinase complex (MPF). Once this complex is activated, the cell is forced into mitosis, by the subsequent activation and regulation of other protein kinases or by direct phosphorylation of structural proteins involved in this cellular reorganisation. After phosphorylation by cyclin B/Cdk 1, the nuclear lamina depolymerises and B-type lamins stay associated with the fragments of the nuclear envelope whereas A-type lamins remain completely soluble throughout the remainder of the mitotic phase.
• Ядерная ламина (30 -100 нм) представляет собой слой белков под внутренней ядерной мембраной и состоит из белков ламинов А-и В-типа и ряда интегральных белков внутренней ядерной мембраны, таких как рецептор ламина B (LBR), эмерин, а также различных изоформ ламин-связанных полипептидов 1 (LAP 1) и других белков • Молекулярная масса ламина A 74 к. Да, ламина В 67 к. Да, ламина C - в 65 к. Да. • Функция ламинов нарушена при ряде наследственных заболваний, например, мутации и вариации гена LMNA ассоциированы с мышечной дистрофией Эмери -Дрейфуса, связанной с потерей функции emerin-lamin A/C комплекса, семейной частичной липодистрофией, конечностно-поясной мышечной дистрофией, дилатационной кардиомиопатией, болезнью Шарко-Мари-Тута и синдромом прогерии Хатчинсона-Гилфорда. Синдром прогерии, исключительно редкое расстройство, вызывается синтезом ламина A неправильной формы, называемой прогерином. • It has been shown that lamin polypeptides have an affinity for binding chromatin through their α-helical (rod like) domains at specific DNA sequences called matrix attachment regions (MAR). A MAR has a length of approximately 300– 1000 bp and has a high A/T content. Lamin A and B can also bind core histones through a sequence element in their tail domain. • This nuclear breakdown is necessary to allow the mitotic spindle to interact with the (condensed) chromosomes and to bind them at their kinetochores. • These different disassembly events are initiated by the cyclin B/Cdk 1 protein kinase complex (MPF). Once this complex is activated, the cell is forced into mitosis, by the subsequent activation and regulation of other protein kinases or by direct phosphorylation of structural proteins involved in this cellular reorganisation. After phosphorylation by cyclin B/Cdk 1, the nuclear lamina depolymerises and B-type lamins stay associated with the fragments of the nuclear envelope whereas A-type lamins remain completely soluble throughout the remainder of the mitotic phase.
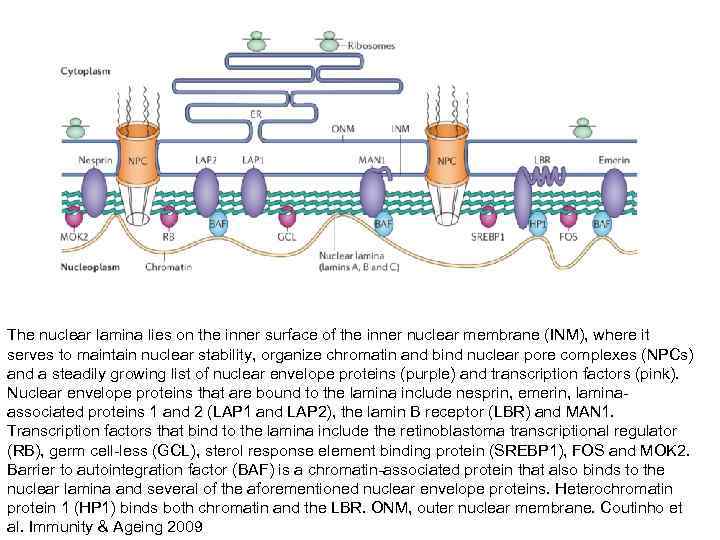
 The nuclear lamina lies on the inner surface of the inner nuclear membrane (INM), where it serves to maintain nuclear stability, organize chromatin and bind nuclear pore complexes (NPCs) and a steadily growing list of nuclear envelope proteins (purple) and transcription factors (pink). Nuclear envelope proteins that are bound to the lamina include nesprin, emerin, lamina- associated proteins 1 and 2 (LAP 1 and LAP 2), the lamin B receptor (LBR) and MAN 1. Transcription factors that bind to the lamina include the retinoblastoma transcriptional regulator (RB), germ cell-less (GCL), sterol response element binding protein (SREBP 1), FOS and MOK 2. Barrier to autointegration factor (BAF) is a chromatin-associated protein that also binds to the nuclear lamina and several of the aforementioned nuclear envelope proteins. Heterochromatin protein 1 (HP 1) binds both chromatin and the LBR. ONM, outer nuclear membrane. Coutinho et al. Immunity & Ageing 2009
The nuclear lamina lies on the inner surface of the inner nuclear membrane (INM), where it serves to maintain nuclear stability, organize chromatin and bind nuclear pore complexes (NPCs) and a steadily growing list of nuclear envelope proteins (purple) and transcription factors (pink). Nuclear envelope proteins that are bound to the lamina include nesprin, emerin, lamina- associated proteins 1 and 2 (LAP 1 and LAP 2), the lamin B receptor (LBR) and MAN 1. Transcription factors that bind to the lamina include the retinoblastoma transcriptional regulator (RB), germ cell-less (GCL), sterol response element binding protein (SREBP 1), FOS and MOK 2. Barrier to autointegration factor (BAF) is a chromatin-associated protein that also binds to the nuclear lamina and several of the aforementioned nuclear envelope proteins. Heterochromatin protein 1 (HP 1) binds both chromatin and the LBR. ONM, outer nuclear membrane. Coutinho et al. Immunity & Ageing 2009
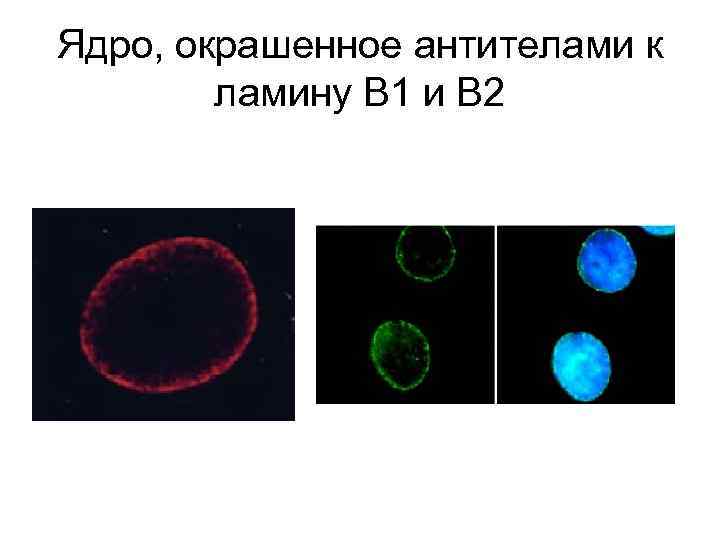
 Ядро, окрашенное антителами к ламину В 1 и В 2
Ядро, окрашенное антителами к ламину В 1 и В 2
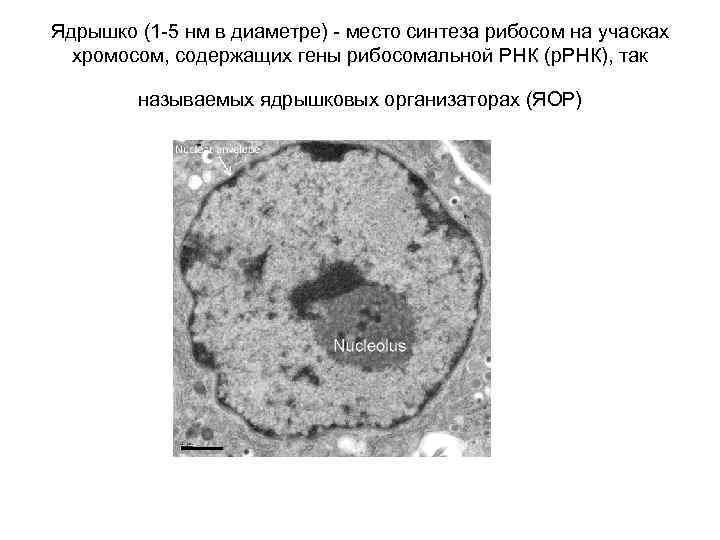
 Ядрышко (1 -5 нм в диаметре) - место синтеза рибосом на учасках хромосом, содержащих гены рибосомальной РНК (р. РНК), так называемых ядрышковых организаторах (ЯОР)
Ядрышко (1 -5 нм в диаметре) - место синтеза рибосом на учасках хромосом, содержащих гены рибосомальной РНК (р. РНК), так называемых ядрышковых организаторах (ЯОР)
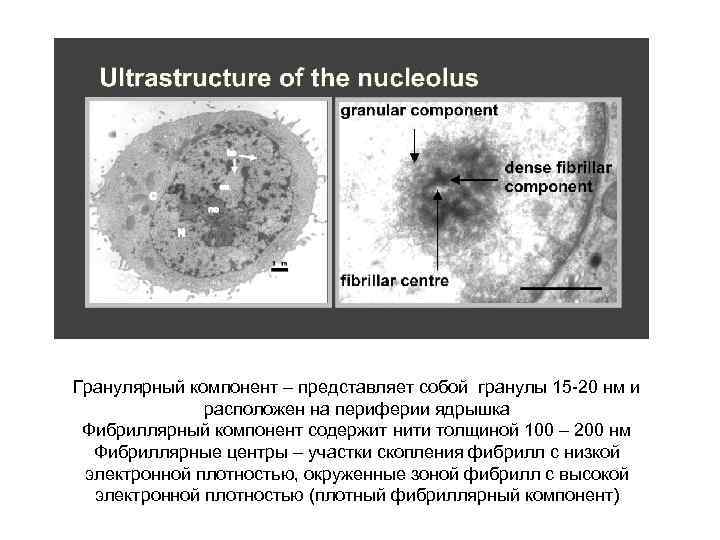
 Гранулярный компонент – представляет собой гранулы 15 -20 нм и расположен на периферии ядрышка Фибриллярный компонент содержит нити толщиной 100 – 200 нм Фибриллярные центры – участки скопления фибрилл с низкой электронной плотностью, окруженные зоной фибрилл с высокой электронной плотностью (плотный фибриллярный компонент)
Гранулярный компонент – представляет собой гранулы 15 -20 нм и расположен на периферии ядрышка Фибриллярный компонент содержит нити толщиной 100 – 200 нм Фибриллярные центры – участки скопления фибрилл с низкой электронной плотностью, окруженные зоной фибрилл с высокой электронной плотностью (плотный фибриллярный компонент)
 • У человека гены, кодирующие р. РНК, также организованы в группы тандемных повторов, расположенных в центральных областях короткого плеча 13, 14, 15, 21 и 22 -й хромосом. • 80 S рибосома эукариот состоит из большой 60 S субъединицы (построенной на основе трех молекул р. РНК — 5 S, 5, 8 S и 28 S) и малой 40 S субъединицы (построенной на основе 18 S р. РНК). • У эукариот 18 S, 5. 8 S и 25/28 р. РНК ко- транскрибируются РНК-полимеразой I, в то время как ген 5 S р. РНК транскибируется РНК- полимеразой III.
• У человека гены, кодирующие р. РНК, также организованы в группы тандемных повторов, расположенных в центральных областях короткого плеча 13, 14, 15, 21 и 22 -й хромосом. • 80 S рибосома эукариот состоит из большой 60 S субъединицы (построенной на основе трех молекул р. РНК — 5 S, 5, 8 S и 28 S) и малой 40 S субъединицы (построенной на основе 18 S р. РНК). • У эукариот 18 S, 5. 8 S и 25/28 р. РНК ко- транскрибируются РНК-полимеразой I, в то время как ген 5 S р. РНК транскибируется РНК- полимеразой III.

