 • Сущность гидролиза сводится к обменному химическому (протолитическому) взаимодействию катионов или анионов соединения с молекулами воды. В результате образуется слабый электролит – сопряженные кислота или основание. • Любая соль – это продукт взаимодействия основания с кислотой. В зависимости от силы основания и кислоты выделяют 4 типа солей.
• Сущность гидролиза сводится к обменному химическому (протолитическому) взаимодействию катионов или анионов соединения с молекулами воды. В результате образуется слабый электролит – сопряженные кислота или основание. • Любая соль – это продукт взаимодействия основания с кислотой. В зависимости от силы основания и кислоты выделяют 4 типа солей.
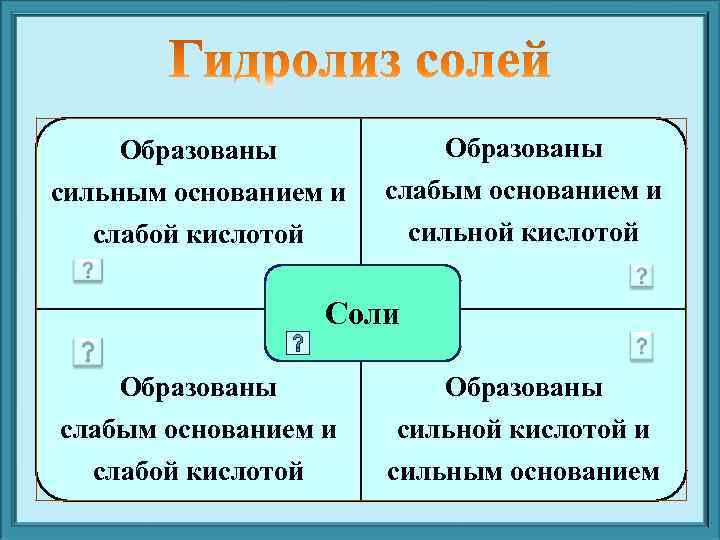 Образованы сильным основанием и слабой кислотой сильной кислотой Соли Образованы слабым основанием и сильной кислотой и слабой кислотой сильным основанием
Образованы сильным основанием и слабой кислотой сильной кислотой Соли Образованы слабым основанием и сильной кислотой и слабой кислотой сильным основанием
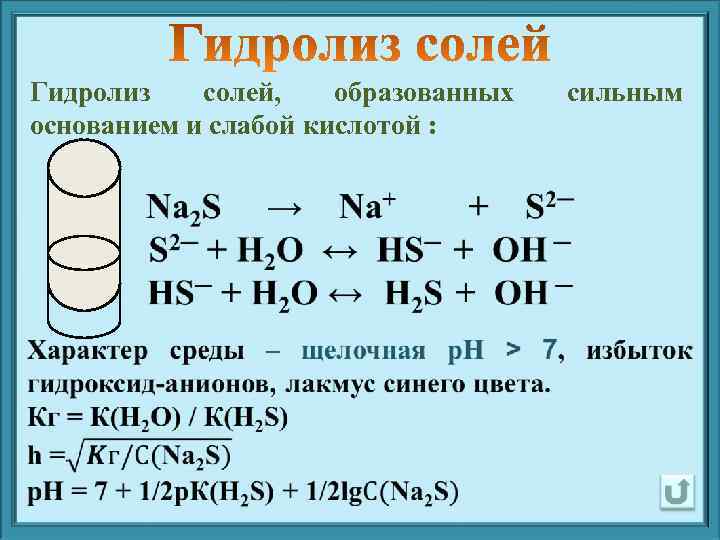 Гидролиз солей, образованных сильным основанием и слабой кислотой :
Гидролиз солей, образованных сильным основанием и слабой кислотой :
 Гидролиз солей, образованных слабым основанием и сильной кислотой: •
Гидролиз солей, образованных слабым основанием и сильной кислотой: •
 Гидролиз солей, образованных слабым основанием и слабой кислотой: •
Гидролиз солей, образованных слабым основанием и слабой кислотой: •
 Необратимый гидролиз солей, образованных слабым основанием и слабой кислотой: Например, соли, которые нельзя получить реакцией обмена между водными растворами двух солей (разлагаются в водной среде) Fe 2(CO 3)3 2 Fe. Cl 3 + 3 Na 2 CO 3 + 3 H 2 O =2 Fe(OH)3↓ +3 CO 2↑+ 6 Na. Cl Fe 2(CO 3)3 + 3 H 2 O = 2 Fe(OH)3↓ +3 CO 2↑ Реакция между двумя растворами ( Fe. Cl 3 и Na 2 CO 3 ) буде необратимой, а карбонат железа (+3) не образуется.
Необратимый гидролиз солей, образованных слабым основанием и слабой кислотой: Например, соли, которые нельзя получить реакцией обмена между водными растворами двух солей (разлагаются в водной среде) Fe 2(CO 3)3 2 Fe. Cl 3 + 3 Na 2 CO 3 + 3 H 2 O =2 Fe(OH)3↓ +3 CO 2↑+ 6 Na. Cl Fe 2(CO 3)3 + 3 H 2 O = 2 Fe(OH)3↓ +3 CO 2↑ Реакция между двумя растворами ( Fe. Cl 3 и Na 2 CO 3 ) буде необратимой, а карбонат железа (+3) не образуется.
 Гидролиз солей, образованных сильным основанием и сильной кислотой: KCl = K+ + Cl− Слабых ионов нет, гидролиз не идет, среда нейтральная, лакмус фиолетового цвета
Гидролиз солей, образованных сильным основанием и сильной кислотой: KCl = K+ + Cl− Слабых ионов нет, гидролиз не идет, среда нейтральная, лакмус фиолетового цвета
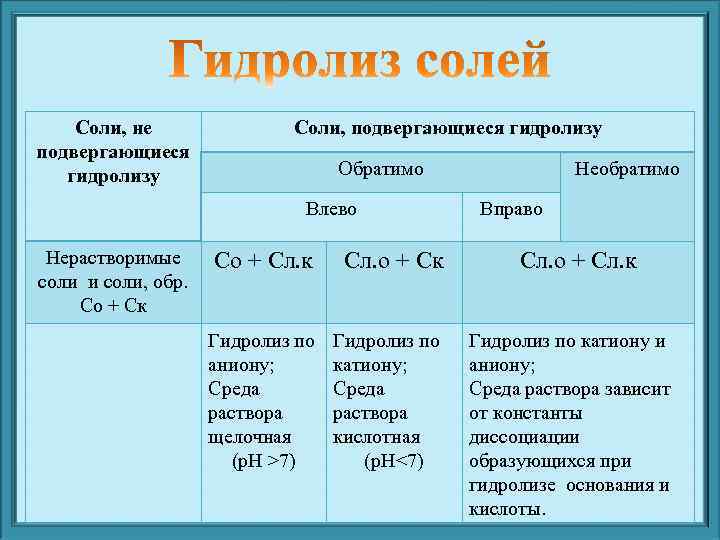 Соли, не Соли, подвергающиеся гидролизу подвергающиеся гидролизу Обратимо Необратимо Влево Вправо Нерастворимые Со + Сл. к Сл. о + Ск Сл. о + Сл. к соли и соли, обр. Со + Ск Гидролиз по катиону и аниону; катиону; аниону; Среда раствора зависит раствора от константы щелочная кислотная диссоциации (р. Н >7) (р. Н<7) образующихся при гидролизе основания и кислоты.
Соли, не Соли, подвергающиеся гидролизу подвергающиеся гидролизу Обратимо Необратимо Влево Вправо Нерастворимые Со + Сл. к Сл. о + Ск Сл. о + Сл. к соли и соли, обр. Со + Ск Гидролиз по катиону и аниону; катиону; аниону; Среда раствора зависит раствора от константы щелочная кислотная диссоциации (р. Н >7) (р. Н<7) образующихся при гидролизе основания и кислоты.
 Условия смещения реакций обратимого гидролиза (согласно принципу Ле Шателье). Усилить гидролиз соли можно следующими способами: 1. Добавить воды (уменьшить концентрацию раствора); 2. Нагреть раствор; 3. Связать один из продуктов гидролиза в труднорастворимое соединение или удалить один из продуктов в газовую фазу.
Условия смещения реакций обратимого гидролиза (согласно принципу Ле Шателье). Усилить гидролиз соли можно следующими способами: 1. Добавить воды (уменьшить концентрацию раствора); 2. Нагреть раствор; 3. Связать один из продуктов гидролиза в труднорастворимое соединение или удалить один из продуктов в газовую фазу.
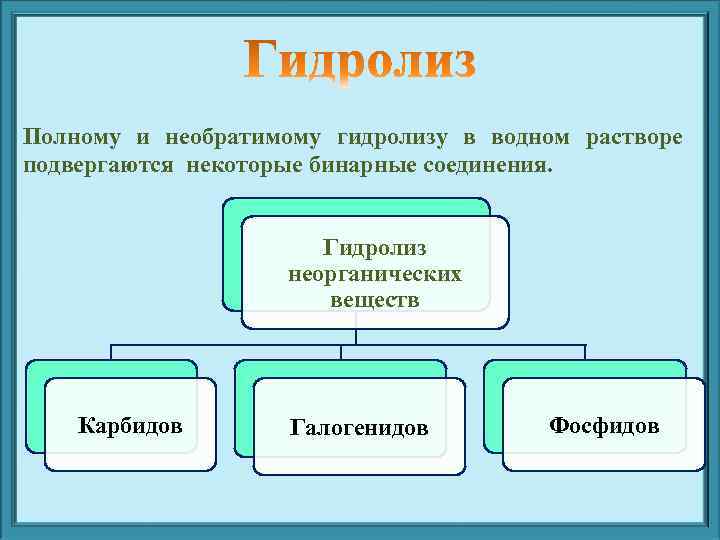 Полному и необратимому гидролизу в водном растворе подвергаются некоторые бинарные соединения. Гидролиз неорганических веществ Карбидов Галогенидов Фосфидов
Полному и необратимому гидролизу в водном растворе подвергаются некоторые бинарные соединения. Гидролиз неорганических веществ Карбидов Галогенидов Фосфидов
 Гидролиз карбидов: Ca. C 2 + 2 H 2 O = Ca(OH)2 + C 2 H 2↑ Карбид ацетилен кальция Al 4 C 3 + 12 H 2 O = 4 Al(OH)3 + 3 CH 4↑ Карбид метан алюминия
Гидролиз карбидов: Ca. C 2 + 2 H 2 O = Ca(OH)2 + C 2 H 2↑ Карбид ацетилен кальция Al 4 C 3 + 12 H 2 O = 4 Al(OH)3 + 3 CH 4↑ Карбид метан алюминия
 Гидролиз галогенидов: Si. Cl 4 + 3 H 2 O = H 2 Si. O 4↓ + 4 HСl хлорид кремния (+4) Гидролиз фосфидов: Са 3 P 2 + 6 H 2 O = 3 Са(OH)2 + 2 PH 3↑ фосфид фосфин кальция
Гидролиз галогенидов: Si. Cl 4 + 3 H 2 O = H 2 Si. O 4↓ + 4 HСl хлорид кремния (+4) Гидролиз фосфидов: Са 3 P 2 + 6 H 2 O = 3 Са(OH)2 + 2 PH 3↑ фосфид фосфин кальция
