53b88590e2cf5219882ab24062b4c814.ppt
- Количество слайдов: 155

מבוא לייצור יין: מושגי יסוד בכימיה מרצה: דינה דנה אנליטיקאית מו"פ – טבע תעשיות פרמצבטיות 1

: מטרת ההרצאה הקנית ידע בסיסי בכימיה כבסיס להבנת כימיית היין CERTIFICATE OF ANALYSIS CABERNET SAUVIGNON Reserve 2003 – Dry Red Wine 1 Actual Alcohol Content by Vol (20 C) 13. 8 % 2 Specific Gravity D 20/20 0. 9931 3 Total Sugars (As Reducing sugars) 1. 1 g/l 4 Sucrose None 5 Total Dry Extract 28. 7 g/l 6 Total Acidity as Tartaric Acid (72. 6 meq/l) 5. 45 g/l 7 Volatile Acidity as Acetic Acid (6. 3 meq/l) 0. 38 g/l 8 Total SO 2 106 mg/l 9 Sorbic Acid 10 Citric Acid None 11 p. H 2 None 3. 67

CERTIFICATE OF ANALYSIS CABERNET SAUVIGNON Reserve 2003 – Dry Red Wine 1 Actual Alcohol Content by Vol (20 C) 13. 8 % 2 Specific Gravity D 20/20 0. 9931 3 Total Sugars (As Reducing sugars) 1. 1 g/l 4 Sucrose None 5 Total Dry Extract 28. 7 g/l 6 Total Acidity as Tartaric Acid (72. 6 meq/l) 5. 45 g/l 7 Volatile Acidity as Acetic Acid (6. 3 meq/l) 0. 38 g/l 8 Total SO 2 106 mg/l 9 Sorbic Acid 10 Citric Acid None 11 p. H 3 None 3. 67

הנושאים: הרכב החומר הכרת האטום ודרך פעולתו הטבלה המחזורית קשרים כימיים מצבי צבירה תמיסות חומציות ו- p. H מבוא לכימיה אורגנית 4

כיצד בנויים חומרים? 5

כיצד בנויים חומרים? חוק שימור החומר: חומרים אינם נעלמים ואינם נוצרים יש מאין! 6
כיצד בנויים חומרים? חוק שימור החומר: חומרים אינם נעלמים ואינם נוצרים יש מאין! אז ממה הם מורכבים? 7

כיום, המודל המקובל במדע הוא: המודל החלקיקי כל אינסוף החומרים בעולמנו מורכבים ממספר קטן יחסית של יסודות )~001( 8

כיום, המודל המקובל במדע הוא: המודל החלקיקי כל אינסוף החומרים בעולמנו מורכבים ממספר קטן יחסית של יסודות )~001( אבני הבניין הבסיסיות של היסודות הם האטומים אטום = החלקיק הקטן ביותר של היסוד שמעורב בתהליכים כימיים 9

נתחיל מאבני היסוד. . . אטום 01
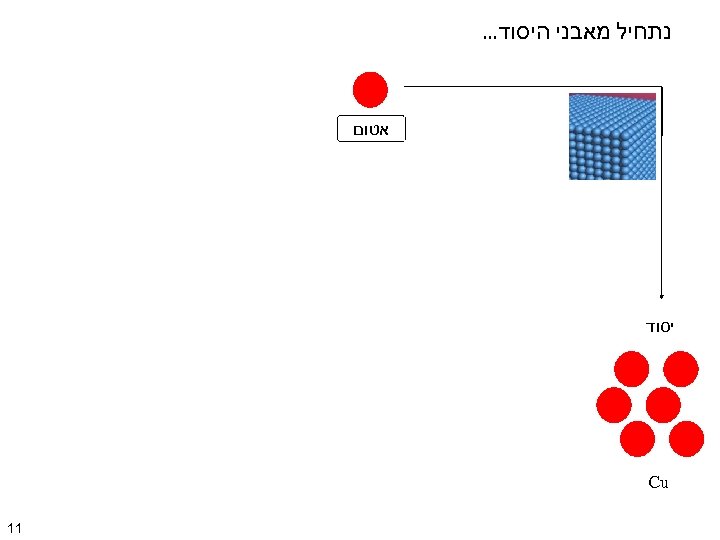
נתחיל מאבני היסוד. . . אטום יסוד Cu 11
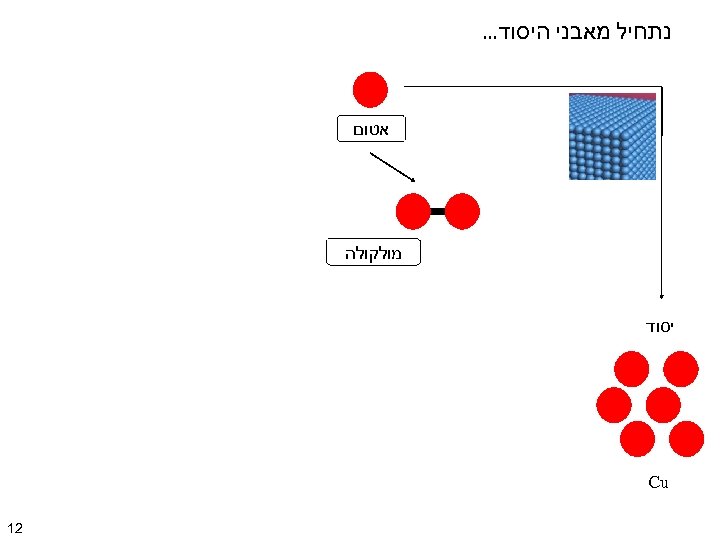
נתחיל מאבני היסוד. . . אטום מולקולה יסוד Cu 21
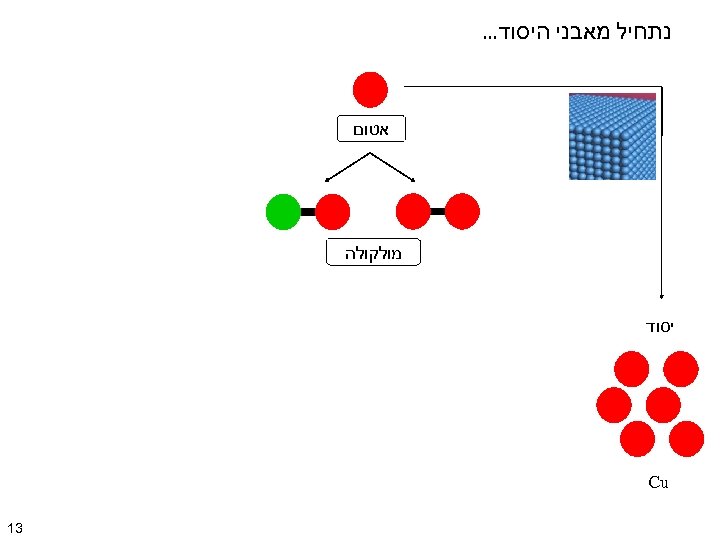
נתחיל מאבני היסוד. . . אטום מולקולה יסוד Cu 31
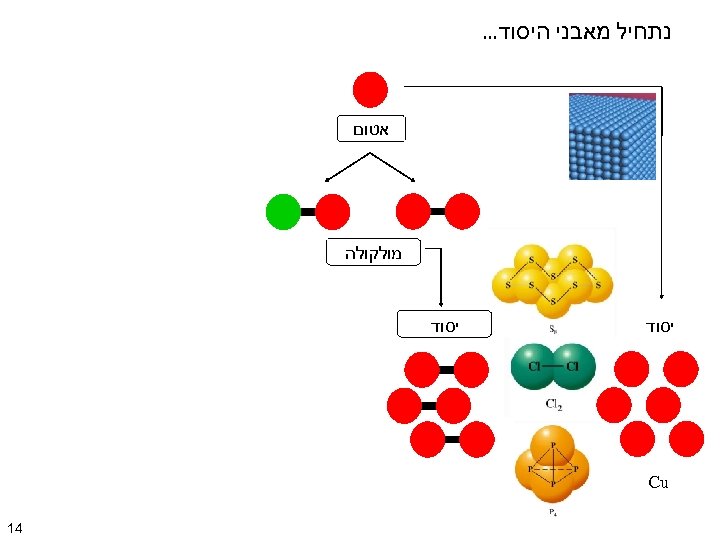
נתחיל מאבני היסוד. . . אטום מולקולה יסוד Cu 41
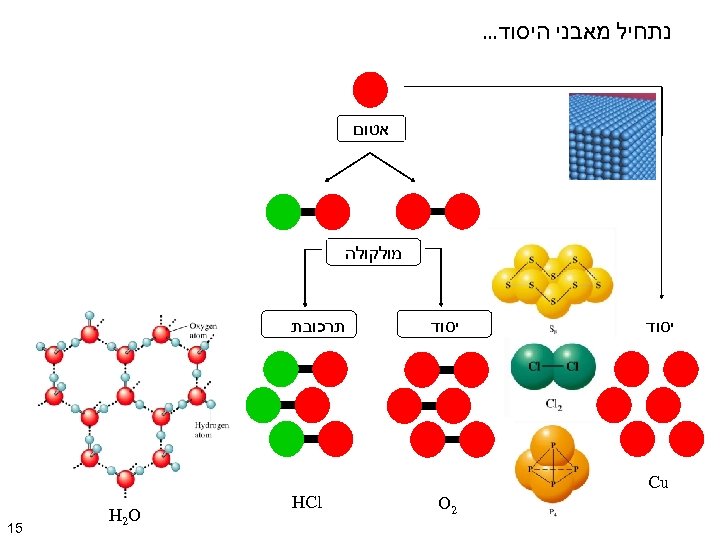
נתחיל מאבני היסוד. . . אטום מולקולה יסוד תרכובת Cu 2 O HCl H 2 O 51
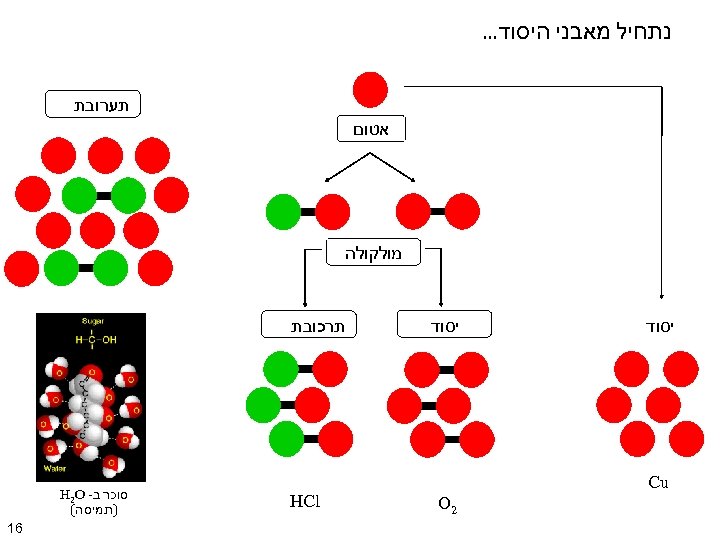
נתחיל מאבני היסוד. . . תערובת אטום מולקולה יסוד Cu 2 O תרכובת HCl סוכר ב- H 2 O )תמיסה( 61
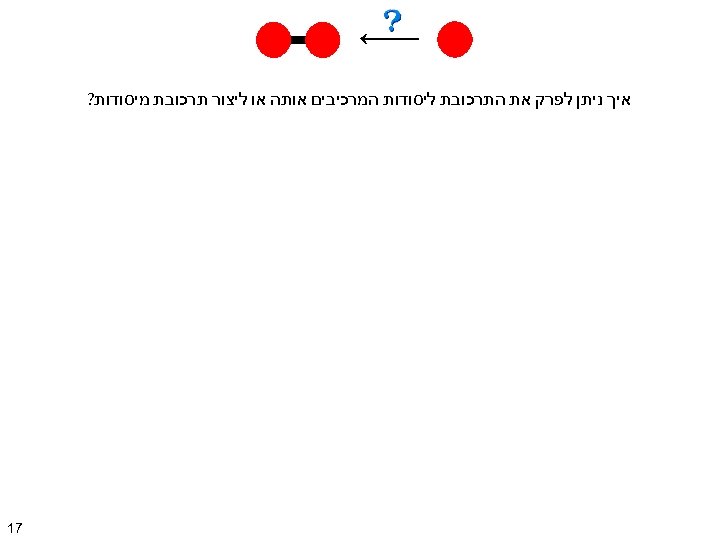
איך ניתן לפרק את התרכובת ליסודות המרכיבים אותה או ליצור תרכובת מיסודות? 71
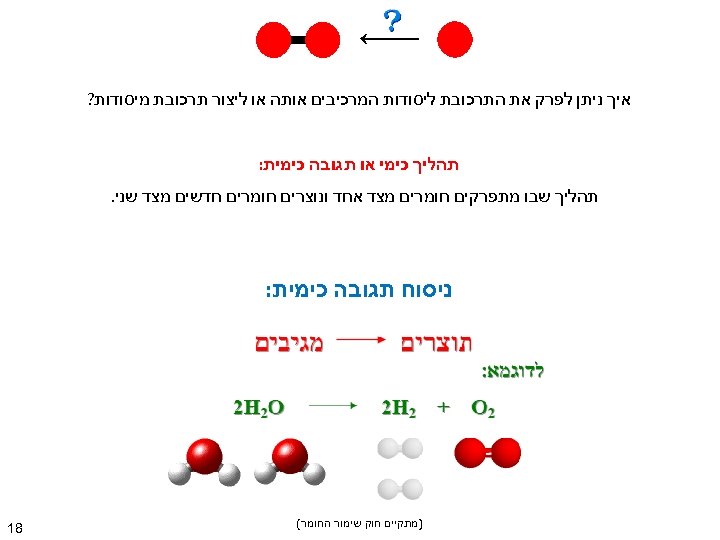
איך ניתן לפרק את התרכובת ליסודות המרכיבים אותה או ליצור תרכובת מיסודות? תהליך כימי או תגובה כימית: תהליך שבו מתפרקים חומרים מצד אחד ונוצרים חומרים חדשים מצד שני. ניסוח תגובה כימית: )מתקיים חוק שימור החומר( 81

לעיתים לא מדובר בפירוק או הרכבה אלא בשינויים אחרים כמו: + 91
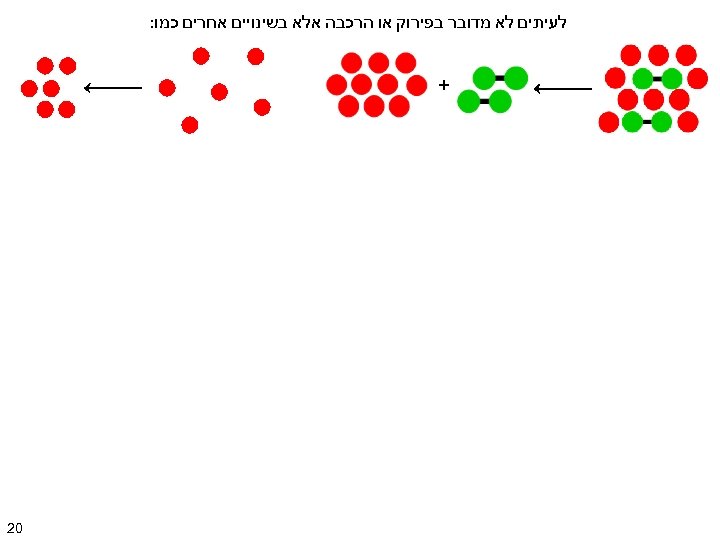
לעיתים לא מדובר בפירוק או הרכבה אלא בשינויים אחרים כמו: + 02
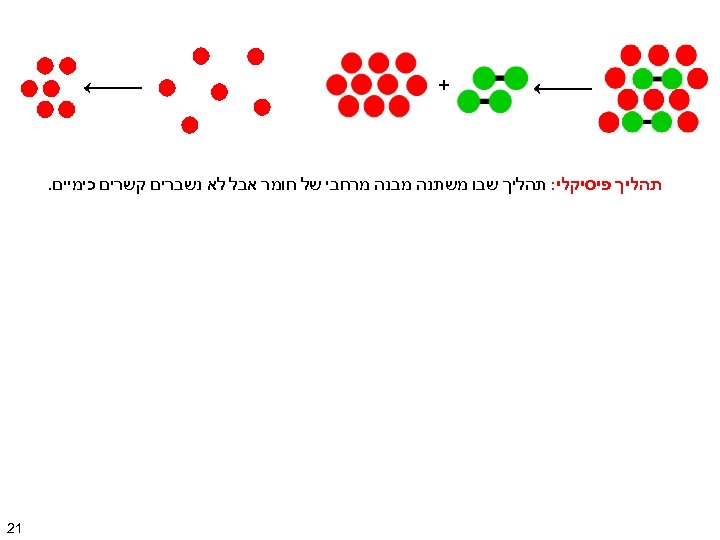
+ תהליך פיסיקלי: תהליך שבו משתנה מבנה מרחבי של חומר אבל לא נשברים קשרים כימיים. 12
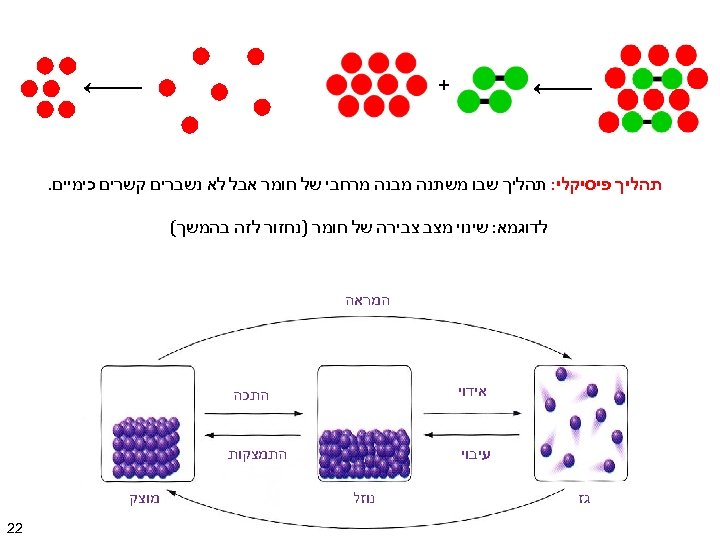
+ תהליך פיסיקלי: תהליך שבו משתנה מבנה מרחבי של חומר אבל לא נשברים קשרים כימיים. לדוגמא: שינוי מצב צבירה של חומר )נחזור לזה בהמשך( המראה אידוי התכה התמצקות עיבוי גז נוזל מוצק 22

דוגמא: הפרדה של תמיסות הומוגניות זיקוק )יין( 32

איך סופרים או שוקלים אטומים? 42
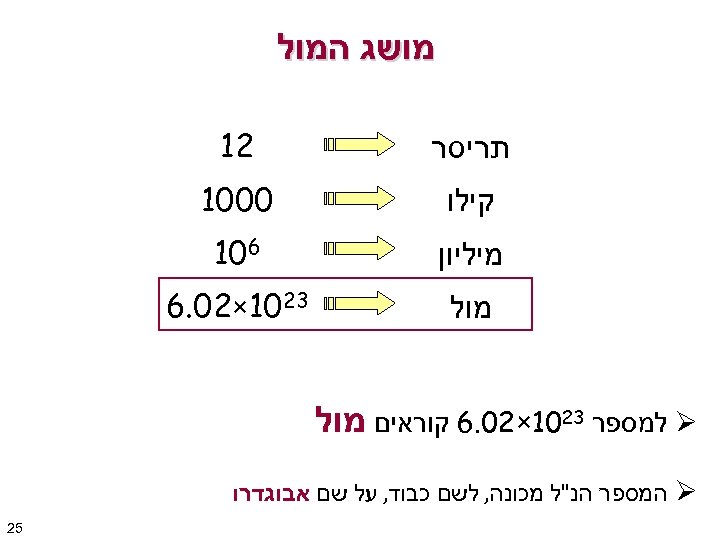
מושג המול תריסר 21 קילו 0001 מיליון 601 מול 3201× 20. 6 Ø למספר 3201× 20. 6 קוראים מול Ø המספר הנ"ל מכונה, לשם כבוד, על שם אבוגדרו 52

למה מול ? v אטום מימן אחד מסתו )1 פרוטון( 1. 673× 10 -24 g = 1∙ H v תריסר אטומים של מימן 12∙H = 12∙ 1. 673× 10 -24 g = 2. 0× 10 -23 g v שישים אטומים 60∙H = 60∙ 1. 673× 10 -24 g = 1. 0× 10 -22 g v מיליון אטומים 106∙H = 1. 673× 10 -18 g 62
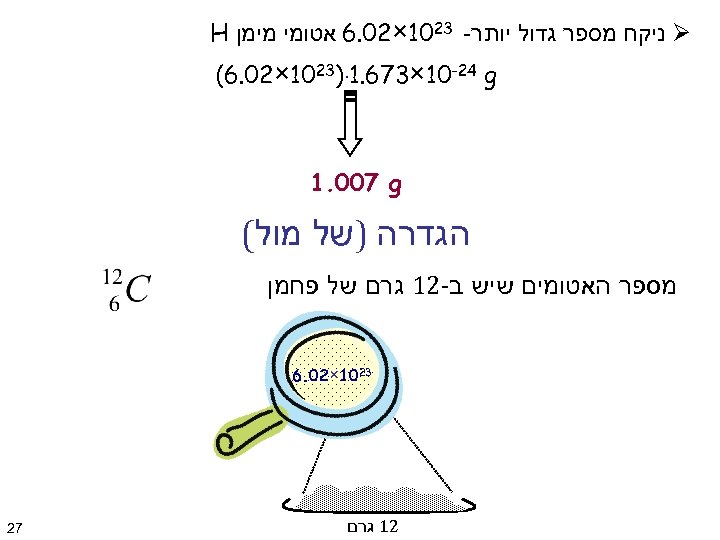
Ø ניקח מספר גדול יותר- 3201× 20. 6 אטומי מימן H (6. 02× 1023)∙ 1. 673× 10 -24 g 1. 007 g הגדרה )של מול( מספר האטומים שיש ב-21 גרם של פחמן 3201× 20. 6 21 גרם 72
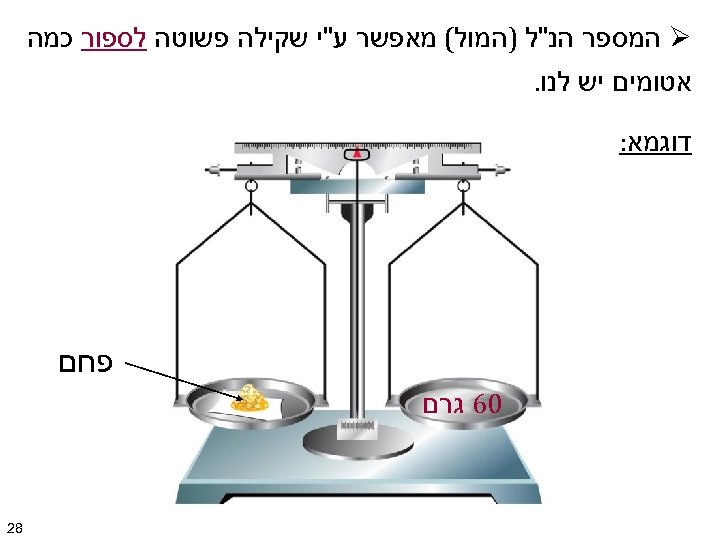
Ø המספר הנ"ל )המול( מאפשר ע"י שקילה פשוטה לספור כמה אטומים יש לנו. דוגמא: פחם 06 גרם 82
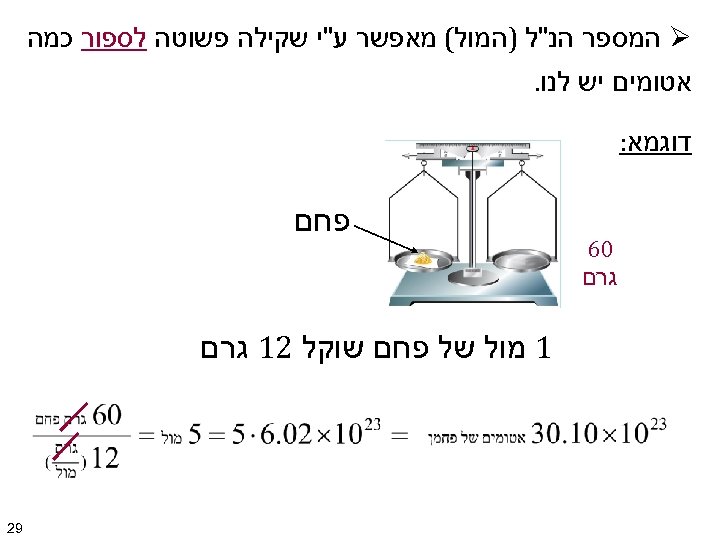
Ø המספר הנ"ל )המול( מאפשר ע"י שקילה פשוטה לספור כמה אטומים יש לנו. דוגמא: 06 גרם פחם 1 מול של פחם שוקל 21 גרם 92
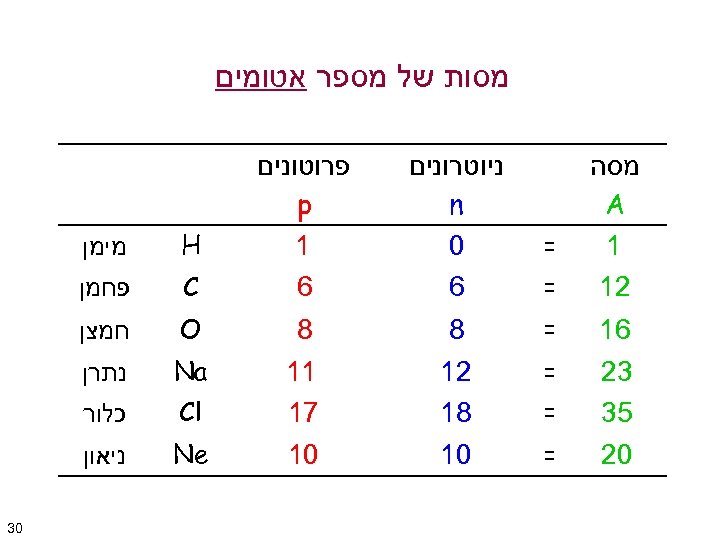
מסות של מספר אטומים מסה A 1 21 = 61 = 8 32 53 = = 21 81 11 71 Cl 02 = 01 Ne = ניוטרונים n 0 6 פרוטונים p 1 6 H מימן C פחמן 8 O חמצן Na נתרן כלור ניאון 03
איך נחשב משקל של מולקולה? 13
איך נחשב משקל של מולקולה? נחבר את המסות של האטומים המרכיבים אותה 23
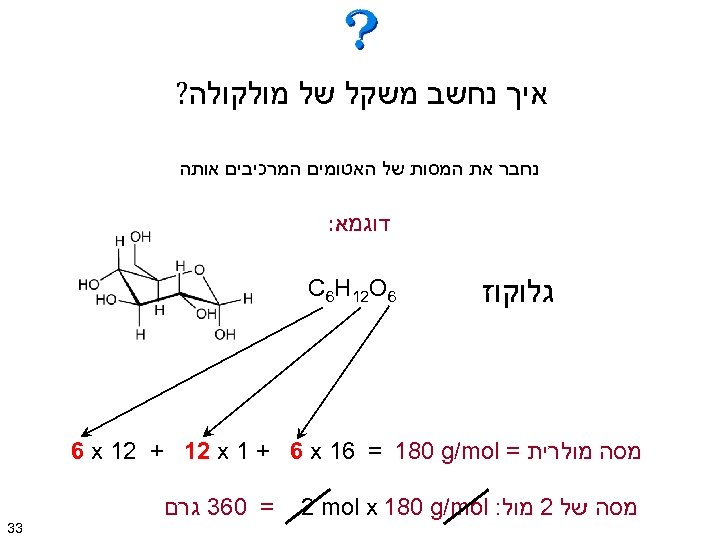
איך נחשב משקל של מולקולה? נחבר את המסות של האטומים המרכיבים אותה דוגמא: גלוקוז 6 C 6 H 12 O מסה מולרית = 6 x 12 + 12 x 1 + 6 x 16 = 180 g/mol מסה של 2 מול: 2 mol x 180 g/mol = 063 גרם 33
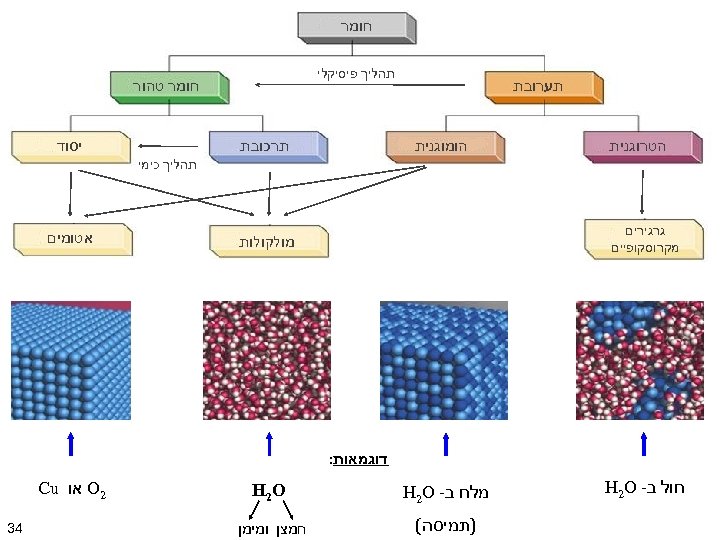
חומר תהליך פיסיקלי תערובת הטרוגנית הומוגנית חומר טהור יסוד תרכובת תהליך כימי גרגירים מקרוסקופיים מולקולות אטומים דוגמאות: חול ב- H 2 O מלח ב- H 2 O H 2 O )תמיסה( חמצן ומימן 2 O או Cu 43
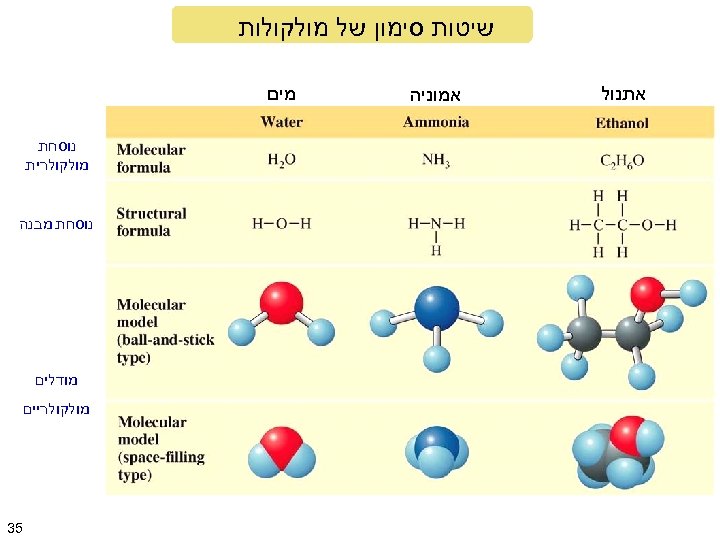
שיטות סימון של מולקולות אתנול אמוניה מים נוסחת מולקולרית נוסחת מבנה מודלים מולקולריים 53

וידוא הבנה… 63
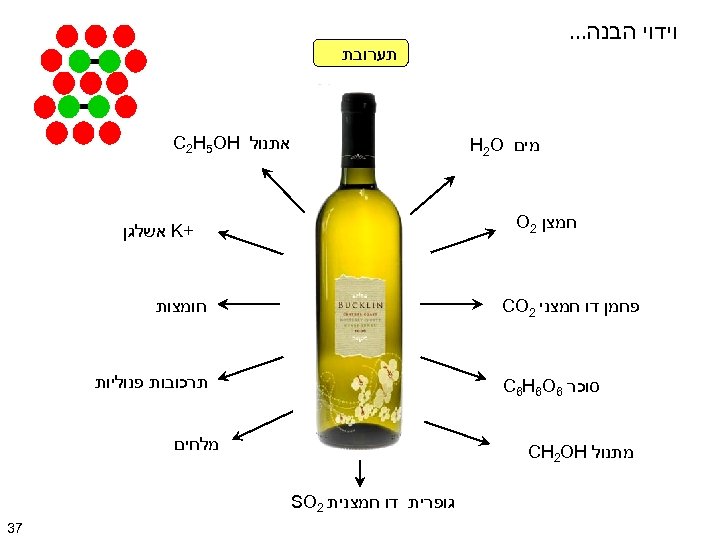
וידוי הבנה… תערובת אתנול C 2 H 5 OH מים H 2 O חמצן 2 O + K אשלגן חומצות פחמן דו חמצני 2 CO תרכובות פנוליות סוכר 6 C 6 H 6 O מלחים מתנול CH 2 OH גופרית דו חמצנית 2 SO 73
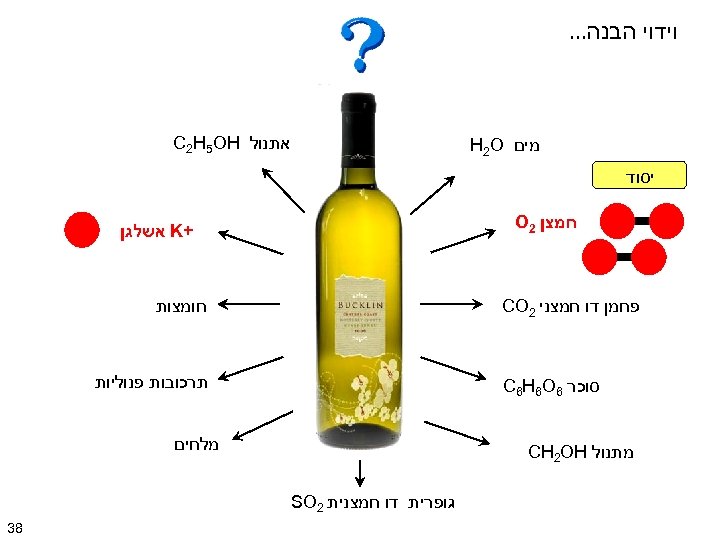
וידוי הבנה… אתנול C 2 H 5 OH מים H 2 O יסוד חמצן 2 O + K אשלגן חומצות פחמן דו חמצני 2 CO תרכובות פנוליות סוכר 6 C 6 H 6 O מלחים מתנול CH 2 OH גופרית דו חמצנית 2 SO 83
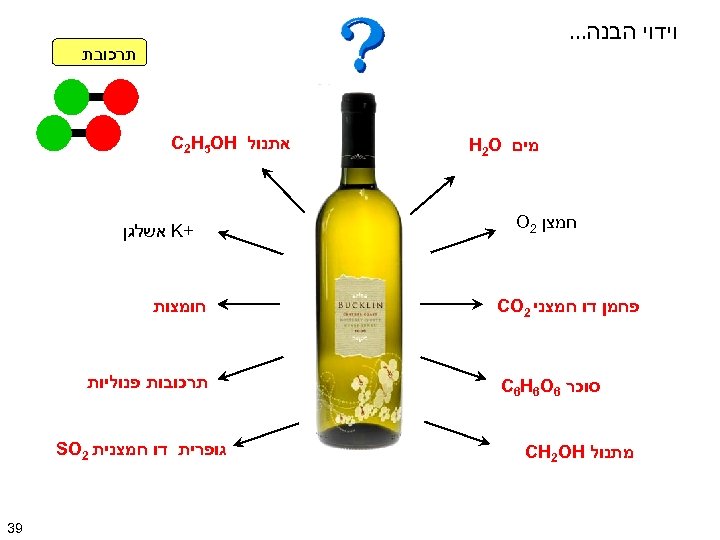
וידוי הבנה… תרכובת מים H 2 O חמצן 2 O פחמן דו חמצני 2 CO סוכר 6 C 6 H 6 O מתנול CH 2 OH אתנול C 2 H 5 OH + K אשלגן חומצות תרכובות פנוליות גופרית דו חמצנית 2 SO 93

מבנה והרכב האטום 04
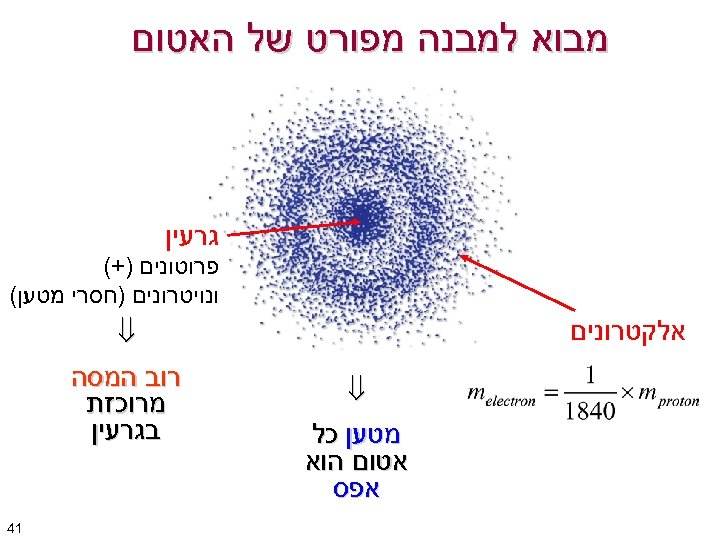
מבוא למבנה מפורט של האטום גרעין פרוטונים )+( ונויטרונים )חסרי מטען( אלקטרונים מטען כל אטום הוא אפס רוב המסה מרוכזת בגרעין 14
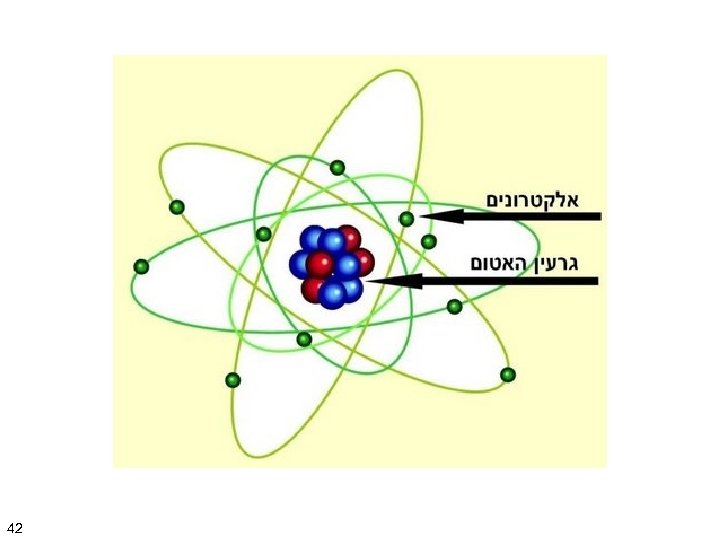
42

סוג האטום נקבע אך ורק ע"י מספר הפרוטונים בגרעין יעקב רוטשילד ת. ז 5050 4002 3002 2002 34

האטום הפשוט ביותר. . . אטום מימן H אלקטרון אחד פרוטון אחד + 44
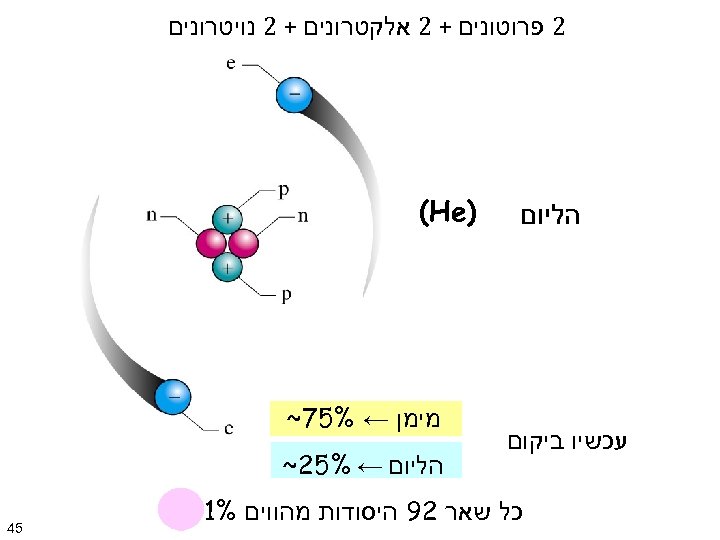
2 פרוטונים + 2 אלקטרונים + 2 נויטרונים הליום עכשיו ביקום ) (He מימן ← %57~ הליום ← %52~ כל שאר 29 היסודות מהווים %1 54
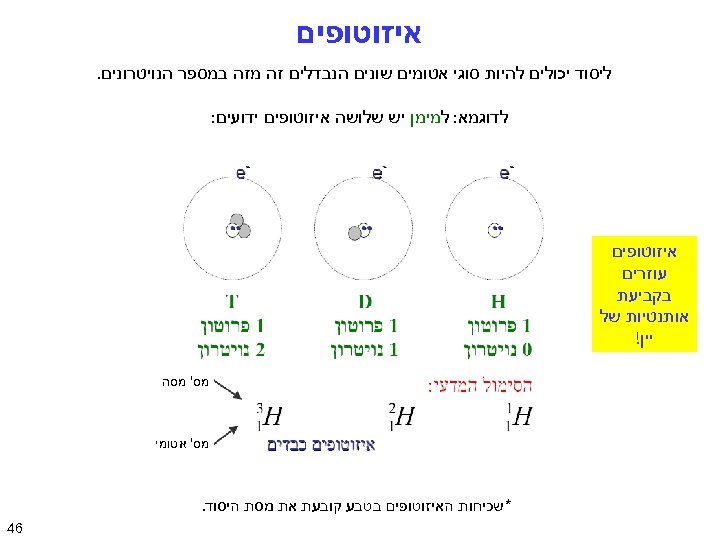
איזוטופים ליסוד יכולים להיות סוגי אטומים שונים הנבדלים זה מזה במספר הנויטרונים. לדוגמא: למימן יש שלושה איזוטופים ידועים: איזוטופים עוזרים בקביעת אותנטיות של יין! מס' מסה מס' אטומי *שכיחות האיזוטופים בטבע קובעת את מסת היסוד. 64
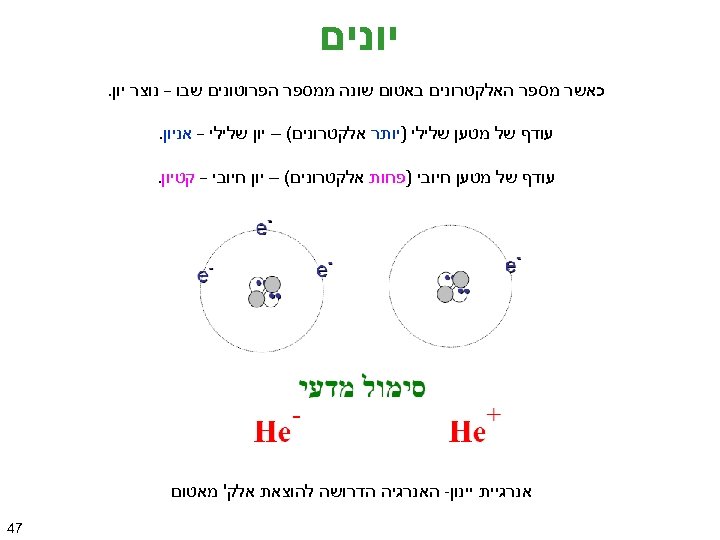
יונים כאשר מספר האלקטרונים באטום שונה ממספר הפרוטונים שבו – נוצר יון. עודף של מטען שלילי )יותר אלקטרונים( – יון שלילי – אניון. עודף של מטען חיובי )פחות אלקטרונים( – יון חיובי – קטיון. אנרגיית יינון- האנרגיה הדרושה להוצאת אלק' מאטום 74

הטבלה המחזורית מציגה את היסודות בסדר מסוים המבוסס על התכונות הכימיות שלהם – הוצעה ב-9681 על-ידי דימיטרי מנדלייב לפי 07 יסודות ידועים. נשמרו מקומות ריקים ליסודות שעדיין לא התגלו. 84

49
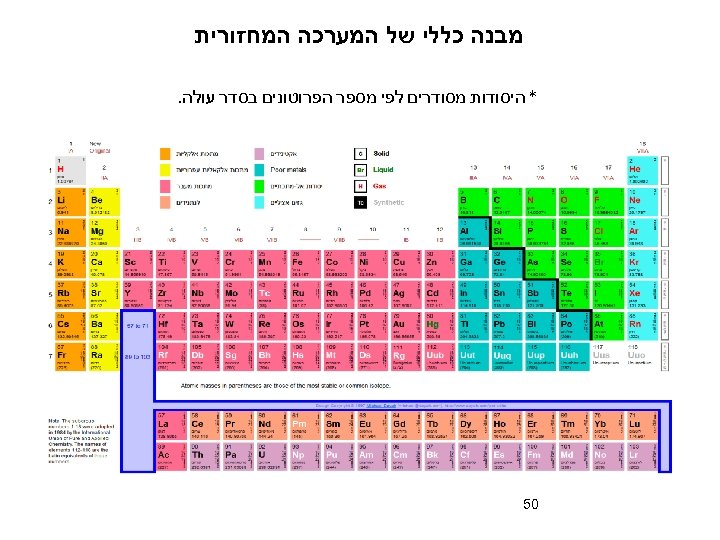
מבנה כללי של המערכה המחזורית * היסודות מסודרים לפי מספר הפרוטונים בסדר עולה. 05
51
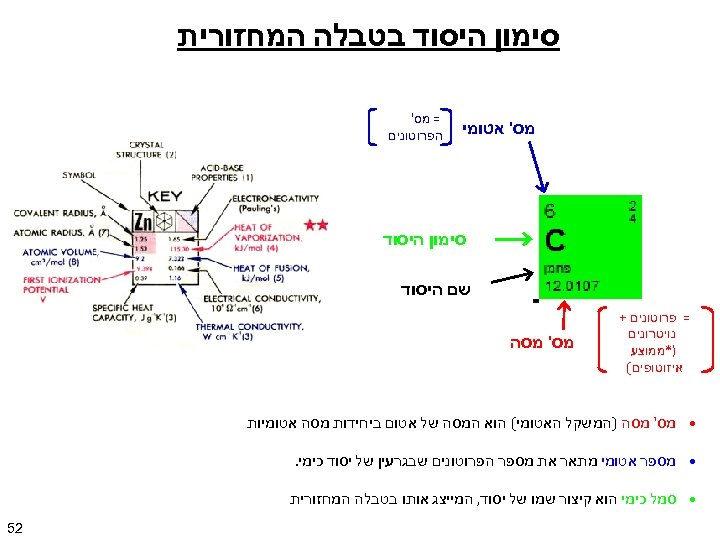
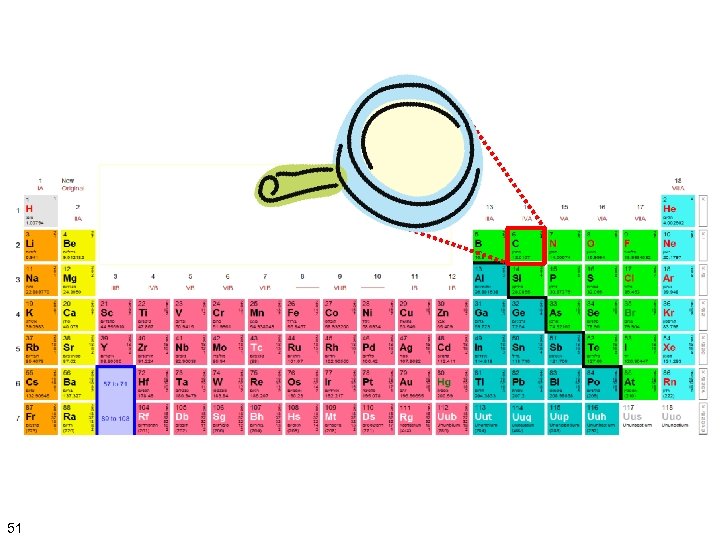
סימון היסוד בטבלה המחזורית מס' אטומי = מס' הפרוטונים סימון היסוד שם היסוד = פרוטונים + נויטרונים מס' מסה )*ממוצע איזוטופים( • מס' מסה )המשקל האטומי( הוא המסה של אטום ביחידות מסה אטומיות • מספר אטומי מתאר את מספר הפרוטונים שבגרעין של יסוד כימי. • סמל כימי הוא קיצור שמו של יסוד, המייצג אותו בטבלה המחזורית 25
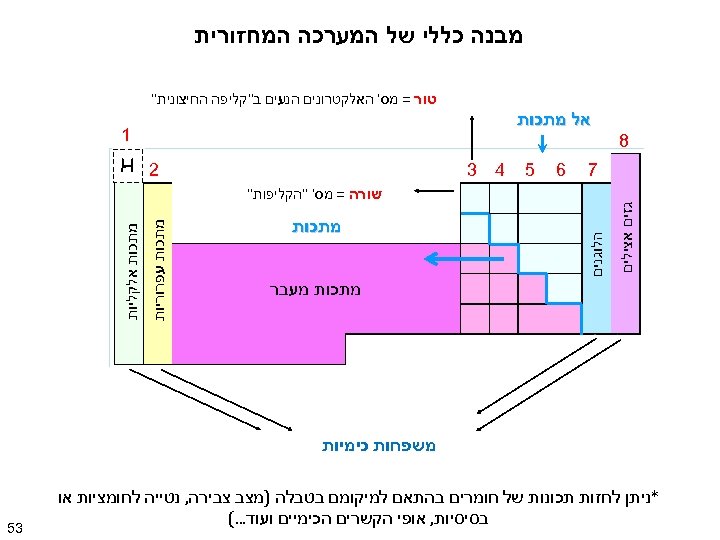
מבנה כללי של המערכה המחזורית טור = מס' האלקטרונים הנעים ב"קליפה החיצונית" אל מתכות 1 8 7 6 5 2 H 4 3 הלוגנים מתכות מעבר מתכות עפרוריות מתכות אלקליות גזים אצילים שורה = מס' "הקליפות" משפחות כימיות *ניתן לחזות תכונות של חומרים בהתאם למיקומם בטבלה )מצב צבירה, נטייה לחומציות או בסיסיות, אופי הקשרים הכימיים ועוד. . . ( 35
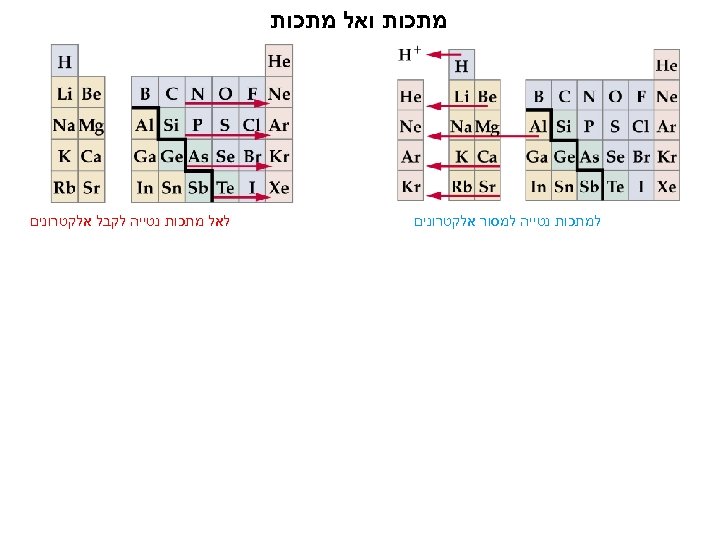
מתכות ואל מתכות למתכות נטייה למסור אלקטרונים לאל מתכות נטייה לקבל אלקטרונים
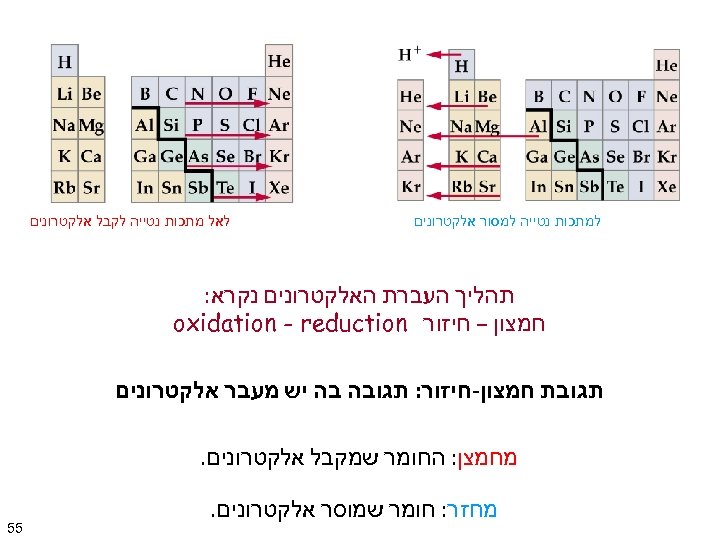
למתכות נטייה למסור אלקטרונים לאל מתכות נטייה לקבל אלקטרונים תהליך העברת האלקטרונים נקרא: חמצון – חיזור oxidation - reduction תגובת חמצון-חיזור: תגובה בה יש מעבר אלקטרונים מחמצן: החומר שמקבל אלקטרונים. מחזר: חומר שמוסר אלקטרונים. 55
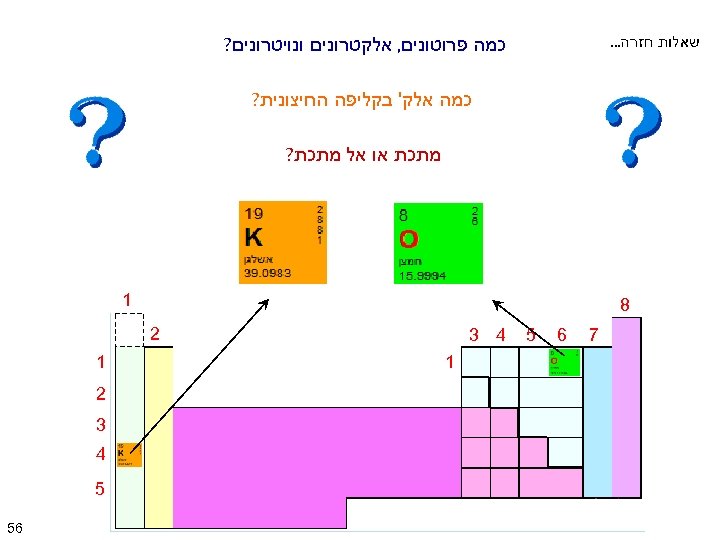
שאלות חזרה. . . כמה פרוטונים, אלקטרונים ונויטרונים? כמה אלק' בקליפה החיצונית? מתכת או אל מתכת? 1 8 7 6 5 2 4 3 1 1 2 3 4 5 65
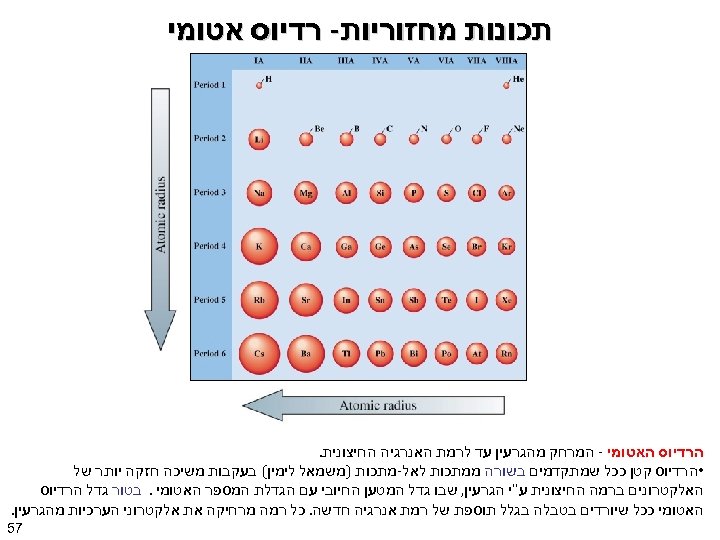
תכונות מחזוריות- רדיוס אטומי הרדיוס האטומי - המרחק מהגרעין עד לרמת האנרגיה החיצונית. • הרדיוס קטן ככל שמתקדמים בשורה ממתכות לאל-מתכות )משמאל לימין( בעקבות משיכה חזקה יותר של האלקטרונים ברמה החיצונית ע"י הגרעין, שבו גדל המטען החיובי עם הגדלת המספר האטומי. בטור גדל הרדיוס האטומי ככל שיורדים בטבלה בגלל תוספת של רמת אנרגיה חדשה. כל רמה מרחיקה את אלקטרוני הערכיות מהגרעין. 75
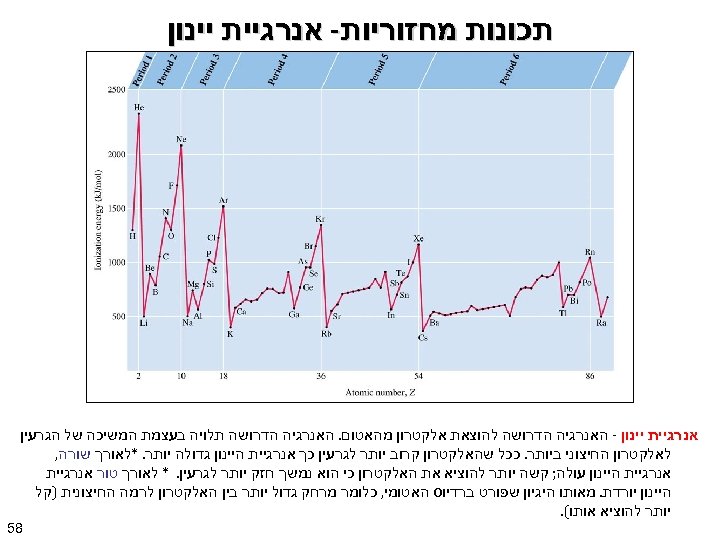
תכונות מחזוריות- אנרגיית יינון - האנרגיה הדרושה להוצאת אלקטרון מהאטום. האנרגיה הדרושה תלויה בעצמת המשיכה של הגרעין לאלקטרון החיצוני ביותר. ככל שהאלקטרון קרוב יותר לגרעין כך אנרגיית היינון גדולה יותר. *לאורך שורה, אנרגיית היינון עולה; קשה יותר להוציא את האלקטרון כי הוא נמשך חזק יותר לגרעין. * לאורך טור אנרגיית היינון יורדת. מאותו היגיון שפורט ברדיוס האטומי, כלומר מרחק גדול יותר בין האלקטרון לרמה החיצונית )קל יותר להוציא אותו(. 85

תכונות מחזוריות- אלקטרושליליות בהסתמך על שני גדלים )אלקטרון אפיניות ואנרגית יוניזציה( הגדיר פאולינג אלקטרושליליות = סולם אשר ערכו המרבי 4 • כשהאלקטרושליליות של אטום • • נמוכה קטיון גבוהה אניון האלקטרושליליות מבטאת את הנטייה היחסית של אטום למשוך אליו את אלקטרוני הקשר הכימי ככל שלאטום משיכה חזקה יותר כך ערך האלקטרושליליות גדול יותר. לאטום הפלואור הערך הגבוה ביותר של אלקטרושליליות והדבר משתלב עם תכונותיו הנוספות כגון רדיוס אטומי קטן ואנרגיית יינון גבוהה. * לאורך שורה, האלקטרושליליות עולה יש "רצון" חזק להפוך למצב אלקטרוני של גז אציל. * לאורך טור האלקטרושליליות יורדת המרחק מהגרעין עולה. 95

הקשר הכימי מה פירוש קשר? כיצד נוכל להגיד שבין שני חלקיקים קיים קשר? למה צריך קשר כימי? 06

גז כלור 07 גרם/מול ) Cl 2(g מתכת ליתיום 7 גרם/מול Li מדוע היסוד ליתיום הוא מתכת ואילו הכלור הכבד ממנו פי 01 הוא גז? 16

קשרים! או יותר מדויק קשרים כימיים. יש קשרים חזקים ויש חלשים מסוגים שונים ומשונים. הכוח היחיד שמאפשר קשר הוא כוח + המשיכה בין פלוס למינוס. המשיכה היא חשמלית ונקראת אלקטרוסטאטית 26

שיטת לואיס: בהסתמך על העובדה שמבנה של )8 אלקטרונים( הוא יציב גזים "אצילים" מבחינה כימית, הציע לואיס את כלל האוקטט השאיפה ל – 8 ליצירת קשר כימי. לואיס הציע להתייחס לאלקטרונים שברמה הבלתי מלאה בלבד )"הקליפה החיצונית( 36

קשרים כימיים כוחות משיכה חזקים בין אטומים מסוימים במולקולה. מבחינה אנרגטית : רמת האנרגיה של הקשר נמוכה מרמת אנרגיה של שני אטומים נפרדים. קשרים כימיים מתחלקים ל-2 קבוצות: 1. קשרים תוך מולקולאריים )קשר יוני וקשר קוולנטי(. 2. קשרים בין מולקולאריים )קשרי מימן, קשרי ואן דר ואלס וקשר מתכתי(. 46
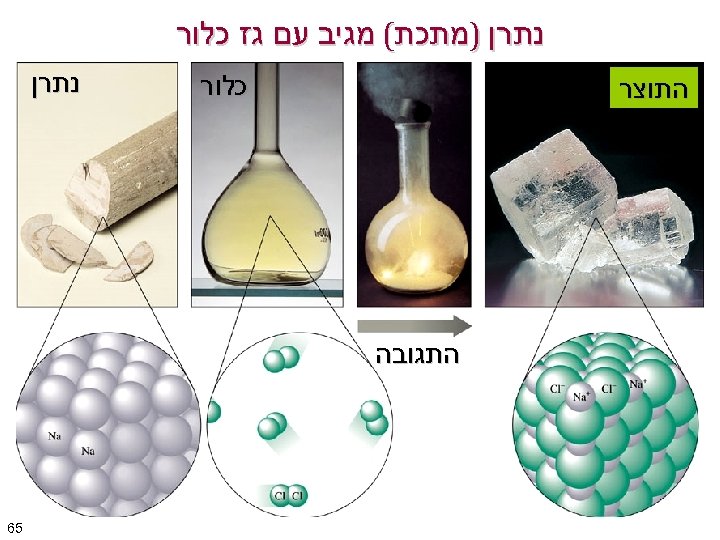
נתרן )מתכת( מגיב עם גז כלור התוצר נתרן התגובה 56
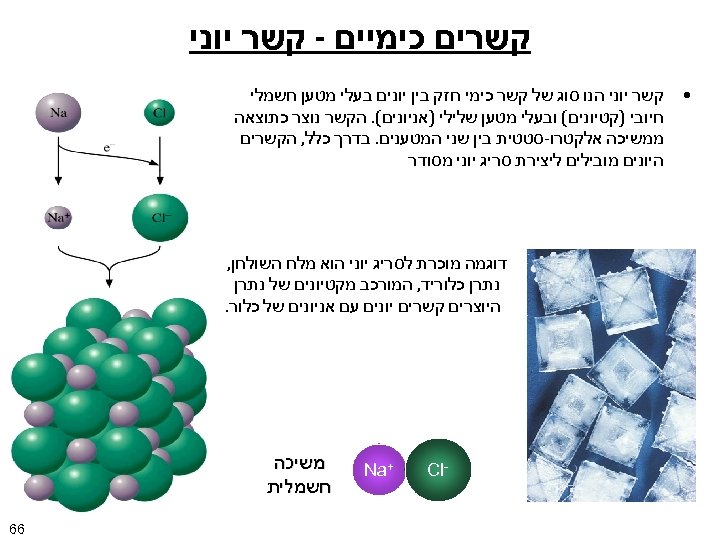
קשרים כימיים - קשר יוני • קשר יוני הנו סוג של קשר כימי חזק בין יונים בעלי מטען חשמלי חיובי )קטיונים( ובעלי מטען שלילי )אניונים(. הקשר נוצר כתוצאה ממשיכה אלקטרו-סטטית בין שני המטענים. בדרך כלל, הקשרים היונים מובילים ליצירת סריג יוני מסודר דוגמה מוכרת לסריג יוני הוא מלח השולחן, נתרן כלוריד, המורכב מקטיונים של נתרן היוצרים קשרים יונים עם אניונים של כלור. - Cl + Na משיכה חשמלית 66
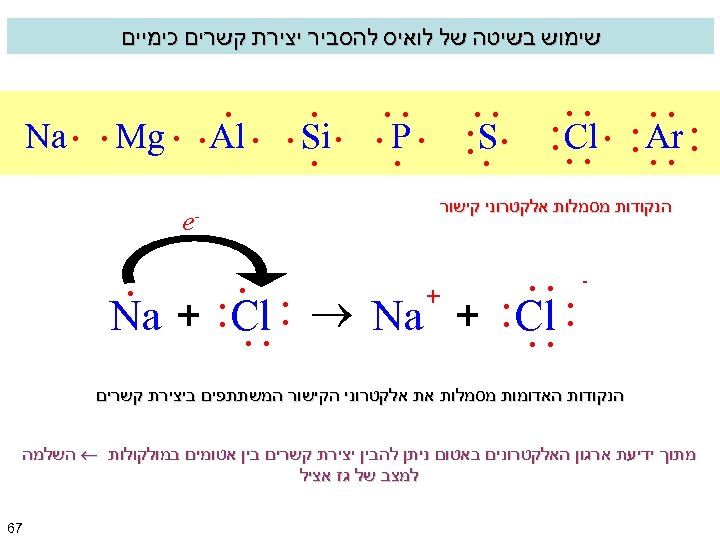
שימוש בשיטה של לואיס להסביר יצירת קשרים כימיים : : : Na. . Mg. . Al. . Si. . P. : S. : Cl. : Ar . : . הנקודות מסמלות אלקטרוני קישור + . . : : : Na + : Cl : - - e הנקודות האדומות מסמלות את אלקטרוני הקישור המשתתפים ביצירת קשרים מתוך ידיעת ארגון האלקטרונים באטום ניתן להבין יצירת קשרים בין אטומים במולקולות השלמה למצב של גז אציל 76
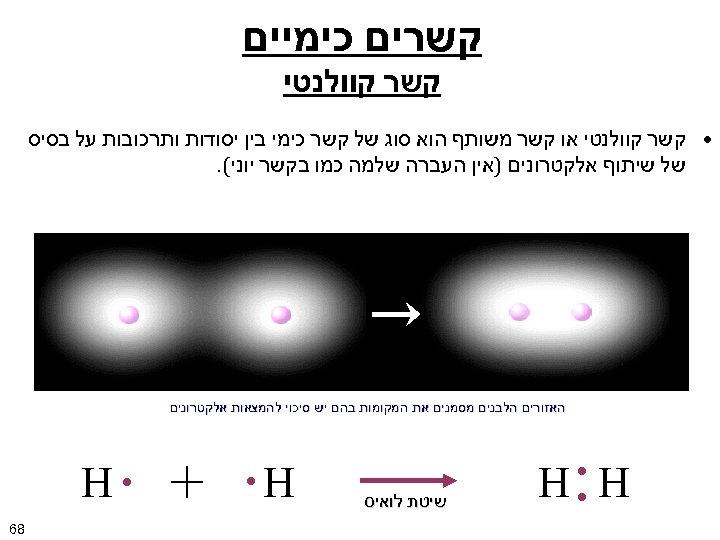
קשרים כימיים קשר קוולנטי • קשר קוולנטי או קשר משותף הוא סוג של קשר כימי בין יסודות ותרכובות על בסיס של שיתוף אלקטרונים )אין העברה שלמה כמו בקשר יוני(. האזורים הלבנים מסמנים את המקומות בהם יש סיכוי להמצאות אלקטרונים : H H שיטת לואיס . +. H H 86

קשרים כימיים קשר קוולנטי • דוגמה: באטום חמצן ) (O נייטרלי, ששה אלקטרונים ברמת האנרגיה הגבוהה ביותר, ועל כן ישנם שני זוגות אלקטרונים , ושני אלקטרונים חופשיים. לדוגמה, אטום חמצן יסומן כך: • בקשר קוולנטי, 'משתפים' שני אטומים את האלקטרונים החופשיים שלהם ברמת האנרגיה הגבוהה ביותר, ליצירת אורביטלים משותפים )בהם זוגות אלקטרונים( המצויים בין שני האטומים. • קשרים קוולנטים אותם יוצר אטום עם אטומים אחרים משלימים את מצבו האלקטרוני של האטום למצב הדומה בין שני אטומים עשוי להיווצר קשר קוולנטי יחיד )זוג אלקטרונים משותף(, כפול )שני זוגות אלקטרונים משותפים( או משולש )שלושה זוגות(. 96
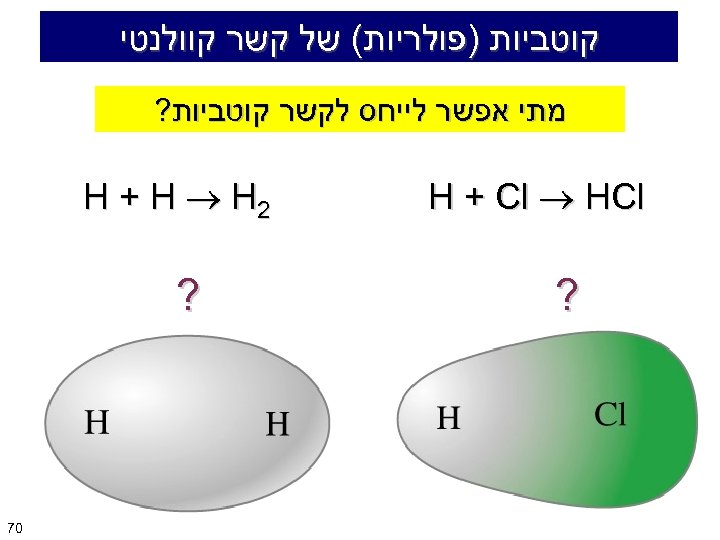
קוטביות )פולריות( של קשר קוולנטי מתי אפשר לייחס לקשר קוטביות? H + Cl HCl ? 2 H + H H ? 07
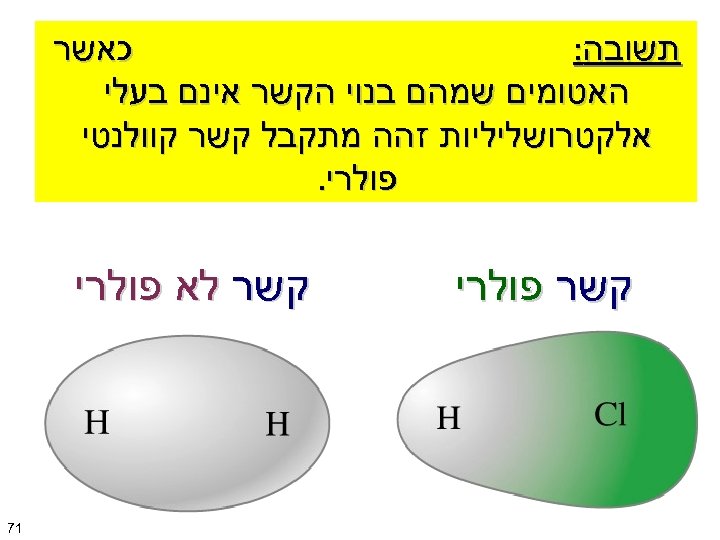
כאשר תשובה: האטומים שמהם בנוי הקשר אינם בעלי אלקטרושליליות זהה מתקבל קשר קוולנטי פולרי. קשר פולרי קשר לא פולרי 17
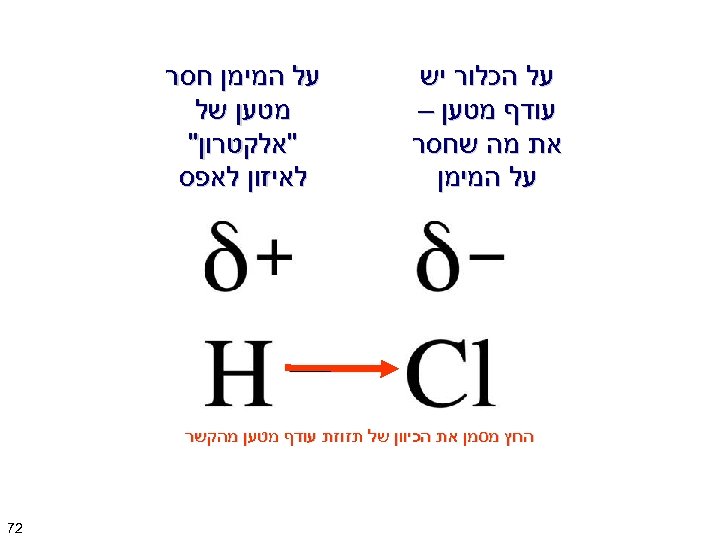
על הכלור יש עודף מטען – את מה שחסר על המימן חסר מטען של "אלקטרון" לאיזון לאפס החץ מסמן את הכיוון של תזוזת עודף מטען מהקשר 27

קוטביות )פולריות( של קשר קוולנטי • קוטביות הינה תכונה של קשרים כימיים, המבוססת על חלוקת המטען החשמלי בין שני האטומים המשתתפים בקשר כך שהאטום האלקטרושלילי מושך אליו את האלקטרונים המשותפים ביתר חוזקה. • קשרים קוטביים במולקולה אינם גורמים בהכרח לכל המולקולה להיות קוטבית. דוגמת פחמן דו-חמצני, הינה מולקולה קווית הנראית כך מבחינה מרחבית: . O=C=O • חיזוי מבנה התלת-ממדי של המולקולה • תכונותיה הפיזיקליות )נקודת התכה, רתיחה וכו'( ואת נטייתה להגיב עם מולקולות אחרות. 37

שלושה כוחות ידועים כקיימים בין מולקולות ואטומים ניאוטראליים א. כוחות דיפול - דיפול קבוע )דו קוטב( ב. כוחות לונדון )דיספרסיה( המונח כוחות ואן-דר-ואלס הוא מונח כללי אשר כולל א + ב ג. קשרי מימן 47
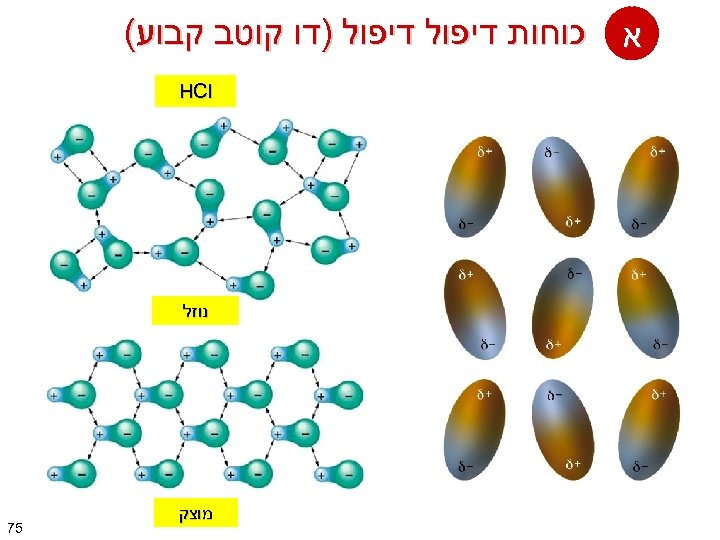
א כוחות דיפול )דו קוטב קבוע( HCl נוזל מוצק 57

מהם הכוחות המאפשרים יצירת מוצק מגז ניאון, מגז כלור, מפרפין וכו' שאין בהם קוטביות קבועה? ב כוחות דיספרסיה לונדון במולקולות בלתי פולריות אין מומנט דיפול ובכל זאת חומרים אלו נמצאים לפעמים במצב נוזלי ומוצק. 67
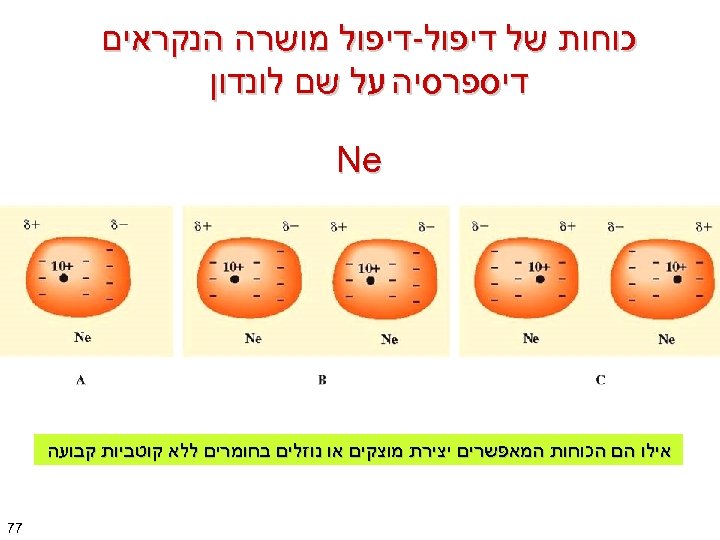
כוחות של דיפול-דיפול מושרה הנקראים דיספרסיה על שם לונדון Ne אילו הם הכוחות המאפשרים יצירת מוצקים או נוזלים בחומרים ללא קוטביות קבועה 77

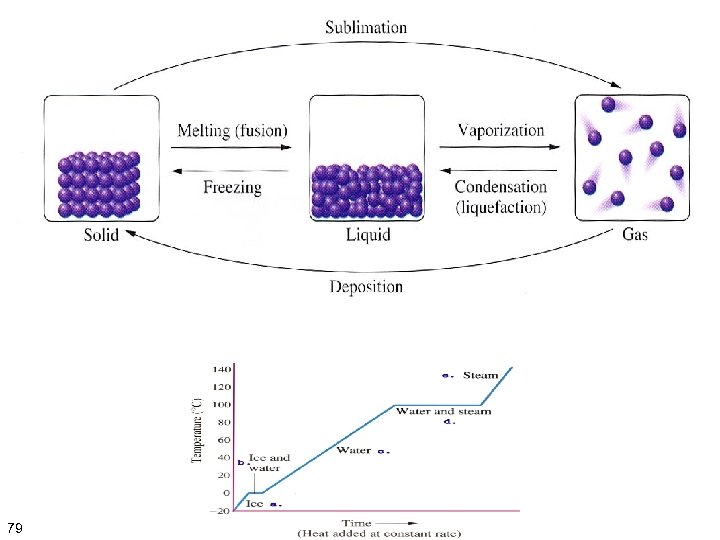
מצבי צבירה מוצק - זהו מצב הצבירה הצפוף והקשה ביותר בו המולקולות של החומר קרובות האחת לשנייה יותר מאשר בשני מצבי הצבירה האחרים. למרות שאין היפרדות בין החלקיקים, מתרחשות תנודות של כל אטום, בהן הוא רועד ומתנגש בשאר האטומים שלידו. לחומרים במצב מוצק צורה מוגדרת ונפח מוגדר. נוזל - זהו מצב צבירה בו נפח החומר נקבע על-פי תנאי הטמפרטורה והלחץ בהם הנוזל שרוי, ואשר צורתו בצדדיו נקבעת לרוב לפי צורת הכלי בו הוא נתון. לנוזלים יש מתח פנים, ונימיות. לרוב הם מתפשטים כאשר הם מחוממים, ומתכווצים בקירור. גז: זהו מצב צבירה של החומר, בו המולקולות אינן צמודות )ישנו רווח ביניהן( אלא רחוקות אחת מהשנייה, המשיכה ביניהן נמוכה, והן נעות בחופשיות יחסית. גז, מסוגל לזרום, ואין נפח קבוע, והוא נוטה להתפשט כדי למלא את כל הנפח שהוקצב לו )עקרון אבוגדרו(. גזים נבדלים במשוואת המצב שלהם. ככל שהגז נמצא בטמפרטורה הקרובה יותר לטמפרטורת הרתיחה שלו, הוא קרוב יותר למצב הנוזל. 87
79
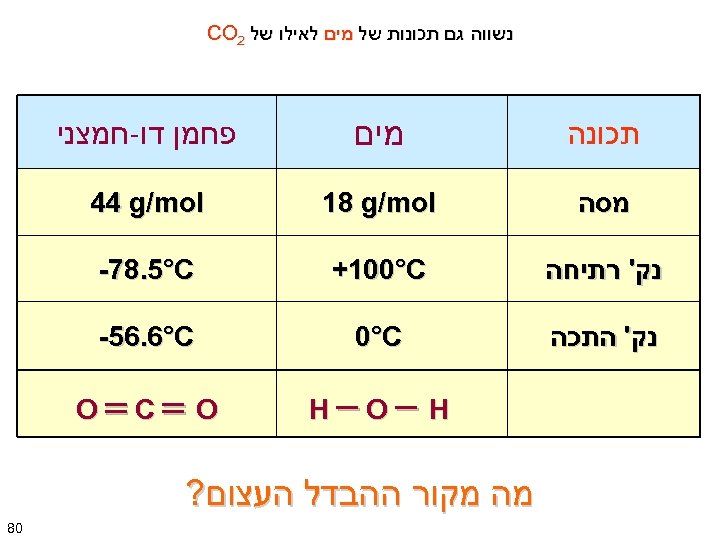
נשווה גם תכונות של מים לאילו של 2 CO תכונה מים פחמן דו-חמצני מסה 18 g/mol 44 g/mol נק' רתיחה +100°C -78. 5°C נק' התכה 0°C -56. 6°C H O C O מה מקור ההבדל העצום? 08
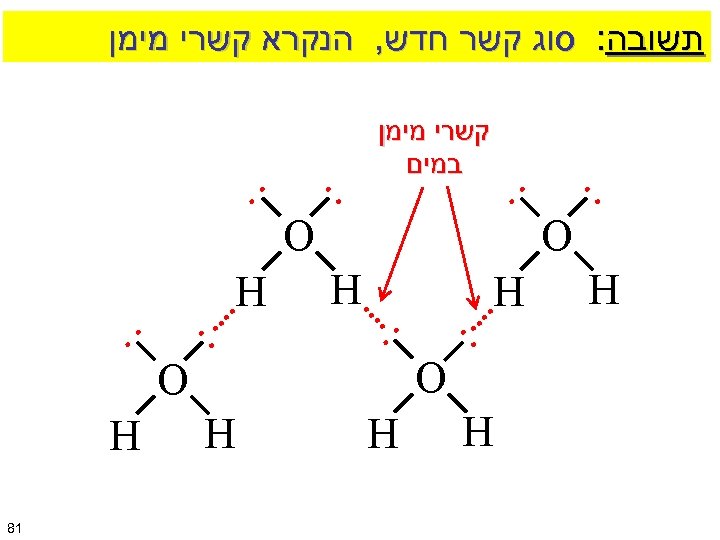
תשובה: סוג קשר חדש, הנקרא קשרי מימן : H קשרי מימן במים : O H : H : O H 18
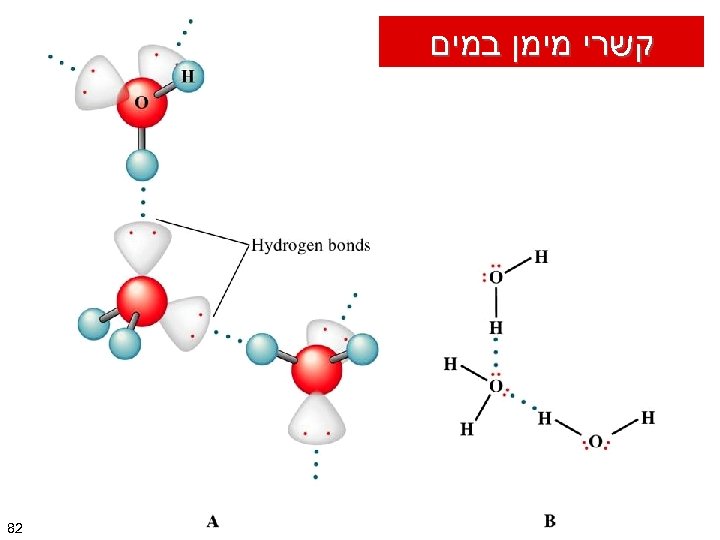
קשרי מימן במים 28
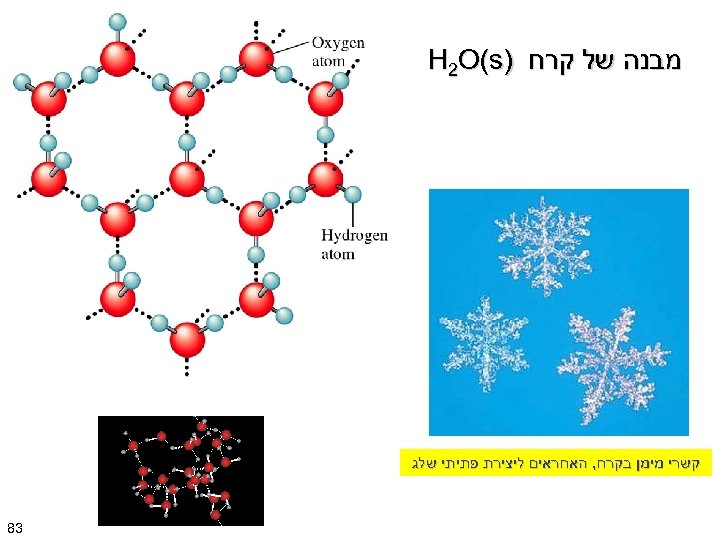
מבנה של קרח ) H 2 O(s קשרי מימן בקרח, האחראים ליצירת פתיתי שלג 38
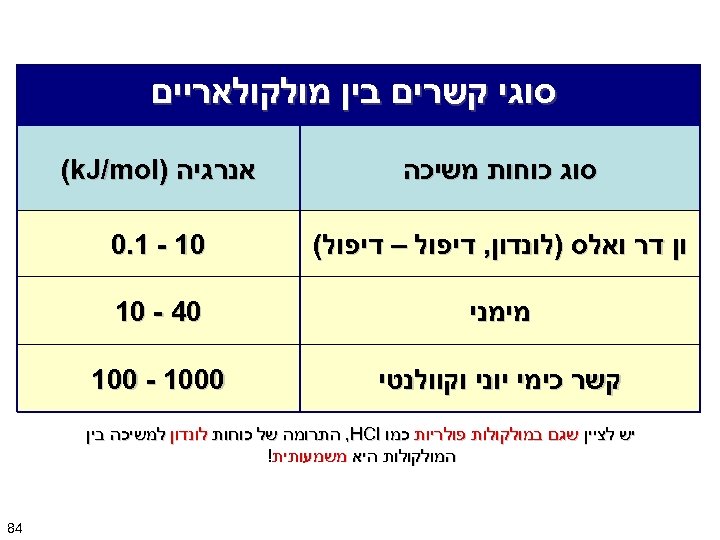
סוגי קשרים בין מולקולאריים סוג כוחות משיכה אנרגיה ) (k. J/mol ון דר ואלס )לונדון, דיפול – דיפול( 01 - 1. 0 מימני 04 - 01 קשר כימי יוני וקוולנטי 0001 - 001 יש לציין שגם במולקולות פולריות כמו , HCl התרומה של כוחות לונדון למשיכה בין המולקולות היא משמעותית! 48
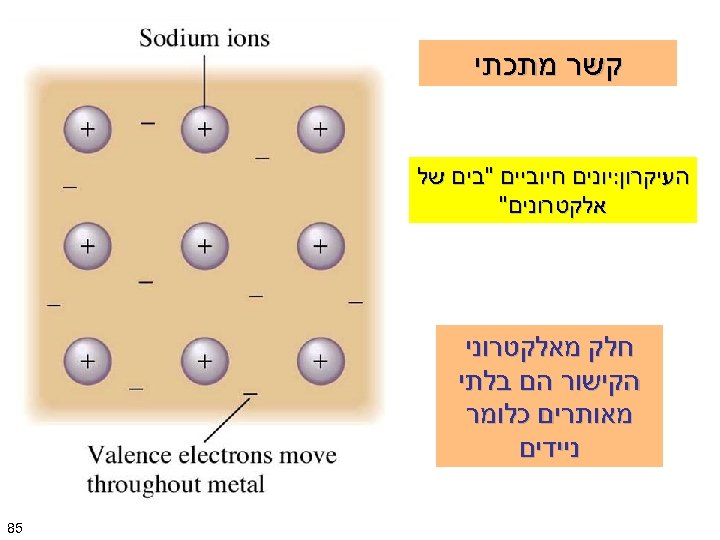
קשר מתכתי העיקרון: יונים חיוביים "בים של אלקטרונים" חלק מאלקטרוני הקישור הם בלתי מאותרים כלומר ניידים 58
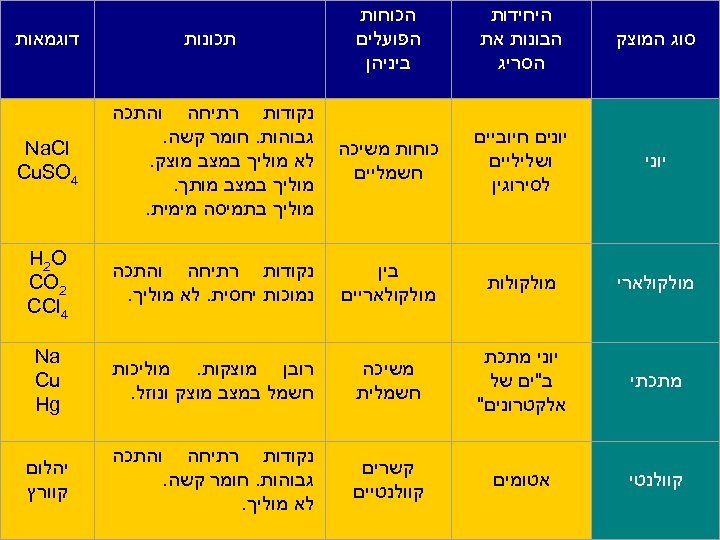
הכוחות הפועלים ביניהן סוג המוצק היחידות הבונות את הסריג תכונות דוגמאות יונים חיוביים ושליליים לסירוגין כוחות משיכה חשמליים נקודות רתיחה והתכה גבוהות. חומר קשה. לא מוליך במצב מוצק. מוליך במצב מותך. מוליך בתמיסה מימית. Na. Cl 4 Cu. SO מולקולארי מולקולות בין מולקולאריים נקודות רתיחה והתכה נמוכות יחסית. לא מוליך. H 2 O 2 CO 4 CCl מתכתי יוני מתכת ב"ים של אלקטרונים" משיכה חשמלית רובן מוצקות. מוליכות חשמל במצב מוצק ונוזל. Na Cu Hg קוולנטי אטומים קשרים קוולנטיים נקודות רתיחה והתכה גבוהות. חומר קשה. לא מוליך. יהלום קוורץ 68
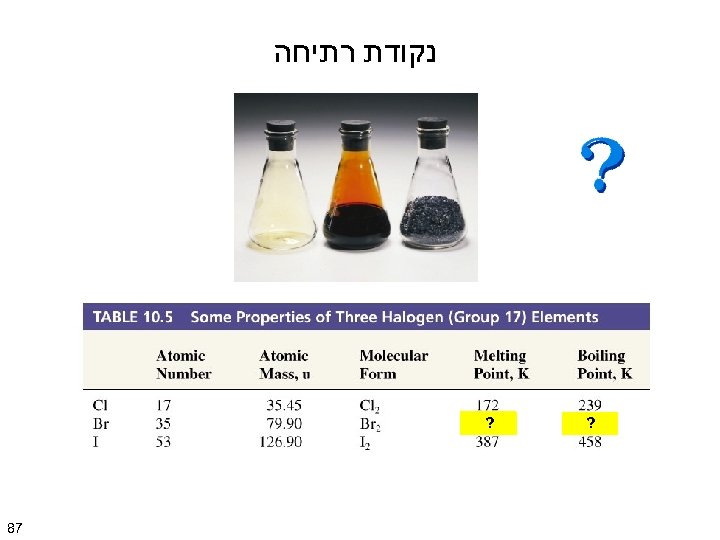
נקודת רתיחה ? 233 ? 662 78

תמיסות מי נמס במי ולמה? נוזל בתוך נוזל מוצק בתוך מוצק מה הם הגורמים הקובעים והמשפיעים 88
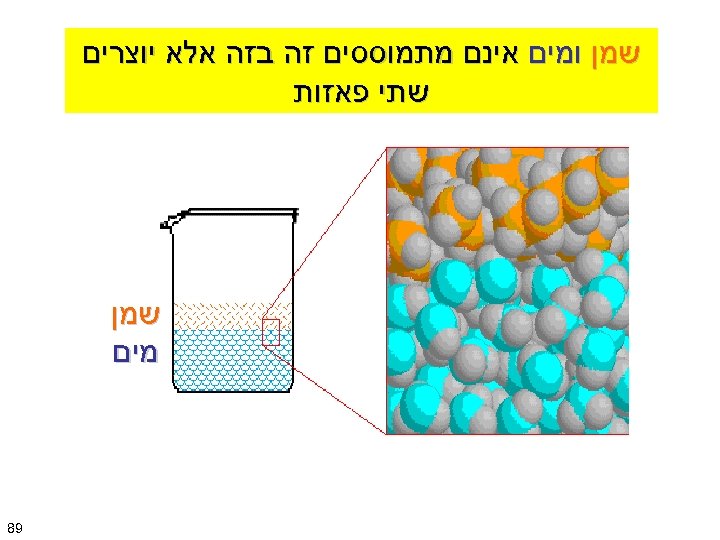
שמן ומים אינם מתמוססים זה בזה אלא יוצרים שתי פאזות שמן מים 98
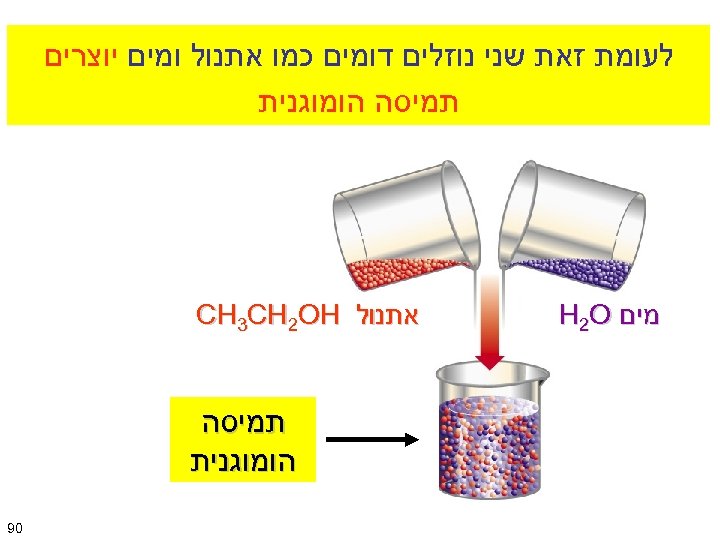
לעומת זאת שני נוזלים דומים כמו אתנול ומים יוצרים תמיסה הומוגנית מים H 2 O אתנול CH 3 CH 2 OH תמיסה הומוגנית 09
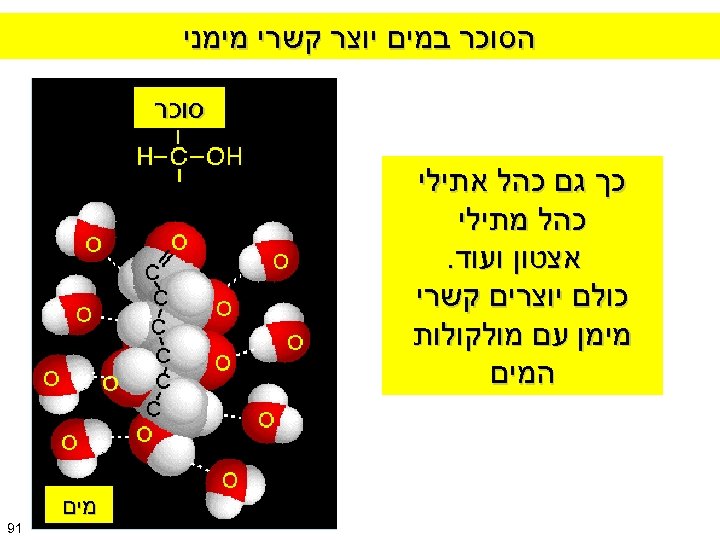
הסוכר במים יוצר קשרי מימני סוכר כך גם כהל אתילי כהל מתילי אצטון ועוד. כולם יוצרים קשרי מימן עם מולקולות המים 19
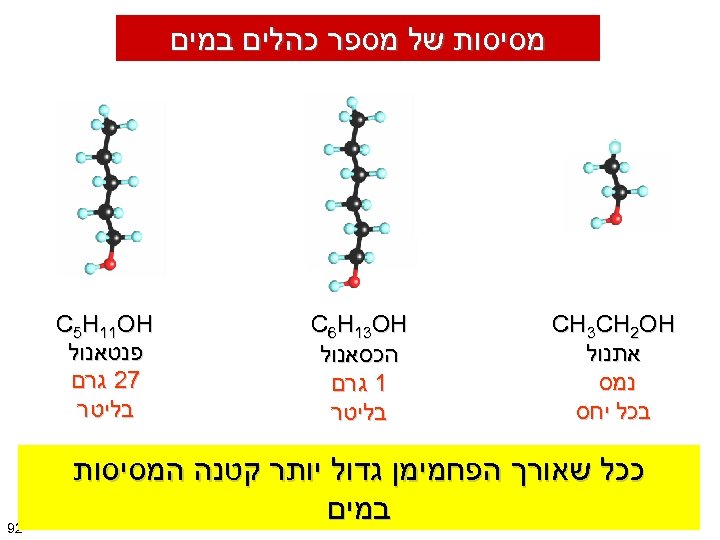
מסיסות של מספר כהלים במים CH 3 CH 2 OH אתנול נמס בכל יחס C 6 H 13 OH הכסאנול 1 גרם בליטר C 5 H 11 OH פנטאנול 72 גרם בליטר ככל שאורך הפחמימן גדול יותר קטנה המסיסות במים 29

איך יודעים כמה מולקולות יש בתמיסה?
![יחידות ריכוז ] = [M ) Mole (n = C ריכוז מולרי ) יחידות ריכוז ] = [M ) Mole (n = C ריכוז מולרי )](https://present5.com/presentation/53b88590e2cf5219882ab24062b4c814/image-94.jpg)
יחידות ריכוז ] = [M ) Mole (n = C ריכוז מולרי ) Liter (L
![יחידות ריכוז ] = [M מולליות = ) Mole (n = C ריכוז יחידות ריכוז ] = [M מולליות = ) Mole (n = C ריכוז](https://present5.com/presentation/53b88590e2cf5219882ab24062b4c814/image-95.jpg)
יחידות ריכוז ] = [M מולליות = ) Mole (n = C ריכוז מולרי ) Liter (L מספר מולים מומסים ב 1 ק"ג ממס ppm אחוז נפחי אחוז משקלי 59

p. H וחומציות • חומצות ובסיסים • p. H ומדידת p. H • תגובות סתירה וטיטרציה • בופר • חומצות ביין 69

חומצות ובסיסים מקור השם חומצה – – acidus חמוץ. לבסיסים לרוב טעם מר והם סותרים את פעולת החומצה. ההגדרה על פי ארהניוס: חומצה חומר המגדיל את ריכוז יוני ה- + H במים ובסיס חומר המגדיל את ריכוז ה- - OH אנחנו נאמץ את ההגדרה של בראונסטד-לאורי חומצה – חומר המסוגל למסור פרוטון. בסיס – חומר המסוגל לקלוט פרוטון. 79
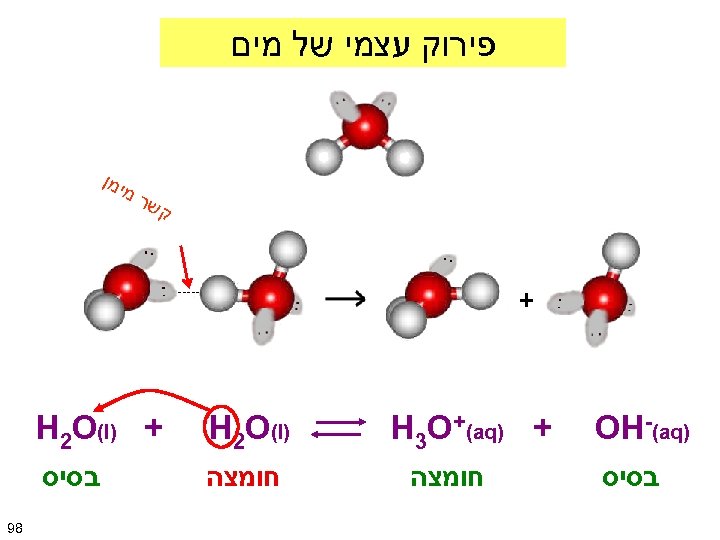
פירוק עצמי של מים קש ) OH-(aq בסיס + ) H 3 O+(aq חומצה ימן רמ ) H 2 O(l + ) H 2 O(l חומצה בסיס 89
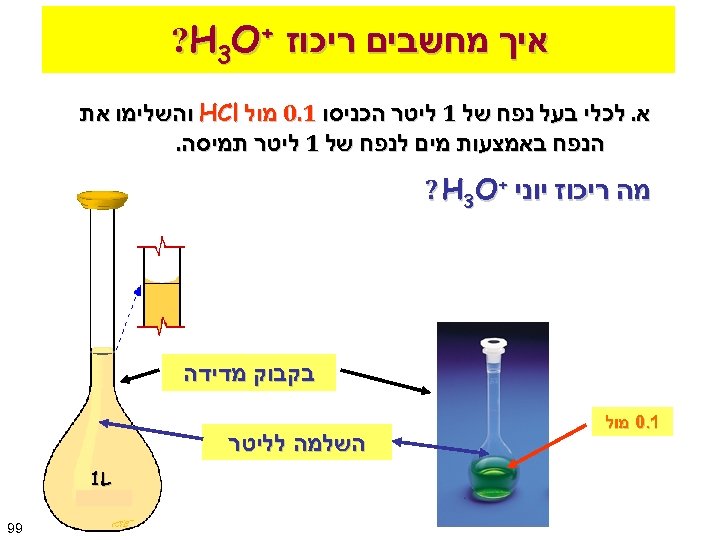
איך מחשבים ריכוז + ? H 3 O א. לכלי בעל נפח של 1 ליטר הכניסו 1. 0 מול HCl והשלימו את הנפח באמצעות מים לנפח של 1 ליטר תמיסה. מה ריכוז יוני + ? H 3 O בקבוק מדידה 1. 0 מול השלמה לליטר 1 L 99
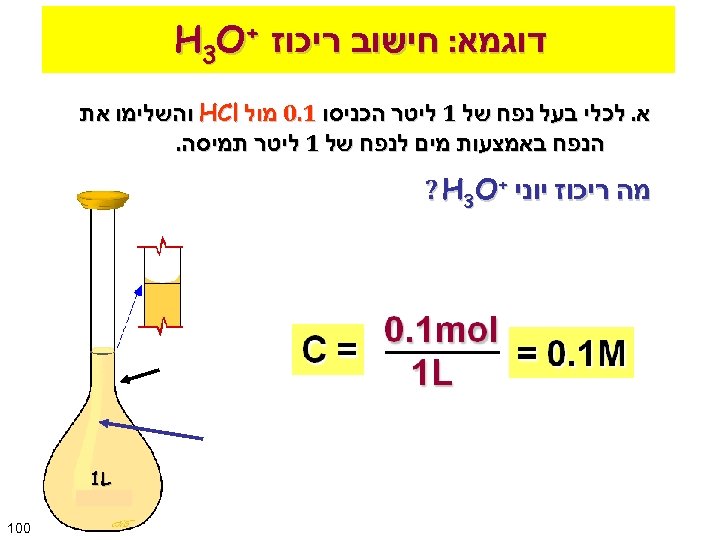
דוגמא: חישוב ריכוז + H 3 O א. לכלי בעל נפח של 1 ליטר הכניסו 1. 0 מול HCl והשלימו את הנפח באמצעות מים לנפח של 1 ליטר תמיסה. מה ריכוז יוני + ? H 3 O 1 L 001
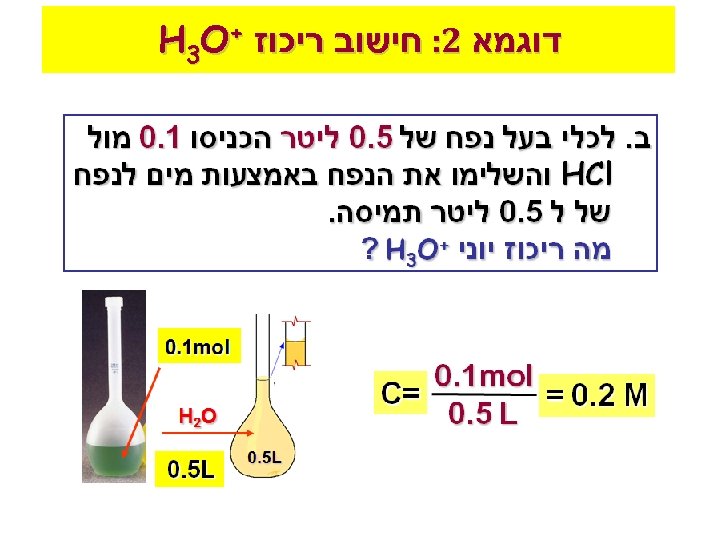
דוגמא 2: חישוב ריכוז + H 3 O

הגדרת ה - p. H פונקצית P צורת ביטוי כללית P( ) = -log( )

הגדרת ה - p. H פונקצית P צורת ביטוי כללית P( ) = -log( ) ] p. H = -log[H 3 O+] -log[H
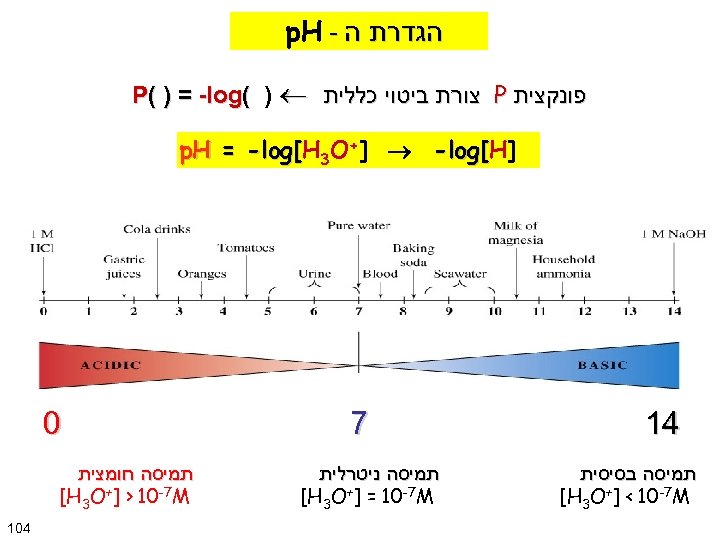
הגדרת ה - p. H פונקצית P צורת ביטוי כללית P( ) = -log( ) ] p. H = -log[H 3 O+] -log[H 41 תמיסה בסיסית [H 3 O+] < 10 -7 M 7 תמיסה ניטרלית [H 3 O+] = 10 -7 M 0 תמיסה חומצית [H 3 O+] > 10 -7 M 401
![41 תמיסה בסיסית [H 3 O+] < 10 -7 M 7 תמיסה ניטרלית 41 תמיסה בסיסית [H 3 O+] < 10 -7 M 7 תמיסה ניטרלית](https://present5.com/presentation/53b88590e2cf5219882ab24062b4c814/image-105.jpg)
41 תמיסה בסיסית [H 3 O+] < 10 -7 M 7 תמיסה ניטרלית [H 3 O+] = 10 -7 M 0 תמיסה חומצית [H 3 O+] > 10 -7 M 501
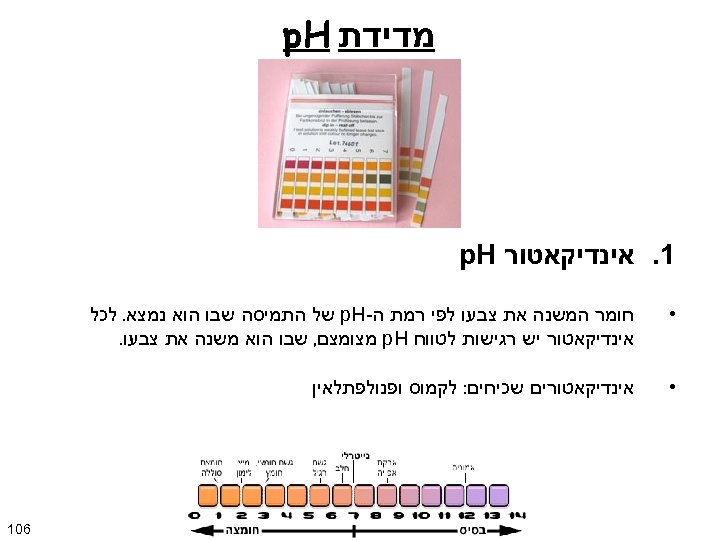
מדידת p. H 1. אינדיקאטור p. H • חומר המשנה את צבעו לפי רמת ה- p. H של התמיסה שבו הוא נמצא. לכל אינדיקאטור יש רגישות לטווח p. H מצומצם, שבו הוא משנה את צבעו. • אינדיקאטורים שכיחים: לקמוס ופנולפתלאין 601
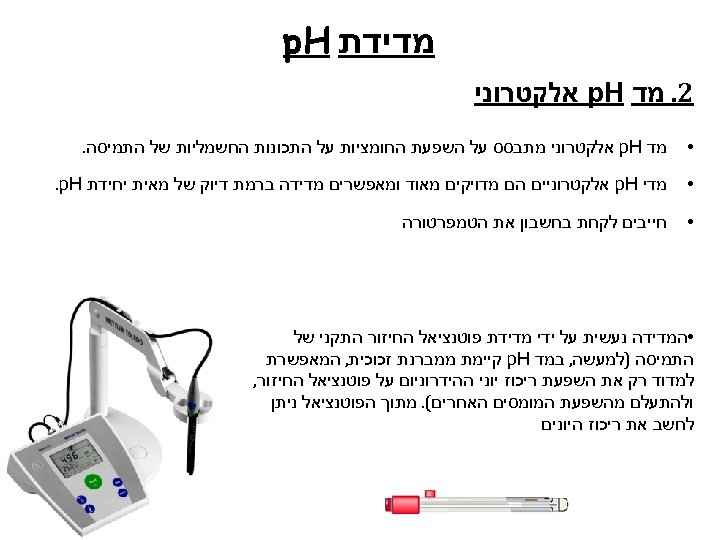
מדידת p. H 2. מד p. H אלקטרוני • מד p. H אלקטרוני מתבסס על השפעת החומציות על התכונות החשמליות של התמיסה. • מדי p. H אלקטרוניים הם מדויקים מאוד ומאפשרים מדידה ברמת דיוק של מאית יחידת . p. H • חייבים לקחת בחשבון את הטמפרטורה • המדידה נעשית על ידי מדידת פוטנציאל החיזור התקני של התמיסה )למעשה, במד p. H קיימת ממברנת זכוכית, המאפשרת למדוד רק את השפעת ריכוז יוני ההידרוניום על פוטנציאל החיזור, ולהתעלם מהשפעת המומסים האחרים(. מתוך הפוטנציאל ניתן לחשב את ריכוז היונים 701

למה חשוב לדעת p. H ביין? 801

למה חשוב לדעת p. H ביין? • השפעת ה -p. H על היין היא מעיקרה כימית ומיקרוביולוגית )ההגנה מפני חמצון ומפני קלקולים מיקרוביולוגים( ולא כל כך אורגנולפטית. ל- p. H השפעות נוספות בשלבים השונים בעשיית היין כמו בסלקציה של מיקרו אורגניזמים בתסיסות ספונטאניות. על פי רוב p. H נמוך בורר את השמרים ואת החיידקים המלולקטייים המועדפים בייננות, אם כי p. H נמוך מידי יכול לעכב ואף למנוע כליל תסיסה מלולקטית. • גם בשלב ייצוב ועיצוב היין ידועה השפעה ל . ; p. H בנטוניט לדוגמא יהיה יעיל יותר ב -p. H נמוך. בנוסף p. H נמוך מעצים את עוצמת הצבע ביינות אדומים )יותר פיגמנטים נמצאים במצב אדום(. 901

למה חשוב לדעת p. H ביין? • השפעת ה -p. H על היין היא מעיקרה כימית ומיקרוביולוגית )ההגנה מפני חמצון ומפני קלקולים מיקרוביולוגים( ולא כל כך אורגנולפטית. • ל- p. H השפעות נוספות בשלבים השונים בעשיית היין כמו בסלקציה של מיקרו אורגניזמים בתסיסות ספונטאניות. על פי רוב p. H נמוך בורר את השמרים ואת החיידקים המלולקטייים המועדפים בייננות, אם כי p. H נמוך מידי יכול לעכב ואף למנוע כליל תסיסה מלולקטית. • גם בשלב ייצוב ועיצוב היין ידועה השפעה ל . ; p. H בנטוניט לדוגמא יהיה יעיל יותר ב -p. H נמוך. בנוסף p. H נמוך מעצים את עוצמת הצבע ביינות אדומים )יותר פיגמנטים נמצאים במצב אדום(. 011

למה חשוב לדעת p. H ביין? • השפעת ה -p. H על היין היא מעיקרה כימית ומיקרוביולוגית )ההגנה מפני חמצון ומפני קלקולים מיקרוביולוגים( ולא כל כך אורגנולפטית. • ל- p. H השפעות נוספות בשלבים השונים בעשיית היין כמו בסלקציה של מיקרו אורגניזמים בתסיסות ספונטאניות. על פי רוב p. H נמוך בורר את השמרים ואת החיידקים המלולקטייים המועדפים בייננות, אם כי p. H נמוך מידי יכול לעכב ואף למנוע כליל תסיסה מלולקטית. • גם בשלב ייצוב ועיצוב היין ידועה השפעה ל . ; p. H בנטוניט לדוגמא יהיה יעיל יותר ב -p. H נמוך. בנוסף p. H נמוך מעצים את עוצמת הצבע ביינות אדומים )יותר פיגמנטים נמצאים במצב אדום(. 111
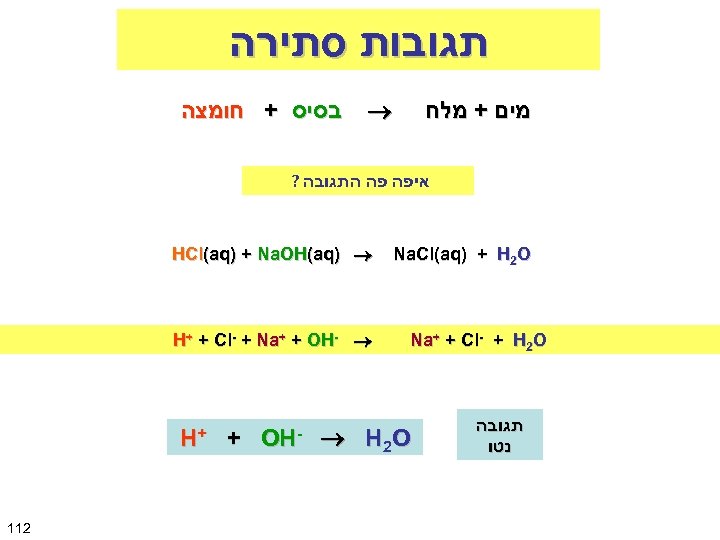
תגובות סתירה מים + מלח בסיס + חומצה איפה פה התגובה ? Na. Cl(aq) + H 2 O Na+ + Cl- + H 2 O תגובה נטו HCl(aq) + Na. OH(aq) H+ + Cl- + Na+ + OH- H 2 O - OH + + H 211
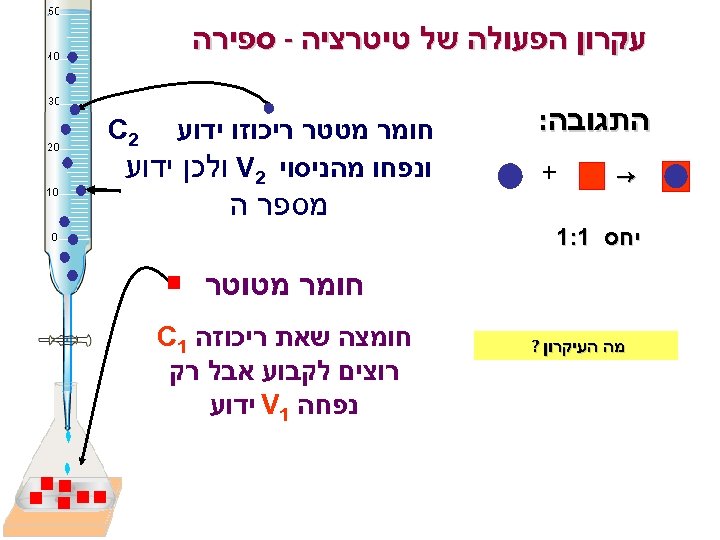
עקרון הפעולה של טיטרציה - ספירה התגובה: + 2 C חומר מטטר ריכוזו ידוע ונפחו מהניסוי 2 V ולכן ידוע מספר ה יחס 1: 1 חומר מטוטר מה העיקרון ? חומצה שאת ריכוזה 1 C רוצים לקבוע אבל רק נפחה 1 V ידוע 311
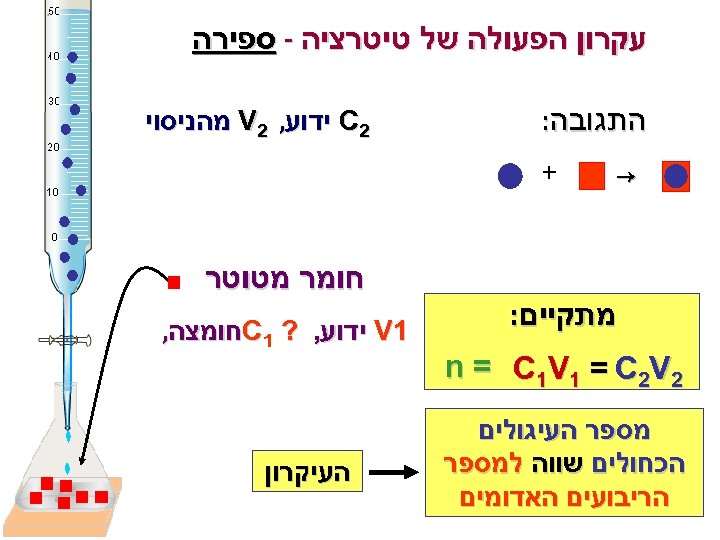
עקרון הפעולה של טיטרציה - ספירה התגובה: 2 C ידוע, 2 V מהניסוי + מתקיים: 2 n = C 1 V 1 = C 2 V מספר העיגולים הכחולים שווה למספר הריבועים האדומים חומר מטוטר 1 V ידוע, ? 1 C חומצה, העיקרון 411

כיצד נדע שתגובת הסתירה נסתיימה ? כלומר איך נדע שסתרנו את כל החומצה ? 511

כיצד נדע שתגובת הסתירה נסתיימה ? כלומר איך נדע שסתרנו את כל החומצה ? דרוש )בוחן( אינדיקאטור חומר אשר ישנה את צבעו 611
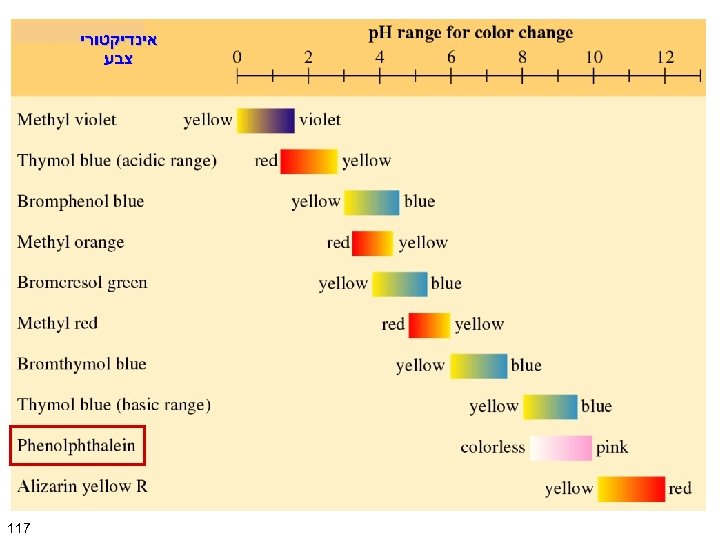
אינדיקטורי צבע 711
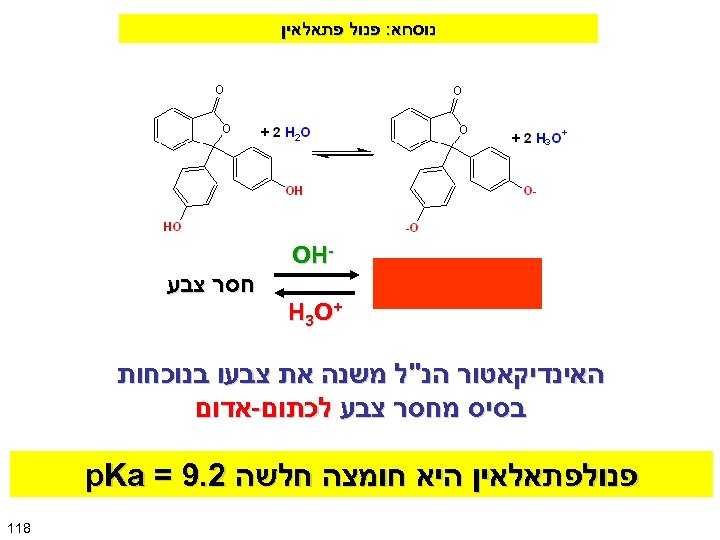
נוסחא: פנול פתאלאין OH חסר צבע + H 3 O האינדיקאטור הנ"ל משנה את צבעו בנוכחות בסיס מחסר צבע לכתום-אדום פנולפתאלאין היא חומצה חלשה 2. 9 = p. Ka 811
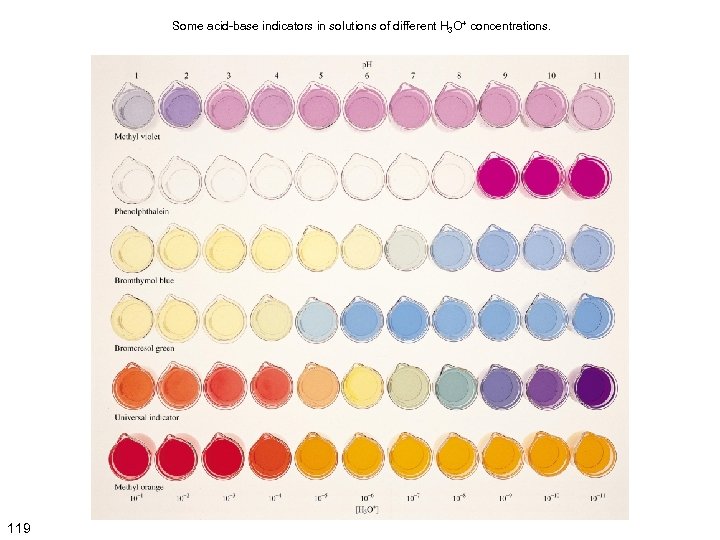
Some acid-base indicators in solutions of different H 3 O+ concentrations. 119

סתירה של חומצה על ידי בסיס - טיטרציה תהליך קביעה כמותית של חומצה )או בסיס( על ידי הוספת בסיס )או חומצה( בריכוז ידוע בצורה מבוקרת והדרגתית ומעקב אחר התגובה הכימית ביניהם עד השלמתה 2 C בסיס ריכוז ידוע 2 V ניסוי 1 C ? סיום התגובה ביצוע הסתירה 1 V נמדד חומצה, ריכוז לא ידוע 021
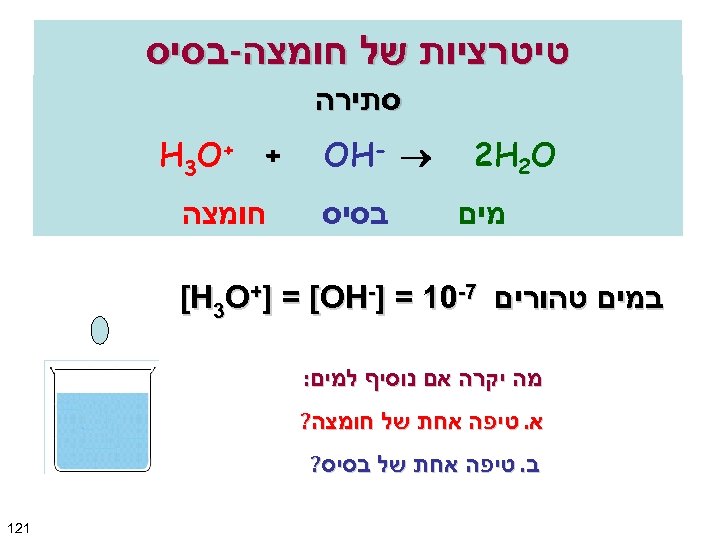
טיטרציות של חומצה-בסיס סתירה 2 H 2 O מים OH- בסיס + + H 3 O חומצה במים טהורים 7 -01 = ]- [H 3 O+] = [OH מה יקרה אם נוסיף למים: א. טיפה אחת של חומצה? ב. טיפה אחת של בסיס? 121
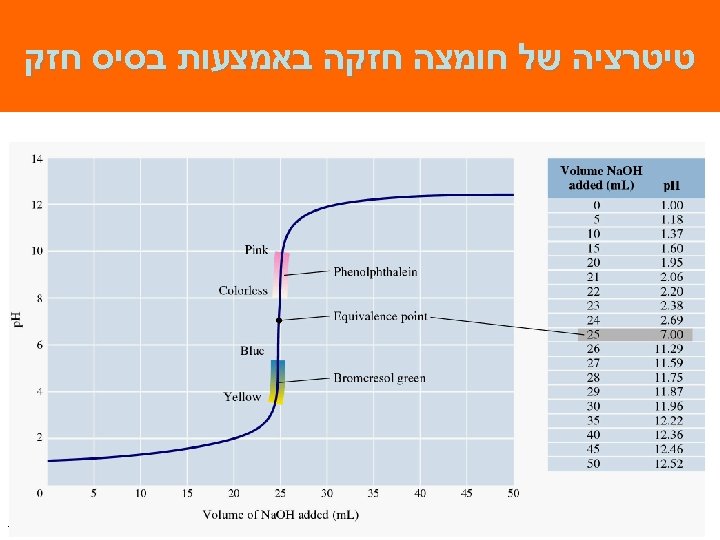
טיטרציה של חומצה חזקה באמצעות בסיס חזק 221

חומצות ובסיסים חלשים תצפיות ניסיוניות – מוליכים גרועים של חשמל בתמיסה 1. חומצת חומץ )אצטית( CH 3 COOH 2. תמיסת אמוניה 3 NH הסבר שניהם מפורקים מעט ליונים במים או במילים אחרות שניהם חומצה ובסיס חלשים 321
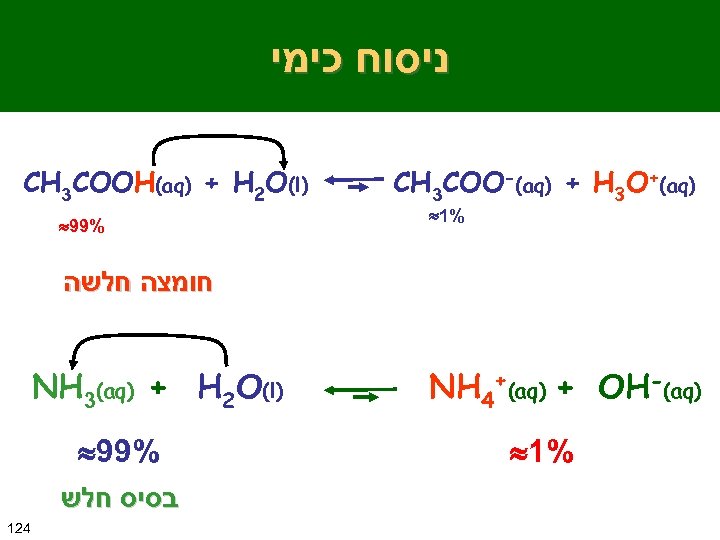
ניסוח כימי CH 3 COOH(aq) + H 2 O(l) 99% CH 3 COO-(aq) + H 3 O+(aq) 1% חומצה חלשה NH 3(aq) + H 2 O(l) 99% בסיס חלש 124 NH 4+(aq) + OH-(aq) 1%
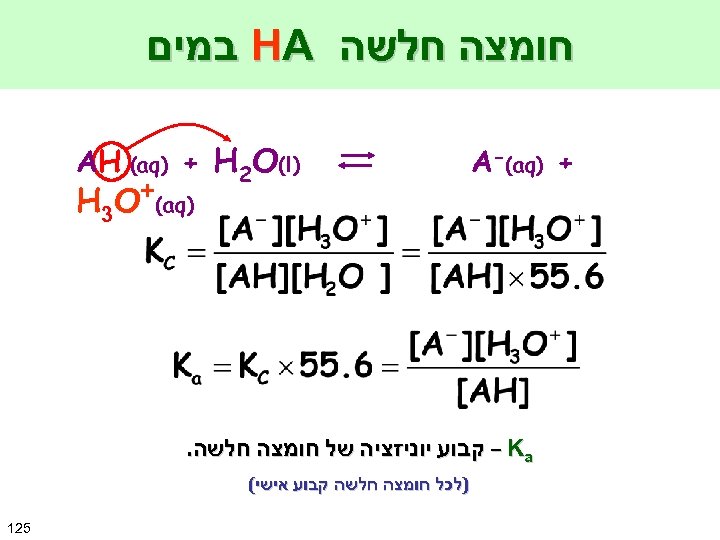
חומצה חלשה HA במים + ) A-(aq ) AH (aq) + H 2 O(l ) H 3 O+(aq – Ka קבוע יוניזציה של חומצה חלשה. )לכל חומצה חלשה קבוע אישי( 521
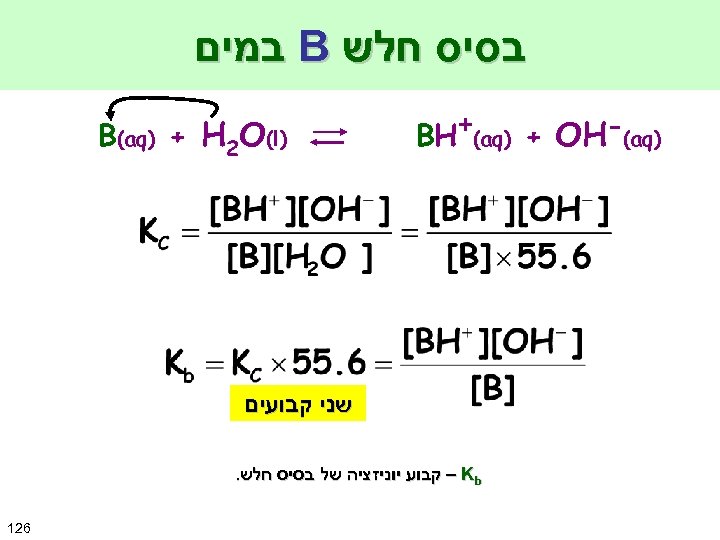
בסיס חלש B במים ) BH+(aq) + OH-(aq ) B(aq) + H 2 O(l שני קבועים – Kb קבוע יוניזציה של בסיס חלש. 621
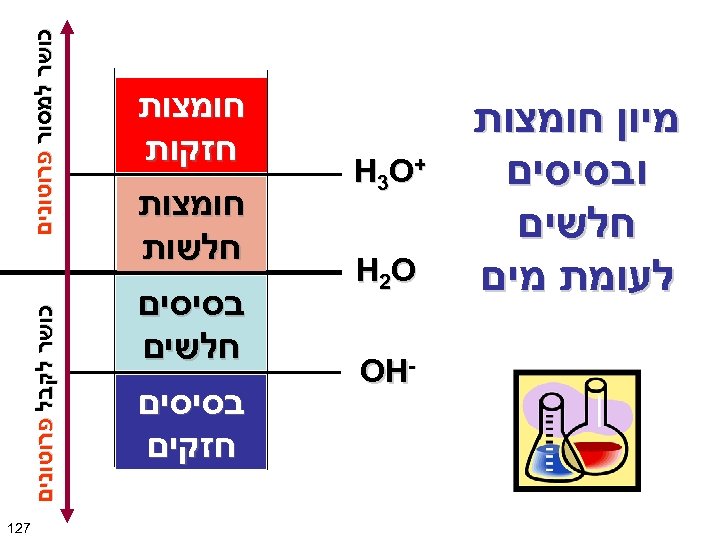
- OH בסיסים חלשים בסיסים חזקים H 2 O כושר לקבל פרוטונים + H 3 O כושר למסור פרוטונים מיון חומצות ובסיסים חלשים לעומת מים חומצות חזקות חומצות חלשות 721
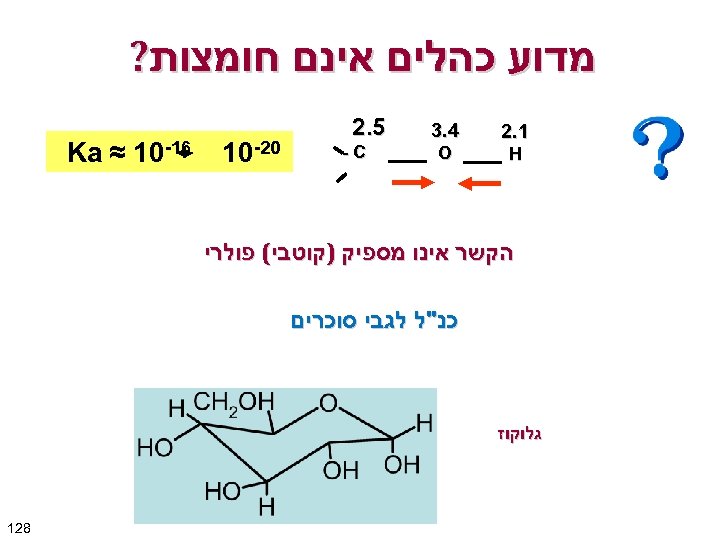
מדוע כהלים אינם חומצות? 1. 2 H 4. 3 O 5. 2 -C 02 -01 61 -01 ≈ Ka הקשר אינו מספיק )קוטבי( פולרי כנ"ל לגבי סוכרים גלוקוז 821
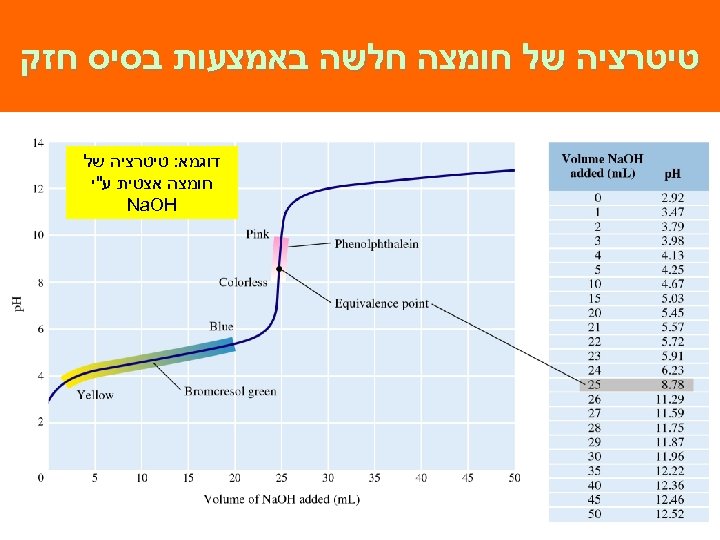
טיטרציה של חומצה חלשה באמצעות בסיס חזק דוגמא: טיטרציה של חומצה אצטית ע"י Na. OH 921
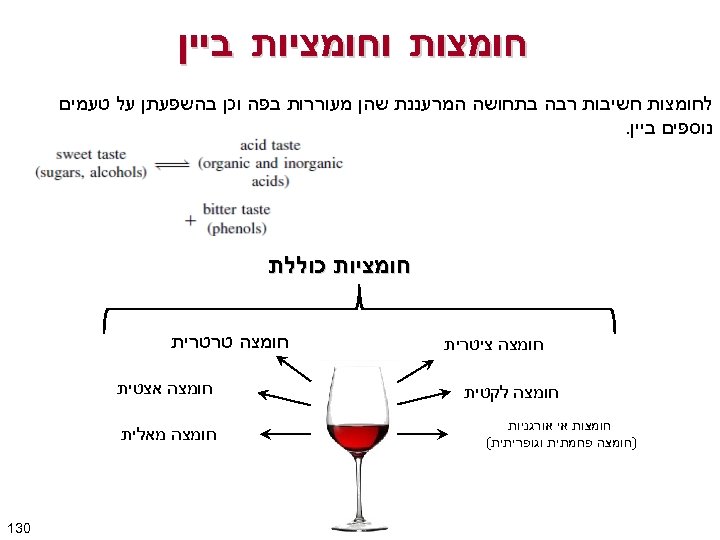
חומצות וחומציות ביין לחומצות חשיבות רבה בתחושה המרעננת שהן מעוררות בפה וכן בהשפעתן על טעמים נוספים ביין. חומציות כוללת חומצה ציטרית חומצה לקטית חומצות אי אורגניות )חומצה פחמתית וגופריתית( חומצה טרטרית חומצה אצטית חומצה מאלית 031

בופרים: בעברית - תמיסות מתריסות בופר הוא תמיסה המתנגדת לשינוי ברמת החומציות שלה )רמת ה- , (p. H כלומר: תמיסה המתנגדת לשינוי בריכוז יוני ההידרוניום ואיננה גורמת לתנודות משמעותיות ב-. p. H למעשה הבופר הוא תמיסה המכילה חומצה חלשה ובסיס מצומד שלה. החומצה מגיבה עם מים לתת את הבסיס ויון הידורוניום, ומצד שני הבסיס מגיב עם יוני הידורוניום לתת חזרה את החומצה. ) A-(aq) + H 3 O+(aq חומצה בסיס צמוד ) HA (aq) + H 2 O(l בסיס חומצה
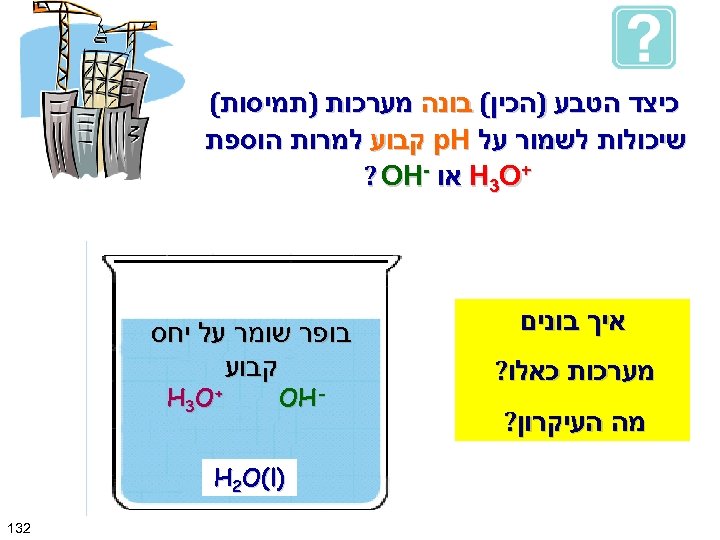
כיצד הטבע )הכין( בונה מערכות )תמיסות( שיכולות לשמור על p. H קבוע למרות הוספת + H 3 O או - ? OH איך בונים מערכות כאלו? מה העיקרון? בופר שומר על יחס קבוע - OH + H 3 O ) H 2 O(l 231
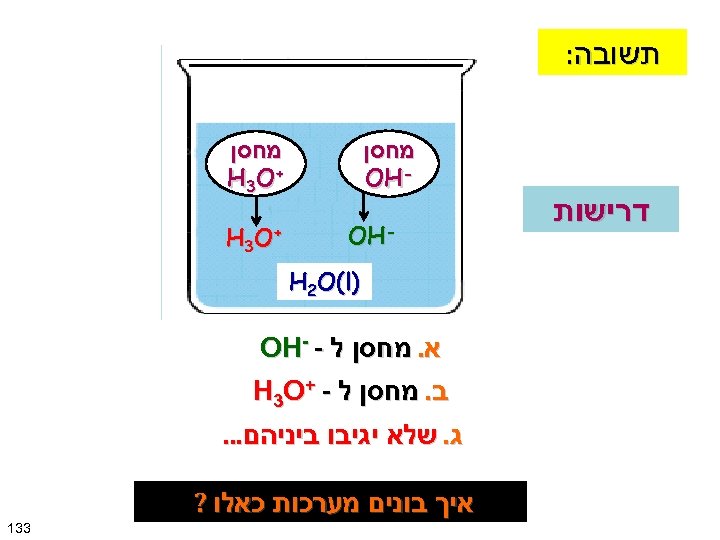
תשובה: דרישות מחסן - OH מחסן + H 3 O - OH + H 3 O ) H 2 O(l א. מחסן ל - - OH ב. מחסן ל - + H 3 O ג. שלא יגיבו ביניהם. . . איך בונים מערכות כאלו ? 331
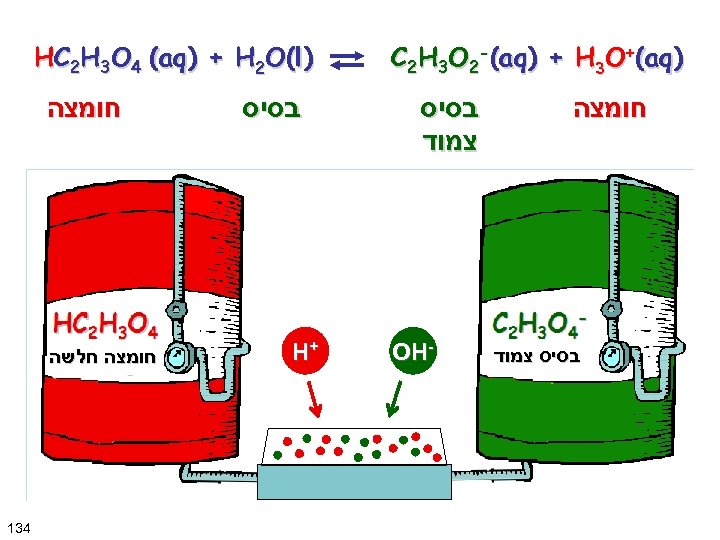
) C 2 H 3 O 2 -(aq) + H 3 O+(aq חומצה בסיס צמוד בסיס צמוד - OH ) HC 2 H 3 O 4 (aq) + H 2 O(l בסיס + H חומצה חלשה 431
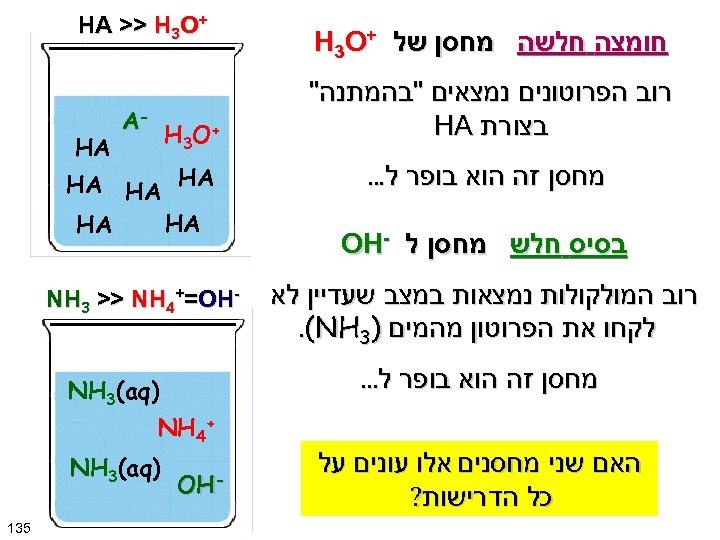
חומצה חלשה מחסן של + H 3 O רוב הפרוטונים נמצאים "בהמתנה" בצורת HA מחסן זה הוא בופר ל. . . בסיס חלש מחסן ל - OH רוב המולקולות נמצאות במצב שעדיין לא לקחו את הפרוטון מהמים )3. (NH + HA >> H 3 O - A + H 3 O HA HA HA - NH 3 >> NH 4+=OH מחסן זה הוא בופר ל. . . ) NH 3(aq +4 NH האם שני מחסנים אלו עונים על כל הדרישות? - OH ) NH 3(aq 531
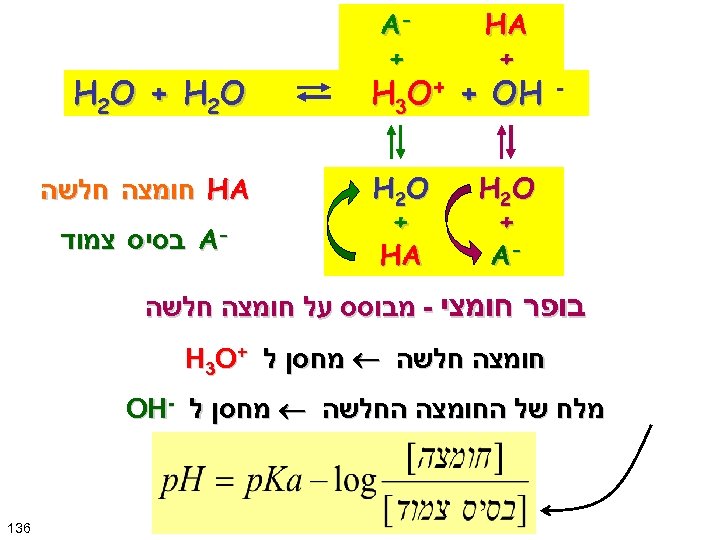
H 2 O + - A - HA + H 2 O + HA H 3 O+ + OH H 2 O + H 2 O HA חומצה חלשה - A בסיס צמוד בופר חומצי - מבוסס על חומצה חלשה מחסן ל + H 3 O מלח של החומצה החלשה מחסן ל - OH 631
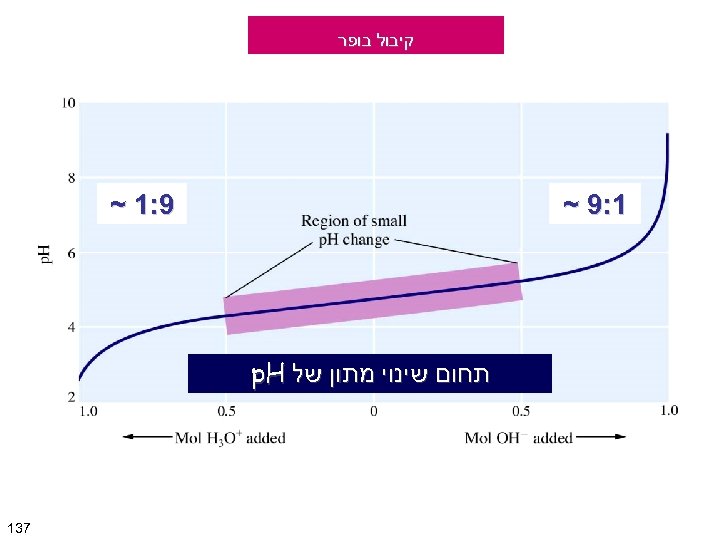
קיבול בופר 9: 1 ~ 1: 9 ~ תחום שינוי מתון של p. H 731
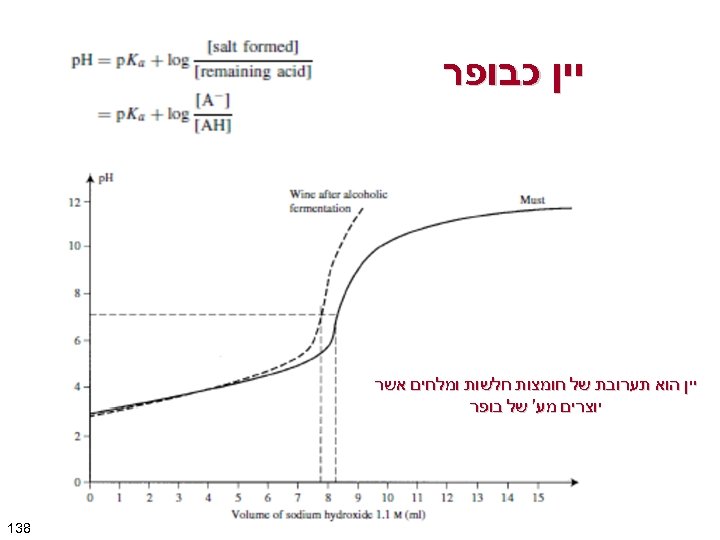
יין כבופר יין הוא תערובת של חומצות חלשות ומלחים אשר יוצרים מע' של בופר 831

מבוא לכימיה אורגנית היא ענף של הכימיה העוסק בחקר תרכובות אורגניות, שהן תרכובות המכילות פחמן ומימן 931

פחמימנים ) (Hydrocarbons הם תרכובות אורגניות המכילות אך ורק אטומי פחמן ומימן. מבחינים בין שלושה סוגי פחמימנים, לפי סוגי הקשרים הקוולנטיים בין אטומי הפחמן שלהם: 041

פחמימנים ) (Hydrocarbons הם תרכובות אורגניות המכילות אך ורק אטומי פחמן ומימן. מבחינים בין שלושה סוגי פחמימנים, לפי סוגי הקשרים הקוולנטיים בין אטומי הפחמן שלהם: אליפטיים )שם כולל לכל מולקולה שאינה ארומטית(: 1. רוויים ) (Saturated פחמימנים המכילים קשרים בודדים בלבד ונקראים אלקאנים. 141

פחמימנים ) (Hydrocarbons הם תרכובות אורגניות המכילות אך ורק אטומי פחמן ומימן. מבחינים בין שלושה סוגי פחמימנים, לפי סוגי הקשרים הקוולנטיים בין אטומי הפחמן שלהם: אליפטיים )שם כולל לכל מולקולה שאינה ארומטית(: 1. רוויים ) (Saturated פחמימנים המכילים קשרים בודדים בלבד ונקראים אלקאנים. 2. בלתי-רוויים: מכילים קשרים כפולים או משולשים )קשר אחד לפחות בכל מולקולה(. אלקנים, אלקינים ווינילים. 241

פחמימנים ) (Hydrocarbons הם תרכובות אורגניות המכילות אך ורק אטומי פחמן ומימן. מבחינים בין שלושה סוגי פחמימנים, לפי סוגי הקשרים הקוולנטיים בין אטומי הפחמן שלהם: אליפטיים )שם כולל לכל מולקולה שאינה ארומטית(: 1. רוויים ) (Saturated פחמימנים המכילים קשרים בודדים בלבד ונקראים אלקאנים. 2. בלתי-רוויים: מכילים קשרים כפולים או משולשים )קשר אחד לפחות בכל מולקולה(. אלקנים, אלקינים ווינילים. 3. ארומטיים: מכילים טבעות המכילות קשרים כפולים מצומדים. 341
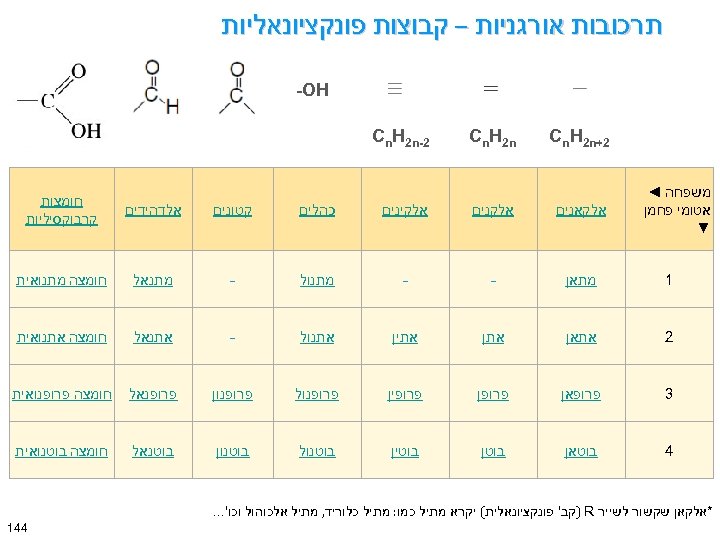
תרכובות אורגניות – קבוצות פונקציונאליות -OH 2+ Cn. H 2 n משפחה ◄ אטומי פחמן ▼ Cn. H 2 n 2 - Cn. H 2 n אלקאנים אלקינים כהלים קטונים אלדהידים חומצות קרבוקסיליות 1 מתאן - - מתנול - מתנאל חומצה מתנואית 2 אתאן אתין אתנול - אתנאל חומצה אתנואית 3 פרופאן פרופין פרופנול פרופנון פרופנאל חומצה פרופנואית 4 בוטאן בוטין בוטנול בוטנון בוטנאל חומצה בוטנואית *אלקאן שקשור לשייר ) R קב' פונקציונאלית( יקרא מתיל כמו: מתיל כלוריד, מתיל אלכוהול וכו'. . . 441
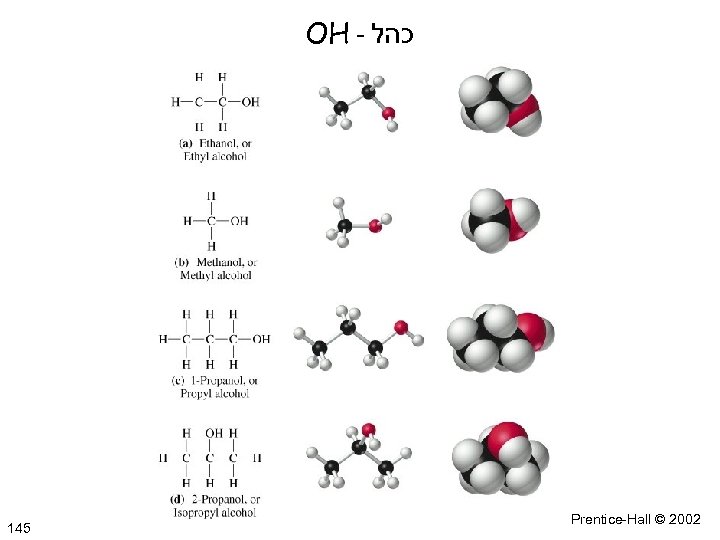
OH - כהל General Chemistry: Chapter 3 145 Prentice-Hall © 2002
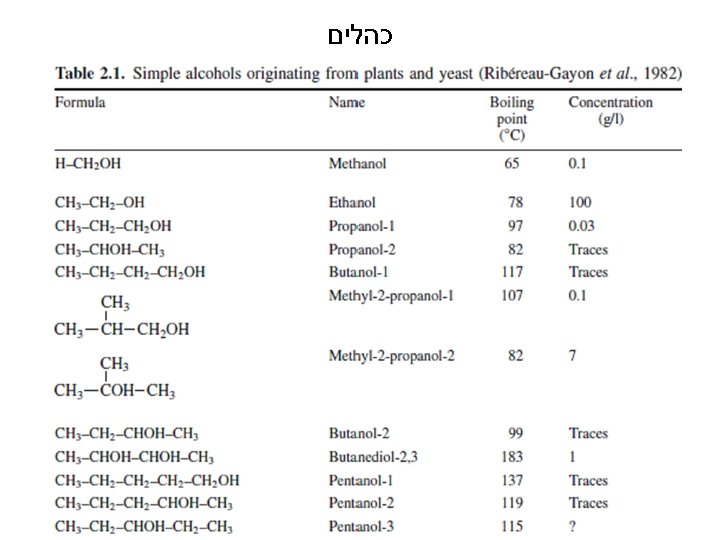
כהלים 641
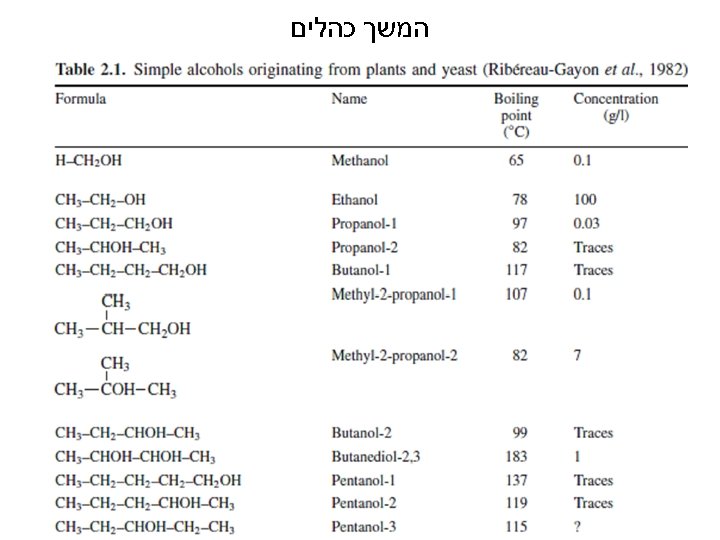
המשך כהלים 741
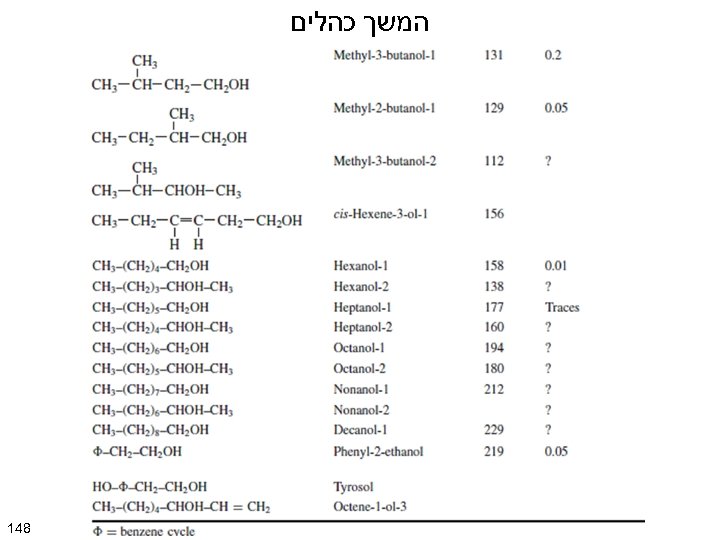
המשך כהלים 841
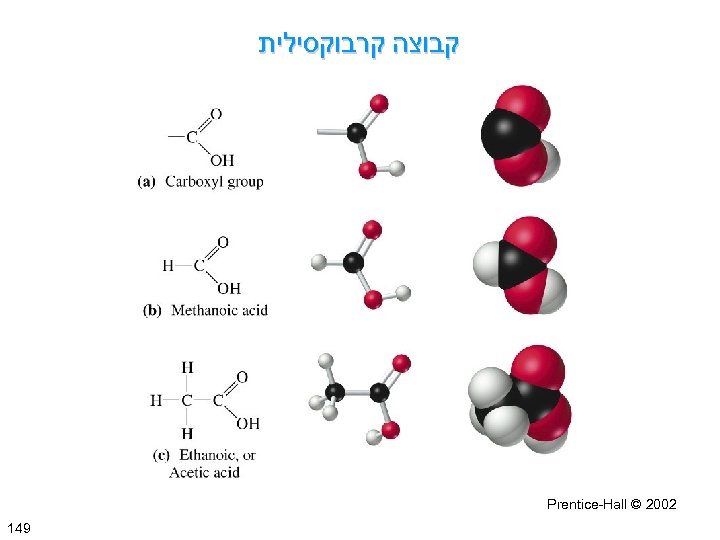
קבוצה קרבוקסילית 2002 © Prentice-Hall 941
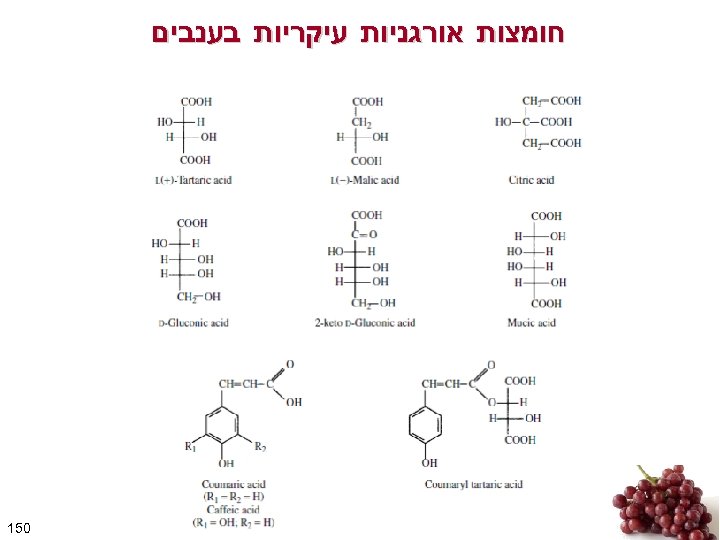
חומצות אורגניות עיקריות בענבים 051
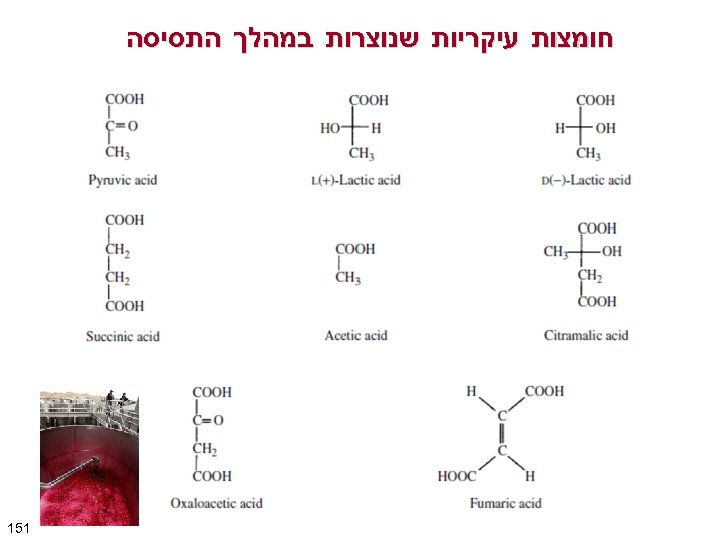
חומצות עיקריות שנוצרות במהלך התסיסה 151
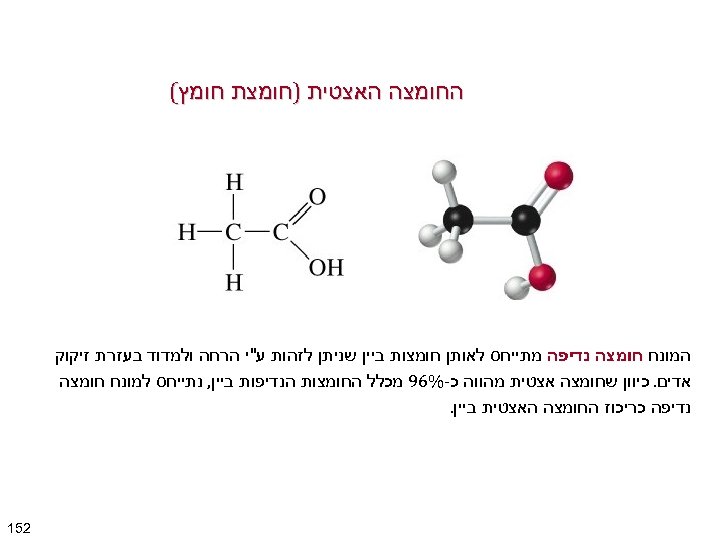
החומצה האצטית )חומצת חומץ( המונח חומצה נדיפה מתייחס לאותן חומצות ביין שניתן לזהות ע"י הרחה ולמדוד בעזרת זיקוק אדים. כיוון שחומצה אצטית מהווה כ-%69 מכלל החומצות הנדיפות ביין, נתייחס למונח חומצה נדיפה כריכוז החומצה האצטית ביין. 251
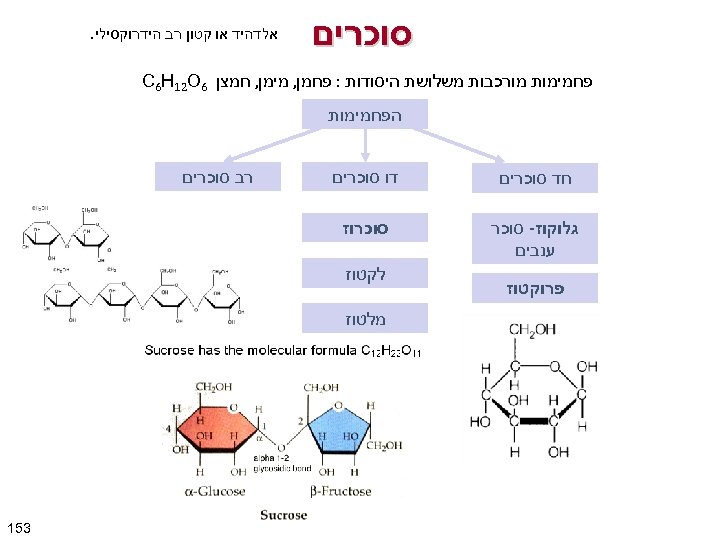
סוכרים אלדהיד או קטון רב הידרוקסילי. פחמימות מורכבות משלושת היסודות : פחמן, מימן, חמצן 6 C 6 H 12 O הפחמימות חד סוכרים דו סוכרים גלוקוז- סוכר ענבים סוכרוז פרוקטוז רב סוכרים לקטוז מלטוז 351

שלמי תודה מיוחדת לדר' רונית יערי מנהלת המעבדה במכון היין הישראלי 451

תודה על ההקשבה! 551
53b88590e2cf5219882ab24062b4c814.ppt