Лекция кинетика.pptx
- Количество слайдов: 24
 ӨЗДІГІНЕН ЖҮРЕТІН ПРОЦЕСТЕРДІ РЕТТЕЙТІН ФАКТОРЛАР G = H - T S Процестің өздігінен жүру мүкіндігі: Н<0, S>0 Кез келген температурада жүру мүмкін Н<0, S<0 Н>0, S>0 Төменгі температураларда жүру мүмкін Жоғары температураларда жүру мүмкін Н>0, S<0 Процесс мүмкін емес
ӨЗДІГІНЕН ЖҮРЕТІН ПРОЦЕСТЕРДІ РЕТТЕЙТІН ФАКТОРЛАР G = H - T S Процестің өздігінен жүру мүкіндігі: Н<0, S>0 Кез келген температурада жүру мүмкін Н<0, S<0 Н>0, S>0 Төменгі температураларда жүру мүмкін Жоғары температураларда жүру мүмкін Н>0, S<0 Процесс мүмкін емес
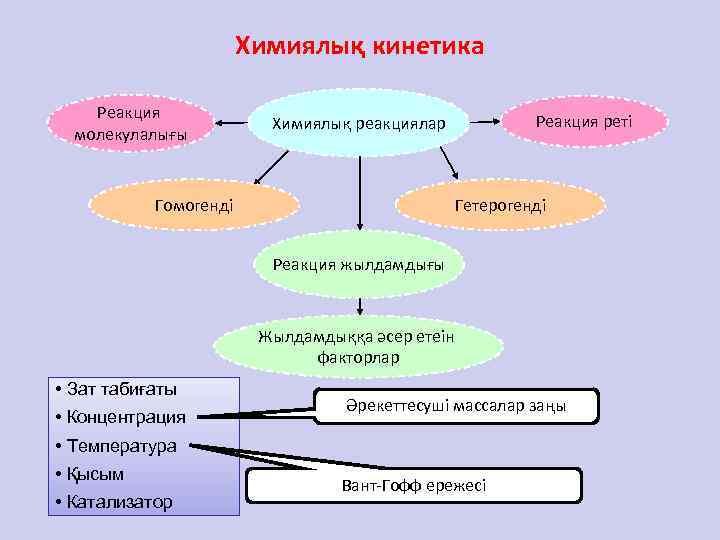 Химиялық кинетика Реакция молекулалығы Реакция реті Химиялық реакциялар Гомогенді Гетерогенді Реакция жылдамдығы Жылдамдыққа әсер етеін факторлар • Зат табиғаты • Концентрация Әрекеттесуші массалар заңы • Температура • Қысым • Катализатор Вант-Гофф ережесі
Химиялық кинетика Реакция молекулалығы Реакция реті Химиялық реакциялар Гомогенді Гетерогенді Реакция жылдамдығы Жылдамдыққа әсер етеін факторлар • Зат табиғаты • Концентрация Әрекеттесуші массалар заңы • Температура • Қысым • Катализатор Вант-Гофф ережесі
 Гомогенді реакцияда реакцияның барлық заттары бір агрегаттық күйге өтеді а) ерітіндіде: NH 3(г) + HCl (с) NH 4 Cl(с) б) газ фазада: 2 SO 2(г) + O 2(г) 2 SO 3(г) Гетерогенді реакцияда аз дегенде бір зат өзінің агрегаттық күйімен ерекшеленеді Са. Cl 2(крист) + H 2 SO 4(с) Ca. SO 4 (қатты) + 2 HCl(с)
Гомогенді реакцияда реакцияның барлық заттары бір агрегаттық күйге өтеді а) ерітіндіде: NH 3(г) + HCl (с) NH 4 Cl(с) б) газ фазада: 2 SO 2(г) + O 2(г) 2 SO 3(г) Гетерогенді реакцияда аз дегенде бір зат өзінің агрегаттық күйімен ерекшеленеді Са. Cl 2(крист) + H 2 SO 4(с) Ca. SO 4 (қатты) + 2 HCl(с)
 Химиялық реакциялардың жылдамдықтарын, оларға әсер ететін факторлар және олардың жүру механизмін зерттейтін химияның бөлімін химиялық кинетика деп атайды. Химиялық кинетиканың негізгі шамаларының бірі – реакция жылдамдығы. Химиялық реакцияның жылдамдығы деп көлем өзгермеген жағдайда реакцияға қатысатын заттардың біреуінің концентрациясының ( C) белгілі бір уақыт бірлігінде ( t) өзгеруін айтады:
Химиялық реакциялардың жылдамдықтарын, оларға әсер ететін факторлар және олардың жүру механизмін зерттейтін химияның бөлімін химиялық кинетика деп атайды. Химиялық кинетиканың негізгі шамаларының бірі – реакция жылдамдығы. Химиялық реакцияның жылдамдығы деп көлем өзгермеген жағдайда реакцияға қатысатын заттардың біреуінің концентрациясының ( C) белгілі бір уақыт бірлігінде ( t) өзгеруін айтады:
 Қарапайым (бір сатылы) реакциялар Реакцияларды химиялық әрекеттесудің элементарлық актісіне қатысатын молекулалардың санымен, яғни реакция молекулалығымен жіктеуге болады Мономолекулық А I 2 өнімдер 2 I Бимолекулалық А + В NO(г) + O 3(г) өнімдер NO 2(г) + O 2(г) Үшмолекулалық (сирек кездеседі) 2 NO(г) + H 2(г) N 2 O(г) + H 2 O(г)
Қарапайым (бір сатылы) реакциялар Реакцияларды химиялық әрекеттесудің элементарлық актісіне қатысатын молекулалардың санымен, яғни реакция молекулалығымен жіктеуге болады Мономолекулық А I 2 өнімдер 2 I Бимолекулалық А + В NO(г) + O 3(г) өнімдер NO 2(г) + O 2(г) Үшмолекулалық (сирек кездеседі) 2 NO(г) + H 2(г) N 2 O(г) + H 2 O(г)
 Күрделі реакциялар – жүйеде бірнеше (минимум екеу) қарапайым реакциялар бірден бірнеше сатыда жүреді. Оларға: - Реакцияның реті әртүрлі қайтымды реакциялар, - Реакцияның реті әртүрлі параллельді реакциялар, - кезекті реакциялар, - қатар жүретін реакциялар. Мұнда сонымен бірге тізбекті және фотохимиялық реакциялар жатады. Күрделі реакцияның жалпы жылдамдығы ең баяу жүретін реакцияның (сатының) жылдамыдығымен анықталады
Күрделі реакциялар – жүйеде бірнеше (минимум екеу) қарапайым реакциялар бірден бірнеше сатыда жүреді. Оларға: - Реакцияның реті әртүрлі қайтымды реакциялар, - Реакцияның реті әртүрлі параллельді реакциялар, - кезекті реакциялар, - қатар жүретін реакциялар. Мұнда сонымен бірге тізбекті және фотохимиялық реакциялар жатады. Күрделі реакцияның жалпы жылдамдығы ең баяу жүретін реакцияның (сатының) жылдамыдығымен анықталады
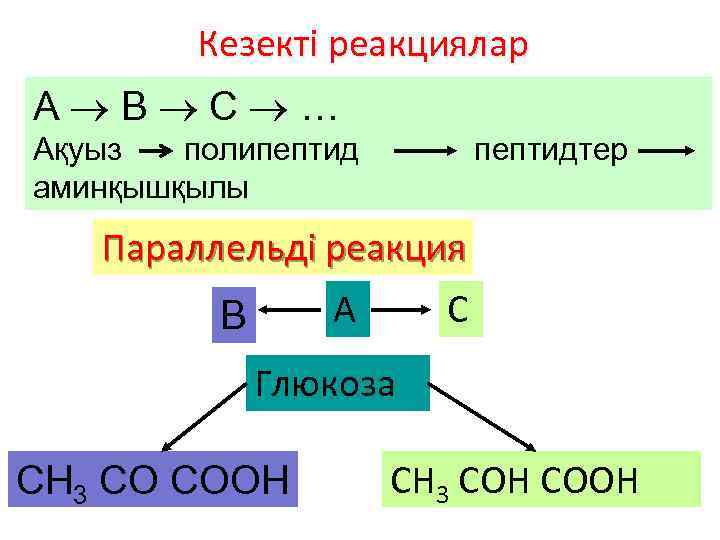 Кезекті реакциялар А B C … Ақуыз полипептид пептидтер аминқышқылы Параллельді реакция A B C Глюкоза СН 3 СО СООН СН 3 СОН СООН
Кезекті реакциялар А B C … Ақуыз полипептид пептидтер аминқышқылы Параллельді реакция A B C Глюкоза СН 3 СО СООН СН 3 СОН СООН
 Қатар жүретін реакция Реакция түрі: А+В→М (1) және A+D→N (2) Мұнда екінші реакция (2) тек бірінші реакция басталып, сонымен қатар жүреді, яғни онымен индуциирленеді. В заты индуктор, ал 1 -і және 2 -і реакцияларға қатысатын А заты актор деп аталады. D заты – акцептор. Мұндай реакцияларда байланыстырғыш компонет ретінде 1 -ші реакцияда түзілетін М-аралық өнім болып табылады.
Қатар жүретін реакция Реакция түрі: А+В→М (1) және A+D→N (2) Мұнда екінші реакция (2) тек бірінші реакция басталып, сонымен қатар жүреді, яғни онымен индуциирленеді. В заты индуктор, ал 1 -і және 2 -і реакцияларға қатысатын А заты актор деп аталады. D заты – акцептор. Мұндай реакцияларда байланыстырғыш компонет ретінде 1 -ші реакцияда түзілетін М-аралық өнім болып табылады.
 Цепные реакции Многие гомогенные реакции окисления, расщепления и др. имеют такие особенности, которые не могут быть объяснены на основе рассмотренных нами закономерностях – это: 1) реакции не подчиняются уравнению первого, второго и высшего порядков; 2) скорость реакции очень велика; 3) необычайная чувствительность к следам примесей; 4) зависимость скорости реакции от формы и размеров реакционного сосуда, а так же материала стенок из которого изготовлен реакционный сосуд; 5) наличие индукционного периода, когда реакция начинается не сразу, а лишь спустя некоторое время; 6) возможность протекания реакции в определённом интервале давления. Все эти положения легко объясняются цепным механизмом реакции.
Цепные реакции Многие гомогенные реакции окисления, расщепления и др. имеют такие особенности, которые не могут быть объяснены на основе рассмотренных нами закономерностях – это: 1) реакции не подчиняются уравнению первого, второго и высшего порядков; 2) скорость реакции очень велика; 3) необычайная чувствительность к следам примесей; 4) зависимость скорости реакции от формы и размеров реакционного сосуда, а так же материала стенок из которого изготовлен реакционный сосуд; 5) наличие индукционного периода, когда реакция начинается не сразу, а лишь спустя некоторое время; 6) возможность протекания реакции в определённом интервале давления. Все эти положения легко объясняются цепным механизмом реакции.
 Сущность заключается в том, что вначале в системе образуются активные частицы чаще всего это свободные радикалы. Эти частицы вступают в реакцию, но при этом вновь возникает валентно насыщенный остаток и радикал. Процесс исчезновения и появления каждой активной частицы и создаёт цепь превращений. Любая цепная реакция может быть представлена как реакция, состоящая из трёх стадий: 1) зарождение активной частицы (зарождение цепи); 2) рост цепи; 3) обрыв цепи.
Сущность заключается в том, что вначале в системе образуются активные частицы чаще всего это свободные радикалы. Эти частицы вступают в реакцию, но при этом вновь возникает валентно насыщенный остаток и радикал. Процесс исчезновения и появления каждой активной частицы и создаёт цепь превращений. Любая цепная реакция может быть представлена как реакция, состоящая из трёх стадий: 1) зарождение активной частицы (зарождение цепи); 2) рост цепи; 3) обрыв цепи.
 Химиялық реакцияның жылдамдығы уақыт бірлігінде заттардың концентрацияларының өзгеруі Моль/м 3 сек Моль/м 2 сек Моль/л сек
Химиялық реакцияның жылдамдығы уақыт бірлігінде заттардың концентрацияларының өзгеруі Моль/м 3 сек Моль/м 2 сек Моль/л сек
 РЕАКЦИЯ ЖЫЛДАМДЫҒЫНА ӘСЕР ЕТЕТІН ФАКТОРЛАР • Заттардың концентрациясы • Температура • Катализаторлар • Қысым (газ жүйелері үшін) • Әрекеттесетін заттардың табиғаты • Қатты заттар үшін жанасу беттерінің аумағы Н 2 + I 2 2 НI (баяу жүреді) Н+ + ОН– Н 2 О (тез жүреді) О 2 + О О 3 (тым лезде) Н • + Cl • HCl (өте лезде)
РЕАКЦИЯ ЖЫЛДАМДЫҒЫНА ӘСЕР ЕТЕТІН ФАКТОРЛАР • Заттардың концентрациясы • Температура • Катализаторлар • Қысым (газ жүйелері үшін) • Әрекеттесетін заттардың табиғаты • Қатты заттар үшін жанасу беттерінің аумағы Н 2 + I 2 2 НI (баяу жүреді) Н+ + ОН– Н 2 О (тез жүреді) О 2 + О О 3 (тым лезде) Н • + Cl • HCl (өте лезде)
 ӘРЕКЕТТЕСУШЫ МАССАЛАР ЗАҢЫ Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях их стехиометрических коэффициентов. a. A + b. B + с. С + d. D Пример простой реакции: 2 SO 2 + O 2 = 2 SO 3 = k ·[SO 2] 2·[O 2] При этом порядок реакции равен: n=a+b => n=2+1=3 Константа скорости реакции k (индивидуальная характеристика реакции) равна скорости реакции при концентрациях веществ, равных 1 моль/л. Она зависит от природы реагентов, температуры и наличия катализаторов. Порядок реакции (n) по данному веществу — показатель степени при концентрации этого вещества в кинетическом уравнении реакции.
ӘРЕКЕТТЕСУШЫ МАССАЛАР ЗАҢЫ Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях их стехиометрических коэффициентов. a. A + b. B + с. С + d. D Пример простой реакции: 2 SO 2 + O 2 = 2 SO 3 = k ·[SO 2] 2·[O 2] При этом порядок реакции равен: n=a+b => n=2+1=3 Константа скорости реакции k (индивидуальная характеристика реакции) равна скорости реакции при концентрациях веществ, равных 1 моль/л. Она зависит от природы реагентов, температуры и наличия катализаторов. Порядок реакции (n) по данному веществу — показатель степени при концентрации этого вещества в кинетическом уравнении реакции.
 Применение Закона действующих масс для сложных реакций a. A + b. B + c. C + … Показатели , , частные порядки реакций n = + + - общий порядок реакций + + a+b+c
Применение Закона действующих масс для сложных реакций a. A + b. B + c. C + … Показатели , , частные порядки реакций n = + + - общий порядок реакций + + a+b+c
 ЗАВИСИМОСТЬ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ (Правило Вант-Гоффа) При увеличении температуры системы на каждые 10 градусов скорость простой реакции возрастает примерно в 2 4 раза: - температурный коэффициент – это число, показывающее во сколько раз увеличится скорость реакции при повышении температуры на 10 градусов Пример: как изменится скорость реакции при повышении температуры на если =3 Решение: Ответ: скорость реакции увеличится в 9 раз
ЗАВИСИМОСТЬ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ (Правило Вант-Гоффа) При увеличении температуры системы на каждые 10 градусов скорость простой реакции возрастает примерно в 2 4 раза: - температурный коэффициент – это число, показывающее во сколько раз увеличится скорость реакции при повышении температуры на 10 градусов Пример: как изменится скорость реакции при повышении температуры на если =3 Решение: Ответ: скорость реакции увеличится в 9 раз
 ЭНЕРГИЯ АКТИВАЦИИ. ТЕОРИЯ СТОЛКНОВЕНИЙ АРРЕНИУСА Для совершения элементарного акта химического взаимодействия, реагирующие частицы должны столкнуться друг с другом. Однако, не каждое столкновение частиц приводит к их химическому взаимодействию. Следовательно, сталкивающиеся частицы должны обладать энергией, достаточной для преодоления сил отталкивания (энергетического барьера), возникающих между их электронными оболочками. Такие, реакционно-способные частицы называют активными, а энергия, необходимая для преодоления энергетического барьера, называется энергией активации реакции. Энергия активации (Еа, к. Дж/моль) – это избыточный запас энергии молекулы над средне статистическим запасом энергии, позволяющий молекуле реализовать химическое взаимодействие
ЭНЕРГИЯ АКТИВАЦИИ. ТЕОРИЯ СТОЛКНОВЕНИЙ АРРЕНИУСА Для совершения элементарного акта химического взаимодействия, реагирующие частицы должны столкнуться друг с другом. Однако, не каждое столкновение частиц приводит к их химическому взаимодействию. Следовательно, сталкивающиеся частицы должны обладать энергией, достаточной для преодоления сил отталкивания (энергетического барьера), возникающих между их электронными оболочками. Такие, реакционно-способные частицы называют активными, а энергия, необходимая для преодоления энергетического барьера, называется энергией активации реакции. Энергия активации (Еа, к. Дж/моль) – это избыточный запас энергии молекулы над средне статистическим запасом энергии, позволяющий молекуле реализовать химическое взаимодействие
 Cогласно, молекулярно-кинетической теории газов для каждой системы существует порог энергии Еа, начиная с которого энергия достаточна для протекания реакции Еа меняется от 0 до 500 к. Дж/моль Еа >100 к. Дж – велика, скорость реакции – мала Еа <50 к. Дж – мала, скорость – велика УРАВНЕНИЕ АРРЕНИУСА Предэкспоненциальный множитель (А) дает некоторую характеристику полного числа столкновений - доля результативных столкновений
Cогласно, молекулярно-кинетической теории газов для каждой системы существует порог энергии Еа, начиная с которого энергия достаточна для протекания реакции Еа меняется от 0 до 500 к. Дж/моль Еа >100 к. Дж – велика, скорость реакции – мала Еа <50 к. Дж – мала, скорость – велика УРАВНЕНИЕ АРРЕНИУСА Предэкспоненциальный множитель (А) дает некоторую характеристику полного числа столкновений - доля результативных столкновений
 ОПРЕДЕЛЕНИЕ ЭНЕРГИИ АКТИВАЦИИ
ОПРЕДЕЛЕНИЕ ЭНЕРГИИ АКТИВАЦИИ
 КАТАЛИЗАТОРЫ. КАТАЛИЗ В химической практике часто используют метод ускорения химических реакций – катализ. Катализ – это явление ускорения реакции под действием веществ не расходующихся в реакции. Каталитические реакции – это реакции, в которых изменяется путь при неизменных реагентах и продуктах. Катализатор – это вещество, которое многократно участвует в промежуточных стадиях реакции, но выходит из нее химически неизменным. Еа промежуточных стадий с участием катализатора меньше, чем Еа р-ции без катализатора
КАТАЛИЗАТОРЫ. КАТАЛИЗ В химической практике часто используют метод ускорения химических реакций – катализ. Катализ – это явление ускорения реакции под действием веществ не расходующихся в реакции. Каталитические реакции – это реакции, в которых изменяется путь при неизменных реагентах и продуктах. Катализатор – это вещество, которое многократно участвует в промежуточных стадиях реакции, но выходит из нее химически неизменным. Еа промежуточных стадий с участием катализатора меньше, чем Еа р-ции без катализатора
![КАТАЛИЗ Положительный Отрицательный Автокатализ [A…B]' G [A…K]' A+B [B…AK]' ∆(∆G)' Путь реакции яды – КАТАЛИЗ Положительный Отрицательный Автокатализ [A…B]' G [A…K]' A+B [B…AK]' ∆(∆G)' Путь реакции яды –](https://present5.com/presentation/1/-77111444_339870736.pdf-img/-77111444_339870736.pdf-20.jpg) КАТАЛИЗ Положительный Отрицательный Автокатализ [A…B]' G [A…K]' A+B [B…AK]' ∆(∆G)' Путь реакции яды – вещества, ухудшающие действие катализаторов. Промоторы – вещества, +K Gисходное Каталитические AB Gконечное усиливающие катализаторов. действие Ингибиторы – вещества, уменьшающие реакции. скорость
КАТАЛИЗ Положительный Отрицательный Автокатализ [A…B]' G [A…K]' A+B [B…AK]' ∆(∆G)' Путь реакции яды – вещества, ухудшающие действие катализаторов. Промоторы – вещества, +K Gисходное Каталитические AB Gконечное усиливающие катализаторов. действие Ингибиторы – вещества, уменьшающие реакции. скорость
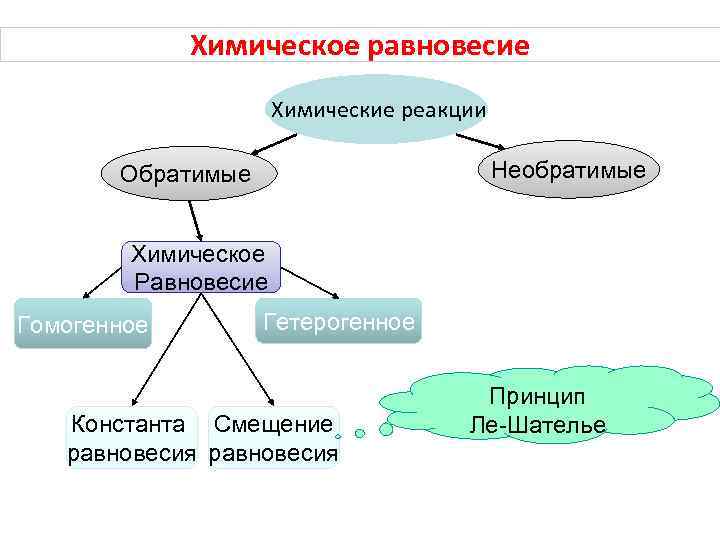 Химическое равновесие Химические реакции Необратимые Обратимые Химическое Равновесие Гомогенное Гетерогенное Константа Смещение равновесия Принцип Ле-Шателье
Химическое равновесие Химические реакции Необратимые Обратимые Химическое Равновесие Гомогенное Гетерогенное Константа Смещение равновесия Принцип Ле-Шателье
 Химическое равновесие в гомогенных системах 2 NO 2 N 2 O 4 ∆G 0 = RT ln. Kp
Химическое равновесие в гомогенных системах 2 NO 2 N 2 O 4 ∆G 0 = RT ln. Kp
 Смещение химического равновесия Принцип Ле-Шателье: если находящаяся в химическом равновесии система подвергается внешнему воздействию, то в ней возникают процессы, стремящиеся ослабить это воздействие. Анри-Луи Ле-Шателье (1850– 1936 ) константа химического равновесия 0 неидущие реакции 10 -6 обратимые реакции 106 необратимые реакции
Смещение химического равновесия Принцип Ле-Шателье: если находящаяся в химическом равновесии система подвергается внешнему воздействию, то в ней возникают процессы, стремящиеся ослабить это воздействие. Анри-Луи Ле-Шателье (1850– 1936 ) константа химического равновесия 0 неидущие реакции 10 -6 обратимые реакции 106 необратимые реакции
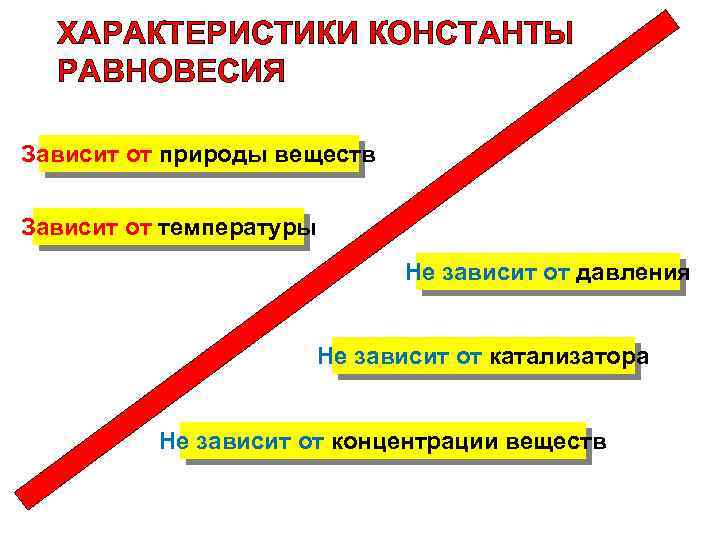 ХАРАКТЕРИСТИКИ КОНСТАНТЫ РАВНОВЕСИЯ Зависит от природы веществ Зависит от температуры Не зависит от давления Не зависит от катализатора Не зависит от концентрации веществ
ХАРАКТЕРИСТИКИ КОНСТАНТЫ РАВНОВЕСИЯ Зависит от природы веществ Зависит от температуры Не зависит от давления Не зависит от катализатора Не зависит от концентрации веществ


