Шаматова Г_Ж_ ЭДТ.ppt
- Количество слайдов: 36

Өскемен қаласы химия-биология бағытындағы Назарбаев Зияткерлік мектебі Химия пәнінің мұғалімі: Шаматова Гаухар Жанибековна 2011 жыл

• Адамнан ғылым айла асырмаған, құпиясын құлыптап жасырмаған. Кел, бәріміз ғылымның тілін зерттеп, Бір жұмбағын ашайық ашылмаған.

Электролиттік диссоциация

Электролиттік диссоциация теориясы

Фарадея терминдері 1833 -1834 гг. Майкл Фарадей (1791 -1867) Ион. Катион. Анион. Электролит. Катод. Анод. Электролиз. Диэлектрдік өткізгіштік -

Менделеевтің ерітінділер теориясы 1865 -1887 ж. Ерітіндінің гидраттану теориясы 1865 г. Докторлық диссертация «спирттердің сумен қосылысы» 1887 г. «салмақтары арқылы сулы ерітінділерді зерттеу. » Д. И. Менделеев (1834 -1907) 233 затты құрамындағы тығыздықтары арқылы H 2 SO 4 анықтады H 2 SO 4 H 2 O 1889 ж. РФХО отырысында H 2 SO 4 6 H 2 O «судағы ерітінділердің ерігіштік диссосиациясы» H 2 SO 4 150 H 2 O

ЭДТ-сының ашылуы 1857 ж. Р. Клаузиус электрөткізгіштік теориясын жасады. Тоқ күшінің әсерінен ерітінде иондар пайда болады. . Рудольф Клаузиус

электролитической диссоциация теориясы 1883 г. – диссертацияны қорғау «Химическая теория электролитов» Полюсті еріткіштің әсерінен электролиттер ерітіндіде иондарға ыдырайды. Сванте Аррениус Электролититік диссоциация (1859 -1927) Ионы существенно отличаются от атомов. В растворе ионы движутся хаотично. При пропускании через раствор электролита постоянно электрического тока ионы перемещаются направленно катионы к катоду, анионы к аноду.
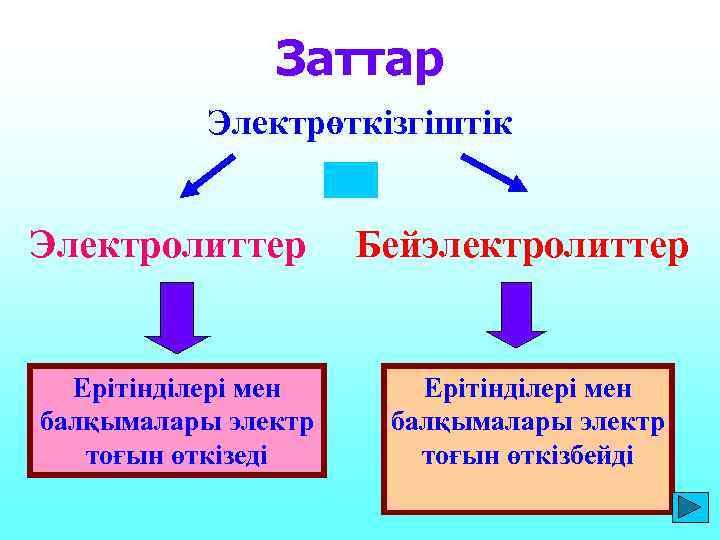
Заттар Электрөткізгіштік Электролиттер Ерітінділері мен балқымалары электр тоғын өткізеді Бейэлектролиттер Ерітінділері мен балқымалары электр тоғын өткізбейді
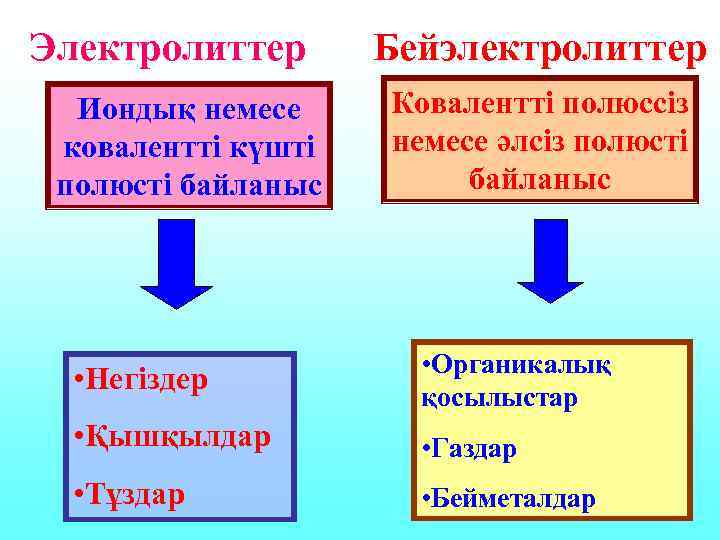
Электролиттер Иондық немесе ковалентті күшті полюсті байланыс Бейэлектролиттер Ковалентті полюссіз немесе әлсіз полюсті байланыс • Негіздер • Органикалық қосылыстар • Қышқылдар • Газдар • Тұздар • Бейметалдар

Электролиттік диссоциация теориясы Электролиттердің еру немесе балқу процессі электр тогын өткізе алатын зарядталған бөлшектер түзе С. А. Аррениус (1859 -1927) жүретін процесс

1. Электролиттік диссоциацияэлектролиттердің суда ерігенде оң және теріс зарядталған иондарға ыдырауы. 2. Электр тоғының әсерінен теріс полюсқа оң зарядталған иондар жылжиды(катиондар), ал оң полюсқа теріс зарядталған иондар жылжиды(аниондар). 3. Диссоциация – қайтымды процесс. Молекулалардың иондарға ыдырау процесімен қатар иондардың молекулалар процесі жүреді. (ассоциация)
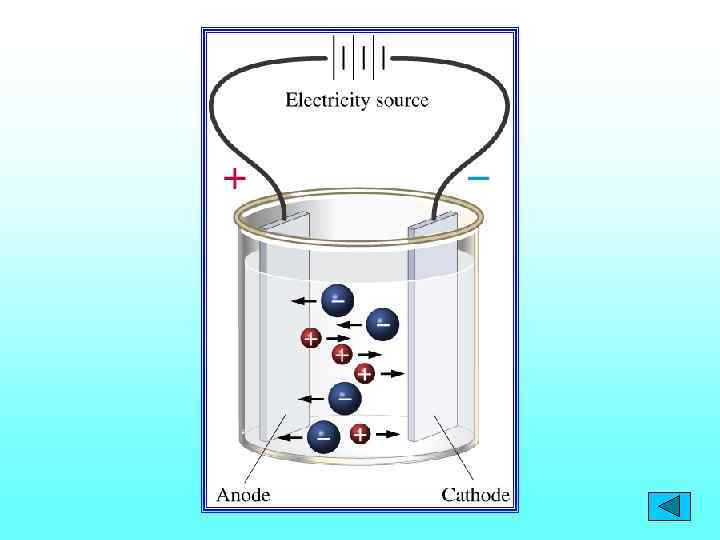
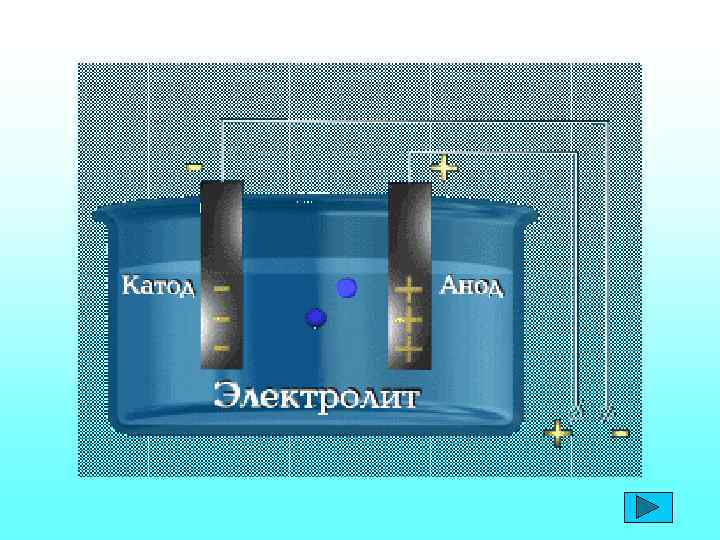


Натрий хлориді кристалдарының құрылысы қант кристалдары құрылысынан мүлде өзгеше • Ас тұзы суда ерігенде заряды бар бөлшектер – иондар түзіліп, электр тоғын тасымалдайды ал, • Қант ерігенде зарядсыз бөлшектер – молекулаларға дейін ғана ыдырайтындықтан, электр тоғын тасымалдай алмайды.
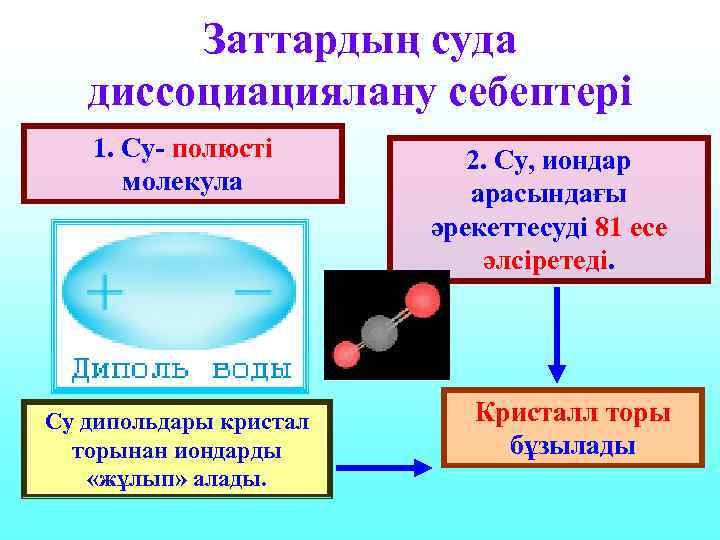
Заттардың суда диссоциациялану себептері 1. Су- полюсті молекула Су дипольдары кристал торынан иондарды «жұлып» алады. 2. Су, иондар арасындағы әрекеттесуді 81 есе әлсіретеді. Кристалл торы бұзылады

Балқымаларда заттардың иондарға ыдырау себептері Қыздырғанда кристал торларының түйіндерінде орналасқан иондар тербелісі күшейеді – кристалл торы бұзылады.
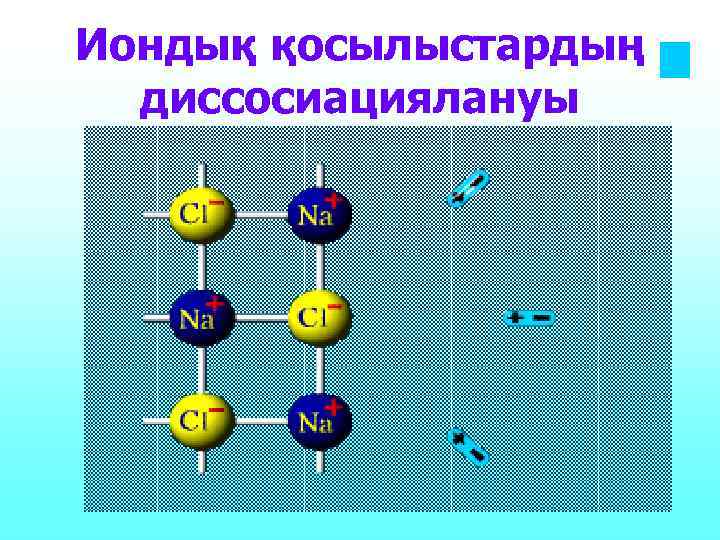
Иондық қосылыстардың диссосиациялануы
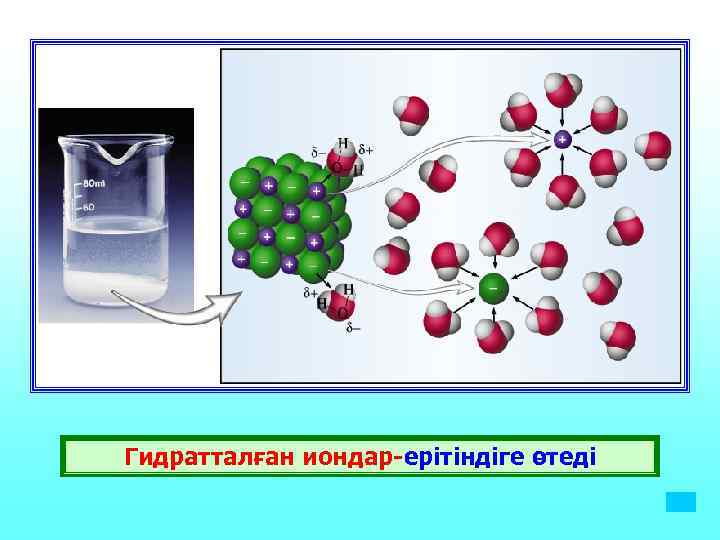
Гидратталған иондар-ерітіндіге өтеді

Гидраттанған иондар • Гидраттану реакциясының мәнін алғаш ашқан орыс ғалымы И. А Каблуков • Гидраттану нәтижесінде кристаллогидраттар түзіледі. • Кристалл торында өз молекулаларымен және иондарымен қоса су молекулалары да болады ондай су кристалдық су деп аталады. Мысалы: Mg. SO 4 *10 H 2 O •

Ковалентті полюсті байланысқан қосылыстардың диссоциациясы

Электролиттік ыдырау нәтижесінде түзілген гидратталған иондардыңдың қысқашадиссоциация теңдеуі.
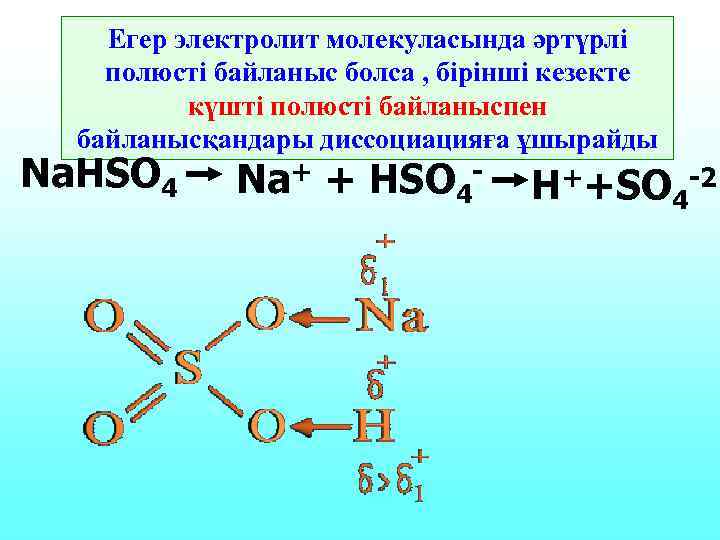
Егер электролит молекуласында әртүрлі полюсті байланыс болса , бірінші кезекте күшті полюсті байланыспен байланысқандары диссоциацияға ұшырайды Na. HSO 4 Na+ + HSO 4 - H++SO 4 -2

Диссоциацияға ұшыраған молекулалар санының жалпы молекулаларға қатынасы Электролиттердің күші
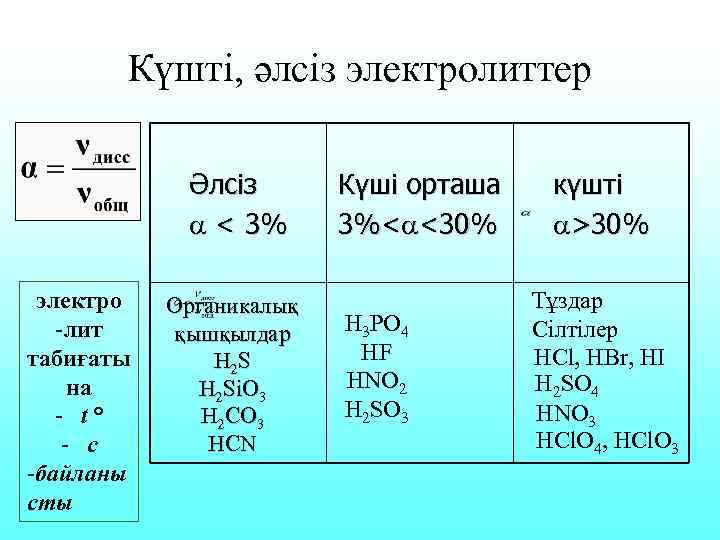
Күшті, әлсіз электролиттер Әлсіз < 3% электро -лит табиғаты на - t° - с -байланы сты Органикалық қышқылдар Н 2 S H 2 Si. O 3 H 2 CO 3 HCN Күші орташа 3%< <30% H 3 PO 4 HF HNO 2 H 2 SO 3 күшті >30% Тұздар Сілтілер HCl, HBr, HI H 2 SO 4 HNO 3 HCl. O 4, HCl. O 3
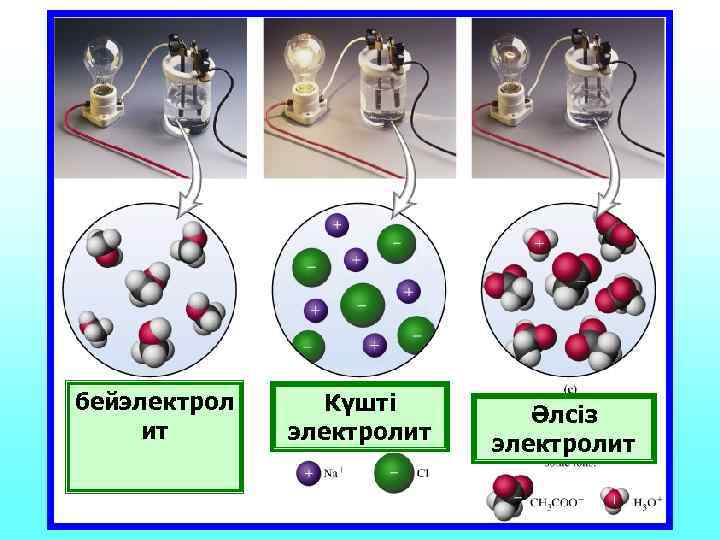
бейэлектрол ит Күшті электролит Әлсіз электролит

Электролиттік диссоциация теориясы 1883 г. – «Электролиттердің химиялық теориясы» диссертациясын қорғау Электролиттік диссоциация ерітіндідегі электролиттер полярлы еріткіштердің әсерінен иондарға ыдырауы. Сванте Аррениус (1859 -1927) Иондар атомдардан ерекшеленеді. Ерітіндіде иондар ретсіз қозғалады. Тұрақты электр тогы әсерінен электролит ерітіндісіндегі иондар бағытталып қозғалады: Катиондар катодка, аниондар анодқа тартылады.

Күшті электролиттер Суда еритін орта тұздар Сілтілік және сілтілік жер металдарының гидроксидтері LIOH- Cs. OH Ca(OH)2 - --Ba(OH)2 Минералды қышқылдар H 2 SO 4 , HNO 3 , HCIO 4 HBr. O 3 , HJO 3 , HCI , HBr , HJ

Күші орташа электролиттер H 3 PO 4 HPO 3 , HCIO 2, H 4 P 2 O 7 , H 2 SO 3 , HF , Fe(OH)2

Әлсіз электролиттер Органикалық қышқылдар HCOOH CH 3 COOH, C 2 H 5 COOH, Минералды қышқылдар HNO 2, HCIO, , H 2 Si. O 3, H 2 CO 3 H 3 BO 3, H 3 PO 3, H 2 S Белсенділігі аз металдардың гидроксидтері Cu(OH)2, Fe(OH)3, Ae(OH)3, Cr(OH)3, NH 4 OH
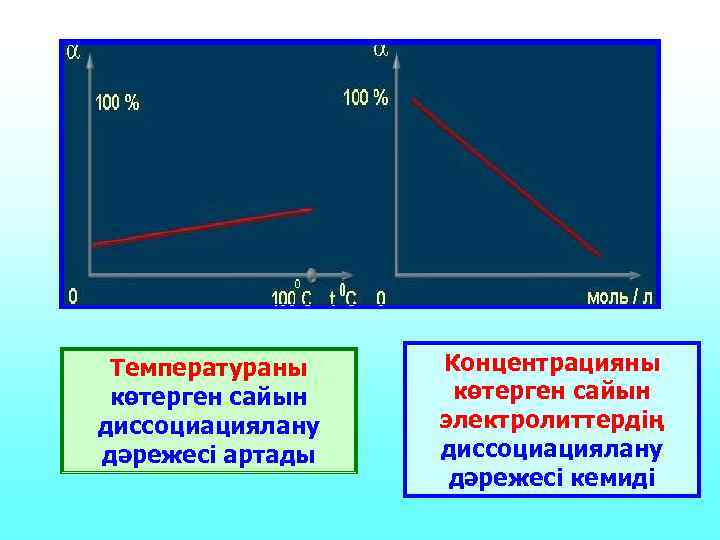
Температураны көтерген сайын диссоциациялану дәрежесі артады Концентрацияны көтерген сайын электролиттердің диссоциациялану дәрежесі кемиді

Диссоциациялану Константасы Әлсіз электролиттің иондарға ыдырау қабілеттілігін көрсетеді
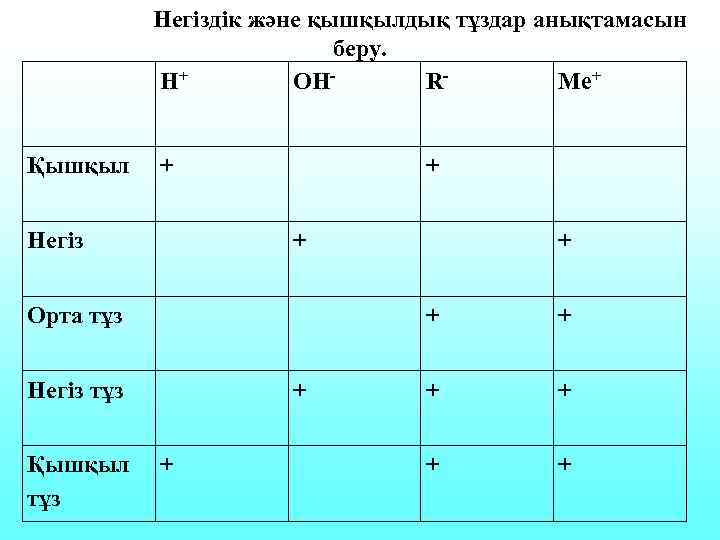
Негіздік және қышқылдық тұздар анықтамасын беру. Н+ ОНRMe+ Қышқыл + Негіз + + Орта тұз + Негіз тұз Қышқыл тұз + + + +
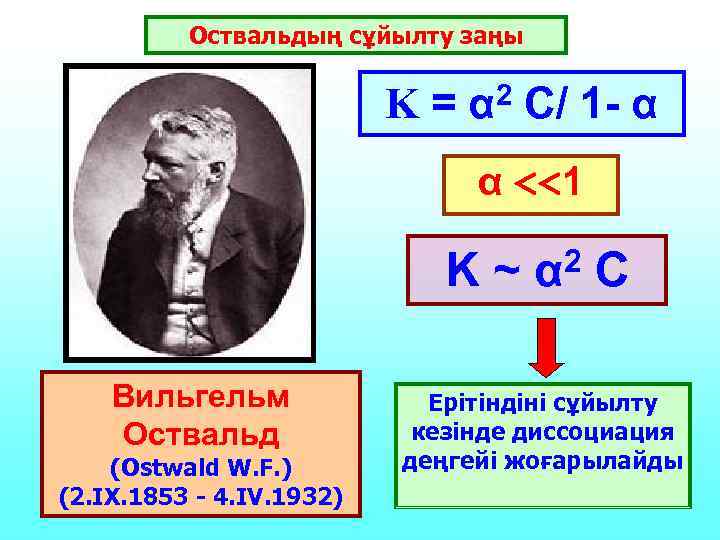
Оствальдың сұйылту заңы K = α 2 C/ 1 - α α <<1 K~ Вильгельм Оствальд (Ostwald W. F. ) (2. IX. 1853 - 4. IV. 1932) 2 α C Ерітіндіні сұйылту кезінде диссоциация деңгейі жоғарылайды

Назарларыңызға рахмет!
Шаматова Г_Ж_ ЭДТ.ppt