
«Қорғасын»

Қорғасын ҚОРҒАСЫН, Pb (plumbum), IV А тобының химиялық элементі, периодтық жүйедегі C, Si, Ge, Sn, Pb химиялық элементтер қатарынан. Атомдық нөмірі 82 Атомдық массасы 207, 2 Қорғасынның изотопы Тұрақтысы 204, 206 208 Тұрақсызы 194 203, 205, 209 214 Балқу температурасы С 327, 500 Қайнау температурасы С 17500 Тығыздығы г/см 3 11, 34 Қаттылығы(масса б/ша) 1, 5 Жер қыртысында таралуы % (масс. ) 0, 0016 Тотығуы +2, +4

Қорғасынның изотопы Қорғасынның 20 -дан астам радиоактивті изотопы белгілі: 206 Pb(24, 1%); 207 Pb(22, 1%); 208 Pb(52, 4%) – Уран, актиния, тория элементтерінің радиоактивті ыдырауының соңғы өнімі болып табылады. *Ұзақ ыдырайтындар: 202 Pb; 205 Pb (ыдырау уақыты: 300 мың және 15 млн. жыл) *Тез ыдыраушы изотоптар: 209 Pb; 210 Pb; 212 Pb; 214 Pb ( ыдырау уақыты: 3, 25 пен 27, 1 жыл және 26, 8 мин. )

Табиғатта таралуы . Жер қыртысындаы – 0, 0016% масса б/ша; . Құрғақ гранитті қабатта – 108864*106 тонна; . Тірі ағзада– 1*10 -4% (В. В. Добровольский 1983 ж. ); . Теңіз суларында – 3*10 -9%

Барлығы 100 ден астам қорғасын минералдары бар екені белгілі. Негізгісі: n Галенит Pb. S; n Англезит Pb. SO 4; n Церрусит Pb. CO 3; Табиғатта сирек кездесетіндері: n Пироморфит ( «жасыл қорғасын рудасы» ) Pb. Cl 2*3 Pb 3(PO 4)3 n Миметит Pb. Cl 2*3 Pb 3(As. O 4)2 ; n Крокоит ( «қызыл қорғасын рудасы» ) Pb. Cr. O 4; n Вульфенит ( «сары қорғасын рудасы» ) Pb. Mo. O 4; n Штольцит Pb. WO 4.
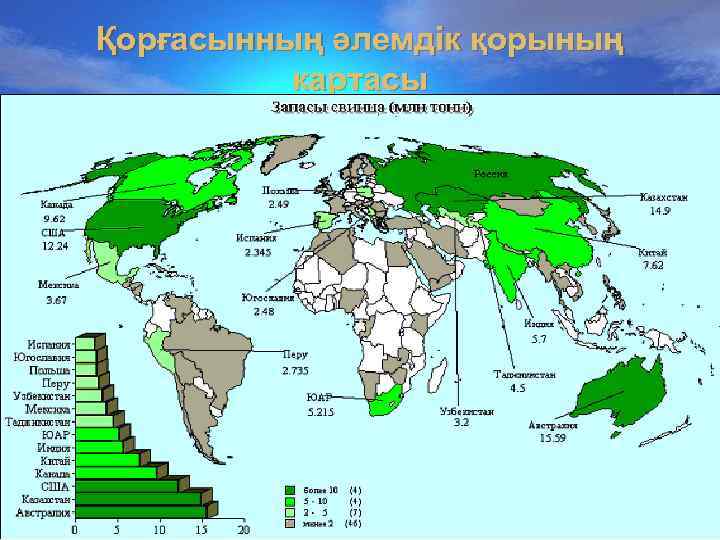
Қорғасынның әлемдік қорының картасы
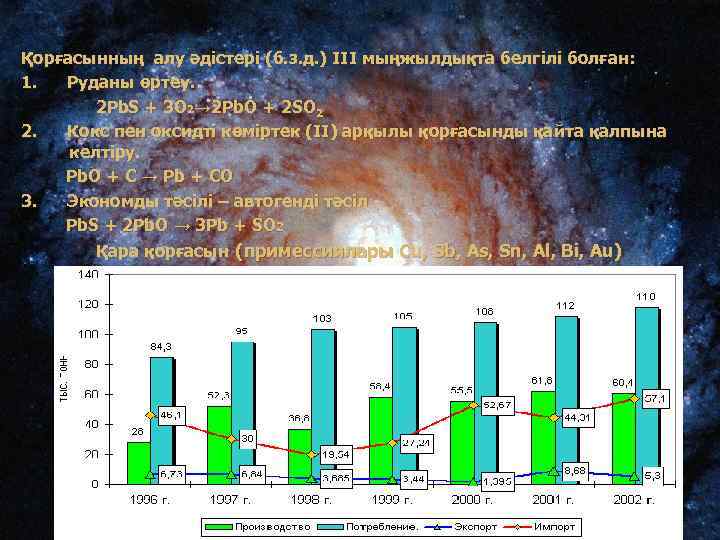
Қорғасынның алу әдістері (б. з. д. ) III мыңжылдықта белгілі болған: 1. Руданы өртеу. 2 Pb. S + 3 O 2→ 2 Pb. O + 2 SO 2 2. Кокс пен оксидті көміртек (II) арқылы қорғасынды қайта қалпына келтіру. Pb. O + C → Pb + CО 3. Экономды тәсілі – автогенді тәсіл Pb. S + 2 Pb. O → 3 Pb + SO 2 Қара қорғасын (примессиялары Cu, Sb, As, Sn, Al, Bi, Au)

Құрамы→ құрылымы→ қасиеті→ қолданылуы Қорғасын көкшіл ақ түсті, ауыр металл. Ол өте жұмсақ болғандықтан пышақпен кесуге болады. . Егер жаңадан кесілген қиындысына қарасақ ақ сұр екенін байқаймыз. Бірақ ол көп кешікпей тотықтанып өте жұқа қабыршақпен қапталып, қалыпты түске енеді. Германий мен қалайыға қарағанда қорғасынның 2+ болатын қосылыстары тұрақты болады. Қорғасынды қыздырғанда галогендермен, оттегімен, күкіртпен әрекеттеседі.

Қорғасынның химиялық қасиеті Қорғасын – аса белсенді емес металл. Pb + H 2 O≠ 2 Pb + O 2 + 2 H 2 O=2 Pb(OH)2 (ауаның қатысуымен) Pb + 4 KOH + 2 H 2 O=K 4[Pb(OH)6] + H 2 калий гидроксоплюмбиті Металдардың электрохимиялық кернеу қатары (қайта қалпына келтіру белсенділігініңтөмендеуі )
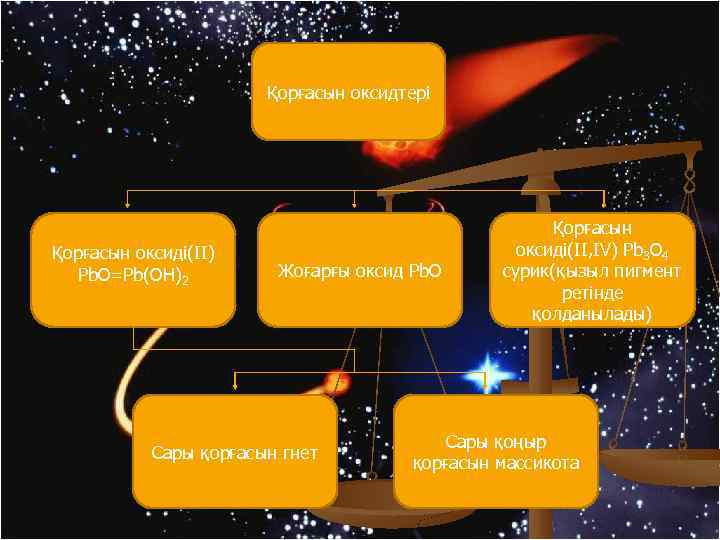
Қорғасын оксидтері Қорғасын оксиді(ІІ) Pb. O=Pb(OH)2 Жоғарғы оксид Pb. O Сары қорғасын гнет Қорғасын оксиді(ІІ, IV) Pb 3 O 4 сурик(қызыл пигмент ретінде қолданылады) Сары қоңыр қорғасын массикота

Қорғасын қосылыстары n n Pb(NO 3)2 – Ca 2 Pb. O 4 - коррозияны болдырмайтын бояулар Кальций ортоплюмбаты n n n n Ba. Pb. O 3 барий метаплюмбаты Pb(CH 3 COO)2 – 2% су ерітіндісі дененің сырқатын жазады. Pb. SO 4 –аналитикалық химияда қорғасынның мөлшерін анықтайды. Pb. Cr. O 4 –сары минералды бояу және майлы бояуға арналған пигмент Pb. S – бұйымдарды қаптауға арналған қорғасын жылтыры, жартылайөткізгіштік қасиетке ие. Pb. O + HCl ≠ Pb + H 2 SO 4 ≠ ерімейтін тұздардан пленка қалыптасады. 2 Pb + 4 CH 3 COOH + O 2 → 2 Pb(CH 3 COO)2 +2 H 2 O «қорғасын қанты» Қорғасын иондарының сапалы реакциясы: Pb(NO 3)2 + 2 KJ = Pb. J 2 + 2 KNO 3 Pb 2+ + 2 J - = PBJ 2 Қорғасынның барлық қосылыстары улы!

Қорытынды Қорғасын – бұл өте ауыр металдардың бірі, және Au, Hg, Bi-ке қарағанда ең көп тараған. Қорғасын өте ерте заманнан белгілі, одан жасалған тиын ақша, медальондар ертедегі Египет қазбаларынан көп табылған. Жер қыртысындағы мөлшері 1. 6 07 %, ол жеке күйінде кездеседі. Ең маңызды кені- галенит- қорғасын жылтыры Pb. S; Қазақстандағы кендері Оңтүстік және Шығыс Қазақстанда және Қарағанды облысында. Қорғасын бос күйінде көкшіл-сұр түсті жұмсақ және ауыр металл, оңай балқиды. Қорғасынды өндіру үшін, оның рудасын алдымен байытады, одан шыққан концентратта 4078% қорғасын болады. Концентраттағы қорғасын көбіне полиметаллургия әдісімен алынады. Қорғасын-өнеркәсіп пен техникада кең пайдаланылатын түсті металл. Ол атмосферада коррозия және қышқылдар әсеріне төзімді болғандықтан, химиялык аппапатуралар (әсіресе, күкірт қышқылы өндірісінде) және кабель, оқ, бытыра дайындауда, радиоактив сәулелерінен қорғануда, медицинада кең қолданады.

Уранның ыдырауы 238 - 235 -

Торияның ыдырауы

Галенит

Сіздермен бірге болған Жарасов Эльдар, 106 топ студенті. Көңіл бөлгендеріңізге РАХМЕТ!