3. Закон Аррениуса.ppt
- Количество слайдов: 10

Зависимость скорости реакции от температуры Закон Максвелла-Больцмана Закон Аррениуса

Закон Максвелла-Больцмана l Скорость химической реакции в значительной степени зависит от температуры. Чаще всего для начала активной реакции систему реагирующих веществ необходимо подогреть. При этом увеличивается число так называемых “активных молекул”, имеющих энергию выше энергии активации. l Число молекул, обладающих тем или иным уровнем энергии Е, определяется статистическим законом Максвелла – Больцмана NE = No exp(–E/RT) No – полное число молекул в единице объёма, R = 8, 314 к. Дж/(кмоль∙К)
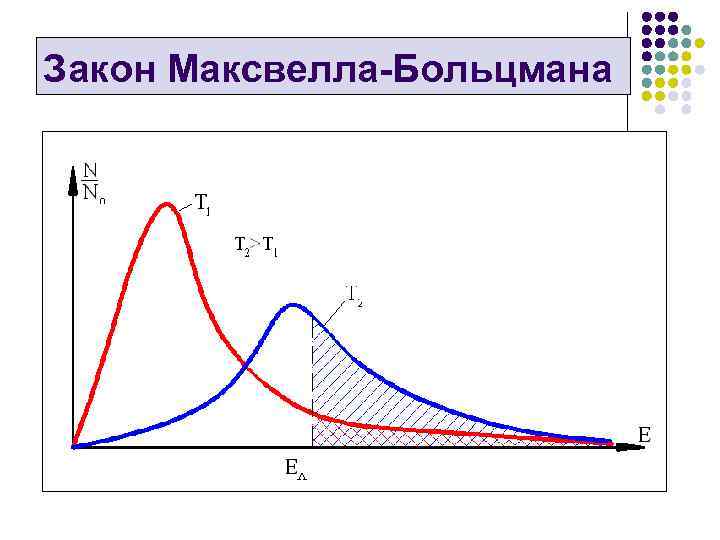
Закон Максвелла-Больцмана

Закон Максвелла-Больцмана l l При низкой температуре Т 1 лишь малая доля молекул (заштрихованная площадь под кривой Т 1) имеет энергию выше энергии активации ЕА. Их так мало, что тепла, выделяющегося в результате отдельных актов реакции, недостаточно, чтобы заметно повысить температуру смеси. C повышением температуры до Т 2 происходит перераспределение энергий молекул (заштрихованная площадь под кривой Т 2), в результате чего становится возможной активная реакция, сопровождающаяся ростом температуры. Естественно, что при более низком уровне энергии активации ЕА химическая реакция может протекать при более низкой температуре. Одновременно c увеличением числа “активных молекул” растёт и скорость химической реакции.

Закон Аррениуса l Закон Аррениуса устанавливает зависимость константы скорости химической реакции от температуры и представляет собой частный случай закона Максвелла - Больцмана применительно к химическим реакциям k 0 – коэффициент пропорциональности, характеризующий частоту столкновений всех реагирующих молекул (активных и неактивных) в единице объёма реагирующей смеси.
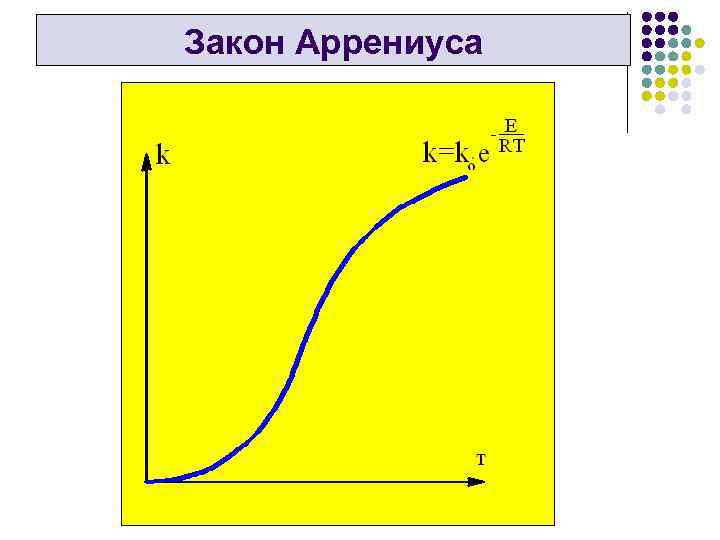
Закон Аррениуса

Закон Аррениуса l l l Частота столкновений зависит от скорости свободного пробега молекул, которая в свою очередь согласно кинетической теории пропорциональна корню квадратному из температуры, т. е. k 0=A∙T 0, 5. Оценки этого параметра показывают, что изменение температуры в диапазоне от 200 до 300°C приводит к увеличению частоты столкновений на 10 %. Множитель exp(Е/RT) отражает долю общего числа столкновений, которые возникают между “активными” молекулами и приводят к реакции. Таким образом, с повышением температуры константа скорости реакции увеличивается, что при сохранении концентрации исходных веществ приводит к росту скорости реакции.
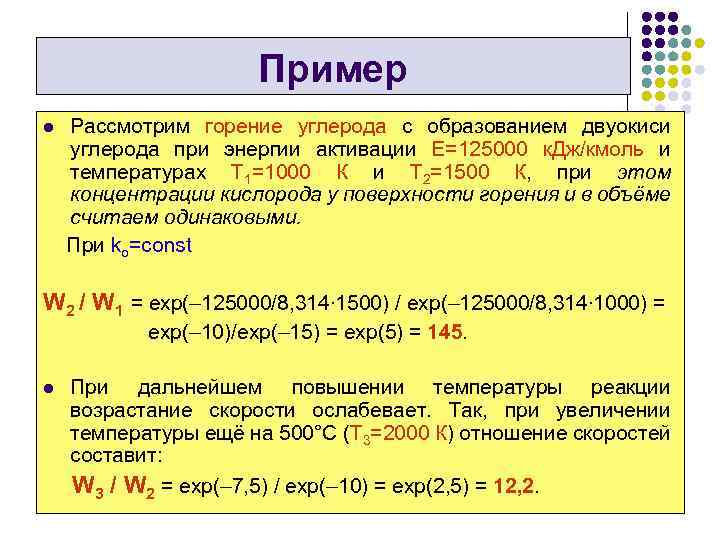
Пример l Рассмотрим горение углерода c образованием двуокиси углерода при энергии активации Е=125000 к. Дж/кмоль и температурах Т 1=1000 К и Т 2=1500 К, при этом концентрации кислорода у поверхности горения и в объёме считаем одинаковыми. При ko=const W 2 / W 1 = exp(– 125000/8, 314∙ 1500) / exp(– 125000/8, 314∙ 1000) = еxp(– 10)/еxp(– 15) = еxp(5) = 145. l При дальнейшем повышении температуры реакции возрастание скорости ослабевает. Так, при увеличении температуры ещё на 500°C (Т 3=2000 К) отношение скоростей составит: W 3 / W 2 = exp(– 7, 5) / exp(– 10) = exp(2, 5) = 12, 2.

Пример l l В то же время за счёт роста температуры увеличиваются и скорости движения молекул, а, следовательно, и значение множителя k 0: ko 2 / ko 1 = (1500 / 1000)0, 5 = 1, 22. Очевидно, что изменение k 0 несоизмеримо c влиянием температуры на рост числа реакционно-способных молекул и их соударений. C учётом изменения k 0 суммарное увеличение скорости реакции cоcтавит: n = W 2 / W 1 = 145∙ 1, 22 = 177. Как видно из примеров, воздействие роста температуры на скорость химической реакции постепенно ослабевает, а скорость реакции стремится к какому-то ограниченному максимуму.

Тяжело в учении …
3. Закон Аррениуса.ppt