болезни легких 2.ppt
- Количество слайдов: 78


Хронические диффузные заболевания легких являются наиболее распространенными среди хронической патологии бронхолегочной системы. В странах бывшего СССР рост заболеваемости хроническими воспалительными заболеваниями легких составлял в среднем 6 7% в год для городского и 2 3% для сельского населения. Наибольший удельный вес в структуре хронических диффуз ных заболеваний легких приходится на хронический бронхит 65 90% больных. Особую тревогу вызывает рост заболеваемости бронхиальной астмой, эпидемические вспышки которой были описаны в городах России (Кириши, Ангарск).

Хронические диффузные заболевания легких в соответствии с функциональными и морфологическими особенностями поражения воздухо проводяших или респираторных отделов легких разделены на три группы: v обструктивные, v рестриктивные, v смешанные обструктивные с рестриктивными нарушениями или рестриктивные с обструктивны ми нарушениями. Сочетание рестрикции с обструкцией наблюдается на поздних стадиях практически всех хронических диффузных заболеваний легких.

-это болезни воздухопроводящих путей, характеризующиеся увеличением сопротивления прохождению воздуха за счет частичной или полной обструкции их на любом уровне (от трахеи до респираторных бронхиол). К обструктивным относят следующие заболевания: v хроническую обструктивную эмфизему легких, v хронический обструктивный бронхит, v бронхоэктатическую болезнь, v хронические бронхиолиты. В основе обструктивных болезней легких лежит нарушение дренажной функции бронхов, что является главной причиной их обструкции. В последние годы широко используют групповое понятие "обструктивная болезнь легких" применительно к группе хронических обструктивных болезней.

Рестриктивные болезни легких характеризуются уменьшением объема легочной паренхимы с понижением жизненной емкости легких. В эту группу входят интерстициальные болезни легких. В основе рестриктивных заболеваний лежит развитие воспаления и фиброза в интерстиции респираторных отделов легких (нередко на иммунной основе), ведущее к интерстициальному фиброзу и блоку аэрогематического барьера, что сопровождается клиническими симптомами прогрессирующей дыхательной недостаточности. Большинство легочных заболеваний на поздних стадиях развития имеет, как правило, одновременно обструктивный и рестриктивный компоненты.

По отношению к хроническим диффузным заболеваниям легких до сих пор используют термин "хронические неспецифические заболевания легких"(ХНЗЛ), предложенный на симпозиуме, организованном фармацевтической фирмой «Ciba» в 1962 г. Тогда было окончательно сформировано понятие ХНЗЛ как группы болезней легких различных этиологии, патогенеза и морфологии, при которых характерно развитие хронического кашля с выделением мокроты и пароксизмальным или постоянным затруднением дыхания, что не связано со специфическими инфекционными заболеваниями, прежде всего туберкулезом легких. До 80 х годов XX в. выделяли такую нозологическую единицу, как хроническая пневмония, подчеркивая, что данный вид хронического заболевания легких характеризуется сочетанием многих патологических процессов в легких карнификации, хронических абсцессов, бронхоэктазов, хронического бронхита, пневмофиброза с явным преобладаем поражений респираторных отделов легких. В настоящее время в подобных случаях вопрос решается путем выяснения преобладающей патологии, истории заболевания с тем, чтобы установить первопричину патологического процесса в легких хронический абсцесс, бронхоэктатическая болезнь или хронический бронхит. Сейчас хроническая пневмония как нозологическая форма признается не всеми.

неблагоприятных факторов внешней среды (выбросов в атмосферу поллютантов), курения, профессиональных факторов (контакта с органическими и минеральными пылями, токсическими газами, изоцианатами и др. ), острых инфекций дыхательных путей (прежде всего вирусных), состоя ния иммунной системы, наличия генетической предрасположенности (фенотипы Pi. ZZ, Pi. SS). Взаимосвязь между хроническими диффузными заболеваниями легких и неблагоприятными экологическими факторами может быть объяснена морфофункциональными особенностями легких.

Хронические диффузные заболевания легких развиваются по одному из трех морфогенетических путей: q бронхитогенному, q пневмонитогенному. Развитие по бронхитогенному механизму обусловлено нарушением дренажной функции легких и бронхиальной проходимости и приводит к таким обструктив ным заболеваниям легких, как хронический бронхит, бронхоэктатическая бо лезнь, хроническая обструктивная эмфизема легких. Пневмониогенный механизм связан с бронхопневмониями, крупозной пневмо нией и их осложнениями острым абсцессом и карнификацией. Развивающиеся в исходе данных осложнений хронические абсцесс и пневмония имеют выра женный рестриктивный компонент. Пневмонитогенный механизм определяет хроническое воспаление и фиброз на территории интерстиция респираторных отделов легких и встречается при ин терстициальных заболеваниях легких. В финале все три механизма хронических диффузных заболеваний легких ведут к развитию пневмосклероза (пневмоцирроза), вторичной легочной гипертензии, гипертрофии правого желудочка сердца и легочно-сердечной недостаточности. Хронические диффузные заболевания легких являются фоновыми заболеваниями для возникновения рака легкого.
Хронический обструктивный бронхит Хроническую обструктивную эмфизему легких Бронхоэктатическую болезнь

Это заболевание, характеризующееся гиперплазией и избыточной продукцией слизи бронхиальными железами, что приводит к появлению продуктивного кашля по меньшей мере в течение 3 месяцев ежегодно на протяжении 2 лет. Хронический бронхит может быть простым и обструктивным. Обструктивный хронический бронхит отличается от простого обструкцией периферических отделов бронхиального дерева в результате воспаления бронхиол (бронхиолита). Морфологический субстрат хронического бронхита – хроническое воспаление бронхиальной стенки с гиперплазией продуцирующих слизь бокаловидных клеток и слизистых желез, что в клинике выражается симптомом выделения мокроты.

Курение наиболее важный этиологический фактор хронического брон хита. В эксперименте установлено влияние табачного дыма на актив ность движения ресничек бронхиального эпителия, что приводит к нару шению мукоцилпарного клиренса, повреждению бронхиального покров ного эпителия с его плоскоклеточной метаплазией, а затем дисплазией и развитием рака. Кроме того, табакокурение снижает активность аль веолярных макрофагов, повреждая тем самым механизмы местной легочной защиты. Вторично гиперплазируются клетки, продуцирующие слизь. Атмосферные поллютанты имеют наибольшее значение в развитии хронического бронхита в индустриально развитых урбанизированных регионах. Обострения хронического бронхита отчетливо связаны с выбросами в атмосферу SO 2 и NО 2. Высокая частота хронического бронхита у рабочих, имеющих по роду своей профессиональной дея тельности контакты с органическими, минеральными пылями и токси ческими газами, доказывает этиологическую роль этих факторов. Обсуждается этиологическое значение респираторных вирусных инфекций и генетических факторов. Развитие хронического бронхита при наследственных заболеваниях может быть проиллюстрировано синдромом "неподвижных ресничек" синдромом Картагенера, а также хроническим бронхитом у людей с муковисцидозом.

Они обусловлены нарушением дренажной функции прежде всего мелких бронхов в результате длительного воздействия различных этиологических факторов. При этом в стенке бронхов развиваются хроническое воспаление, патологическая регенерация (метаплазия), адаптивная гиперпродукция слизи продуцирующими слизь бокаловидными клетками и слизистыми железами. В бронхах возникает хроническое катаральное воспаление слизистый или гнойный катар. Описанные изменения могут ассоциироваться с бронхообструктивными изменениями и астматическим компонентом.

наличии бронхиальной обструкции, виде воспаления, распространенности процесса. По распространенности хронический бронхит может быть локальным и диффузным Локальный хронический бронхит чаще возникает в бронхах II, IV, VIII, IX и X сегментов, особенно правого легкого.

Макроскопически стенки бронхов становятся утолщенными, окружа ются прослойками соединительной ткани, иногда отмечается дефор мация бронхов. При длительном течении хронического бронхита могут возникать мешотчатые и цилиндрические бронхоэктазы расширения просветов бронхов. Микроскопические изменения обусловлены развитием в бронхах хронического слизистого или гнойного катарального воспаления с мета плазией покровного эпителия и гиперплазией слизистых желез и бока ловидных клеток. При этом в стенке бронха выражены клеточная вос палительная инфильтрация, разрастание грануляционной ткани, кото рая может приводить к формированию воспалительных полипов сли зистой оболочки бронха, склероз и атрофия мышечного слоя. Гиперплазия слизистых желез является одним из основных морфоло гических признаков хронического бронхита. На уровне мелких бронхов имеет значение оценка гиперплазии бокаловидных клеток бронхи альной выстилки. Следует подчеркнуть, что при хроническом бронхите наи более выраженные изменения наблюдают именно в этих отделах.

бронхопневмония, формирование очагов ателектаза, обструк тивной эмфиземы легких и пневмофиброза.

Это заболевание характеризуется определенным комплексом легочных и внелегочных изменений (хронической легочной недостаточностью с признаками тканевой гипоксии и развитием легочного сердца) при наличии бронхоэктазов в бронхах. Термин "бронхоэктаз" принят для обозначения стойкого патологического расширения одного или нескольких бронхов, содержащих хрящевые пластинки и слизистые железы, с разрушением эластического и мышечного слоев бронхиальной стенки.

Бронхоэктазы могут быть : • врожденными (2 3 % всех диффузных заболеваний легких) • приобретенными. Приобретенные бронхоэктазы развиваются при бронхоэктатической болезни и хроническом бронхите. Различия между этими двумя легочными заболеваниями определяются по характерному для бронхоэктатической болезни внелегочному симпто мокомплексу и степени выраженности расширения бронхов. На основании макроскопических особенностей выделяют: • мешотчатые (кистевидные) (локализуются преимущественно на уровне проксимальных бронхов, включая бронхи 4 го порядка, и имеют форму мешка); • цилиндрические, (находятся на уровне бронхов 6 10 го порядка, имеют вид последовательно соединенных между собой полых бусинок цилин дрической формы, образованных бронхиальной стенкой; • варикозные бронхоэктазы (напоминают варикозно расширенные вены).

При врожденных и приобретенных бронхоэктазах они имеют некоторые особен ности. Врожденные бронхоэктазы формируются у детей с различными пре и постна тальными дефектами развития трахеобронхиального дерева, что приводит к застою и инфицированию бронхиального секрета. Нарушения качества секрета при муковисцидозе и синдроме Картагенера являются благоприятным фоном для повторных эпизодов бронхолегочного воспаления. Присоединение бактери альной инфекции приводит к деструкции эластического каркаса и мышечной оболочки стенки бронхов, последующему склерозу и дилатации их просвета. В развитии приобретенных бронхоэктазов большое значение имеет механизм обструкции бронхов в сочетании с вторичной бактериальной инфекцией. Поскольку бронхиальная обструкция обычно ограничена одним или несколь кими бронхами, то приобретенные бронхоэктазы, как правило имеют локальный характер в отличие от врожденных бронхоэктазов диффузного характера. Исключение составляют больные с диффузной бронхиальной обструкцией и распространенными приобретенными бронхоэктазами. Особое место занимают бронхоэктазы, патогенез которых связан с предшест вующими им бронхопневмониями с выраженной деструкцией легочной ткани, что наблюдается при осложненной кори, дифтерии, аденовирусной инфекции, гриппе. Иногда бронхоэктазы могут развиваться вследствие попадания в бронхи инородного тела, казеозных масс при туберкулезе, сдавления бронхов опухолью.

Патологическая анатомия определяется сочетанием выраженных бронхоэктазов и внелегочного симптомокомплекса. Бронхоэктазы имеют, как правило, приобретенный характер, связаны с бронхообс труктивным синдромом, предшествующей бронхопневмонией, попаданием инородного тела и поэтому носят локальный характер. Наиболее часто поража ются бронхи нижней доли правого легкого. Микроскопически в полости бронхоэктаза обнаруживается гнойный экссудат, содержащий микробные тела и слущенный эпителий. Покровный эпителий представлен оголенными базальными клетками, очагами полипоза и плоско клеточной метаплазии. Базальная мембрана гиалинизирована, имеет гофриро ванный вид. Обнаруживаются дистрофия и разрушение хряшевой пластинки бронха, атрофия и разрушение мышечного и эластического слоев, склероз и диффузная гистиолимфоцитарная инфильтрация всех слоев стенки бронхоэк таза с примесью полиморфно ядерных лейкоцитов. В прилежащей легочной паренхиме видны поля фиброза, очаги обструктивной эмфиземы легких. Внелегочный симптомокомплекс при бронхоэктатической болезни обусловлен выраженной дыхательной гипоксией и развитием гипертензии в малом круге кровообращения. У больных обнаруживают следующие симптомы: деформацию дистальных ногтевых фаланг в виде "барабанных палочек", изменения ногтевых пластинок по типу "часовых стекол", "теплый" цианоз. Гипертензия в малом круге кровообращения ведет к гипертрофии правого желудочка и развитию легочного сердца.
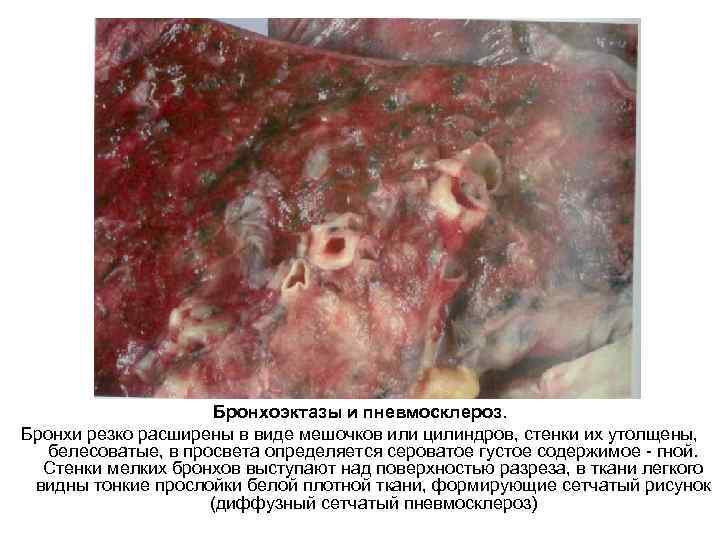
Бронхоэктазы и пневмосклероз. Бронхи резко расширены в виде мешочков или цилиндров, стенки их утолщены, белесоватые, в просвета определяется сероватое густое содержимое гной. Стенки мелких бронхов выступают над поверхностью разреза, в ткани легкого видны тонкие прослойки белой плотной ткани, формирующие сетчатый рисунок (диффузный сетчатый пневмосклероз)
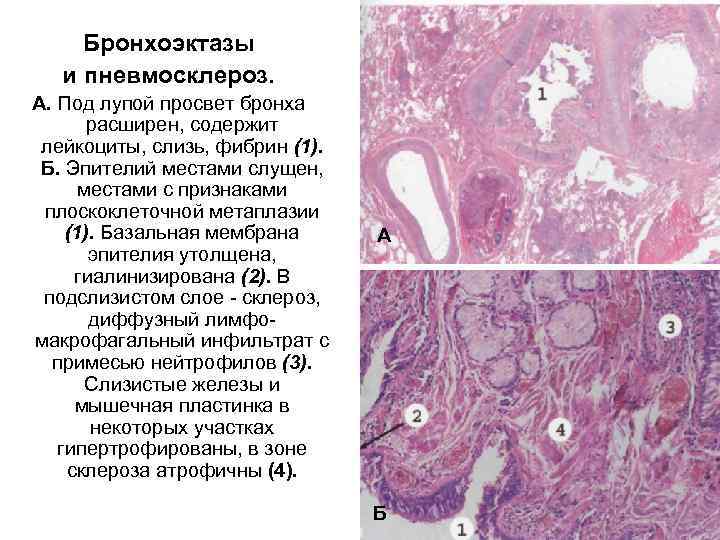
Бронхоэктазы и пневмосклероз. А. Под лупой просвет бронха расширен, содержит лейкоциты, слизь, фибрин (1). Б. Эпителий местами слущен, местами с признаками плоскоклеточной метаплазии (1). Базальная мембрана эпителия утолщена, гиалинизирована (2). В подслизистом слое склероз, диффузный лимфо макрофагальный инфильтрат с примесью нейтрофилов (3). Слизистые железы и мышечная пластинка в некоторых участках гипертрофированы, в зоне склероза атрофичны (4). А Б

Связаны с возможностью развития: Ø легочного кровотечения, Ø абсцессов легкого, Ø эмпиемы плевры, Ø хронической легочно-сердечной недостаточности. Ø амилоидоза (вторичный - АА-амилоид), Ø абсцессов головного мозга. Каждое из названных осложнений может стать причиной смерти пациента с бронхоэктатической болезнью.

"Эмфизема легких" это синдромное понятие, связанное со стойким расширением воздухоносных пространств дистальнее терминальных бронхиол (от греч. emphysio - вздуваю) и, как правило, сопровождающееся нарушением целостности межальвеолярных перегородок.

хроническая обструктивная, хроническая очаговая (перифокальная, рубцовая), викарная, старческая, идиопатическая, По данным патологоанатомических межуточная. исследований примерно у 2/3 больных мужчин и 1/4 женщин выявляются различные виды эмфиземы легких.

v Она та же, что и хронического бронхита, который в боль шинстве случаев ей и предшествует. v Имеется определенная генетическая предрасположенность к развитию данной патологии, сцепленная с М-геном. У больных хронической обструктивной эмфиземой легких описаны два патологических фенотипа этого гена Pi. ZZ и Pi. SS, что обусловливает низкий уровень сывороточного α 1 антитрипсина ингибитора протеаз, разрушающих соедини тельнотканный каркас межальвеолярных перегородок. v Основной источник α 1 антитрипсина гепатоциты и брон хиолярные экзокриноциты терминальных бронхиол.

Связаны с относительной или абсолютной недостаточностью α 1 - антитрипсина. Абсолютная недостаточность α 1 антитрипсина может быть врожденной или приобретенной. При врожденной недостаточности ингибитора протеаз даже незначительная воспалительная инфильтрация легочной ткани гистиоцитами, полиморфно ядерными лейкоцитами, плазмоцитами и другими клетками, выде ляющими эластазу и иные протеазы, локализованными на уровне респиратор ных отделов легкого, заканчивается лизисом эластических волокон межальвео лярной перегородки и развитием эмфиземы. Приобретенная недостаточность ингибитора может быть обусловлена как забо леваниями печени, так и хроническим бронхитом, при котором в результате метаплазии и бокал обидно клеточной трансформации бронхиального эпителия резко снижается количество бронхиолярных экзокриноцитов, синтезирующих α 1 антитрипсин и осуществляющих местную защиту межальвеолярной пере городки от действия протеаз воспалительного инфильтрата. Относительная недостаточность ингибитора протеаз может возникать при чрезмерно высокой несбалансированной активности клеток воспалительного инфильтрата. Вентильный (клапанный) механизм патогенеза имеет место при выраженной бронхиальной обструкции.

Макроскопически легкие увеличены в размерах, прикрывают своими краями переднее средостение, вздутые, бледные, мягкие, не спадаются, режутся с хрустом. Из просвета бронхов выдавливается слизисто гнойный экссудат. Микроскопически характерно сочетание признаков хрони ческого обструктивного бронхита, бронхиолита и эмфиземы легких. Отмечают расширение и уплощение альвеол, ис тончение межальвеолярных перегородок с лизисом и фраг ментацией эластики, гипертрофия и гиперэластоз замыка тельных пластинок, редукция альвеолярно капиллярного кровотока с развитием его блока. Нарушения микроцирку ляции в малом кругу кровообращения являются причиной легочной гипертензии, гипертрофии правого желудочка и развития легочного сердца.
В соответствии с распространенностью изменений в ацинусе выделяют Центроацинарная эмфизема Панацинарная эмфизема Парасептальная эмфизема Иррегулярная эмфизема
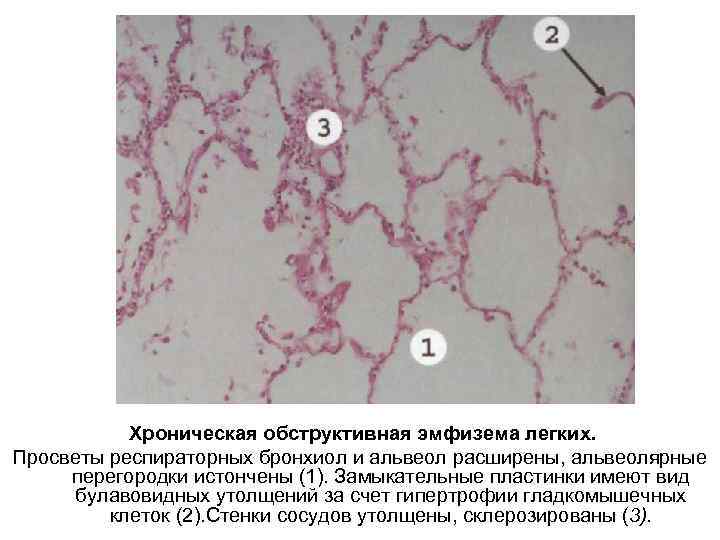
Хроническая обструктивная эмфизема легких. Просветы респираторных бронхиол и альвеол расширены, альвеолярные перегородки истончены (1). Замыкательные пластинки имеют вид булавовидных утолщений за счет гипертрофии гладкомышечных клеток (2). Стенки сосудов утолщены, склерозированы (3).
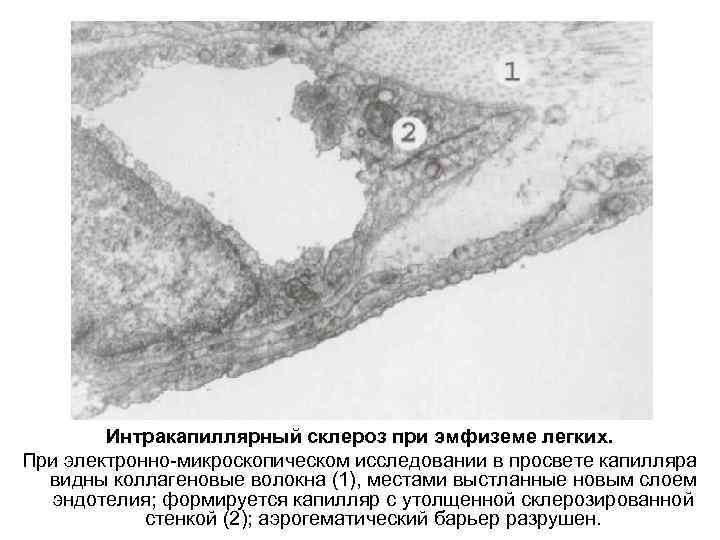
Интракапиллярный склероз при эмфиземе легких. При электронно микроскопическом исследовании в просвете капилляра видны коллагеновые волокна (1), местами выстланные новым слоем эндотелия; формируется капилляр с утолщенной склерозированной стенкой (2); аэрогематический барьер разрушен.
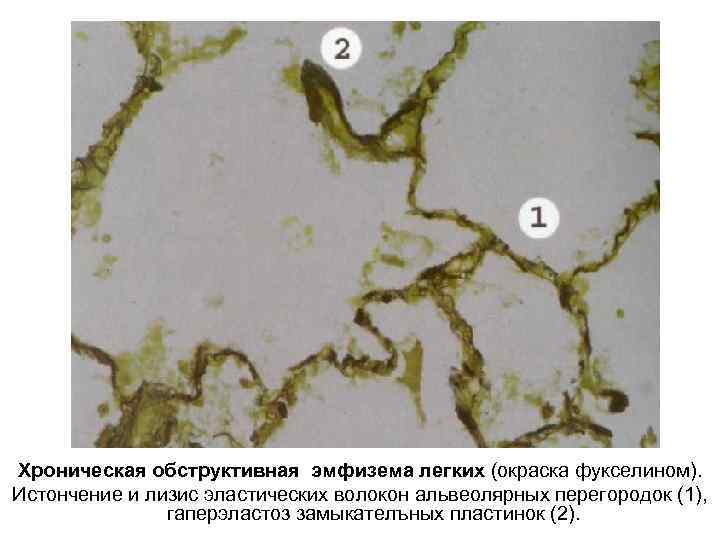
Хроническая обструктивная эмфизема легких (окраска фукселином). Истончение и лизис эластических волокон альвеолярных перегородок (1), гаперэластоз замыкателъных пластинок (2).

Центроацинарная эмфизема легких обусловлена преобладанием расширения респираторных бронхиол и альвеолярных ходов, тогда как периферические отделы долек остаются относительно сохранными. Поскольку легкие обладают большими компенсаторными возможностями, то лишь вовлечение в патологический процесс абсолютного большинства долек легочной паренхимы сопровождается развитием вентиляционной недостаточности. При панацинарной эмфиземе легких в процесс вовлекаются как цент ральные, так и периферические отделы ацинусов. При этом формиру ется блок аэрогематического барьера за счет спадения межальвеоляр ных капилляров и склероза межальвеолярных перегородок с быстрым развитием тяжелой вентиляционной недостаточности. При парасептальной эмфиземе легких изменена вся дистальная часть ацинуса, проксимальная же часть выглядит неизмененной. Наиболее часто она встречается в верхних долях легкого, субплевральных отде лах и вокруг очагов пневмосклероза. Прогрессирование заболевания может приводить к формированию кистозных полостей, заполненных воздухом, до нескольких сантиметров в диаметре буллами, что пос лужило основанием называть данный процесс в легких буллезной эмфиземой. При иррегулярной эмфиземе легких ацинус поражен неравномерно, и клинические проявления эмфиземы, как правило, отсутствуют.

К осложнениям относится прогрессирующая легочно сердечная недостаточность, быстро приводящая к смерти при отсутствии оксигено терапии и других современных методов лечения.
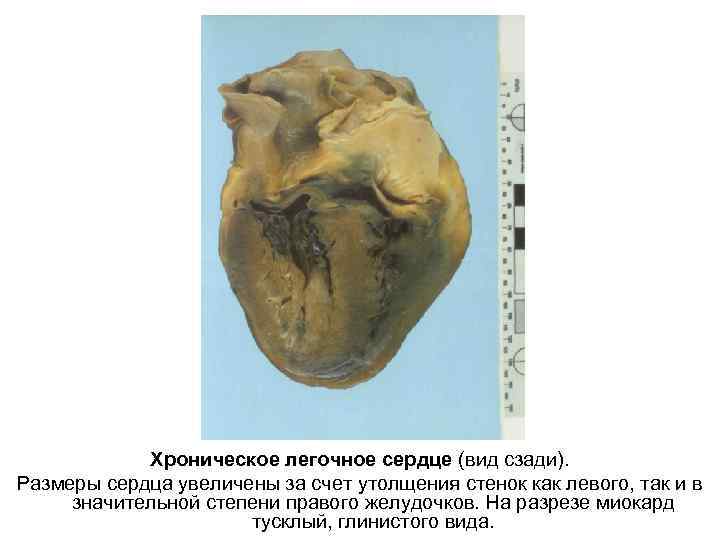
Хроническое легочное сердце (вид сзади). Размеры сердца увеличены за счет утолщения стенок как левого, так и в значительной степени правого желудочков. На разрезе миокард тусклый, глинистого вида.

Интерстициальные болезни легких – гетерогенная группа заболеваний, характеризующихся преобладанием диффузного и обычно хронического поражения легочного интерстиция респираторных отделов легких, прежде всего альвеол и бронхиол. История изучения интерстициальных болезней легких связана с именами американских врачей Хаммена и Рича. В последние годы достигнут определенный успех в изучении интерстици альных болезней легких, однако вопросы этиологии, патогенеза и классификации многих из них остаются дискуссионными.

v При большинстве интерстициальных болезней легких развивается фиброзирующий альвеолит. v Сложность проблемы фиброзирующего альвеолита свя зана с отсутствием четкого определения данного понятия и употреблением множества синонимов для его обозначения: склерозирующий альвеолит, идиопатический фиброзиру ющий альвеолит, диффузный интерстициальный фиброз, интерстициальный пневмонит, болезнь Хаммена Рича (острый и первичный варианты), синдром Скеддинга, болезнь Ослера Шарко, фиброзная дисплазия легких. v Ситуация усугубляется еще и тем, что перечисленными терминами часто одновременно называют патологический процесс, синдром и заболевание.

Термином "фиброзирующий альвеолит" следует обозначать патологический процесс, характеризующийся диффузным или очаговым, острым или хроническим негнойным воспалением с исходом в фиброз, который развивается на территории интерстиция респираторных отделов легких: альвеол, альвеолярных ходов и респираторных бронхиол. Фиброзирующий альвеолит является характерным морфологическим проявлением большинства интерстициальных болезней легких и в первую очередь таких, как идио патический фиброзирующий альвеолит, вторичных фиброзирующих альвеолитов при ревматических заболеваниях, аллергических экзогенных альвеолитов и пневмокониозов. Фиброзирующий альвеолит формируется не только при интерстициальных бо лезнях легких с диффузным поражением интерстиция, но и при гранулематозном воспалении. В последней группе заболеваний фиброзирующий альвеолит обнаруживается на предгра нулематозной стадии (пневмокониозы, саркоидоз), а также в легочной ткани, прилежа щей к гранулеме. Имеются как стереотипные морфологические признаки, повторяющиеся при разных заболеваниях, так и нозологические особенности, отличающие их между собой. Стереотипным для всех антерстициальных болезней легких является развитие в начале заболевания альвеолита и интерстициального фиброза в финале заболевания. Крайним выражением интерстициального фиброза служит формирование сотового легкого, характеризующегося сочетанием интерстициального фиброза и кистозной трансформа ции терминальных и респираторных бронхиол, что сопровождается блоком аэрогемати ческого барьера, развитием вторичной легочной гипертензии, гипертрофии правого желу дочка и легочного сердца. Нозологические же особенности проявляются преимуществен но на ранних стадиях интерстициальных болезней легких.

v вирусы, v бактерии, v грибы, v органические и неорганические пыли, v радионуклиды, v гипероксия в условиях гипербарической оксигенации, v токсические факторы, v лекарственные препараты и др. Однако при большинстве интерстициальных болезней легких их этиология остается невыясненной. v Среди лекарственных препаратов наибольшую опасность представляют цитостатики (блеомицин, бусульфан, кармус тин, циклофосфамид, метотрексат, прокарбозид, митоми цин) и некоторые другие препараты (амидарон, амитрипти лин, нитрофурантоин).

Они различны в зависимости от характера инициального воспаления на территории респираторных отделов легкого. Воспаление может быть иммунным (как это бывает, например, при идиопатическом фиброзирующем альвеолите) или саркоидозе, или неиммунным (при большинстве пневмокониозов). Однако независимо от природы воспалительной реакции и вида этиологического фактора происходит повреждение межальвеолярной перегородки. Морфогенез инициального повреждения может быть связан с попада нием этиологического фактора с воздухом и повреждением альвеоло цитов 1 го порядка, в других случаях с кровью, тогда речь может идти об иммунных комплексах. Возможно также сочетание описанных путей попадания в легкие повреждающего агента.

Существует несколько принципов классификации интерстициальных болезней легких, основными из которых являются: по этиологии интерстициальные болезни легких подразделяются на заболевания с установленной и неустановленной этиологией; по виду продуктивного воспаления в легких: продуктивное интерстициальное или гранулематозное. Среди основных интерстициальных болезней легких с установленной этиологией следует назвать пневмокониозы, вызванные органическими и неорганическими пылями, острые межуточные пневмонии (вирусные, грибковые, пневмоцистная, экзогенный аллергический альвеолит лекарственный и др. ). Подавляющее большинство интерстициальных болезней легких относится к бо лезням с неустановленной этиологией, важнейшими из которых являются: этиологией v идиопатический фиброзирующий альвеолит (болезнь Хаммена Рича), v вторичный фиброзирующий альвеолит при ревматических болезнях, v вторичный фиброзирующий альвеолит при инфекции HBV, легочных васкули тах, саркоидозе, v фиброзирующий альвеолит при синдроме Гудпасчера и других легочно почеч ных синдромах, v идиопатический гемосидероз легких, v эозинофильная пневмония, v гистиоцитоз X, v альвеолярный протеиноз, v десквамативная интерстициальная пневмония и др.

Они обусловлены рестриктивным характером изменений, резким прогрессирующим снижением жизненной емкости легких и диффузионной способности, появлением одышки, тахипноэ, цианоза.

Идиопатический фиброзирующий альвеолит. Это заболевание легких встречается у 15 % пациентов ле гочных стационаров, нередко протекает "под маской" пневмонии и наиболее часто поражает людей в возрасте 30 50 лет. Идиопатический фиброзирующий альвеолит - это группа интерстициальных заболеваний легких с неустановленной этиологией, характеризующаяся развитием фиброзируюшего альвеолита, который сопровождается прогрессирующей легочной недостаточностью. Идиопатический фиброзирующий альвеолит представляет собой группу заболеваний, включающую: классическую интерстициальную пневмонию, "неспецифическую" интерстициальную пневмонию, десквамативную пневмонию, облитерирующий бронхиолит с организующейся пневмонией, гигантоклеточную интерстициальную пневмонию.

Важная роль в морфогенезе альвеолита отводится альвеолярным макро фагам и полиморфно ядерным лейкоцитам, первыми появляющимися в альвеолах и призванными оказывать защитное действие. Однако в активированном состоянии эти клетки генерируют большие количества активных форм кислорода, протеаз, а также цитокинов, вызывающих повреждение и склероз легочной паренхимы. Диагностика идиопатического фиброзирующего альвеолита базируется на комплексе клинико лабораторных данных, включающие результаты исследования лаважной жидкости и открытой биопсии легкого. В лаважной жидкости характерны наличие цитоза, увеличение количества нейтрофилов (нейтрофильный характер лаважа) или лимфоцитов (лимфоцитарный характер лаважа), что бывает при некоторых видах идиопатического фиброзирующего альвеолита, а также на фоне терапии.

Заболевание протекает в несколько стадий. На ранней стадии в лаважной жидкости отмечают выраженный цитоз. Клеточный состав жидкости варьирует в зависимости от типа альвеолита и нозологии: при идиопатическом фиброзирующем альвеолите чаще, чем при других интерсти циальных болезнях легких, встречается нейтрофильный и нейтрофильно лим фоцитарный лаваж. Макроскопические изменения легких в начальной стадии фиброзирующего альве олита описаны на основе данных открытых и торакоскопических биопсий. Легкие могут быть изменены незначительно: неравномерно воздушные, полно кровные, с увеличенной плотностью. Микроскопические проявления начальных изменений при идиопатическом фибро зируюшем альвеолите укладываются в картину экссудативного и экссудативно продуктивного воспаления. В межальвеолярных перегородках обнаруживают явления отека, воспалительную инфильтрацию и начальные проявления склероза. Нарушение проницаемости сосудов приводит к скоплению экссудата в просветах альвеол, протеинозу, десквамации эпителия, выпадению фибрина, вплоть до образования гиалиновых мембран. Нередко обнаруживаются деструктивные, продуктивные и деструктивно продуктивные капилляриты. Склеротические процессы на ранней стадии фиброзируюшего альвеолита сопровождаются усиленной секрецией различных цитокинов прежде всего альвеолярными макрофагами: факторов роста (ТФРβ ФРФβ, фибронектина и др. ), онкопротеинов, стимулирующих пролиферацию фибробластов и склероз. Одновременно усиливается синтез фибробластами коллагенов III, IV и V типов.
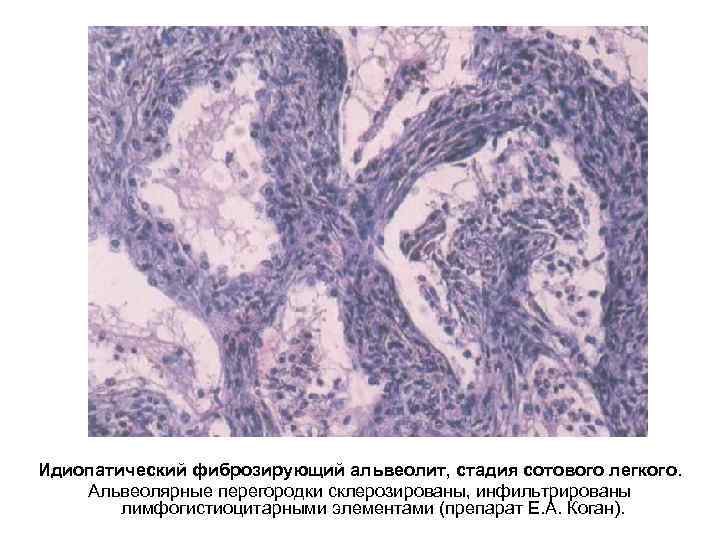
Идиопатический фиброзирующий альвеолит, стадия сотового легкого. Альвеолярные перегородки склерозированы, инфильтрированы лимфогистиоцитарными элементами (препарат Е. А. Коган).

Поздняя стадия фиброзирующего альвеолита характеризуется типичными макроскопическими изменениями в виде уплотнения легочной ткани, которая при этом приобретает резиновую плотность, понижения воздушности и эластичности с формированием ячеистых структур, напоминающих пчелиные соты "сотовое легкое". При микроскопическом исследовании выявляются выраженный склероз интерсти ция респираторных отделов легких и кистозная перестройка легочной ткани с плоско клеточной метаплазией, дисплазией эпителия и формированием в отдельных случаях очагов аденоматоза. Использование иммуногистохимического и электронно-микроскопического методов позволяет обнаружить тяжелую патологию, развивающуюся в области аэрогематического барьера, которая и проявляется в клинике в виде прогресси рующей дыхательной недостаточности. Аэрогематический барьер блокируется и перестает функционировать за счет как выраженного фиброза интерстиция межальвеолярных перегородок, так и дисрегенераторных изменений в эпители альной выстилке. Легочный эпителий на поздних стадиях фиброзирующего альвеолита подвергается перестройке. Альвеолоциты 1 го типа на больших участках замещаются альвеолоцитами 2 го типа с незрелыми осмиофильными мультиламеллярными тельцами, нередко с признаками незрелости и клеточ ного атипизма. Из за нарушенной продукции сурфактанта и облитерации бронхиол развиваются очаги ателектаза легочной ткани.

Связаны с развитием легочного сердца и прогрессированием легочно сердечной недостаточности. Атипическая аденоматозная гиперплазия, обнаруживаемая в сотовом легком в 12, 5% случаев, заканчивается раком легкого.

Наиболее часто встречающееся среди интерстициальных болезней легких заболевание с неустановленной этиологией. Это системное заболевание характеризуется развитием неказеозных гранулем (макрофагальных, эпителиоидноклеточных и гигантоклеточных) в легких, лимфатических узлах и других органах (кожа, печень, селезенка, глаза). Заболеваемость саркоидозом у женщин выше, чем у мужчин. Заболевание может протекать бессимптомно и обнаруживаться случайно при рентгенологическом обследовании или уже на аутопсии в виде диссеминированного процесса в легких в сочетании с лимфаденопатией. Клинически может проявляться в виде лихорадки, ночных потов, узловой эритемы, полиартрита. В крови отмечается повышение Ig. G и Са 2+. Окончательный диагноз обычно ставят на основании результатов биопсии. Этиология саркоидоза неизвестна. Высказывают предположение о значении в раз витии саркоидоза L форм туберкулезной микобактерии. В пользу этого свиде тельствует обнаружение у больных саркоидозом ряда изменений, типичных для туберкулеза: положительные данные полимеразно цепной реакции на фрагменты ДНК микобактерии в саркоидных гранулемах и аккумуляция Тγδ клеток (ассоциированы с микобактериальными инфекциями).

Патогенез иммунный с развитием реакции гиперчувс твительности IV типа с участием СD 4+Т лимфоци тов. Об иммунном патогенезе саркоидоза свиде тельствуют следующие факты: Ø лимфоцитарный характер альвеолита с аккумуля цией СD 4+Т лимфоцитов, усиленно продуцирую щих ИЛ 2 и экспрессирующих HLA DR; Ø активация альвеолярных макрофагов, продуци рующих ИЛ 1, активные формы кислорода и ФНОα; Ø кожная анергия при введении туберкулина; Ø снижение циркулирующих Т лимфоцитов при нали чии нормального уровня В лимфоцитов.

v В органах и тканях имеются иммунное воспаление с лимфогистиоцитарной инфильтрацией, васкулиты, саркоидные гранулемы, интерстициальный фиброз. Легкие при саркоидозе поражаются обязательно. Полагают, что для постановки диагноза саркоидоза необходимо доказать поражение легких и лимфаденопатию. В противном случае ставят диагноз саркоидной реакции. v Изменения в легких развиваются в две стадии - лимфоцитарного альвеолита и гранулематозную. Фиброз в исходе заболевания может быть выражен в разной степени. Саркоидоз легких характеризуется минимально выраженным фиброзирующим альвеолитом со слабой лимфогистиоцитарной инфильтра цией и ха рактерными гранулемами, которые иногда могут отсутствовать (догранулематозная стадия заболевания). Альвеолярные макрофаги содержат как первичные, так и вторичные лизосомы, генерируют большие количества активных форм кислорода, но меньше, чем при идиопатическом фиброзирую щем альвеолите, и значительные количества ФНОα. v Саркоидные гранулемы - типичные гранулемы иммунного типа, состоят из кле ток моноцитарного происхождения макрофагов, эпителиоидных и гигантских многоядерных клеток типа Пирогова Лангханса, СО 4+Т лимфоцитов и фибро бластов. Характерной особенностью саркоидных гранулем являются отсутс твие казеозного некроза, "штампованный" вид за счет периферически распо ложенных фибробластов и коллагена и единообразная морфология. v Примерно в 60 % случаев в гигантских многоядерных клетках можно обнаржить характерные цитоплазматические включения- звездчатые или астероидные тельца. Нередко в ткани легкого выявляют кальцифицированные пластинчатые тельца - тельца Шаумана.

У большинства больных саркоидоз имеет хороший прогноз. Излечение может наступать спонтанно. У 65 70 % пациентов имеются минимальные оста точные изменения, связанные с незначительным пневмосклерозом. У 20 % больных саркоидоз протекает как медленно прогрессирующее хроническое заболевание с эпи зодами ремиссий и обострений. И только в 10 % случаев саркоидоз приводит к прог рессирующему фиброзу с развитием легочного сердца и легочно сердечной недостаточности.

представляет собой интерстициальное заболевание легких установленной этиологии с развитием гранулематозного воспаления и относится к группе пнезмокониозов пылевых профессиональных заболеваний легких, индуцированных неорганическими пылями. Является самым распространенным профессиональным заболеванием.

Характеризуется узелковым и диффузным пневмосклерозом. На ранних стадиях можно обнаружить крошечные черно белые узелки, расположенные преимущественно в верхних отделах легкого. При микроскопическом исследовании им соответствуют силикотические гранулемы, состоящие из кониофагов, которые содержат пылевые частицы, легко определяемые в поляризованном свете. На поздних стадиях по мере прогрессирования в узелках накапливается коллаген, узелки гиалинизируются, слива ются в большие конгломераты. В центре таких конгломера тов со временем возникают очаги некроза и даже каверноз ные полости. Выявляются пневмосклероз и признаки вто ричной легочной гипертензии.
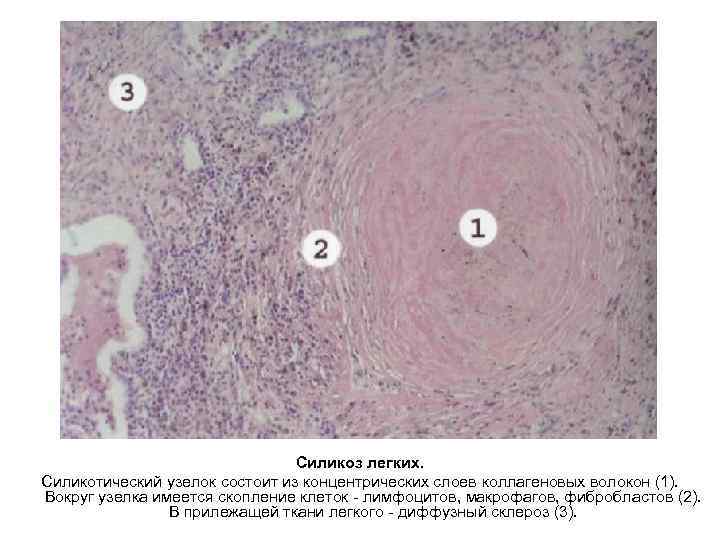
Силикоз легких. Силикотический узелок состоит из концентрических слоев коллагеновых волокон (1). Вокруг узелка имеется скопление клеток лимфоцитов, макрофагов, фибробластов (2). В прилежащей ткани легкого диффузный склероз (3).
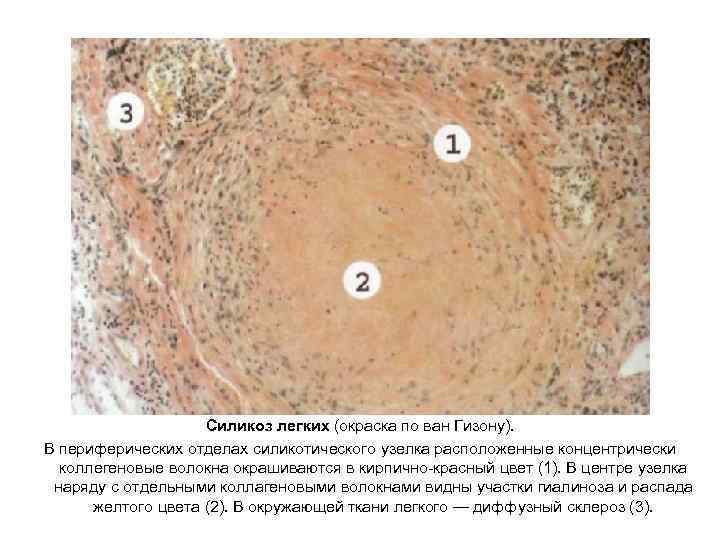
Силикоз легких (окраска по ван Гизону). В периферических отделах силикотического узелка расположенные концентрически коллегеновые волокна окрашиваются в кирпично красный цвет (1). В центре узелка наряду с отдельными коллагеновыми волокнами видны участки гиалиноза и распада желтого цвета (2). В окружающей ткани легкого — диффузный склероз (3).

Обусловлены развитием легочного сердца, прогрессированием легочно сердечной недостаточности. Встречаются случаи присоединения туберку леза (силикотуберкулез) и возникновение рака легкого.

Это хроническое рецидивирующее воспалительное заболевание, характеризующееся повышенной возбудимостью трахеобронхиального дерева в ответ на различные стимулы и приводящее к пароксизмальной констрикции воздухопроводящих путей. Выделяют два основных вида заболевания: экзогенная, атоническая (аллергическая, реагинобусловленная) бронхиальная астма; эндогенная нереагиновая (идиопатическая) или индуцированная различными факторами. Кроме того, встречаются ятрогенная (лекарственная) и профессиональная бронхиальная астма.

Этиология экзогенной, атопической бронхиальной астмы связана с аллергенами окружающей среды, например пылевыми частицами, пыльцой растений, пищевыми факторами и др. Нередко имеется семейная предрасположенность. Нереагиновую бронхиальную астму могут вызывать самые разные факторы и прежде всего инфекционные, химические агенты и лекарства. Семейный анамнез отсутствует в большинстве случаев. Причина гиперреактивности бронхов остается неизвестной.

связан с lg. E обусловленной реакцией гиперчувствительности 1 типа. Ранние изменения в бронхиальном дереве ини циируются связыванием антигена тучными клетками, пок рытыми Ig. E, что приводит к высвобождению из них вначале первичных (лейкотриенов и др. ), а затем и вторичных (ци токинов, нейропептидов и др. ) медиаторов. Данные медиаторы, выбрасываемые в острой фазе, индуци руют бронхоспазм, отек слизистой оболочки, секрецию слизи и инфильтрацию лейкоцитами. Поздние изменения инициируются лейкоцитами инфильтрата (эозинофилами, нейтрофилами, моноцитами). Морфологически при этом наблюдаются бронхоспазм, отек, лейкоцитарная инфильтрация и слущивание бронхиального эпителия.

В легком развиваются разнообразные опухоли. Однако 90 95 % всех опухолей составляет рак легкого, около 5 % - карциноиды и 2 5 % - опухоли мезенхимального происхождения. Рак легкого называют также бронхогенной карциномой, или бронхогенным раком, что подчерки раком вает наиболее распространенное мнение о гис тогенезе данной опухоли из эпителия бронхов и бронхиол.

Ее считают "убийцей № 1" в индустриально развитых странах по двум причинам. Во первых, она является самой распространенной злокачественной опу холью, на ее долю приходится примерно 30% смертей от всех видов злокачественных новообразований среди мужского населения. Хотя среди женщин уровень заболеваемости и смертности от рака легкого значительно ниже, за последние 20 лет отмечается значительный рост этого показателя. Поэтому в настоящее время показатели смертности от рака легкого опережают таковые при раке молочной железы. Во вторых, бронхогенная карцинома относится к наиболее фатальным злокачественным опухолям человека, так как в подавляющем большинстве случаев (75%) диагностируется на поздних стадиях, когда хирургическое лечение уже не проводится. Но даже после полномасш табной комплексной современной терапии показатели выживаемости пациентов с диагнозом бронхогенной карциномы чрезвычайно низкие.

В 98 % случаев этиология связана с воздействием экзогенных канцерогенных агентов (курение, профессиональные вредности, радиация) итолько в единичных случаях с генетическими факторами.

Патогенез и морфогенез подчиняются общим закономернос тям и связаны с нарушением процессов пролиферации, дифференцировки и апоптоза в эпителиальных клетках под действием канцерогенных факторов, с появлением очагов гиперплазии, метаплазии и дисплазии бронхиального, бронхиолярного и альвеолярного эпителия. Ключевым моментом патогенеза рака легкого служит повреж дение генома эпителиальной клетки. При этом регистрируются хромосомные аберрации и мутации генов, большинство из которых не являются строго специфическими и постоянно встречающимися только при раке легкого. Наиболее типична для мелкоклеточного рака легкого делеция в коротком плече хромосомы 3 — Зр14 -23.
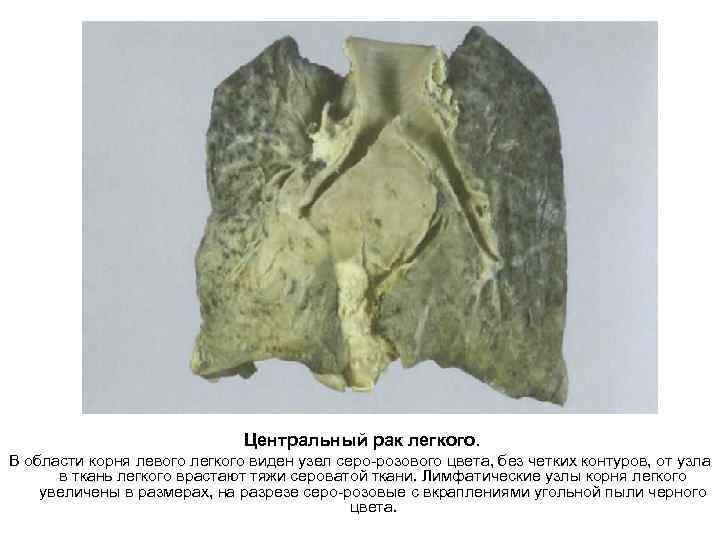
Центральный рак легкого. В области корня левого легкого виден узел серо розового цвета, без четких контуров, от узла в ткань легкого врастают тяжи сероватой ткани. Лимфатические узлы корня легкого увеличены в размерах, на разрезе серо розовые с вкраплениями угольной пыли черного цвета.

В патогенезе рака легкого наибольшее значение имеют клеточные онкогены 4 семейств: туc, ras, bcl и erb-B. Семейство клеточных онкогенов туc, с-тус, Lmyc, N-myc кодирует синтез клеточных регуляторных белков, индуцирующих пролиферацию и подавляющих дифференцировку. • Семейство клеточных онкогенов ras нередко подвергается изменениям при опухолевом росте. Гены кодируют синтез белков р21, обладающих ГТФазной активностью и действующих на передачу ростового сигнала клетке. Описаны мутации, активирующие гены ras. Наиболее часто в раке легкого обнаруживают мутации K-ras, присущие только немелкоклеточному раку легкого в отличие от мелкоклеточного рака легкого. • Семейство bcl состоит из bcl-2, bax, bak и bcl. XL, bcl. XS. Его белковые продукты способны образовывать гомо и гетеродимеры, оказывающие диаметрально противоположное действие на пролиферацию и апоптоз опухолевых клеток. Наиболее изученный из данного семейства ген bcl-2 локализуется на внутреней мембране митохондрий, а также в ядре, стимулирует пролиферацию клеток и ингибирует апоптоз. Протеины, синтез которых кодирует bax, транскрипция и синтез которых регулируются р53, блокируют пролиферацию и стимулируют апоптоз опухолевых клеток. Bcl. XL ингибирует апоптоз и стимулирует пролифе рацию, a bcl. XS, напротив, индуцирует апоптоз. Таким образом, баланс между белковыми продуктами bcl-2 - bax, bel. XL- bcl. XS определяет сдвиг равновесия в сторону пролиферации или апоптоза в опухоли.

Роль генов-супрессоров при развитии опухолей сводится к блокированию апоптоза. • Ген р53 подвергается наиболее частым изменениям при опухолевом росте. Дикий тип р53 (природный) является транскрипционным фактором с множественными функциями, включающими регулировку перехода клеток из фазы G 1 в фазу S, репарацию ДНК, апоптоз вслед за повреждением генома. Мутированный р53 действует фактически как клеточный онкоген, стимулируя пролиферацию опухолевых клеток и вызывая образование антител. • Ген Rb кодирует синтез ядерного фосфопротеина и контролирует выход клетки из фазы G 1. Гипофосфорилирование Rb приводит к блокаде клетки на стадии GI и апоптозу. Инактивация Rb в опухолях достигается потерей одного из ал лелей и мутацией второго аллеля гена. • Большое значение в прогрессировании рака легкого имеют и некоторые факторы роста бомбезин, ЭФР и система инсулинподобных факторов роста. Роль хронического воспаления в канцерогенезе обусловлена генерацией клетками гранулем, клеточных пролифератов и инфильтратов, а также самими фибро бластами различных факторов роста и онкобелков, способствующих проли ферации эпителия. Значение рубцов в морфогенезе периферического рака легкого заключается в том, что в рубце может происходить депонирование экзо и эндогенных канцеро генов, вызывающих активацию протоонкогенов, а также возникают местная гипоксия и иммунодепрессия, нарушение межклеточных взаимодействий, из менение состава коллагенов внеклеточного матрикса. Пневмосклероз неза висимо от его происхождения может играть роль пробластоматозного, фоно вого процесса для развития рака.

v характеризуется развитием изменений как в паренхиматозных, так и в стро мальных элементах. Основными морфологическими критериями диспластичес ких процессов считают появление признаков клеточного атипизма в паренхиме органа при сохранной структуре ткани. В строме же очагов дисплазии регистри руют изменения состава внеклеточного матрикса, появление клеточного ин фильтрата, фибробластической реакции и др. Генетические перестройки могут значительно опережать морфологические изме нения и служить ранними признаками предопухолевых изменений. В крупных бронхах перечисленные выше процессы развиваются при попадании канцеро генов с вдыхаемым воздухом, что приводит к повреждению мукоцилиарного барьера и плоскоклеточной метаплазии, дисплазии и злокачественной транс формации. Описанные механизмы имеют большое значение для возникно вения рака крупных бронхов. В мелкие бронхи, бронхиолы и альвеолы канцерогенные агенты не только могут попадать с вдыхаемым воздухом, но и приноситься с кровью и лимфой и стать причиной развития периферического рака легкого. Наибольшее значение для развития периферического рака легкого имеют хрони ческое воспаление и пневмосклероз при туберкулезе, идиопатическом фибро зирующем альвеолите, в рубцах после перенесенного инфаркта легкого, вокруг инородных тел("рак в рубце"). В очагах хронического воспаления и пневмоскле роза возникают фокусы пролиферации эпителия бронхов, бронхиол и альвеол, состоящие из базальных, реснитчатых, слизистых клеток, бронхиолярных экзок риноцитов, альвеолоцитов 2 го типа. При прогрессировании процесса развиваются метаплазия и дисплазия бронхиаль ного и бронхиолярного эпителия, очаги аденоматоза с атипией эпителиальных клеток и атипическая гиперплазия эпителия.

Классификация построена на основе локализации опухоли, характере роста, макроскопическом виде, стадии процесса, гистогенезе (по Струкову А. И. , 1956; ВОЗ, I 999). По локализации выделяют: 1) прикорневой (центральный), исходящий из стволового, долевого и проксимальной части сегментарного бронха; 2) периферический, исходящий из бронхов меньшего калибра, бронхиол и, вероятно, альвеол; 3) смешанный (массивный) рак. По характеру роста выделяют: 1) экзофитный (эндобронхиальный); 2) эндофитный (экзобронхиальный и перибронхиальный) рак. По макроскопической форме: 1) бляшковидный; 2) полипозный; 3) эндобронхиальный диффузный; 4) узловатый; 5) разветвленный; 6) узловато разветвленный; 7) полостной; 8) пневмониоподобный рак.

По микроскопическому виду (гистогенезу): 1) плоскоклеточный (варианты по гистологическому строе нию и уровню дифференцировки); 2) мелкоклеточный классический (овсяноклеточный, лимфоцитоподобный, промежуточно клеточный), комбинированный; 3) аденокарцинома ацинарная, сосочковая, бронхиоло аль веолярная карцинома, солидная с продукцией слизи; 4) крупноклеточный рак гигантоклеточный рак, светлокле точный рак; 5) железисто-плоскоклеточный рак; 6) карциноидная опухоль; 7) рак бронхиальных желез аденоидно кистозный рак, мукоэпидермоидный рак и др.
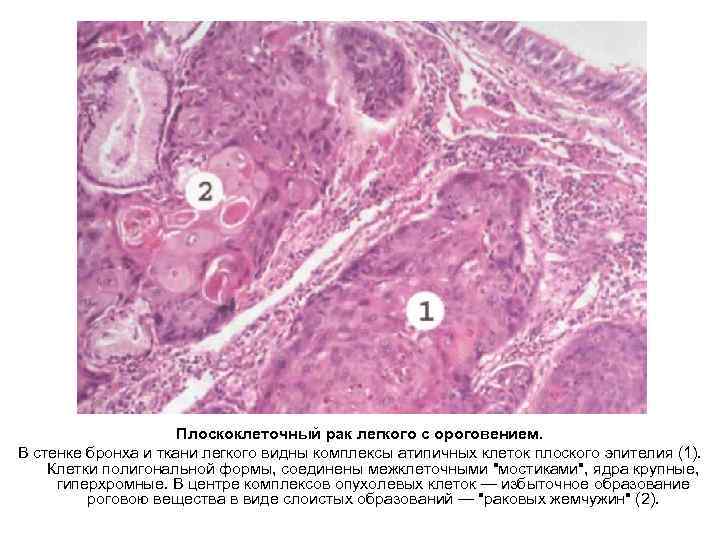
Плоскоклеточный рак легкого с ороговением. В стенке бронха и ткани легкого видны комплексы атипичных клеток плоского эпителия (1). Клетки полигональной формы, соединены межклеточными "мостиками", ядра крупные, гиперхромные. В центре комплексов опухолевых клеток — избыточное образование роговою вещества в виде слоистых образований — "раковых жемчужин" (2).
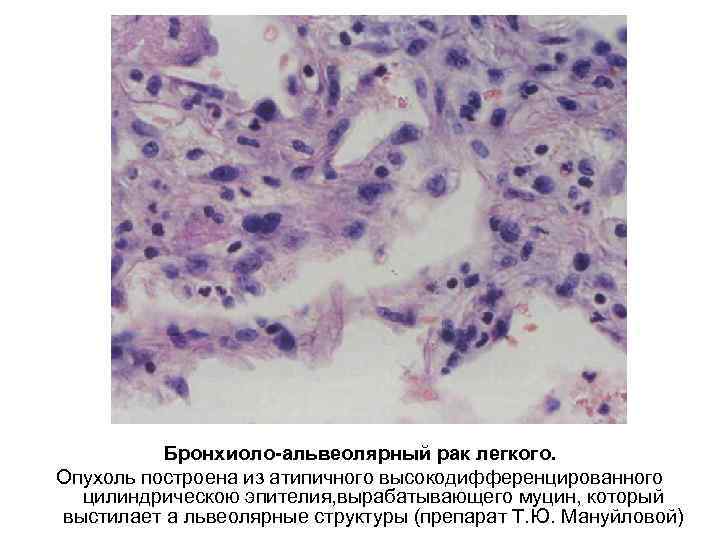
Бронхиоло-альвеолярный рак легкого. Опухоль построена из атипичного высокодифференцированного цилиндрическою эпителия, вырабатывающего муцин, который выстилает а львеолярные структуры (препарат Т. Ю. Мануйловой)

Крупноклеточный рак легкого при световой микроскопии содержит крупные раковые клетки, которые при гистохимическом и электронномикроскопическом исследованиях обнаруживают признаки плоского или железистого эпителия. Мелкоклеточный рак легкого - группа опухолей, которые на светооптическом уровне построены из мелких недифференцированных раковых клеток. Однако при гистохимическом и электронно-микроскопическом исследованиях в этой группе обнаруживают опухоли различной дифференцировки: плоскоклеточную, железистую, нейроэндокринную (преобладает) а также неклассифицируемые опухоли. Мелкоклеточный рак легкого характеризуется особыми биомолекулярными маркерами из группы клеточных онкогенов, генов-супрессоров и факторов роста. Кроме того, мелкоклеточный рак отличается и признаками нейроэндокринной дифференцировки, выявляемыми более чем в 90% случаев. Паренхиматозные клетки экспрессируют и хромогранин, и панцитокератины. Немелкоклеточный рак легкого - это гетерогенная группа опухолей, относящихся к разным гистогенетическим группам: плоскоклеточный рак (маркерами являются цитокератины, кератогиалин), аденокарцинома (цитокератины, слизь, сурфактант), а также крупноклеточный рак, который может быть представлен как низкодифференцированной аденокарииномой, так и низкодифференцированным плоскоклеточным раком.

• высокодифференцированная нейроэндокринная карцинома (синоним типичный, "доброкачествен ный" карциноид), • умеренно дифференцированная нейроэндокрин ная карцинома (атипичный, "злокачественный" карциноид), • низкодифференцированная нейроэндокринная карцинома (мелкоклеточный рак с нейроэндокрин ной дифференцировкой).

Патологическая анатомия прикорневого и периферического рака различна. Массивный рак фактически является поздней стадией развития централь ного или периферического рака. Ø Прикорневой рак. Этот рак развивается в крупных бронхах. Предраковые процессы: плоскоклеточная метаплазия и дисплазия брон хиального эпителия возникают, как правило, на фоне хронического воспаления. Преобладающие макроскопические формы: полипозный, узловатый, разветвленный, узловато разветвленный рак. Гистологически прикорневой рак связан с клетками бронхиального эпи телия базальной, бокаловидной и реснитчатой. Наиболее часто встре чающиеся гистологические типы прикорневого рака плоскоклеточный и мелкоклеточный. Его течение нередко осложняется ретростеничес кими абсцессами легких, ателектазами. Опухоль может прорастать в средостение, сердечную сорочку, пищевод, сосудистые стволы, что может стать причиной легочного кровотечения.

Ø Периферический рак легкого нередко развивается на фоне предшествующих склеротических измене ний — очаговых или диффузных. Предраковые процессы: плоскоклеточная метаплазия, дисплазия эпите лия мелких бронхов и бронхиол, аденоматоз с атипией клеток и атипи ческая гиперплазия эпителия. Преобладающие макроскопические формы: узловатая, узловато развет вленная, полостная и пневмониоподобная. Гистогенез периферического рака связан не только с базальной, бокало видной и реснитчатой клетками бронхов и бронхиол, но и с бронхиоляр ными экзокриноцитами (клетки Клара) и альвеолоцитами 2 го типа. Это определяет существование большего разнообразия гистологических типов периферического рака легкого по сравнению с центральным. Так, в периферических отделах легкого преобладают железистые карциномы, встречается бронхиоло-альвеолярная карцинома. Плоскоклеточный рак и мелкоклеточный рак выявляются значительно реже. Осложнения опухоли связаны с ее прорастанием в плевральную полость с развитием серозно геморрагического или геморрагического плеврита, распространением на крупные бронхи, распадом и нагноением самой опухоли.
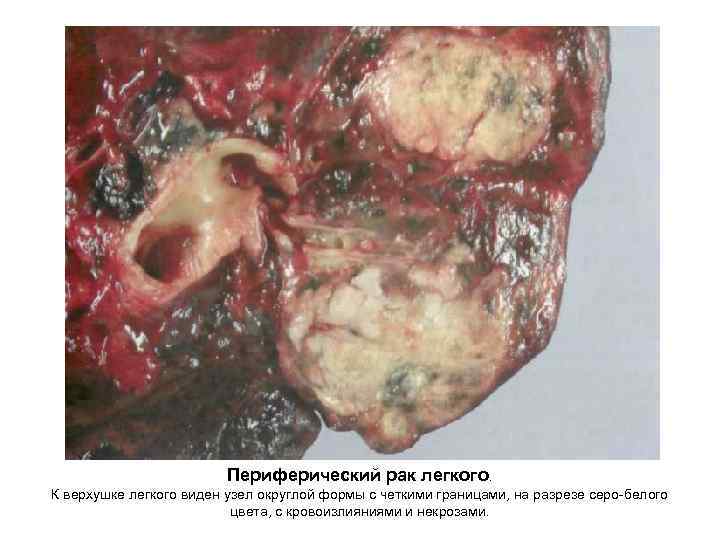
Периферический рак легкого. К верхушке легкого виден узел округлой формы с четкими границами, на разрезе серо белого цвета, с кровоизлияниями и некрозами.

На начальных стадиях метастазирование происходит преимущественно лимфогенным путем. Первые метастазы обнаруживаются в региональных лимфатических узлах. На поздних стадиях лимфогенные метастазы распространя ются в бифуркационные, паратрахеальные, медиастиналь ные и шейные лимфатические узлы, может развиться канцероматоз легких, плевры и брюшины, появляются гематогенные метастазы в печени, костях, надпочечниках, головном мозге.

болезни легких 2.ppt