лекция 4 хроматография инстр мет.ppt
- Количество слайдов: 87
 Хроматография газовая. ГЖХ и ВЭЖХ История открытия. Колоночная хроматография. Цвет Явления на границе раздела фаз. Адсорбция, изотермы адсорбции. Динамика адсорбционных процессов. Упрощенная модель распределительной хроматографии Жидкостная хроматография. Эффективность. Сопротивление неподвижной фазы. Аппаратурное оформление — хроматограф. ВЭЖХ. Детекторы Ионная хроматография. Детектор. Газовая хроматография. Хроматограф, блок-схема. Абсорбция, ГЖХ. Детекторы. Примеры применения.
Хроматография газовая. ГЖХ и ВЭЖХ История открытия. Колоночная хроматография. Цвет Явления на границе раздела фаз. Адсорбция, изотермы адсорбции. Динамика адсорбционных процессов. Упрощенная модель распределительной хроматографии Жидкостная хроматография. Эффективность. Сопротивление неподвижной фазы. Аппаратурное оформление — хроматограф. ВЭЖХ. Детекторы Ионная хроматография. Детектор. Газовая хроматография. Хроматограф, блок-схема. Абсорбция, ГЖХ. Детекторы. Примеры применения.
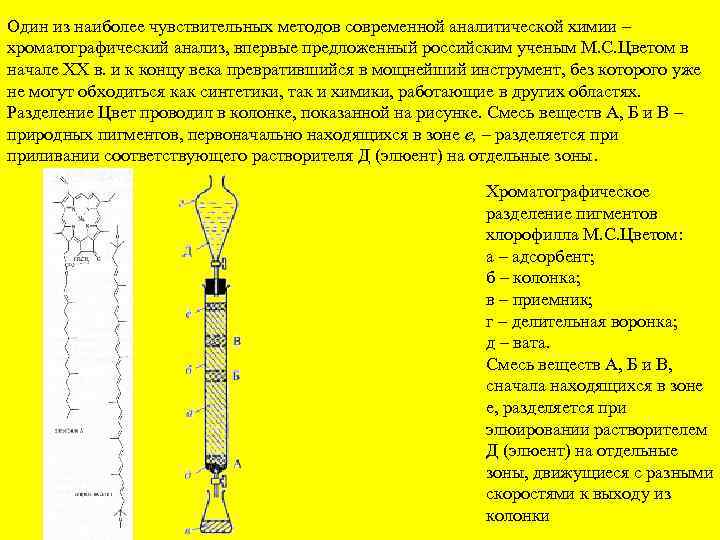 Один из наиболее чувствительных методов современной аналитической химии – хроматографический анализ, впервые предложенный российским ученым М. С. Цветом в начале XX в. и к концу века превратившийся в мощнейший инструмент, без которого уже не могут обходиться как синтетики, так и химики, работающие в других областях. Разделение Цвет проводил в колонке, показанной на рисунке. Смесь веществ А, Б и В – природных пигментов, первоначально находящихся в зоне е, – разделяется приливании соответствующего растворителя Д (элюент) на отдельные зоны. Хроматографическое разделение пигментов хлорофилла М. C. Цветом: а – адсорбент; б – колонка; в – приемник; г – делительная воронка; д – вата. Смесь веществ А, Б и В, сначала находящихся в зоне е, разделяется при элюировании растворителем Д (элюент) на отдельные зоны, движущиеся с разными скоростями к выходу из колонки
Один из наиболее чувствительных методов современной аналитической химии – хроматографический анализ, впервые предложенный российским ученым М. С. Цветом в начале XX в. и к концу века превратившийся в мощнейший инструмент, без которого уже не могут обходиться как синтетики, так и химики, работающие в других областях. Разделение Цвет проводил в колонке, показанной на рисунке. Смесь веществ А, Б и В – природных пигментов, первоначально находящихся в зоне е, – разделяется приливании соответствующего растворителя Д (элюент) на отдельные зоны. Хроматографическое разделение пигментов хлорофилла М. C. Цветом: а – адсорбент; б – колонка; в – приемник; г – делительная воронка; д – вата. Смесь веществ А, Б и В, сначала находящихся в зоне е, разделяется при элюировании растворителем Д (элюент) на отдельные зоны, движущиеся с разными скоростями к выходу из колонки
 Что является причиной хроматографического процесса? Адсорбция (лат. ad — на, при; sorbeo — поглощаю) — процесс концентрирования вещества из объёма фаз на границе их раздела. Поглощаемое вещество, еще находящееся в объеме фазы, называют адсорбтив, поглощенное — адсорбат. В более узком смысле под адсорбцией часто понимают поглощение примеси из газа или жидкости твердым веществом — адсорбентом. При этом, как и в общем случае адсорбции, происходит концентрирование примеси на границе раздела адсорбент-жидкость либо адсорбент-газ. Процесс, обратный адсорбции, то есть перенос вещества с поверхности раздела фаз в объем фазы, называется десорбция. И адсорбция и десорбция происходят одновременно. Только скорости у них разные.
Что является причиной хроматографического процесса? Адсорбция (лат. ad — на, при; sorbeo — поглощаю) — процесс концентрирования вещества из объёма фаз на границе их раздела. Поглощаемое вещество, еще находящееся в объеме фазы, называют адсорбтив, поглощенное — адсорбат. В более узком смысле под адсорбцией часто понимают поглощение примеси из газа или жидкости твердым веществом — адсорбентом. При этом, как и в общем случае адсорбции, происходит концентрирование примеси на границе раздела адсорбент-жидкость либо адсорбент-газ. Процесс, обратный адсорбции, то есть перенос вещества с поверхности раздела фаз в объем фазы, называется десорбция. И адсорбция и десорбция происходят одновременно. Только скорости у них разные.
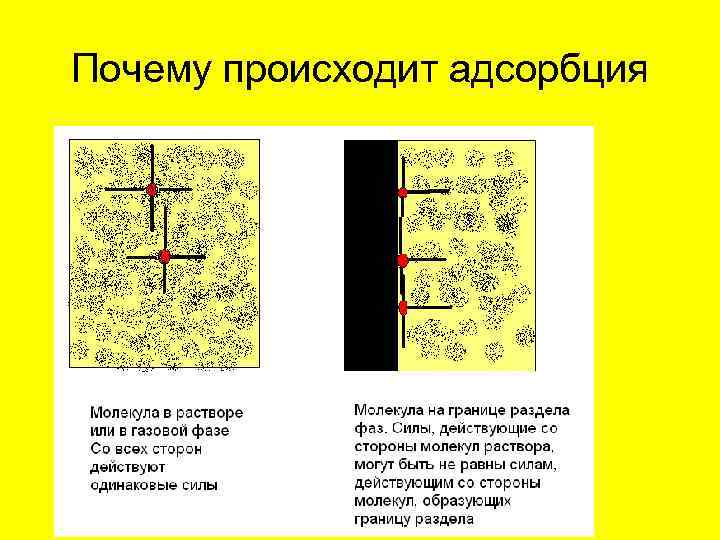 Почему происходит адсорбция
Почему происходит адсорбция

 Кроме Адсорбции существует еще Абсорбция. Если Адсорбция происходит на самой поверхности раздела, где адсорбированное вещество и остается, то при Абсорбции абсорбированное вещество уходит вглубь абсорбента. Если вы, например, выльете «Дюшес» на смазанный жиром противень, то через некоторое время вся отдушка «Дюшеса» (Амилацетат (амиловый эфир уксусной кислоты) СН 3(СН 2)4 ОСОСН 3) перейдет в жир Принципиальной разницы между этими явлениями нет
Кроме Адсорбции существует еще Абсорбция. Если Адсорбция происходит на самой поверхности раздела, где адсорбированное вещество и остается, то при Абсорбции абсорбированное вещество уходит вглубь абсорбента. Если вы, например, выльете «Дюшес» на смазанный жиром противень, то через некоторое время вся отдушка «Дюшеса» (Амилацетат (амиловый эфир уксусной кислоты) СН 3(СН 2)4 ОСОСН 3) перейдет в жир Принципиальной разницы между этими явлениями нет
 Если мы нальем в колбу воду из Москва-реки, содержащую нефтепродукты и другие загрязнения и насыпем в эту колбу адсорбент — березовый уголь, например, и потом некоторое время эту колбу повстряхиваем, то большая часть нефтепродуктов из воды адсорбируется на угле. Сколько нефтепродуктов адсорбируется, установить не так сложно. Нужно определить их количество в воде до и после процесса адсорбции. (Определить можно по поглощению в ИК-области и даже по поглощению в УФ-области, хотя это будет не совсем корректно). Если мы не будем лениться и будем определять содержание нефтепродуктов в воде через каждые пять минут встряхивания колбы, то мы увидим, что через некоторое время содержание нефтепродуктов в воде изменяться уже не будет. Это вовсе не значит, что процесс адсорбции прекратился. Это значит, что по мере того, как нефтепродукты адсорбировались на угле, в воде их становилось все меньше и меньше, а на угле все больше и больше. И чем больше их становилось на угле, тем чаще адсорбированные на угле нефтепродукты отрывались от него и переходили в воду. В конце концов скорости адсорбции и десорбции сравняются. И в воде установится «равновесие» . Это равновесие описывается «изотермой» адсорбции.
Если мы нальем в колбу воду из Москва-реки, содержащую нефтепродукты и другие загрязнения и насыпем в эту колбу адсорбент — березовый уголь, например, и потом некоторое время эту колбу повстряхиваем, то большая часть нефтепродуктов из воды адсорбируется на угле. Сколько нефтепродуктов адсорбируется, установить не так сложно. Нужно определить их количество в воде до и после процесса адсорбции. (Определить можно по поглощению в ИК-области и даже по поглощению в УФ-области, хотя это будет не совсем корректно). Если мы не будем лениться и будем определять содержание нефтепродуктов в воде через каждые пять минут встряхивания колбы, то мы увидим, что через некоторое время содержание нефтепродуктов в воде изменяться уже не будет. Это вовсе не значит, что процесс адсорбции прекратился. Это значит, что по мере того, как нефтепродукты адсорбировались на угле, в воде их становилось все меньше и меньше, а на угле все больше и больше. И чем больше их становилось на угле, тем чаще адсорбированные на угле нефтепродукты отрывались от него и переходили в воду. В конце концов скорости адсорбции и десорбции сравняются. И в воде установится «равновесие» . Это равновесие описывается «изотермой» адсорбции.
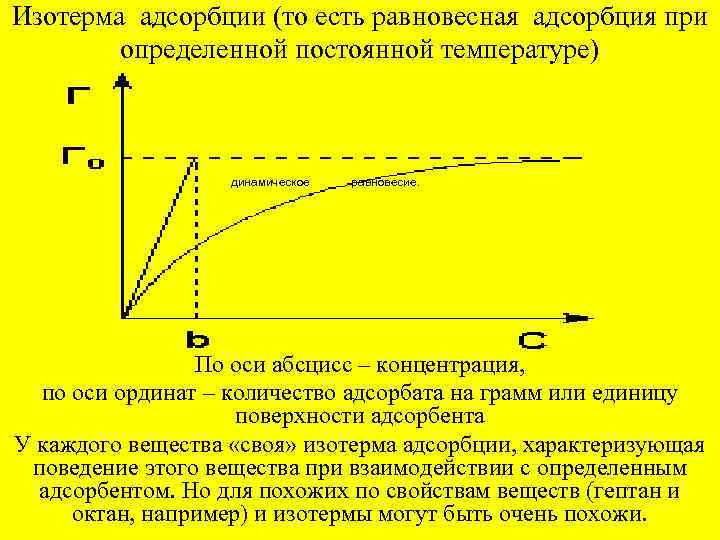 Изотерма адсорбции (то есть равновесная адсорбция при определенной постоянной температуре) динамическое равновесие. По оси абсцисс – концентрация, по оси ординат – количество адсорбата на грамм или единицу поверхности адсорбента У каждого вещества «своя» изотерма адсорбции, характеризующая поведение этого вещества при взаимодействии с определенным адсорбентом. Но для похожих по свойствам веществ (гептан и октан, например) и изотермы могут быть очень похожи.
Изотерма адсорбции (то есть равновесная адсорбция при определенной постоянной температуре) динамическое равновесие. По оси абсцисс – концентрация, по оси ординат – количество адсорбата на грамм или единицу поверхности адсорбента У каждого вещества «своя» изотерма адсорбции, характеризующая поведение этого вещества при взаимодействии с определенным адсорбентом. Но для похожих по свойствам веществ (гептан и октан, например) и изотермы могут быть очень похожи.
 Различие изотерм (то есть различие содержания адсорбированного вещества и вещества в растворе) и позволяет нам производить хроматографическое разделение веществ. Хроматография основана на следующем: еcли две фазы находятся в контакте друг с другом, причем одна из них или обе содержат растворенное вещество, это вещество будет распределяться между двумя фазами. Этот процесс именуется распределением и количественно описывается коэффициентом распределения, представляющим собой отношение концентраций растворенного вещества в каждой из двух фаз. Рассмотрим распределительную хроматографию на колонке, где колонкой служит трубка, заполненная сорбентом и растворителем. Раствор, содержащий разделяемую смесь, вводят в колонку так, чтобы растворенные вещества проникли в сорбент. Затем через колонку пропускают растворитель. Хотя сорбент и растворитель распределены по всей колонке равномерно, колонку можно рассматривать как совокупность множества отдельных слоев ( «теоретических тарелок» ), каждый из которых содержит две фазы.
Различие изотерм (то есть различие содержания адсорбированного вещества и вещества в растворе) и позволяет нам производить хроматографическое разделение веществ. Хроматография основана на следующем: еcли две фазы находятся в контакте друг с другом, причем одна из них или обе содержат растворенное вещество, это вещество будет распределяться между двумя фазами. Этот процесс именуется распределением и количественно описывается коэффициентом распределения, представляющим собой отношение концентраций растворенного вещества в каждой из двух фаз. Рассмотрим распределительную хроматографию на колонке, где колонкой служит трубка, заполненная сорбентом и растворителем. Раствор, содержащий разделяемую смесь, вводят в колонку так, чтобы растворенные вещества проникли в сорбент. Затем через колонку пропускают растворитель. Хотя сорбент и растворитель распределены по всей колонке равномерно, колонку можно рассматривать как совокупность множества отдельных слоев ( «теоретических тарелок» ), каждый из которых содержит две фазы.
 Представим, что 256 идентичных молекул, которые равномерно распределяются между неподвижной и подвижной фазами, введены в колонку с 18 теоретическими тарелками (верхний рисунок справа далее по тексту). В верхней теоретической тарелке (начальной) 256 молекул распределены так, что в каждой фазе находится по 128 молекул. При переходе 128 подвижных молекул с первой теоретической тарелки па вторую они распределяются на ней по 64; оставшиеся на первой теоретической тарелке 128 молекул перераспределяются по 64 в каждой фазе, как показано на рисунке. При продвижении подвижных фаз еще на одну теоретическую тарелку снова происходит перераспределение. После 20 последовательных переносов достигается состояние, изображенное на рисунке.
Представим, что 256 идентичных молекул, которые равномерно распределяются между неподвижной и подвижной фазами, введены в колонку с 18 теоретическими тарелками (верхний рисунок справа далее по тексту). В верхней теоретической тарелке (начальной) 256 молекул распределены так, что в каждой фазе находится по 128 молекул. При переходе 128 подвижных молекул с первой теоретической тарелки па вторую они распределяются на ней по 64; оставшиеся на первой теоретической тарелке 128 молекул перераспределяются по 64 в каждой фазе, как показано на рисунке. При продвижении подвижных фаз еще на одну теоретическую тарелку снова происходит перераспределение. После 20 последовательных переносов достигается состояние, изображенное на рисунке.

 Предположим, что на первой теоретической тарелке находится 256 молекул другого типа (на рисунке цифры снаружи колонки), которые в 3 раза больше распределяются в неподвижную фазу. На рисунке показано также их распределение после 20 переносов. Распределение этих двух видов молекул сильно различается, поэтому в результате отделяется значительная часть молекул. Чем больше число теоретических тарелок (т. е. длина колонки), тем лучше разделение. Следует отметить, что при увеличении числа теоретических тарелок вещество распределяется по большей части колонки. В действительности, когда число молекул огромно (т. е. больше 1016), число молекул на первой теоретической тарелке отличается от нуля. С другой стороны, степень распределения уменьшается в том смысле, что большая доля вещества находится на небольшой части теоретических тарелок. Например, после 8 переносов 40% молекул, которые на рисунке распределяются 1: 1, содержится в 4/8 теоретических тарелок, после 20 переносов 40% содержится уже в 6/16, или 3/8, теоретических тарелок. Отсюда ясно, что в идеальном случае, когда разделение определяется только распределением, разделение двух веществ будет более эффективным при увеличении длины колонки.
Предположим, что на первой теоретической тарелке находится 256 молекул другого типа (на рисунке цифры снаружи колонки), которые в 3 раза больше распределяются в неподвижную фазу. На рисунке показано также их распределение после 20 переносов. Распределение этих двух видов молекул сильно различается, поэтому в результате отделяется значительная часть молекул. Чем больше число теоретических тарелок (т. е. длина колонки), тем лучше разделение. Следует отметить, что при увеличении числа теоретических тарелок вещество распределяется по большей части колонки. В действительности, когда число молекул огромно (т. е. больше 1016), число молекул на первой теоретической тарелке отличается от нуля. С другой стороны, степень распределения уменьшается в том смысле, что большая доля вещества находится на небольшой части теоретических тарелок. Например, после 8 переносов 40% молекул, которые на рисунке распределяются 1: 1, содержится в 4/8 теоретических тарелок, после 20 переносов 40% содержится уже в 6/16, или 3/8, теоретических тарелок. Отсюда ясно, что в идеальном случае, когда разделение определяется только распределением, разделение двух веществ будет более эффективным при увеличении длины колонки.
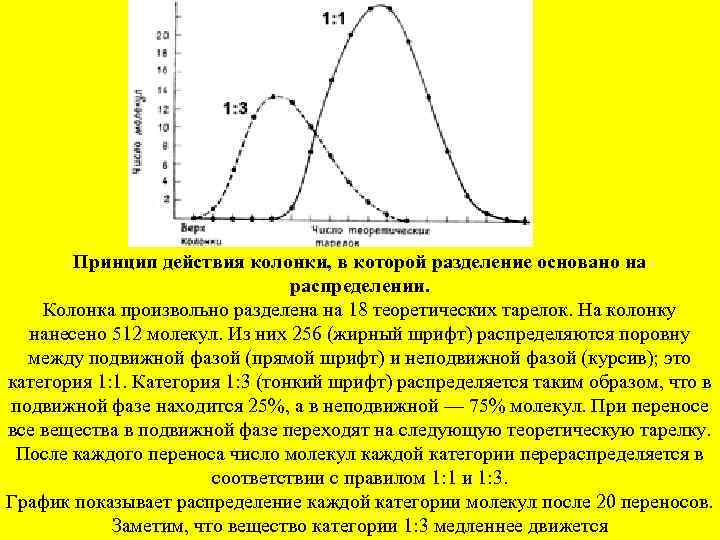 Принцип действия колонки, в которой разделение основано на распределении. Колонка произвольно разделена на 18 теоретических тарелок. На колонку нанесено 512 молекул. Из них 256 (жирный шрифт) распределяются поровну между подвижной фазой (прямой шрифт) и неподвижной фазой (курсив); это категория 1: 1. Категория 1: 3 (тонкий шрифт) распределяется таким образом, что в подвижной фазе находится 25%, а в неподвижной — 75% молекул. При переносе вещества в подвижной фазе переходят на следующую теоретическую тарелку. После каждого переноса число молекул каждой категории перераспределяется в соответствии с правилом 1: 1 и 1: 3. График показывает распределение каждой категории молекул после 20 переносов. Заметим, что вещество категории 1: 3 медленнее движется
Принцип действия колонки, в которой разделение основано на распределении. Колонка произвольно разделена на 18 теоретических тарелок. На колонку нанесено 512 молекул. Из них 256 (жирный шрифт) распределяются поровну между подвижной фазой (прямой шрифт) и неподвижной фазой (курсив); это категория 1: 1. Категория 1: 3 (тонкий шрифт) распределяется таким образом, что в подвижной фазе находится 25%, а в неподвижной — 75% молекул. При переносе вещества в подвижной фазе переходят на следующую теоретическую тарелку. После каждого переноса число молекул каждой категории перераспределяется в соответствии с правилом 1: 1 и 1: 3. График показывает распределение каждой категории молекул после 20 переносов. Заметим, что вещество категории 1: 3 медленнее движется

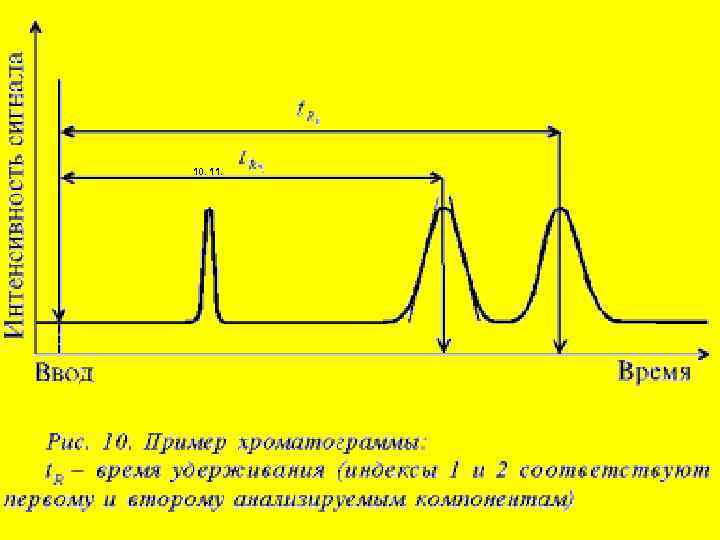
 В зависимости от способа регистрации различают внутренние и внешние хроматограммы. При внутренне. м способе регистрации компоненты анализируемой смеси за одно и то же время проходят различные расстояния. По окончании процесса разделения все они находятся внутри разделяющего устройства и там детектируются. Этот способ регистрации характерен для тонкослойной или бумажной хроматографии. В этом случае хроматографической характеристикой вещества я вляется отношение расстояние, которое вещество пройдет от начала хроматографирования до его окончания к расстоянию, которое пройдет растворитель (Rf). Данные по этим величинам (с указанием неподвижной фазы и элюэнта) сведены в базы данных. При внешнем способе регистрации все компоненты проходят одно расстояние (длину колонки) и регистрируются на выходе из колонки. В этом случае хроматографической характеристикой является «время удерживания» -- то время, через которое вещество при данных условиях (неподвижная фаза, температура, скорость подвижной фазы) выходит из колонки.
В зависимости от способа регистрации различают внутренние и внешние хроматограммы. При внутренне. м способе регистрации компоненты анализируемой смеси за одно и то же время проходят различные расстояния. По окончании процесса разделения все они находятся внутри разделяющего устройства и там детектируются. Этот способ регистрации характерен для тонкослойной или бумажной хроматографии. В этом случае хроматографической характеристикой вещества я вляется отношение расстояние, которое вещество пройдет от начала хроматографирования до его окончания к расстоянию, которое пройдет растворитель (Rf). Данные по этим величинам (с указанием неподвижной фазы и элюэнта) сведены в базы данных. При внешнем способе регистрации все компоненты проходят одно расстояние (длину колонки) и регистрируются на выходе из колонки. В этом случае хроматографической характеристикой является «время удерживания» -- то время, через которое вещество при данных условиях (неподвижная фаза, температура, скорость подвижной фазы) выходит из колонки.
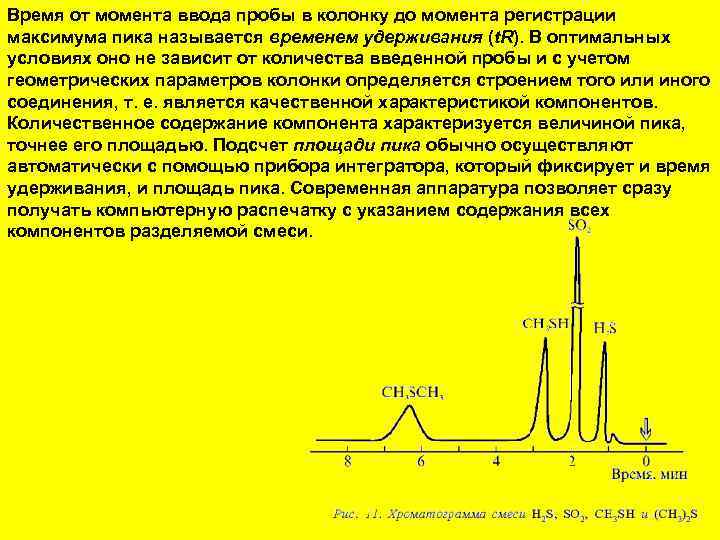 Время от момента ввода пробы в колонку до момента регистрации максимума пика называется временем удерживания (t. R). В оптимальных условиях оно не зависит от количества введенной пробы и с учетом геометрических параметров колонки определяется строением того или иного соединения, т. е. является качественной характеристикой компонентов. Количественное содержание компонента характеризуется величиной пика, точнее его площадью. Подсчет площади пика обычно осуществляют автоматически с помощью прибора интегратора, который фиксирует и время удерживания, и площадь пика. Современная аппаратура позволяет сразу получать компьютерную распечатку с указанием содержания всех компонентов разделяемой смеси.
Время от момента ввода пробы в колонку до момента регистрации максимума пика называется временем удерживания (t. R). В оптимальных условиях оно не зависит от количества введенной пробы и с учетом геометрических параметров колонки определяется строением того или иного соединения, т. е. является качественной характеристикой компонентов. Количественное содержание компонента характеризуется величиной пика, точнее его площадью. Подсчет площади пика обычно осуществляют автоматически с помощью прибора интегратора, который фиксирует и время удерживания, и площадь пика. Современная аппаратура позволяет сразу получать компьютерную распечатку с указанием содержания всех компонентов разделяемой смеси.
 10, 11.
10, 11.

 Современный газовый хроматограф
Современный газовый хроматограф
 Современный жидкостной хроматограф
Современный жидкостной хроматограф
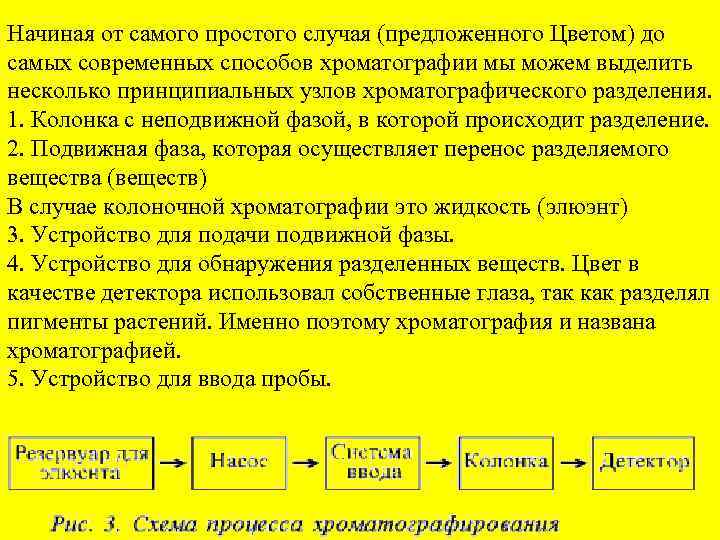 Начиная от самого простого случая (предложенного Цветом) до самых современных способов хроматографии мы можем выделить несколько принципиальных узлов хроматографического разделения. 1. Колонка с неподвижной фазой, в которой происходит разделение. 2. Подвижная фаза, которая осуществляет перенос разделяемого вещества (веществ) В случае колоночной хроматографии это жидкость (элюэнт) 3. Устройство для подачи подвижной фазы. 4. Устройство для обнаружения разделенных веществ. Цвет в качестве детектора использовал собственные глаза, так как разделял пигменты растений. Именно поэтому хроматография и названа хроматографией. 5. Устройство для ввода пробы.
Начиная от самого простого случая (предложенного Цветом) до самых современных способов хроматографии мы можем выделить несколько принципиальных узлов хроматографического разделения. 1. Колонка с неподвижной фазой, в которой происходит разделение. 2. Подвижная фаза, которая осуществляет перенос разделяемого вещества (веществ) В случае колоночной хроматографии это жидкость (элюэнт) 3. Устройство для подачи подвижной фазы. 4. Устройство для обнаружения разделенных веществ. Цвет в качестве детектора использовал собственные глаза, так как разделял пигменты растений. Именно поэтому хроматография и названа хроматографией. 5. Устройство для ввода пробы.
 Для оценки эффективности хроматографических процессов, исходя из теоретического представления о дистилляции (по аналогии с разделением нефти на ректификационных колоннах, где теоретическая тарелка соответствует части ректификационной колонны, в которой пар и жидкость находятся в равновесии), вводят понятие «высота, эквивалентная теоретической тарелке» (ВЭТТ). Хроматографическая колонка, таким образом, рассматривается как набор гипотетических слоев (тарелок). Под ВЭТТ обычно подразумевают такую толщину слоя, которая необходима для того, чтобы смесь, поступившая из предыдущего слоя, пришла в равновесие со средней концентрацией вещества в подвижной фазе этого слоя. Ее можно описать следующей формулой: ВЭТТ = L/N, где L – длина колонки, N – число теоретических тарелок. ВЭТТ является суммарной характеристикой разделения веществ. И уж если мы говорим о «равновесии» , то это значит, что скорость подачи подвижной фазы увеличивать можно только до определенного (и небольшого) предела. Иначе разделения не произойдет – в подвижной фазе будет оставаться слишком много веществ, не успевших прореагировать с неподвижной фазой. И за счет этого различие в коэффициентах распределения веществ будет невелировано. На выходе из колонки вместо пика, характеризующего одно вещество, будет смесь веществ, пусть и не того состава, который введен в колонку.
Для оценки эффективности хроматографических процессов, исходя из теоретического представления о дистилляции (по аналогии с разделением нефти на ректификационных колоннах, где теоретическая тарелка соответствует части ректификационной колонны, в которой пар и жидкость находятся в равновесии), вводят понятие «высота, эквивалентная теоретической тарелке» (ВЭТТ). Хроматографическая колонка, таким образом, рассматривается как набор гипотетических слоев (тарелок). Под ВЭТТ обычно подразумевают такую толщину слоя, которая необходима для того, чтобы смесь, поступившая из предыдущего слоя, пришла в равновесие со средней концентрацией вещества в подвижной фазе этого слоя. Ее можно описать следующей формулой: ВЭТТ = L/N, где L – длина колонки, N – число теоретических тарелок. ВЭТТ является суммарной характеристикой разделения веществ. И уж если мы говорим о «равновесии» , то это значит, что скорость подачи подвижной фазы увеличивать можно только до определенного (и небольшого) предела. Иначе разделения не произойдет – в подвижной фазе будет оставаться слишком много веществ, не успевших прореагировать с неподвижной фазой. И за счет этого различие в коэффициентах распределения веществ будет невелировано. На выходе из колонки вместо пика, характеризующего одно вещество, будет смесь веществ, пусть и не того состава, который введен в колонку.
 С этого и началась современная высокоэффективная жидкостная хроматография (ВЭЖХ). Разделять вещества на коротких колонках оказалось невозможно. А разделение на длинных требовало слишком много времени. Выход был — надо было уменьшить толщину теоретической тарелки за счет повышения ее эффективности, то есть за счет увеличения поверхности неподвижной фазы, следовательно — за счет повышения степени ее измельчения. Однако колонка, набитая очень мелкой (3 -10 мкм) неподвижной фазой, жидкость не пропускала. А при попытке увеличения давления стеклянные колонки лопались. И так было до тех пор, пока не стали использовать колонки из нержавеющей стали. Так появился жидкостной хроматограф, который вы видите на следующем слайде.
С этого и началась современная высокоэффективная жидкостная хроматография (ВЭЖХ). Разделять вещества на коротких колонках оказалось невозможно. А разделение на длинных требовало слишком много времени. Выход был — надо было уменьшить толщину теоретической тарелки за счет повышения ее эффективности, то есть за счет увеличения поверхности неподвижной фазы, следовательно — за счет повышения степени ее измельчения. Однако колонка, набитая очень мелкой (3 -10 мкм) неподвижной фазой, жидкость не пропускала. А при попытке увеличения давления стеклянные колонки лопались. И так было до тех пор, пока не стали использовать колонки из нержавеющей стали. Так появился жидкостной хроматограф, который вы видите на следующем слайде.
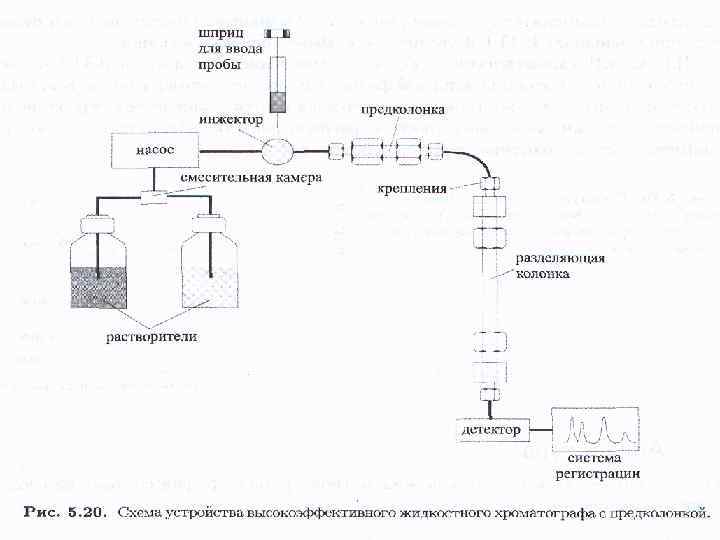

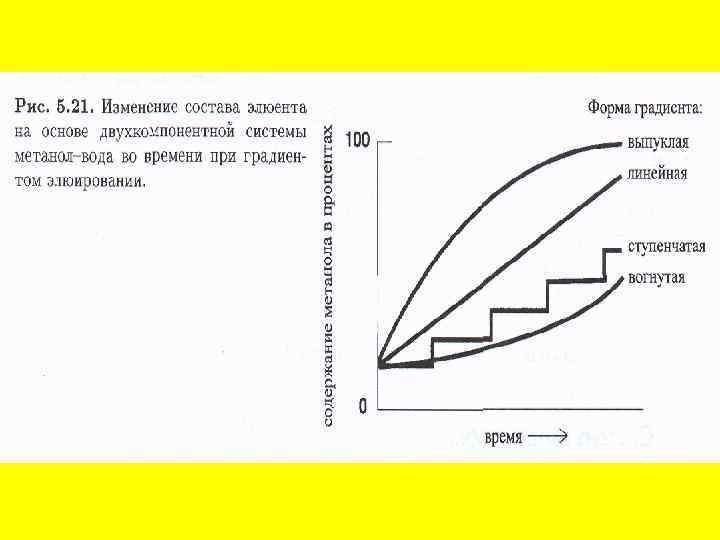



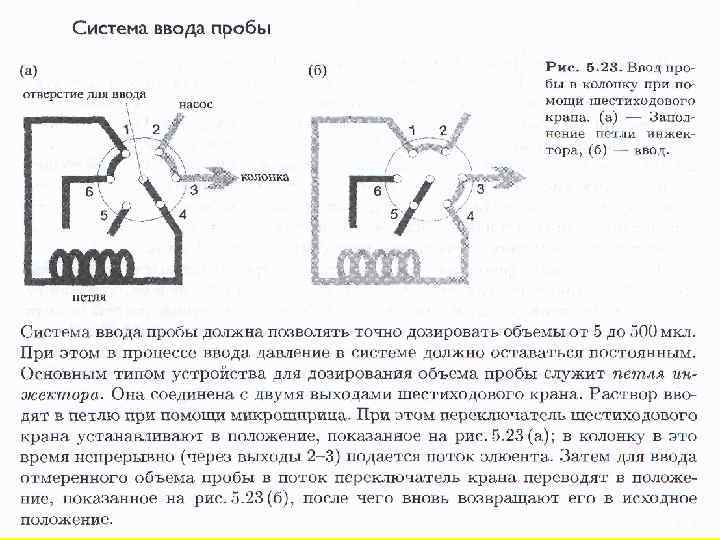
 Колонки делают из нержавеющей стали из специального толстостенного химического стекла (пирекс). Иногда, для защиты колонки, ставят «предколонку» где может происходить предварительное разделение. Обычно ее заполняют более крупной неподвижной фазой. В основной же колонке размер фазы – 3 -10 мкм. Поэтому давление в системе доходит до 60 МПа (около 600 атм). Однако разделить компоненты смеси важно, но недостаточно. Необходимо идентифицировать каждый компонент и определить его количество в пробе. Обычно это осуществляют с помощью обработки хроматограмм – зависимости интенсивности сигнала, пропорционального концентрации вещества, от времени разделения. Для этого служит система детектирования.
Колонки делают из нержавеющей стали из специального толстостенного химического стекла (пирекс). Иногда, для защиты колонки, ставят «предколонку» где может происходить предварительное разделение. Обычно ее заполняют более крупной неподвижной фазой. В основной же колонке размер фазы – 3 -10 мкм. Поэтому давление в системе доходит до 60 МПа (около 600 атм). Однако разделить компоненты смеси важно, но недостаточно. Необходимо идентифицировать каждый компонент и определить его количество в пробе. Обычно это осуществляют с помощью обработки хроматограмм – зависимости интенсивности сигнала, пропорционального концентрации вещества, от времени разделения. Для этого служит система детектирования.
 ДЕТЕКТОРЫ ХРОМАТОГРАФИЧЕСКИЕ (лат. detector -тот, кто раскрывает, обнаруживает), устройства для количеств. и качеств. определения в-в разделяемой смеси в потоке подвижной фазы на выходе из хроматографич. колонки. детекторы хроматографические можно рассматривать также как преобразоват. элемент, в к-ром изменение состава проходящей через него смеси преобразуется в изменение выходного сигнала. Различают детекторы хроматографические дифференциального и интегрального типа. Первые регистрируют мгновенное значение одной из характеристик (концентрации или потока), вторые суммируют кол-во в-ва за определенный промежуток времени.
ДЕТЕКТОРЫ ХРОМАТОГРАФИЧЕСКИЕ (лат. detector -тот, кто раскрывает, обнаруживает), устройства для количеств. и качеств. определения в-в разделяемой смеси в потоке подвижной фазы на выходе из хроматографич. колонки. детекторы хроматографические можно рассматривать также как преобразоват. элемент, в к-ром изменение состава проходящей через него смеси преобразуется в изменение выходного сигнала. Различают детекторы хроматографические дифференциального и интегрального типа. Первые регистрируют мгновенное значение одной из характеристик (концентрации или потока), вторые суммируют кол-во в-ва за определенный промежуток времени.
 Основные характеристики хроматографических детекторов: чувствительность, предел обнаружения, линейный динамич. диапазон. Чувствительность - отношение изменения выходного сигнала к изменению концентрации (или массовой скорости) анализируемого в-ва, поступающего в детектор. Предел обнаружения — миним. концентрация анализируемого в-ва, к-рые еще можно обнаружить. Предел обнаружения хроматографич. методики — наименьшее содержание контрольного в-ва, определяемое детектором с заданной доверит. вероятностью; при этом выходной сигнал должен в 2 раза превышать уровень флуктуационных шумов. Линейный динамич. диапазон — интервал, в к-ром сохраняется линейная зависимость показаний детектора от концентрации или кол -ва анализируемого в-ва. Он определяется как отношение макс. концентрации, при к-рой сохраняется линейность, к миним. определяемой концентрации. Значение чувствительности детектора в линейном динамич. диапазоне величина постоянная. Детекторы должны обладать: низким пределом обнаружения; миним. размыванием хроматографич. зон; широким линейным динамич. диапазоном; низким значением дрейфа выходного сигнала во времени под влиянием разл. факторов и низким уровнем шума; малой инерционностью; слабой зависимостью показаний от состава подвижной фазы, изменения скорости ее потока и пульсаций, а также от изменения т-ры; надежностью и простотой в обслуживании.
Основные характеристики хроматографических детекторов: чувствительность, предел обнаружения, линейный динамич. диапазон. Чувствительность - отношение изменения выходного сигнала к изменению концентрации (или массовой скорости) анализируемого в-ва, поступающего в детектор. Предел обнаружения — миним. концентрация анализируемого в-ва, к-рые еще можно обнаружить. Предел обнаружения хроматографич. методики — наименьшее содержание контрольного в-ва, определяемое детектором с заданной доверит. вероятностью; при этом выходной сигнал должен в 2 раза превышать уровень флуктуационных шумов. Линейный динамич. диапазон — интервал, в к-ром сохраняется линейная зависимость показаний детектора от концентрации или кол -ва анализируемого в-ва. Он определяется как отношение макс. концентрации, при к-рой сохраняется линейность, к миним. определяемой концентрации. Значение чувствительности детектора в линейном динамич. диапазоне величина постоянная. Детекторы должны обладать: низким пределом обнаружения; миним. размыванием хроматографич. зон; широким линейным динамич. диапазоном; низким значением дрейфа выходного сигнала во времени под влиянием разл. факторов и низким уровнем шума; малой инерционностью; слабой зависимостью показаний от состава подвижной фазы, изменения скорости ее потока и пульсаций, а также от изменения т-ры; надежностью и простотой в обслуживании.


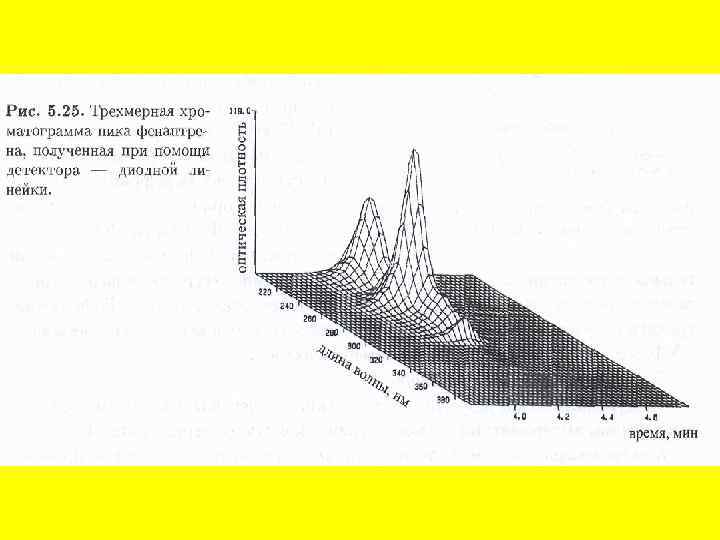










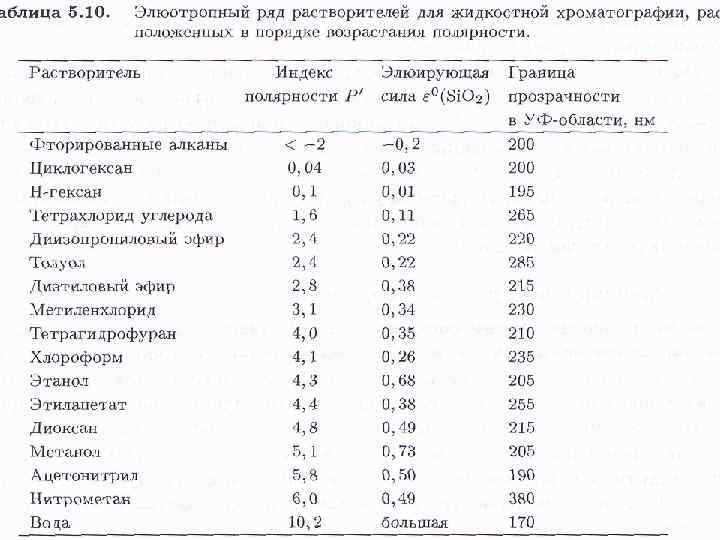

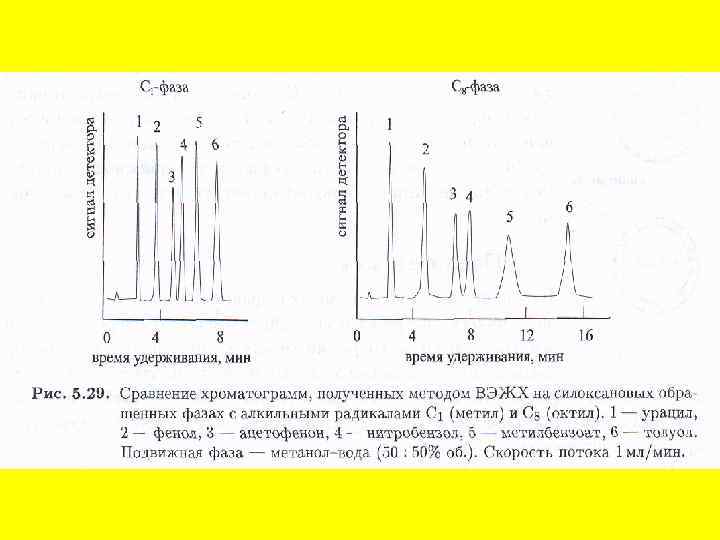
 Ионообменная хроматография. В качестве неподвижной фазы используют ионообменные смолы (рис. 4) как в колонках, так и в виде тонкого слоя на пластинке или бумаге. Разделение обычно проводят в водных средах, поэтому этот метод используется главным образом в неорганической химии, хотя применяются и смешанные растворители. Движущей силой разделения в этом случае является различное сродство разделяемых ионов раствора к ионообменным центрам противоположной полярности в неподвижной фазе Изображение структуры частицы ионообменной смолы: · – заряженные функциональные группы, ковалентно связанные с нитями решетки; ° – свободно перемещающиеся противоположно заряженные протовоионы, электростатически связанные с частицей смолы, способные претерпевать обмен с другими ионами
Ионообменная хроматография. В качестве неподвижной фазы используют ионообменные смолы (рис. 4) как в колонках, так и в виде тонкого слоя на пластинке или бумаге. Разделение обычно проводят в водных средах, поэтому этот метод используется главным образом в неорганической химии, хотя применяются и смешанные растворители. Движущей силой разделения в этом случае является различное сродство разделяемых ионов раствора к ионообменным центрам противоположной полярности в неподвижной фазе Изображение структуры частицы ионообменной смолы: · – заряженные функциональные группы, ковалентно связанные с нитями решетки; ° – свободно перемещающиеся противоположно заряженные протовоионы, электростатически связанные с частицей смолы, способные претерпевать обмен с другими ионами


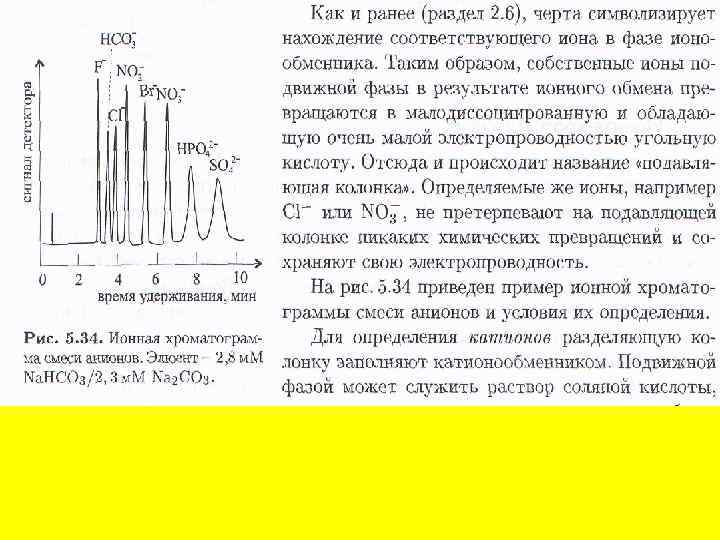
 А подавляющую колонку заполняют анионообменником в ОНформе. Реакция элюента в подавляющей колонке в этом случае проходит по уравнению Однако емкость ионообменника в этом случае быстро исчерпывается и его приходится регенерировать
А подавляющую колонку заполняют анионообменником в ОНформе. Реакция элюента в подавляющей колонке в этом случае проходит по уравнению Однако емкость ионообменника в этом случае быстро исчерпывается и его приходится регенерировать

 Проблемы количественного анализа и градуировки — общие для всех видов хроматографии и мы рассмотрим их позже.
Проблемы количественного анализа и градуировки — общие для всех видов хроматографии и мы рассмотрим их позже.
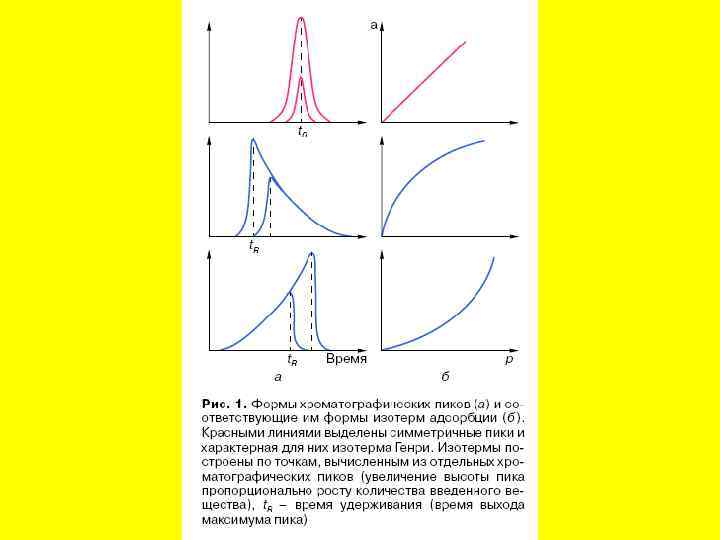
 Газовая хроматография. Хотя первой появилась на свет жидкостная хроматография, первым хроматографом был газовый. То есть тот, в котором подвижной фазой был газ, а неподвижной — твердый адсорбент. Из-за этого конструкции жидкостного и газового хроматографов отличаются, но принципиальных различий нет. Газовая хроматография существует в двух видах – в первом случае неподвижная фаза сама является сорбентом, во втором случае она является инертным носителем очень вязкой и термически устойчивой жидкой фазы, которая и взаимодействует (абсорбирует их) с разделяемыми веществами. Механизмы хроматографического разделения и у газовой и у жидкостной хроматографии можно считать подобными. Вещества можно разделить тогда, когда их изотермы адсорбции на неподвижной фазе – адсорбенте – различны. В зависимости от вида изотерм различаются и формы выходящих пиков.
Газовая хроматография. Хотя первой появилась на свет жидкостная хроматография, первым хроматографом был газовый. То есть тот, в котором подвижной фазой был газ, а неподвижной — твердый адсорбент. Из-за этого конструкции жидкостного и газового хроматографов отличаются, но принципиальных различий нет. Газовая хроматография существует в двух видах – в первом случае неподвижная фаза сама является сорбентом, во втором случае она является инертным носителем очень вязкой и термически устойчивой жидкой фазы, которая и взаимодействует (абсорбирует их) с разделяемыми веществами. Механизмы хроматографического разделения и у газовой и у жидкостной хроматографии можно считать подобными. Вещества можно разделить тогда, когда их изотермы адсорбции на неподвижной фазе – адсорбенте – различны. В зависимости от вида изотерм различаются и формы выходящих пиков.
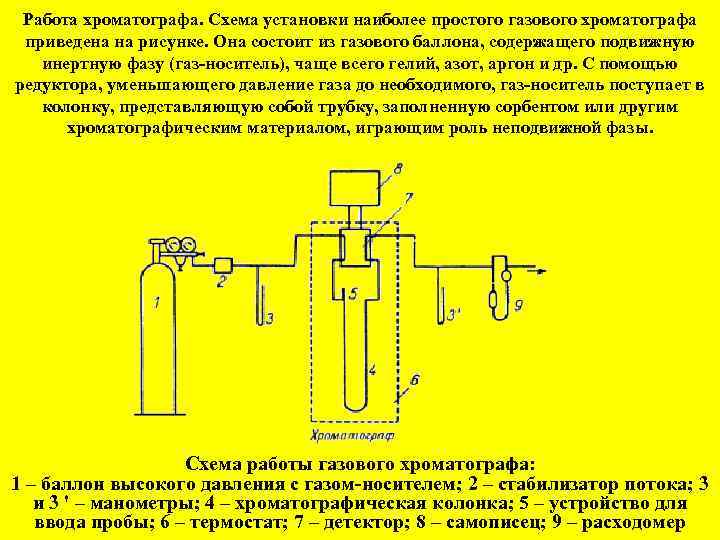 Работа хроматографа. Схема установки наиболее простого газового хроматографа приведена на рисунке. Она состоит из газового баллона, содержащего подвижную инертную фазу (газ-носитель), чаще всего гелий, азот, аргон и др. С помощью редуктора, уменьшающего давление газа до необходимого, газ-носитель поступает в колонку, представляющую собой трубку, заполненную сорбентом или другим хроматографическим материалом, играющим роль неподвижной фазы. Схема работы газового хроматографа: 1 – баллон высокого давления с газом-носителем; 2 – стабилизатор потока; 3 и 3 ' – манометры; 4 – хроматографическая колонка; 5 – устройство для ввода пробы; 6 – термостат; 7 – детектор; 8 – самописец; 9 – расходомер
Работа хроматографа. Схема установки наиболее простого газового хроматографа приведена на рисунке. Она состоит из газового баллона, содержащего подвижную инертную фазу (газ-носитель), чаще всего гелий, азот, аргон и др. С помощью редуктора, уменьшающего давление газа до необходимого, газ-носитель поступает в колонку, представляющую собой трубку, заполненную сорбентом или другим хроматографическим материалом, играющим роль неподвижной фазы. Схема работы газового хроматографа: 1 – баллон высокого давления с газом-носителем; 2 – стабилизатор потока; 3 и 3 ' – манометры; 4 – хроматографическая колонка; 5 – устройство для ввода пробы; 6 – термостат; 7 – детектор; 8 – самописец; 9 – расходомер

 Хроматографическая колонка – это «сердце» хроматографа, поскольку именно в ней происходит разделение смесей. Колонки чаще всего изготавливают из стекла; бывают стальные, тефлоновые, а также капиллярные колонки. Вблизи от ввода газа в колонку устанавливают устройство для ввода пробы. Чаще всего вводят пробу с помощью шприца, протыкая резиновую мембрану. Анализируемая смесь разделяется в колонке и поступает в детектор – прибор, преобразующий результаты разделения в форму, удобную для регистрации
Хроматографическая колонка – это «сердце» хроматографа, поскольку именно в ней происходит разделение смесей. Колонки чаще всего изготавливают из стекла; бывают стальные, тефлоновые, а также капиллярные колонки. Вблизи от ввода газа в колонку устанавливают устройство для ввода пробы. Чаще всего вводят пробу с помощью шприца, протыкая резиновую мембрану. Анализируемая смесь разделяется в колонке и поступает в детектор – прибор, преобразующий результаты разделения в форму, удобную для регистрации



 Прямой ввод пробы в капиллярную колонку невозможен - она будет перегружена. И потому за испарителем устанавливают "делитель", который отбирает часть испарившейся пробы и вводит эту часть в колонку, а остальное сбрасывает. Условия деления необходимо учитывать при последующей работе.
Прямой ввод пробы в капиллярную колонку невозможен - она будет перегружена. И потому за испарителем устанавливают "делитель", который отбирает часть испарившейся пробы и вводит эту часть в колонку, а остальное сбрасывает. Условия деления необходимо учитывать при последующей работе.





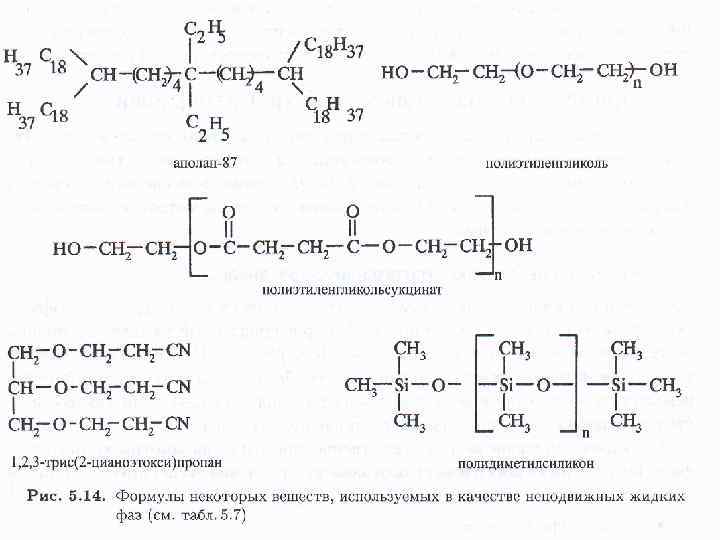
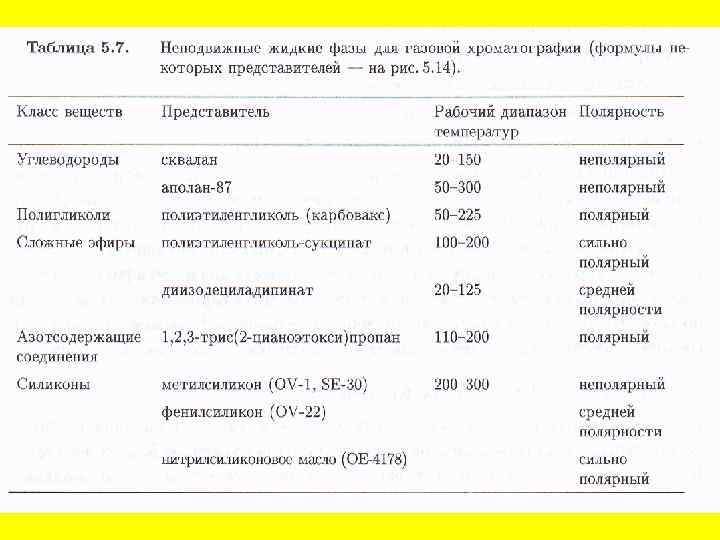

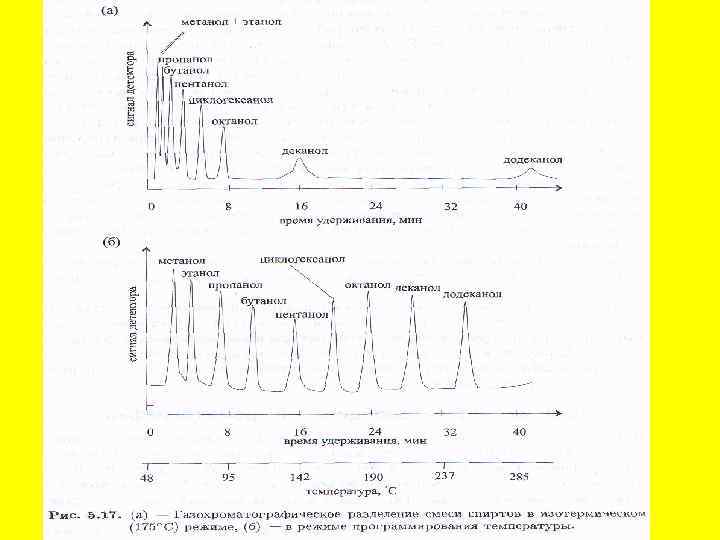
 Хроматографический анализ можно проводить в изотермическом режиме и с программированием температуры
Хроматографический анализ можно проводить в изотермическом режиме и с программированием температуры
 ДЕТЕКТОРЫ
ДЕТЕКТОРЫ
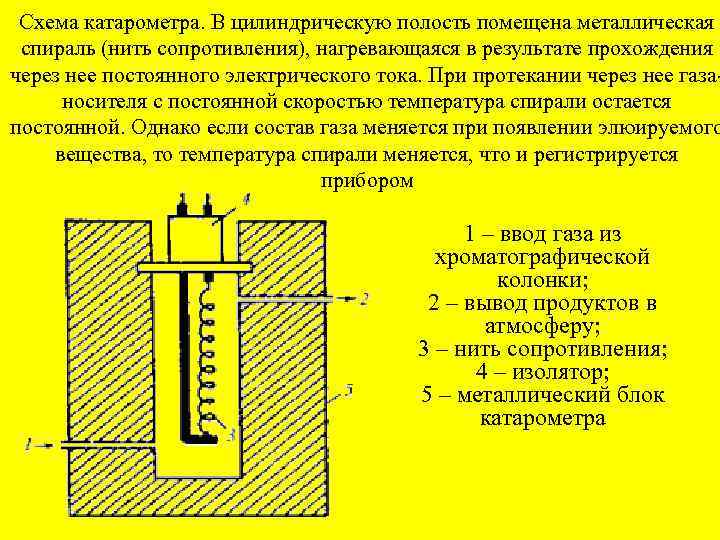 Схема катарометра. В цилиндрическую полость помещена металлическая спираль (нить сопротивления), нагревающаяся в результате прохождения через нее постоянного электрического тока. При протекании через нее газаносителя c постоянной скоростью температура спирали остается постоянной. Однако если состав газа меняется при появлении элюируемого вещества, то температура спирали меняется, что и регистрируется прибором 1 – ввод газа из хроматографической колонки; 2 – вывод продуктов в атмосферу; 3 – нить сопротивления; 4 – изолятор; 5 – металлический блок катарометра
Схема катарометра. В цилиндрическую полость помещена металлическая спираль (нить сопротивления), нагревающаяся в результате прохождения через нее постоянного электрического тока. При протекании через нее газаносителя c постоянной скоростью температура спирали остается постоянной. Однако если состав газа меняется при появлении элюируемого вещества, то температура спирали меняется, что и регистрируется прибором 1 – ввод газа из хроматографической колонки; 2 – вывод продуктов в атмосферу; 3 – нить сопротивления; 4 – изолятор; 5 – металлический блок катарометра
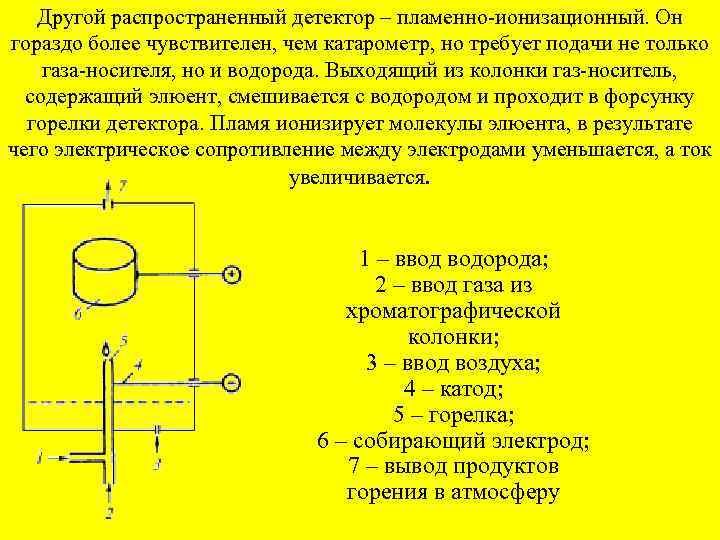 Другой распространенный детектор – пламенно-ионизационный. Он гораздо более чувствителен, чем катарометр, но требует подачи не только газа-носителя, но и водорода. Выходящий из колонки газ-носитель, содержащий элюент, смешивается с водородом и проходит в форсунку горелки детектора. Пламя ионизирует молекулы элюента, в результате чего электрическое сопротивление между электродами уменьшается, а ток увеличивается. 1 – ввод водорода; 2 – ввод газа из хроматографической колонки; 3 – ввод воздуха; 4 – катод; 5 – горелка; 6 – собирающий электрод; 7 – вывод продуктов горения в атмосферу
Другой распространенный детектор – пламенно-ионизационный. Он гораздо более чувствителен, чем катарометр, но требует подачи не только газа-носителя, но и водорода. Выходящий из колонки газ-носитель, содержащий элюент, смешивается с водородом и проходит в форсунку горелки детектора. Пламя ионизирует молекулы элюента, в результате чего электрическое сопротивление между электродами уменьшается, а ток увеличивается. 1 – ввод водорода; 2 – ввод газа из хроматографической колонки; 3 – ввод воздуха; 4 – катод; 5 – горелка; 6 – собирающий электрод; 7 – вывод продуктов горения в атмосферу
 Модификация ПИД-термоионный хроматографический детектор с источником ионов щелочного металла (напр. , К, Rb, Cs), поступающих в пламя. Характеризуется повыш. чувствительностью к фосфор-, азот- и галогенсодержащим соед. Пламенно-фотометрический детектор измеряет интенсивность излучения в-в в водородном пламени. Его можно рассматривать как вариант пламенно-эмиссионного фотометра. При сгорании в-в образующиеся атомы и простые молекулярные частицы возбуждаются, переходят в состояние с более высокой энергией и испускают определенное характеристич. излучение. Оптич. фильтры, используемые в детекторе, позволяют выделить линию, характерную для соед. определенного класса (напр. , для серосодержащих 394 нм, для фосфорсодержащих 526 нм). Излучение, соответствующее этой линии, усиливается фотоумножителем.
Модификация ПИД-термоионный хроматографический детектор с источником ионов щелочного металла (напр. , К, Rb, Cs), поступающих в пламя. Характеризуется повыш. чувствительностью к фосфор-, азот- и галогенсодержащим соед. Пламенно-фотометрический детектор измеряет интенсивность излучения в-в в водородном пламени. Его можно рассматривать как вариант пламенно-эмиссионного фотометра. При сгорании в-в образующиеся атомы и простые молекулярные частицы возбуждаются, переходят в состояние с более высокой энергией и испускают определенное характеристич. излучение. Оптич. фильтры, используемые в детекторе, позволяют выделить линию, характерную для соед. определенного класса (напр. , для серосодержащих 394 нм, для фосфорсодержащих 526 нм). Излучение, соответствующее этой линии, усиливается фотоумножителем.
 Электронозахватный детектор представляет собой камеру с двумя электродами, к-рые используют для измерения ионного тока, и радиоизотопным источником для ионизации газов. В качестве источника используют b-активные (напр. , 63 Ni) и a-активные (напр. , 239 Рu) излучатели, а в качестве газа-носителя N 2, H 2, Не. Под влиянием радиоактивного излучения газ ионизируется с образованием электронов. Если приложить к электродам камеры определенный потенциал, возникает заметный фоновый ток Молекулы анализируемых в-в, обладающие сродством к электрону, при поступлении в детектор захватывают электроны, в результате чего концентрация последних уменьшается, что приводит к пропорциональному снижению фонового тока. Электронозахватный детектор можно использовать также и для определения соед. , не способных к захвату электронов, после количеств. перевода их в производные, к-рые определяются этим детектором с высокой чувствительностью. При добавлении к газу-носителю "допингов" (напр. , NO), чувствительность электронозахватного детектора резко увеличивается по отношению к нек-рым соед. , к-рые обычно характеризуются миним. сигналом.
Электронозахватный детектор представляет собой камеру с двумя электродами, к-рые используют для измерения ионного тока, и радиоизотопным источником для ионизации газов. В качестве источника используют b-активные (напр. , 63 Ni) и a-активные (напр. , 239 Рu) излучатели, а в качестве газа-носителя N 2, H 2, Не. Под влиянием радиоактивного излучения газ ионизируется с образованием электронов. Если приложить к электродам камеры определенный потенциал, возникает заметный фоновый ток Молекулы анализируемых в-в, обладающие сродством к электрону, при поступлении в детектор захватывают электроны, в результате чего концентрация последних уменьшается, что приводит к пропорциональному снижению фонового тока. Электронозахватный детектор можно использовать также и для определения соед. , не способных к захвату электронов, после количеств. перевода их в производные, к-рые определяются этим детектором с высокой чувствительностью. При добавлении к газу-носителю "допингов" (напр. , NO), чувствительность электронозахватного детектора резко увеличивается по отношению к нек-рым соед. , к-рые обычно характеризуются миним. сигналом.
 В фотоионизационном детекторе источником ионизации служит УФ излучение, под действием к-рого анализируемое в-во ионизируется, образуя ион и электрон. При этом энергия фотона должна быть больше потенциала ионизации анализируемого в-ва. В результате проводимость газовой среды в детекторе резко увеличивается и возрастает пропорционально концентрации в-ва. Детектор состоит из источника излучения, примыкающего к ионизационной камере с двумя электродами, используемыми для измерения тока ионизации. Используя лампу с энергией излучения 11, 7 э. В, возможно анализировать соед. разл. классов, включая алифатич. углеводороды. Подбирая излучение с подходящей энергией, можно избирательно анализировать соед. , обладающие разл. потенциалами ионизации. Детектор относится к концентрационному недеструктивному типу, поэтому целесообразно использовать его при последоват. соединении с др. детекторами, напр. ПИД
В фотоионизационном детекторе источником ионизации служит УФ излучение, под действием к-рого анализируемое в-во ионизируется, образуя ион и электрон. При этом энергия фотона должна быть больше потенциала ионизации анализируемого в-ва. В результате проводимость газовой среды в детекторе резко увеличивается и возрастает пропорционально концентрации в-ва. Детектор состоит из источника излучения, примыкающего к ионизационной камере с двумя электродами, используемыми для измерения тока ионизации. Используя лампу с энергией излучения 11, 7 э. В, возможно анализировать соед. разл. классов, включая алифатич. углеводороды. Подбирая излучение с подходящей энергией, можно избирательно анализировать соед. , обладающие разл. потенциалами ионизации. Детектор относится к концентрационному недеструктивному типу, поэтому целесообразно использовать его при последоват. соединении с др. детекторами, напр. ПИД

 В качестве детектора используют ИК-спектрометр с Фурьепреобразованием, потому что он позволяет снять полный спектр, по которому можно провести идентификацию вещества очень быстро — за то время, в течение которого вещество находится в кювете.
В качестве детектора используют ИК-спектрометр с Фурьепреобразованием, потому что он позволяет снять полный спектр, по которому можно провести идентификацию вещества очень быстро — за то время, в течение которого вещество находится в кювете.
 Однако самым совершенным детектором является масс-спектрометр, с которым мы познакомимся на следующей лекции А теперь о применении хроматографии
Однако самым совершенным детектором является масс-спектрометр, с которым мы познакомимся на следующей лекции А теперь о применении хроматографии
 Хроматографические методы незаменимы в контроле качества пищевых продуктов. Пищевую ценность продуктов определяют, анализируя аминокислотный состав белков, изомерный состав жирных кислот и глицеридов в жирах, углеводы, органические кислоты и витамины. В последние годы многие из этих анализов выполняются с помощью высокоэффективной жидкостной хроматографии. Для оценки безопасности продуктов в них выявляют пищевые добавки (консерванты, антиоксиданты, подслащивающие вещества, красители и др. ), определяют свежесть продуктов, устанавливают ранние стадии порчи и допустимые сроки хранения.
Хроматографические методы незаменимы в контроле качества пищевых продуктов. Пищевую ценность продуктов определяют, анализируя аминокислотный состав белков, изомерный состав жирных кислот и глицеридов в жирах, углеводы, органические кислоты и витамины. В последние годы многие из этих анализов выполняются с помощью высокоэффективной жидкостной хроматографии. Для оценки безопасности продуктов в них выявляют пищевые добавки (консерванты, антиоксиданты, подслащивающие вещества, красители и др. ), определяют свежесть продуктов, устанавливают ранние стадии порчи и допустимые сроки хранения.
 В природных жирах преобладают цис-изомеры жирных кислот. Недавно обнаружено, что транс-изомеры повышают содержание липопротеинов низкой плотности и уменьшают концентрацию липопротеинов высокой плотности в крови, что может способствовать развитию атеросклероза. Разработка методики газохроматографического разделения и анализа всех изомеров жирных кислот заставила производителей в несколько раз снизить содержание транс-изомеров ненасыщенных кислот в маргарине. Методом газовой хроматографии в некоторых сырах выявлено много нежелательных физиологически активных биогенных аминов, и эти сорта сыра были запрещены. В Японии в пищевых продуктах используется L-триптофан, полученный с помощью генной инженерии и биотехнологии. И когда у тысяч людей обнаружили неизвестное ранее заболевание и десятки заболевших умерли, хроматографическими методами было установлено, что эти трагические последствия вызваны наличием токсичных загрязнений в триптофане (выявлено 60 примесей). Газохроматографическому анализу подвергаются вина, коньяки и другая спиртосодержащая продукция. В 1997 г. в России вышел ГОСТ по определению методом газовой хроматографии микропримесей в водке и пищевом этиловом спирте.
В природных жирах преобладают цис-изомеры жирных кислот. Недавно обнаружено, что транс-изомеры повышают содержание липопротеинов низкой плотности и уменьшают концентрацию липопротеинов высокой плотности в крови, что может способствовать развитию атеросклероза. Разработка методики газохроматографического разделения и анализа всех изомеров жирных кислот заставила производителей в несколько раз снизить содержание транс-изомеров ненасыщенных кислот в маргарине. Методом газовой хроматографии в некоторых сырах выявлено много нежелательных физиологически активных биогенных аминов, и эти сорта сыра были запрещены. В Японии в пищевых продуктах используется L-триптофан, полученный с помощью генной инженерии и биотехнологии. И когда у тысяч людей обнаружили неизвестное ранее заболевание и десятки заболевших умерли, хроматографическими методами было установлено, что эти трагические последствия вызваны наличием токсичных загрязнений в триптофане (выявлено 60 примесей). Газохроматографическому анализу подвергаются вина, коньяки и другая спиртосодержащая продукция. В 1997 г. в России вышел ГОСТ по определению методом газовой хроматографии микропримесей в водке и пищевом этиловом спирте.


