Химия хром.ppt
- Количество слайдов: 27

Химия элементов. Лекция 11 Общая характеристика элементов VIБ-группы. Хром 900 igr. net
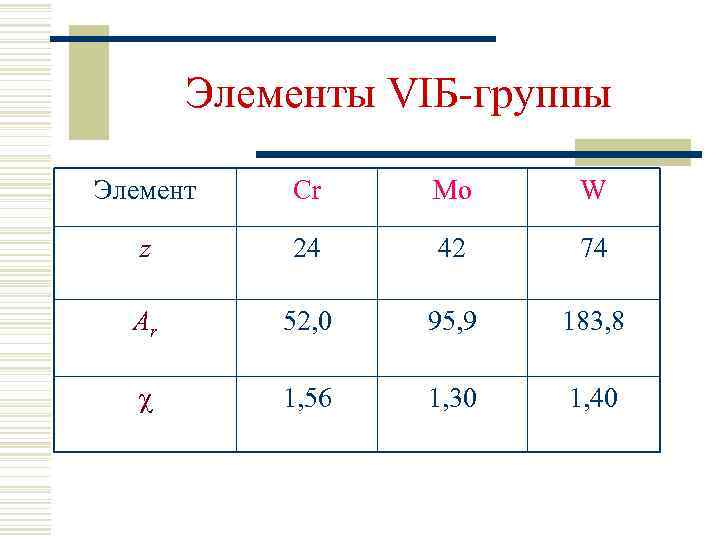
Элементы VIБ-группы Элемент Cr Mo W z 24 42 74 Ar 52, 0 95, 9 183, 8 1, 56 1, 30 1, 40
![w Cr: […] 4 s 1 3 d 5 4 p 0 Электронное строение w Cr: […] 4 s 1 3 d 5 4 p 0 Электронное строение](https://present5.com/presentation/96159131_161404597/image-3.jpg)
w Cr: […] 4 s 1 3 d 5 4 p 0 Электронное строение w Mo: […] 5 s 1 4 d 55 p 0 w W: […] 6 s 2 4 f 145 d 46 p 0 Cr, Mo: np 0 ns 1 (n– 1)d 5 Валентность (КЧ): Cr 6; Mo 6, 8; W 6, 8, 9; Ст. окисления: 0, +III, +IV, +VI (Cr); 0, +IV, +VI (Mo, W)

Простые вещества т. пл. , С т. кип. , С , г/см 3 Cr Mo W 1890 2680 2620 4630 3387 5680 7, 1 10, 2 19, 4 Вольфрам Хром Молибден

Простые вещества Cr , В Mo W – 0, 70 для 0, 00 для – 0, 09 для (Cr 3+/Сr) (Mo. O 3/Mo) (WO 3/W) – 0, 85 для (Cr 2+/Сr) Cr + 2 H 3 O+ + 4 H 2 O = [Cr(H 2 O)6]2+ + H 2 Mo(W) + H 3 O+

Простые вещества w. Кислоты-окислители (пассивация на холоду): ЭVIБ + HNO 3(конц), H 2 SO 4(конц) w. Э (Mo, W) + 2 HNO 3 + 8 HF = = Н 2[ЭVIF 8] + 2 NO + 4 H 2 O Э + 8 HF – 6 e– = [ЭF 8]2– + 2 H+ NO 3 – + 4 H+ + 3 e– = NO + 2 H 2 O w. Э (Cr, Mo, W) + 3 Na. NO 3 + 2 Na. OH = = Na 2 ЭVIO 4 + 3 Na. NO 2 + H 2 O w. Cr + Na. OH (р)

Металлы Хром электролитический Вольфрам проволока Вольфрам монокристалл Молибден прессованный и молибденовая проволока

w + II: Cr. O – черн. , т. разл. 700 C (до Cr 2 O 3 и Cr); Cr(OH)2 – желт. (основный) w +III: Cr 2 O 3 – зел. уст. ; Cr(OH)3 – серо-гол. ; Cr. O(OH) – зел. (амфотерн. ) w+IV: Cr. O 2 черн. , т. разл. 450 C (до Cr 2 O 3 и O 2) w+VI: Cr. O 3 – красн. , т. разл. 220 C (до Cr 2 O 3 и O 2); H 2 Cr. O 4 и H 2 Cr 2 O 7 (желт. и оранж. р-р, до 75% масс. ) Усиление кислотных свойств Кислородные соединения Cr Mo, W w + II: — w +IV: Mo. O 2 – кор. -фиол. , т. разл. 1800 C (до Mo. O 3 и Mo); Mo. O(OH)2; WO 2 – т. -кор. w +VI: Mo. O 3 – бесцв. , уст. ; WO 3 – желт. , уст. ; Mo. O 3. 2 H 2 O – желт. , тв. ; WO 3. 2 H 2 O – желт. , тв.
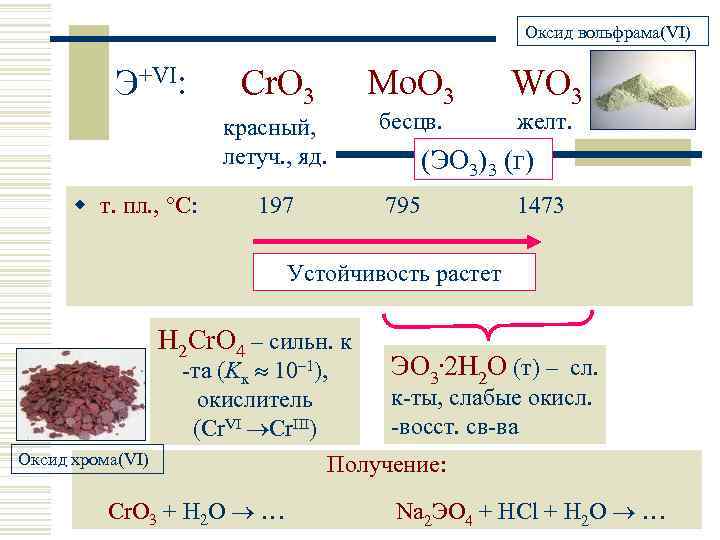
Оксид вольфрама(VI) Э+VI: Cr. O 3 Mo. O 3 WO 3 красный, летуч. , яд. w т. пл. , °С: 197 бесцв. желт. (ЭO 3)3 (г) 795 1473 Устойчивость растет H 2 Cr. O 4 – сильн. к -та (Kк 10– 1), окислитель (Cr. VI Cr. III) Оксид хрома(VI) Cr. O 3 + H 2 O … ЭО 3. 2 Н 2 О (т) – сл. к-ты, слабые окисл. -восст. св-ва Получение: Na 2 ЭO 4 + HCl + H 2 O …
![Комплексные соединения w Ст. ок. 0: [Э 0(CO)6] OC 0(CO) ] – w [Cr Комплексные соединения w Ст. ок. 0: [Э 0(CO)6] OC 0(CO) ] – w [Cr](https://present5.com/presentation/96159131_161404597/image-10.jpg)
Комплексные соединения w Ст. ок. 0: [Э 0(CO)6] OC 0(CO) ] – w [Cr 6 гексакарбонилхром: OC диамагнитный [Cr+ (CO– /6) | | = 0, 4 e– 6] CO CO Cr CO CO d 2 sp 3, октаэдр 1 Cr Cr : : CO 6 CO
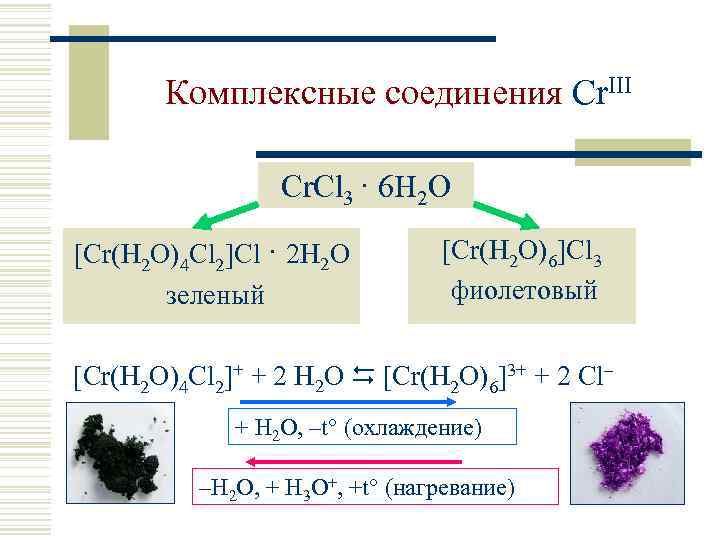
Комплексные соединения Cr. III Cr. Cl 3 · 6 H 2 O [Cr(H 2 O)4 Cl 2]Cl · 2 H 2 O зеленый [Cr(H 2 O)6]Cl 3 фиолетовый [Cr(H 2 O)4 Cl 2]+ + 2 H 2 O [Cr(H 2 O)6]3+ + 2 Cl– + H 2 O, –t° (охлаждение) –H 2 O, + H 3 O+, +t° (нагревание)

Изополисоединения (ст. ок. +VI) I. 2 Cr. O 42 + 2 H 3 O+ Cr 2 O 72 + 3 H 2 O; Kc. I 1014 II. 3 Cr 2 O 72 + 2 H 3 O+ 2 Cr 3 O 102 + 3 H 2 O …………. III. Cr 2 O 72 + 2 OH– 2 Cr. O 42 + H 2 O; Kc. III 1014 Равновесие хромат-ион – дихромат-ион в растворе (видеофрагмент)
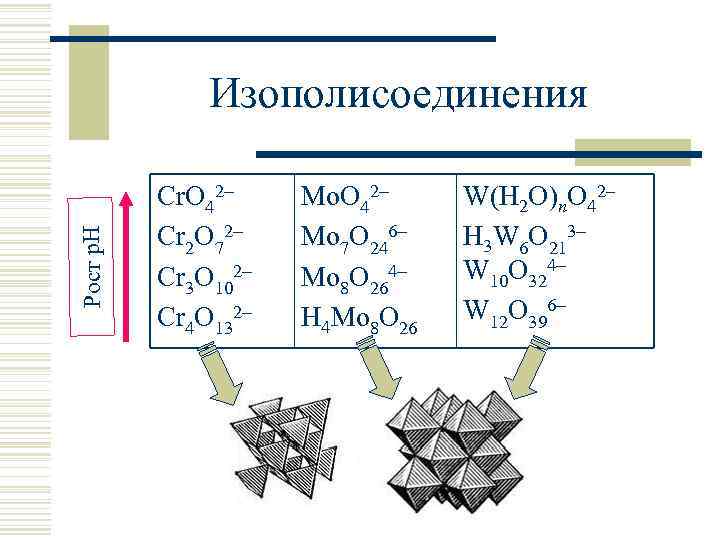
Рост р. Н Изополисоединения Cr. O 42 Cr 2 O 72 Cr 3 O 102 Cr 4 O 132 Mo. O 42 Mo 7 O 246 Mo 8 O 264 H 4 Mo 8 O 26 W(H 2 O)n. O 42– H 3 W 6 O 213 W 10 O 324 W 12 O 396
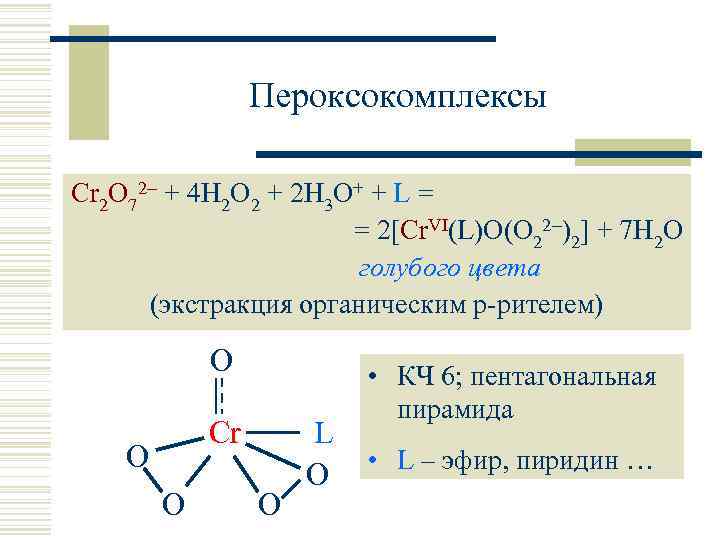
Пероксокомплексы Cr 2 O 72 + 4 H 2 O 2 + 2 H 3 O+ + L = = 2[Cr. VI(L)O(O 22 )2] + 7 H 2 O голубого цвета (экстракция органическим р-рителем) O Cr O O O L O • КЧ 6; пентагональная пирамида • L – эфир, пиридин …

Распространение в природе и важнейшие минералы Молибденит w 21. Cr 0, 019% масс. w 39. Mo 1· 10– 3% w 27. W 7· 10– 3% Редкие эл-ты • хромит (Cr 2 IIIFe. II)O 4 • крокоит Pb. Cr. O 4 • молибденит Mo. S 2 • вольфрамит (Mn, Fe)WO 4 • шеелит Ca. WO 4 Крокоит Вольфрамит Шеелит Хромит

Минералы Ферберит Рубины w гюбнерит Mn. WO 4 w повеллит Ca. Mo. O 4 w молибдошеелит Ca(W, Mo)O 4 w ферберит Fe. WO 4 Повеллит Гюбнерит Уваровит Хром входит в состав минералов: александрит, рубин, аквамарин, изумруд, уваровит Ca 3 Cr 2 III(Si. O 4)3 из семейства гранатов Аквамарин Александрит

Получение Хром w. Cr 2 O 3 + 2 Al = 2 Cr + Al 2 O 3 (t°) w(Cr 2 IIIFe. II)O 4 + 4 C = Fe + 2 Cr + 4 CO феррохром w. WO 3 + 3 H 2 = W + 3 H 2 O (t°) w. Mo. O 3 + 3 H 2 = Mo + 3 H 2 O (t°) Молибден листовой Вольфрам (порошок и прессованный)

Химия хрома. Cr(II) w Cr(OH)2 – основный гидроксид, восстановитель w Cr. II(OH)2(т) + O 2 Cr 2 IIIO 3 · n. H 2 O(т) w Cr(OH)2(т) + 2 H 3 O+ + 2 H 2 O = [Cr. II(H 2 O)6]2+ желтый (HCl. O 4) голубой w Cr. II(OH)2(т) + 2 HCl + 2 H 2 O = = [Cr. II(H 2 O)4 Cl 2](р)

Аквакатион хрома(II) w. Сильнейший восст-ль: (Cr 3+/Cr 2+) = – 0, 41 В w 4[Cr. II(H 2 O)6]2+ + O 2 + 4 H 3 O+ = = 4[Cr. III(H 2 O)6]3+ + 6 H 2 O w 2[Cr. II(H 2 O)4 Cl 2] + [Sn. IICl 3]– = = 2[Cr. III(H 2 O)4 Cl 2]+ + Sn 0 + 3 Cl– w. Стабилизация степени окисления +II: w 2[Cr. II(H 2 O)4 Cl 2] + 4 CH 3 COO– = = [Cr 2 II(H 2 O)2(CH 3 COO)4] + 4 Cl– + 6 H 2 O красного цвета, устойч.
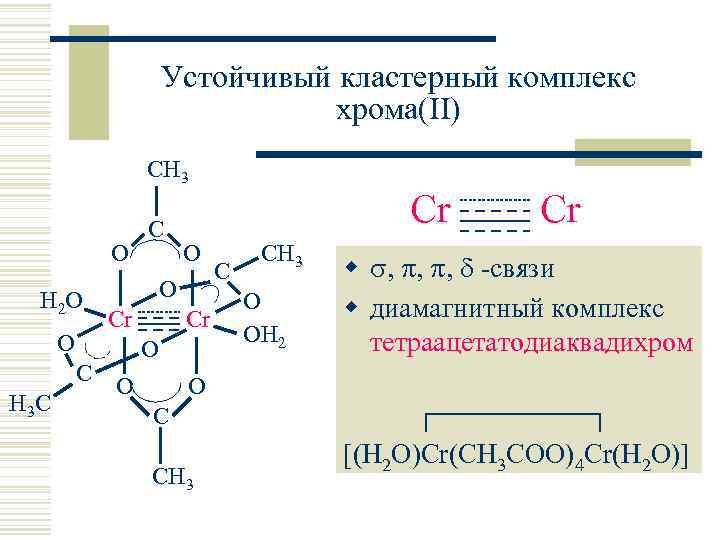
Устойчивый кластерный комплекс хрома(II) CH 3 O H 2 O O C H 3 C C Cr O O Cr Cr O O C CH 3 O OH 2 Cr w , -связи w диамагнитный комплекс тетраацетатодиаквадихром O C CH 3 [(H 2 O)Cr(CH 3 COO)4 Cr(H 2 O)]

Оксид хрома(III) Cr 2 O 3 w Cr 2 O 3 - пигмент (зелен. ), амфотерн. , уст. в ОВР Получение: w (NH 4)2 Cr 2 O 7 = Cr 2 O 3 + N 2 + 4 H 2 O w Cr 2 O 3 + H 2 O, H 3 O+, OH– Сплавление: w Cr 2 O 3 + 2 Na. OH = 2 Na. Cr. O 2 + H 2 O w Cr 2 O 3 + 3 Na 2 S 2 O 7 = Cr 2(SO 4)3 + 3 Na 2 SO 4
![[Cr(H 2 O)6]3+ + 3 NH 3·H 2 O Cr 2 O 3·n. H [Cr(H 2 O)6]3+ + 3 NH 3·H 2 O Cr 2 O 3·n. H](https://present5.com/presentation/96159131_161404597/image-22.jpg)
[Cr(H 2 O)6]3+ + 3 NH 3·H 2 O Cr 2 O 3·n. H 2 O(т) + … серо-зеленый гель H 3 O+ Cr(OH)3, Cr. O(OH) – зелен. крист. OH– [Cr(H 2 O)6]3+ [Cr(OH)6]3– d 2 sp 3 – октаэдр. , парамагн. фиолет. (р. Н < 5) зелен. (р. Н > 11) w[Cr(H 2 O)6]3+ + H 2 O [Cr(H 2 O)5 OH]2+ + H 3 O+; KK = 1, 12 · 10– 4 w 2[Cr(H 2 O)5 OH]2+ [(H 2 O)5 Cr(OH)2 Cr(H 2 O)5]4+
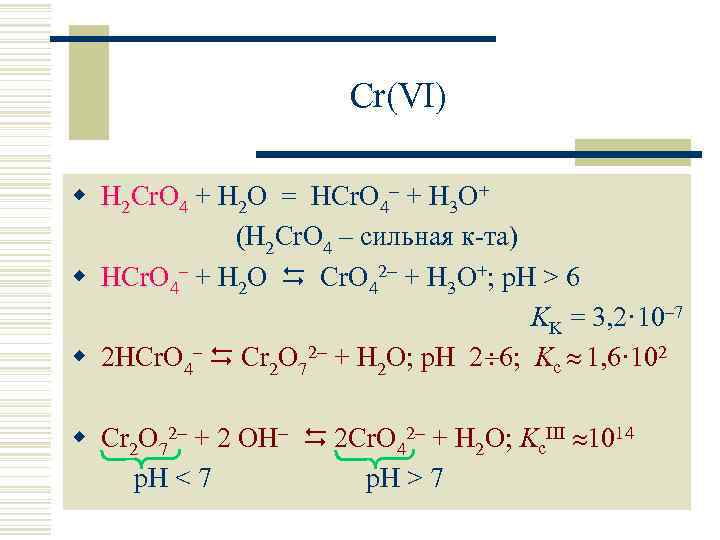
Cr(VI) w H 2 Cr. O 4 + H 2 O = HCr. O 4 + H 3 O+ (H 2 Cr. O 4 – сильная к-та) w HCr. O 4– + H 2 O Cr. O 42 + H 3 O+; p. H > 6 KK = 3, 2· 10– 7 w 2 HCr. O 4– Cr 2 O 72 + H 2 O; p. H 2 6; Kc 1, 6· 102 w Cr 2 O 72 + 2 OH 2 Cr. O 42 + H 2 O; Kc. III 1014 p. H < 7 p. H > 7

Окислительно-восстановительные свойства р. Н < 7: w Cr 2 O 72 + 14 H 3 O+ + 6 e = 2[Cr(H 2 O)6]3+ + 9 H 2 O; = +1, 33 В р. Н > 7: w Cr. O 42 + 4 H 2 O + 3 e = [Cr(OH)6]3 + 2 OH ; = – 0, 16 В Окислительные свойства сильнее выражены в кислотной среде K 2 Cr. O 4 K 2 Cr 2 O 7

Cr(VI) Cr(II) w K 2 Cr 2 O 7(т) + 14 HCl(конц. ) + H 2 O = = 2[Cr. III(H 2 O)4 Cl 2]Cl(р) + 3 Cl 2 + 2 KCl зеленый w Zn + 2 HCl = Zn. Cl 2 + H 2 w 2[Cr. III(H 2 O)4 Cl 2]Cl(р) + Zn = = 2[Cr. II(H 2 O)4 Cl 2](р) + Zn. Cl 2 голубого цвета

Разложение дихромата аммония w (NH 4)2 Cr 2 O 7 = Cr 2 O 3 + N 2 + 4 H 2 O «Дихроматный вулкан» (видеофрагмент)

Cr(VI) Оксид хрома(VI) w Cr. O 3(т) + 2 HCl(г) = Cr. Cl 2 O 2(ж) + H 2 O(г); +t° диоксид-дихлорид хрома (бинарное соединение) Получение: w K 2 Cr 2 O 7 + Na. Cl + H 2 SO 4(конц. ) Cr. Cl 2 O 2 + … w Гидролиз: Cr. Cl 2 O 2 + 2 H 2 O = H 2 Cr. O 4 + 2 HCl недост. H 2 O: H 2 Cr. O 4 изб. H 2 O, р. Н 2 6: 2 HCr. O 4–, Cr 2 O 72– w [Cr. O 3(OH)]– + Cl– + H 3 O+ [Cr. O 3 Cl]– + 2 H 2 O
Химия хром.ppt