Химия элементов Комплексные соединения. Основные понятия координационной теории.





![Простые и комплексные соединения HgI2 + 2KI = K2[HgI4] SO3(т) + K2O(т) = Простые и комплексные соединения HgI2 + 2KI = K2[HgI4] SO3(т) + K2O(т) =](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_4.jpg)
![Координационная теория (1893 г. ) Внутренняя и внешняя сфера комплексного соединения [MLx]Yz Комплексообразователь M± Координационная теория (1893 г. ) Внутренняя и внешняя сфера комплексного соединения [MLx]Yz Комплексообразователь M±](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_6.jpg)
![Внутренняя сфера [комплекс] Внешняя сфера (противоион) [Ni(NH3)6]Cl2 Внутренняя сфера [комплекс] Внешняя сфера (противоион) [Ni(NH3)6]Cl2](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_7.jpg)
![Комплексообразователь, лиганды, КЧ и дентатность. Примеры [NH4]Cl – КЧ 4, дент.1 [Al(H2O)6]Cl3 – КЧ Комплексообразователь, лиганды, КЧ и дентатность. Примеры [NH4]Cl – КЧ 4, дент.1 [Al(H2O)6]Cl3 – КЧ](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_8.jpg)

![2. Формулы и названия компл. соединений. [M(L+)(L0)(L–)]±,0 Число лигандов – греч. числит. 1 2. Формулы и названия компл. соединений. [M(L+)(L0)(L–)]±,0 Число лигандов – греч. числит. 1](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_12.jpg)
![3. Названия комплексных соединений А) Комплексы без внешней сферы [MLn] 3. Названия комплексных соединений А) Комплексы без внешней сферы [MLn]](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_13.jpg)
![Названия комплексных соединений Б) Комплексный катион [MLn]+X– «анион катиона»: Названия комплексных соединений Б) Комплексный катион [MLn]+X– «анион катиона»:](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_14.jpg)
![Названия комплексных соединений В) Комплексный анион X+[MLn]– «анион катиона»: Названия комплексных соединений В) Комплексный анион X+[MLn]– «анион катиона»:](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_15.jpg)
![Упражнения: Na3[AgI(SO3S)2] – бис(тиосульфато)аргентат(I) натрия [PtII(py)4]2[FeII(CN)6] – гексацианоферрат(II) тетрапиридинплатины(II) [K(H2O)6][Al(H2O)6](SO4)2 – Упражнения: Na3[AgI(SO3S)2] – бис(тиосульфато)аргентат(I) натрия [PtII(py)4]2[FeII(CN)6] – гексацианоферрат(II) тетрапиридинплатины(II) [K(H2O)6][Al(H2O)6](SO4)2 –](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_16.jpg)

![Геометрическая изомерия [ML5L]: изомеров нет цис- и транс-изомеры дигидроксотетраамминкобальта(II) Геометрическая изомерия [ML5L]: изомеров нет цис- и транс-изомеры дигидроксотетраамминкобальта(II)](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_21.jpg)
![Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O [Co(H2O)(en)2Cl]Cl2 Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O [Co(H2O)(en)2Cl]Cl2](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_24.jpg)
![Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 [Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4 Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 [Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_25.jpg)
![Комплексные соединения в растворах Неэлектролиты (слабые электролиты) [Pt(NH3)2Cl2] (ср. H2O2, CO(NH2)2 ) Сильные электролиты Комплексные соединения в растворах Неэлектролиты (слабые электролиты) [Pt(NH3)2Cl2] (ср. H2O2, CO(NH2)2 ) Сильные электролиты](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_26.jpg)
![[MLn] + H2O [MLn-1(H2O)] + L0 (n = КЧ) [MLn] + H2O [MLn-1(H2O)] + L0 (n = КЧ)](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_27.jpg)
![Сравнение устойчивости аммиачных комплексов Ступени комплексообразования [Cu(NH3)2]+ K2(обр) = 5,0·104 [Cu(NH3)]+ Сравнение устойчивости аммиачных комплексов Ступени комплексообразования [Cu(NH3)2]+ K2(обр) = 5,0·104 [Cu(NH3)]+](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_32.jpg)
![Хелат-эффект [Ni(NH3)6]2+ 6(обр)= 5,3 . 108 [Ni(en)3]2+ 3(обр)= 1,3 . 1019 [Ni(NH3)6]2+ + Хелат-эффект [Ni(NH3)6]2+ 6(обр)= 5,3 . 108 [Ni(en)3]2+ 3(обр)= 1,3 . 1019 [Ni(NH3)6]2+ +](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_33.jpg)




![Ni+II [Ni(CN)4]2– уст., диамагн., квадрат КЧ 4 [Ni(CN)5]3– уст., диамагн., квадратная пирамида КЧ Ni+II [Ni(CN)4]2– уст., диамагн., квадрат КЧ 4 [Ni(CN)5]3– уст., диамагн., квадратная пирамида КЧ](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_38.jpg)
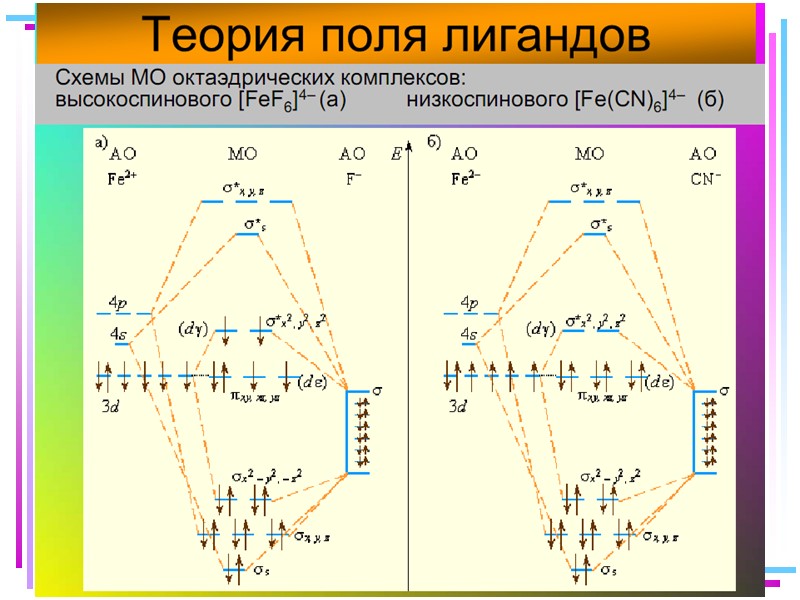
![Fe+II [FeF6]4– уст., парамагн., октаэдр КЧ 6 Fe+II [Fe(CN)6]4– уст., Fe+II [FeF6]4– уст., парамагн., октаэдр КЧ 6 Fe+II [Fe(CN)6]4– уст.,](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_39.jpg)

![В случае [ML6]±,0 : октаэдрическое поле лигандов Поле слабо влияет (энергия падает) в случае В случае [ML6]±,0 : октаэдрическое поле лигандов Поле слабо влияет (энергия падает) в случае](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_41.jpg)

![Типы комплексных соединений. 1. Аквакомплексы В водных растворах: [Be(H2O)4]2+ [Al(H2O)6]3+ Типы комплексных соединений. 1. Аквакомплексы В водных растворах: [Be(H2O)4]2+ [Al(H2O)6]3+](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_49.jpg)
![Аквакомплексы Термич. разложение: CuSO4·5H2O CuSO4·4H2O + H2O(г) CuSO4 + 4H2O(г) [Cu(H2O)4]SO4·H2O Аквакомплексы Термич. разложение: CuSO4·5H2O CuSO4·4H2O + H2O(г) CuSO4 + 4H2O(г) [Cu(H2O)4]SO4·H2O](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_50.jpg)
![Аквакомплексы [Fe(H2O)6]SO4·H2O («железный купорос») Аквакомплексы [Fe(H2O)6]SO4·H2O («железный купорос»)](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_51.jpg)
![2. Гидроксокомплексы Получение: Zn(OH)2 + 2OH–(изб.) = [Zn(OH)4]2–; pH >> 7 Разрушение: 2. Гидроксокомплексы Получение: Zn(OH)2 + 2OH–(изб.) = [Zn(OH)4]2–; pH >> 7 Разрушение:](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_52.jpg)
![3. Аммины (аммиакаты) Получение: AgCl(т) + 2NH3·H2O(изб.) = [Ag(NH3)2]+ +Cl– + 2H2O Разрушение: 3. Аммины (аммиакаты) Получение: AgCl(т) + 2NH3·H2O(изб.) = [Ag(NH3)2]+ +Cl– + 2H2O Разрушение:](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_53.jpg)
![Получение: HgI2(т) + 2I–(изб.) = [HgI4]2– [Fe(H2O)6]3+ + 6NCS−=[Fe(NCS)6]3− + 6H2O Разрушение: Получение: HgI2(т) + 2I–(изб.) = [HgI4]2– [Fe(H2O)6]3+ + 6NCS−=[Fe(NCS)6]3− + 6H2O Разрушение:](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_54.jpg)
![6. Анионгалогенаты M[ЭГ¢mГ²n] (Э, Г¢ и Г² – галогены) Получение: KI + 6. Анионгалогенаты M[ЭГ¢mГ²n] (Э, Г¢ и Г² – галогены) Получение: KI +](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_55.jpg)
![Получение: 4 NaH + B(OCH3)3 = Na[BH4] + 3CH3ONa (при 250 °C) 4 Получение: 4 NaH + B(OCH3)3 = Na[BH4] + 3CH3ONa (при 250 °C) 4](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_56.jpg)
 (ниже 50 °С) тетракарбонилникель(0) Получение: Ni(т) + 4CO(г) = [Ni(CO)4](ж) (ниже 50 °С) тетракарбонилникель(0)](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_57.jpg)

![Правило Сиджвика (примеры) * 27Co0 [Ar]3d74s2 || 36Kr * 18 – 9 = 9e Правило Сиджвика (примеры) * 27Co0 [Ar]3d74s2 || 36Kr * 18 – 9 = 9e](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_59.jpg)

 + Реакция Чугаева Ni2+ + 2 NH3·H2O + 2H2L = = [Ni(HL)2](т) +](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_62.jpg)
![Решение задач. 2. Реакция обмена лигандов [Co(NH3)6]3+ + 6 CN– [Co(CN)6]3– + Решение задач. 2. Реакция обмена лигандов [Co(NH3)6]3+ + 6 CN– [Co(CN)6]3– +](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_66.jpg)
![Решение задач. 3. Разрушение комплекса [Cu(NH3)4]2+ + 4 H3O+ [Cu(H2O)4]2+ + 4 Решение задач. 3. Разрушение комплекса [Cu(NH3)4]2+ + 4 H3O+ [Cu(H2O)4]2+ + 4](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_67.jpg)
![Решение задач. 4. Направление реакции CuCN(т) + H2O + HCN [Cu(CN)2]– + Решение задач. 4. Направление реакции CuCN(т) + H2O + HCN [Cu(CN)2]– +](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_68.jpg)























145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt
- Количество слайдов: 131
 Химия элементов Комплексные соединения. Основные понятия координационной теории. Номенклатура. Поведение в растворе
Химия элементов Комплексные соединения. Основные понятия координационной теории. Номенклатура. Поведение в растворе



![>Простые и комплексные соединения HgI2 + 2KI = K2[HgI4] SO3(т) + K2O(т) = >Простые и комплексные соединения HgI2 + 2KI = K2[HgI4] SO3(т) + K2O(т) =](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_4.jpg) Простые и комплексные соединения HgI2 + 2KI = K2[HgI4] SO3(т) + K2O(т) = = K2SO4(т) HgI2(т) + 2K+(р) + 2I–(р)= = 2K+(р) + [HgI4]2–(р) K2O(т) + SO3(т) = = 2K+(р) + SO42–(р)
Простые и комплексные соединения HgI2 + 2KI = K2[HgI4] SO3(т) + K2O(т) = = K2SO4(т) HgI2(т) + 2K+(р) + 2I–(р)= = 2K+(р) + [HgI4]2–(р) K2O(т) + SO3(т) = = 2K+(р) + SO42–(р)
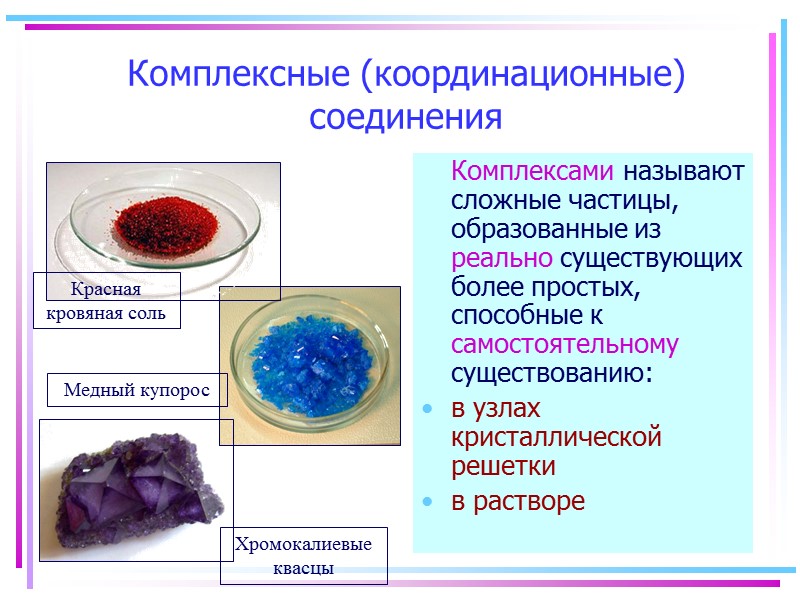
 Комплексные (координационные) соединения Комплексами называют сложные частицы, образованные из реально существующих более простых, способные к самостоятельному существованию: в узлах кристаллической решетки в растворе
Комплексные (координационные) соединения Комплексами называют сложные частицы, образованные из реально существующих более простых, способные к самостоятельному существованию: в узлах кристаллической решетки в растворе
![>Координационная теория (1893 г. ) Внутренняя и внешняя сфера комплексного соединения [MLx]Yz Комплексообразователь M± >Координационная теория (1893 г. ) Внутренняя и внешняя сфера комплексного соединения [MLx]Yz Комплексообразователь M±](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_6.jpg) Координационная теория (1893 г. ) Внутренняя и внешняя сфера комплексного соединения [MLx]Yz Комплексообразователь M± Лиганды L± Координационное число КЧ Дентатность лигандов Многоядерные комплексы (мостиковые, смешанные, кластеры)
Координационная теория (1893 г. ) Внутренняя и внешняя сфера комплексного соединения [MLx]Yz Комплексообразователь M± Лиганды L± Координационное число КЧ Дентатность лигандов Многоядерные комплексы (мостиковые, смешанные, кластеры)
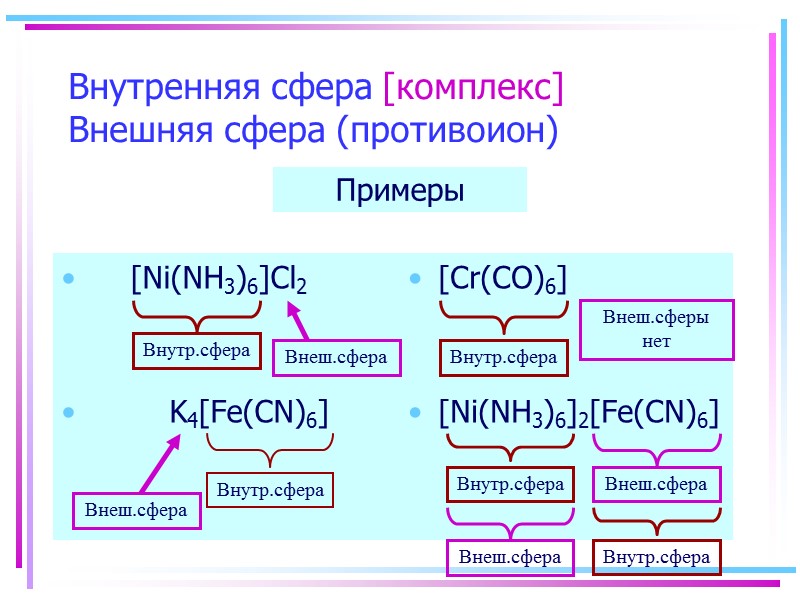
![>Внутренняя сфера [комплекс] Внешняя сфера (противоион) [Ni(NH3)6]Cl2 >Внутренняя сфера [комплекс] Внешняя сфера (противоион) [Ni(NH3)6]Cl2](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_7.jpg) Внутренняя сфера [комплекс] Внешняя сфера (противоион) [Ni(NH3)6]Cl2 K4[Fe(CN)6] [Cr(CO)6] [Ni(NH3)6]2[Fe(CN)6] Примеры Внеш.сферы нет
Внутренняя сфера [комплекс] Внешняя сфера (противоион) [Ni(NH3)6]Cl2 K4[Fe(CN)6] [Cr(CO)6] [Ni(NH3)6]2[Fe(CN)6] Примеры Внеш.сферы нет
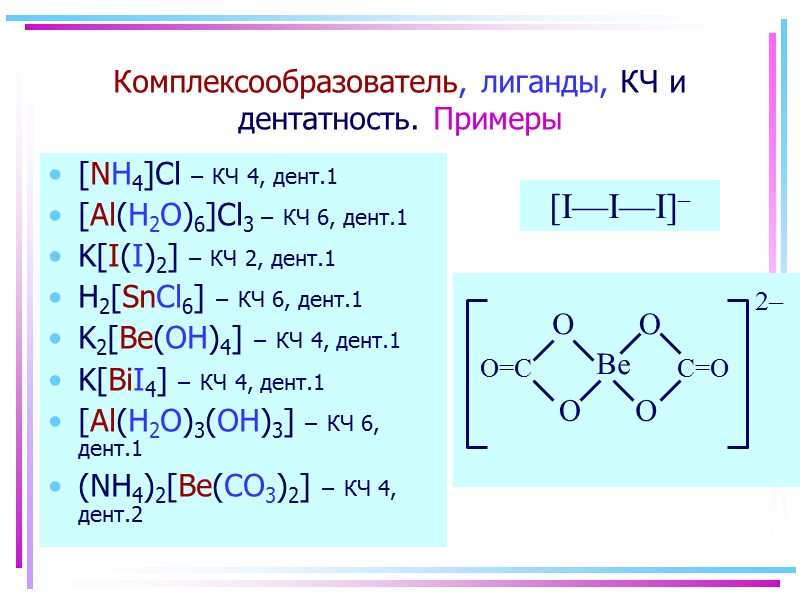
![>Комплексообразователь, лиганды, КЧ и дентатность. Примеры [NH4]Cl – КЧ 4, дент.1 [Al(H2O)6]Cl3 – КЧ >Комплексообразователь, лиганды, КЧ и дентатность. Примеры [NH4]Cl – КЧ 4, дент.1 [Al(H2O)6]Cl3 – КЧ](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_8.jpg) Комплексообразователь, лиганды, КЧ и дентатность. Примеры [NH4]Cl – КЧ 4, дент.1 [Al(H2O)6]Cl3 – КЧ 6, дент.1 K[I(I)2] – КЧ 2, дент.1 H2[SnCl6] – КЧ 6, дент.1 K2[Be(OH)4] – КЧ 4, дент.1 K[BiI4] – КЧ 4, дент.1 [Al(H2O)3(OH)3] – КЧ 6, дент.1 (NH4)2[Be(CO3)2] – КЧ 4, дент.2 [I—I—I]–
Комплексообразователь, лиганды, КЧ и дентатность. Примеры [NH4]Cl – КЧ 4, дент.1 [Al(H2O)6]Cl3 – КЧ 6, дент.1 K[I(I)2] – КЧ 2, дент.1 H2[SnCl6] – КЧ 6, дент.1 K2[Be(OH)4] – КЧ 4, дент.1 K[BiI4] – КЧ 4, дент.1 [Al(H2O)3(OH)3] – КЧ 6, дент.1 (NH4)2[Be(CO3)2] – КЧ 4, дент.2 [I—I—I]–
 Полидентатные лиганды
Полидентатные лиганды
 Многоядерные комплексы КЧ 4, дент. 1 и 2 Мостиковый Кластер Смешанный тип КЧ 6, дент. 1 и 2
Многоядерные комплексы КЧ 4, дент. 1 и 2 Мостиковый Кластер Смешанный тип КЧ 6, дент. 1 и 2
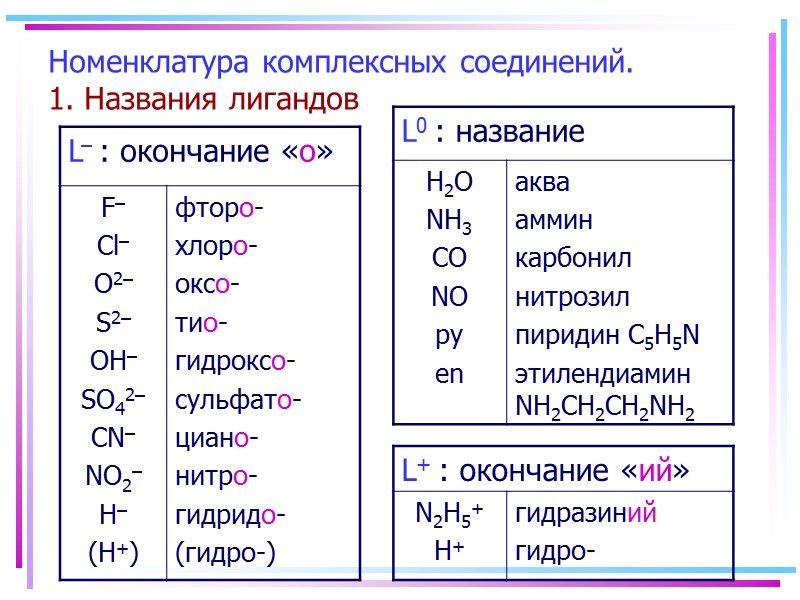
 Номенклатура комплексных соединений. 1. Названия лигандов
Номенклатура комплексных соединений. 1. Названия лигандов
![>2. Формулы и названия компл. соединений. [M(L+)(L0)(L–)]±,0 Число лигандов – греч. числит. 1 >2. Формулы и названия компл. соединений. [M(L+)(L0)(L–)]±,0 Число лигандов – греч. числит. 1](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_12.jpg) 2. Формулы и названия компл. соединений. [M(L+)(L0)(L–)]±,0 Число лигандов – греч. числит. 1 – (моно) 2 – ди 3 – три 4 – тетра 5 – пента 6 – гекса 7 – гепта … Число сложных лигандов: бис-, трис-, тетракис-, пентакис- … [M(en)4] - тетракис(этилендиамин)… [M(SO42-)2] бис(сульфато-)… Название комплекса: число лигандов каждого типа название лигандов название комплексообр. в нужной форме
2. Формулы и названия компл. соединений. [M(L+)(L0)(L–)]±,0 Число лигандов – греч. числит. 1 – (моно) 2 – ди 3 – три 4 – тетра 5 – пента 6 – гекса 7 – гепта … Число сложных лигандов: бис-, трис-, тетракис-, пентакис- … [M(en)4] - тетракис(этилендиамин)… [M(SO42-)2] бис(сульфато-)… Название комплекса: число лигандов каждого типа название лигандов название комплексообр. в нужной форме
![>3. Названия комплексных соединений А) Комплексы без внешней сферы [MLn] >3. Названия комплексных соединений А) Комплексы без внешней сферы [MLn]](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_13.jpg) 3. Названия комплексных соединений А) Комплексы без внешней сферы [MLn] n L M (в одно слово) Примеры: [Ni(CO)4] – тетракарбонилникель; [Co2(CO)8] – октакарбонилдикобальт; [Al2Cl6] – гексахлородиалюминий; [Co+III(NH3)3Cl3] – трихлоротриамминкобальт(III) [Co+II(H2O)4(NO2)2] – динитротетрааквакобальт(II)
3. Названия комплексных соединений А) Комплексы без внешней сферы [MLn] n L M (в одно слово) Примеры: [Ni(CO)4] – тетракарбонилникель; [Co2(CO)8] – октакарбонилдикобальт; [Al2Cl6] – гексахлородиалюминий; [Co+III(NH3)3Cl3] – трихлоротриамминкобальт(III) [Co+II(H2O)4(NO2)2] – динитротетрааквакобальт(II)
![>Названия комплексных соединений Б) Комплексный катион [MLn]+X– «анион катиона»: >Названия комплексных соединений Б) Комплексный катион [MLn]+X– «анион катиона»:](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_14.jpg) Названия комплексных соединений Б) Комплексный катион [MLn]+X– «анион катиона»: n L M(ст.ок.) Примеры: [AgI(NH3)2]OH – гидроксид диамминсеребра(I); [CoIII(NH3)6](OH)2Cl – хлорид-дигидроксид гексаамминкобальта(III); [Cr2III(NH3)9(OH)2]Cl4 – хлорид дигидроксононаамминдихрома(III)
Названия комплексных соединений Б) Комплексный катион [MLn]+X– «анион катиона»: n L M(ст.ок.) Примеры: [AgI(NH3)2]OH – гидроксид диамминсеребра(I); [CoIII(NH3)6](OH)2Cl – хлорид-дигидроксид гексаамминкобальта(III); [Cr2III(NH3)9(OH)2]Cl4 – хлорид дигидроксононаамминдихрома(III)
![>Названия комплексных соединений В) Комплексный анион X+[MLn]– «анион катиона»: >Названия комплексных соединений В) Комплексный анион X+[MLn]– «анион катиона»:](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_15.jpg) Названия комплексных соединений В) Комплексный анион X+[MLn]– «анион катиона»: анион n L M(ст.ок.)-«ат» Ag – аргент- Au – аур- Cu – купр- Fe – ферр- Hg – меркур- Mn – манган- Ni – никкол- Pb – плюмб- Sb – стиб- Sn – станн- Примеры: [Fe(CN)6]3– – гексацианоферрат(III)-ион [Ag(CN)2]– – дицианоаргентат(I)-ион K2[HgI4] – тетраиодомеркурат(II) калия K2[PtCl6] – гексахлороплатинат(IV) калия
Названия комплексных соединений В) Комплексный анион X+[MLn]– «анион катиона»: анион n L M(ст.ок.)-«ат» Ag – аргент- Au – аур- Cu – купр- Fe – ферр- Hg – меркур- Mn – манган- Ni – никкол- Pb – плюмб- Sb – стиб- Sn – станн- Примеры: [Fe(CN)6]3– – гексацианоферрат(III)-ион [Ag(CN)2]– – дицианоаргентат(I)-ион K2[HgI4] – тетраиодомеркурат(II) калия K2[PtCl6] – гексахлороплатинат(IV) калия
![>Упражнения: Na3[AgI(SO3S)2] – бис(тиосульфато)аргентат(I) натрия [PtII(py)4]2[FeII(CN)6] – гексацианоферрат(II) тетрапиридинплатины(II) [K(H2O)6][Al(H2O)6](SO4)2 – >Упражнения: Na3[AgI(SO3S)2] – бис(тиосульфато)аргентат(I) натрия [PtII(py)4]2[FeII(CN)6] – гексацианоферрат(II) тетрапиридинплатины(II) [K(H2O)6][Al(H2O)6](SO4)2 –](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_16.jpg) Упражнения: Na3[AgI(SO3S)2] – бис(тиосульфато)аргентат(I) натрия [PtII(py)4]2[FeII(CN)6] – гексацианоферрат(II) тетрапиридинплатины(II) [K(H2O)6][Al(H2O)6](SO4)2 – сульфат гексаакваалюминия-гексааквакалия [(CO)5Mn-Mn(CO)5] – бис(пентакарбонилмарганец) [(H2O)4Al(OH)2Al(H2O)4](SO4)2 – сульфат ди(-гидроксо)бис(тетраакваалюминия)
Упражнения: Na3[AgI(SO3S)2] – бис(тиосульфато)аргентат(I) натрия [PtII(py)4]2[FeII(CN)6] – гексацианоферрат(II) тетрапиридинплатины(II) [K(H2O)6][Al(H2O)6](SO4)2 – сульфат гексаакваалюминия-гексааквакалия [(CO)5Mn-Mn(CO)5] – бис(пентакарбонилмарганец) [(H2O)4Al(OH)2Al(H2O)4](SO4)2 – сульфат ди(-гидроксо)бис(тетраакваалюминия)
 Изомерия комплексных соединений Изомерия – явление существования соединений, одинаковых по составу и мол. массе, но различающихся по строению и свойствам (изомеров). В случае комплексных соединений изомерия обусловлена: различием в строении и координации лигандов различием в строении внутренней координационной сферы различным распределением частиц между внутренней и внешней сферой.
Изомерия комплексных соединений Изомерия – явление существования соединений, одинаковых по составу и мол. массе, но различающихся по строению и свойствам (изомеров). В случае комплексных соединений изомерия обусловлена: различием в строении и координации лигандов различием в строении внутренней координационной сферы различным распределением частиц между внутренней и внешней сферой.
 Изомерия лигандов Связевая —NO2– и —ONO– нитро- нитрито- [Co(NH3)5NO2]2+ (желто-коричн.р-р) [Co(NH3)5ONO]2+ (розов.р-р) —NCS– и —SCN– тиоцианато-N тиоцианато-S [Cr(H2O)5(NCS)]2+ [Cr(H2O)5(SCN)]2+ Изомерия лигандов Лиганды сложного строения (напр., аминокислоты) образуют изомеры, координация которых ведет к получению комплексов с разными свойствами.
Изомерия лигандов Связевая —NO2– и —ONO– нитро- нитрито- [Co(NH3)5NO2]2+ (желто-коричн.р-р) [Co(NH3)5ONO]2+ (розов.р-р) —NCS– и —SCN– тиоцианато-N тиоцианато-S [Cr(H2O)5(NCS)]2+ [Cr(H2O)5(SCN)]2+ Изомерия лигандов Лиганды сложного строения (напр., аминокислоты) образуют изомеры, координация которых ведет к получению комплексов с разными свойствами.
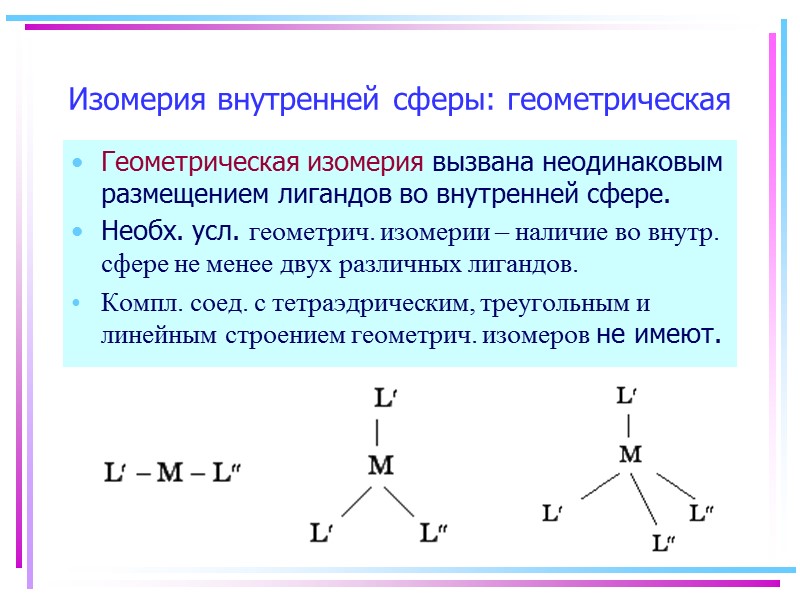
 Изомерия внутренней сферы: геометрическая Геометрическая изомерия вызвана неодинаковым размещением лигандов во внутренней сфере. Необх. усл. геометрич. изомерии – наличие во внутр. сфере не менее двух различных лигандов. Компл. соед. с тетраэдрическим, треугольным и линейным строением геометрич. изомеров не имеют.
Изомерия внутренней сферы: геометрическая Геометрическая изомерия вызвана неодинаковым размещением лигандов во внутренней сфере. Необх. усл. геометрич. изомерии – наличие во внутр. сфере не менее двух различных лигандов. Компл. соед. с тетраэдрическим, треугольным и линейным строением геометрич. изомеров не имеют.
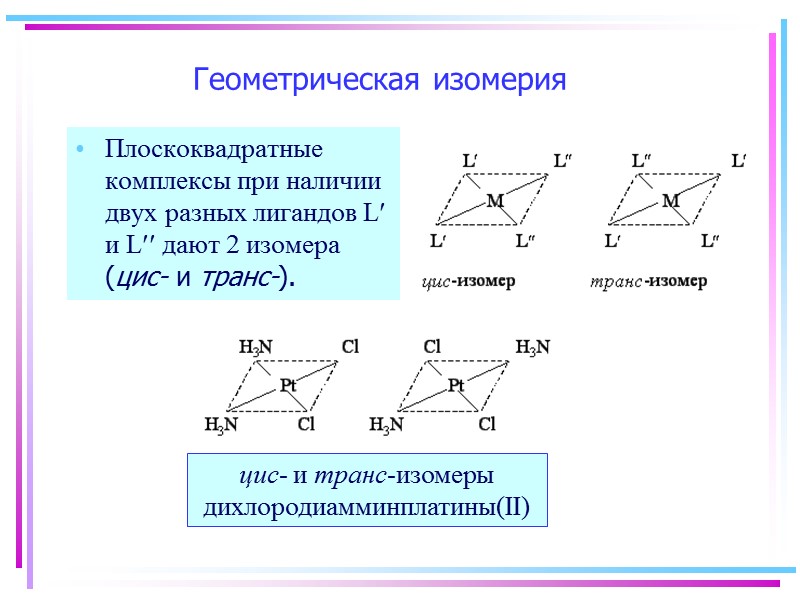
 Геометрическая изомерия Плоскоквадратные комплексы при наличии двух разных лигандов L и L дают 2 изомера (цис- и транс-).
Геометрическая изомерия Плоскоквадратные комплексы при наличии двух разных лигандов L и L дают 2 изомера (цис- и транс-).
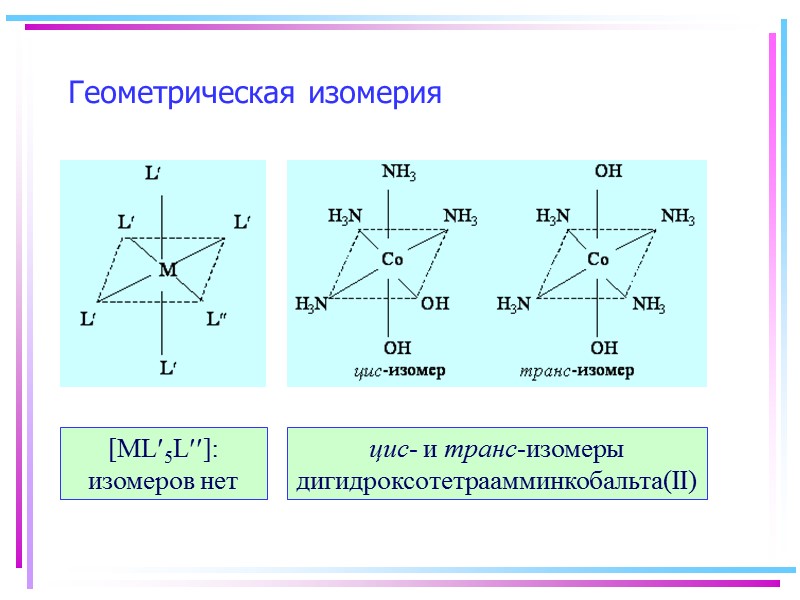
![>Геометрическая изомерия [ML5L]: изомеров нет цис- и транс-изомеры дигидроксотетраамминкобальта(II) >Геометрическая изомерия [ML5L]: изомеров нет цис- и транс-изомеры дигидроксотетраамминкобальта(II)](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_21.jpg) Геометрическая изомерия [ML5L]: изомеров нет цис- и транс-изомеры дигидроксотетраамминкобальта(II)
Геометрическая изомерия [ML5L]: изомеров нет цис- и транс-изомеры дигидроксотетраамминкобальта(II)
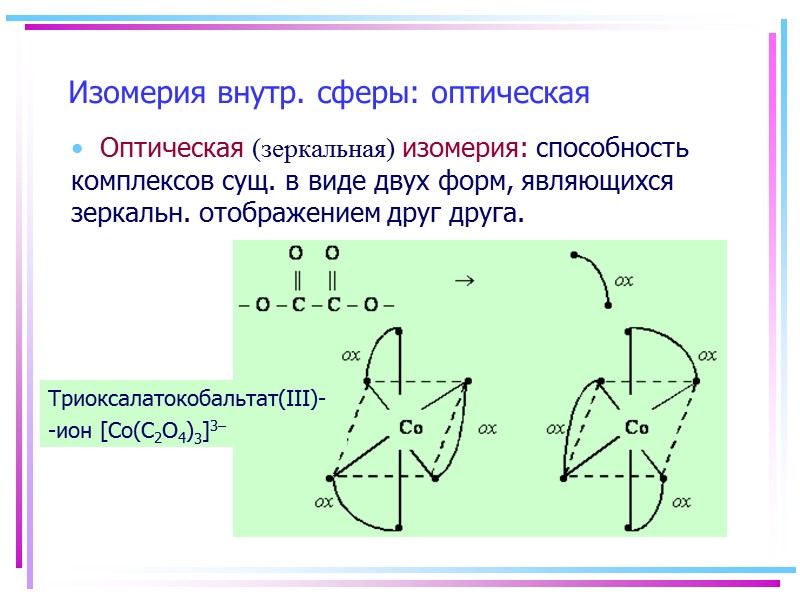
 Изомерия внутр. сферы: оптическая Оптическая (зеркальная) изомерия: способность комплексов сущ. в виде двух форм, являющихся зеркальн. отображением друг друга. Триоксалатокобальтат(III)- -ион [Co(С2O4)3]3–
Изомерия внутр. сферы: оптическая Оптическая (зеркальная) изомерия: способность комплексов сущ. в виде двух форм, являющихся зеркальн. отображением друг друга. Триоксалатокобальтат(III)- -ион [Co(С2O4)3]3–
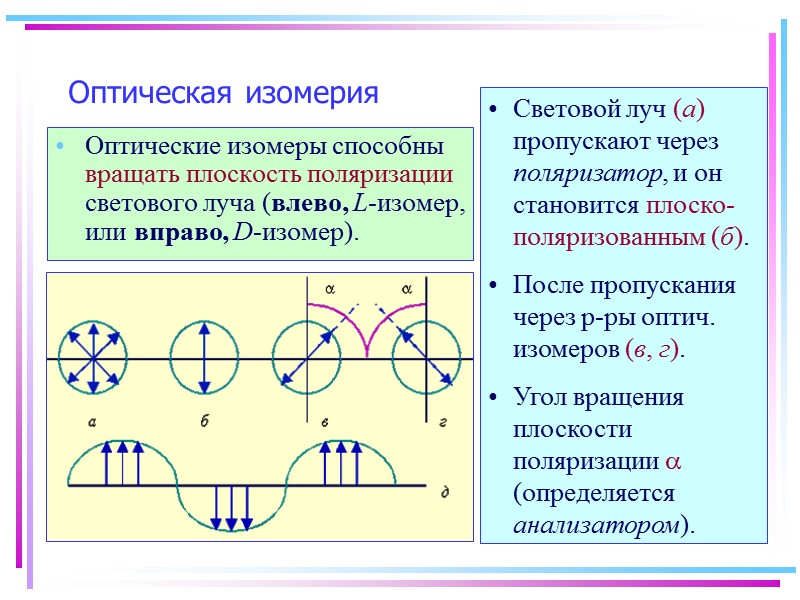
 Оптическая изомерия Оптические изомеры способны вращать плоскость поляризации светового луча (влево, L-изомер, или вправо, D-изомер). Световой луч (а) пропускают через поляризатор, и он становится плоско-поляризованным (б). После пропускания через р-ры оптич. изомеров (в, г). Угол вращения плоскости поляризации a (определяется анализатором).
Оптическая изомерия Оптические изомеры способны вращать плоскость поляризации светового луча (влево, L-изомер, или вправо, D-изомер). Световой луч (а) пропускают через поляризатор, и он становится плоско-поляризованным (б). После пропускания через р-ры оптич. изомеров (в, г). Угол вращения плоскости поляризации a (определяется анализатором).
![>Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O [Co(H2O)(en)2Cl]Cl2 >Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O [Co(H2O)(en)2Cl]Cl2](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_24.jpg) Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O [Co(H2O)(en)2Cl]Cl2 [Co(NH3)5I]SO4 [Co(NH3)5SO4]I 1 Cl–; H2O (AgCl) 2 Cl– (2 AgCl) SO42– (BaSO4) I– (AgI)
Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O [Co(H2O)(en)2Cl]Cl2 [Co(NH3)5I]SO4 [Co(NH3)5SO4]I 1 Cl–; H2O (AgCl) 2 Cl– (2 AgCl) SO42– (BaSO4) I– (AgI)
![>Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 [Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4 >Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 [Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_25.jpg) Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 [Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4 pH 7 pH 7 Координационные изомеры [Cr(NH3)4(NCS)2][Cr(NH3)2(NCS)4] [Cr(NH3)6][Cr(NCS)6]
Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 [Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4 pH 7 pH 7 Координационные изомеры [Cr(NH3)4(NCS)2][Cr(NH3)2(NCS)4] [Cr(NH3)6][Cr(NCS)6]
![>Комплексные соединения в растворах Неэлектролиты (слабые электролиты) [Pt(NH3)2Cl2] (ср. H2O2, CO(NH2)2 ) Сильные электролиты >Комплексные соединения в растворах Неэлектролиты (слабые электролиты) [Pt(NH3)2Cl2] (ср. H2O2, CO(NH2)2 ) Сильные электролиты](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_26.jpg) Комплексные соединения в растворах Неэлектролиты (слабые электролиты) [Pt(NH3)2Cl2] (ср. H2O2, CO(NH2)2 ) Сильные электролиты [Pt(NH3)4]Cl2 = [Pt(NH3)4]2+ + 2Cl– соль [Zn(NH3)4](OH)2 = [Zn(NH3)4]2+ + 2OH– с. осн. pH 7 H[BF4] + H2O = H3O+ + [BF4]– с. к-та pH 7 Акватация: [ … ] + H2O [ … ] + L
Комплексные соединения в растворах Неэлектролиты (слабые электролиты) [Pt(NH3)2Cl2] (ср. H2O2, CO(NH2)2 ) Сильные электролиты [Pt(NH3)4]Cl2 = [Pt(NH3)4]2+ + 2Cl– соль [Zn(NH3)4](OH)2 = [Zn(NH3)4]2+ + 2OH– с. осн. pH 7 H[BF4] + H2O = H3O+ + [BF4]– с. к-та pH 7 Акватация: [ … ] + H2O [ … ] + L
![>[MLn] + H2O [MLn-1(H2O)] + L0 (n = КЧ) >[MLn] + H2O [MLn-1(H2O)] + L0 (n = КЧ)](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_27.jpg) [MLn] + H2O [MLn-1(H2O)] + L0 (n = КЧ) [H2O] = Const, р-р разбавленный Ступенчатая диссоциация комплекса: [MLn] [ML(n-1)] + L [MLn-1] [ML(n-2)] + L … [ML2] [ML] + L [ML] M + L Суммарное уравнение диссоциации комплекса: [MLn] M + nL Реакции обмена лигандов
[MLn] + H2O [MLn-1(H2O)] + L0 (n = КЧ) [H2O] = Const, р-р разбавленный Ступенчатая диссоциация комплекса: [MLn] [ML(n-1)] + L [MLn-1] [ML(n-2)] + L … [ML2] [ML] + L [ML] M + L Суммарное уравнение диссоциации комплекса: [MLn] M + nL Реакции обмена лигандов
 Чем больше значение Ki(обр), тем сильнее смещено равновесие в сторону образования данного комплекса. … Ступенчатая константа образования комплекса
Чем больше значение Ki(обр), тем сильнее смещено равновесие в сторону образования данного комплекса. … Ступенчатая константа образования комплекса
 Полные (суммарные) константы образования Характеристика устойчивости комплексного соединения: чем больше значение bn(обр), тем более устойчив комплекс данного состава. ……
Полные (суммарные) константы образования Характеристика устойчивости комплексного соединения: чем больше значение bn(обр), тем более устойчив комплекс данного состава. ……
 Связь между полной и ступенчатой константами образования bn(обр) = K1(обр)·K2(обр)·K3(обр)·… ·Kn(обр)
Связь между полной и ступенчатой константами образования bn(обр) = K1(обр)·K2(обр)·K3(обр)·… ·Kn(обр)
 Сравнение констант образования и устойчивости комплексов
Сравнение констант образования и устойчивости комплексов
![>Сравнение устойчивости аммиачных комплексов Ступени комплексообразования [Cu(NH3)2]+ K2(обр) = 5,0·104 [Cu(NH3)]+ >Сравнение устойчивости аммиачных комплексов Ступени комплексообразования [Cu(NH3)2]+ K2(обр) = 5,0·104 [Cu(NH3)]+](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_32.jpg) Сравнение устойчивости аммиачных комплексов Ступени комплексообразования [Cu(NH3)2]+ K2(обр) = 5,0·104 [Cu(NH3)]+ K1(обр) = 1,4·106 Природа комплексообразователя [Cu(NH3)2]+ 2(обр) = 7,0·1010 [Ag(NH3)2]+ 2(обр) = 1,1·107 Комплекс Cu(I) устойчивее, чем комплекс Ag(I) Степень окисления комплексообразователя [CoII(NH3)6]2+ 6(обр) = 1,3·105 [CoIII(NH3)6]3+ 6(обр) = 3,2·1032 Комплекс Co(III) устойчивее, чем комплекс Co(II)
Сравнение устойчивости аммиачных комплексов Ступени комплексообразования [Cu(NH3)2]+ K2(обр) = 5,0·104 [Cu(NH3)]+ K1(обр) = 1,4·106 Природа комплексообразователя [Cu(NH3)2]+ 2(обр) = 7,0·1010 [Ag(NH3)2]+ 2(обр) = 1,1·107 Комплекс Cu(I) устойчивее, чем комплекс Ag(I) Степень окисления комплексообразователя [CoII(NH3)6]2+ 6(обр) = 1,3·105 [CoIII(NH3)6]3+ 6(обр) = 3,2·1032 Комплекс Co(III) устойчивее, чем комплекс Co(II)
![>Хелат-эффект [Ni(NH3)6]2+ 6(обр)= 5,3 . 108 [Ni(en)3]2+ 3(обр)= 1,3 . 1019 [Ni(NH3)6]2+ + >Хелат-эффект [Ni(NH3)6]2+ 6(обр)= 5,3 . 108 [Ni(en)3]2+ 3(обр)= 1,3 . 1019 [Ni(NH3)6]2+ +](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_33.jpg) Хелат-эффект [Ni(NH3)6]2+ 6(обр)= 5,3 . 108 [Ni(en)3]2+ 3(обр)= 1,3 . 1019 [Ni(NH3)6]2+ + 3 en + 6H2O = [Ni(en)3]2+ + 6 NH3·H2O
Хелат-эффект [Ni(NH3)6]2+ 6(обр)= 5,3 . 108 [Ni(en)3]2+ 3(обр)= 1,3 . 1019 [Ni(NH3)6]2+ + 3 en + 6H2O = [Ni(en)3]2+ + 6 NH3·H2O
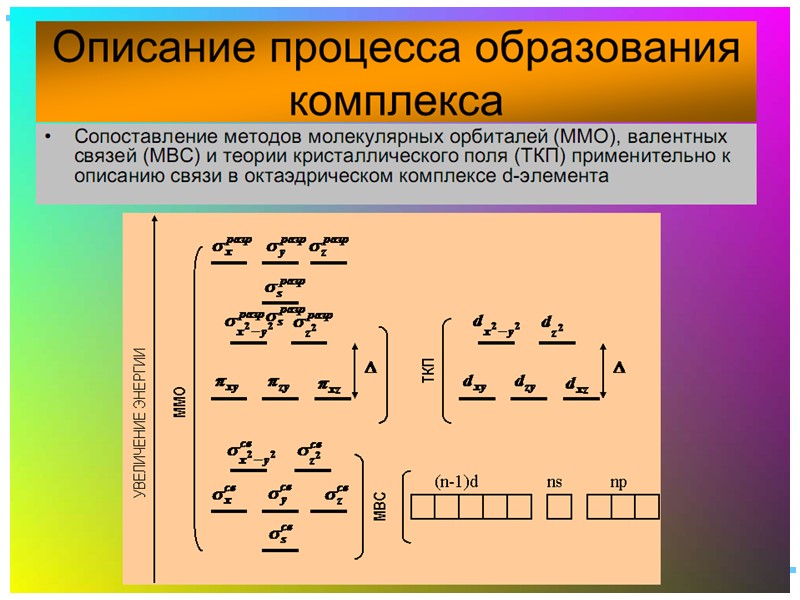
 Квантовомеханические теории строения комплексных соединений Для объяснения строения комплексных соединений наиболее широко применяются теория валентных связей (метод валентных связей) и теория кристаллического поля. В рамках метода валентных связей считается, что между комплексообразователем и лигандами существует чисто ковалентная связь, которая реализуется по донорно-акцепторному механизму.
Квантовомеханические теории строения комплексных соединений Для объяснения строения комплексных соединений наиболее широко применяются теория валентных связей (метод валентных связей) и теория кристаллического поля. В рамках метода валентных связей считается, что между комплексообразователем и лигандами существует чисто ковалентная связь, которая реализуется по донорно-акцепторному механизму.
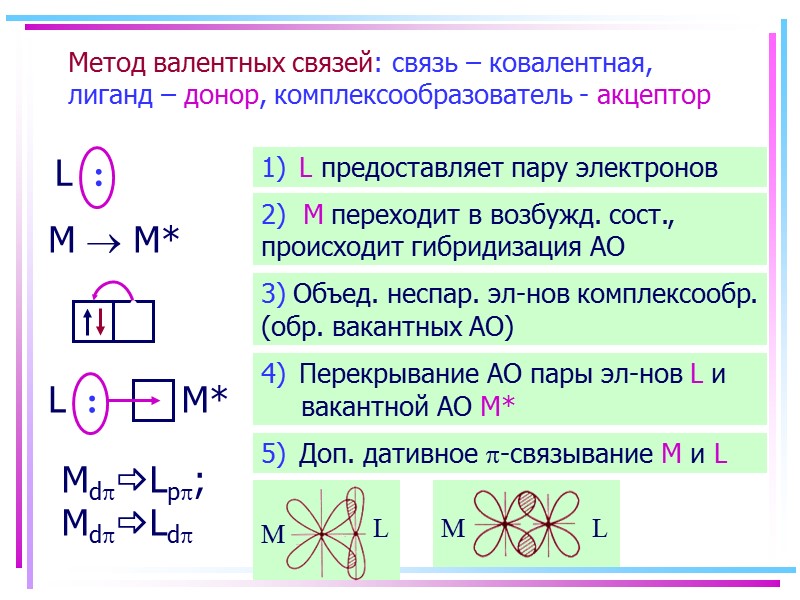
 Метод валентных связей: связь – ковалентная, лиганд – донор, комплексообразователь - акцептор L : M M* L : MdLp; MdLd 1) L предоставляет пару электронов 2) M переходит в возбужд. сост., происходит гибридизация АО 3) Объед. неспар. эл-нов комплексообр. (обр. вакантных АО) 4) Перекрывание АО пары эл-нов L и вакантной АО M* 5) Доп. дативное -связывание M и L
Метод валентных связей: связь – ковалентная, лиганд – донор, комплексообразователь - акцептор L : M M* L : MdLp; MdLd 1) L предоставляет пару электронов 2) M переходит в возбужд. сост., происходит гибридизация АО 3) Объед. неспар. эл-нов комплексообр. (обр. вакантных АО) 4) Перекрывание АО пары эл-нов L и вакантной АО M* 5) Доп. дативное -связывание M и L
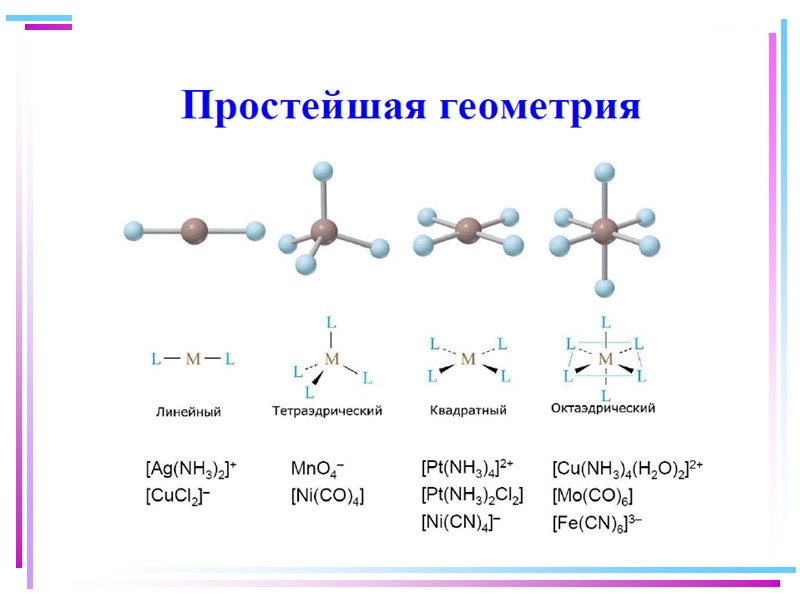
 Геометрическая конфигурация комплексов
Геометрическая конфигурация комплексов
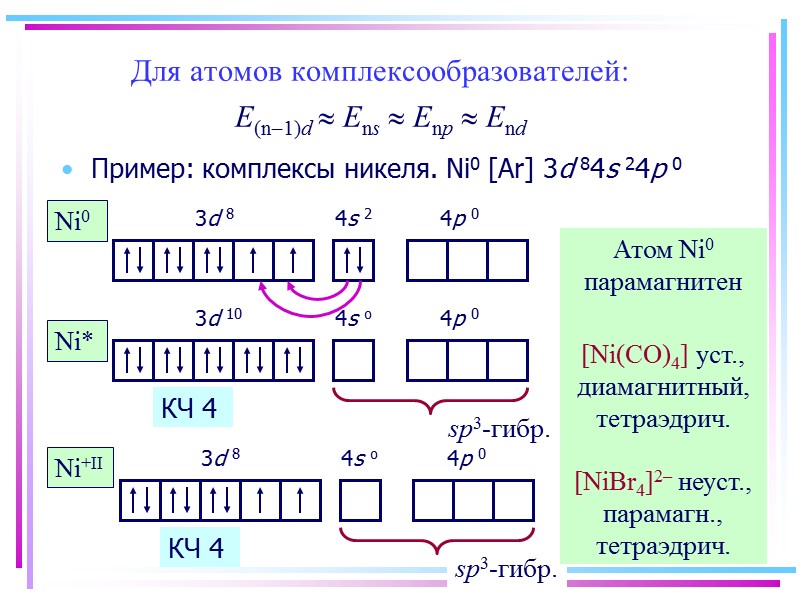
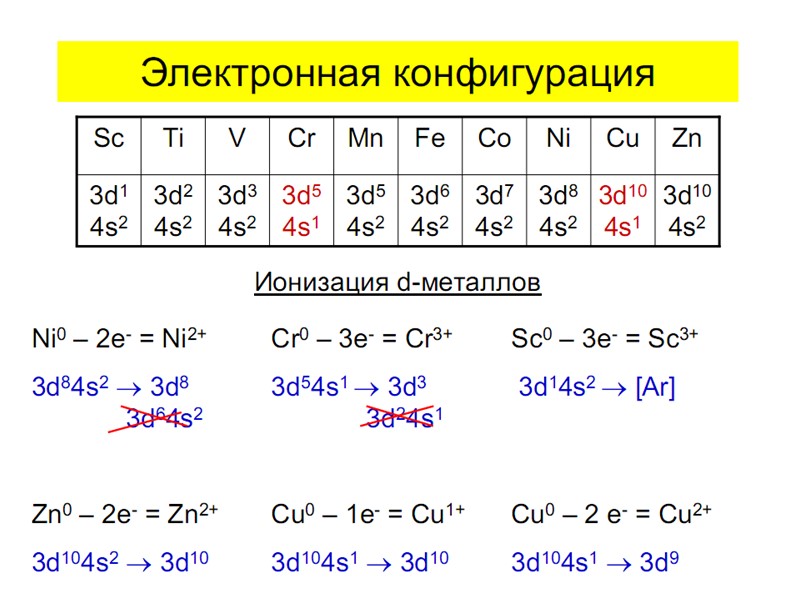
 Для атомов комплексообразователей: E(n-1)d » Ens » Enp » End Пример: комплексы никеля. Ni0 [Ar] 3d 84s 24p 0 Атом Ni0 парамагнитен Ni0 Ni* [Ni(CO)4] уст., диамагнитный, тетраэдрич. Ni+II [NiBr4]2– неуст., парамагн., тетраэдрич. КЧ 4 КЧ 4
Для атомов комплексообразователей: E(n-1)d » Ens » Enp » End Пример: комплексы никеля. Ni0 [Ar] 3d 84s 24p 0 Атом Ni0 парамагнитен Ni0 Ni* [Ni(CO)4] уст., диамагнитный, тетраэдрич. Ni+II [NiBr4]2– неуст., парамагн., тетраэдрич. КЧ 4 КЧ 4
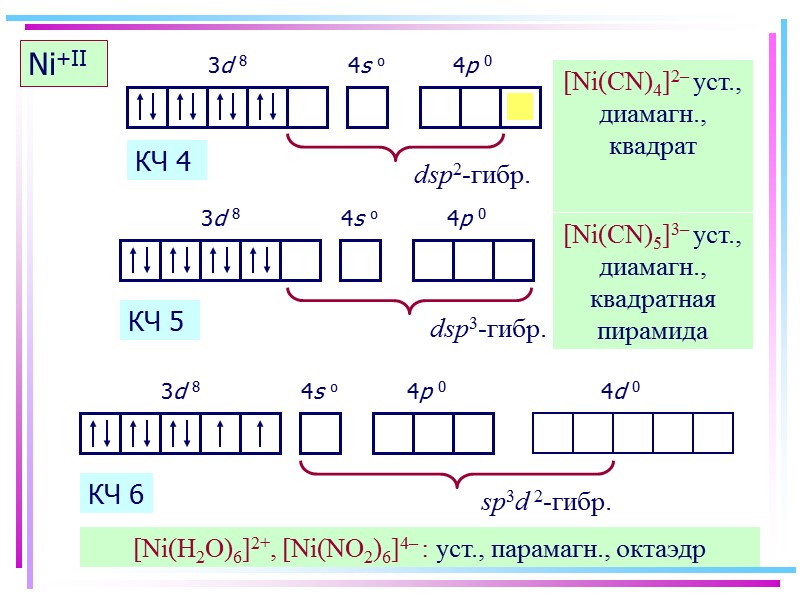
![>Ni+II [Ni(CN)4]2– уст., диамагн., квадрат КЧ 4 [Ni(CN)5]3– уст., диамагн., квадратная пирамида КЧ >Ni+II [Ni(CN)4]2– уст., диамагн., квадрат КЧ 4 [Ni(CN)5]3– уст., диамагн., квадратная пирамида КЧ](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_38.jpg) Ni+II [Ni(CN)4]2– уст., диамагн., квадрат КЧ 4 [Ni(CN)5]3– уст., диамагн., квадратная пирамида КЧ 5 [Ni(H2O)6]2+, [Ni(NO2)6]4– : уст., парамагн., октаэдр КЧ 6 Ni+II
Ni+II [Ni(CN)4]2– уст., диамагн., квадрат КЧ 4 [Ni(CN)5]3– уст., диамагн., квадратная пирамида КЧ 5 [Ni(H2O)6]2+, [Ni(NO2)6]4– : уст., парамагн., октаэдр КЧ 6 Ni+II
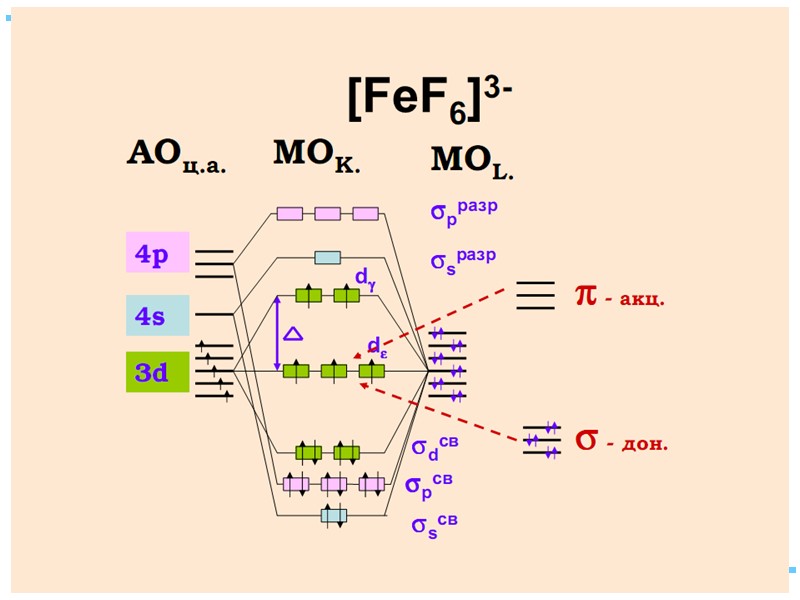
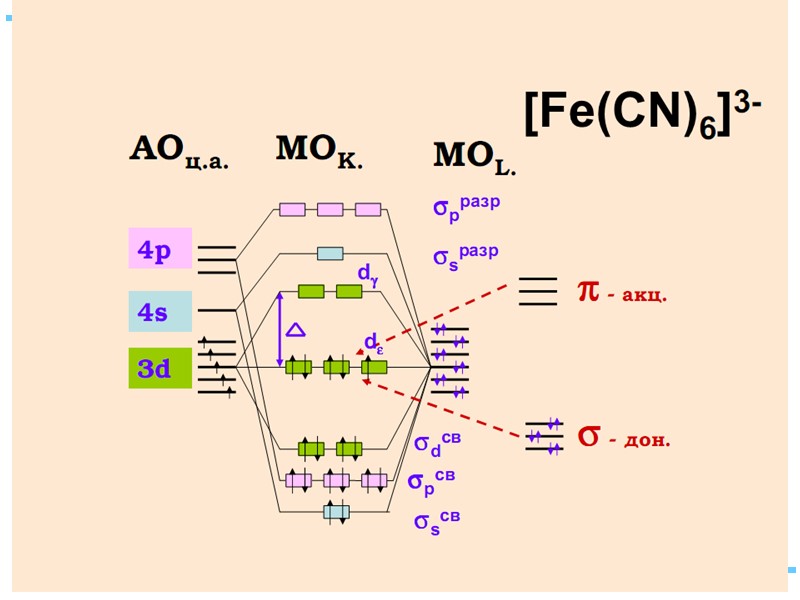
![>Fe+II [FeF6]4– уст., парамагн., октаэдр КЧ 6 Fe+II [Fe(CN)6]4– уст., >Fe+II [FeF6]4– уст., парамагн., октаэдр КЧ 6 Fe+II [Fe(CN)6]4– уст.,](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_39.jpg) Fe+II [FeF6]4– уст., парамагн., октаэдр КЧ 6 Fe+II [Fe(CN)6]4– уст., диамагн., октаэдр КЧ 6
Fe+II [FeF6]4– уст., парамагн., октаэдр КЧ 6 Fe+II [Fe(CN)6]4– уст., диамагн., октаэдр КЧ 6
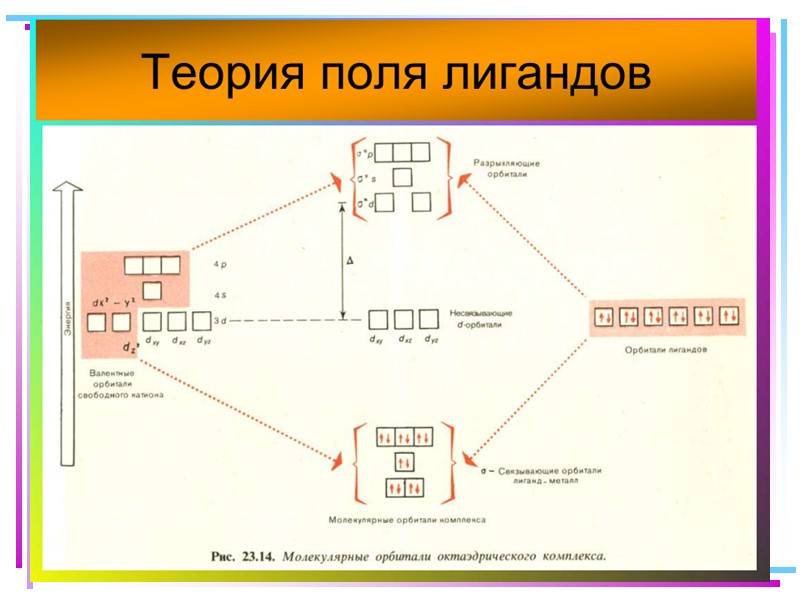
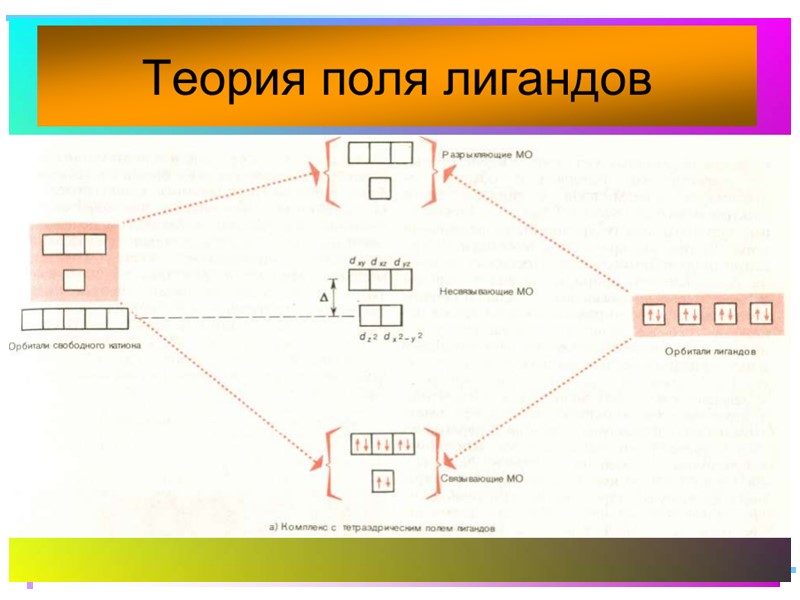
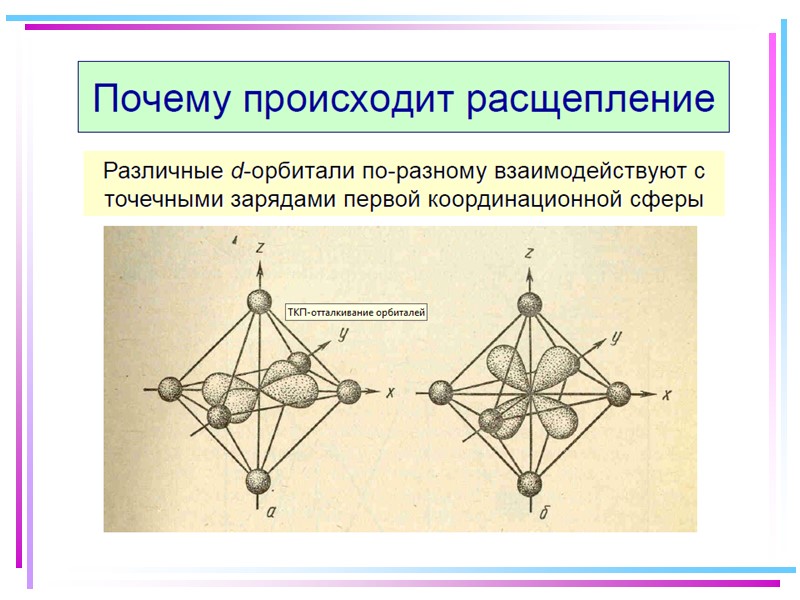
 Основные положения теории кристаллического поля (поля лигандов) Связь комплексообразователя (центр. атома) Mе с лигандами L считается чисто ионной Лиганды L – точечные заряды в вершинах правильных полиэдров, т.е. на максимальном расстоянии друг от друга Взаимодействие L между собой не рассматр. Детально рассматривается влияние электростатич. поля лигандов на Mе, а именно, на энергетич. подуровни (ЭПУ) центрального атома
Основные положения теории кристаллического поля (поля лигандов) Связь комплексообразователя (центр. атома) Mе с лигандами L считается чисто ионной Лиганды L – точечные заряды в вершинах правильных полиэдров, т.е. на максимальном расстоянии друг от друга Взаимодействие L между собой не рассматр. Детально рассматривается влияние электростатич. поля лигандов на Mе, а именно, на энергетич. подуровни (ЭПУ) центрального атома
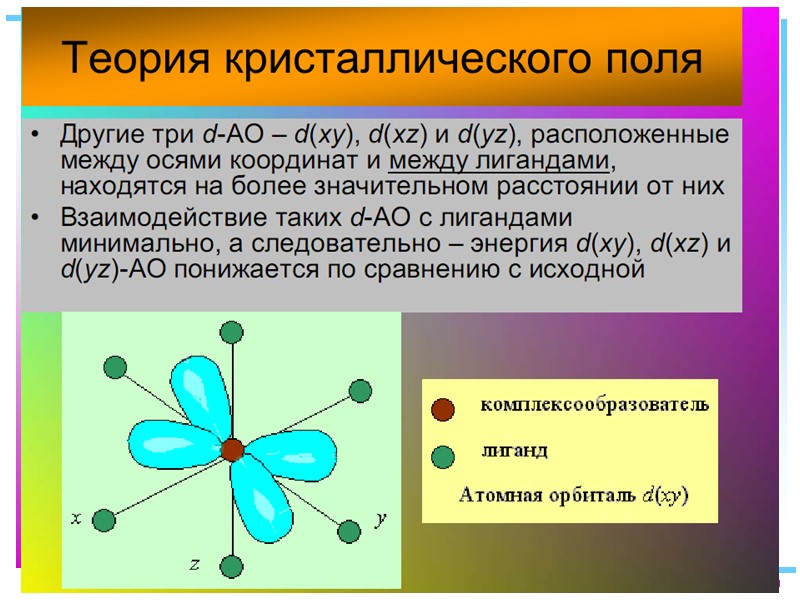
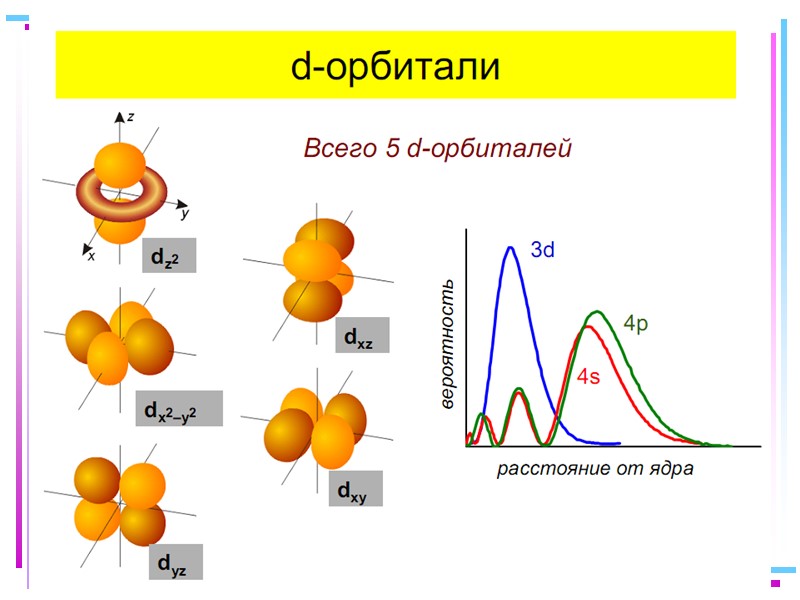
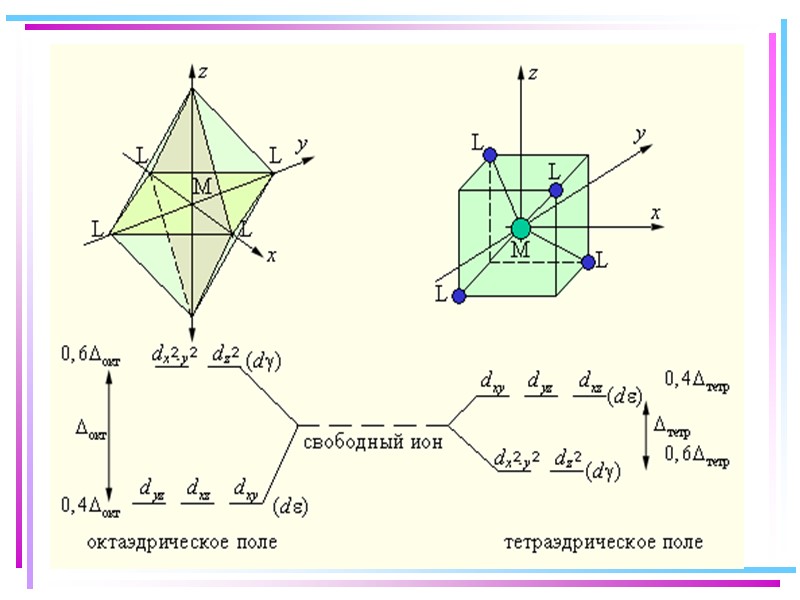
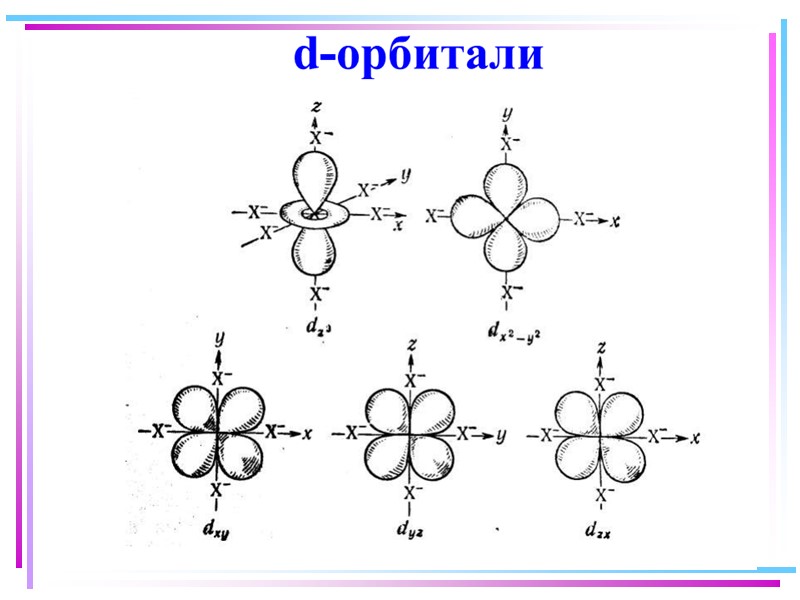
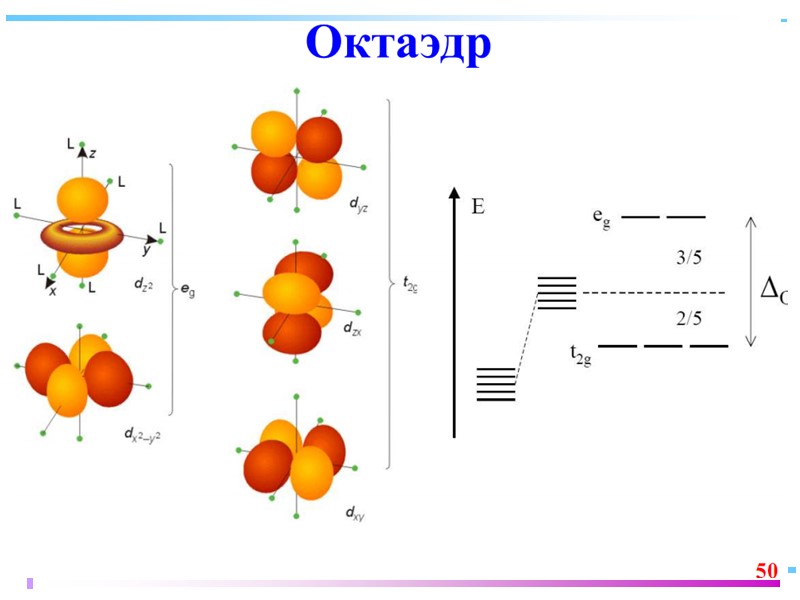
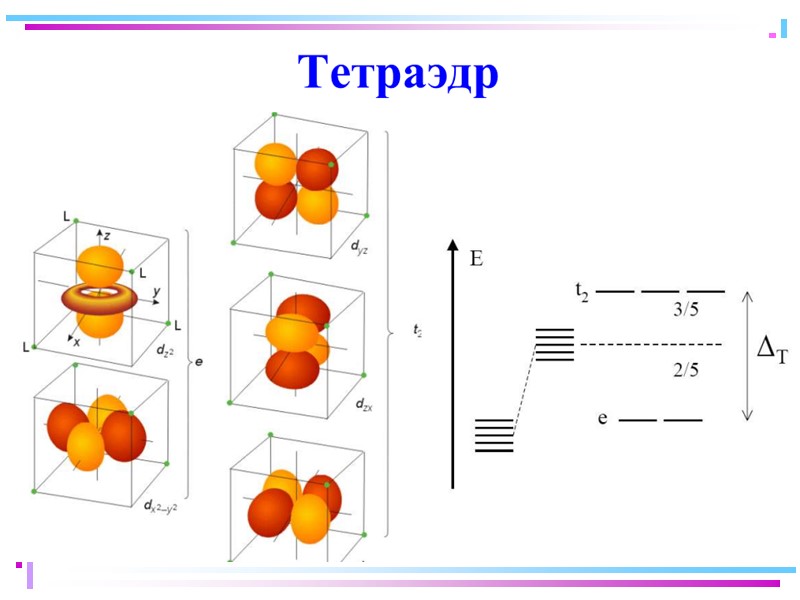
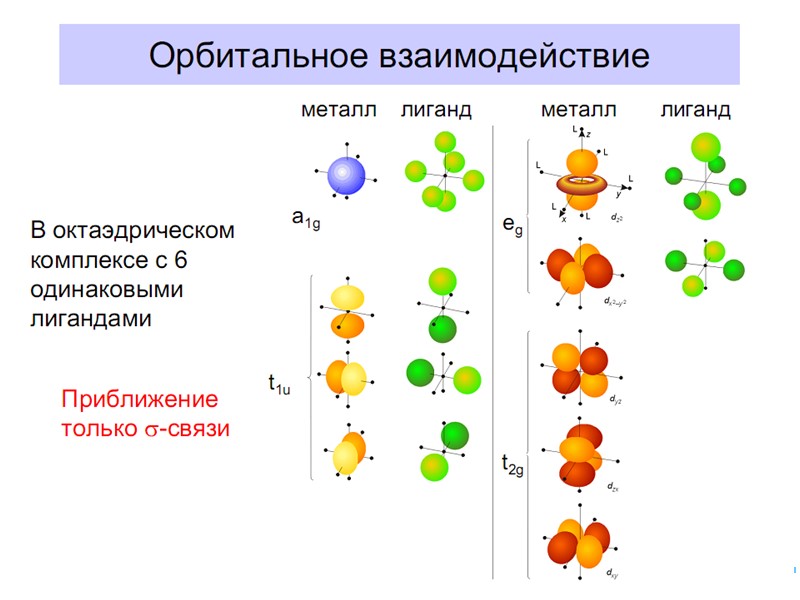
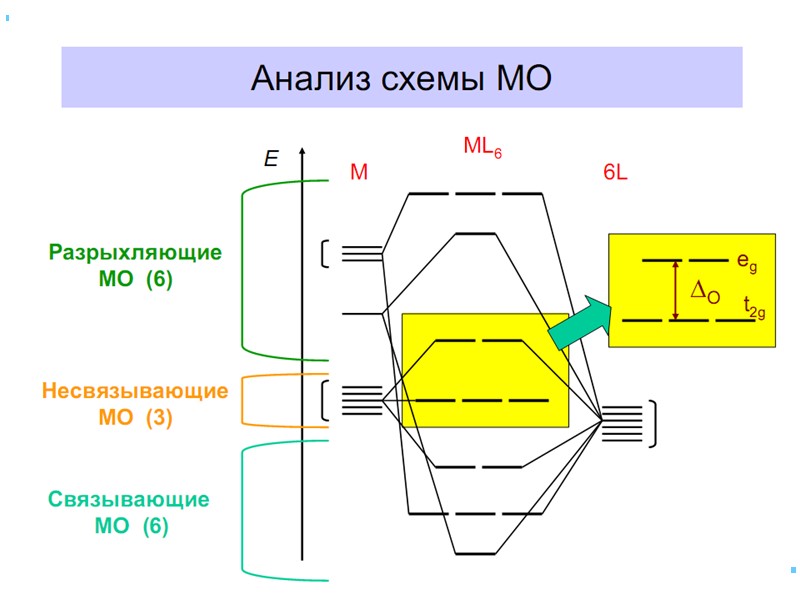
![>В случае [ML6]±,0 : октаэдрическое поле лигандов Поле слабо влияет (энергия падает) в случае >В случае [ML6]±,0 : октаэдрическое поле лигандов Поле слабо влияет (энергия падает) в случае](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_41.jpg) В случае [ML6]±,0 : октаэдрическое поле лигандов Поле слабо влияет (энергия падает) в случае АО d(xy), d(xz) и d(yz), располож. между осей координат (между лигандами) Поле сильно влияет (энергия растет) в случае АО d(z2) и d(x2–y2), располож. вдоль осей координат (ближе всего к лигандам) Eо |E–Eо| = 3/5 ; |E–Eо| = 2/5
В случае [ML6]±,0 : октаэдрическое поле лигандов Поле слабо влияет (энергия падает) в случае АО d(xy), d(xz) и d(yz), располож. между осей координат (между лигандами) Поле сильно влияет (энергия растет) в случае АО d(z2) и d(x2–y2), располож. вдоль осей координат (ближе всего к лигандам) Eо |E–Eо| = 3/5 ; |E–Eо| = 2/5
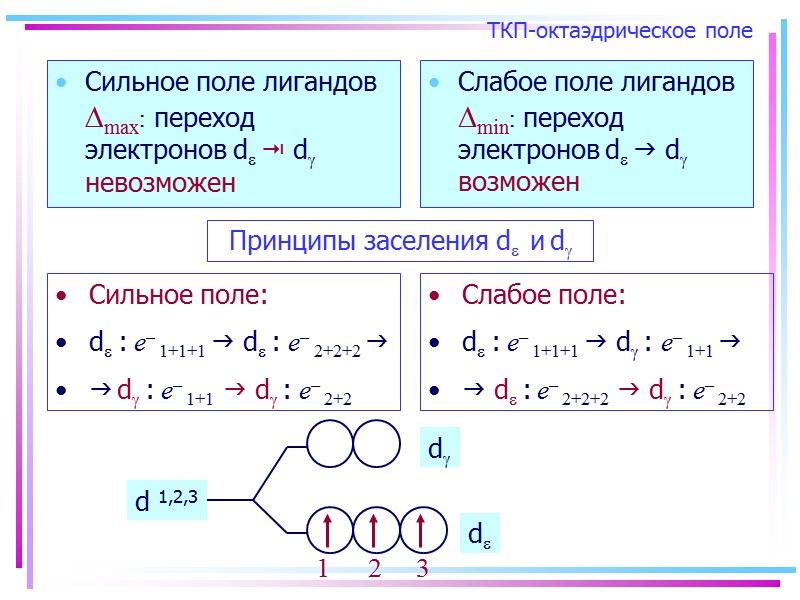
 ТКП-октаэдрическое поле Сильное поле лигандов max: переход электронов d d невозможен Слабое поле лигандов min: переход электронов d d возможен Принципы заселения d и d Сильное поле: d : e– 1+1+1 d : e– 2+2+2 d : e– 1+1 d : e– 2+2 Слабое поле: d : e– 1+1+1 d : e– 1+1 d : e– 2+2+2 d : e– 2+2 d 1,2,3
ТКП-октаэдрическое поле Сильное поле лигандов max: переход электронов d d невозможен Слабое поле лигандов min: переход электронов d d возможен Принципы заселения d и d Сильное поле: d : e– 1+1+1 d : e– 2+2+2 d : e– 1+1 d : e– 2+2 Слабое поле: d : e– 1+1+1 d : e– 1+1 d : e– 2+2+2 d : e– 2+2 d 1,2,3
 Параметр расщепления и волновое число 1 см–1 соответствует ок. 12 Дж/моль : 60 420 кДж/моль или 5000 35000 см–1 Примеры [Mn(H2O)6]2+ : 7800 см–1 [Fe(H2O)6]2+ : 10400 см–1 [Mn(H2O)6]3+ : 21000 см–1 [Fe(H2O)6]3+ : 13700 см–1
Параметр расщепления и волновое число 1 см–1 соответствует ок. 12 Дж/моль : 60 420 кДж/моль или 5000 35000 см–1 Примеры [Mn(H2O)6]2+ : 7800 см–1 [Fe(H2O)6]2+ : 10400 см–1 [Mn(H2O)6]3+ : 21000 см–1 [Fe(H2O)6]3+ : 13700 см–1
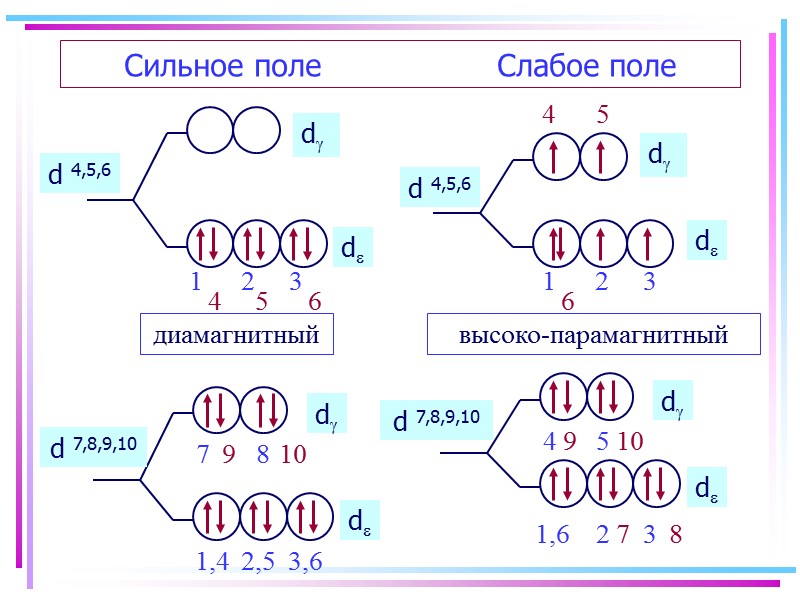
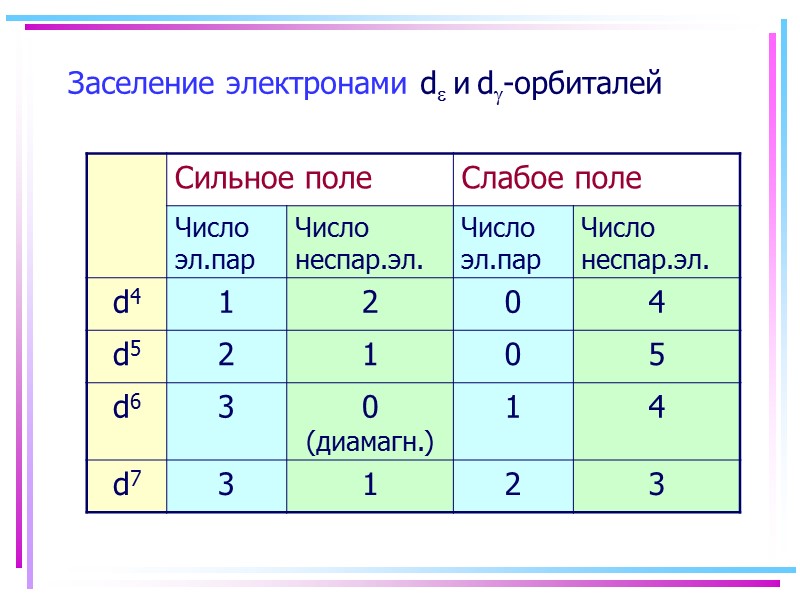
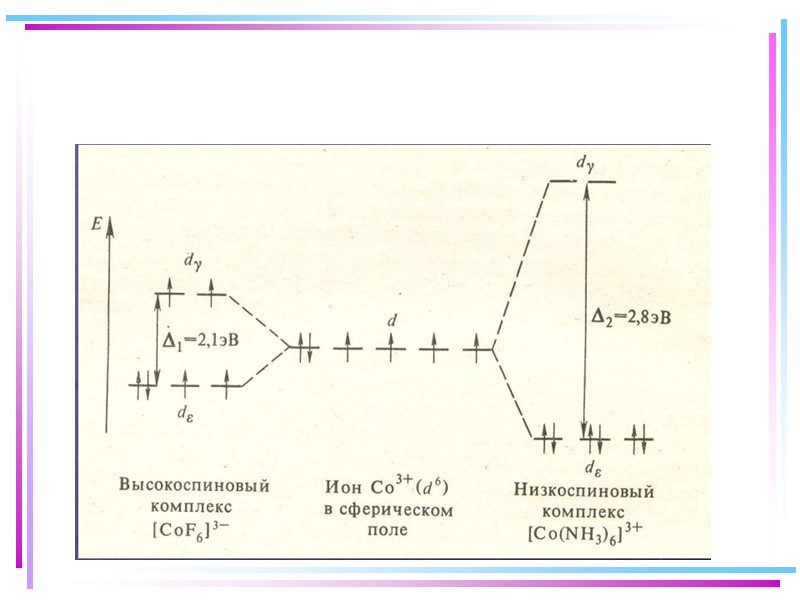
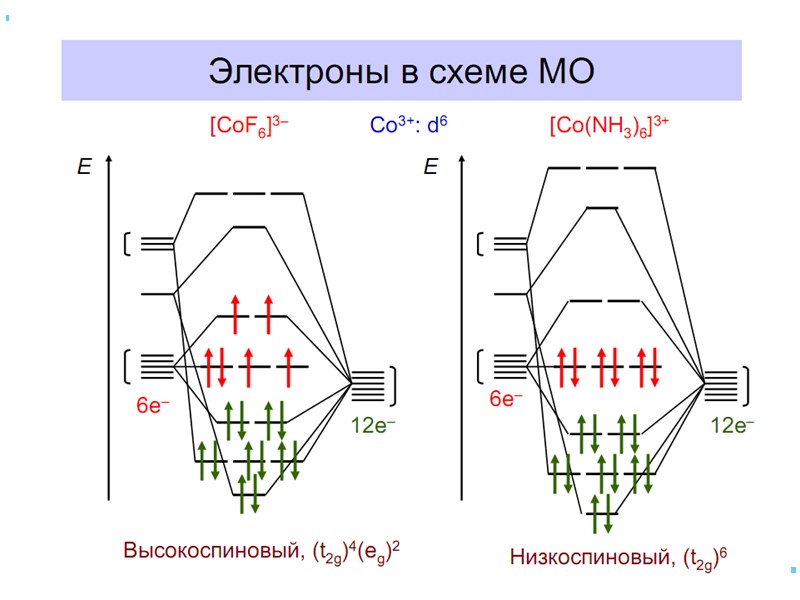
 Сильное поле Слабое поле d 4,5,6 d 4,5,6 диамагнитный высоко-парамагнитный d 7,8,9,10 d 7,8,9,10
Сильное поле Слабое поле d 4,5,6 d 4,5,6 диамагнитный высоко-парамагнитный d 7,8,9,10 d 7,8,9,10
 Заселение электронами d и d-орбиталей
Заселение электронами d и d-орбиталей
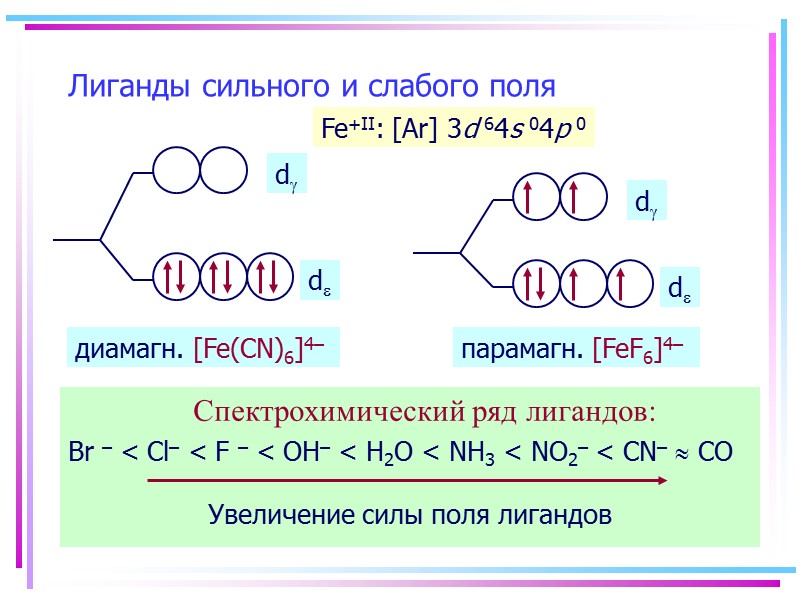
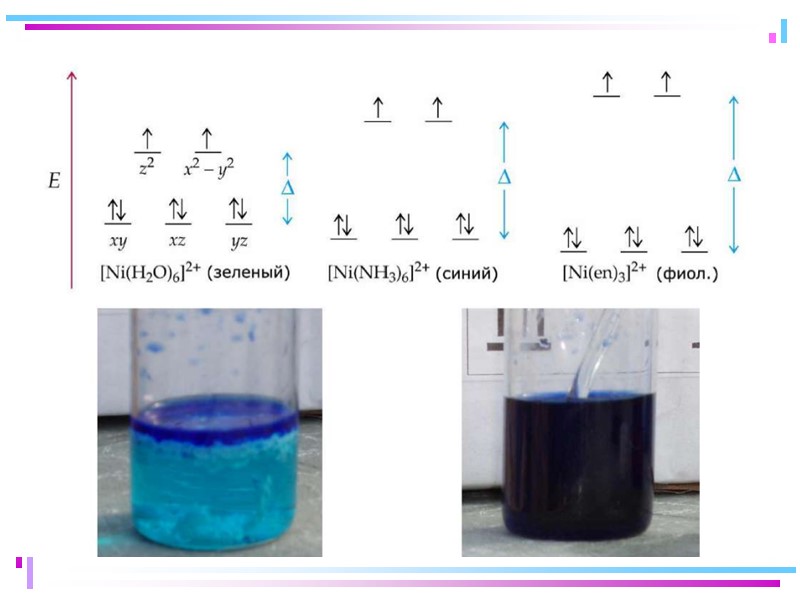
 Лиганды сильного и слабого поля Спектрохимический ряд лигандов: Br – < Cl– < F – < OH– < H2O < NH3 < NO2– < CN– CO Fe+II: [Ar] 3d 64s 04p 0 диамагн. [Fe(CN)6]4– парамагн. [FeF6]4–
Лиганды сильного и слабого поля Спектрохимический ряд лигандов: Br – < Cl– < F – < OH– < H2O < NH3 < NO2– < CN– CO Fe+II: [Ar] 3d 64s 04p 0 диамагн. [Fe(CN)6]4– парамагн. [FeF6]4–
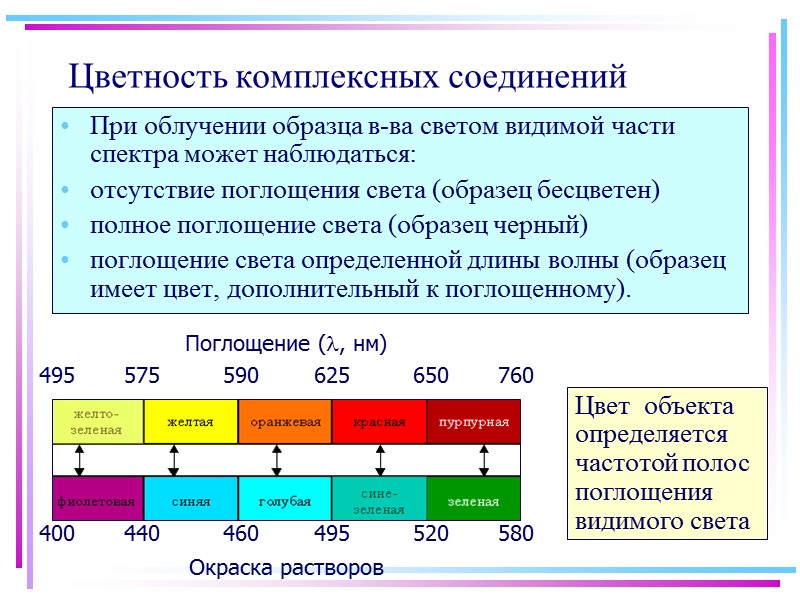
 Цветность комплексных соединений При облучении образца в-ва светом видимой части спектра может наблюдаться: отсутствие поглощения света (образец бесцветен) полное поглощение света (образец черный) поглощение света определенной длины волны (образец имеет цвет, дополнительный к поглощенному). Цвет объекта определяется частотой полос поглощения видимого света
Цветность комплексных соединений При облучении образца в-ва светом видимой части спектра может наблюдаться: отсутствие поглощения света (образец бесцветен) полное поглощение света (образец черный) поглощение света определенной длины волны (образец имеет цвет, дополнительный к поглощенному). Цвет объекта определяется частотой полос поглощения видимого света
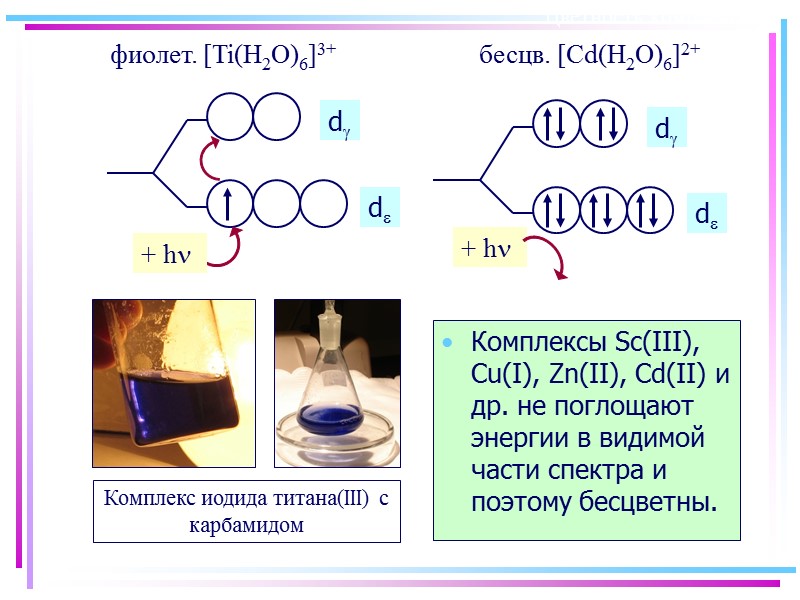
 Цветность комплексов Комплексы Sc(III), Cu(I), Zn(II), Cd(II) и др. не поглощают энергии в видимой части спектра и поэтому бесцветны. фиолет. [Ti(H2O)6]3+ бесцв. [Cd(H2O)6]2+
Цветность комплексов Комплексы Sc(III), Cu(I), Zn(II), Cd(II) и др. не поглощают энергии в видимой части спектра и поэтому бесцветны. фиолет. [Ti(H2O)6]3+ бесцв. [Cd(H2O)6]2+
![>Типы комплексных соединений. 1. Аквакомплексы В водных растворах: [Be(H2O)4]2+ [Al(H2O)6]3+ >Типы комплексных соединений. 1. Аквакомплексы В водных растворах: [Be(H2O)4]2+ [Al(H2O)6]3+](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_49.jpg) Типы комплексных соединений. 1. Аквакомплексы В водных растворах: [Be(H2O)4]2+ [Al(H2O)6]3+ [Cr(H2O)6]3+ … Кристаллогидраты: [Be(H2O)4]SO4 [Al(H2O)6]Cl3 [K(H2O)6][Cr(H2O)6](SO4)2 [Cu(H2O)4]SO4·H2O [Ni(H2O)6]SO4·H2O : OH2
Типы комплексных соединений. 1. Аквакомплексы В водных растворах: [Be(H2O)4]2+ [Al(H2O)6]3+ [Cr(H2O)6]3+ … Кристаллогидраты: [Be(H2O)4]SO4 [Al(H2O)6]Cl3 [K(H2O)6][Cr(H2O)6](SO4)2 [Cu(H2O)4]SO4·H2O [Ni(H2O)6]SO4·H2O : OH2
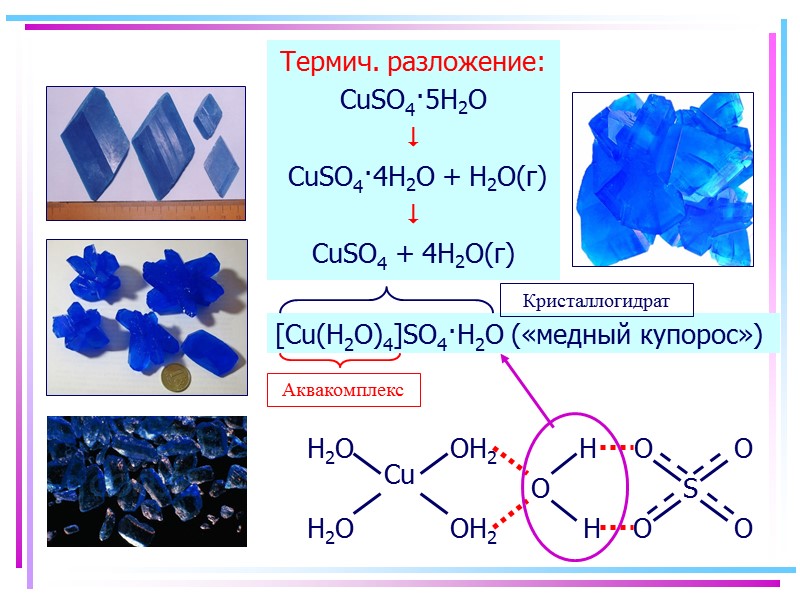
![>Аквакомплексы Термич. разложение: CuSO4·5H2O CuSO4·4H2O + H2O(г) CuSO4 + 4H2O(г) [Cu(H2O)4]SO4·H2O >Аквакомплексы Термич. разложение: CuSO4·5H2O CuSO4·4H2O + H2O(г) CuSO4 + 4H2O(г) [Cu(H2O)4]SO4·H2O](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_50.jpg) Аквакомплексы Термич. разложение: CuSO4·5H2O CuSO4·4H2O + H2O(г) CuSO4 + 4H2O(г) [Cu(H2O)4]SO4·H2O («медный купорос»)
Аквакомплексы Термич. разложение: CuSO4·5H2O CuSO4·4H2O + H2O(г) CuSO4 + 4H2O(г) [Cu(H2O)4]SO4·H2O («медный купорос»)
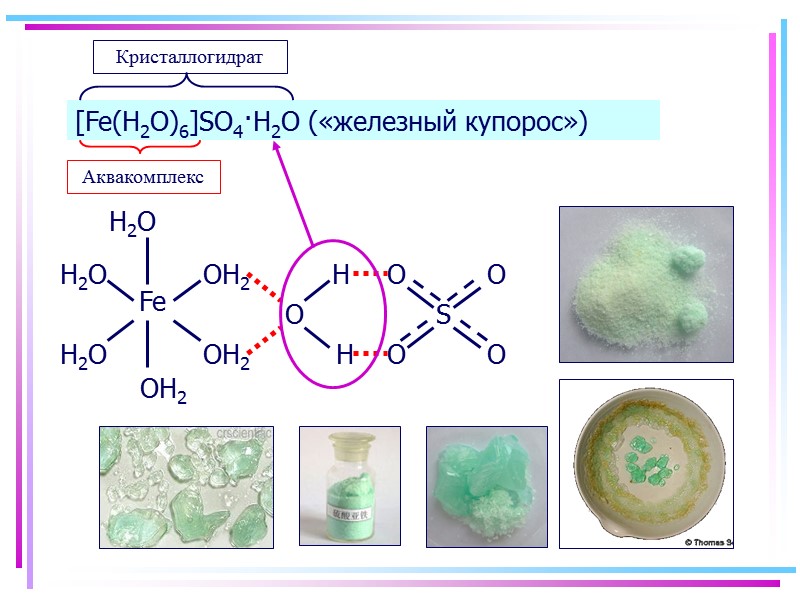
![>Аквакомплексы [Fe(H2O)6]SO4·H2O («железный купорос») >Аквакомплексы [Fe(H2O)6]SO4·H2O («железный купорос»)](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_51.jpg) Аквакомплексы [Fe(H2O)6]SO4·H2O («железный купорос»)
Аквакомплексы [Fe(H2O)6]SO4·H2O («железный купорос»)
![>2. Гидроксокомплексы Получение: Zn(OH)2 + 2OH–(изб.) = [Zn(OH)4]2–; pH >> 7 Разрушение: >2. Гидроксокомплексы Получение: Zn(OH)2 + 2OH–(изб.) = [Zn(OH)4]2–; pH >> 7 Разрушение:](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_52.jpg) 2. Гидроксокомплексы Получение: Zn(OH)2 + 2OH–(изб.) = [Zn(OH)4]2–; pH >> 7 Разрушение: [Zn(OH)4]2– (+H3O+) + CH3COOH; CO2; NH4+ (сл.к-ты, pH 7) Zn(OH)2(т) + H3O+ (сильн.к-ты, pH < 7) [Zn(H2O)4]2+ Образование гидроксокомплексов характерно для амфотерных элементов. : OH–
2. Гидроксокомплексы Получение: Zn(OH)2 + 2OH–(изб.) = [Zn(OH)4]2–; pH >> 7 Разрушение: [Zn(OH)4]2– (+H3O+) + CH3COOH; CO2; NH4+ (сл.к-ты, pH 7) Zn(OH)2(т) + H3O+ (сильн.к-ты, pH < 7) [Zn(H2O)4]2+ Образование гидроксокомплексов характерно для амфотерных элементов. : OH–
![>3. Аммины (аммиакаты) Получение: AgCl(т) + 2NH3·H2O(изб.) = [Ag(NH3)2]+ +Cl– + 2H2O Разрушение: >3. Аммины (аммиакаты) Получение: AgCl(т) + 2NH3·H2O(изб.) = [Ag(NH3)2]+ +Cl– + 2H2O Разрушение:](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_53.jpg) 3. Аммины (аммиакаты) Получение: AgCl(т) + 2NH3·H2O(изб.) = [Ag(NH3)2]+ +Cl– + 2H2O Разрушение: [Ag(NH3)2]+ + H3O+ NH4+ + … [Ag(NH3)2]+ + I– AgI(т) + … [Ag(NH3)2]+ + t° NH3(г) + … : NH3
3. Аммины (аммиакаты) Получение: AgCl(т) + 2NH3·H2O(изб.) = [Ag(NH3)2]+ +Cl– + 2H2O Разрушение: [Ag(NH3)2]+ + H3O+ NH4+ + … [Ag(NH3)2]+ + I– AgI(т) + … [Ag(NH3)2]+ + t° NH3(г) + … : NH3
![>Получение: HgI2(т) + 2I–(изб.) = [HgI4]2– [Fe(H2O)6]3+ + 6NCS−=[Fe(NCS)6]3− + 6H2O Разрушение: >Получение: HgI2(т) + 2I–(изб.) = [HgI4]2– [Fe(H2O)6]3+ + 6NCS−=[Fe(NCS)6]3− + 6H2O Разрушение:](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_54.jpg) Получение: HgI2(т) + 2I–(изб.) = [HgI4]2– [Fe(H2O)6]3+ + 6NCS−=[Fe(NCS)6]3− + 6H2O Разрушение: [HgI4]2– + S2– = HgS(т) + 4I– [Fe(NCS)6]3− + 4F− = [FeF4]− + 6NCS− 4. Ацидокомплексы : Х–
Получение: HgI2(т) + 2I–(изб.) = [HgI4]2– [Fe(H2O)6]3+ + 6NCS−=[Fe(NCS)6]3− + 6H2O Разрушение: [HgI4]2– + S2– = HgS(т) + 4I– [Fe(NCS)6]3− + 4F− = [FeF4]− + 6NCS− 4. Ацидокомплексы : Х–
![>6. Анионгалогенаты M[ЭГ¢mГ²n] (Э, Г¢ и Г² – галогены) Получение: KI + >6. Анионгалогенаты M[ЭГ¢mГ²n] (Э, Г¢ и Г² – галогены) Получение: KI +](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_55.jpg) 6. Анионгалогенаты M[ЭГ¢mГ²n] (Э, Г¢ и Г² – галогены) Получение: KI + I2 = K[I(I)2]; CsCl + IBr = Cs[I(Br)(Cl)] Разрушение: K[I(I)2] + t° = KI + I2(г) Cs[I(Br)(Cl)] + t° = CsCl + IBr(г) 7. Катионгалогены [ЭГ¢mГ²n]Z (Э, Г¢ и Г² – галогены) Получение: ICl3 + SbCl5 = [ICl2][SbCl6]; BrF3 + AsF5 = [BrF2][AsF6] Свойства: Ag[BrF4](s) + [BrF2][SbF6](s) = Ag[SbF6](s) + 2BrF3(ж) в среде BrF3(ж)
6. Анионгалогенаты M[ЭГ¢mГ²n] (Э, Г¢ и Г² – галогены) Получение: KI + I2 = K[I(I)2]; CsCl + IBr = Cs[I(Br)(Cl)] Разрушение: K[I(I)2] + t° = KI + I2(г) Cs[I(Br)(Cl)] + t° = CsCl + IBr(г) 7. Катионгалогены [ЭГ¢mГ²n]Z (Э, Г¢ и Г² – галогены) Получение: ICl3 + SbCl5 = [ICl2][SbCl6]; BrF3 + AsF5 = [BrF2][AsF6] Свойства: Ag[BrF4](s) + [BrF2][SbF6](s) = Ag[SbF6](s) + 2BrF3(ж) в среде BrF3(ж)
![>Получение: 4 NaH + B(OCH3)3 = Na[BH4] + 3CH3ONa (при 250 °C) 4 >Получение: 4 NaH + B(OCH3)3 = Na[BH4] + 3CH3ONa (при 250 °C) 4](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_56.jpg) Получение: 4 NaH + B(OCH3)3 = Na[BH4] + 3CH3ONa (при 250 °C) 4 LiH + AlCl3 = Li[AlH4] + 3LiCl 3 Li[BH4] + AlCl3 = Al[BH4]3 + 3LiCl Разрушение: Na[AlH4] + 4 H2O = NaOH + Al(OH)3 + 4 H2 (ОВР) 2 Na[BH4] + H2SO4 = Na2SO4 + B2H6 + 2 H2 (ОВР) 5. Гидридокомплексы : H–
Получение: 4 NaH + B(OCH3)3 = Na[BH4] + 3CH3ONa (при 250 °C) 4 LiH + AlCl3 = Li[AlH4] + 3LiCl 3 Li[BH4] + AlCl3 = Al[BH4]3 + 3LiCl Разрушение: Na[AlH4] + 4 H2O = NaOH + Al(OH)3 + 4 H2 (ОВР) 2 Na[BH4] + H2SO4 = Na2SO4 + B2H6 + 2 H2 (ОВР) 5. Гидридокомплексы : H–
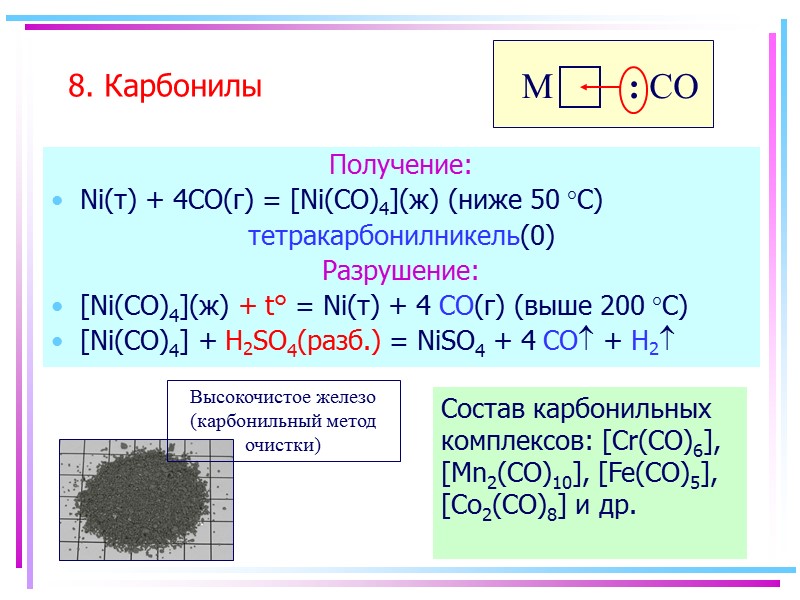
 (ниже 50 °С) тетракарбонилникель(0) >Получение: Ni(т) + 4CO(г) = [Ni(CO)4](ж) (ниже 50 °С) тетракарбонилникель(0)](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_57.jpg) Получение: Ni(т) + 4CO(г) = [Ni(CO)4](ж) (ниже 50 °С) тетракарбонилникель(0) Разрушение: [Ni(CO)4](ж) + t° = Ni(т) + 4 CO(г) (выше 200 °С) [Ni(CO)4] + H2SO4(разб.) = NiSO4 + 4 CO + H2 8. Карбонилы : CO Состав карбонильных комплексов: [Cr(CO)6], [Mn2(CO)10], [Fe(CO)5], [Co2(CO)8] и др.
Получение: Ni(т) + 4CO(г) = [Ni(CO)4](ж) (ниже 50 °С) тетракарбонилникель(0) Разрушение: [Ni(CO)4](ж) + t° = Ni(т) + 4 CO(г) (выше 200 °С) [Ni(CO)4] + H2SO4(разб.) = NiSO4 + 4 CO + H2 8. Карбонилы : CO Состав карбонильных комплексов: [Cr(CO)6], [Mn2(CO)10], [Fe(CO)5], [Co2(CO)8] и др.
 Правило Сиджвика для определения состава комплексов Устойчивым является комплекс, в котором реализована 18-эл-ная оболочка из s-, p- и d-электронов М и x эл. пар лигандов (L) 26Fe0 [Ar]3d64s2 || 36Kr 18 – 8 = 10e – или 36 – 26 = 10e – x = 10/2 = 5 эл.пар (5 молекул CO) [Fe(CO)5] пентакарбонилжелезо
Правило Сиджвика для определения состава комплексов Устойчивым является комплекс, в котором реализована 18-эл-ная оболочка из s-, p- и d-электронов М и x эл. пар лигандов (L) 26Fe0 [Ar]3d64s2 || 36Kr 18 – 8 = 10e – или 36 – 26 = 10e – x = 10/2 = 5 эл.пар (5 молекул CO) [Fe(CO)5] пентакарбонилжелезо
![>Правило Сиджвика (примеры) * 27Co0 [Ar]3d74s2 || 36Kr * 18 – 9 = 9e >Правило Сиджвика (примеры) * 27Co0 [Ar]3d74s2 || 36Kr * 18 – 9 = 9e](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_59.jpg) Правило Сиджвика (примеры) * 27Co0 [Ar]3d74s2 || 36Kr * 18 – 9 = 9e –; * х = 9/2 = 4,5 (?) * радикал [·Co(CO)4] * тетракарбонилкобальт (неуст.) * димер [Co2(CO)8] (уст.) октакарбонилдикобальт 23V0 [Ar]3d34s2 || 36Kr 18–5 = 13e –; х = 13/2 = 6,5 (?) радикал [·V(CO)6] (неуст.) или компл.соединение состава K[:V–I(CO)6] гексакарбонилванадат(-I) калия (уст.)
Правило Сиджвика (примеры) * 27Co0 [Ar]3d74s2 || 36Kr * 18 – 9 = 9e –; * х = 9/2 = 4,5 (?) * радикал [·Co(CO)4] * тетракарбонилкобальт (неуст.) * димер [Co2(CO)8] (уст.) октакарбонилдикобальт 23V0 [Ar]3d34s2 || 36Kr 18–5 = 13e –; х = 13/2 = 6,5 (?) радикал [·V(CO)6] (неуст.) или компл.соединение состава K[:V–I(CO)6] гексакарбонилванадат(-I) калия (уст.)
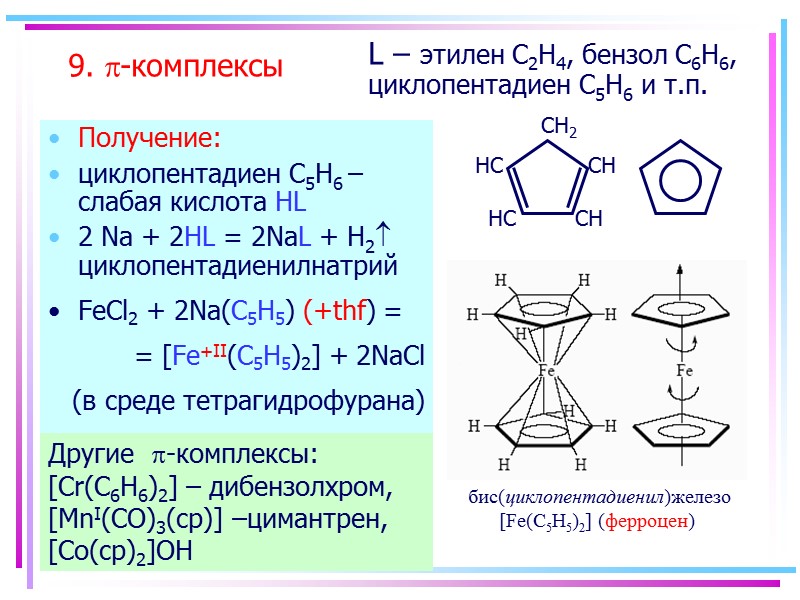
 9. p-комплексы Получение: циклопентадиен С5H6 – слабая кислота HL 2 Na + 2HL = 2NaL + H2 циклопентадиенилнатрий FeCl2 + 2Na(C5H5) (+thf) = = [Fe+II(C5H5)2] + 2NaCl (в среде тетрагидрофурана) Другие -комплексы: [Cr(C6H6)2] – дибензолхром, [MnI(CO)3(cp)] –цимантрен, [Co(cp)2]OH L – этилен C2H4, бензол C6H6, циклопентадиен С5H6 и т.п.
9. p-комплексы Получение: циклопентадиен С5H6 – слабая кислота HL 2 Na + 2HL = 2NaL + H2 циклопентадиенилнатрий FeCl2 + 2Na(C5H5) (+thf) = = [Fe+II(C5H5)2] + 2NaCl (в среде тетрагидрофурана) Другие -комплексы: [Cr(C6H6)2] – дибензолхром, [MnI(CO)3(cp)] –цимантрен, [Co(cp)2]OH L – этилен C2H4, бензол C6H6, циклопентадиен С5H6 и т.п.
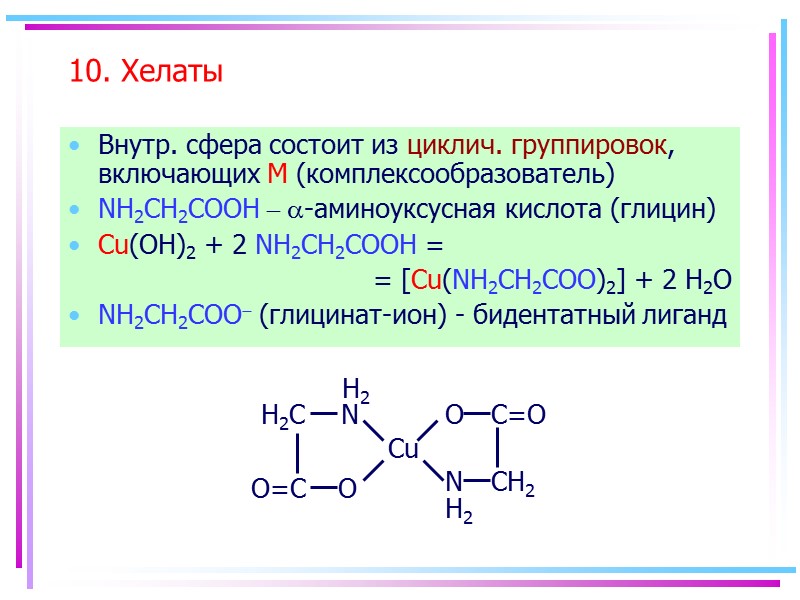
 10. Хелаты Внутр. сфера состоит из циклич. группировок, включающих M (комплексообразователь) NH2CH2COOH - a-аминоуксусная кислота (глицин) Cu(OH)2 + 2 NH2CH2COOH = = [Cu(NH2CH2COO)2] + 2 H2O NH2CH2COO- (глицинат-ион) - бидентатный лиганд
10. Хелаты Внутр. сфера состоит из циклич. группировок, включающих M (комплексообразователь) NH2CH2COOH - a-аминоуксусная кислота (глицин) Cu(OH)2 + 2 NH2CH2COOH = = [Cu(NH2CH2COO)2] + 2 H2O NH2CH2COO- (глицинат-ион) - бидентатный лиганд
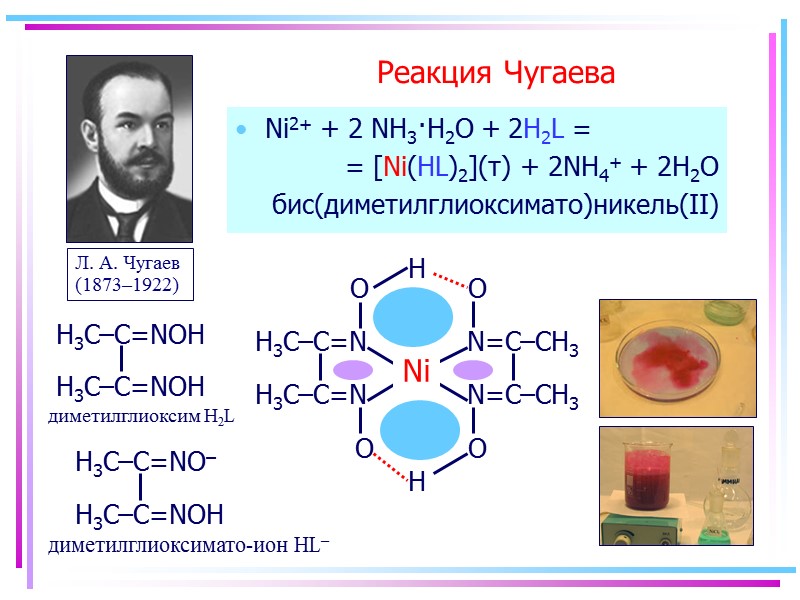
 + >Реакция Чугаева Ni2+ + 2 NH3·H2O + 2H2L = = [Ni(HL)2](т) +](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_62.jpg) Реакция Чугаева Ni2+ + 2 NH3·H2O + 2H2L = = [Ni(HL)2](т) + 2NH4+ + 2H2O бис(диметилглиоксимато)никель(II)
Реакция Чугаева Ni2+ + 2 NH3·H2O + 2H2L = = [Ni(HL)2](т) + 2NH4+ + 2H2O бис(диметилглиоксимато)никель(II)
 Методы синтеза комплексных соединений Реакция обмена лигандов А) в водном растворе (обр, принцип Ле Шателье): [Сu(H2O)4]2+ + 4NH3·H2O = [Cu(NH3)4]2+ + 8H2O (обр. прод.) > (обр. исх.реаг.) Б) в неводном растворителе: [Al(H2O)6]3+ + NH3·H2O [Al(H2O)6]3+(s) + 6NH3(ж) = [Al(NH3)6]3+(s) + 6H2O(s) В) без растворителя: [Ni(H2O)6]Cl2(т) + 6NH3(г) = [Ni(NH3)6]Cl2(т) +6H2O(г) Г) внутримол. обмен лигандов в тв. фазе: 2[Co(H2O)6]Cl2(т) + t° = Co[CoCl4](т) + 12H2O розовый синий
Методы синтеза комплексных соединений Реакция обмена лигандов А) в водном растворе (обр, принцип Ле Шателье): [Сu(H2O)4]2+ + 4NH3·H2O = [Cu(NH3)4]2+ + 8H2O (обр. прод.) > (обр. исх.реаг.) Б) в неводном растворителе: [Al(H2O)6]3+ + NH3·H2O [Al(H2O)6]3+(s) + 6NH3(ж) = [Al(NH3)6]3+(s) + 6H2O(s) В) без растворителя: [Ni(H2O)6]Cl2(т) + 6NH3(г) = [Ni(NH3)6]Cl2(т) +6H2O(г) Г) внутримол. обмен лигандов в тв. фазе: 2[Co(H2O)6]Cl2(т) + t° = Co[CoCl4](т) + 12H2O розовый синий
 Методы синтеза комплексных соединений Д) ОВР + реакции обмена лигандов +Ок.+ L [СoII(H2O)6]2+ [СoIIIL6]3+ Ок.: H2O2, KNO2 … L – NH3, NO2– … Примеры: 2CoIICl2 + 12NH3 + H2O2 = 2[CoIII(NH3)6](OH)Cl2 CoIICl2 + 7KNO2 + 2CH3COOH = = K3[CoIII(NO2)6] + NO + 2KCl + 2CH3COOK + H2O + Вс [NiII(CN)4]2– [Ni0(CN)4]4–
Методы синтеза комплексных соединений Д) ОВР + реакции обмена лигандов +Ок.+ L [СoII(H2O)6]2+ [СoIIIL6]3+ Ок.: H2O2, KNO2 … L – NH3, NO2– … Примеры: 2CoIICl2 + 12NH3 + H2O2 = 2[CoIII(NH3)6](OH)Cl2 CoIICl2 + 7KNO2 + 2CH3COOH = = K3[CoIII(NO2)6] + NO + 2KCl + 2CH3COOK + H2O + Вс [NiII(CN)4]2– [Ni0(CN)4]4–
 Решение задач. 1. Растворение осадка при комплексообразовании AgBr(т) Ag+ + Br – ; ПРAgBr = 7,7·10–13 Ag+ + 2 SO3S2– [Ag(SO3S)2]3– ; обр = 4·1013 AgBr(т) + 2 SO3S2– [Ag(SO3S)2]3– + Br –; Kc = ? Kc = ПРAgBr обр = 7,7·10–13 4·1013 = 30,8 >> 1 Наблюдается растворение осадка (смещение равновесия вправо ) = ПРAgBr обр
Решение задач. 1. Растворение осадка при комплексообразовании AgBr(т) Ag+ + Br – ; ПРAgBr = 7,7·10–13 Ag+ + 2 SO3S2– [Ag(SO3S)2]3– ; обр = 4·1013 AgBr(т) + 2 SO3S2– [Ag(SO3S)2]3– + Br –; Kc = ? Kc = ПРAgBr обр = 7,7·10–13 4·1013 = 30,8 >> 1 Наблюдается растворение осадка (смещение равновесия вправо ) = ПРAgBr обр
![>Решение задач. 2. Реакция обмена лигандов [Co(NH3)6]3+ + 6 CN– [Co(CN)6]3– + >Решение задач. 2. Реакция обмена лигандов [Co(NH3)6]3+ + 6 CN– [Co(CN)6]3– +](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_66.jpg) Решение задач. 2. Реакция обмена лигандов [Co(NH3)6]3+ + 6 CN– [Co(CN)6]3– + 6 NH3 ; Kc = ? Co3+ + 6 NH3 [Co(NH3)6]3+ ; обр(1) = 1,6·1035 Co3+ + 6 CN– [Co(CN)6]3– ; обр(2) = 1,0·1064 Kc = обр(2) / обр(1) = (1,0·1064)/(1,6·1035) = 6,2·1029 >> 1 Наблюдается смещение равновесия вправо обр(2) обр(1)
Решение задач. 2. Реакция обмена лигандов [Co(NH3)6]3+ + 6 CN– [Co(CN)6]3– + 6 NH3 ; Kc = ? Co3+ + 6 NH3 [Co(NH3)6]3+ ; обр(1) = 1,6·1035 Co3+ + 6 CN– [Co(CN)6]3– ; обр(2) = 1,0·1064 Kc = обр(2) / обр(1) = (1,0·1064)/(1,6·1035) = 6,2·1029 >> 1 Наблюдается смещение равновесия вправо обр(2) обр(1)
![>Решение задач. 3. Разрушение комплекса [Cu(NH3)4]2+ + 4 H3O+ [Cu(H2O)4]2+ + 4 >Решение задач. 3. Разрушение комплекса [Cu(NH3)4]2+ + 4 H3O+ [Cu(H2O)4]2+ + 4](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_67.jpg) Решение задач. 3. Разрушение комплекса [Cu(NH3)4]2+ + 4 H3O+ [Cu(H2O)4]2+ + 4 NH4+ ; Kc = ? Cu2+ + 4 NH3 [Cu(NH3)4]2+ ; обр = 7,9·1012 NH4+ + 2H2O NH3·H2O + H3O+ ; Kк = 5,75·10–10 Kc = 1 / (7,9·1012·5,754·10–40 ) = 1,16·1020 >> 1 Наблюдается разрушение аммиачного комплекса в кислотной среде (смещение равновесия вправо ) 1 обр Kк 4
Решение задач. 3. Разрушение комплекса [Cu(NH3)4]2+ + 4 H3O+ [Cu(H2O)4]2+ + 4 NH4+ ; Kc = ? Cu2+ + 4 NH3 [Cu(NH3)4]2+ ; обр = 7,9·1012 NH4+ + 2H2O NH3·H2O + H3O+ ; Kк = 5,75·10–10 Kc = 1 / (7,9·1012·5,754·10–40 ) = 1,16·1020 >> 1 Наблюдается разрушение аммиачного комплекса в кислотной среде (смещение равновесия вправо ) 1 обр Kк 4
![>Решение задач. 4. Направление реакции CuCN(т) + H2O + HCN [Cu(CN)2]– + >Решение задач. 4. Направление реакции CuCN(т) + H2O + HCN [Cu(CN)2]– +](https://present5.com/presentacii/20170504/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_images/145-2017_prezentaciya_komp_soed_dlya_btk,_bos.ppt_68.jpg) Решение задач. 4. Направление реакции CuCN(т) + H2O + HCN [Cu(CN)2]– + H3O+ Kc = ? Cu+ + 2CN– [Cu(CN)2]– ; обр = 1,0·1024 HCN + H2O CN– + H3O+ ; Kк = = 4,93·10–10 CuCN(т) Cu+ + CN– ; ПРCuCN = 3,2·10–20 Kc = 1,0·1024 · 4,93·10–10 · 3,2·10–20 = 1,6·10–6 << 1 Растворение осадка не наблюдается (равновесие смещено влево ) = обр·Kк·ПРCuCN
Решение задач. 4. Направление реакции CuCN(т) + H2O + HCN [Cu(CN)2]– + H3O+ Kc = ? Cu+ + 2CN– [Cu(CN)2]– ; обр = 1,0·1024 HCN + H2O CN– + H3O+ ; Kк = = 4,93·10–10 CuCN(т) Cu+ + CN– ; ПРCuCN = 3,2·10–20 Kc = 1,0·1024 · 4,93·10–10 · 3,2·10–20 = 1,6·10–6 << 1 Растворение осадка не наблюдается (равновесие смещено влево ) = обр·Kк·ПРCuCN










































 Спектр атома водорода
Спектр атома водорода
 Спектр атома водорода
Спектр атома водорода











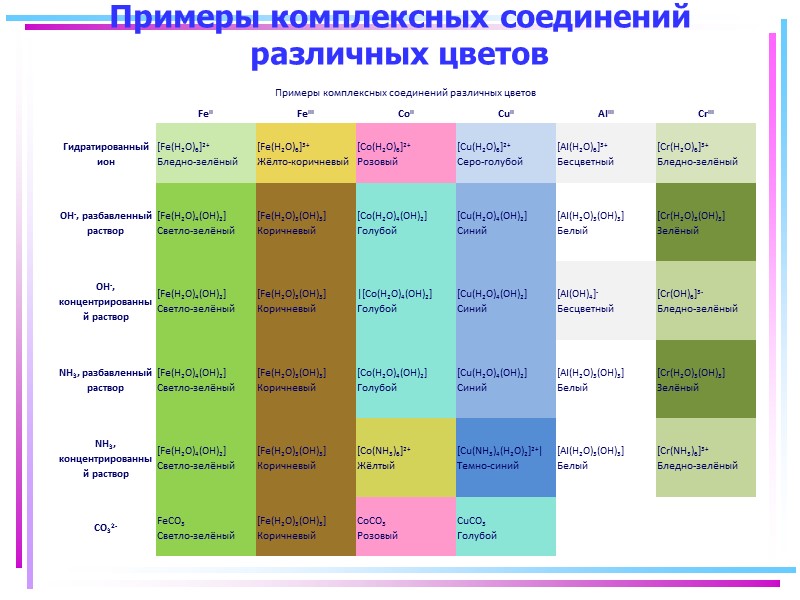
 Примеры комплексных соединений различных цветов
Примеры комплексных соединений различных цветов


 Магнитные моменты высокоспиновых КС
Магнитные моменты высокоспиновых КС
 Содержание Введение Комплексные ионы Комплексные соединения Реакции комплексообразования Координационные соединения Глава 1. Основные понятия координационной теории 1.1. Комплексообразователь 1.2. Лиганды 1.3. Дентатность 1.4. Координационное число 1.5. Внутренняя и внешняя сфера 1.6. Многоядерные комплексы Глава 2. Номенклатура комплексных соединений 2.1. Названия лигандов 2.2. Порядок перечисления лигандов 2.3. Нейтральные комплексы 2.4. Комплексные катионы 2.5. Комплексные анионы 2.6. Мостиковые группы и многоядерные комплексы 2.7. Геометрические изомеры Глава 3. Строение комплексных соединений 3.1. Координационное число 2 3.2. Координационное число 3 3.3. Координационное число 4 3.4. Координационное число 5 3.5. Координационное число 6 и выше
Содержание Введение Комплексные ионы Комплексные соединения Реакции комплексообразования Координационные соединения Глава 1. Основные понятия координационной теории 1.1. Комплексообразователь 1.2. Лиганды 1.3. Дентатность 1.4. Координационное число 1.5. Внутренняя и внешняя сфера 1.6. Многоядерные комплексы Глава 2. Номенклатура комплексных соединений 2.1. Названия лигандов 2.2. Порядок перечисления лигандов 2.3. Нейтральные комплексы 2.4. Комплексные катионы 2.5. Комплексные анионы 2.6. Мостиковые группы и многоядерные комплексы 2.7. Геометрические изомеры Глава 3. Строение комплексных соединений 3.1. Координационное число 2 3.2. Координационное число 3 3.3. Координационное число 4 3.4. Координационное число 5 3.5. Координационное число 6 и выше
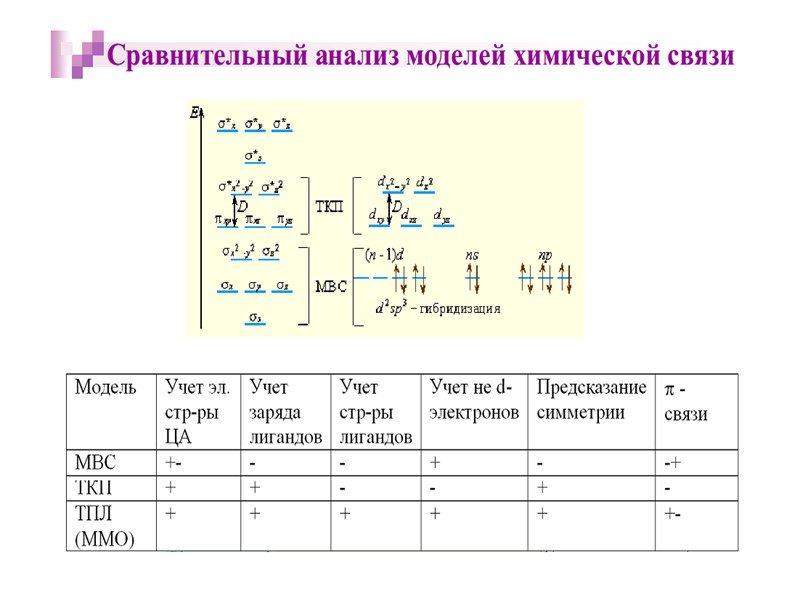
 Глава 4. Изомерия комплексных соединений 4.1. Изомерия лигандов 4.2. Геометрическая изомерия 4.3. Оптическая изомерия 4.4. Сольватная (гидратная) изомерия 4.5. Ионная изомерия Вопросы к 4 главе Глава 5. Устойчивость комплексных соединений в растворе 5.1. Комплексные соединения без внешней сферы 5.2. Отщепление ионов внешней сферы 5.3. Обратимая диссоциация комплексов 5.4. Ступенчатая и полная константы образования 5.5. Прочность комплексов 5.6. Константы нестойкости 5.7. Примеры образования и разрушения комплексов Вопросы к 5 главе Глава 6. Квантовомеханические теории строения комплексов 6.1. Теория валентных связей 6.2. Гибридизация орбиталей и структура комплексов 6.3. Теория кристаллического поля 6.4. Цветность 6.5. ММО для комплексных соединений
Глава 4. Изомерия комплексных соединений 4.1. Изомерия лигандов 4.2. Геометрическая изомерия 4.3. Оптическая изомерия 4.4. Сольватная (гидратная) изомерия 4.5. Ионная изомерия Вопросы к 4 главе Глава 5. Устойчивость комплексных соединений в растворе 5.1. Комплексные соединения без внешней сферы 5.2. Отщепление ионов внешней сферы 5.3. Обратимая диссоциация комплексов 5.4. Ступенчатая и полная константы образования 5.5. Прочность комплексов 5.6. Константы нестойкости 5.7. Примеры образования и разрушения комплексов Вопросы к 5 главе Глава 6. Квантовомеханические теории строения комплексов 6.1. Теория валентных связей 6.2. Гибридизация орбиталей и структура комплексов 6.3. Теория кристаллического поля 6.4. Цветность 6.5. ММО для комплексных соединений
 Глава 7. Типы комплексных соединений 7.1. Аквакомплексы 7.2. Гидроксокомплексы 7.3. Аммиакаты 7.4. Ацидокомплексы 7.5. Анионгалогенаты 7.6. Катионгалогены 7.7. Гидридные комплексы 7.8. Карбонильные комплексы 7.9. p-комплексы 7.10. Хелаты 7.11. Многоядерные комплексы Глава 8. Элементы Периодической системы Д.И. Менделеева: способность к образованию комплексов 8.1. Элементы s-секции 8.2. Элементы p-секции 8.3. Элементы d-секции 8.4. Лантаноиды и актиноиды
Глава 7. Типы комплексных соединений 7.1. Аквакомплексы 7.2. Гидроксокомплексы 7.3. Аммиакаты 7.4. Ацидокомплексы 7.5. Анионгалогенаты 7.6. Катионгалогены 7.7. Гидридные комплексы 7.8. Карбонильные комплексы 7.9. p-комплексы 7.10. Хелаты 7.11. Многоядерные комплексы Глава 8. Элементы Периодической системы Д.И. Менделеева: способность к образованию комплексов 8.1. Элементы s-секции 8.2. Элементы p-секции 8.3. Элементы d-секции 8.4. Лантаноиды и актиноиды

