Л12 - Биоэлементы(все-все).ppt
- Количество слайдов: 48

Химический состав Земли изучает геохимия. Часть земной оболочки, занятую растительными и животными организмами, называют биосферой. Её верхняя граница [тропосфера] на высоте 12– 15 км, а нижняя — литосфера — на глубине до 5 км.

• Около 50% массы земной коры приходится на O, • более 25% — на Si. • 18 элементов — O, Si, Al, Fe, Ca, Na, K, Mg, H, Ti, C, Cl, P, S, N, Mn, F, Ba — составляют 99, 8% • сходство химического состава земной коры и живых организмов. Но: • в земной коре Si [27, 6%], . Al -7, 45%, • а в живых организмах — 1 10– 5%. • Причина: Si. O 2 и Al 2 O 3 практически нерастворимы в воде и не усваиваются живыми организмами. Наоборот: C 0, 35% в коре, а в живых организмах его 21%- положение в ПС- образует -, = и др. связи , ВМС • Увеличение содержания элемента в организме по сравнению с окружающей средой называют биологическим концентрированием элемента.

- Все биогенные элементы можно разделить на три категории: 1. Органогены [они составляют в организме 97, 4%]. С, Н, О, N, Р и S [по Ершову; по другим источникам вместо S берут Са]. Это относительно лёгкие атомы с малыми размерами и небольшим зарядом ядер. Это основной строительный материал, из которого состоят белки, жиры, углеводы, нуклеиновые кислоты.

• II— элементы электролитного фона. • Они обеспечивают электрохимические процессы, ==регулируют осмотическое давление и ряд других жизненных процессов, ионный и кислотно-основной состав биожидкостей. Это К, Na, Cl, Mg, Са и другие элементы. • III— микроэлементы. • Входя в состав ферментов, гормонов, витаминов, биологически активных веществ в качестве комплексообразователей или активаторов, ==микроэлементы участвуют в обмене веществ, тканевом дыхании, размножении, обезвреживании токсических веществ, процессах кроветворения и т. д. Это Fe, I, Cu, As, F, Br, Sr, Ba, Co, Mn, Mo, Zn, V и другие.

• Достаточно распространена следующая классификация: • 1. Макроэлементы [содержание в организме свыше 10– 2%]. • 2. Микроэлементы [содержание в организме от 10– 3 до 10– 5%]. • 3. Ультрамикроэлементы [ниже 10– 5%].

• Органы человека по-разному концентрируют в себе различные химические элементы. • Zn — в поджелудочной железе, • I — в щитовидной железе; • F — в эмали зубов; • Al, As, V — в волосах и ногтях; • Cd, Hg, Mo — в почках; • Sn — в тканях кишечника; • Sr — в предстательной железе, костной ткани; • Ba — в пигментной сетчатке глаза; • Br, Mn, Cr — в гипофизе; • Ca — в костной ткани, зубной ткани.

• В организме массой 70 кг содержится 10 «металлов жизни» : • Са — 1700 г • К — 160 г • Na — 60 г • • • Mg — 42 г Fe — 5 г Zn — 3 г Cu — 0, 2 г Mn, Mo, Co — менее 0, 1 г

• меняется с возрастом: • ===Содержание Cd в почках и Мо в печени к старости повышается. • ===Zn больше всего в периоде полового созревания, а к старости его содержание снижается до минимума. ==С возрастом уменьшается содержание ванадия и хрома

Геохимические провинции — области с аномальным содержанием элементов в почве, воде и воздухе. Это районы с повышенным содержанием стронция [река Уров, Восточная Сибирь], меди [Башкортостан], молибдена [Армения]. йода [на западе Украины], кобальта [Ярославская область]. – Местность, отличающаяся не только геохимическим фоном, но и биологической реакцией, называется биогеохимической провинцией. – эндемические заболевания: – Дефицит фтора вызывает кариес зубов, – дефицит йода — эндемический зоб, – избыток молибдена — эндемическую подагру.

• Биологическая роль элементов в зависимости от их положения в ПС • ===С увеличением заряда ядра атомов увеличивается токсичность и содержание элемента в организме уменьшается, т. к. его соединения плохо усваиваются живыми организмами [сложность электронных конфигураций, малая растворимость соединений]. • ==В организме в значительных количествах содержатся лёгкие элементы s- и р-блоков. • ==d-элементы пятого и шестого периодов, за исключением молибдена, не проявляют положительной физиологической активности. • == f-элементы высокотоксичны.

• Сходство и различие биологического действия связано с электронным строением атомов и ионов • СХОДСТВО обусловливает эффекты замещения элементов в биологических системах ( синергизм и антагонизм) • Например, сходные Li и Na, как правило, синергисты. • Рубидий и цезий могут заместить калий. • Бериллий и магний схожи и они антагонисты. • Ионы Mn 2+, Fe 2+, Co 2+, Ni 2+, Cu 2+ стимулируют кроветворение, у них большое сходство. • Ni, Mn, Fe взаимозамещают друга. • Большую роль играют связи данного элемента с другими. • === р-элементы IIIA группы входят в состав биомолекул, т. к. связываются с атомом кислорода, • == таллий связывается с серой [блокирует SH-группы] и токсичен. • == мышьяк, сурьма и висмут из-за связи с серой - синергисты. • фтор не замещает бром, йод и хлор, • бром, йод и хлор -как синергисты или как антагонисты.

• s-элементы • Водород и его соединения. • в организме человека — 10% [7 кг] по сравнению с его содержанием в земной коре [1%] • Соединения водорода: • вода. • Н 2 О 2 — водородпероксид — побочный продукт метаболизма, образуется при неполном восстановлении кислорода.

IA группа. Щелочные металлы. Na и Li накапливаются во внеклеточной жидкости, калий, рубидий и цезий — во внутриклеточной. Na и Li имеют близкое биологическое действие и чаще являются синергистами. • Na и К, как правило, антагонисты, но могут и замещать друга; доказательство: при увеличении содержания Na в организме усиливается выведение почками калия. • Na и К — макроэлементы. • Натрия [при массе 70 кг] содержится около 60 г. Депонируется в костной ткани. – Калия в организме 160 г • • • Перенос К+ и Na+ через мембрану осуществляется при гидролизе АТФ. При гидролизе 1 молекулы АТФ 3 Na+ выводятся из клетки, а 2 К+ поступают внутрь клетки.

• Роль ионов калия и натрия: • участвуют • в поддержании тонуса скелетных мышц и миокарда, • возникновении мембранного потенциала, • проведении нервных импульсов, • в осмотических явлениях, • являются активаторами ферментов.
![• 0, 9% раствор Na. Cl — изотонический [подкожно, в/в и в клизмах]; • 0, 9% раствор Na. Cl — изотонический [подкожно, в/в и в клизмах];](https://present5.com/presentation/3/-30500059_18306259.pdf-img/-30500059_18306259.pdf-15.jpg)
• 0, 9% раствор Na. Cl — изотонический [подкожно, в/в и в клизмах]; • 3– 10% раствор Na. Cl — гипертонический [примочки для гнойных ран]. • Na. HCO 3 — при коррекции ацидоза. • Na 2 B 4 O 7 10 H 2 O — натрия тетраборат — антисептик.

• KCl применяется при гипокалиемии, при нарушениях сердечного ритма. • СН 3 СООК — мочегонное средство. • С 6 Н 6 О 2 N 2 СООК — оротат калия используется при заболеваниях печени, при дистрофии миокарда.

• • • • s-элементы IIA группы. Щелочноземельные металлы. Во IIА группу ПСЭ входят Ве, Mg, Ca, Sr, Ba, Ra. Mg и Ве — антагонисты. роль Mg: ион Mg 2+ является комплексообразователем в хлорофилле. Внутри клеток активной формой АТФ является комплекс Mg. АТФ 2–, от концентрации Mg зависит устойчивость рибосом. Чаще Са и Mg — антагонисты, реже синергисты. Ион Mg 2+ активирует внутриклеточные ферменты, ион Са 2+ — внеклеточные. Са 2+, Ва 2+ и Sr 2+ — синергисты. Уровская болезнь — вытеснение ионов Са ионами стронция — размягчение костей. Ва 2+ конкурирует с К+, имея одинаковый радиус; вызывает гипокалиемию, инактивирует ферменты.

• Са 2+. • Кристаллы кости относятся к гидроксилапатитам, имеют форму пластин или палочек и следующий химический состав: Са 10[РО 4]6[ОН]2. • Другая часть минеральной фазы костной ткани представлена аморфным фосфатом кальция Са 3[РО 4]2. Аморфный фосфат Са преобладает в раннем возрасте, в зрелом возрасте в кости преобладает гидроксилапатит — очень твёрдое, труднорастворимое соединение. • ==кристаллизации и минерализации костной ткани способствует цитрат, он образует комплексные соединения с солями Са и Р и обеспечивает повышение концентрации их в ткани. • ===При оссификации в пространстве между коллагеновыми волокнами откладывается гидроксилапатит.

• Mg. SО 4 7 Н 2 О — седативное и слабительное. • 2 Mg. Si. O 3 Mg[HSi. O 3]2 — тальк — адсорбирующее средство, компонент паст и таблеток. • Кальция гидроксид — пломбировочный материал. • Са. Cl 2 6 Н 2 О используется при отравлении солями магния, фторидами, щавелевой кислотой, как кровоостанавливающее средство, при аллергических заболеваниях. • Глюконат кальция, лактат кальция применяют внутрь в тех же случаях, что и хлорид кальция. • Са. СО 3 — антацидное средство, а также входит в состав зубных порошков. • Са. SO 4. ½Н 2 О — гипсовые повязки при переломах костей. • Ва. SО 4 — контрастное вещество.

• Биологическая роль щелочноземельных металлов: • Ве — токсичный примесный ультрамикроэлемент [прочные связи с биолигандами], сильный ингибитор ряда ферментов. • Mg [в организме 20 г [0, 027%]] — дентин, эмаль зубов, кости, а также другие органы. • Са [в организме 1700 г] — • строительный материал костей и зубов, свёртывание крови, передача нервных импульсов, сокращение мышц, работа сердца. • Sr [10– 3%] может концентрироваться в костях, замещая Са, особенно в областях интенсивного остеогенеза. Избыток ведёт к размягчению костей [уровская болезнь], вызывает патологические изменения не только в скелете, но и в костном мозге, нарушая кроветворение. • Ва и Ra — примесные микроэлементы.

d-элементы - имеют незавершённый предвнешний d‑слой и переменную валентность - с высшей степенью окисления имеют кислотные и окислительные свойства, с низшей- основные и восстановительные. Амфотерные свойства характерны для соединений с промежуточными степенями окисления ( и для живых организмов). - d-элементы образуют комплексы с ОН, SH, COO, NH 2 -группами белков, аминокислот
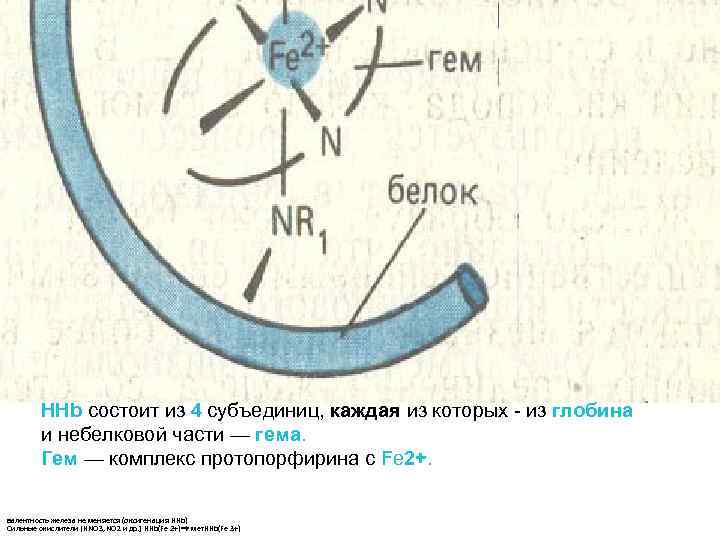
Fe HHb состоит из 4 субъединиц, каждая из которых - из глобина и небелковой части — гема. Гем — комплекс протопорфирина с Fе 2+. валентность железа не меняется (оксигенация HHb) Сильные окислители [HNO 3, NO 2 и др. ] HHb(Fe 2+) мет. HHb(Fe 3+)

HHb(Fe 2+ ) +O 2 HHb(Fe 2+ )O 2 Дезоксигемоглобин- оксигемоглобин HHb. O 2 + CO HHb. CO + O 2 HHb(Fe 2+ ) + CO HHb(Fe 2+ )CO Карбоксигемоглобин HHb(Fe 2+ ) HHb(Fe 3+ ) (с НNO 3, NO 2) метгемоглобин

• Железо организма • • внутриклеточное • 1. Гемопротеиды • • • [гемоглобин, миоглобин, ферменты ( ферменты цитохромы, каталаза, пероксидаза). 2. Ферменты негеминовой группы [сукцинатдегидрогеназа]. 3. Ферритин [запасные белки]. 4. Fe, рыхло связанное с белками , рыхло связанное и другими органическими соединениями внеклеточное трансферрин(транспорт Fe) трансферрин
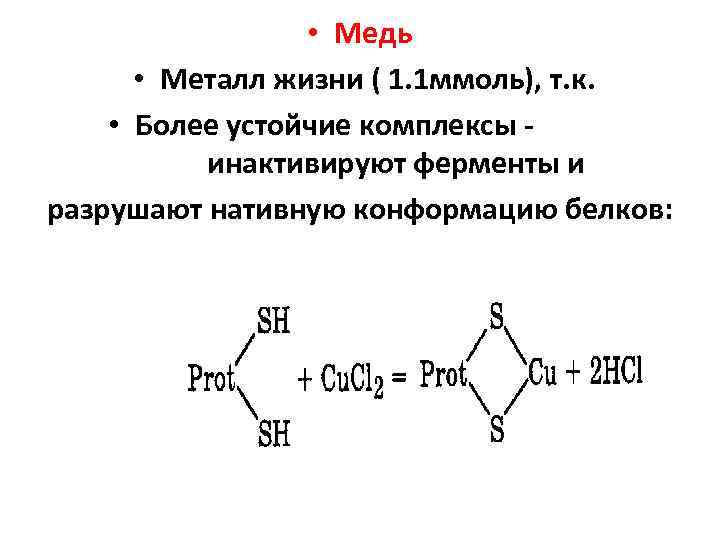
• Медь • Металл жизни ( 1. 1 ммоль), т. к. • Более устойчие комплексы инактивируют ферменты и разрушают нативную конформацию белков:
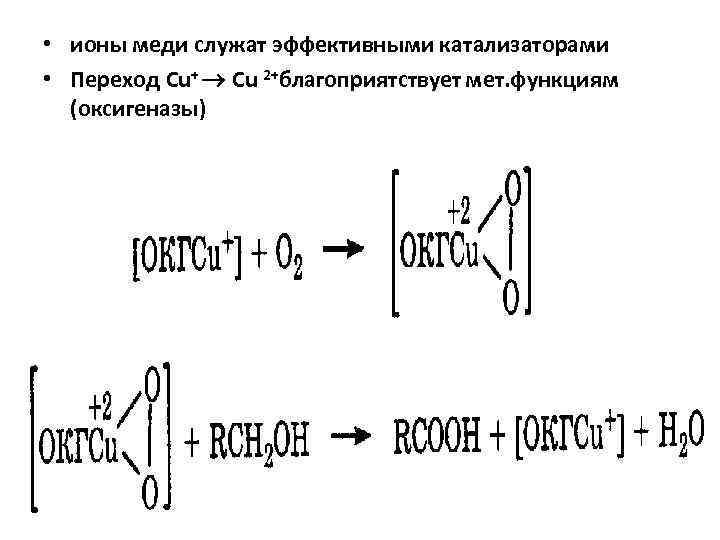
• ионы меди служат эффективными катализаторами • Переход Cu+ Cu 2+благоприятствует мет. функциям (оксигеназы)
![супероксиддисмутаза [СОДСи 2+ ] и цитохромоксидаза [Fе 2+ЦХОСи+] супероксиддисмутаза [СОДСи 2+ ] и цитохромоксидаза [Fе 2+ЦХОСи+]](https://present5.com/presentation/3/-30500059_18306259.pdf-img/-30500059_18306259.pdf-27.jpg)
супероксиддисмутаза [СОДСи 2+ ] и цитохромоксидаза [Fе 2+ЦХОСи+]
![Белок церулоплазмин [ЦПСи 2+] • -резервуар для Cu, • -транспортную функцию Cu регулируя баланс Белок церулоплазмин [ЦПСи 2+] • -резервуар для Cu, • -транспортную функцию Cu регулируя баланс](https://present5.com/presentation/3/-30500059_18306259.pdf-img/-30500059_18306259.pdf-28.jpg)
Белок церулоплазмин [ЦПСи 2+] • -резервуар для Cu, • -транспортную функцию Cu регулируя баланс меди и обеспечивая выведение избытка меди из организма • -катализирует окисление Fe 2+ в Fe 3+, участвуя в кроветворении:

• Ag • • • c. o. +1 -10 -8 ммоль/л Аg в Н 2 О - протаргол (белковый комплекс Аg) - колларгол (коллоидное Аg) - ляпис Ag. NO 3 Антидот - Na. Cl Ag. Cl.

Zn находится в полости комплекса и является компонентом активного центра фермента. • - влияет на процесс дыхания: • -влияет на углеводный обмен. • - Цинк активирует биосинтез витаминов С и В. • - стимулирует фагоцитарную активность лейкоцитов.

• • • Hg • блокирует 100 S-H- содержащих ферментов • Hg. O, Hg 2 O • СH 3 Hg+ Hg. Cl 2 — сулема, очень ядовита. В виде раствора 1: 1000 применяется для дезинфекции. Hg 2 Cl 2 — каломель (в виде мази) Детоксиканты Hg: - белковые растворы, - Na 2 S 2 O 3 5 H 2 O — тиосульфат натрия, - комплексоны.

• • • • Р-элементы. C, N, P, O, S — органогены а [F, Cl, I] -микроэлементы. Бор Ортоборная кислота Н 3 ВО 3 - и бура —антисептики: Na 2 B 4 O 7 + 7 H 2 O 4 H 3 BO 3 + 2 Na. OH Na. BO 2 + Al(OH)3 Избыток бора вреден, т. к. угнетает амилазы, протеиназы, уменьшает активность адреналина Алюминий + влияет на развитие эпителиальной и соединительной тканей, на регенерацию костных тканей, на обмен фосфора. тормозит синтез гемоглобина и катализирует реакцию трансаминирования. Избыток Al тормозит синтез гемоглобина, т. к. блокирует активные центры ферментов, участвующих в кроветворении. Al катализирует реакцию трансаминирования.

1 V группа - С, Si, Ge, Sn, Pb. С -21, 15%, органоген № 1 Антидот при отравлениях СО - восстановл. Fe Si кремний влияет на формирование соединительной и эпителиальной ткани в организме, • Si попадает в организм через пищеварительный тракт и через лёгкие. • При вдыхании пыли, содержащей Si. O 2, возникает силикоз( образуется гель поликремниевой кислоты, что ведёт к гибели клеток) • • •
![• • • ]. • Pb с. о. +2 и +4, образует К. • • • ]. • Pb с. о. +2 и +4, образует К.](https://present5.com/presentation/3/-30500059_18306259.pdf-img/-30500059_18306259.pdf-34.jpg)
• • • ]. • Pb с. о. +2 и +4, образует К. С. ( с SH-группами белков) Очень токсичен, особенно его органические соединения. Pb влияет: -на синтез белка, - кроветворение, - энергетический баланс клетки и её генетический аппарат [является слабым мутагеном]. - денатурацию белка, - на развитие кариеса, инактивирует ферменты, нарушает синтез гемоглобина [Pb+4 окисляет Fe 2+ в Fe 3+ ]. Детоксиканты : молоко, белковые растворы, тиосульфат натрия, комплексоны.

• VA группа ПСЭ -N, P, As • N- 3, 1% • связывает неорганическую и органическую части молекулы. • Растения усваивают нитраты ион аммония глутаминовая к-та 19 альфа аминокислот

• Аммиак —токсичный газ • при алкалозе в качестве мочегонного средства применяют хлорид аммония NH 4 C 1. • NH 4 OH применяют при обмороках для возбуждения дыхания. • образует прочные аммиачные комплексы( токсичность аммиака). • NH 4 Cl — отхаркивающее и мочегонное средство. • Na. NO 2 — сосудорасширяющее средство при стенокардии и мигрени.

• N 20 (закись азота) - несолеобразующий оксид, используется для наркоза. • NO - несолеобразующий токсичный оксид образует нитрозогемоглобин • N 203 - кислотный оксид N 2 O 3 + Н 2 О = 2 HNO 2
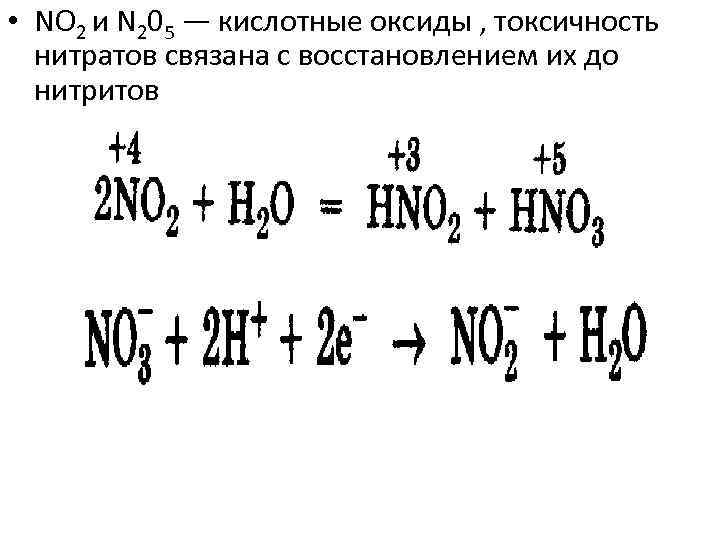
• NO 2 и N 205 — кислотные оксиды , токсичность нитратов связана с восстановлением их до нитритов
![Р- Макроэлемент [0, 95%], органоген. === Входит в состав: АТФ и креатинфосфата, белков, нуклеиновых Р- Макроэлемент [0, 95%], органоген. === Входит в состав: АТФ и креатинфосфата, белков, нуклеиновых](https://present5.com/presentation/3/-30500059_18306259.pdf-img/-30500059_18306259.pdf-39.jpg)
Р- Макроэлемент [0, 95%], органоген. === Входит в состав: АТФ и креатинфосфата, белков, нуклеиновых кислот, нуклеотидов , костей [кальция ортофосфат, гидроксилапатит], зубов [гидроксилапатит, фторапатит]. • === Важную роль выполняет фосфатная буферная система. • ===Сахара и жирные кислоты используются организмом только после их фосфорилирования. • === Энергия АТФ необходима для сокращения мышц, в том числе сердечной мышцы, проведения нервного импульса, биохимических реакций. • • •

–P – Белый фосфор очень токсичен – Уменьшение содержания неорганического фосфора ведёт к увеличению содержания Са в крови [антагонизм]. – Фосфорорганические соединения — нервнопаралитические яды [ОВ]. – очень токсичный гидрид фосфора РН 3
![• • Макроэлемент [62%]. - O - окисление питательных веществ в организме, окислительно-- • • Макроэлемент [62%]. - O - окисление питательных веществ в организме, окислительно--](https://present5.com/presentation/3/-30500059_18306259.pdf-img/-30500059_18306259.pdf-41.jpg)
• • Макроэлемент [62%]. - O - окисление питательных веществ в организме, окислительно-- восстановительные реакции. Уменьшение содержания О 2 в организме понижает его защитные свойства [в фагоцитах О 2 превращается в О 2– — супероксид-ион, который инициирует радикальноцепные процессы окисления инородных органических веществ]. СОД 2 О 2·¯ +2 Н+ → Н 2 О 2+О 2 каталаза 2 Н 2 О 2 2 Н 2 О+О 2. • S • R 1—S—S—R 2 R 1 SH + R 2 SH
![• Озон — сильный окислитель [дезинфекция помещений, обеззараживание воздуха и очистка питьевой воды]; • Озон — сильный окислитель [дезинфекция помещений, обеззараживание воздуха и очистка питьевой воды];](https://present5.com/presentation/3/-30500059_18306259.pdf-img/-30500059_18306259.pdf-42.jpg)
• Озон — сильный окислитель [дезинфекция помещений, обеззараживание воздуха и очистка питьевой воды]; благотворно действует на лёгочных больных [в небольших количествах]. • Озоносфера поддерживает тепловой режим планеты и поглощает ультрафиолетовое излучение Солнца. • Слой озона толщиной в 3 мм [при давлении на уровне моря] ослабляет ультрафиолетовое излучение в 1040 раз. • Под действием повышенных доз УФ-излучения происходит повреждение нуклеиновых кислот, приводящее к возникновению мутаций.
![• • • • S -Макроэлемент [0, 16%], . Суточная потребность 4 -5 • • • • S -Макроэлемент [0, 16%], . Суточная потребность 4 -5](https://present5.com/presentation/3/-30500059_18306259.pdf-img/-30500059_18306259.pdf-43.jpg)
• • • • S -Макроэлемент [0, 16%], . Суточная потребность 4 -5 г. Входит в состав +++белков, гормонов, витаминов. +++тиоловых соединений, участвующих в окислительно-восстановительных реакциях. +++ Известны три серусодержащих аминокислоты: цистин, цистеин и метионин. +++ : инсулина, глутатиона, витамина В 1, липоевой кислоты 2 Н +++Обратимый переход R 1—S—S—R 2 R 1 SH + R 2 SH защищает организм от радиационных поражений. +++Образование дисульфидных мостиков стабилизирует и определяет третичную структуру белка. +++Образующаяся в организме Н 2 SО 4 участвует в обезвреживании ядовитых соединений: фенола вырабатываемых в кишечнике из аминокислот микробами. ++++ В соединении с серной кислотой [в виде конъюгатов] выводятся чужеродные вещества.

• ++++. Приём серы внутрь способствует рассасыванию нарывов, • +++++ сера используется как слабительное средство. • +++++В виде мазей и присыпок применяется как антимикробное средство при лечении кожных заболеваний. • Na 2 S 2 O 3 5 H 2 O — тиосульфат натрия — антитоксическое, противовоспалительноесредство. • Na 2 S 2 O 8 — персульфат натрия — антигипоксическое средство. • Na 2 SO 4 10 H 2 O — сульфат натрия — слабительное. • Mg. SO 4 7 H 2 O — сульфат магния — понижает артериальное давление. • Ca. SO 4 2 H 2 O — гипс — используется в хирургической практике. • Cu. SO 4 5 H 2 O — сульфат меди — при анемии. • Fe. SO 4 7 H 2 O — сульфат железа — при анемии.
![• Хлор, фтор, бром, йод • Cl — макроэлемент [0, 15%], остальные — • Хлор, фтор, бром, йод • Cl — макроэлемент [0, 15%], остальные —](https://present5.com/presentation/3/-30500059_18306259.pdf-img/-30500059_18306259.pdf-45.jpg)
• Хлор, фтор, бром, йод • Cl — макроэлемент [0, 15%], остальные — микроэлементы [10– 5%]. Фтор • В организме фтора 7 мг. Больше всего фтора в эмали — около 0, 01% [труднорастворимый фторапатит Са 5[РО 4]3 F]: • Са 5[РО 4]3 ОН + F– Са 5[РО 4]3 F + OH– • ускоряя процесс реминерализации [образования кристаллов]: • 10 Са 2+ + 6 РО 4 3– + 2 F– = 3 Са 3[РО 4]2 Са. F 2 • Для питьевой воды добавляют Na. F до нормы [1 мг/л]. Недостаток F приводит к кариесу. • Если содержание F будет выше 1, 2 мг/л, , кости деформируются [развивается флюороз]. • Механизм токсического действия фтора — образование комплексных соединений с кальцием, магнием и другими элементами — активаторами ферментов, вследствие чего фтор угнетает активность ряда ферментов. • Избыток фтора угнетает функцию щитовидной железы, т. к. фтор — конкурент йода в синтезе гормонов щитовидной железы.

• • • Хлор В организме человека 100 г хлора ионы хлора: - активируют ферменты [амилаза слюны], - создают благоприятную среду для действия ферментов желудочного сока, - обеспечивают ионные потоки через клеточные мембраны, = участвуют в поддержании осмотического равновесия Суточная потребность в Na. Cl составляет 5– 10 г. Na. Cl необходим для выработки НСl в желудке. НСl, помимо участия в пищеварении, уничтожает бактерии холеры, брюшного тифа. Элементарный хлор — высокотоксичный газ.
![• Бром • В организме всего 7 мг [10– 5%]. • Локализуется в • Бром • В организме всего 7 мг [10– 5%]. • Локализуется в](https://present5.com/presentation/3/-30500059_18306259.pdf-img/-30500059_18306259.pdf-47.jpg)
• Бром • В организме всего 7 мг [10– 5%]. • Локализуется в железах внутренней секреции [в гипофизе]. • Роль Br не ясна. • Наиболее чувствительна к Br ЦНС. Бромид-ионы накапливаются в отделах мозга и действуют успокаивающе при повышенной возбудимости. Восстанавливается равновесие между процессами возбуждения и торможения. • Br– может замещать Cl– и I–, он выводится очень медленно. И хотя токсичность его невелика, но накопление может вызвать отравление — «бромизм» .
![• Йод • . В организме 25 мг I [4 10– 5%], — • Йод • . В организме 25 мг I [4 10– 5%], —](https://present5.com/presentation/3/-30500059_18306259.pdf-img/-30500059_18306259.pdf-48.jpg)
• Йод • . В организме 25 мг I [4 10– 5%], — в щитовидной железе в виде гормонов • Щитовидная железа секретирует гормоны, которые влияют на обмен веществ, теплообразование, поглощение кислорода. • Гипотиреоз может быть связан: а/ с уменьшением способности связывать и накапливать йодид-ионы; б/ с недостатком в пище йода [эндемический зоб]. • KI применяют и при гипо-, и при гипертиреозе. • При эндемическом зобе йодид-ионы используются для синтеза гормонов, при гипертиреозе йодид-ионы тормозят йодирование тирозина йодом. • 5% спиртовой раствор I 2 — антисептическое средство. • Раствор йода в йодистом калии [раствор Люголя] применяется для смазывания слизистой оболочки гортани. • Радиоактивный изотоп йода 131 I применяется для диагностических целей при нарушениях работы щитовидной железы, для диагностики опухолей мозга. • Йодиды окисляются кислородом при обычном освещении: • h • 2 KI + 1/2 O 2 + H 2 O I 2 + 2 KOH
Л12 - Биоэлементы(все-все).ppt