5-ВОСПАЛЕНИЕ И РЕПАРАЦИЯ.ppt
- Количество слайдов: 99
 ВОСПАЛЕНИЕ И РЕПАРАЦИЯ. ОСТРОЕ ВОСПAЛЕНИЕ. ИСХОДЫ ВОСПAЛЕНИЯ. РЕПАРАЦИЯ.
ВОСПАЛЕНИЕ И РЕПАРАЦИЯ. ОСТРОЕ ВОСПAЛЕНИЕ. ИСХОДЫ ВОСПAЛЕНИЯ. РЕПАРАЦИЯ.
 Воспаление один из наиболее древних и распространенных патологических процессов, лежащий в основе многих заболеваний человека. § Как общепатологический процесс воспалительная реакция появляется только в многоклеточных организмах, имеющих сосудистую систему. § Терминологически воспаление обозначается прибавлением к корню названия органа суффикса "ит". Например, воспаление миокарда миокардит, почек нефрит, печени – гепатит.
Воспаление один из наиболее древних и распространенных патологических процессов, лежащий в основе многих заболеваний человека. § Как общепатологический процесс воспалительная реакция появляется только в многоклеточных организмах, имеющих сосудистую систему. § Терминологически воспаление обозначается прибавлением к корню названия органа суффикса "ит". Например, воспаление миокарда миокардит, почек нефрит, печени – гепатит.
 Воспаление комплексный, местный и общий патологический процесс, возникающий в ответ на повреждение или действие патогенного раздражителя и проявляющийся в реакциях, направленных на устранение продуктов повреждения, а если возможно, то и агентов (раздражителей), а также приводящий к максимальному для данных условий восстановлению в зоне повреждения. § Воспаление направлено на ограничение очага повреждения, что препятствует распространению повреждающего фактора, а также на элиминацию последнего и погибших клеток с восстановлением поврежденных тканей.
Воспаление комплексный, местный и общий патологический процесс, возникающий в ответ на повреждение или действие патогенного раздражителя и проявляющийся в реакциях, направленных на устранение продуктов повреждения, а если возможно, то и агентов (раздражителей), а также приводящий к максимальному для данных условий восстановлению в зоне повреждения. § Воспаление направлено на ограничение очага повреждения, что препятствует распространению повреждающего фактора, а также на элиминацию последнего и погибших клеток с восстановлением поврежденных тканей.
 Этиология воспаления Оно может быть вызвано экзогенными и эндогенными факторами различного происхождения. § Среди экзогенных факторов, способных индуцировать воспаление, наиболее важное значение имеют следующие: токсические, химические агенты (химические вещества, в том числе лекарства, токсины и яды); физические факторы (воздействие высоких и низких температур, электричества, лучевой энергии, пыли, аэрозолей, травма); микробы и их метаболиты (вирусы, микоплазмы, бактерии, грибы, животные паразиты
Этиология воспаления Оно может быть вызвано экзогенными и эндогенными факторами различного происхождения. § Среди экзогенных факторов, способных индуцировать воспаление, наиболее важное значение имеют следующие: токсические, химические агенты (химические вещества, в том числе лекарства, токсины и яды); физические факторы (воздействие высоких и низких температур, электричества, лучевой энергии, пыли, аэрозолей, травма); микробы и их метаболиты (вирусы, микоплазмы, бактерии, грибы, животные паразиты
 Среди эндогенных факторов, вызывающих воспалительную реакцию в месте их действия, наиболее важны следующие: ишемия (воспаление на границе с зоной ишемического некроза); токсические агенты, образующиеся при некоторых заболеваниях (соли мочевой кислоты при подагре, мочевина и ее метаболиты при уремии); микробы сапрофиты и их метаболиты в условиях иммунодепрессии (пневмонии, вызванные аутогенной флорой); иммунопатологические реакции (реакции гиперчувствительности, аутоиммунные реакции), сопровождающиеся так называемым иммунным воспалением. Несомненное значение в развитии воспалительной реакции имеет ряд генетических и метаболических нарушений.
Среди эндогенных факторов, вызывающих воспалительную реакцию в месте их действия, наиболее важны следующие: ишемия (воспаление на границе с зоной ишемического некроза); токсические агенты, образующиеся при некоторых заболеваниях (соли мочевой кислоты при подагре, мочевина и ее метаболиты при уремии); микробы сапрофиты и их метаболиты в условиях иммунодепрессии (пневмонии, вызванные аутогенной флорой); иммунопатологические реакции (реакции гиперчувствительности, аутоиммунные реакции), сопровождающиеся так называемым иммунным воспалением. Несомненное значение в развитии воспалительной реакции имеет ряд генетических и метаболических нарушений.
 Фазы воспалительных реакций Воспалительные реакции разыгрываются в любой ткани и затрагивают все ее компоненты: паренхиму органа, кровеносные сосуды, циркулирующие в кровотоке клетки, плазму крови, лимфатические сосуды и лимфу, клетки соединительной ткани и внеклеточный матрикс. § Воспаление является динамичным, фазовым процессом, конечная цель которого заключается в элиминации повреждающего агента и репарации тканей. Существуют различные подходы в выделении фаз воспаления. Мы придерживаемся отечественной классификации фаз воспаления, согласно которой воспалительная реакция проходит три последовательные фазы: 1 повреждения, или альтерации; 2 экссудации; 3 пролиферации и дифференцировки клеток. § Наиболее четко и последовательно фазы воспаления представлены при острой его форме, продолжительность которой исчисляется днями и которая заканчивается восстановлением целостности ткани репарацией.
Фазы воспалительных реакций Воспалительные реакции разыгрываются в любой ткани и затрагивают все ее компоненты: паренхиму органа, кровеносные сосуды, циркулирующие в кровотоке клетки, плазму крови, лимфатические сосуды и лимфу, клетки соединительной ткани и внеклеточный матрикс. § Воспаление является динамичным, фазовым процессом, конечная цель которого заключается в элиминации повреждающего агента и репарации тканей. Существуют различные подходы в выделении фаз воспаления. Мы придерживаемся отечественной классификации фаз воспаления, согласно которой воспалительная реакция проходит три последовательные фазы: 1 повреждения, или альтерации; 2 экссудации; 3 пролиферации и дифференцировки клеток. § Наиболее четко и последовательно фазы воспаления представлены при острой его форме, продолжительность которой исчисляется днями и которая заканчивается восстановлением целостности ткани репарацией.
 1 фаза Альтерация (повреждение) ткани и клеток, в том числе клеток носителей медиаторов воспаления химических веществ, регулирующих воспаление (тучных клеток, макрофагов, тромбоцитов). § Альтерация обеспечивает инициальный выброс и накопление медиаторов воспаления в тканях. Нередко альтерация и накопление медиаторов в очаге воспаления занимают очень короткий промежуток времени.
1 фаза Альтерация (повреждение) ткани и клеток, в том числе клеток носителей медиаторов воспаления химических веществ, регулирующих воспаление (тучных клеток, макрофагов, тромбоцитов). § Альтерация обеспечивает инициальный выброс и накопление медиаторов воспаления в тканях. Нередко альтерация и накопление медиаторов в очаге воспаления занимают очень короткий промежуток времени.
 2 фаза Экссудативная фаза воспаления, которая включает в себя реакцию микроциркуляторного русла, выход жидкой части крови и клеток на поле воспаления и клеточные реакции. Выделяют основные компоненты фазы экссудации: 1 изменения кровотока в сосудах микроциркуляторного русла (артериолах, капиллярах и венулах) в ответ на инициальное повреждение; 2 образование жидкой части воспалительного экссудата за счет повышения тканево сосудистой проницаемости в результате структурных перестроек в микроциркуляторном русле; 3 эмиграция клеточных элементов и фагоцитоз в очаге воспаления.
2 фаза Экссудативная фаза воспаления, которая включает в себя реакцию микроциркуляторного русла, выход жидкой части крови и клеток на поле воспаления и клеточные реакции. Выделяют основные компоненты фазы экссудации: 1 изменения кровотока в сосудах микроциркуляторного русла (артериолах, капиллярах и венулах) в ответ на инициальное повреждение; 2 образование жидкой части воспалительного экссудата за счет повышения тканево сосудистой проницаемости в результате структурных перестроек в микроциркуляторном русле; 3 эмиграция клеточных элементов и фагоцитоз в очаге воспаления.
 Изменение кровотока в сосудах микроциркуляторного русла – кратковременный спазм артериол; – приходящее ему на смену расширение артериол, приводящее к увеличению и замедлению кровотока в очаге воспаления (воспалительной артериальной гиперемии); – повышение тканево сосудистой проницаемости с формированием воспалительного отека; – краевое стояние лейкоцитов в кровотоке на фоне его замедления.
Изменение кровотока в сосудах микроциркуляторного русла – кратковременный спазм артериол; – приходящее ему на смену расширение артериол, приводящее к увеличению и замедлению кровотока в очаге воспаления (воспалительной артериальной гиперемии); – повышение тканево сосудистой проницаемости с формированием воспалительного отека; – краевое стояние лейкоцитов в кровотоке на фоне его замедления.
 Образование жидкой части воспалительного экссудата Этот процесс происходит за счет повышения тканево сосудистой проницаемости в результате структурных перестроек в микроциркуляторном русле обеспечивается согласно закону Старлинга увеличением гидростатического давления в сосудах микроициркуляции с одновременным понижением в них осмотического давления в результате выхода в ткани плазменных белков в сочетании с повышением проницаемости стенок сосудов. § При этом в очаге воспаления скапливается воспалительный экссудат жидкость с высоким содержанием белка и детрита, имеющая относительную массу более 1020. В дальнейшем в экссудате в результате миграции из кровотока появляются и клеточные элементы. Экссудат накапливается в полостях органов, просветах трубчатых структур и желез, полостях, возникших в результате вторичного лизиса ткани нейтрофильными лейкоцитами. Накопление гнойного экссудата в предсуществующих полостях тела называется эмпиемой (эмпиема плевры, эмпиема желчного пузыря). Транссудат образуется в результате ультрафильтрации плазмы при повышении гидростатического давления, содержащего небольшое количество низкомолекулярных белков и имеющего низкую относительную массу (менее 1020).
Образование жидкой части воспалительного экссудата Этот процесс происходит за счет повышения тканево сосудистой проницаемости в результате структурных перестроек в микроциркуляторном русле обеспечивается согласно закону Старлинга увеличением гидростатического давления в сосудах микроициркуляции с одновременным понижением в них осмотического давления в результате выхода в ткани плазменных белков в сочетании с повышением проницаемости стенок сосудов. § При этом в очаге воспаления скапливается воспалительный экссудат жидкость с высоким содержанием белка и детрита, имеющая относительную массу более 1020. В дальнейшем в экссудате в результате миграции из кровотока появляются и клеточные элементы. Экссудат накапливается в полостях органов, просветах трубчатых структур и желез, полостях, возникших в результате вторичного лизиса ткани нейтрофильными лейкоцитами. Накопление гнойного экссудата в предсуществующих полостях тела называется эмпиемой (эмпиема плевры, эмпиема желчного пузыря). Транссудат образуется в результате ультрафильтрации плазмы при повышении гидростатического давления, содержащего небольшое количество низкомолекулярных белков и имеющего низкую относительную массу (менее 1020).
 Образование жидкой части экссудата происходит в результате повышения проницаемости эндотелия сосудов в очаге воспаления в связи со следующими событиями: § § § кратковременным сокращением эндотелия в венулах (диаметром 20 60 мкм) с расширением межклеточных промежутков при воздействии гистамина и некоторых других медиаторов, происходящее на ранних этапах воспалительной реакции и имеющее обратимый характер; сокращением эндотелиальных клеток за счет реорганизации их цитоскелета и межклеточных контактов под действием ИЛ I и ФНО , что приводит к относительно более стойкому расширению межэндотелиальных промежутков; непосредственным повреждением эндотелия, заканчивающимся его некрозом и слущиванием, что обычно происходит при сильном повреждении, захватывает все участки микроциркуляции в очаге воспаления и заканчивается тромбозом; повреждением эндотелия, вызванным активными формами кислорода и протеазами, генерируемыми лейкоцитами в момент их эмиграции из кровотока в очаг воспаления; повышением эндоцитоза (трансцитоза) жидкости эндотелиальными клетками под воздействием некоторых цитокинов; экссудацией из вновь образующихся капилляров, которые обладают повышенной проницаемостью.
Образование жидкой части экссудата происходит в результате повышения проницаемости эндотелия сосудов в очаге воспаления в связи со следующими событиями: § § § кратковременным сокращением эндотелия в венулах (диаметром 20 60 мкм) с расширением межклеточных промежутков при воздействии гистамина и некоторых других медиаторов, происходящее на ранних этапах воспалительной реакции и имеющее обратимый характер; сокращением эндотелиальных клеток за счет реорганизации их цитоскелета и межклеточных контактов под действием ИЛ I и ФНО , что приводит к относительно более стойкому расширению межэндотелиальных промежутков; непосредственным повреждением эндотелия, заканчивающимся его некрозом и слущиванием, что обычно происходит при сильном повреждении, захватывает все участки микроциркуляции в очаге воспаления и заканчивается тромбозом; повреждением эндотелия, вызванным активными формами кислорода и протеазами, генерируемыми лейкоцитами в момент их эмиграции из кровотока в очаг воспаления; повышением эндоцитоза (трансцитоза) жидкости эндотелиальными клетками под воздействием некоторых цитокинов; экссудацией из вновь образующихся капилляров, которые обладают повышенной проницаемостью.
 Эмиграция клеточных элементов и фагоцитоз Накопление лейкоцитов в очаге воспаления проходит несколько этапов: § краевое стояние лейкоцитов в кровотоке, прокатывание лейкоцитов по поверхности эндотелиальных клеток и адгезия лейкоцитов к поверхности последних; § миграция лейкоцитов сквозь сосудистую стенку (лейкодиапедез); § миграция лейкоцитов в интерстициальную ткань в очаге воспаления по направлению разницы градиентов концентрации определенных химических веществ (хемотаксис).
Эмиграция клеточных элементов и фагоцитоз Накопление лейкоцитов в очаге воспаления проходит несколько этапов: § краевое стояние лейкоцитов в кровотоке, прокатывание лейкоцитов по поверхности эндотелиальных клеток и адгезия лейкоцитов к поверхности последних; § миграция лейкоцитов сквозь сосудистую стенку (лейкодиапедез); § миграция лейкоцитов в интерстициальную ткань в очаге воспаления по направлению разницы градиентов концентрации определенных химических веществ (хемотаксис).
 § Прокатывание лейкоцитов по поверхности эндотелиальных клеток и адгезия лейкоцитов к их поверхности происходят за счет лигандрецепторных взаимодействий адгезивных молекул, находящихся на поверхности лейкоцитов (лиганды к селектинам Р и Е, интегрины CD 11/CD 18 и YLA 4; L селектин), адгезивных молекул на эндотелиальных клетках (селектинов Р и Е, иммуноглобулинов ICAM I и VСАМ 1). Адгезия лейкоцитов осуществляется путем: перехода адгезивных молекул из цитоплазматических структур на поверхность эндотелиальных клеток, как это происходит с Р селектином при воздействии гистамина; индукции и усиления экспрессии адгезивных молекул на поверхности эндотелия под влиянием ИЛ 1 и ФНО; увеличения силы связывания интегринов лейкоцитов с соответствующими адгезивными молекулами эндотелия, что делает такие связи прочными и подготавливает условия для следующего этапа диапедеза лейкоцитов.
§ Прокатывание лейкоцитов по поверхности эндотелиальных клеток и адгезия лейкоцитов к их поверхности происходят за счет лигандрецепторных взаимодействий адгезивных молекул, находящихся на поверхности лейкоцитов (лиганды к селектинам Р и Е, интегрины CD 11/CD 18 и YLA 4; L селектин), адгезивных молекул на эндотелиальных клетках (селектинов Р и Е, иммуноглобулинов ICAM I и VСАМ 1). Адгезия лейкоцитов осуществляется путем: перехода адгезивных молекул из цитоплазматических структур на поверхность эндотелиальных клеток, как это происходит с Р селектином при воздействии гистамина; индукции и усиления экспрессии адгезивных молекул на поверхности эндотелия под влиянием ИЛ 1 и ФНО; увеличения силы связывания интегринов лейкоцитов с соответствующими адгезивными молекулами эндотелия, что делает такие связи прочными и подготавливает условия для следующего этапа диапедеза лейкоцитов.
 § Миграция лейкоцитов всех типов сквозь сосудистую стенку происходит в области межклеточных контактов эндотелиальных клеток. Базальную мембрану лейкоциты преодолевают благодаря выделению разрушающих ее нейтральных протеаз. § Хемотаксис, т. е. лейкоциты движутся в очаге воспаления в направлении нарастания градиента концентрации хемотаксических агентов. Хемотаксис лейкоцитов обеспечивается лигандрецепторными взаимодействиями между хемотаксическими агентами, находящимися в очаге воспаления, и соответствующими рецепторами на поверхности лейкоцитов. Такое взаимодействие приводит к синтезу вторичных мессенджеров, активации фосфолипазы С и протеинкиназы С, возрастанию концентрации внутриклеточного Са и контрактильных элементов, необходимых для движения лейкоцитов. Первыми в очаг воспаления приходят нейтрофильные лейкоциты, затем моноциты и лимфоциты. § Активация нейтрофильных лейкоцитов индуцируется хемотаксическими агентами и включает такие процессы, как их дегрануляция и секреция ферментов, развитие оксидативного взрыва, продукция метаболитов арахидоновой кислоты, модуляция адгезивных молекул.
§ Миграция лейкоцитов всех типов сквозь сосудистую стенку происходит в области межклеточных контактов эндотелиальных клеток. Базальную мембрану лейкоциты преодолевают благодаря выделению разрушающих ее нейтральных протеаз. § Хемотаксис, т. е. лейкоциты движутся в очаге воспаления в направлении нарастания градиента концентрации хемотаксических агентов. Хемотаксис лейкоцитов обеспечивается лигандрецепторными взаимодействиями между хемотаксическими агентами, находящимися в очаге воспаления, и соответствующими рецепторами на поверхности лейкоцитов. Такое взаимодействие приводит к синтезу вторичных мессенджеров, активации фосфолипазы С и протеинкиназы С, возрастанию концентрации внутриклеточного Са и контрактильных элементов, необходимых для движения лейкоцитов. Первыми в очаг воспаления приходят нейтрофильные лейкоциты, затем моноциты и лимфоциты. § Активация нейтрофильных лейкоцитов индуцируется хемотаксическими агентами и включает такие процессы, как их дегрануляция и секреция ферментов, развитие оксидативного взрыва, продукция метаболитов арахидоновой кислоты, модуляция адгезивных молекул.
 Фагоцитоз поглощение и переваривание клетками (фагоцитами) различных частиц микробов, инородных тел, апоптозных телец, детрита и др. Стадии фагоцитоза: § распознавание и прикрепление объекта фагоцитоза к поверхности лейкоцита; в случае фагоцитоза микробов эти процессы происходят за счет взаимодействия рецепторов, расположенных на поверхности лейкоцита, с опсонинами (Fс фрагментами Ig. G и СЗ компонентами), покрывающими поверхность микробов; § захват объекта фагоцитоза и формирование фаголизосомы; § уничтожение и/или разрушение поглощенноro материала. В случае фагоцитоза бактерий их уничтожение осуществляется, как правило, посредством генерации активных форм кислорода и HOCl , генерируемых в ходе дыхательного взрыва и при взаимодействии миелопероксидазы лейкоцитов с перекисью водорода и ионами хлора. Также существует способ уничтожения бактерий с помощью бактерицидных белков, содержащихся во вторичных гранулах лейкоцитов (бактерицидный катионный белок, лизоцим, лактоферрин), и эозинофилов (главный основной белок).
Фагоцитоз поглощение и переваривание клетками (фагоцитами) различных частиц микробов, инородных тел, апоптозных телец, детрита и др. Стадии фагоцитоза: § распознавание и прикрепление объекта фагоцитоза к поверхности лейкоцита; в случае фагоцитоза микробов эти процессы происходят за счет взаимодействия рецепторов, расположенных на поверхности лейкоцита, с опсонинами (Fс фрагментами Ig. G и СЗ компонентами), покрывающими поверхность микробов; § захват объекта фагоцитоза и формирование фаголизосомы; § уничтожение и/или разрушение поглощенноro материала. В случае фагоцитоза бактерий их уничтожение осуществляется, как правило, посредством генерации активных форм кислорода и HOCl , генерируемых в ходе дыхательного взрыва и при взаимодействии миелопероксидазы лейкоцитов с перекисью водорода и ионами хлора. Также существует способ уничтожения бактерий с помощью бактерицидных белков, содержащихся во вторичных гранулах лейкоцитов (бактерицидный катионный белок, лизоцим, лактоферрин), и эозинофилов (главный основной белок).
 § Фагоцитоз может быть завершенным и незавершенным (не заканчивающимся полным перевариванием объекта фагоцитоза). В случае незавершенности фагоцитоза микробы могут длительно существовать (персистировать) в макрофаге, а макрофаг при этом может продуцировать в окружающие ткани медиаторы воспаления и вызывать тем самым вторичное повреждение, что приводит к хронизации воспаления. § Активированные лейкоциты выделяют лизосомальные ферменты, активные формы кислорода и продукты метаболизма арахидоновой кислоты (простагландины и лейкотриены) в окружающие ткани, что может вызвать вторичное повреждение этих тканей. Данные события часто лежат в основе осложнений острого воспаления и его хронизации. § Пролиферация клеток в очаге воспаления, направленная на восстановление целостности ткани, начинается очень рано, еще в разгар воспалительной реакции. Пролиферация и дифференцировка клеток встречаются в очагах как острого, так и хронического воспаления.
§ Фагоцитоз может быть завершенным и незавершенным (не заканчивающимся полным перевариванием объекта фагоцитоза). В случае незавершенности фагоцитоза микробы могут длительно существовать (персистировать) в макрофаге, а макрофаг при этом может продуцировать в окружающие ткани медиаторы воспаления и вызывать тем самым вторичное повреждение, что приводит к хронизации воспаления. § Активированные лейкоциты выделяют лизосомальные ферменты, активные формы кислорода и продукты метаболизма арахидоновой кислоты (простагландины и лейкотриены) в окружающие ткани, что может вызвать вторичное повреждение этих тканей. Данные события часто лежат в основе осложнений острого воспаления и его хронизации. § Пролиферация клеток в очаге воспаления, направленная на восстановление целостности ткани, начинается очень рано, еще в разгар воспалительной реакции. Пролиферация и дифференцировка клеток встречаются в очагах как острого, так и хронического воспаления.
 Исходы и значение воспаления для организма Воспалительная реакция имеет защитный характер для организма хозяина, так как направлена на: § локализацию и отграничение очага поражения; § нейтрализацию, инактивацию и элиминацию повреждающего агента и поврежденных тканей; § подготовку к восстановлению (репарации) тканей в очаге поражения.
Исходы и значение воспаления для организма Воспалительная реакция имеет защитный характер для организма хозяина, так как направлена на: § локализацию и отграничение очага поражения; § нейтрализацию, инактивацию и элиминацию повреждающего агента и поврежденных тканей; § подготовку к восстановлению (репарации) тканей в очаге поражения.
 Благоприятные исходы воспаления § П о л н о е р а з р е ш е н и е. Полное восстановление ткани наблюдается при малых объемах повреждения. Разрешение воспаления включает в себя нейтрализацию химических медиаторов, восстановление нормальной сосудистой проницаемости, прекращение лейкоцитарной инфильтрации и удаление отечной жидкости, белка, лейкоцитов, инородных агентов и тканевого детрита. § Заживление путем замещения соединительной тканью (фиброз). Процесс начинается после частичного разрушения ткани или развития воспалительного повреждения в тканях, не способных регенерировать, а также при массивной экссудации фибрина. В том случае, если фибринозный экссудат в ткани или серозных полостях (на плевре и брюшине) рассасывается (резорбируется) не полностью, соединительная ткань прорастает экссудат, превращая его в массу фиброзной ткани. Этот процесс называют организацией. § В то же время в ряде ситуаций воспаление может оказывать вредное воздействие на организм хозяина, вызывая местные симптомы в виде боли, отека, а также общие симптомы, такие как общая интоксикация и лихорадка при попадании ряда токсичных продуктов метаболизма и цитокинов из очага воспаления в кровоток.
Благоприятные исходы воспаления § П о л н о е р а з р е ш е н и е. Полное восстановление ткани наблюдается при малых объемах повреждения. Разрешение воспаления включает в себя нейтрализацию химических медиаторов, восстановление нормальной сосудистой проницаемости, прекращение лейкоцитарной инфильтрации и удаление отечной жидкости, белка, лейкоцитов, инородных агентов и тканевого детрита. § Заживление путем замещения соединительной тканью (фиброз). Процесс начинается после частичного разрушения ткани или развития воспалительного повреждения в тканях, не способных регенерировать, а также при массивной экссудации фибрина. В том случае, если фибринозный экссудат в ткани или серозных полостях (на плевре и брюшине) рассасывается (резорбируется) не полностью, соединительная ткань прорастает экссудат, превращая его в массу фиброзной ткани. Этот процесс называют организацией. § В то же время в ряде ситуаций воспаление может оказывать вредное воздействие на организм хозяина, вызывая местные симптомы в виде боли, отека, а также общие симптомы, такие как общая интоксикация и лихорадка при попадании ряда токсичных продуктов метаболизма и цитокинов из очага воспаления в кровоток.
 Неблагоприятные исходы воспаления § Прогрессирование острого воспалительного ответа в различные формы хронического воспаления встречается в тех случаях, когда острый воспалительный ответ не разрешается, имеется персистирование повреждающего агента или нарушение процесса организации. Например, бактериальная инфекция легкого начинается как фокус острого воспаления (пневмония), однако расплавление поврежденных тканей может привести к образованию полости, в которой продолжается воспаление, обусловливающее формирование хронического абсцесса легкого. Другой пример хронического воспаления с персистирующей стимуляцией это развитиепептической язвы желудка или двенадцатиперстной кишки. Пептические язвы могут персистировать в течение месяцев и лет и проявляться как острой, так и хронической воспалительными реакциями. § Образование хронического абсцесса наблюдается при инфекциях и связан с неполным удалением пиогенных микроорганизмов или их фрагментов. Хронический абсцесс отграничен от остальной ткани фиброзной капсулой.
Неблагоприятные исходы воспаления § Прогрессирование острого воспалительного ответа в различные формы хронического воспаления встречается в тех случаях, когда острый воспалительный ответ не разрешается, имеется персистирование повреждающего агента или нарушение процесса организации. Например, бактериальная инфекция легкого начинается как фокус острого воспаления (пневмония), однако расплавление поврежденных тканей может привести к образованию полости, в которой продолжается воспаление, обусловливающее формирование хронического абсцесса легкого. Другой пример хронического воспаления с персистирующей стимуляцией это развитиепептической язвы желудка или двенадцатиперстной кишки. Пептические язвы могут персистировать в течение месяцев и лет и проявляться как острой, так и хронической воспалительными реакциями. § Образование хронического абсцесса наблюдается при инфекциях и связан с неполным удалением пиогенных микроорганизмов или их фрагментов. Хронический абсцесс отграничен от остальной ткани фиброзной капсулой.
 § Распространение воспаления на прилежащие ткани. При этом формируются свищи и фистулы и даже наблюдаются генерализация инфекта (как это бывает при сепсисе), а также расплавление тканей с перфорацией стенок органов и сосудов, являющееся причиной распространения воспаления на брюшину, плевру, а также внутренних кровотечений. § Иммунное воспаление, приобретающее, как правило, хронический характер, лежит в основе таких тяжелых заболеваний человека, как гломерулонефриты, вирусные гепатиты, идиопатический фиброзирующий альвеолит, туберкулез, бронхиальная астма, ревматические болезни, системные васкулиты и др. § Существует целый ряд приобретенных и наследственных болезней, обусловленных нарушениями различных функций лейкоцитов и проявляющихся в предрасположенности пациентов к инфекционным заболеваниям и развитию хронических форм воспаления.
§ Распространение воспаления на прилежащие ткани. При этом формируются свищи и фистулы и даже наблюдаются генерализация инфекта (как это бывает при сепсисе), а также расплавление тканей с перфорацией стенок органов и сосудов, являющееся причиной распространения воспаления на брюшину, плевру, а также внутренних кровотечений. § Иммунное воспаление, приобретающее, как правило, хронический характер, лежит в основе таких тяжелых заболеваний человека, как гломерулонефриты, вирусные гепатиты, идиопатический фиброзирующий альвеолит, туберкулез, бронхиальная астма, ревматические болезни, системные васкулиты и др. § Существует целый ряд приобретенных и наследственных болезней, обусловленных нарушениями различных функций лейкоцитов и проявляющихся в предрасположенности пациентов к инфекционным заболеваниям и развитию хронических форм воспаления.
 Патогенез и морфогенез воспаления наиболее интенсивно изучались в последние десятилетия благодаря исследованиям не только в области патологической анатомии, патологиче ской физиологии и биохимии, но и молекулярной биологии, молекулярной патологии, клеточной биологии и генетики. § Клетки, участвующие в воспалении. В очаге воспаления в органах присутствуют не только клетки мезенхимального происхождения (нейтрофильные лейкоциты, моноциты, лимфоциты, эндотелиоциты, фибробласты, миофибробласты и др. ), но и паренхиматозные клетки. § Ведущая роль в течении воспалительной реакции признается за клетками мезенхимального происхождения. Последние могут быть местного, гистиогенного (эндотелиоциты, фибробласты, миофибробласты и др. ), а также гематогенного происхождения, пришедшие в очаг воспаления из кровотока (нейтрофильные лейкоциты, моноциты, лимфоциты и др. ).
Патогенез и морфогенез воспаления наиболее интенсивно изучались в последние десятилетия благодаря исследованиям не только в области патологической анатомии, патологиче ской физиологии и биохимии, но и молекулярной биологии, молекулярной патологии, клеточной биологии и генетики. § Клетки, участвующие в воспалении. В очаге воспаления в органах присутствуют не только клетки мезенхимального происхождения (нейтрофильные лейкоциты, моноциты, лимфоциты, эндотелиоциты, фибробласты, миофибробласты и др. ), но и паренхиматозные клетки. § Ведущая роль в течении воспалительной реакции признается за клетками мезенхимального происхождения. Последние могут быть местного, гистиогенного (эндотелиоциты, фибробласты, миофибробласты и др. ), а также гематогенного происхождения, пришедшие в очаг воспаления из кровотока (нейтрофильные лейкоциты, моноциты, лимфоциты и др. ).
 § Нейтрофильные лейкоциты (полиморфно ядерные нейтрофилы, нейтрофильные гранулоциты) обнаруживаются в очагах острого воспаления, при хронических абсцессах и эмпиеме. Их количество повышается в периферической крови (лейкоцитоз) при большинстве инфекционных воспалительных заболеваний. В цитоплазматических гранулах (лизосомах) нейтрофильных лейкоцитов содержатся разнообразные ферменты и активные вещества: миелопероксидаза, кислая гидролаза, протеазы, лизоцим и катионные белки. В очаге воспаления нейтрофильные лейкоциты появляются первыми, осуществляют фагоцитоз бактериальных тел и деструкцию (лизис, гистолиз, протеолиз) тканей за счет выделения лизосомальных ферментов.
§ Нейтрофильные лейкоциты (полиморфно ядерные нейтрофилы, нейтрофильные гранулоциты) обнаруживаются в очагах острого воспаления, при хронических абсцессах и эмпиеме. Их количество повышается в периферической крови (лейкоцитоз) при большинстве инфекционных воспалительных заболеваний. В цитоплазматических гранулах (лизосомах) нейтрофильных лейкоцитов содержатся разнообразные ферменты и активные вещества: миелопероксидаза, кислая гидролаза, протеазы, лизоцим и катионные белки. В очаге воспаления нейтрофильные лейкоциты появляются первыми, осуществляют фагоцитоз бактериальных тел и деструкцию (лизис, гистолиз, протеолиз) тканей за счет выделения лизосомальных ферментов.
 § Эозинофильные лейкоциты (эозинофильные гранулоциты) характерны для очагов иммунного воспаления (реакции гиперчувствительности I типа) (бронхиальная астма, экзогенные аллергические альвеолиты, системные эозинофилии), куда они привлекаются хемотаксическим фактором эозинофилов, выделяемым тучными клетками. Содержание эозинофилов может повышаться в кровотоке (эозuнофuлuя) при различных аллергических и паразитарных заболеваниях. В гранулах эозинофилов содержатся гистаминаза, арилсульфатаза и главный основной протеин.
§ Эозинофильные лейкоциты (эозинофильные гранулоциты) характерны для очагов иммунного воспаления (реакции гиперчувствительности I типа) (бронхиальная астма, экзогенные аллергические альвеолиты, системные эозинофилии), куда они привлекаются хемотаксическим фактором эозинофилов, выделяемым тучными клетками. Содержание эозинофилов может повышаться в кровотоке (эозuнофuлuя) при различных аллергических и паразитарных заболеваниях. В гранулах эозинофилов содержатся гистаминаза, арилсульфатаза и главный основной протеин.
 § Базофилы (базофильные гранулоциты) выявляют в периферической крови (реакции гиперчувствительности I типа) и очагах иммунного воспаления с гиперергическим патогенезом (реакции гиперчувствительности 1 типа, Ig. E зависимые реакции, а также IV типа при контактном дерматите). При этом Ig. E антитела, связанные с Fс рецептором на поверхности базофилов, могут взаимодействовать с антигеном, что вызывает дегрануляцию базофилов с высвобождением вазоактивных субстанций гистамина, гепарина и медленно реагирующей субстанции анафилаксии.
§ Базофилы (базофильные гранулоциты) выявляют в периферической крови (реакции гиперчувствительности I типа) и очагах иммунного воспаления с гиперергическим патогенезом (реакции гиперчувствительности 1 типа, Ig. E зависимые реакции, а также IV типа при контактном дерматите). При этом Ig. E антитела, связанные с Fс рецептором на поверхности базофилов, могут взаимодействовать с антигеном, что вызывает дегрануляцию базофилов с высвобождением вазоактивных субстанций гистамина, гепарина и медленно реагирующей субстанции анафилаксии.
 § Тучные клетки (по структуре и функциям похожи на базофилы) в отличие от последних встречаются в соединительной ткани вблизи мелких сосудов. Гранулы тучных клеток дают метахромазию при окраске толуидиновым синим и содержат гистамин, гепарин и медленно реагирующую субстанцию анафилаксии, а также фактор хемотаксиса эозинофилов. Продукция гистамина тучными клетками может стимулироваться некоторыми физическими факторами, лекарственными веществами, иммуноглобулинами, С 3 а и С 5 а компонентами комплемента, катионными белками.
§ Тучные клетки (по структуре и функциям похожи на базофилы) в отличие от последних встречаются в соединительной ткани вблизи мелких сосудов. Гранулы тучных клеток дают метахромазию при окраске толуидиновым синим и содержат гистамин, гепарин и медленно реагирующую субстанцию анафилаксии, а также фактор хемотаксиса эозинофилов. Продукция гистамина тучными клетками может стимулироваться некоторыми физическими факторами, лекарственными веществами, иммуноглобулинами, С 3 а и С 5 а компонентами комплемента, катионными белками.
 § Макрофаги (мононуклеарные фагоциты) входят в состав моноцитарно макрофагальной системы и распределены в разных органах и тканях, имеют костномозговое происхождение. В очаге воспаления моноцит трансформируется в тканевый макрофаг. Кроме того, имеются так называемые тканевые или резидентные макрофаги моноцитарного происхождения. К резидентным макрофагам относятся альвеолярные макрофаги легких, плевральные и перитонеальные макрофаги, звездчатые ретикулоэндотелиоциты (клетки Купфера) печени, гистиоциты соединительной ткани, мезангиальные клетки почек. участвуют в процессах, связанных с воспалительной и иммунной реакциями. Основная функция макрофагов это фагоцитоз. Они осуществляют фагоцитоз повреждающих агентов (например, микробов) и тканевого детрита, подготавливая тем самым почву для репаративных процессов. В иммунных реакциях макрофаг принимает участие на стадии процессинга и представления антигена Т клеткам. Кроме того, макрофаги продуцируют ИЛ I, стимулирующий секрецию ИЛ 2 Т клетками и активацию В клеток. Макрофаги участвуют в уничтожении опухолевых клеток.
§ Макрофаги (мононуклеарные фагоциты) входят в состав моноцитарно макрофагальной системы и распределены в разных органах и тканях, имеют костномозговое происхождение. В очаге воспаления моноцит трансформируется в тканевый макрофаг. Кроме того, имеются так называемые тканевые или резидентные макрофаги моноцитарного происхождения. К резидентным макрофагам относятся альвеолярные макрофаги легких, плевральные и перитонеальные макрофаги, звездчатые ретикулоэндотелиоциты (клетки Купфера) печени, гистиоциты соединительной ткани, мезангиальные клетки почек. участвуют в процессах, связанных с воспалительной и иммунной реакциями. Основная функция макрофагов это фагоцитоз. Они осуществляют фагоцитоз повреждающих агентов (например, микробов) и тканевого детрита, подготавливая тем самым почву для репаративных процессов. В иммунных реакциях макрофаг принимает участие на стадии процессинга и представления антигена Т клеткам. Кроме того, макрофаги продуцируют ИЛ I, стимулирующий секрецию ИЛ 2 Т клетками и активацию В клеток. Макрофаги участвуют в уничтожении опухолевых клеток.
 § Активация макрофагов происходит под действием различных антигенов, повреждающих факторов, иммунных комплексов и цитокинов, выделяемых лимфоцитами (лимфокинов ИЛ 2). При активации в макрофагах происходит дыхательный взрыв, синтезируются радикалы NO и активируются протеазы, что в определенных условиях может приводить к вторичному повреждению тканей, хронизации воспаления и выраженным склеротическим изменениям. § Макрофаги выделяют колониестимулирующий фактор (КСФ), поддерживающий популяцию моноцитов и макрофагов на необходимом уровне, а также ФНОα и ИНФα, блокирующие репликацию вирусов, предшественники простагландинов, индуцирующих совместно с ИЛ 1 лихорадку и лейкоцитоз со сдвигом влево в периферической крови. § Лимфоциты (В и Т клетки), NК клетки, К к л е т к и , п л а з м а т и ч е с к и е клетки участвуют в воспалительных реакциях непосредственно, а также через активацию макрофагов. Их значение особенно велико при иммунном воспалении.
§ Активация макрофагов происходит под действием различных антигенов, повреждающих факторов, иммунных комплексов и цитокинов, выделяемых лимфоцитами (лимфокинов ИЛ 2). При активации в макрофагах происходит дыхательный взрыв, синтезируются радикалы NO и активируются протеазы, что в определенных условиях может приводить к вторичному повреждению тканей, хронизации воспаления и выраженным склеротическим изменениям. § Макрофаги выделяют колониестимулирующий фактор (КСФ), поддерживающий популяцию моноцитов и макрофагов на необходимом уровне, а также ФНОα и ИНФα, блокирующие репликацию вирусов, предшественники простагландинов, индуцирующих совместно с ИЛ 1 лихорадку и лейкоцитоз со сдвигом влево в периферической крови. § Лимфоциты (В и Т клетки), NК клетки, К к л е т к и , п л а з м а т и ч е с к и е клетки участвуют в воспалительных реакциях непосредственно, а также через активацию макрофагов. Их значение особенно велико при иммунном воспалении.
 Химические медиаторы воспаления химические вещества, имеющие плазменное или клеточное происхождение. Биологическое действие медиаторов воспаления на клетки зависит от их природы, при этом выделяют несколько типов взаимодействий: § лигандрецепторные, при которых медиатор воспаления играет роль лиганда, рецептор же локализуется на чувствительной клетке; § ферментативные, при которых медиатор воспаления является ферментом; § свободнорадикальные при генерации клетками активных форм кислорода и радикалов оксида азота.
Химические медиаторы воспаления химические вещества, имеющие плазменное или клеточное происхождение. Биологическое действие медиаторов воспаления на клетки зависит от их природы, при этом выделяют несколько типов взаимодействий: § лигандрецепторные, при которых медиатор воспаления играет роль лиганда, рецептор же локализуется на чувствительной клетке; § ферментативные, при которых медиатор воспаления является ферментом; § свободнорадикальные при генерации клетками активных форм кислорода и радикалов оксида азота.
 § медиаторы стимулируют выработку других медиаторов, которые могут потенцировать или тормозить их действие; § медиаторы относятся к короткоживущим биологическим субстанциям, могут спонтанно разрушаться, быстро расщепляться соответствующими ферментами, соединяться с белками ингибиторами; § практически все медиаторы воспаления потенциально опасны, поскольку могут повреждать ткани. Баланс между медиаторами воспаления контролируется сложной системой субстанций, поддерживающей динамическое равновесие между ними.
§ медиаторы стимулируют выработку других медиаторов, которые могут потенцировать или тормозить их действие; § медиаторы относятся к короткоживущим биологическим субстанциям, могут спонтанно разрушаться, быстро расщепляться соответствующими ферментами, соединяться с белками ингибиторами; § практически все медиаторы воспаления потенциально опасны, поскольку могут повреждать ткани. Баланс между медиаторами воспаления контролируется сложной системой субстанций, поддерживающей динамическое равновесие между ними.
 § Медиаторы воспаления классифицируются в зависимости от их происхождения (плазменные и клеточные), а также их химической природы. В а з о а к т и в н ы е а м и н ы гистамин и серотонин являются медиаторами клеточного происхождения, продуцируются тромбоцитами и тучными клетками на ранних этапах воспаления, вызывают расширение сосудов и усиление сосудистой проницаемости. Кроме того, гистамин обнаруживается в базофильных лейкоцитах, а серотонин в энтерохромаффинных клетках Apu. D системы. Выброс вазоактивных аминов тромбоцитами инициируется при их взаимодействии с коллагеном, тромбином, АДФ, иммунными комплексами и ФАТ. Тучные клетки продуцируют гистамин и серотонин в ответ на физическое повреждение (при травмах, обморожени ях и ожогах), при реакциях гиперчувствительности 1 типа(Ig. E зависимых) и взаимодействии с анафилатоксинами (С 3 а и С 5 а), ИЛ I, ИЛ 8, нейропептидами (субстанция Р), а также с гистамин рилизинг фактором лейкоцитов.
§ Медиаторы воспаления классифицируются в зависимости от их происхождения (плазменные и клеточные), а также их химической природы. В а з о а к т и в н ы е а м и н ы гистамин и серотонин являются медиаторами клеточного происхождения, продуцируются тромбоцитами и тучными клетками на ранних этапах воспаления, вызывают расширение сосудов и усиление сосудистой проницаемости. Кроме того, гистамин обнаруживается в базофильных лейкоцитах, а серотонин в энтерохромаффинных клетках Apu. D системы. Выброс вазоактивных аминов тромбоцитами инициируется при их взаимодействии с коллагеном, тромбином, АДФ, иммунными комплексами и ФАТ. Тучные клетки продуцируют гистамин и серотонин в ответ на физическое повреждение (при травмах, обморожени ях и ожогах), при реакциях гиперчувствительности 1 типа(Ig. E зависимых) и взаимодействии с анафилатоксинами (С 3 а и С 5 а), ИЛ I, ИЛ 8, нейропептидами (субстанция Р), а также с гистамин рилизинг фактором лейкоцитов.
 Плазменные протеазы представлены: системой комплемента; кининовой системой; свертывающей системой крови.
Плазменные протеазы представлены: системой комплемента; кининовой системой; свертывающей системой крови.
 Система комплемента включает группу плазменных протеаз, циркулирующих в крови в неактивной зимогенной форме и активирующихся в виде каскада реакций с образованием в итоге мембрано атакующего комплекса (МАК), представляющего собой С 5 b С 9. МАК образует гидрофобную связь с двойным липидным слоем клеток мишеней и формирует трансмембранные каналы, обеспечивающие лизис клетки. Продукты активации комплемента участвуют при воспалении в следующих процессах: § увеличении сосудистой проницаемости; § опсонизации и фагоцитозе; § индукции хемотаксиса, иммобилизации и адгезии лейкоцитов к эндотелию; § фиксации цитолитических комплексов на поверхности клетки для осуществления цитолитического действия на микробы и клетки мишени. Активация системы комплемента может осуществляться по одному из двух путей: § классическому, инициируемому иммунными комплексами; § альтернативному, активируемому эндотоксином, комплексом полисахаридов и агрегатами глобулинов.
Система комплемента включает группу плазменных протеаз, циркулирующих в крови в неактивной зимогенной форме и активирующихся в виде каскада реакций с образованием в итоге мембрано атакующего комплекса (МАК), представляющего собой С 5 b С 9. МАК образует гидрофобную связь с двойным липидным слоем клеток мишеней и формирует трансмембранные каналы, обеспечивающие лизис клетки. Продукты активации комплемента участвуют при воспалении в следующих процессах: § увеличении сосудистой проницаемости; § опсонизации и фагоцитозе; § индукции хемотаксиса, иммобилизации и адгезии лейкоцитов к эндотелию; § фиксации цитолитических комплексов на поверхности клетки для осуществления цитолитического действия на микробы и клетки мишени. Активация системы комплемента может осуществляться по одному из двух путей: § классическому, инициируемому иммунными комплексами; § альтернативному, активируемому эндотоксином, комплексом полисахаридов и агрегатами глобулинов.
 § Наиболее важными противовоспалительными компонентами системы комплемента являются: – С 3 а вызывает повышение сосудистой проницаемости; – С 5 а вызывает повышение сосудистой проницаемости и хемотаксис лейкоцитов; – С 3 b и С 3 bi являются опсонинами, участвующими в реакциях фагоцитоза; – С 5 b С 9, или МАК, вызывает лизис клеток, стимулирует метаболизм арахидоновой кислоты и продукцию активных форм кислорода лейкоцитами. § Функционирование системы комплемента контролируется белковыми ингибиторами СЗ, С 5 конвертазы и С 1 ингибитором.
§ Наиболее важными противовоспалительными компонентами системы комплемента являются: – С 3 а вызывает повышение сосудистой проницаемости; – С 5 а вызывает повышение сосудистой проницаемости и хемотаксис лейкоцитов; – С 3 b и С 3 bi являются опсонинами, участвующими в реакциях фагоцитоза; – С 5 b С 9, или МАК, вызывает лизис клеток, стимулирует метаболизм арахидоновой кислоты и продукцию активных форм кислорода лейкоцитами. § Функционирование системы комплемента контролируется белковыми ингибиторами СЗ, С 5 конвертазы и С 1 ингибитором.
 Кининовая система состоит из протеинов плазменного происхождения кининогенов, а также сериновых протеаз, калликреинов, их расщепляющих и приводящих к образованию конечного продукта каскадных реакций брадикинина. Эта система содержит плазменные белки: фактор Хагемана (коагуляционный фактор ХН), прекалликреин, высокомолекулярный кининоген и коагуляционный фактор XI. Запуск системы начинается с активации фактора Хагемана, происходящей при контакте с коллагеном или отрицательно заряженными поверхностями. Активная форма фактора Хагемана конвертирует плазменный прекалликреин в калликреин, а затем последний расщепляет высокомолекулярный кининоген, из которого образуется брадикинин. Кининовая система участвует в регуляции следующих процессов в ходе воспаления: § повышения сосудистой проницаемости; § хемотаксиса и агрегации лейкоцитов.
Кининовая система состоит из протеинов плазменного происхождения кининогенов, а также сериновых протеаз, калликреинов, их расщепляющих и приводящих к образованию конечного продукта каскадных реакций брадикинина. Эта система содержит плазменные белки: фактор Хагемана (коагуляционный фактор ХН), прекалликреин, высокомолекулярный кининоген и коагуляционный фактор XI. Запуск системы начинается с активации фактора Хагемана, происходящей при контакте с коллагеном или отрицательно заряженными поверхностями. Активная форма фактора Хагемана конвертирует плазменный прекалликреин в калликреин, а затем последний расщепляет высокомолекулярный кининоген, из которого образуется брадикинин. Кининовая система участвует в регуляции следующих процессов в ходе воспаления: § повышения сосудистой проницаемости; § хемотаксиса и агрегации лейкоцитов.
 Свертывающая система крови состоит из двух взаимосвязанных частей внутренней и внешней. Внутренняя часть системы представляет собой каскад реакций, которые могут вызвать активацию фактора Хагемана, приводящую к активации тромбина, расщеплению фибриногена и образованию фибринового тромба. При этом продуцируются фибринопептиды, вызывающие увеличение сосудистой проницаемости и хемотаксис лейкоцитов. Тромбин также обладает противовоспалительным действием и усиливает адгезию лейкоцитов к эндотелию. § Одновременно активированный фактор Хагемана обусловливает активацию системы фибринолиза, приводящую к синтезу плазмина, который разрушает фибрин и сгусток. Однако плазмин способен влиять на воспалительную реакцию через систему комплемента путем расщепления С 3 компонента, активации фактора Хагемана и образования продуктов деградации фибрина, вызывающих повышение сосудистой проницаемости. § Метаболиты арахидоновой кислоты, участвующие в воспалительных реакциях, образуются в ходе двух различных путей метаболизма этой кислоты. Простагландины и тромбоксан синтезируются в циклооксигеназном, а лейкотриены и липоксины липооксигеназном пути.
Свертывающая система крови состоит из двух взаимосвязанных частей внутренней и внешней. Внутренняя часть системы представляет собой каскад реакций, которые могут вызвать активацию фактора Хагемана, приводящую к активации тромбина, расщеплению фибриногена и образованию фибринового тромба. При этом продуцируются фибринопептиды, вызывающие увеличение сосудистой проницаемости и хемотаксис лейкоцитов. Тромбин также обладает противовоспалительным действием и усиливает адгезию лейкоцитов к эндотелию. § Одновременно активированный фактор Хагемана обусловливает активацию системы фибринолиза, приводящую к синтезу плазмина, который разрушает фибрин и сгусток. Однако плазмин способен влиять на воспалительную реакцию через систему комплемента путем расщепления С 3 компонента, активации фактора Хагемана и образования продуктов деградации фибрина, вызывающих повышение сосудистой проницаемости. § Метаболиты арахидоновой кислоты, участвующие в воспалительных реакциях, образуются в ходе двух различных путей метаболизма этой кислоты. Простагландины и тромбоксан синтезируются в циклооксигеназном, а лейкотриены и липоксины липооксигеназном пути.
 § Циклооксигеназный путь приводит к синтезу простагландинов и тромбоксана А 2, каждый из которых образуется под воздействием специфического фермента. Простагландины Е 2, D 2 и F 2 играют важную роль в развитии острого воспаления, поскольку вызывают расширение сосудов и повышение их проницаемости. В то же время простагландины могут оказывать и противовоспалительный эффект, препятствуя дегрануляции нейтрофильных лейкоцитов и тучных клеток. Простациклин расширяет сосуды и является мощным ингибитором агрегации тромбоцитов. Тромбоксан А 2 и простациклин играют при гемостазе противоположную роль.
§ Циклооксигеназный путь приводит к синтезу простагландинов и тромбоксана А 2, каждый из которых образуется под воздействием специфического фермента. Простагландины Е 2, D 2 и F 2 играют важную роль в развитии острого воспаления, поскольку вызывают расширение сосудов и повышение их проницаемости. В то же время простагландины могут оказывать и противовоспалительный эффект, препятствуя дегрануляции нейтрофильных лейкоцитов и тучных клеток. Простациклин расширяет сосуды и является мощным ингибитором агрегации тромбоцитов. Тромбоксан А 2 и простациклин играют при гемостазе противоположную роль.
 § Липооксигеназный путь под действием 5 липооксигеназы образуются лейкотриены (В 4, С 4, D 4) гидроксиэйкозатетраноидные кислоты (НЕТЕ). Лейкотриен В 4 сильный хемотаксический агент, вызывающий агрегацию и прилипание лейкоцитов к эндотелию венул; он является также выраженным хемотаксическим агентом, действующим в наномолярных концентрациях. Лейкотриены С 4 и D 4 обусловливают гистаминнезависимый спазм сосудов, бронхоспазм и повышение сосудистой проницаемости. НЕТЕ (5 НЕТЕ, 12 НЕТЕ) служат хемотаксическими факторами для нейтрофилов и эозинофилов.
§ Липооксигеназный путь под действием 5 липооксигеназы образуются лейкотриены (В 4, С 4, D 4) гидроксиэйкозатетраноидные кислоты (НЕТЕ). Лейкотриен В 4 сильный хемотаксический агент, вызывающий агрегацию и прилипание лейкоцитов к эндотелию венул; он является также выраженным хемотаксическим агентом, действующим в наномолярных концентрациях. Лейкотриены С 4 и D 4 обусловливают гистаминнезависимый спазм сосудов, бронхоспазм и повышение сосудистой проницаемости. НЕТЕ (5 НЕТЕ, 12 НЕТЕ) служат хемотаксическими факторами для нейтрофилов и эозинофилов.
 § Фактор активации тромбоцитов (Ф А Т) являeтcя мембранным фосфолипидным медиатором. Он образуется после активации фосфолипазы А 2 и часто выделяется совместно с метаболитами арахидоновой кислоты. стимулирует агрегацию и активацию тромбоцитов, вызывает спазм сосудов и бронхов, а в низких концентрациях расширение сосудов и увеличение проницаемости венул в 100 10. 000 раз сильнее, чем гистамин. усиливает прилипание лейкоцитов к эндотелию и хемотаксис. Многие типы клеток, включая базофилы, нейтрофилы, моноциты и эндотелиальные клетки, могут вырабатывать ФАТ, действующий непосредственно на клетки мишени через специфические рецепторы и ускоряющий синтез медиаторов (особенно эйкозаноидов) лейкоцитами или другими клетками.
§ Фактор активации тромбоцитов (Ф А Т) являeтcя мембранным фосфолипидным медиатором. Он образуется после активации фосфолипазы А 2 и часто выделяется совместно с метаболитами арахидоновой кислоты. стимулирует агрегацию и активацию тромбоцитов, вызывает спазм сосудов и бронхов, а в низких концентрациях расширение сосудов и увеличение проницаемости венул в 100 10. 000 раз сильнее, чем гистамин. усиливает прилипание лейкоцитов к эндотелию и хемотаксис. Многие типы клеток, включая базофилы, нейтрофилы, моноциты и эндотелиальные клетки, могут вырабатывать ФАТ, действующий непосредственно на клетки мишени через специфические рецепторы и ускоряющий синтез медиаторов (особенно эйкозаноидов) лейкоцитами или другими клетками.
 § Цитокины и хемокины. В воспаление вовлекается большое число клеток. Сообщение между клетками различных типов осуществляется через сеть молекулярных медиаторов. Цитокuны представляют собой низкомолекулярные полипептиды, которые продуцируются клетками многих типов и модулируют функцию клеток других типов. Хемокuнамu называют химические вещества, вызывающие хемотаксис лейкоцитов. Будучи вовлеченными в клеточный иммунный ответ, эти вещества играют важную роль в воспалении. Основными цитокинами, регулирующими воспаление, являются ИЛ 1, ФНО (α и β), ИНФγ, основной и кислый факторы роста фибробластов (о. ФРФ и к. ФРФ) и ТФРβ. Их эффекты реализуются тремя способами. Они могут действовать на те же клетки, которые их выделяют (аутокринный эффект), на клетки, находящиеся в непосредственной близости от клеток продуцентов (паракринный эффект) или оказывать системное действие, подобно гормонам (эндокринный эффект).
§ Цитокины и хемокины. В воспаление вовлекается большое число клеток. Сообщение между клетками различных типов осуществляется через сеть молекулярных медиаторов. Цитокuны представляют собой низкомолекулярные полипептиды, которые продуцируются клетками многих типов и модулируют функцию клеток других типов. Хемокuнамu называют химические вещества, вызывающие хемотаксис лейкоцитов. Будучи вовлеченными в клеточный иммунный ответ, эти вещества играют важную роль в воспалении. Основными цитокинами, регулирующими воспаление, являются ИЛ 1, ФНО (α и β), ИНФγ, основной и кислый факторы роста фибробластов (о. ФРФ и к. ФРФ) и ТФРβ. Их эффекты реализуются тремя способами. Они могут действовать на те же клетки, которые их выделяют (аутокринный эффект), на клетки, находящиеся в непосредственной близости от клеток продуцентов (паракринный эффект) или оказывать системное действие, подобно гормонам (эндокринный эффект).
 § Семейство интерлейкина 1 (ИЛ 1 ) состоит из двух форм а и f 3 и антагониста рецептора ИЛ 1. Первоначально ИЛ I был описан как основной продукт моноцитов и макрофагов, позже найден в нейтрофилах, лимфоцитах, кератиноцитах, в глиальных, эндотелиальных и большинстве стромальных клеток. Синтез ИЛ 1 стимулирует образование эндотоксина бактериями и вирусами. Его противовоспалительная активность включает стимуляцию лимфоцитов, синтез простагландинов, хемокинов и экспрессию эндотелиальных адгезивных молекул. Повышение уровня ИЛ 1 в крови приводит к нейтрофильному лейкоцитозу, лихорадке и продукции белков острой фазы воспаления. ИЛ 1 стимулирует выработку глюкокортикоидов, которые подавляют продукцию ИЛ 1 по принципу обратной связи. Макрофаги способны синтезировать антагонист рецептора ИЛ 1, который тормозит биологические эффекты ИЛ 1.
§ Семейство интерлейкина 1 (ИЛ 1 ) состоит из двух форм а и f 3 и антагониста рецептора ИЛ 1. Первоначально ИЛ I был описан как основной продукт моноцитов и макрофагов, позже найден в нейтрофилах, лимфоцитах, кератиноцитах, в глиальных, эндотелиальных и большинстве стромальных клеток. Синтез ИЛ 1 стимулирует образование эндотоксина бактериями и вирусами. Его противовоспалительная активность включает стимуляцию лимфоцитов, синтез простагландинов, хемокинов и экспрессию эндотелиальных адгезивных молекул. Повышение уровня ИЛ 1 в крови приводит к нейтрофильному лейкоцитозу, лихорадке и продукции белков острой фазы воспаления. ИЛ 1 стимулирует выработку глюкокортикоидов, которые подавляют продукцию ИЛ 1 по принципу обратной связи. Макрофаги способны синтезировать антагонист рецептора ИЛ 1, который тормозит биологические эффекты ИЛ 1.
 § Факторы некроза опухоли ( Ф Н О) включают в себя две формы – α и β (лимфотоксин). ФНОα, основным источником которого являются моноциты, впервые был открыт в плазме животных после введения бактериального эндотоксина. Многие функции этого цитокина подобны ИЛ 1. Парентеральное введение ФНОα вызывает подъем температуры тела, лейкопению и гипотензию; является главным медиатором септического шока и кахексии при хронических заболеваниях. ФНОβ (лимфотоксин) продуцируют активированные В лимфоциты. § Интерлейкин 8 (ИЛ 8) наиболее известный полипептид из семейства "малых" цитокинов или хемокинов. Наряду с моноцитарным хемоаттрактантным белком 1 и макрофагальными воспалительными белками α и β ИЛ 8 является сильным хемоаттрактантом и активатором лейкоцитов. Хемокины выделяются под действием других цитокинов, главным образом ИЛ l и ФНО α. § Интерферон γ (ИНФ γ) тормозит репликацию вирусов. В отличие от других интерферонов, продуцируемых стромальными клетками, ИНФ γ образуется клетками миелоидного ряда; способен активировать лейкоциты (в первую очередь, моноциты) и поддерживает рост В лимфоцитов.
§ Факторы некроза опухоли ( Ф Н О) включают в себя две формы – α и β (лимфотоксин). ФНОα, основным источником которого являются моноциты, впервые был открыт в плазме животных после введения бактериального эндотоксина. Многие функции этого цитокина подобны ИЛ 1. Парентеральное введение ФНОα вызывает подъем температуры тела, лейкопению и гипотензию; является главным медиатором септического шока и кахексии при хронических заболеваниях. ФНОβ (лимфотоксин) продуцируют активированные В лимфоциты. § Интерлейкин 8 (ИЛ 8) наиболее известный полипептид из семейства "малых" цитокинов или хемокинов. Наряду с моноцитарным хемоаттрактантным белком 1 и макрофагальными воспалительными белками α и β ИЛ 8 является сильным хемоаттрактантом и активатором лейкоцитов. Хемокины выделяются под действием других цитокинов, главным образом ИЛ l и ФНО α. § Интерферон γ (ИНФ γ) тормозит репликацию вирусов. В отличие от других интерферонов, продуцируемых стромальными клетками, ИНФ γ образуется клетками миелоидного ряда; способен активировать лейкоциты (в первую очередь, моноциты) и поддерживает рост В лимфоцитов.
 § Факторы роста ( Ф Р Ф и Т Ф Р β ) являются хемотаксическими агентами для лейкоцитов и мезенхимальных клеток, регулируют их пролиферативную и синтетическую активность. активно участвуют как в контроле воспалительной реакции, так и в процессе репарации поврежденной ткани. ТФР β принимает участие в регуляции инфильтрации зоны повреждения лейкоцитами и регулирует пролиферацию мезенхимальных клеток. § Оксид азота (NО) растворимый свободный газообразный радикал, который выделяется эндотелиальными клетками и макрофагами. синтезируется из L аргинина, молекулярного кислорода и NADP с помощью синтазы NO. вызывает релаксацию гладкомышечных клеток, уменьшает агрегацию и прилипание тромбоцитов. NO, образованный макрофагами, действует как свободный радикал, обладающий цитотоксическими свойствами в отношении микробов и опухолевых клеток.
§ Факторы роста ( Ф Р Ф и Т Ф Р β ) являются хемотаксическими агентами для лейкоцитов и мезенхимальных клеток, регулируют их пролиферативную и синтетическую активность. активно участвуют как в контроле воспалительной реакции, так и в процессе репарации поврежденной ткани. ТФР β принимает участие в регуляции инфильтрации зоны повреждения лейкоцитами и регулирует пролиферацию мезенхимальных клеток. § Оксид азота (NО) растворимый свободный газообразный радикал, который выделяется эндотелиальными клетками и макрофагами. синтезируется из L аргинина, молекулярного кислорода и NADP с помощью синтазы NO. вызывает релаксацию гладкомышечных клеток, уменьшает агрегацию и прилипание тромбоцитов. NO, образованный макрофагами, действует как свободный радикал, обладающий цитотоксическими свойствами в отношении микробов и опухолевых клеток.
 § Содержимое лизосом. Нейтрофилы, моноциты и тромбоциты содержат лuзосомальные гранулы, которые могут участвовать в воспалительном ответе. Более мелкие специфические (вторичные) гранулы содержат лактоферрин, лизоцим, щелочную фосфатазу, компоненты NАDР оксидазы, интрацитоплазматический пул интегринов и коллагеназу. Крупные азурофильные (первичные) гранулы содержат бактерицидные факторы (лизоцим, дефензины), кислые гидролазы и различные нейтральные протеазы (эластаза, неспецифические коллагеназы, протеиназа). Эти ферменты выделяются также после гибели клеток. Имеются, однако, и различия в мобилизации специфических и азурофильных гранул. Специфические гранулы легче секретируются под действием меньших концентраций агонистов. Потенциально более деструктивные азурофильные гранулы выделяют свое содержимое вначале в фагосому, а для выделения за пределы клетки они нуждаются в очень высокой концентрации агонистов.
§ Содержимое лизосом. Нейтрофилы, моноциты и тромбоциты содержат лuзосомальные гранулы, которые могут участвовать в воспалительном ответе. Более мелкие специфические (вторичные) гранулы содержат лактоферрин, лизоцим, щелочную фосфатазу, компоненты NАDР оксидазы, интрацитоплазматический пул интегринов и коллагеназу. Крупные азурофильные (первичные) гранулы содержат бактерицидные факторы (лизоцим, дефензины), кислые гидролазы и различные нейтральные протеазы (эластаза, неспецифические коллагеназы, протеиназа). Эти ферменты выделяются также после гибели клеток. Имеются, однако, и различия в мобилизации специфических и азурофильных гранул. Специфические гранулы легче секретируются под действием меньших концентраций агонистов. Потенциально более деструктивные азурофильные гранулы выделяют свое содержимое вначале в фагосому, а для выделения за пределы клетки они нуждаются в очень высокой концентрации агонистов.
 § Кислые протеазы разрушают белки при кислых значениях р. Н. Наиболее вероятным механизмом их действия является разрушение бактерий и тканевого детрита в фаголизосомах, где имеется кислое значение р. Н. § Нейтральные протеазы способны разрушать различные внеклеточные компоненты. Эти ферменты могут атаковать коллаген, базальную мембрану, фибрин, эластин и хрящ, вызывая разрушение тканей, характерное для гнойного воспаления. § Могут расщеплять С 3 и С 5 компоненты, выделяя анафилатоксины и кининоподобный пептид из кининогена. Моноциты и макрофаги также содержат кислые гидролазы, коллагеназу, эластазу и активатор плазминогена. Они наиболее активны при хроническом воспалении. Изначальная лейкоцитарная инфильтрация может потенцировать дальнейшее увеличение сосудистой проницаемости, хемотаксиса и тканевых повреждений. § Протеазы регулируются системой ингибиторов протеаз, содержащейся в сыворотке крови или тканевой жидкости. Дефицит этих ингибиторов может привести к усилению действия лейкоцитарных протеаз.
§ Кислые протеазы разрушают белки при кислых значениях р. Н. Наиболее вероятным механизмом их действия является разрушение бактерий и тканевого детрита в фаголизосомах, где имеется кислое значение р. Н. § Нейтральные протеазы способны разрушать различные внеклеточные компоненты. Эти ферменты могут атаковать коллаген, базальную мембрану, фибрин, эластин и хрящ, вызывая разрушение тканей, характерное для гнойного воспаления. § Могут расщеплять С 3 и С 5 компоненты, выделяя анафилатоксины и кининоподобный пептид из кининогена. Моноциты и макрофаги также содержат кислые гидролазы, коллагеназу, эластазу и активатор плазминогена. Они наиболее активны при хроническом воспалении. Изначальная лейкоцитарная инфильтрация может потенцировать дальнейшее увеличение сосудистой проницаемости, хемотаксиса и тканевых повреждений. § Протеазы регулируются системой ингибиторов протеаз, содержащейся в сыворотке крови или тканевой жидкости. Дефицит этих ингибиторов может привести к усилению действия лейкоцитарных протеаз.
 § Свободные кислородные радикалы могут выделяться лейкоцитами за пределы клетки под действием хемотаксических агентов, иммунных комплексов или факторов, стимулирующих фагоцитоз. Их продукция зависит от активации NАDР окислительной системы и образования перекиси. Сыворотка, тканевая жидкость и клетки мишени обладают защитными механизмами, которые обеспечивают детоксикацию потенциально опасных радикалов кислорода. Эти антиоксиданты включают содержащий медь сывороточный белок церулоплазмин; железосодержащую фракцию сыворотки трансфер рин фермент супероксиддисмутазу, которая ; находится или может быть активирована в различных типах клеток; ферменты каталазу и глютатионпероксидазу. Таким образом, влияние свободных радикалов кислорода при любой воспалительной реакции зависит от баланса между образованием и разрушением этих метаболитов клетками и тканями. § Нейропептиды (субстанция Р) вызывают расширение сосудов и увеличение их проницаемости как непосредственно, так и путем стимуляции выброса гистамина и эйкозаноидов тучными клетками. Таким образом, любая стадия воспалительного ответа на повреждение характеризуется своим спектром медиаторов, которые обеспечивают регуляцию основных событий, характерных только для этой стадии.
§ Свободные кислородные радикалы могут выделяться лейкоцитами за пределы клетки под действием хемотаксических агентов, иммунных комплексов или факторов, стимулирующих фагоцитоз. Их продукция зависит от активации NАDР окислительной системы и образования перекиси. Сыворотка, тканевая жидкость и клетки мишени обладают защитными механизмами, которые обеспечивают детоксикацию потенциально опасных радикалов кислорода. Эти антиоксиданты включают содержащий медь сывороточный белок церулоплазмин; железосодержащую фракцию сыворотки трансфер рин фермент супероксиддисмутазу, которая ; находится или может быть активирована в различных типах клеток; ферменты каталазу и глютатионпероксидазу. Таким образом, влияние свободных радикалов кислорода при любой воспалительной реакции зависит от баланса между образованием и разрушением этих метаболитов клетками и тканями. § Нейропептиды (субстанция Р) вызывают расширение сосудов и увеличение их проницаемости как непосредственно, так и путем стимуляции выброса гистамина и эйкозаноидов тучными клетками. Таким образом, любая стадия воспалительного ответа на повреждение характеризуется своим спектром медиаторов, которые обеспечивают регуляцию основных событий, характерных только для этой стадии.
 Классификация воспаления § по этиологии с установленной или неустановленной этиологией. Хроническое воспаление бактериальной этиологии подразделяется на банальное и специфическое. Специфическим называют воспаление при 5 хронических инфекционных заболеваниях: туберкулезе, сифилисе, лепре, сапе и риносклероме; § по течению острое и хроническое. При некоторых заболеваниях выделяют также под острый тип воспаления, однако критерии его выделения весьма условны; § по морфологии (по типу преобладающей тканевой реакции) экссудативное и продуктивное, каждое из которых подразделяется на несколько видов. Экссудативное воспаление характеризуется преобладанием экссудации с образованием экссудата в тканях и полостях тела. Продуктивное воспаление характеризуется преобладанием продуктивной тканевой реакции с пролиферацией и дифференцировкой клеточных элементов гематогенного и гистиогенного происхождения в очаге воспаления. Разновидностью продуктивного воспаления является гранулематозное с образованием гранулем.
Классификация воспаления § по этиологии с установленной или неустановленной этиологией. Хроническое воспаление бактериальной этиологии подразделяется на банальное и специфическое. Специфическим называют воспаление при 5 хронических инфекционных заболеваниях: туберкулезе, сифилисе, лепре, сапе и риносклероме; § по течению острое и хроническое. При некоторых заболеваниях выделяют также под острый тип воспаления, однако критерии его выделения весьма условны; § по морфологии (по типу преобладающей тканевой реакции) экссудативное и продуктивное, каждое из которых подразделяется на несколько видов. Экссудативное воспаление характеризуется преобладанием экссудации с образованием экссудата в тканях и полостях тела. Продуктивное воспаление характеризуется преобладанием продуктивной тканевой реакции с пролиферацией и дифференцировкой клеточных элементов гематогенного и гистиогенного происхождения в очаге воспаления. Разновидностью продуктивного воспаления является гранулематозное с образованием гранулем.
 Острое воспаление форма воспалительной реакции, развивающейся немедленно после воздействия повреждающего агента и характеризующейся преобладанием экссудативной тканевой реакции, а также быстрым завершением с элиминацией повреждающего агента и репарацией ткани. § Экссудативная тканевая реакция при остром воспалении характеризуется изменениями кровотока в сосудах микроциркуляторного русла (артериолах, капиллярах и венулах) в ответ на инициальное повреждение; образованием жидкой части воспалительного экссудата за счет повышения тканево сосудистой проницаемости в результате структурных перестроек в микроциркуляторном русле; эмиграцией клеточных элементов (преимущественно нейтрофильных лейкоцитов) и фагоцитозом в очаге воспаления.
Острое воспаление форма воспалительной реакции, развивающейся немедленно после воздействия повреждающего агента и характеризующейся преобладанием экссудативной тканевой реакции, а также быстрым завершением с элиминацией повреждающего агента и репарацией ткани. § Экссудативная тканевая реакция при остром воспалении характеризуется изменениями кровотока в сосудах микроциркуляторного русла (артериолах, капиллярах и венулах) в ответ на инициальное повреждение; образованием жидкой части воспалительного экссудата за счет повышения тканево сосудистой проницаемости в результате структурных перестроек в микроциркуляторном русле; эмиграцией клеточных элементов (преимущественно нейтрофильных лейкоцитов) и фагоцитозом в очаге воспаления.
 Клинические признаки § § § повышение температуры тела (саlоr); покраснение (rubor); отек (tumor); боль (dolor); потеря функции (fuпctio laesa).
Клинические признаки § § § повышение температуры тела (саlоr); покраснение (rubor); отек (tumor); боль (dolor); потеря функции (fuпctio laesa).
 Виды остpoгo воспаления Морфологической особенностью острого воспаления является преобладание экссудативной тканевой реакции. § Острое воспаление классифицируется в зависимости от его локализации и вида образующегося экссудата. § При локализации процесса на слизистых оболочках наблюдается гиперпродукция слизи, которая примешивается к воспалительному экссудату, что и определяет развитие особого вида экссудативного воспаления катарального.
Виды остpoгo воспаления Морфологической особенностью острого воспаления является преобладание экссудативной тканевой реакции. § Острое воспаление классифицируется в зависимости от его локализации и вида образующегося экссудата. § При локализации процесса на слизистых оболочках наблюдается гиперпродукция слизи, которая примешивается к воспалительному экссудату, что и определяет развитие особого вида экссудативного воспаления катарального.
 Виды экссудата § серозный экссудат содержит до 2 % белка, единичные нейтрофильные лейкоциты, слущенные поврежденные эпителиальные клетки; § фибринозный экссудат богат фибрином; § гнойный экссудат богат белками содержит большое количество нейтрофильных лейкоцитов и тканевый детрит, образовавшийся в результате лизиса тканей; § геморрагический экссудат характеризуется преобладанием эритроцитов; § гнилостный экссудат связан с гнилостной флорой; § смешанные формы.
Виды экссудата § серозный экссудат содержит до 2 % белка, единичные нейтрофильные лейкоциты, слущенные поврежденные эпителиальные клетки; § фибринозный экссудат богат фибрином; § гнойный экссудат богат белками содержит большое количество нейтрофильных лейкоцитов и тканевый детрит, образовавшийся в результате лизиса тканей; § геморрагический экссудат характеризуется преобладанием эритроцитов; § гнилостный экссудат связан с гнилостной флорой; § смешанные формы.
 В зависимости от характера экссудата выделяют различные виды экссудативного воспаления: § § § § серозное; фибринозное крупозное и дифтеритическое; гнойное очаговое (абсцесс), диффузное (флегмона), эмпиема; геморрагическое; гнилостное; смешанное; катаральное.
В зависимости от характера экссудата выделяют различные виды экссудативного воспаления: § § § § серозное; фибринозное крупозное и дифтеритическое; гнойное очаговое (абсцесс), диффузное (флегмона), эмпиема; геморрагическое; гнилостное; смешанное; катаральное.
 Серозное воспаление характеризуется образованием серозного экссудата. Серозное воспаление развивается чаще всего в серозных полостях, слизистых оболочках, синовиальных и мягких мозговых оболочках, реже во внутренних органах. § Этиология может определяться различными инфекционными агентами, физическими факторами, эндогенно образующимися токсическими веществами (аутоинтоксикация). Серозное воспаление характерно для многих вирусных инфекций. Так, в коже при инфекциях, вызванных вирусами семейства Herpesviridae (простой герпес, ветряная оспа), возникает серозное воспаление с образованием пузырей. Некоторые бактерии (микобактерия туберкулеза, менингококк, диплококк, шигелла) также могут вызывать серозное воспаление. Термические, реже химические, ожоги характеризуются образованием в коже пузырей, наполненных серозным экссудатом. Серозный экссудат способствует удалению из пораженных тканей возбудителей и токсинов.
Серозное воспаление характеризуется образованием серозного экссудата. Серозное воспаление развивается чаще всего в серозных полостях, слизистых оболочках, синовиальных и мягких мозговых оболочках, реже во внутренних органах. § Этиология может определяться различными инфекционными агентами, физическими факторами, эндогенно образующимися токсическими веществами (аутоинтоксикация). Серозное воспаление характерно для многих вирусных инфекций. Так, в коже при инфекциях, вызванных вирусами семейства Herpesviridae (простой герпес, ветряная оспа), возникает серозное воспаление с образованием пузырей. Некоторые бактерии (микобактерия туберкулеза, менингококк, диплококк, шигелла) также могут вызывать серозное воспаление. Термические, реже химические, ожоги характеризуются образованием в коже пузырей, наполненных серозным экссудатом. Серозный экссудат способствует удалению из пораженных тканей возбудителей и токсинов.
 § Морфология зависит от локализации воспаления. Так, в паренхиматозных органах серозный экссудат скапливается обычно в интерстиции, а при воспалении серозных оболочек в серозных полостях. Макроскопически серозные оболочки несколько утолщены, гиперемированы, тусклые, пропитаны серозным экссудатом, который имеет вид мутноватой жидкости. Такая же картина наблюдается в мягких мозговых оболочках, которые становятся тусклыми, утолщенными, набухшими. При микроскопическом исследовании обнаруживают отек и незначительную инфильтрацию оболочек и тканей нейтрофильными лейкоцитами, полнокровие сосудов микроциркуляции, слущивание мезотелиальных клеток. Серозный экссудат беден клеточными элементами, среди которых преобладают слущенные мезотелиальные клетки и единичные нейтрофильные лейкоциты. В печени серозный экссудат скапливается перисинусоидально, в миокарде между мышечными волокнами, в почках в просвете капсулы клубочка. Серозное воспаление паренхиматозных органов сопровождается дистрофией паренхиматозных клеток. Серозное воспаление кожи характеризуется скоплением выпота в толще эпидермиса, иногда экссудат накапливается под эпидермисом, отслаивая его от дермы с образованием крупных пузырей (например, при ожогах).
§ Морфология зависит от локализации воспаления. Так, в паренхиматозных органах серозный экссудат скапливается обычно в интерстиции, а при воспалении серозных оболочек в серозных полостях. Макроскопически серозные оболочки несколько утолщены, гиперемированы, тусклые, пропитаны серозным экссудатом, который имеет вид мутноватой жидкости. Такая же картина наблюдается в мягких мозговых оболочках, которые становятся тусклыми, утолщенными, набухшими. При микроскопическом исследовании обнаруживают отек и незначительную инфильтрацию оболочек и тканей нейтрофильными лейкоцитами, полнокровие сосудов микроциркуляции, слущивание мезотелиальных клеток. Серозный экссудат беден клеточными элементами, среди которых преобладают слущенные мезотелиальные клетки и единичные нейтрофильные лейкоциты. В печени серозный экссудат скапливается перисинусоидально, в миокарде между мышечными волокнами, в почках в просвете капсулы клубочка. Серозное воспаление паренхиматозных органов сопровождается дистрофией паренхиматозных клеток. Серозное воспаление кожи характеризуется скоплением выпота в толще эпидермиса, иногда экссудат накапливается под эпидермисом, отслаивая его от дермы с образованием крупных пузырей (например, при ожогах).
 Исходы серозного воспаления § Благоприятные(экссудат обычно рассасывается без каких либо последствий). § Неблагоприятные интерстициальный фиброз паренхиматозных органов; серозный экссудат в мозговых оболочках может привести к нарушению оттока цереброспинальной жидкости (ликвора) и отеку мозга, выпот в перикарде затрудняет работу сердца серозное воспаление паренхимы легкого может привести к острой дыхательной недостаточности.
Исходы серозного воспаления § Благоприятные(экссудат обычно рассасывается без каких либо последствий). § Неблагоприятные интерстициальный фиброз паренхиматозных органов; серозный экссудат в мозговых оболочках может привести к нарушению оттока цереброспинальной жидкости (ликвора) и отеку мозга, выпот в перикарде затрудняет работу сердца серозное воспаление паренхимы легкого может привести к острой дыхательной недостаточности.
 Фибринозное воспаление § характеризуется образованием фибринозного экссудата. Помимо фибрина в экссудате обнаруживают также нейтрофильные лейкоциты и элементы некротизированных тканей. Фибринозное воспаление чаще локализуется на серозных и слизистых оболочках. Кроме того, оно может развиваться в легком при крупозной пневмонии и очаговой пневмонии с фибринозным экссудатом. § Этиология фибринозного воспаления разнообразна. Это воспаление вызывают бактерии, вирусы, химические вещества экзогенного и эндогенного происхождения.
Фибринозное воспаление § характеризуется образованием фибринозного экссудата. Помимо фибрина в экссудате обнаруживают также нейтрофильные лейкоциты и элементы некротизированных тканей. Фибринозное воспаление чаще локализуется на серозных и слизистых оболочках. Кроме того, оно может развиваться в легком при крупозной пневмонии и очаговой пневмонии с фибринозным экссудатом. § Этиология фибринозного воспаления разнообразна. Это воспаление вызывают бактерии, вирусы, химические вещества экзогенного и эндогенного происхождения.
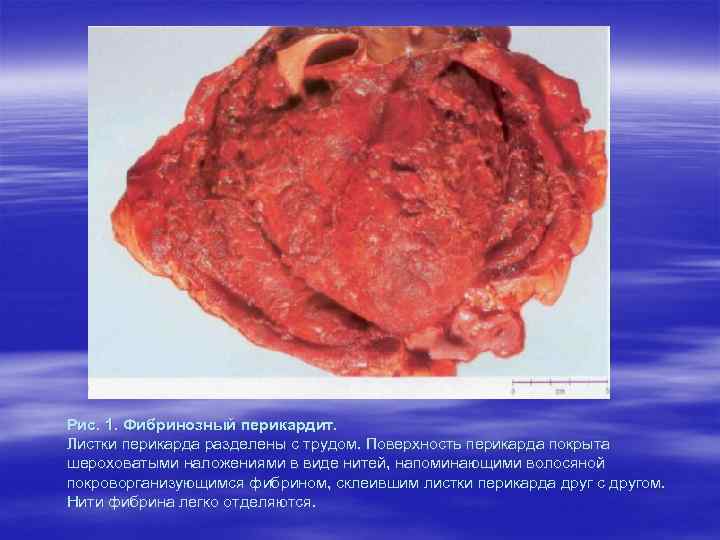 Рис. 1. Фибринозный перикардит. Листки перикарда разделены с трудом. Поверхность перикарда покрыта шероховатыми наложениями в виде нитей, напоминающими волосяной покроворганизующимся фибрином, склеившим листки перикарда друг с другом. Нити фибрина легко отделяются.
Рис. 1. Фибринозный перикардит. Листки перикарда разделены с трудом. Поверхность перикарда покрыта шероховатыми наложениями в виде нитей, напоминающими волосяной покроворганизующимся фибрином, склеившим листки перикарда друг с другом. Нити фибрина легко отделяются.
 § Иногда этиология может быть неустановленной, как это бывает при ревматических болезнях. Фиброзное воспаление может развиваться при реакциях гиперчувствительности I, II и III типов, а также при аутоиммунных заболеваниях. Среди инфекционных агентов следует назвать дифтерийную коринебактерию, шигеллы, диплококки, пневмококки, стрептококки и стафилококки, некоторые вирусы. Примером фибринозного воспаления, вызванного аутоинтоксикацией, служит фибринозное воспаление при почечной недостаточности (уремии). § Патогенез определяется: выраженным повреждением ткани в очаге воспаления с развитием ее некроза резким повышением проницаемости сосудистой стенки, что может быть обусловлено, с одной стороны, особенностями бактериальных токсинов (например, вазопаралитическое действие экзотоксина дифтерийной коринебактерии), с другой гиперергической реакцией организма.
§ Иногда этиология может быть неустановленной, как это бывает при ревматических болезнях. Фиброзное воспаление может развиваться при реакциях гиперчувствительности I, II и III типов, а также при аутоиммунных заболеваниях. Среди инфекционных агентов следует назвать дифтерийную коринебактерию, шигеллы, диплококки, пневмококки, стрептококки и стафилококки, некоторые вирусы. Примером фибринозного воспаления, вызванного аутоинтоксикацией, служит фибринозное воспаление при почечной недостаточности (уремии). § Патогенез определяется: выраженным повреждением ткани в очаге воспаления с развитием ее некроза резким повышением проницаемости сосудистой стенки, что может быть обусловлено, с одной стороны, особенностями бактериальных токсинов (например, вазопаралитическое действие экзотоксина дифтерийной коринебактерии), с другой гиперергической реакцией организма.
 § Морфология фибринозного воспаления. При макроскопическом исследовании на поверхности слизистых или серозных оболочек обнаруживают светло серую пленку. Из за внешнего сходства с пленкой или мембраной в зарубежной литературе фибринозное воспаление получило название мембранозного или псевдомембранозного. Выделяют 2 вида фибринозного воспаления в зависимости от глубины некроза и вида эпителия: § крупозное § дифтеритическое.
§ Морфология фибринозного воспаления. При макроскопическом исследовании на поверхности слизистых или серозных оболочек обнаруживают светло серую пленку. Из за внешнего сходства с пленкой или мембраной в зарубежной литературе фибринозное воспаление получило название мембранозного или псевдомембранозного. Выделяют 2 вида фибринозного воспаления в зависимости от глубины некроза и вида эпителия: § крупозное § дифтеритическое.
 Крупозное воспаление развивается при поверхностном некрозе и чаще на однослойном эпителии слизистой или серозной оболочки, имеющем плотную соединительнотканную основу. При крупозном воспалении пленка рыхло связана с подлежащими тканями. При этом фибринозная пленка тонкая, легко снимающаяся. При отделении такой пленки образуются поверхностные дефекты. Слизистая оболочка набухшая, тусклая. Серозная оболочка тусклая, покрыта серо белым налетом или серыми нитями фибрина, поэтому ее образно сравнивают с маслом, покрывающим хлеб ("bred аnd butter "), или же с волосяным покровом (фибринозное воспаление перикарда называют волосатым сердцем). Фибринозное воспаление в легком с образованием крупозного экссудата в альвеолах и на плевре называют крупозной пневмонией.
Крупозное воспаление развивается при поверхностном некрозе и чаще на однослойном эпителии слизистой или серозной оболочки, имеющем плотную соединительнотканную основу. При крупозном воспалении пленка рыхло связана с подлежащими тканями. При этом фибринозная пленка тонкая, легко снимающаяся. При отделении такой пленки образуются поверхностные дефекты. Слизистая оболочка набухшая, тусклая. Серозная оболочка тусклая, покрыта серо белым налетом или серыми нитями фибрина, поэтому ее образно сравнивают с маслом, покрывающим хлеб ("bred аnd butter "), или же с волосяным покровом (фибринозное воспаление перикарда называют волосатым сердцем). Фибринозное воспаление в легком с образованием крупозного экссудата в альвеолах и на плевре называют крупозной пневмонией.
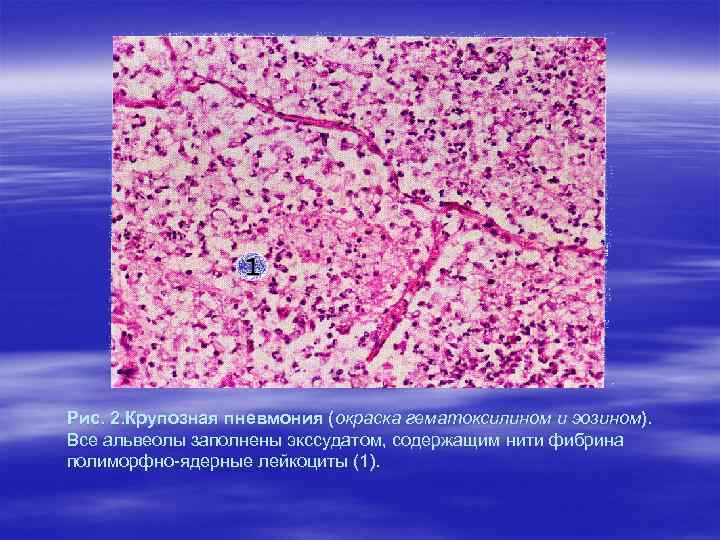 Рис. 2. Крупозная пневмония (окраска гематоксилином и эозином). Все альвеолы заполнены экссудатом, содержащим нити фибрина полиморфно ядерные лейкоциты (1).
Рис. 2. Крупозная пневмония (окраска гематоксилином и эозином). Все альвеолы заполнены экссудатом, содержащим нити фибрина полиморфно ядерные лейкоциты (1).
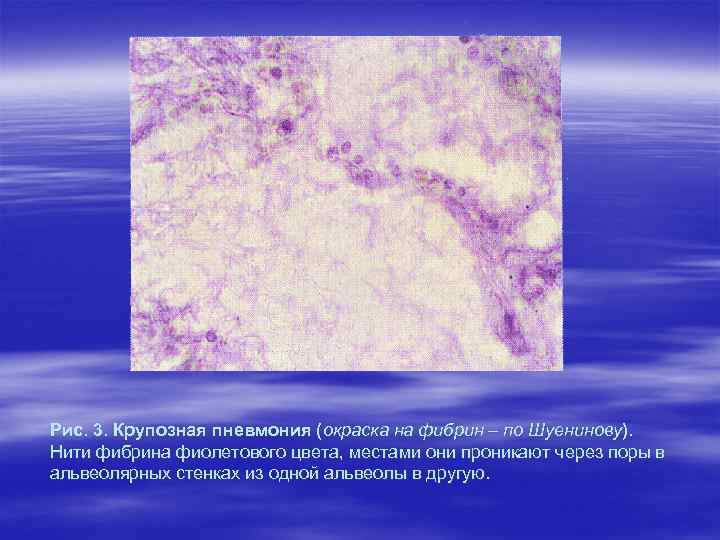 Рис. 3. Крупозная пневмония (окраска на фибрин – по Шуенинову). Нити фибрина фиолетового цвета, местами они проникают через поры в альвеолярных стенках из одной альвеолы в другую.
Рис. 3. Крупозная пневмония (окраска на фибрин – по Шуенинову). Нити фибрина фиолетового цвета, местами они проникают через поры в альвеолярных стенках из одной альвеолы в другую.
 Дифтеритическое воспаление возникает при глубоком некрозе и чаще на слизистых оболочках, покрытых многослойным плоским эпителием или однослойным эпителием с рыхлой соединительнотканной основой, способствующей развитию глубокого некроза ткани. В таких случаях фибринозная пленка толстая, трудно снимающаяся, при ее отторжении возникает глубокий дефект ткани. Дифтеритическое воспаление может появиться в зеве, на истинных голосовых связках, в эндометрии, на слизистой оболочке влагалища, мочевого пузыря, желудка и кишечника, как казуистический случай – в ранах.
Дифтеритическое воспаление возникает при глубоком некрозе и чаще на слизистых оболочках, покрытых многослойным плоским эпителием или однослойным эпителием с рыхлой соединительнотканной основой, способствующей развитию глубокого некроза ткани. В таких случаях фибринозная пленка толстая, трудно снимающаяся, при ее отторжении возникает глубокий дефект ткани. Дифтеритическое воспаление может появиться в зеве, на истинных голосовых связках, в эндометрии, на слизистой оболочке влагалища, мочевого пузыря, желудка и кишечника, как казуистический случай – в ранах.
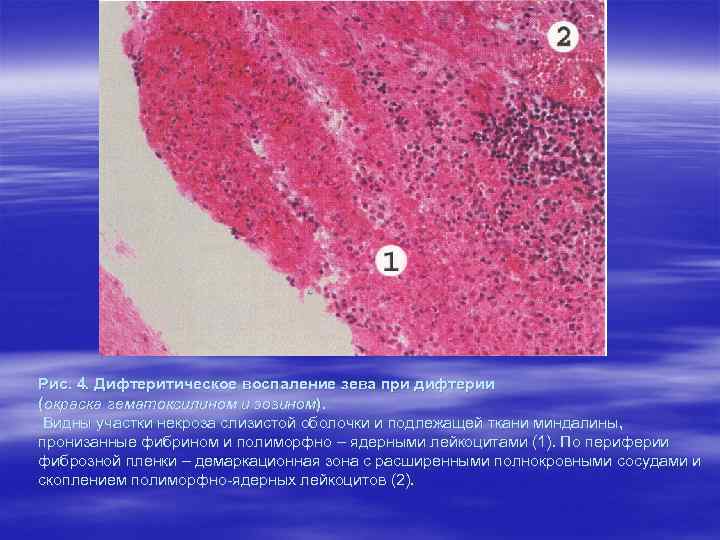 Рис. 4. Дифтеритическое воспаление зева при дифтерии (окраска гематоксилином и эозином). Видны участки некроза слизистой оболочки и подлежащей ткани миндалины, пронизанные фибрином и полиморфно – ядерными лейкоцитами (1). По периферии фиброзной пленки – демаркационная зона с расширенными полнокровными сосудами и скоплением полиморфно ядерных лейкоцитов (2).
Рис. 4. Дифтеритическое воспаление зева при дифтерии (окраска гематоксилином и эозином). Видны участки некроза слизистой оболочки и подлежащей ткани миндалины, пронизанные фибрином и полиморфно – ядерными лейкоцитами (1). По периферии фиброзной пленки – демаркационная зона с расширенными полнокровными сосудами и скоплением полиморфно ядерных лейкоцитов (2).
 Исходы фибринозного воспаления § § Благоприятные на слизистых оболочках: заживление с полным или неполным (с формированием рубца) восстановлением тканей. Вид заживления определяется тем, что при отторжении фибринозных пленок образуются язвы: поверхностные при крупозном воспалении и глубокие при дифтеритическом. Поверхностные язвы обычно регенерируют полностью, при заживлении глубоких язв образуются рубцы. В легком при крупозной пневмонии экссудат расплавляется протеолитическими ферментами нейтрофилов и рассасывается макрофагами. Неблагоприятные развитием разного рода осложнений. Судьба экссудата во многом зависит от активности и сбалансированной работы нейтрофильного лейкоцита и макрофага. Следует отметить, что фибринозный экссудат трудно поддается резорбции лейкоцитами. При недостаточной протеолитической функции нейтрофилов на месте экссудата появляется соединительная ткань (происходит организация экссудата). На серозных оболочках фибринозный экссудат чаще подвергается организации с образованием спаек между листками этих оболочек. Может произойти полная облитерация серозной полости с последующим кальцинозом, как это бывает при развитии панцирного сердца в исходе ревматического перикардита. Напротив, при чрезмерной активности нейтрофилов и макрофагов возможно возникновение гнойного воспаления, например абсцесса легкого или эмпиемы плевры, как это бывает при крупозной пневмонии.
Исходы фибринозного воспаления § § Благоприятные на слизистых оболочках: заживление с полным или неполным (с формированием рубца) восстановлением тканей. Вид заживления определяется тем, что при отторжении фибринозных пленок образуются язвы: поверхностные при крупозном воспалении и глубокие при дифтеритическом. Поверхностные язвы обычно регенерируют полностью, при заживлении глубоких язв образуются рубцы. В легком при крупозной пневмонии экссудат расплавляется протеолитическими ферментами нейтрофилов и рассасывается макрофагами. Неблагоприятные развитием разного рода осложнений. Судьба экссудата во многом зависит от активности и сбалансированной работы нейтрофильного лейкоцита и макрофага. Следует отметить, что фибринозный экссудат трудно поддается резорбции лейкоцитами. При недостаточной протеолитической функции нейтрофилов на месте экссудата появляется соединительная ткань (происходит организация экссудата). На серозных оболочках фибринозный экссудат чаще подвергается организации с образованием спаек между листками этих оболочек. Может произойти полная облитерация серозной полости с последующим кальцинозом, как это бывает при развитии панцирного сердца в исходе ревматического перикардита. Напротив, при чрезмерной активности нейтрофилов и макрофагов возможно возникновение гнойного воспаления, например абсцесса легкого или эмпиемы плевры, как это бывает при крупозной пневмонии.
 § При дифтерии зева некроз тканей глубокий, фибринозная пленка плотно связана с подлежащими тканями, что обеспечивает благоприятные условия для размножения возбудителей и продукции ими большого количества экзотоксина, поступающего в кровоток. При этом развивается токсическая форма дифтерии тяжелая интоксикация токсинами коринебактерий и продуктами распада некротизированных тканей. § При дифтерии трахеи интоксикация выражена незначительно, однако легко отторгающиеся пленки закрывают просвет верхних дыхательных путей, что приводит к истинному крупу (по шотландски crоup хриплый кашель) и может закончиться асфиксией.
§ При дифтерии зева некроз тканей глубокий, фибринозная пленка плотно связана с подлежащими тканями, что обеспечивает благоприятные условия для размножения возбудителей и продукции ими большого количества экзотоксина, поступающего в кровоток. При этом развивается токсическая форма дифтерии тяжелая интоксикация токсинами коринебактерий и продуктами распада некротизированных тканей. § При дифтерии трахеи интоксикация выражена незначительно, однако легко отторгающиеся пленки закрывают просвет верхних дыхательных путей, что приводит к истинному крупу (по шотландски crоup хриплый кашель) и может закончиться асфиксией.
 Гнойное воспаление развивается при образовании гнойного экссудата (гноя). Гнойный экссудат содержит много белков (в основном глобулинов), нейтрофильных лейкоцитов, лизированные ткани (тканевый детрит) и колонии гноеродных микроорганизмов. Нейтрофилы погибают через 8 12 ч. после попадания в очаг воспаления. Такие распадающиеся клетки называют гнойными тельцами. Помимо живых нейтрофилов и гнойных телец, в гнойном экссудате могут присутствовать немногочисленные лимфоциты и макрофаги. Гнойный экссудат содержит большое количество ферментов, в первую очередь нейтральных протеаз (эластаза, катепсин G и коллагеназа), выделяющихся из лизосом распадающихся нейтрофилов, расплавляющих ткани (гистолиз). Поэтому при вскрытии очага гнойного воспаления и дренировании гноя на его месте остается полость. Протеиназы нейтрофилов повышают проницаемость сосудов, способствуют образованию хемотаксических веществ и усиливают фагоцитоз. Гной обладает также бактерицидными свойствами благодаря бактерицидным веществам, выделяемым нейтрофилами (катионные белки, активные формы кислорода).
Гнойное воспаление развивается при образовании гнойного экссудата (гноя). Гнойный экссудат содержит много белков (в основном глобулинов), нейтрофильных лейкоцитов, лизированные ткани (тканевый детрит) и колонии гноеродных микроорганизмов. Нейтрофилы погибают через 8 12 ч. после попадания в очаг воспаления. Такие распадающиеся клетки называют гнойными тельцами. Помимо живых нейтрофилов и гнойных телец, в гнойном экссудате могут присутствовать немногочисленные лимфоциты и макрофаги. Гнойный экссудат содержит большое количество ферментов, в первую очередь нейтральных протеаз (эластаза, катепсин G и коллагеназа), выделяющихся из лизосом распадающихся нейтрофилов, расплавляющих ткани (гистолиз). Поэтому при вскрытии очага гнойного воспаления и дренировании гноя на его месте остается полость. Протеиназы нейтрофилов повышают проницаемость сосудов, способствуют образованию хемотаксических веществ и усиливают фагоцитоз. Гной обладает также бактерицидными свойствами благодаря бактерицидным веществам, выделяемым нейтрофилами (катионные белки, активные формы кислорода).
 § Этиология Гнойное воспаление вызывают гноеродные бактерии и грибы: стафилококки, стрептококки, гонококки, менингококки, диплококки, брюшнотифозные палочки, аспергиллы, кандиды и др. Возможно также и асептическое гнойное воспаление, например при попадании в ткани некоторых химических агентов (скипидар, керосин, отравляющие вещества), патогенез которого связан с индукцией данными агентами чрезмерной активности нейтрофильных лейкоцитов. § Морфология Гнойное воспаление может возникать в любых органах и тканях и быть острым и хроническим. При макроскопическом исследовании гной представляет собой густую сливкообразную массу желто зеленого цвета с характерным запахом.
§ Этиология Гнойное воспаление вызывают гноеродные бактерии и грибы: стафилококки, стрептококки, гонококки, менингококки, диплококки, брюшнотифозные палочки, аспергиллы, кандиды и др. Возможно также и асептическое гнойное воспаление, например при попадании в ткани некоторых химических агентов (скипидар, керосин, отравляющие вещества), патогенез которого связан с индукцией данными агентами чрезмерной активности нейтрофильных лейкоцитов. § Морфология Гнойное воспаление может возникать в любых органах и тканях и быть острым и хроническим. При макроскопическом исследовании гной представляет собой густую сливкообразную массу желто зеленого цвета с характерным запахом.
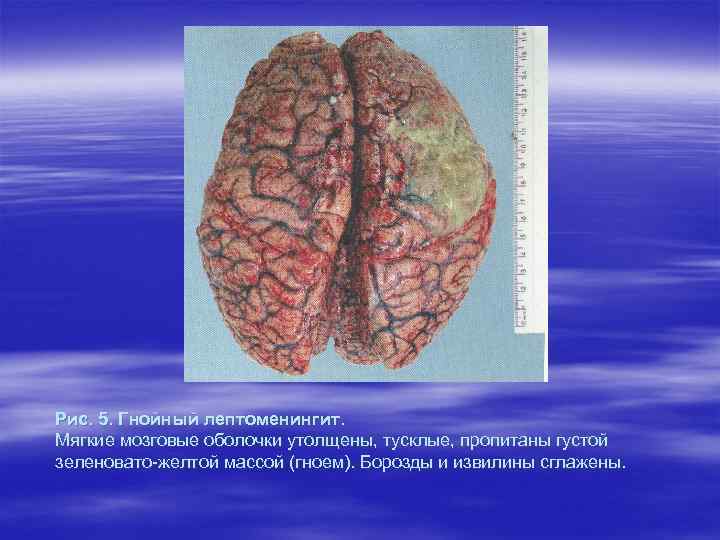 Рис. 5. Гнойный лептоменингит. Мягкие мозговые оболочки утолщены, тусклые, пропитаны густой зеленовато желтой массой (гноем). Борозды и извилины сглажены.
Рис. 5. Гнойный лептоменингит. Мягкие мозговые оболочки утолщены, тусклые, пропитаны густой зеленовато желтой массой (гноем). Борозды и извилины сглажены.
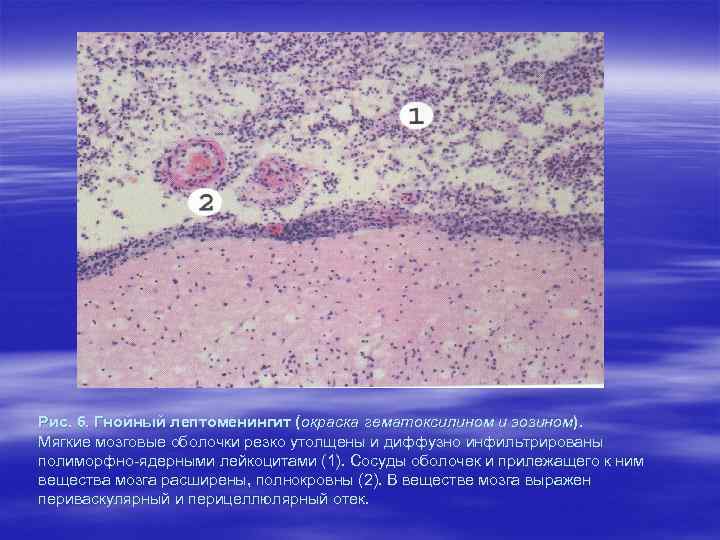 Рис. 6. Гнойный лептоменингит (окраска гематоксилином и эозином). Мягкие мозговые оболочки резко утолщены и диффузно инфильтрированы полиморфно ядерными лейкоцитами (1). Сосуды оболочек и прилежащего к ним вещества мозга расширены, полнокровны (2). В веществе мозга выражен периваскулярный и перицеллюлярный отек.
Рис. 6. Гнойный лептоменингит (окраска гематоксилином и эозином). Мягкие мозговые оболочки резко утолщены и диффузно инфильтрированы полиморфно ядерными лейкоцитами (1). Сосуды оболочек и прилежащего к ним вещества мозга расширены, полнокровны (2). В веществе мозга выражен периваскулярный и перицеллюлярный отек.
 Формы гнойного воспаления 1 абсцесс; 2 флегмона; 3 эмпиема.
Формы гнойного воспаления 1 абсцесс; 2 флегмона; 3 эмпиема.
 § Абсцесс очаговое гнойное воспаление, характеризующееся расплавлением ткани с образованием полости, заполненной гноем. Вокруг острого абсцесса формируется зона демаркационного серозного воспаления. Абсцесс может иметь хроническое течение. При этом он окружается валом грануляционной ткани, через многочисленные капилляры которой в полость абсцесса поступают лейкоциты, поэтому ее называют пиогенной мембраной. При длительном течении воспаления грануляционная ткань, образующая пиогенную мембрану, созревает, и в мембране формируются два слоя: внутренний, состоящий из грануляций, и наружный, представленный зрелой волокнистой соединительной тканью.
§ Абсцесс очаговое гнойное воспаление, характеризующееся расплавлением ткани с образованием полости, заполненной гноем. Вокруг острого абсцесса формируется зона демаркационного серозного воспаления. Абсцесс может иметь хроническое течение. При этом он окружается валом грануляционной ткани, через многочисленные капилляры которой в полость абсцесса поступают лейкоциты, поэтому ее называют пиогенной мембраной. При длительном течении воспаления грануляционная ткань, образующая пиогенную мембрану, созревает, и в мембране формируются два слоя: внутренний, состоящий из грануляций, и наружный, представленный зрелой волокнистой соединительной тканью.
 Рис. 7. Эмболический гнойный нефрит. Почка увеличена в размерах, дряблой консистенции. На поверхности и на разрезе почки в корковом и мозговом веществе видны многочисленные округлой формы очажки серовато желтого цвета, содержащие гной (абсцессы).
Рис. 7. Эмболический гнойный нефрит. Почка увеличена в размерах, дряблой консистенции. На поверхности и на разрезе почки в корковом и мозговом веществе видны многочисленные округлой формы очажки серовато желтого цвета, содержащие гной (абсцессы).
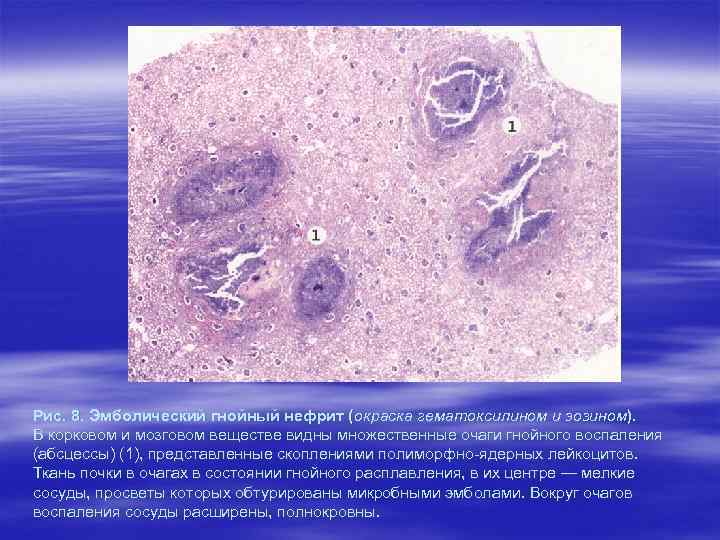 Рис. 8. Эмболический гнойный нефрит (окраска гематоксилином и эозином). В корковом и мозговом веществе видны множественные очаги гнойного воспаления (абсцессы) (1), представленные скоплениями полиморфно ядерных лейкоцитов. Ткань почки в очагах в состоянии гнойного расплавления, в их центре — мелкие сосуды, просветы которых обтурированы микробными эмболами. Вокруг очагов воспаления сосуды расширены, полнокровны.
Рис. 8. Эмболический гнойный нефрит (окраска гематоксилином и эозином). В корковом и мозговом веществе видны множественные очаги гнойного воспаления (абсцессы) (1), представленные скоплениями полиморфно ядерных лейкоцитов. Ткань почки в очагах в состоянии гнойного расплавления, в их центре — мелкие сосуды, просветы которых обтурированы микробными эмболами. Вокруг очагов воспаления сосуды расширены, полнокровны.
 § Флегмона диффузное гнойное воспаление, характеризующееся диффузным распространением гнойного экссудата в тканях, с лизисом тканевых элементов. Флегмона развивается в тканях, где есть условия для легкого распространения гноя в жировой клетчатке, области сухожилий, фасций, по ходу сосудисто нервных пучков и т. д. Диффузное гнойное воспаление может наблюдаться также в мягких мозговых оболочках головного и спинного мозга. При образовании флегмоны, кроме анатомических особенностей, важную роль играют патогенность возбудителя и состояние защитных систем организма. Различают мягкую и твердую флегмону. Мягкая флегмона характеризуется отсутствием видимых очагов некроза в тканях, при твердой флегмоне в тканях образуются очаги коагуляционного некроза, которые не подвергаются расплавлению, а постепенно отторгаются. Флегмону жировой клетчатки называют целлюлитом.
§ Флегмона диффузное гнойное воспаление, характеризующееся диффузным распространением гнойного экссудата в тканях, с лизисом тканевых элементов. Флегмона развивается в тканях, где есть условия для легкого распространения гноя в жировой клетчатке, области сухожилий, фасций, по ходу сосудисто нервных пучков и т. д. Диффузное гнойное воспаление может наблюдаться также в мягких мозговых оболочках головного и спинного мозга. При образовании флегмоны, кроме анатомических особенностей, важную роль играют патогенность возбудителя и состояние защитных систем организма. Различают мягкую и твердую флегмону. Мягкая флегмона характеризуется отсутствием видимых очагов некроза в тканях, при твердой флегмоне в тканях образуются очаги коагуляционного некроза, которые не подвергаются расплавлению, а постепенно отторгаются. Флегмону жировой клетчатки называют целлюлитом.
 § Эмпиема гнойное воспаление полых органов или полостей тела со скоплением в них гноя. В полостях тела эмпиема может образоваться при наличии гнойных очагов в соседних органах (например, эмпиема плевры при абсцессе легкого). Эмпиема полых органов развивается при нарушении оттока гноя при гнойном воспалении (эмпиема желчного пузыря, червеобразного отростка, сустава и т. д. ). При длительном течении эмпиемы слизистые, серозные или синовиальные оболочки некротизируются, на их месте появляется грануляционная ткань, в результате созревания которой образуются спайки или происходит облитерация полостей.
§ Эмпиема гнойное воспаление полых органов или полостей тела со скоплением в них гноя. В полостях тела эмпиема может образоваться при наличии гнойных очагов в соседних органах (например, эмпиема плевры при абсцессе легкого). Эмпиема полых органов развивается при нарушении оттока гноя при гнойном воспалении (эмпиема желчного пузыря, червеобразного отростка, сустава и т. д. ). При длительном течении эмпиемы слизистые, серозные или синовиальные оболочки некротизируются, на их месте появляется грануляционная ткань, в результате созревания которой образуются спайки или происходит облитерация полостей.
 Исходы зависят от множества факторов: вирулентности микробов, состояния защитных сил организма, распространенности воспаления. § Благоприятный исход наблюдается в тех случаях, когда происходит разрешение гнойного воспаления спонтанно или благодаря вскрытию очага хирургом. При спонтанном или хирургическом опорожнении абсцесса его полость спадается и заполняется грануляционной тканью, которая созревает с образованием рубца. Реже абсцесс инкапсулируется, гной сгущается и может подвергнуться петрификации. При флегмоне заживление начинается с отграничения процесса с последующим образованием грубого рубца. § Неблагоприятные исходы и осложнения обусловлены аккумуляцией в очаге воспаления большого числа активных нейтрофильных лейкоцитов, генерирующих высокое количество протеаз, которые способствуют распространению и воспаления, и фактора, его вызвавшего.
Исходы зависят от множества факторов: вирулентности микробов, состояния защитных сил организма, распространенности воспаления. § Благоприятный исход наблюдается в тех случаях, когда происходит разрешение гнойного воспаления спонтанно или благодаря вскрытию очага хирургом. При спонтанном или хирургическом опорожнении абсцесса его полость спадается и заполняется грануляционной тканью, которая созревает с образованием рубца. Реже абсцесс инкапсулируется, гной сгущается и может подвергнуться петрификации. При флегмоне заживление начинается с отграничения процесса с последующим образованием грубого рубца. § Неблагоприятные исходы и осложнения обусловлены аккумуляцией в очаге воспаления большого числа активных нейтрофильных лейкоцитов, генерирующих высокое количество протеаз, которые способствуют распространению и воспаления, и фактора, его вызвавшего.
 § Осложнения: прогрессирующее расплавление окружающих тканей; образование свищей в случаях недостаточного или отсутствия дренирования полости абсцесса, флегмоны или эмпиемы. Свищ представляет собой канал, выстланный грануляционной тканью или эпителием и соединяющий полость абсцесса с полым органом либо поверхностью тела; образование натечников в тех случаях, когда гной распространяется под влиянием силы тяжести по ходу мышечно сухожильных влагалищ, нервно сосудистых пучков, жировых прослоек в нижележащие отделы и образует там скопления. Такие скопления гноя обычно не сопровождаются заметной гиперемией, чувством жара и болью, в связи с чем их называют также холодными абсцессами. Обширные затеки гноя вызывают резкую интоксикацию и приводят к истощению организма; аррозия сосудов с развитием кровотечения при распространении гнойного воспаления на сосудистую стенку; септические инфаркты и гангрена при тромбозе пораженных сосудов (в случае контакта органа с внешней средой говорят о вторичной гангрене); генерализация инфекции при распространении гнойно го воспаления на кровеносные и лимфатические сосуды, при этом возможны гематогенное и лимфогенное рас пространение возбудителя, сепсис и кровотечение; хроническое гнойное воспаление, при длительном течении ведущее к интоксикации, кахексии и развитию вторичного амилоидоза.
§ Осложнения: прогрессирующее расплавление окружающих тканей; образование свищей в случаях недостаточного или отсутствия дренирования полости абсцесса, флегмоны или эмпиемы. Свищ представляет собой канал, выстланный грануляционной тканью или эпителием и соединяющий полость абсцесса с полым органом либо поверхностью тела; образование натечников в тех случаях, когда гной распространяется под влиянием силы тяжести по ходу мышечно сухожильных влагалищ, нервно сосудистых пучков, жировых прослоек в нижележащие отделы и образует там скопления. Такие скопления гноя обычно не сопровождаются заметной гиперемией, чувством жара и болью, в связи с чем их называют также холодными абсцессами. Обширные затеки гноя вызывают резкую интоксикацию и приводят к истощению организма; аррозия сосудов с развитием кровотечения при распространении гнойного воспаления на сосудистую стенку; септические инфаркты и гангрена при тромбозе пораженных сосудов (в случае контакта органа с внешней средой говорят о вторичной гангрене); генерализация инфекции при распространении гнойно го воспаления на кровеносные и лимфатические сосуды, при этом возможны гематогенное и лимфогенное рас пространение возбудителя, сепсис и кровотечение; хроническое гнойное воспаление, при длительном течении ведущее к интоксикации, кахексии и развитию вторичного амилоидоза.
 Геморрагическое воспаление вид воспаления характеризуется геморрагическим экссудатом. В возникновении воспаления основное значение принадлежит резкому повышению проницаемости сосудов микроциркуляторного русла и отрицательному хемотаксису нейтрофилов. § Этиология Геморрагическое воспаление характерно для некоторых тяжелых инфекционных заболеваний из группы карантинных инфекций (чумы, сибирской язвы, натуральной оспы). При этих заболеваниях в экссудате с самого начала преобладают эритроциты. Геморрагическое воспаление при многих инфекциях может быть компонентом смешанного воспаления, как это происходит, например, при гриппе. Кроме того, существует ряд заболеваний легких неустановленной этиологии с иммунным патогенезом, характеризующихся развитием геморрагического воспаления респираторных отделов легких (геморрагические альвеолиты). § Морфология Макроскопически участки геморрагического воспаления напоминают кровоизлияния. Микроскопически в очаге воспаления определяются большое количество эритроцитов, единичные нейтрофилы и макрофаги. Характерно значительное повреждение тканей. § Исход часто неблагоприятный, определяется высокой патогенностью возбудителей, обычно вызывающих геморрагическое воспаление, и тяжестью иммунопатологического процесса.
Геморрагическое воспаление вид воспаления характеризуется геморрагическим экссудатом. В возникновении воспаления основное значение принадлежит резкому повышению проницаемости сосудов микроциркуляторного русла и отрицательному хемотаксису нейтрофилов. § Этиология Геморрагическое воспаление характерно для некоторых тяжелых инфекционных заболеваний из группы карантинных инфекций (чумы, сибирской язвы, натуральной оспы). При этих заболеваниях в экссудате с самого начала преобладают эритроциты. Геморрагическое воспаление при многих инфекциях может быть компонентом смешанного воспаления, как это происходит, например, при гриппе. Кроме того, существует ряд заболеваний легких неустановленной этиологии с иммунным патогенезом, характеризующихся развитием геморрагического воспаления респираторных отделов легких (геморрагические альвеолиты). § Морфология Макроскопически участки геморрагического воспаления напоминают кровоизлияния. Микроскопически в очаге воспаления определяются большое количество эритроцитов, единичные нейтрофилы и макрофаги. Характерно значительное повреждение тканей. § Исход часто неблагоприятный, определяется высокой патогенностью возбудителей, обычно вызывающих геморрагическое воспаление, и тяжестью иммунопатологического процесса.
 Гнилостное воспаление характеризуется наличием в очагах поражения гнилостной флоры. Может развиваться при ранениях во время войн и катастроф, а также в виде спорадических случаев, например в матке после криминального аборта, в толстой кишке у новорожденных (так называемый некротический колит новорожденных). § Этиология Гнилостное воспаление вызывают возбудители анаэробной инфекции и группа клостридий С. peifriпgeпs, С. пovyi, C. septicuт. В развитии воспаления могут участвовать и аэробные бактерии (стафилококки, стрептококки), образующие масляную и уксусную кислоты, СО 2, сероводород и аммиак, что придает экссудату характерный гнилостный (ихорозный) запах. Источником заражения человека, как правило, является земля, где много бактерий и их спор. Гнилостное воспаление чаще всего возникает в ранах с обширным размозжением ткани и нарушенными условиями кровоснабжения. Гнилостное воспаление тканей называют анаэробной гангреной.
Гнилостное воспаление характеризуется наличием в очагах поражения гнилостной флоры. Может развиваться при ранениях во время войн и катастроф, а также в виде спорадических случаев, например в матке после криминального аборта, в толстой кишке у новорожденных (так называемый некротический колит новорожденных). § Этиология Гнилостное воспаление вызывают возбудители анаэробной инфекции и группа клостридий С. peifriпgeпs, С. пovyi, C. septicuт. В развитии воспаления могут участвовать и аэробные бактерии (стафилококки, стрептококки), образующие масляную и уксусную кислоты, СО 2, сероводород и аммиак, что придает экссудату характерный гнилостный (ихорозный) запах. Источником заражения человека, как правило, является земля, где много бактерий и их спор. Гнилостное воспаление чаще всего возникает в ранах с обширным размозжением ткани и нарушенными условиями кровоснабжения. Гнилостное воспаление тканей называют анаэробной гангреной.
 § Морфология Макроскопически очаг гнилостного воспаления (анаэробной гангрены) имеет характерный вид: некротизированные ткани бледные, местами синюшные, выбухают над поверхностью, при пальпации в тканях определяется крепитация, рана издает неприятный запах. Микроскопически на ранних стадиях выявляется серозное или серозно геморрагическое воспаление, которое сменяется распространенными некротическими изменениями. Нейтрофилы, попадающие в очаг воспаления, быстро погибают. Появление достаточно большого количества лейкоцитов служит прогностически благоприятным признаком и свидетельствует о затухании процесса. § Исходы обычно неблагоприятные, что связано с массивностью поражения и снижением резистентности макроорганизма. Выздоровление возможно при активной антибиотикотерапии в сочетании с хирургическим лечением.
§ Морфология Макроскопически очаг гнилостного воспаления (анаэробной гангрены) имеет характерный вид: некротизированные ткани бледные, местами синюшные, выбухают над поверхностью, при пальпации в тканях определяется крепитация, рана издает неприятный запах. Микроскопически на ранних стадиях выявляется серозное или серозно геморрагическое воспаление, которое сменяется распространенными некротическими изменениями. Нейтрофилы, попадающие в очаг воспаления, быстро погибают. Появление достаточно большого количества лейкоцитов служит прогностически благоприятным признаком и свидетельствует о затухании процесса. § Исходы обычно неблагоприятные, что связано с массивностью поражения и снижением резистентности макроорганизма. Выздоровление возможно при активной антибиотикотерапии в сочетании с хирургическим лечением.
 Катаральное воспаление Отличительной особенностью катарального воспаления является примесь слизи к любому экссудату, поскольку оно развивается на слизистых оболочках и характеризуется обильным выделением экссудата, стекающего с поверхности слизистой оболочки, отсюда и название этого вида воспаления (греч. katarrheo стекаю). Следует отметить, что секреция слизи при воспалении слизистых оболочек является защитной реакцией, направленной на удаление повреждающего агента и создание защитного барьера на поверхности эпителия. § Катаральное воспаление может быть острым и хроническим. Острое катаральное воспаление характерно для острых респираторных вирусных инфекций.
Катаральное воспаление Отличительной особенностью катарального воспаления является примесь слизи к любому экссудату, поскольку оно развивается на слизистых оболочках и характеризуется обильным выделением экссудата, стекающего с поверхности слизистой оболочки, отсюда и название этого вида воспаления (греч. katarrheo стекаю). Следует отметить, что секреция слизи при воспалении слизистых оболочек является защитной реакцией, направленной на удаление повреждающего агента и создание защитного барьера на поверхности эпителия. § Катаральное воспаление может быть острым и хроническим. Острое катаральное воспаление характерно для острых респираторных вирусных инфекций.
 Рис. 9. Катаральный гастрит. Складки слизистой оболочки желудка набухшие, покрыты большим количеством вязкого мутного экссудата. Слизистая оболочка полнокровна, с петехиальными кровоизлияниями.
Рис. 9. Катаральный гастрит. Складки слизистой оболочки желудка набухшие, покрыты большим количеством вязкого мутного экссудата. Слизистая оболочка полнокровна, с петехиальными кровоизлияниями.
 Виды острого катарального воспаления: § серозное серозный катар; § слизистое слизистый катар; § гнойное гнойный катар; § геморрагическое геморрагический катар.
Виды острого катарального воспаления: § серозное серозный катар; § слизистое слизистый катар; § гнойное гнойный катар; § геморрагическое геморрагический катар.
 Хроническое катаральное воспаление может встречаться как при инфекционных (хронический гнойный катаральный бронхит), так и неинфекционных (хронический катаральный гастрит) заболеваниях. § Этиология Воспаление развивается при многих респираторных и кишечных, бактериальных и вирусных инфекциях, аллергических реакциях (аллергический ринит), под действием химических и термических факторов, эндогенных токсинов (уремический катаральный колит и гастрит).
Хроническое катаральное воспаление может встречаться как при инфекционных (хронический гнойный катаральный бронхит), так и неинфекционных (хронический катаральный гастрит) заболеваниях. § Этиология Воспаление развивается при многих респираторных и кишечных, бактериальных и вирусных инфекциях, аллергических реакциях (аллергический ринит), под действием химических и термических факторов, эндогенных токсинов (уремический катаральный колит и гастрит).
 § Морфология Слизистая оболочка отечная, полнокровная, с ее поверхности стекает обильный экссудат. Характер экссудата может быть различным (серозным, слизистым, гнойным), но обязательным его компонентом является слизь, вследствие чего экссудат принимает вид тягучей, вязкой массы. При микроскопическом исследовании в экссудате определяются лейкоциты, слущенные клетки покровного эпителия и слизистых желез. Сама слизистая оболочка имеет признаки отека, гиперемии, инфильтрирована лейкоцитами, плазматическими клетками, в железах слизистой оболочки много бокаловидных клеток. Хроническое воспаление в слизистой оболочке нередко сопровождается нарушением регенерации эпителиальных клеток с развитием атрофии или гипертрофии. В первом случае оболочка становится гладкой и тонкой, во втором утолщается, поверхность ее становится неровной, может выбухать в просвет органа в виде полипов. § Исходы Острое катаральное воспаление продолжается 2 3 нед и обычно заканчивается полным выздоровлением. Хроническое катаральное воспаление опасно развитием атрофии или гипертрофии слизистой оболочки.
§ Морфология Слизистая оболочка отечная, полнокровная, с ее поверхности стекает обильный экссудат. Характер экссудата может быть различным (серозным, слизистым, гнойным), но обязательным его компонентом является слизь, вследствие чего экссудат принимает вид тягучей, вязкой массы. При микроскопическом исследовании в экссудате определяются лейкоциты, слущенные клетки покровного эпителия и слизистых желез. Сама слизистая оболочка имеет признаки отека, гиперемии, инфильтрирована лейкоцитами, плазматическими клетками, в железах слизистой оболочки много бокаловидных клеток. Хроническое воспаление в слизистой оболочке нередко сопровождается нарушением регенерации эпителиальных клеток с развитием атрофии или гипертрофии. В первом случае оболочка становится гладкой и тонкой, во втором утолщается, поверхность ее становится неровной, может выбухать в просвет органа в виде полипов. § Исходы Острое катаральное воспаление продолжается 2 3 нед и обычно заканчивается полным выздоровлением. Хроническое катаральное воспаление опасно развитием атрофии или гипертрофии слизистой оболочки.
 Репарация процесс восстановления целостности ткани. Репарация тесно связана с воспалением, поскольку является его закономерным исходом. Репарацию трудно дифференцировать с пролиферативной фазой воспаления. Воспаление и репарация разделены лишь условно, так как пролиферация клеточных элементов и прежде всего фибробластов в очаге воспаления начинается уже в 1 e сутки после повреждения. Варианты репарации поврежденной ткани: § поврежденная ткань восстанавливается в результате регенерации паренхиматозных клеток; § поврежденная ткань замещается путем заполнения дефекта соединительной тканью (рубцевание); § поврежденная ткань восстанавливается в результате комбинации этих двух процессов.
Репарация процесс восстановления целостности ткани. Репарация тесно связана с воспалением, поскольку является его закономерным исходом. Репарацию трудно дифференцировать с пролиферативной фазой воспаления. Воспаление и репарация разделены лишь условно, так как пролиферация клеточных элементов и прежде всего фибробластов в очаге воспаления начинается уже в 1 e сутки после повреждения. Варианты репарации поврежденной ткани: § поврежденная ткань восстанавливается в результате регенерации паренхиматозных клеток; § поврежденная ткань замещается путем заполнения дефекта соединительной тканью (рубцевание); § поврежденная ткань восстанавливается в результате комбинации этих двух процессов.
 По способности к регенерации все клетки могут быть разделены на три вида: § лабильные клетки сохранившие способность пролиферировать и тем самым поддерживать тканевый гомеостаз. Такой тип клеток характерен для тканей с высоким уровнем гибели клеток в физиологических условиях, например для лимфоидной и костномозговой ткани, эпителиальной ткани слизистых оболочек; § стабильные клетки имеют ограниченную способность к пролиферации, они могут регенерировать в случае повреждения, но в обычных условиях не делятся. Печень, поджелудочная железа, почки, эндокринные железы и кровеносные сосуды построены из стабильных клеток. Для восстановления нормальной структуры в данных органах имеет значение сохранение целостности базальной мембраны; § перманентные клетки не обладают способностью делиться(нейроны и кардиомиоциты).
По способности к регенерации все клетки могут быть разделены на три вида: § лабильные клетки сохранившие способность пролиферировать и тем самым поддерживать тканевый гомеостаз. Такой тип клеток характерен для тканей с высоким уровнем гибели клеток в физиологических условиях, например для лимфоидной и костномозговой ткани, эпителиальной ткани слизистых оболочек; § стабильные клетки имеют ограниченную способность к пролиферации, они могут регенерировать в случае повреждения, но в обычных условиях не делятся. Печень, поджелудочная железа, почки, эндокринные железы и кровеносные сосуды построены из стабильных клеток. Для восстановления нормальной структуры в данных органах имеет значение сохранение целостности базальной мембраны; § перманентные клетки не обладают способностью делиться(нейроны и кардиомиоциты).
 § В органах и тканях, построенных из лабильных клеток возможна репарация с полным восстановлением целостности и структуры ткани, получившая название реституции. § В органах и тканях из стабильных клеток реституция не всегда возможна, поэтому в них нередко происходит восстановление целостности ткани в очаге повреждения с образованием соединительной ткани, т. е. рубца. Такой тип репарации нaзван неполной репарацией или субституцией. § Наконец, при гибели кардиомиоцитов и нейронов возможно только неполное заживление субституция с образованием фиброзного (в миокарде) или глиального (в нервной ткани) рубца.
§ В органах и тканях, построенных из лабильных клеток возможна репарация с полным восстановлением целостности и структуры ткани, получившая название реституции. § В органах и тканях из стабильных клеток реституция не всегда возможна, поэтому в них нередко происходит восстановление целостности ткани в очаге повреждения с образованием соединительной ткани, т. е. рубца. Такой тип репарации нaзван неполной репарацией или субституцией. § Наконец, при гибели кардиомиоцитов и нейронов возможно только неполное заживление субституция с образованием фиброзного (в миокарде) или глиального (в нервной ткани) рубца.
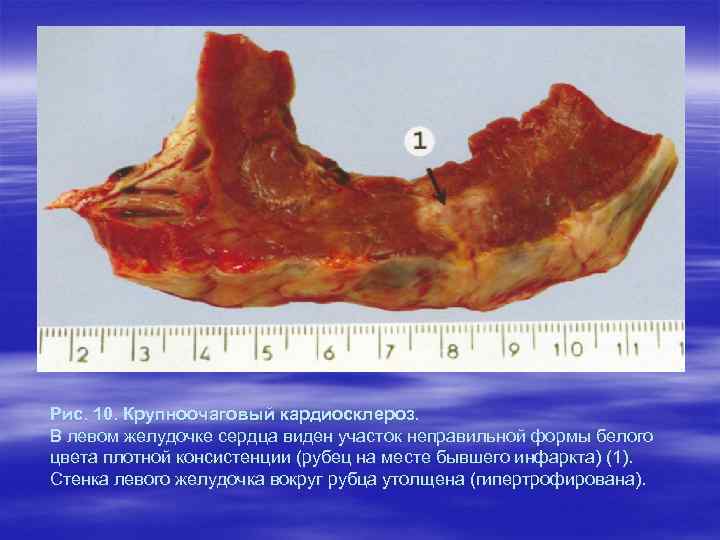 Рис. 10. Крупноочаговый кардиосклероз. В левом желудочке сердца виден участок неправильной формы белого цвета плотной консистенции (рубец на месте бывшего инфаркта) (1). Стенка левого желудочка вокруг рубца утолщена (гипертрофирована).
Рис. 10. Крупноочаговый кардиосклероз. В левом желудочке сердца виден участок неправильной формы белого цвета плотной консистенции (рубец на месте бывшего инфаркта) (1). Стенка левого желудочка вокруг рубца утолщена (гипертрофирована).
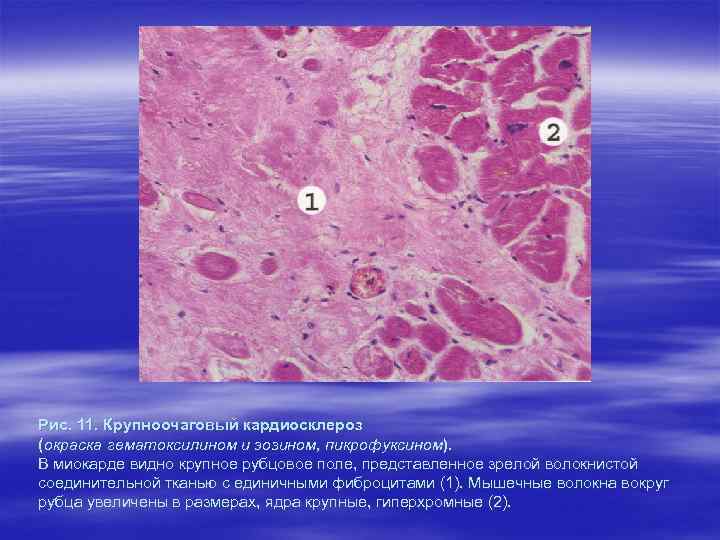 Рис. 11. Крупноочаговый кардиосклероз (окраска гематоксилином и эозином, пикрофуксином). В миокарде видно крупное рубцовое поле, представленное зрелой волокнистой соединительной тканью с единичными фиброцитами (1). Мышечные волокна вокруг рубца увеличены в размерах, ядра крупные, гиперхромные (2).
Рис. 11. Крупноочаговый кардиосклероз (окраска гематоксилином и эозином, пикрофуксином). В миокарде видно крупное рубцовое поле, представленное зрелой волокнистой соединительной тканью с единичными фиброцитами (1). Мышечные волокна вокруг рубца увеличены в размерах, ядра крупные, гиперхромные (2).
 Различают компоненты процесса заживления с образованием соединительной ткани: § новообразование кровеносных сосудов (ангиогенез) ; § миграция и пролиферация фибробластов; § продукция внеклеточного матрикса; § созревание соединительной ткани.
Различают компоненты процесса заживления с образованием соединительной ткани: § новообразование кровеносных сосудов (ангиогенез) ; § миграция и пролиферация фибробластов; § продукция внеклеточного матрикса; § созревание соединительной ткани.
 § Процесс восстановления начинается в раннюю фазу воспаления. Иногда уже через 24 ч после повреждения пролиферируют фибробласты и эндотелиальные клетки, образуя (через 3 5 дней) специализированный тип ткани (грануляционную ткань), которая играет главную роль в рубцевании. Эта ткань называется грануляционной потому что, располагаясь на поверхности раны, она имеет зернистый (гранулярный) вид. Для нее характерна пролиферация вновь образованных мелких кровеносных сосудов и фибробластов. § Множественные изгибы мелких сосудов макроскопически выглядят сероватыми зернами (гранулами). Новые сосуды образуются от существующих почкованием или ответвлением. Этот процесс называют ангиогенезом или неоваскуляризацией.
§ Процесс восстановления начинается в раннюю фазу воспаления. Иногда уже через 24 ч после повреждения пролиферируют фибробласты и эндотелиальные клетки, образуя (через 3 5 дней) специализированный тип ткани (грануляционную ткань), которая играет главную роль в рубцевании. Эта ткань называется грануляционной потому что, располагаясь на поверхности раны, она имеет зернистый (гранулярный) вид. Для нее характерна пролиферация вновь образованных мелких кровеносных сосудов и фибробластов. § Множественные изгибы мелких сосудов макроскопически выглядят сероватыми зернами (гранулами). Новые сосуды образуются от существующих почкованием или ответвлением. Этот процесс называют ангиогенезом или неоваскуляризацией.
 • Вновь образованные сосуды имеют проницаемые межэндотелиальные контакты, допускающие выход белков и эритроцитов из сосудистого русла. Поэтому грануляционная ткань нередко бывает отечной. Этапы развития новых капилляров: § протеолитическое разрушение базальной мембраны сосудов с образованием капиллярных отростков и одновременной миграции клеток; § миграция эндотелиальных клеток в направлении ангиогенного стимула; § пролиферация эндотелиальных клеток сразу после миграции клеток; § созревание эндотелиальных клеток и их организация в капиллярные трубки.
• Вновь образованные сосуды имеют проницаемые межэндотелиальные контакты, допускающие выход белков и эритроцитов из сосудистого русла. Поэтому грануляционная ткань нередко бывает отечной. Этапы развития новых капилляров: § протеолитическое разрушение базальной мембраны сосудов с образованием капиллярных отростков и одновременной миграции клеток; § миграция эндотелиальных клеток в направлении ангиогенного стимула; § пролиферация эндотелиальных клеток сразу после миграции клеток; § созревание эндотелиальных клеток и их организация в капиллярные трубки.
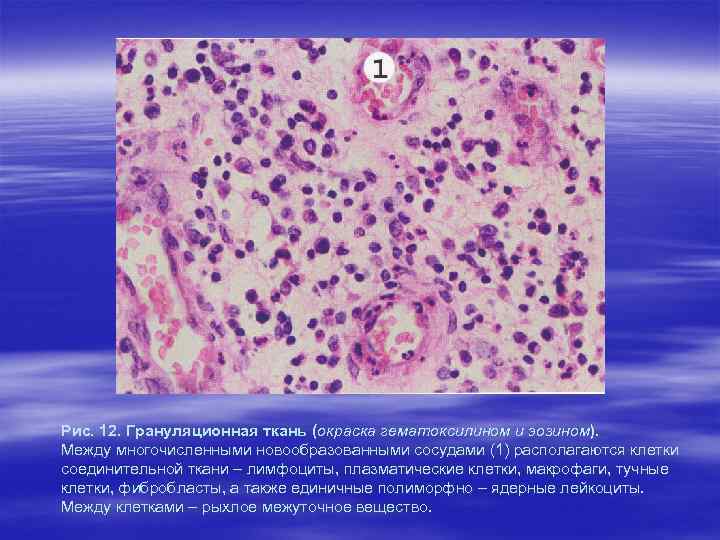 Рис. 12. Грануляционная ткань (окраска гематоксилином и эозином). Между многочисленными новообразованными сосудами (1) располагаются клетки соединительной ткани – лимфоциты, плазматические клетки, макрофаги, тучные клетки, фибробласты, а также единичные полиморфно – ядерные лейкоциты. Между клетками – рыхлое межуточное вещество.
Рис. 12. Грануляционная ткань (окраска гематоксилином и эозином). Между многочисленными новообразованными сосудами (1) располагаются клетки соединительной ткани – лимфоциты, плазматические клетки, макрофаги, тучные клетки, фибробласты, а также единичные полиморфно – ядерные лейкоциты. Между клетками – рыхлое межуточное вещество.
 § Некоторые факторы могут стимулировать ангиогенез, в том числе о. ФРФ и фактор роста эндотелия сосудов. о. ФРФ выделяется активированными макрофагами и может влиять на любые этапы ангиогенеза; Фактор роста эндотелия сосудов продуцируют опухолевые клетки; он вызывает как ангиогенез, так и повышение проницаемости сосудов (влияет на опухолевый ангиогенез и рост кровеносных сосудов в норме), а также участвует в хроническом воспалении и заживлении ран. Миграцию фибробластов к месту повреждения и их одновременную пролиферацию вызывают факторы роста и фиброгенные цитокины, которые образуются макрофагами. Некоторые из этих факторов роста стимулируют синтез коллагена и других молекул соединительной ткани, а также модулируют синтез и активацию металлопротеиназ и ферментов, участвующих в разрушении компонентов внеклеточного матрикса.
§ Некоторые факторы могут стимулировать ангиогенез, в том числе о. ФРФ и фактор роста эндотелия сосудов. о. ФРФ выделяется активированными макрофагами и может влиять на любые этапы ангиогенеза; Фактор роста эндотелия сосудов продуцируют опухолевые клетки; он вызывает как ангиогенез, так и повышение проницаемости сосудов (влияет на опухолевый ангиогенез и рост кровеносных сосудов в норме), а также участвует в хроническом воспалении и заживлении ран. Миграцию фибробластов к месту повреждения и их одновременную пролиферацию вызывают факторы роста и фиброгенные цитокины, которые образуются макрофагами. Некоторые из этих факторов роста стимулируют синтез коллагена и других молекул соединительной ткани, а также модулируют синтез и активацию металлопротеиназ и ферментов, участвующих в разрушении компонентов внеклеточного матрикса.
 § Когда происходит значительная утрата клеток и тканей, например при инфаркте, изъязвлении, образовании абсцесса, а также поверхностных ранах с большими дефектами тканей, репаративные процессы затруднены. § Основной проблемой во всех этих случаях является значительный дефект ткани, который должен быть замещен. § Регенерация паренхиматозных клеток не может полностью восстановить оригинальную архитектонику. § Обильная грануляционная ткань растет с краев, формируя рубец. Такое заживление ран называют заживлением вторичным соединением или вторичным натяжением.
§ Когда происходит значительная утрата клеток и тканей, например при инфаркте, изъязвлении, образовании абсцесса, а также поверхностных ранах с большими дефектами тканей, репаративные процессы затруднены. § Основной проблемой во всех этих случаях является значительный дефект ткани, который должен быть замещен. § Регенерация паренхиматозных клеток не может полностью восстановить оригинальную архитектонику. § Обильная грануляционная ткань растет с краев, формируя рубец. Такое заживление ран называют заживлением вторичным соединением или вторичным натяжением.
 Заживление ран Классическим примером полного заживления ран является заживление чистых неинфицированных хирургических разрезов, соединенных с помощью хирургического шва. Такое заживление называют первичным соединением или заживлением первичным натяжением. При этом последовательно развиваются следующие изменения: § заполнение дефекта свертками крови, содержащими фибрин и клетки крови; § дегидратация поверхности свертка крови с образованием струпа, закрывающего рану; § инфильтрация нейтрофильными лейкоцитами и резорбция тканевого детрита; § пролиферация базальных кератиноцитов, фибробластов и миофибробластов, стягивающих края раны; § синтез компонентов базальной мембраны базальными кератиноцитами; § формирование непрерывного тонкого слоя эпителия; § смена лейкоцитарной инфильтрации на макрофагальную.
Заживление ран Классическим примером полного заживления ран является заживление чистых неинфицированных хирургических разрезов, соединенных с помощью хирургического шва. Такое заживление называют первичным соединением или заживлением первичным натяжением. При этом последовательно развиваются следующие изменения: § заполнение дефекта свертками крови, содержащими фибрин и клетки крови; § дегидратация поверхности свертка крови с образованием струпа, закрывающего рану; § инфильтрация нейтрофильными лейкоцитами и резорбция тканевого детрита; § пролиферация базальных кератиноцитов, фибробластов и миофибробластов, стягивающих края раны; § синтез компонентов базальной мембраны базальными кератиноцитами; § формирование непрерывного тонкого слоя эпителия; § смена лейкоцитарной инфильтрации на макрофагальную.
 Отличия вторичного заживления от первичного: § значительные тканевые дефекты вначале заполняются большим количеством фибрина и остатков некротизированных тканей, а также экссудатом, которые должны быть удалены. Следовательно, развивается более интенсивная воспалительная реакция; § образуется значительно большее количество грануляционной ткани. Когда крупные дефекты имеются в более глубоких тканях (например, в органах), формируется грануляционная ткань, которая утилизирует остатки разрушенной ткани, так как поверхностный дренаж отсутствует; § возможно особенностью, которая позволяет легче всего отличить первичное заживление от вторичного, является феномен сжатия раны. Последний наблюдается при больших раневых поверхностях. Сжатие связывают с наличием миофибробластов измененных фибробластов, которые имеют ультраструктурные характеристики гладкомышечных тканей и экспрессируют гладкомышечный актин (SМA), нехарактерный для типичных фибробластов.
Отличия вторичного заживления от первичного: § значительные тканевые дефекты вначале заполняются большим количеством фибрина и остатков некротизированных тканей, а также экссудатом, которые должны быть удалены. Следовательно, развивается более интенсивная воспалительная реакция; § образуется значительно большее количество грануляционной ткани. Когда крупные дефекты имеются в более глубоких тканях (например, в органах), формируется грануляционная ткань, которая утилизирует остатки разрушенной ткани, так как поверхностный дренаж отсутствует; § возможно особенностью, которая позволяет легче всего отличить первичное заживление от вторичного, является феномен сжатия раны. Последний наблюдается при больших раневых поверхностях. Сжатие связывают с наличием миофибробластов измененных фибробластов, которые имеют ультраструктурные характеристики гладкомышечных тканей и экспрессируют гладкомышечный актин (SМA), нехарактерный для типичных фибробластов.
 Таким образом, заживление ран является сложным феном, включающим: § острое воспаление, § регенерацию паренхиматозных клеток, § миграцию и пролиферацию как паренхиматозных, так и соединительнотканных клеток, § синтез белков внеклеточного матрикса, § перестройку соединительной ткани и паренхиматозных компонентов, § коллагенизацию и натяжение раны. В основе большинства этих процессов лежат уже описанные факторы и механизмы: медиаторы острого воспаления, факторы роста, взаимодействие клеток с внеклеточным веществом в процессе миграции клеток, их пролиферации и дифференцировки, механизмы ангиогенеза и фиброза.
Таким образом, заживление ран является сложным феном, включающим: § острое воспаление, § регенерацию паренхиматозных клеток, § миграцию и пролиферацию как паренхиматозных, так и соединительнотканных клеток, § синтез белков внеклеточного матрикса, § перестройку соединительной ткани и паренхиматозных компонентов, § коллагенизацию и натяжение раны. В основе большинства этих процессов лежат уже описанные факторы и механизмы: медиаторы острого воспаления, факторы роста, взаимодействие клеток с внеклеточным веществом в процессе миграции клеток, их пролиферации и дифференцировки, механизмы ангиогенеза и фиброза.


