Вещества Простые Сложные Металлы Неметаллы Бинарные Три элемента

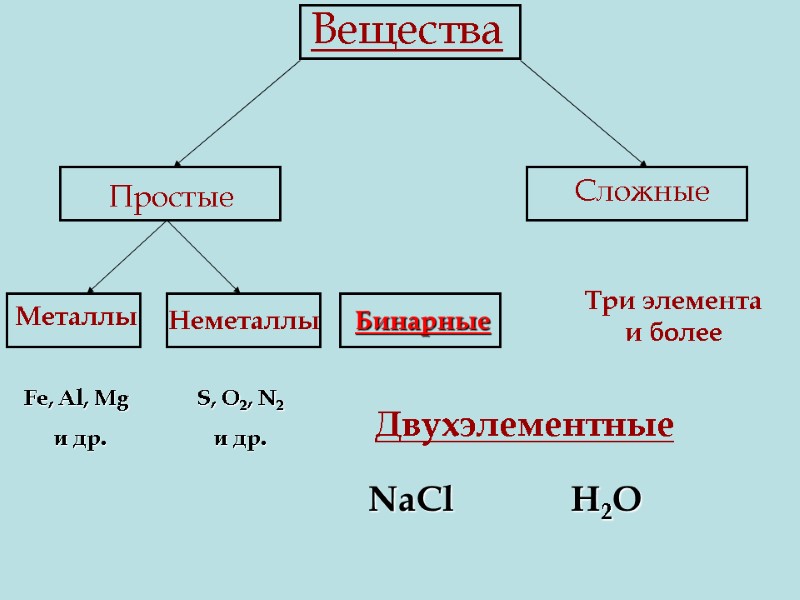
Вещества Простые Сложные Металлы Неметаллы Бинарные Три элемента и более Двухэлементные Fe, Al, Mg и др. S, O2, N2 и др. NaCl H2O

- это сложные вещества, состоящие из двух химических элементов. Например: хлорид натрия и хлороводород

Химической связь? Какого типа бывают? От чего зависит?
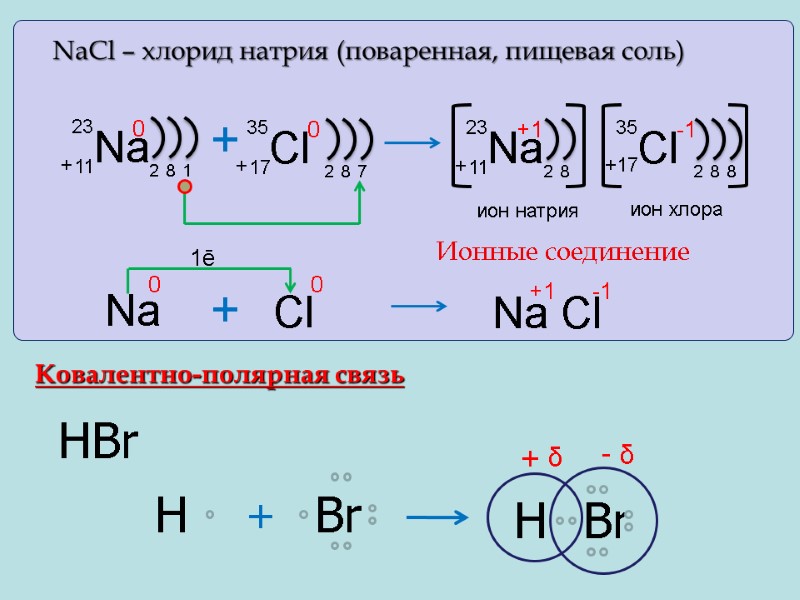
НBr Н Br + Н Br - δ + δ NaCl – хлорид натрия (поваренная, пищевая соль) 1ē Ионные соединение Ковалентно-полярная связь - δ
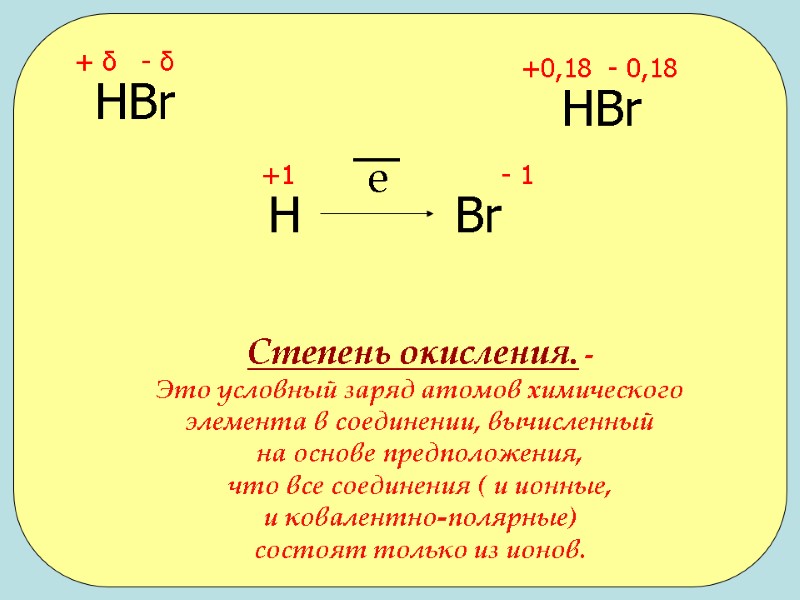
+ δ - δ +0,18 - 0,18 НBr Н Br е НBr +1 - 1 Степень окисления. - Это условный заряд атомов химического элемента в соединении, вычисленный на основе предположения, что все соединения ( и ионные, и ковалентно-полярные) состоят только из ионов.

Степень окисления бывает: «+», «-», «0». Степень окисления бывает: постоянной и непостоянной Mg3N2 2+ 3- N2O5 +5 2- NO2 2- +4
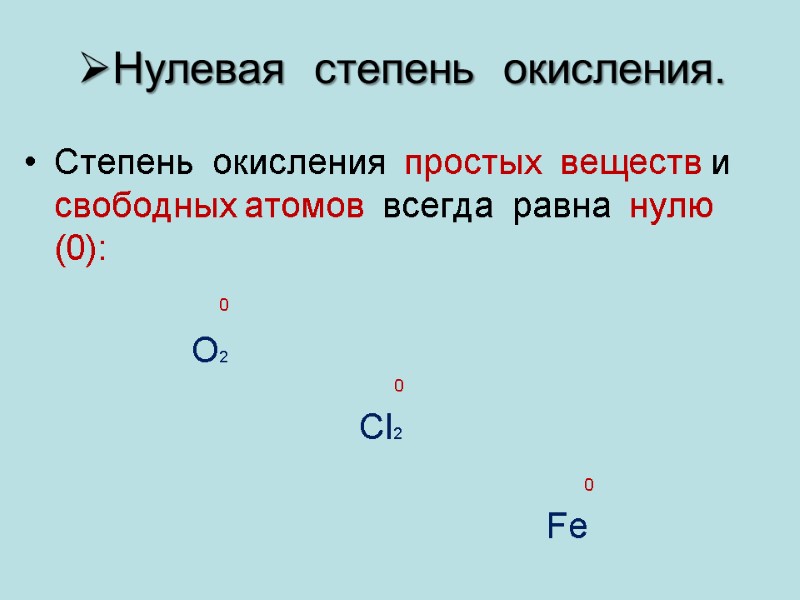
Нулевая степень окисления. Степень окисления простых веществ и свободных атомов всегда равна нулю (0): 0 О2 0 Cl2 0 Fe

Отрицательная степень окисления Степень окисления фтора (F) всегда равна -1

-1 +1

Положительная степень окисления. У металлов степень окисления всегда положительна и равна номеру группы (для металлов главных подгрупп). У металлов I группы С.О.= +1 У металлов II группы С.О.= +2 У металлов III группы С.О.= +3 Na2O +1 -2 CaO +2 -2 Al2O3 +3 -2
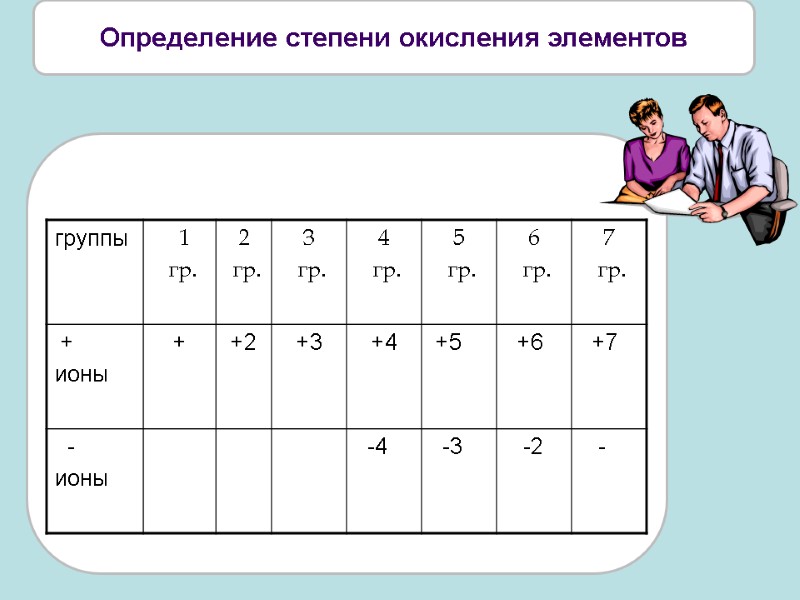
Определение степени окисления элементов
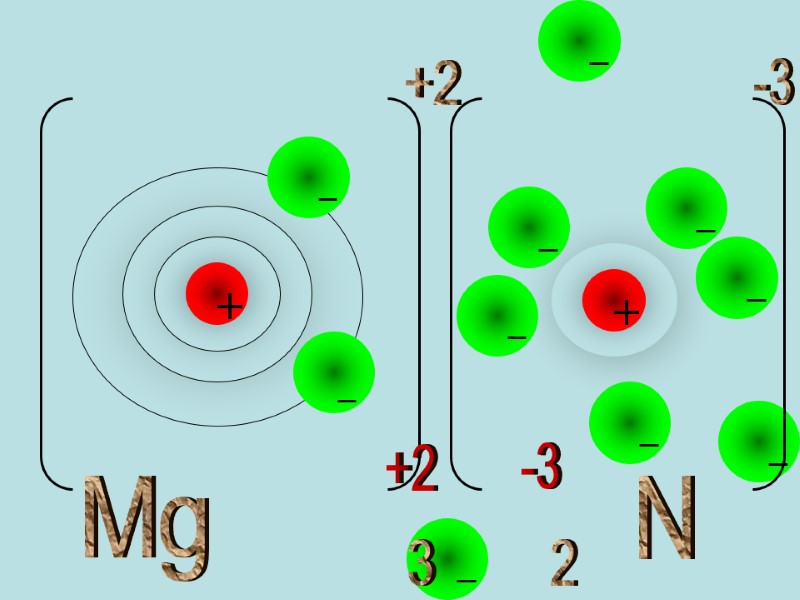
Mg +2 N 3 -3 2 +2 -3

Валентность и Степень окисления Н2 Валентность (I) H-Н Н2, HCl, CaH2 0 +2 -1 -1 +1 F2 F-F F2 0 KF HF -1 +1 -1 +1 Валентность (I)

ВЫВОД В ЧЁМ ОТЛИЧИЯ ??? Валентность, характеризующая число химических связей может не иметь знака Валентность не может равняться нулю (по определению) Валентность не может быть дробным числом Валентность имеет определённый предел применения. Степень окисления имеет знак Степень окисления элемента может быть равна нулю Степень окисления может быть дробным числом Степень окисления атомов химических элементов можно определять в любых веществах Сравним понятия «степень окисления» и «валентность», а точнее, разграничим их. Даже если абсолютные значения степени окисления и валентности совпадают, их нельзя отождествлять.

Алгоритм составления формул химических соединений Определить формулу вещества ОКСИД АЛЮМИНИЯ Записать химические знаки элементов Al O Определить с.о. элементов Al+3O-2 3. Найти НОК записанных чисел и определить индексы. Al+3O-2 ЗАПОМНИТЕ ПРАВИЛО: Суммарная степень окисления элементов в соединении равна нулю. (+3)∙2 + (-2)∙3 = 6 - 6 = 0 6 Al2O3

Бинарные соединения. Бинарные соединения – это соединения, состоящие из двух химических элементов.

Бинарные соединения. На первом месте всегда записывается элемент с положительной степенью окисления, а на втором - с отрицательной. HY + -

Названия бинарных соединений. На первом месте в названии бинарного соединения записывается латинское название элемента с отрицательной степенью окисления с суффиксом -ид, а затем название элемента с положительной степенью окисления в родительном падеже. Элемент- ид + элемента ( с.о., если переменная)

Названия бинарных соединений. Названия элементов с отрицательной степенью окисления: Cl - хлорид О - оксид Н - гидрид S - сульфид N - нитрид P - фосфид С - карбид Br - бромид
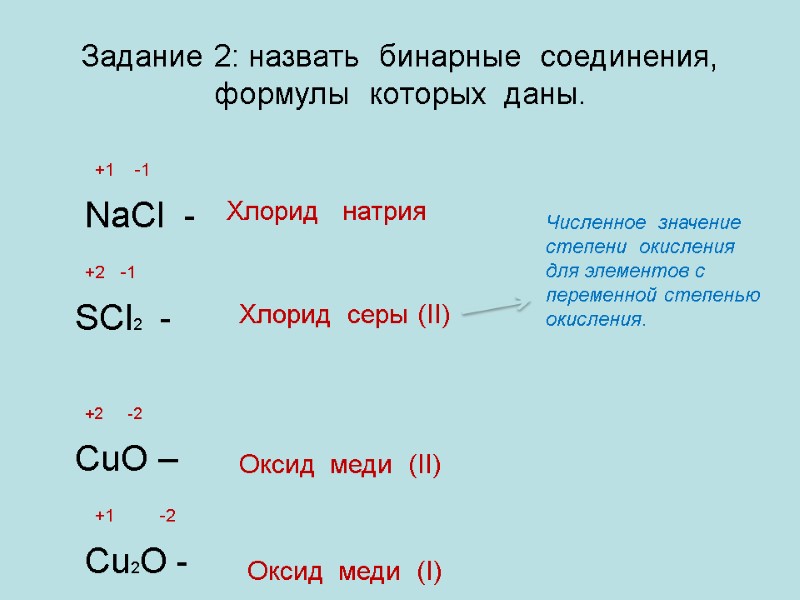
Задание 2: назвать бинарные соединения, формулы которых даны. +1 -1 NaCl - +2 -1 SCl2 - +2 -2 CuO – +1 -2 Cu2O - Хлорид натрия Численное значение степени окисления для элементов с переменной степенью окисления. Оксид меди (II) Хлорид серы (II) Оксид меди (I)

Составление формул бинарных соединений по названию. оксид углерода (IV). 1) Записать символы химических элементов образующих соединение: СО

Составление формул бинарных соединений по названию. 2) Над атомами химических элементов в соединении проставить их степени окисления (в скобках указана переменная степень окисления элемента – она положительна): +4 -2 СО оксид углерода (IV).

Составление формул бинарных соединений по названию. 3) Найти наименьшее общее кратное между значениями степеней окисления: +4 -2 СО 4

Составление формул бинарных соединений по названию. Определить индексы, разделив НОК на значения степеней окисления каждого элемента. +4 -2 СО СО2 - оксид углерода (IV) 4 2 Индекс «1» не пишут
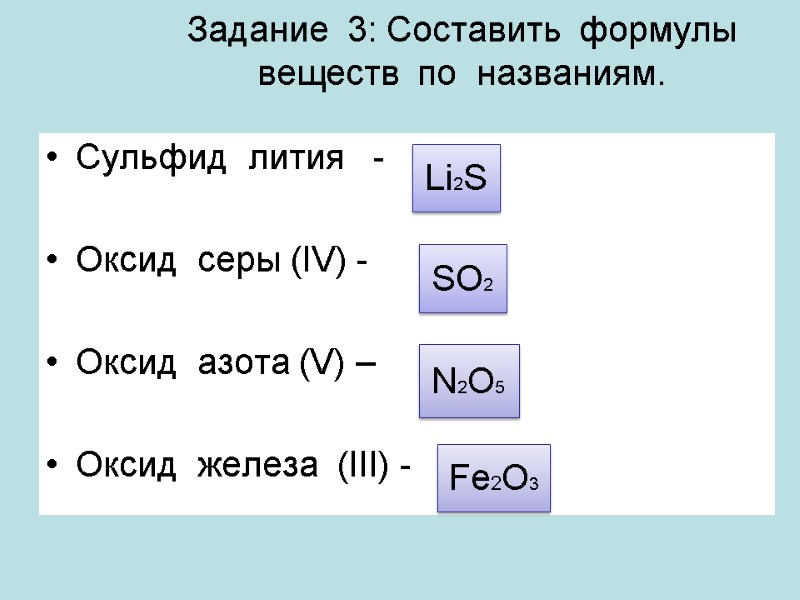
Задание 3: Составить формулы веществ по названиям. Сульфид лития - Оксид серы (IV) - Оксид азота (V) – Оксид железа (III) - Li2S SO2 N2O5 Fe2O3
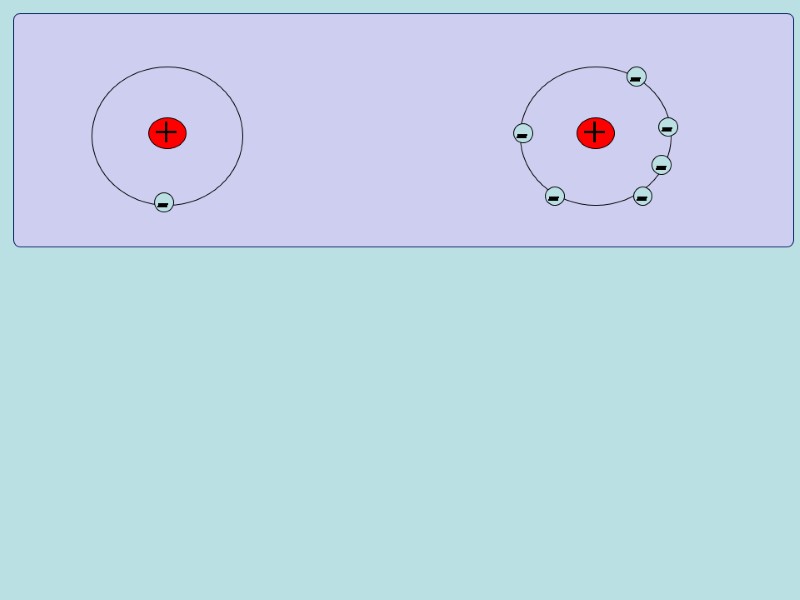
+ - + - - - - - -
Степень окисления – условный заряд атома в соединении Степень окисления показывает заряд только одного атома в соединении , а там их может быть несколько. Например, степень окисления атома кислорода во многих случаях О-2, а в оксиде углерода (IV)СО2 суммарный заряд двух атомов кислорода равен -4 Степень окисления атома определяется только в соединении его с другими атомами. Поэтому степень окисления простых веществ равна «0». В простом веществе О2 степень окисления атома – 0 Fe0, S0, P0, H20
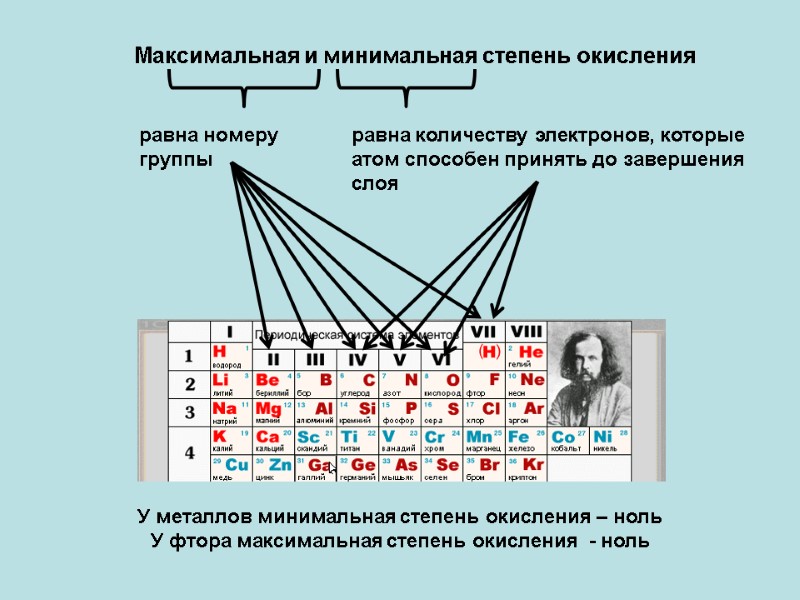
Максимальная и минимальная степень окисления равна номеру группы равна количеству электронов, которые атом способен принять до завершения слоя У металлов минимальная степень окисления – ноль У фтора максимальная степень окисления - ноль

СОБЛЮДАЙ ПРАВИЛО: Суммарная степень окисления элементов в соединении равна нулю. K2+1O-2 2∙1 + (-2) =0 Fe2+3O3-2 2∙3 + 3∙ (-2) =0 N2+5O5-2 2∙5 + 5∙(-2) =0 Mg3+2N2-3 2∙3 + 3∙(-2) =0 Al+3Cl3-1 1∙3 + 3∙ (-1) =0

Определите степени oкисления химических элементов: Al2O3 Ca3N2 K2S P2O5 Cl2O7 Al2+3O3-2 Ca3+2N2-3 K2+1S-2 P2+5O5-2 Cl2+7O7-2
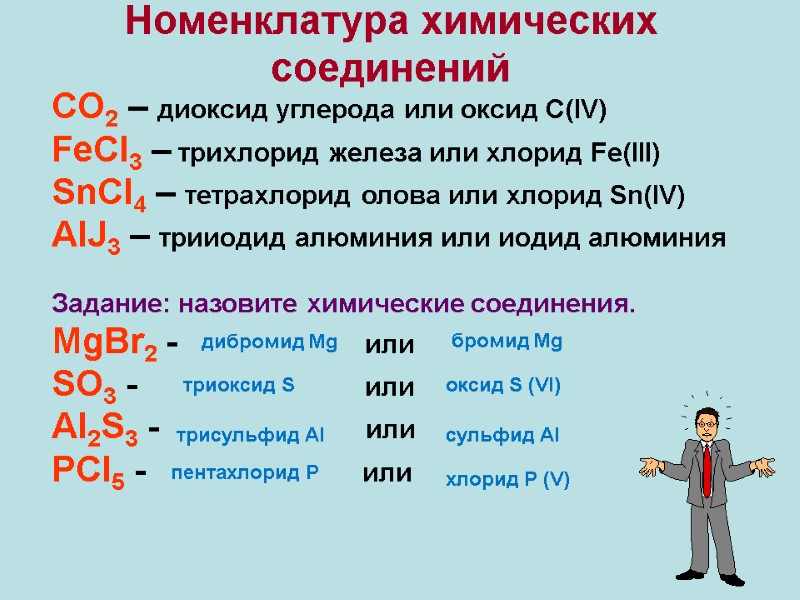
Номенклатура химических соединений CO2 – диоксид углерода или оксид C(IV) FeCl3 – трихлорид железа или хлорид Fe(III) SnCl4 – тетрахлорид олова или хлорид Sn(IV) AlJ3 – трииодид алюминия или иодид алюминия Задание: назовите химические соединения. MgBr2 - или SO3 - или Al2S3 - или PCl5 - или дибромид Mg бромид Mg триоксид S оксид S (VI) трисульфид Al сульфид Al пентахлорид Р хлорид Р (V)
17524-mks_6_urok_stepen_okislenia.ppt
- Количество слайдов: 31

